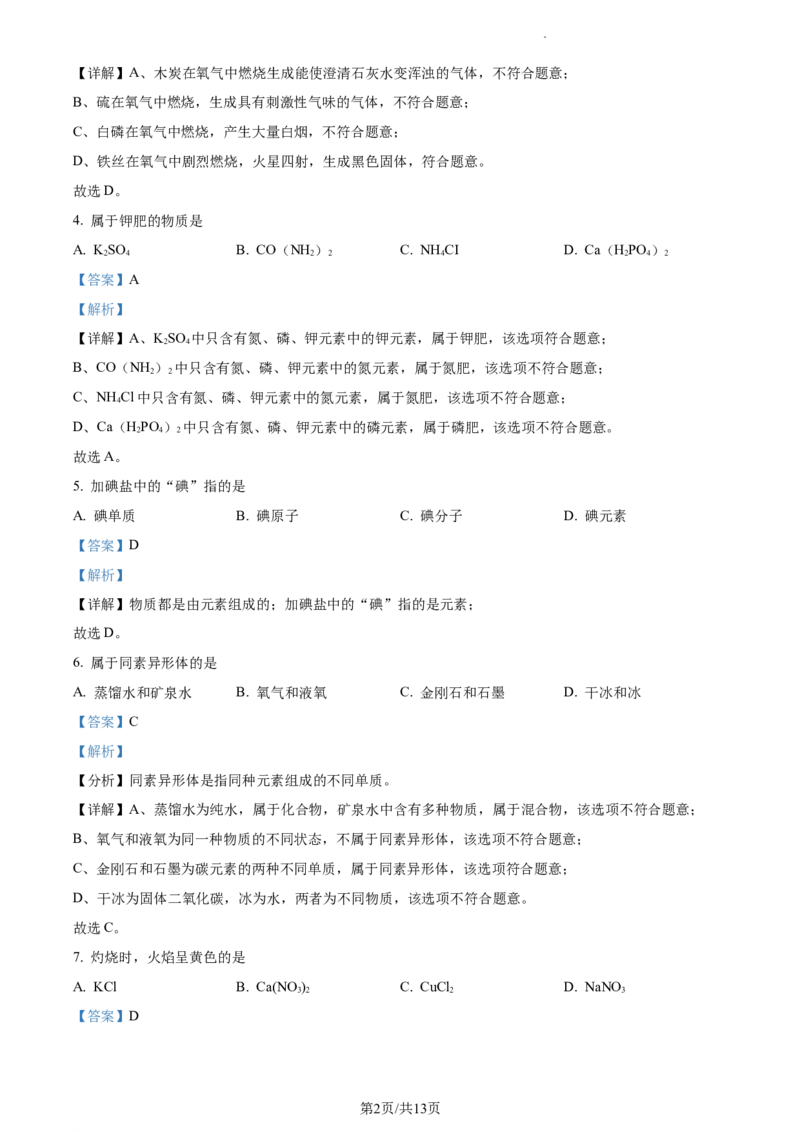文档内容
杨浦区 2022 学年第二学期初三质量调研
(2023.04)
(满分50分,考试时间40分钟)
考生注意:
1.本试卷化学部分含二个大题。
2.答题时,考生务必按答题要求在答题纸规定的位置上作答,在草稿纸、本试卷上答题一律
无效。
相对原子质量:H-1 C-12 O-16 Cl-35.5 Fe-56 Cu-64 Zn-65
一、选择题(本大题共17题,共20分1~14每题只有1个正确选项,每题1分,共14分)
1. 氢元素以游离态存在的物质是
A. HO B. HSO C. H D. NaOH
2 2 4 2
【答案】C
【解析】
【详解】A、HO为化合物,则氢元素以化合态形式存在,该选项不符合题意;
2
B、HSO 为化合物,则氢元素以化合态形式存在,该选项不符合题意;
2 4
C、H 为单质,则氢元素以游离态形式存在,该选项符合题意;
2
D、NaOH为化合物,则氢元素以化合态形式存在,该选项不符合题意。
故选C。
2. 物质对应的类别正确的是
A. 氧气:氧化物 B. 胆矾:盐
.
C 大理石:纯净物 D. 汽水:化合物
【答案】B
【解析】
【详解】A、氧气中只含有氧元素,属于单质,而不是氧化物,该选项分类不正确;
B、胆矾为硫酸铜,其是由金属离子和酸根构成的,属于盐,该选项分类正确;
C、大理石的主要成分为碳酸钙,还含有其它物质,属于混合物,该选项分类不正确;
D、汽水中含有多种物质,属于混合物,该选项不符合题意。
故选B。
3. 下列物质在氧气中燃烧,生成黑色固体物质的是
A. 木炭 B. 硫粉 C. 白磷 D. 铁丝
【答案】D
【解析】
第1页/共13页
学科网(北京)股份有限公司【详解】A、木炭在氧气中燃烧生成能使澄清石灰水变浑浊的气体,不符合题意;
B、硫在氧气中燃烧,生成具有刺激性气味的气体,不符合题意;
C、白磷在氧气中燃烧,产生大量白烟,不符合题意;
D、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,符合题意。
故选D。
4. 属于钾肥的物质是
A. KSO B. CO(NH ) C. NH CI D. Ca(HPO )
2 4 2 2 4 2 4 2
【答案】A
【解析】
【详解】A、KSO 中只含有氮、磷、钾元素中的钾元素,属于钾肥,该选项符合题意;
2 4
B、CO(NH ) 中只含有氮、磷、钾元素中的氮元素,属于氮肥,该选项不符合题意;
2 2
C、NH Cl中只含有氮、磷、钾元素中的氮元素,属于氮肥,该选项不符合题意;
4
D、Ca(HPO ) 中只含有氮、磷、钾元素中的磷元素,属于磷肥,该选项不符合题意。
2 4 2
故选A。
5. 加碘盐中的“碘”指的是
A. 碘单质 B. 碘原子 C. 碘分子 D. 碘元素
【答案】D
【解析】
【详解】物质都是由元素组成的;加碘盐中的“碘”指的是元素;
故选D。
6. 属于同素异形体的是
A. 蒸馏水和矿泉水 B. 氧气和液氧 C. 金刚石和石墨 D. 干冰和冰
【答案】C
【解析】
【分析】同素异形体是指同种元素组成的不同单质。
【详解】A、蒸馏水为纯水,属于化合物,矿泉水中含有多种物质,属于混合物,该选项不符合题意;
B、氧气和液氧为同一种物质的不同状态,不属于同素异形体,该选项不符合题意;
C、金刚石和石墨为碳元素的两种不同单质,属于同素异形体,该选项符合题意;
D、干冰为固体二氧化碳,冰为水,两者为不同物质,该选项不符合题意。
故选C。
7. 灼烧时,火焰呈黄色的是
A. KCl B. Ca(NO ) C. CuCl D. NaNO
3 2 2 3
【答案】D
第2页/共13页
学科网(北京)股份有限公司【解析】
【分析】含钠元素的化合物灼烧时,火焰呈黄色。
【详解】A、KCl中不含有Na,而含有K,焰色反应为紫色,错误;
B、Ca(NO ) 中不含有Na,错误;
3 2
C、CuCl 中不含Na,而含Cu,焰色反应为绿色,错误;
2
D、硝酸钠中含有Na,焰色反应为黄色,正确;
故选D。
8. 下列方法可将海水转化为淡水的是( )
A. 蒸馏 B. 静置 C. 过滤 D. 消毒
【答案】A
【解析】
【详解】海水淡化是除掉海水的可溶性物质。
A、将海水蒸馏,能将水从海水中分离出来,从而实现海水淡化,故选项正确;
B、静置,只能使大颗粒的不溶性杂质,不能使海水淡化,故选项错误;
C、将海水过滤,只能除去海水的不溶性杂质,不能使海水淡化,故选项错误;
D、消毒,能杀灭细菌,不能使海水淡化,故选项错误。
故选A。
9. 下列物质发生分解反应不可能生成氧气的是
A. KMnO B. NaCl C. KClO D. HO
4 3 2 2
【答案】B
【解析】
【详解】A、高锰酸钾中含有氧元素,根据元素守恒,高锰酸钾可能发生分解反应生成氧气,该选项不符
合题意;
B、氯化钠中不含氧元素,则不可能发生分解反应生成氧气,该选项符合题意;
C、氯化钾中含有氧元素,则可能发生分解反应生成氧气,该选项不符合题意;
D、过氧化氢中含有氧元素,则可能发生分解反应生成氧气,该选项不符合题意。
故选B。
10. 物质的用途错误的是
A. 食盐:调味剂 B. 干冰:人工降雨
C. 一氧化碳:冶炼金属 D. 熟石灰:改良碱性土壤
【答案】D
【解析】
【详解】A、食盐氯化钠由咸味,可用作调味剂,正确;
第3页/共13页
学科网(北京)股份有限公司B、干冰升华吸热,可用于人工降雨,正确;
C、一氧化碳具有还原性,可还原金属氧化物,可用于冶炼金属,正确;
D、熟石灰氢氧化钙是一种碱,可中和酸性土壤中的酸性物质,改良酸性土壤,错误;
故选D。
11. 能鉴别稀硫酸和稀盐酸的试剂是
A. 石蕊试液 B. 硝酸银溶液 C. 硝酸钡溶液 D. 碳酸钠溶液
【答案】C
【解析】
【分析】根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相
同,则无法鉴别它们。
【详解】A、盐酸和硫酸均能使紫色石蕊试液变红色,不能鉴别,故A不符合题意;
B、硝酸银溶液与盐酸和硫酸反应均生成白色沉淀,不能鉴别,故B不符合题意;
C、硝酸钡溶液能与硫酸反应生成硫酸钡白色沉淀,与盐酸不反应,可以鉴别,故C符合题意;
D、碳酸钠溶液与盐酸和硫酸反应均生成二氧化碳气体,不能鉴别,故D不符合题意;
故选:C 。
【点睛】本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的物质反应并出
现明显不同的现象。
12. 下表中除杂方法正确的是
物质 所含杂质 除去杂质的方法
A NaCl NaCO 加入过量稀硫酸
2 3
B CuO Cu 加入过量稀盐酸
C CO CO 通入过量氢氧化钠溶液
2
D NaOH Ca(OH) 加入过量碳酸钠溶液
2
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、加入过量稀硫酸,碳酸钠和稀硫酸反应生成硫酸钠、二氧化碳和水,虽然除去了杂质,但是
引入了新的杂质硫酸钠和硫酸,不符合题意;
B、加入过量稀盐酸,铜和稀盐酸不反应,氧化铜和稀盐酸反应生成氯化铜和水,除去了原物质,不符合
题意;
C、通入过量氢氧化钠溶液,二氧化碳和氢氧化钠反应生成碳酸钠和水,一氧化碳和氢氧化钠不反应,可
第4页/共13页
学科网(北京)股份有限公司除去杂质,符合题意;
D、加入过量碳酸钠溶液,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,虽然除去了杂质,但是引入了
新的杂质碳酸钠,不符合题意。
故选C。
13. 甲烷和水蒸气制氢气的化学方程式:CH+HO CO+3H,有关说法正确的是
4 2 2
A. 反应中CO是还原剂
B. 参加反应的CH 和HO的质量比为1:1
4 2
C. 若生成3mol H,则有1mol CH 参加反应
2 4
D. 反应物的摩尔质量之和等于生成物的摩尔质量之和
【答案】C
【解析】
【详解】A、在该反应中,一氧化碳为生成物,不属于还原剂,该选项说法不正确;
B、由化学方程式可知,参加反应的CH 和HO的质量比为(12+1×4):(1×2+16)=22:9,该选项说法
4 2
不正确;
C、化学计量数之比为该反应的物质的量之比,则若生成3mol H,则有1mol CH 参加反应,该选项说法
2 4
正确;
D、反应前后物质的总质量不变,但反应物的摩尔质量之和不一定相等,该选项说法不正确。
故选C。
14. 在一定量的氯化铜溶液中加入一定量锌和金属R(化合物中,化合价为+2)的混合粉末,溶液质量的
变化情况如图所示。下列说法正确的是
A. 金属活动性:RZn,该选项说法不正确;
B、由于R与氯化铜反应过程中溶液质量减小,且在化合物中,R和铜的化合价均为+2价,则R的相对原
子质量比铜小,该选项说法正确;
C、a点时,表示R与氯化铜已经完全反应,锌和氯化铜开始反应但氯化铜还未完全反应,则此时溶液中的
溶质有R的化合物、氯化锌、氯化铜,该选项说法不正确;
D、由于R、锌均能将铜从氯化铜溶液中置换出来,则溶液中铜元素的质量渐渐减小,该选项说法不正确。
故选B。
15~17每题有1~2个正确选项,每题2分,共6分。
的
15. 酸 组成中一定含有
A. 金属元素 B. 氢元素 C. 原子团 D. 酸根
【答案】BD
【解析】
【详解】酸是由氢离子和酸根离子构成的,则组成中一定含有氢离子和酸根,一定不含金属元素,可能含
有原子团(如盐酸中不含原子团),故选BD。
16. 关于燃烧的说法错误的是
A. 一定要有氧气 B. 一定要达到可燃物的着火点
C. 一定会放出热量 D. 一定发生化学反应
【答案】A
【解析】
【详解】A、燃烧时不一定需要氧气,如镁可以在氮气中燃烧,该选项说法错误;
B、燃烧的条件之一为温度达到着火点以上,该选项说法正确;
C、所有的燃烧反应均放热,该选项说法正确;
D、燃烧过程中有新物质生成,属于化学变化,该选项说法正确。
故选A。
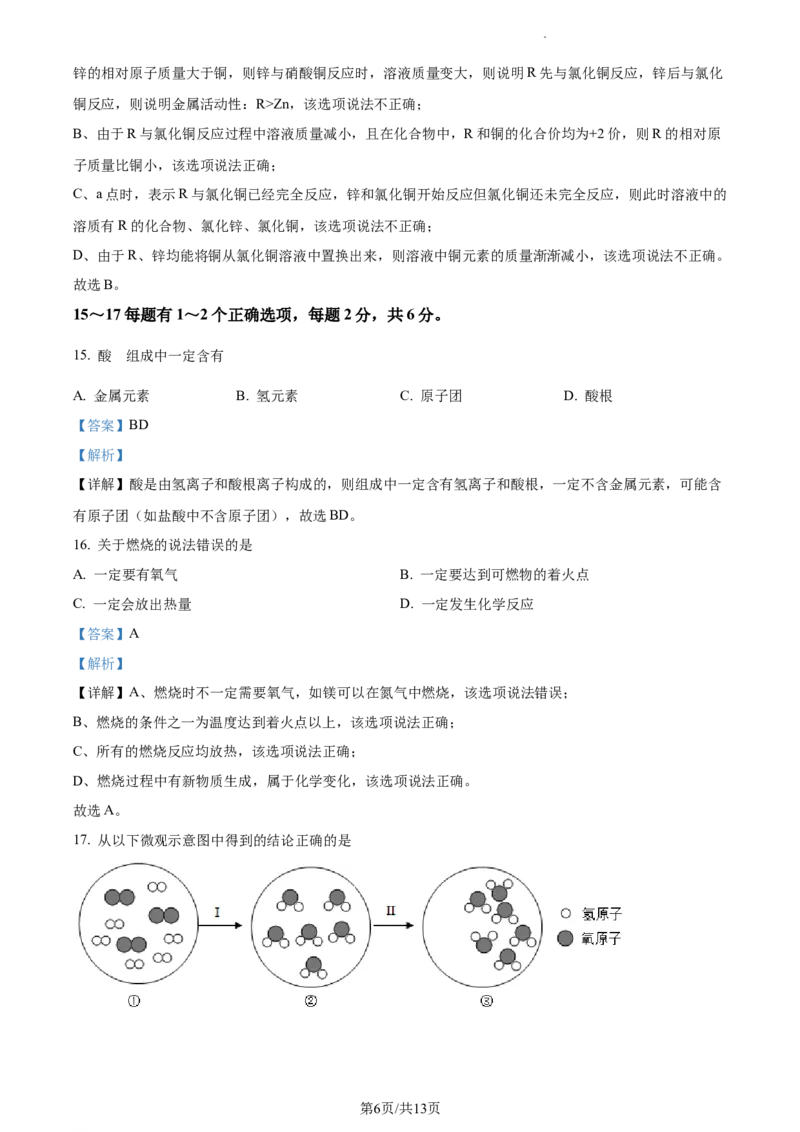
17. 从以下微观示意图中得到的结论正确的是
第6页/共13页
学科网(北京)股份有限公司A. 变化:I是化学变化 B. 质量:① > ②
C. 结构:②③分子结构相同 D. 条件:I、II变化时需要的条件相同
【答案】AC
【解析】
【详解】A、由图可知,Ⅰ过程中分子种类发生改变,为化学变化,该选项结论正确;
的
B、根据质量守恒定律,反应前后物质 总质量不变,则①②质量相等,该选项结论不正确;
C、Ⅱ过程中分子种类不变,只是分子的间隔发生改变,即②③分子结构相同,该选项结论正确;
D、Ⅰ为化学变化,Ⅱ为物理变化,变化条件不同,该选项结论不正确。
故选AC。
二、简答题(本大题共4题,共30分)
18. 古代冶金技术彰显了我国劳动人民的智慧。
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。金在自然界中主要以______
(填“单质”或“化合物”)形式存在,金具有______(填“难溶”或“易溶”)于水的性质。
(2)《淮南万毕术》记载有“曾青(指硫酸铜溶液)得铁化为铜”,该反应的化学方程式是______,反
应的基本类型是______
(3)《格致粗谈》记载“赤铜入炉甘石炼为黄铜,其色如金”。把赤铜(Cu O)和炉甘石、木炭粉混合
2
高温制得黄铜。
I、Cu O中铜元素的化合价是______,1mol Cu O中约含有______个Cu原子。
2 2
II、反应的化学方程式:X+Cu O+C Zn+2Cu+2CO↑。则炉甘石主要成分X的化学式是______,根据
2 2
产物可知黄铜中含有的金属是______
【答案】(1) ①. 单质 ②. 难溶
(2) ①. Fe+CuSO =FeSO +Cu ②. 置换反应
4 4
(3) ①. +1 ②. 1.204×1024 ③. ZnCO ④. Cu和Zn
3
【解析】
【小问1详解】
金的化学性质不活泼,则自然界中主要以单质形式存在;金难溶于水。
【小问2详解】
铁与硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为 ;该反应为一种单质
和一种化合物反应生成另一种反应和另一种化合物的反应,属于置换反应。
【小问3详解】
第7页/共13页
学科网(北京)股份有限公司Ⅰ、Cu O中,氧元素的化合价为-2价,设铜元素的化合价为x,根据“化合物中各元素化合价代数和为
2
零”,则2x+(-2)=0,解得x=+1;
1个Cu O分子中含有2个Cu原子,则1mol Cu O中约含有1mol×2×6.02×1023mol-1=1.204×1024。
2 2
Ⅱ、反应前后原子的种类和个数不变,等号右边有1个锌原子、2个铜原子、2个碳原子和4个氧原子,而
等号左边除X外,有2个铜原子、1个氧原子和1个碳原子,则还少1个锌原子、1个碳原子和3个氧原子,
则X为ZnCO 。
3
根据元素守恒,可知黄铜中含有的金属为铜和锌。
19. 二氧化碳具有广泛的应用价值。
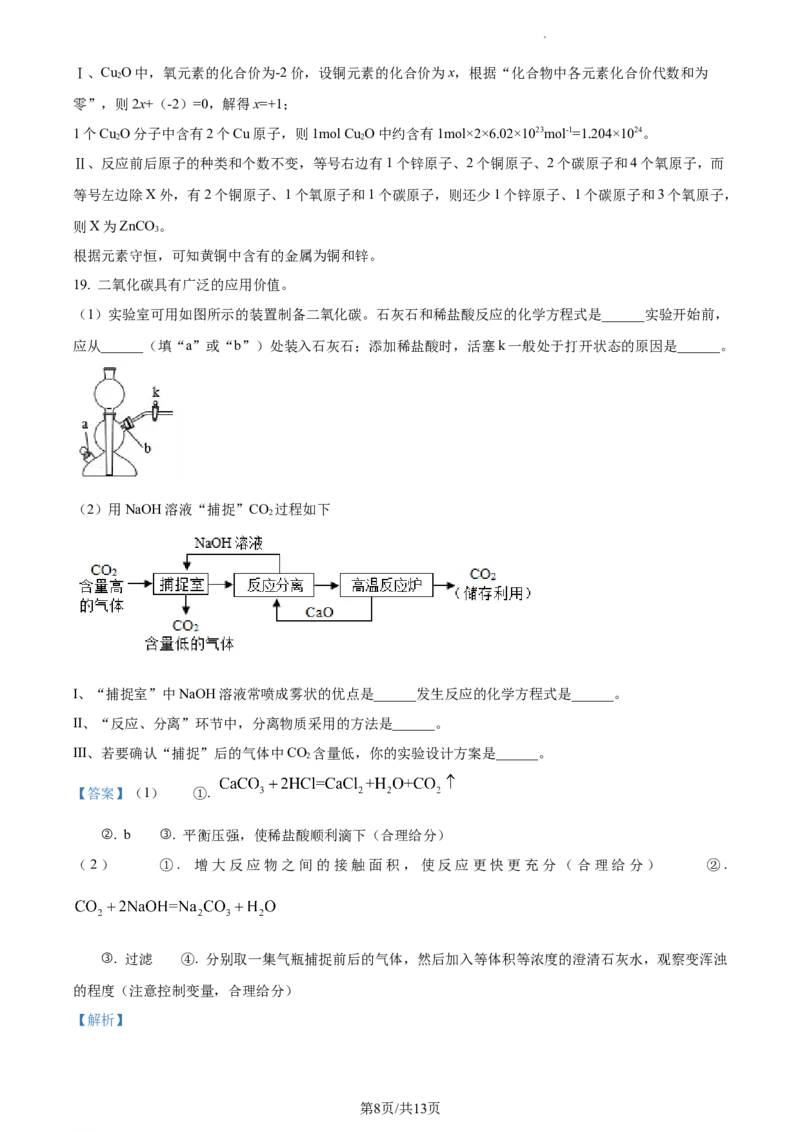
(1)实验室可用如图所示的装置制备二氧化碳。石灰石和稀盐酸反应的化学方程式是______实验开始前,
应从______(填“a”或“b”)处装入石灰石;添加稀盐酸时,活塞k一般处于打开状态的原因是______。
(2)用NaOH溶液“捕捉”CO 过程如下
2
I、“捕捉室”中NaOH溶液常喷成雾状的优点是______发生反应的化学方程式是______。
II、“反应、分离”环节中,分离物质采用的方法是______。
III、若要确认“捕捉”后的气体中CO 含量低,你的实验设计方案是______。
2
【答案】(1) ①.
②. b ③. 平衡压强,使稀盐酸顺利滴下(合理给分)
(2) ①. 增大反应物之间的接触面积,使反应更快更充分(合理给分) ②.
③. 过滤 ④. 分别取一集气瓶捕捉前后的气体,然后加入等体积等浓度的澄清石灰水,观察变浑浊
的程度(注意控制变量,合理给分)
【解析】
第8页/共13页
学科网(北京)股份有限公司【小问1详解】
石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:
;
启普发生器中,固体试剂由容器上的气体出口加入,故应从b处加入石灰石;
添加稀盐酸时,活塞k一般处于打开状态的原因是:平衡压强,使稀盐酸顺利滴下;
【小问2详解】
I、“捕捉室”中NaOH溶液常喷成雾状的优点是:增大反应物之间的接触面积,使反应更快更充分;
发生反应为二氧化碳和氢氧化钠反应生成碳酸钠和水,该反应的化学方程式为:
;
II、“反应、分离”环节中,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化
钠,故分离物质采用的方法是过滤,过滤可实现固液分离;
III、检验二氧化碳应选择澄清石灰水,因为二氧化碳能使澄清石灰水变浑浊,故若要确认“捕捉”后的气
体中CO 含量低,可分别取一集气瓶捕捉前后的气体,然后加入等体积等浓度的澄清石灰水,观察变浑浊
2
的程度,“捕捉”后的气体反应后的浑浊现象不明显,说明“捕捉”后的气体中CO 含量低。
2
20. 氢氧化钠是重要的化工原料,在生产过程中常含少量的氯化钠杂质。
(1)氢氧化钠溶液的pH______7(填“>”、“<”或 “=”)。
(2)检验NaOH样品中含有NaCl杂质。
操作 现象 结论
步骤一:取少量样品溶于水,先滴入
______
酚酞试液,再滴入足量稀硝酸
样品中含有NaCl
步骤二:在上述反应所得的溶液中滴
产生白色沉淀
加______溶液
(3)提纯NaOH样品。
氯化钠和氢氧化钠的部分溶解度数据如下表。
温度(℃) 0 20 60 80
NaCl 35.7 36.0 37.1 38.4
NaOH 42 109 174 314
I、60℃时,NaCl的溶解度为______g/100g水;20℃时,10g水中最多溶解NaOH_______g。
第9页/共13页
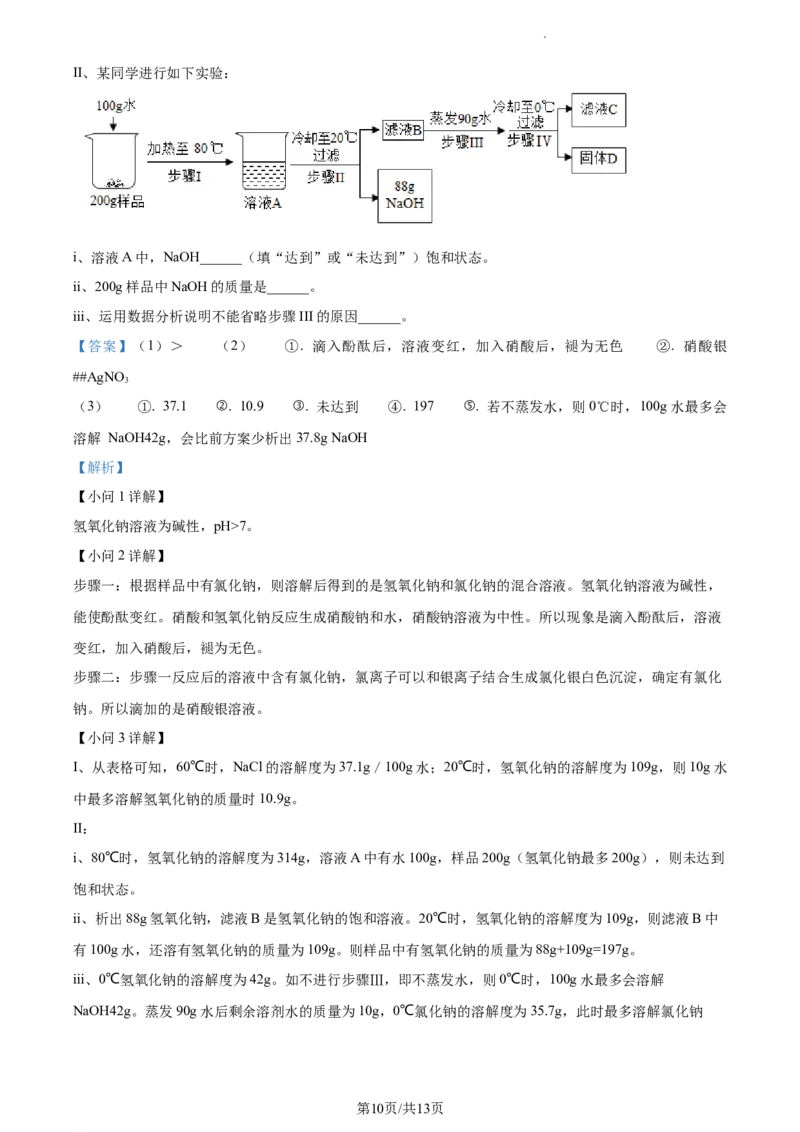
学科网(北京)股份有限公司II、某同学进行如下实验:
i、溶液A中,NaOH______(填“达到”或“未达到”)饱和状态。
ii、200g样品中NaOH的质量是______。
iii、运用数据分析说明不能省略步骤III的原因______。
【答案】(1)> (2) ①. 滴入酚酞后,溶液变红,加入硝酸后,褪为无色 ②. 硝酸银
##AgNO
3
(3) ①. 37.1 ②. 10.9 ③. 未达到 ④. 197 ⑤. 若不蒸发水,则0℃时,100g水最多会
溶解 NaOH42g,会比前方案少析出37.8g NaOH
【解析】
【小问1详解】
氢氧化钠溶液为碱性,pH>7。
【小问2详解】
步骤一:根据样品中有氯化钠,则溶解后得到的是氢氧化钠和氯化钠的混合溶液。氢氧化钠溶液为碱性,
能使酚酞变红。硝酸和氢氧化钠反应生成硝酸钠和水,硝酸钠溶液为中性。所以现象是滴入酚酞后,溶液
变红,加入硝酸后,褪为无色。
步骤二:步骤一反应后的溶液中含有氯化钠,氯离子可以和银离子结合生成氯化银白色沉淀,确定有氯化
钠。所以滴加的是硝酸银溶液。
【小问3详解】
I、从表格可知,60℃时,NaCl的溶解度为37.1g/100g水;20℃时,氢氧化钠的溶解度为109g,则10g水
中最多溶解氢氧化钠的质量时10.9g。
II:
i、80℃时,氢氧化钠的溶解度为314g,溶液A中有水100g,样品200g(氢氧化钠最多200g),则未达到
饱和状态。
ii、析出88g氢氧化钠,滤液B是氢氧化钠的饱和溶液。20℃时,氢氧化钠的溶解度为109g,则滤液B中
有100g水,还溶有氢氧化钠的质量为109g。则样品中有氢氧化钠的质量为88g+109g=197g。
iii、0℃氢氧化钠的溶解度为42g。如不进行步骤Ⅲ,即不蒸发水,则0℃时,100g水最多会溶解
NaOH42g。蒸发90g水后剩余溶剂水的质量为10g,0℃氯化钠的溶解度为35.7g,此时最多溶解氯化钠
第10页/共13页
学科网(北京)股份有限公司3.57g,比样品中的200g-197g=3g多,氯化钠不会析出。此时10g水最多溶解氢氧化钠的质量为4.2g。则若
不蒸发水会比前方案少析出42g-4.2g=37.8g,所以不能省略步骤Ⅲ。
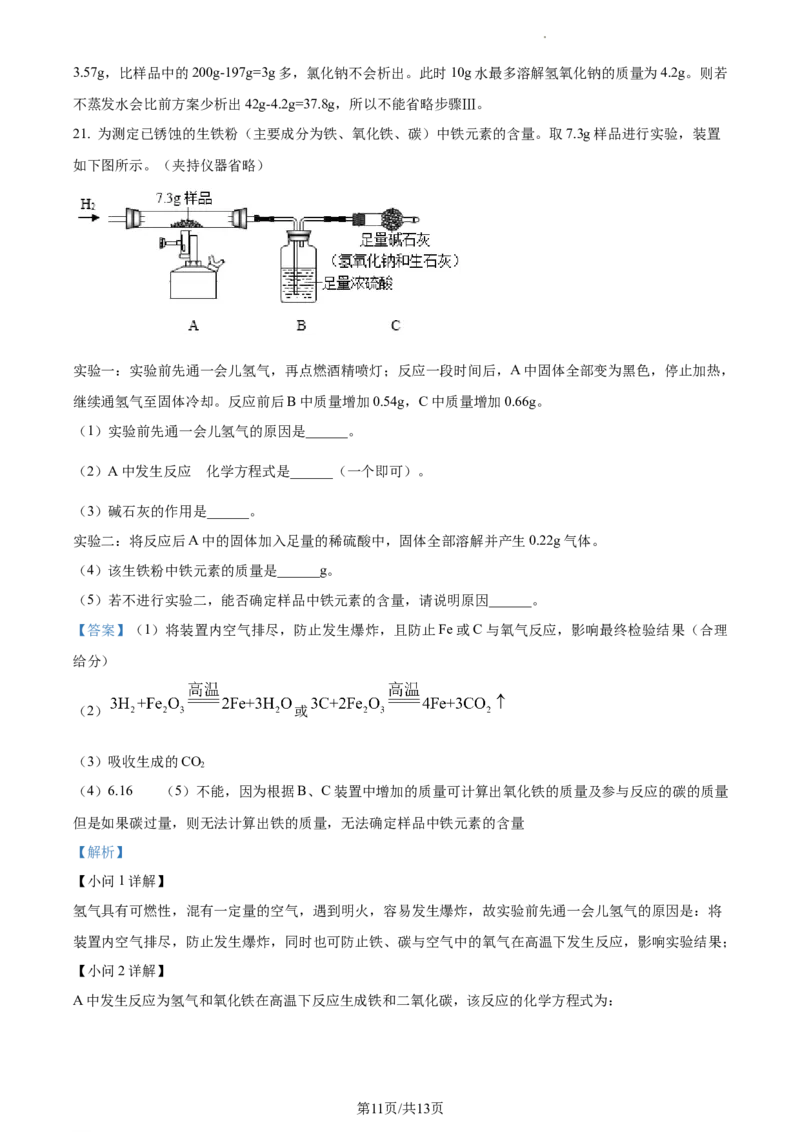
21. 为测定已锈蚀的生铁粉(主要成分为铁、氧化铁、碳)中铁元素的含量。取7.3g样品进行实验,装置
如下图所示。(夹持仪器省略)
实验一:实验前先通一会儿氢气,再点燃酒精喷灯;反应一段时间后,A中固体全部变为黑色,停止加热,
继续通氢气至固体冷却。反应前后B中质量增加0.54g,C中质量增加0.66g。
(1)实验前先通一会儿氢气的原因是______。
的
(2)A中发生反应 化学方程式是______(一个即可)。
(3)碱石灰的作用是______。
实验二:将反应后A中的固体加入足量的稀硫酸中,固体全部溶解并产生0.22g气体。
(4)该生铁粉中铁元素的质量是______g。
(5)若不进行实验二,能否确定样品中铁元素的含量,请说明原因______。
【答案】(1)将装置内空气排尽,防止发生爆炸,且防止Fe或C与氧气反应,影响最终检验结果(合理
给分)
(2) 或
(3)吸收生成的CO
2
(4)6.16 (5)不能,因为根据B、C装置中增加的质量可计算出氧化铁的质量及参与反应的碳的质量
但是如果碳过量,则无法计算出铁的质量,无法确定样品中铁元素的含量
【解析】
【小问1详解】
氢气具有可燃性,混有一定量的空气,遇到明火,容易发生爆炸,故实验前先通一会儿氢气的原因是:将
装置内空气排尽,防止发生爆炸,同时也可防止铁、碳与空气中的氧气在高温下发生反应,影响实验结果;
【小问2详解】
A中发生反应为氢气和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:
第11页/共13页
学科网(北京)股份有限公司,碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:
;
【小问3详解】
二氧化碳能与氢氧化钠反应生成碳酸钠和水,故碱石灰的作用是:吸收反应生成的二氧化碳;
【小问4详解】
将反应后A中的固体加入足量的稀硫酸中,铁能与稀硫酸反应生成硫酸亚铁和氢气,碳和稀硫酸不反应,
固体全部溶解,说明固体中不含碳,根据质量守恒定律,化学反应前后,元素的种类和质量不变,则反应
后得到铁的质量与铁粉中铁元素的质量相同。
解:设反应后铁的质量为x
x=6.16g
则该生铁粉中铁元素的质量是6.16g;
【小问5详解】
B装置增加的质量为氢气和氧化铁反应生成水的质量,可根据生成水的质量计算出与氢气反应的氧化铁的
质量,C装置增加的质量为反应生成二氧化碳的质量,可根据二氧化碳的质量计算出与碳反应的氧化铁的
质量及参加反应的碳的质量,故可计算出已锈蚀的生铁粉中氧化铁的质量,但是碳可能完全反应,也可能
过量,如果碳过量,则无法计算出铁的质量,无法确定样品中铁元素的含量,故若不进行实验二,不能确
定样品中铁元素的含量。
第12页/共13页
学科网(北京)股份有限公司第13页/共13页
学科网(北京)股份有限公司