文档内容
化学部分
相对原子质量: H-1 C-12 O-16 Na-23 Ca-40
五、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮檫去,重新
填涂。
第21-34题,每题均只有1个正确选项。
1. 属于化学变化的是
A. 苹果榨汁 B. 酒精挥发 C. 冰块融化 D. 钢铁生锈
【答案】D
【解析】
【详解】A、苹果榨汁时没有生成新物质,属于物理变化,选项错误;
B、酒精挥发只是物质的状态发生了变化,没有生成新物质,属于物理变化,选项错误;
C、冰块融化只是物质的状态发生了变化,没有生成新物质,属于物理变化,选项错误;
D、钢铁生锈后说出来新物质,属于化学变化,选项正确,故选D。
2. 属于氧化物的是
A. O B. CO C. NaOH D. NaCO
2 2 2 3
【答案】B
【解析】
【详解】A、氧气是由氧元素组成的纯净物,属于单质,选项错误;
B、氧化物是由两种元素组成,其中一种元素为氧元素的纯净物,二氧化碳是由碳元素和氧元素两种组成
的纯净物,属于氧化物,选项正确;
C、氢氧化钠是由钠元素、氧元素和氢元素组成的纯净物,属于碱,选项错误;
C、碳酸钠是由钠元素、碳元素和氧元素组成的纯净物,属于盐,选项错误;
故选:B。
3. 下列物质未计入空气污染指数项目的是
A. 二氧化硫 B. 二氧化氮 C. 二氧化碳 D. 可吸入颗粒物
【答案】C
【解析】
【详解】A、二氧化硫有毒,污染空气,计入空气污染指数项目,不符合题意;
B、二氧化氮有毒,污染空气,计入空气污染指数项目,不符合题意;
C、二氧化碳无毒且为空气的成分之一,不被计入空气污染指数项目,符合题意;
第1页/共14页
学科网(北京)股份有限公司D、可吸入颗粒物污染空气,计入空气污染指数项目,不符合题意;
故选:C。
4. 高铁酸钠(Na FeO)是一种常用的净水剂,其中铁元素的化合价是
2 4
A. +6 B. +3 C. +2 D. 0
【答案】A
【解析】
【详解】化合物中元素的化合价代数和为0,设铁元素化合价为 ,则 ,
故选:A。
5. 把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是
A. 冰块 B. 面粉 C. 汽油 D. 蔗糖
【答案】D
【解析】
【详解】A、水和冰是一种物质,不是混合物,故选项错误;
的
B、面粉不溶于水,不能和水形成均一、稳定 混合物,即不能够形成溶液,故选项错误;
C、汽油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项错误;
D、蔗糖易溶于水,形成均一、稳定的混合物,属于溶液,故选项正确;
故选D。
6. 氧元素以游离态存在的是
A. 水 B. 二氧化碳 C. 氧气 D. 一氧化碳
【答案】C
【解析】
【详解】A、水中氧元素以化合物的形式存在,属于氧元素的化合态;
B、二氧化碳中氧元素以化合物的形式存在,属于氧元素的化合态;
C、氧气中氧元素以单质的形式存在,属于氧元素的游离态;
D、一氧化碳中氧元素以化合物的形式存在,属于氧元素的化合态;
答案:C。
7. 属于同素异形体的是
A. 烧碱与纯碱 B. 水与冰 C. 金刚石与活性炭 D. 氧气与臭氧
【答案】D
【解析】
【分析】 同素异形体是相同元素组成,不同形态的单质;
第2页/共14页
学科网(北京)股份有限公司【详解】A、烧碱是NaOH,纯碱是NaCO,两者都是化合物,不属于同素异形体;
2 3
B、水与冰都是由水分子构成,属于同种物质,不属于同素异形体;
C、金刚石是碳单质,活性炭的主要成分是碳,属于混合物,则两者不属于同素异形体;
D、O、O 都是由氧元素组成的单质,则属于同素异形体。
2 3
故选D。
8. 有关实验现象的描述正确的是
A. 硫在空气中燃烧,生成二氧化硫气体
B. 红磷在空气中燃烧,产生白色烟雾
C. 将紫色的石蕊溶液滴入稀硫酸中,溶液变为红色
D. 稀盐酸中放入少量铁锈,溶液变蓝色
【答案】C
【解析】
【详解】A、硫在空气中燃烧,生成有刺激性气味的气体,生成二氧化硫是实验结论,故A不符合题意;
B、红磷在空气中燃烧,产生大量白烟,故B不符合题意;
C、硫酸能使石蕊溶液变红,将紫色的石蕊溶液滴入稀硫酸中,所以溶液变为红色,故C符合题意;
D、稀盐酸中放入少量铁锈(铁锈主要成分氧化铁),氧化铁和盐酸反应生成氯化铁和水,溶液变黄色,
故D不符合题意。
故选C。
9. 属于复合肥的是
A. KNO B. NH Cl C. Ca (PO ) D. CO(NH)
3 4 3 4 2 2 2
【答案】A
【解析】
【详解】A、KNO 中含有氮元素和钾元素,属于复合肥,故A正确;
3
B、NH Cl中含有氮元素,属于氮肥,故B错误;
4
C、Ca (PO ) 中含有磷元素,属于磷肥,故C错误;
3 4 2
D、CO(NH) 中含有氮元素,属于氮肥,故D错误。
2 2
故选:A。
10. 化学方程式书写正确的是
A. CO+CuO Cu+CO ↑ B. C+CO 2CO
2 2
C. 4Fe+3O 2Fe O D. CO+Ca(OH) = CaCO+H O
2 2 3 2 2 3 2
第3页/共14页
学科网(北京)股份有限公司【答案】B
【解析】
【详解】A、一氧化碳是气体,生成物二氧化碳不标记气体符号,化学方程式为 ,
故选项书写错误;
B、CO 与C在高温的条件下反应生成CO,化学反应方程式为:C+CO 2CO,故选项书写正确;
2 2
C、Fe在O 中燃烧生成Fe O,化学反应方程式为:3Fe+2O Fe O,故选项书写错误;
2 3 4 2 3 4
D、CO 与Ca(OH) 反应生成CaCO 沉淀与HO,化学反应方程式为:CO+Ca(OH) = CaCO +H O,故
2 2 3 2 2 2 3 2
选项书写错误。 ↓
故选B。
11. 我国是最早使用湿法炼铜的国家,湿法炼铜涉及到的主要化学方程式是:Fe+CuSO═FeSO +Cu。这一
4 4
化学反应的类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
【答案】C
【解析】
【详解】A、化合反应是指由两种或两种以上物质反应生成一种物质的反应,不符合题意;
B、分解反应是指由一种物质生成两种或两种以上物质的反应,不符合题意;
C、置换反应是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应,符合题意;
D、复分解反应是指由两种化合物反应,生成另外两种化合物的反应,不符合题意。
故选C。
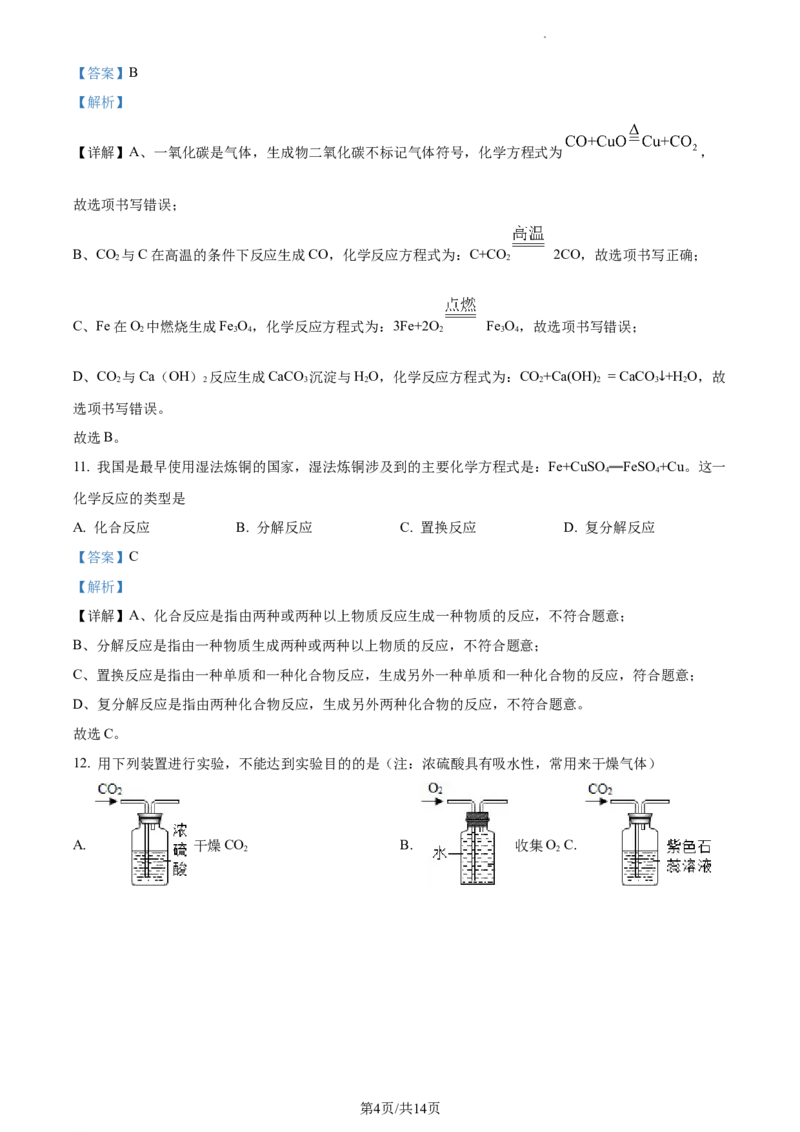
12. 用下列装置进行实验,不能达到实验目的的是(注:浓硫酸具有吸水性,常用来干燥气体)
A. 干燥CO B. 收集O C.
2 2
第4页/共14页
学科网(北京)股份有限公司验证CO 性质 D. 监控气体流速
2
【答案】B
【解析】
【详解】A、酸性干燥剂可以干燥酸性气体CO,故能达到实验目的;
2
B、因氧气不易溶于水,且密度小于水的密度,若用排水气法收集氧气,瓶内先装满水,氧气应该“短进
长出”,故不能达到实验目的;
C、二氧化碳的水溶液呈酸性,能使石蕊试液变红,所以该实验验证了CO 与HO反应生成HCO,故能
2 2 2 3
达到实验目的;
D、气体流速越快,气泡冒出的速度也越快,故能达到实验目的。
13. 能鉴别氢氧化钠溶液和氢氧化钙溶液的试剂是
A. 酚酞试液 B. 稀盐酸 C. 碳酸钠溶液 D. 硫酸铜溶液
【答案】C
【解析】
【详解】试题分析:鉴别物质所加试剂后要出现不同的现象,A选项氢氧化钠和氢氧化钙溶液都能使酚酞
试液变红色;B选项稀盐酸与二者反应无明显现象;C选项碳酸钠与氢氧化钠不反应,与氢氧化钙反应生
成沉淀;C选项二 者都能生成蓝色沉淀;故答案选择C
考点:物质的鉴别
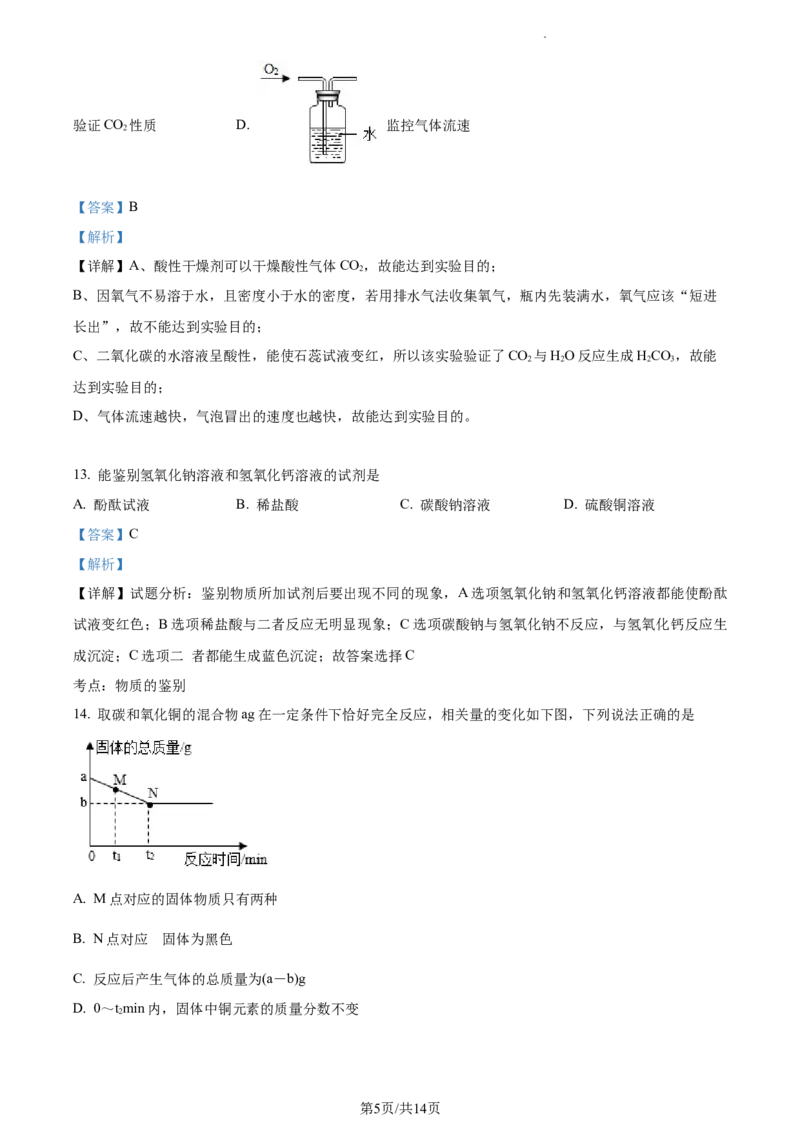
14. 取碳和氧化铜的混合物ag在一定条件下恰好完全反应,相关量的变化如下图,下列说法正确的是
A. M点对应的固体物质只有两种
的
B. N点对应 固体为黑色
C. 反应后产生气体的总质量为(a-b)g
D. 0~tmin内,固体中铜元素的质量分数不变
2
第5页/共14页
学科网(北京)股份有限公司【答案】C
【解析】
【详解】A、碳和氧化铜在高温下反应生成铜和二氧化碳,M点时还未完全反应,此时对应的固体物质有
氧化铜、碳、铜三种物质,不符合题意;
B、N点时,恰好完全反应,此时固体为铜,为紫红色,不符合题意;
C、根据质量守恒定律,化学反应前后,物质的总质量不变,故反应后产生气体的总质量为(a-b)g,符合
题意;
D、根据质量守恒定律,化学反应前后,元素的种类和质量不变,故铜元素的质量不变,但是0~tmin内,
2
固体的质量减少,故固体中铜元素的质量分数增大,不符合题意。
故选C。
第35~37题,每题有一个或两个正确选项。
15. 用0.9%的生理盐水可以清洗伤口,这里的0.9%表示
A. 氯化钠的溶质质量分数 B. 氯化钠的溶解度为0.9g/100g水
C. 每100g溶液中含0.9g氯化钠 D. 氯化钠与水的质量比为0.9:100
【答案】AC
【解析】
【详解】A、0.9%是氯化钠溶液的质量分数,A正确;
B、质量分数不是溶解度,在100g水中能溶解的氯化钠的最大质量大于0.9g,B错误;
C、0.9%说明每100g溶液中含0.9g氯化钠,C正确;
的
D、氯化钠 质量为0.9g时,水的质量对应为100g-0.9g=99.1g,质量比为0.9:99.1,D错误。
故选:AC。
16. 为验证Fe、Cu和Ag三种金属的活动性顺序,下列实验方案能达到实验目的的是
A. 将Fe、Cu分别加入AgNO 溶液中 B. 将Fe、Ag分别加入CuSO 溶液中
3 4
C. 将Fe、Cu和Ag分别加入稀盐酸中 D. 将Fe分别放入CuSO 、AgNO 溶液中
4 3
【答案】B
【解析】
【详解】A、将Fe、Cu分别加入AgNO 溶液中,铁、铜表面都有银白色固体析出,说明铜、铁金属活动
3
性比银强,无法比较铜、铁的金属活动性,实验方案不能达到实验目的;
B、将Fe、Ag分别加入CuSO 溶液中,铁表面有银白色固体析出,说明铁的金属活动性比铜强,银表面没
4
有明显现象,说明铜的金属活动性比银强,可以得出铁>铜>银,实验方案能达到实验目的;
C、将Fe、Cu和Ag分别加入稀盐酸中,铁表面有气泡生成,说明铁金属活动性比氢强,铜、银表面没有
明显现象,说明铜、银金属活动性比氢弱,可以得出铁>铜、铁>银,无法比较铜、银金属活动性,实验方
第6页/共14页
学科网(北京)股份有限公司案不能达到实验目的;
D、将Fe分别放入CuSO 、AgNO 溶液中,铁表面有红色固体析出,说明铁的金属活动性比铜强,铁丝表
4 3
面有白色固体析出,说明铁的金属活动性比银强,无法比较铜、银金属活动性,实验方案不能达到实验目
的;
答案:B。
17. 关于中和反应的说法正确的是
A. 凡是有盐和水生成的反应就是中和反应 B. 中和反应不一定属于复分解反应
C. 中和反应一定是放热的 D. 可以利用中和反应改良酸性土壤
【答案】CD
【解析】
【详解】A、有盐和水生成的反应不一定是中和反应,如二氧化碳和氢氧化钠的反应,故选项A说法错误;
B、中和反应是酸和碱互相交换成分生成另外两种化合物的反应,反应过程中有水生成,所以中和反应一
定属于复分解反应,故选项B说法错误;
C、中和反应是酸和碱反应生成盐和水的反应,属于放热反应,故选项C说法正确;
D、中和反应是酸和碱反应生成盐和水的反应,可以利用中和反应改良酸性土壤,故选项D说法正确;
故选:CD。
六、简答题(共 30分)
18. 化学知识在疫情防控中具有重要作用。
(1)免洗手凝胶消毒剂携带方便,使用时会闻到酒精的气味,说明分子具有的特性是____。
(2)公共场所佩戴口罩已成为防疫常态。生产医用口罩的过程中常用环氧乙烷(C HO)灭菌,环氧乙烷由
2 4
____种元素组成,其中碳、氢、氧三种元素的质量比为__________,0.5mol环氧乙烷中约含有______个氧
原子。
(3)日常消杀也是必需的防疫措施。二氧化氯(ClO )是一种常用消毒剂,其制取的一种原理是Cl+
2 2
2NaClO═ 2ClO + 2X,则X的化学式为________。
2 2
【答案】(1)分子在不断运动
(2) ①. 三##3 ②. 6:1:4 ③. 3.01×1023
(3)NaCl
【解析】
【小问1详解】
分子在不断运动,消毒剂中,有酒精气味的物质的分子运动到人的鼻孔处,使人温度酒精的气味,故填分
子在不断运动。
【小问2详解】
第7页/共14页
学科网(北京)股份有限公司由化学式可知,环氧乙烷由碳、氢、氧三种元素组成,故填三或3;
环氧乙烷中,碳、氢、氧三种元素的质量比 (12 2):(1 4):16 6:1:4,故填6:1:4;
由化学式可知,1个环氧乙烷反应中含有1个=氧原子×,则0.5m×ol环氧乙=烷中约含有氧原子的数目
0.5mol 6.02×1023个 3.01×1023,故填3.01×1023。
=【小问3×详解】 /mol=
由化学方程式可知,反应前出现了4个氯原子、2个钠原子和4个氧原子,反应后出现了2个氯原子和4个
氧原子,由质量守恒定律可知,反应后尚缺的2个氯原子、2个钠原子存在于2X中,则X的化学式为
NaCl,故填NaCl。
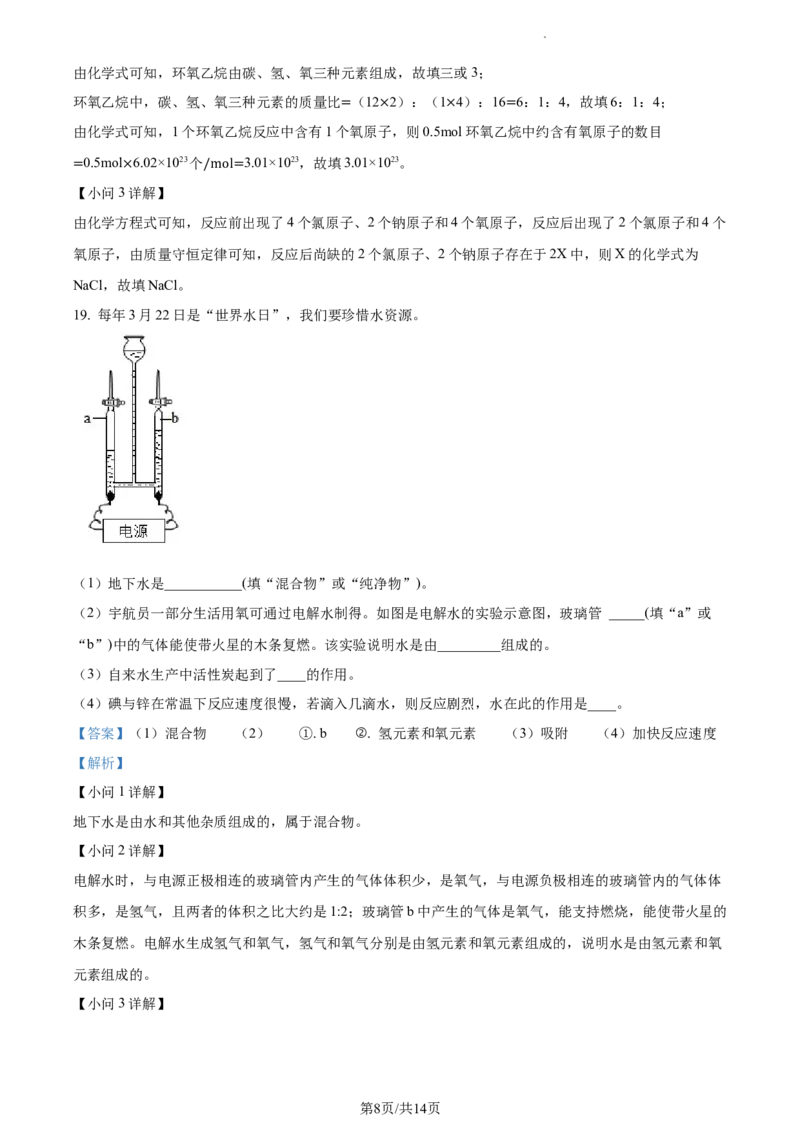
19. 每年3月22日是“世界水日”,我们要珍惜水资源。
(1)地下水是___________(填“混合物”或“纯净物”)。
(2)宇航员一部分生活用氧可通过电解水制得。如图是电解水的实验示意图,玻璃管 _____(填“a”或
“b”)中的气体能使带火星的木条复燃。该实验说明水是由_________组成的。
(3)自来水生产中活性炭起到了____的作用。
(4)碘与锌在常温下反应速度很慢,若滴入几滴水,则反应剧烈,水在此的作用是____。
【答案】(1)混合物 (2) ①. b ②. 氢元素和氧元素 (3)吸附 (4)加快反应速度
【解析】
【小问1详解】
地下水是由水和其他杂质组成的,属于混合物。
【小问2详解】
电解水时,与电源正极相连的玻璃管内产生的气体体积少,是氧气,与电源负极相连的玻璃管内的气体体
积多,是氢气,且两者的体积之比大约是1:2;玻璃管b中产生的气体是氧气,能支持燃烧,能使带火星的
木条复燃。电解水生成氢气和氧气,氢气和氧气分别是由氢元素和氧元素组成的,说明水是由氢元素和氧
元素组成的。
【小问3详解】
第8页/共14页
学科网(北京)股份有限公司活性炭具有疏松多孔的结构,可以吸附色素和异味,所以自来水生产中活性炭起到了吸附的作用。
【小问4详解】
碘与锌在常温下反应速度很慢,若滴入几滴水,则反应剧烈,反应速率变大,故水在此的作用是加快反应
速度。
20. 《天工开物》中记载了许多我国古代劳动人民对物质的认识和应用的事例。如:
为
石灰:“凡石灰经火焚炼 用。……用以砌墙、石,则筛去石块,水调黏合。”
硝石:“硝质与盐同母,大地之下潮气蒸成,现于地面。”
(1)文中石灰指氧化钙,请写出水调黏合过程中,氧化钙和水发生反应的化学方程式为____。
(2)硝石(硝酸钾)属于_________(选填“酸”“碱”或“盐)类物质,用洁净的铂丝蘸取硝酸钾溶液灼烧,
透过蓝色钴玻璃,火焰为_________色。
(3)下表是硝酸钾和氯化钠在不同温度下的溶解度。
温度(℃) 0 10 20 30 40 100
溶解度 NaCl 35.7 35.8 36.0 36.3 36.6 39.8
(g/100g
水) KNO 3 13.3 20.9 31.6 45.8 63.9 246
I.溶解度受温度的影响较大的物质是______(选填“KNO”或“NaCl”)。
3
II.20℃时,在50 g水中投入20 g NaCl,待充分溶解后,所得溶液的质量为____ g。
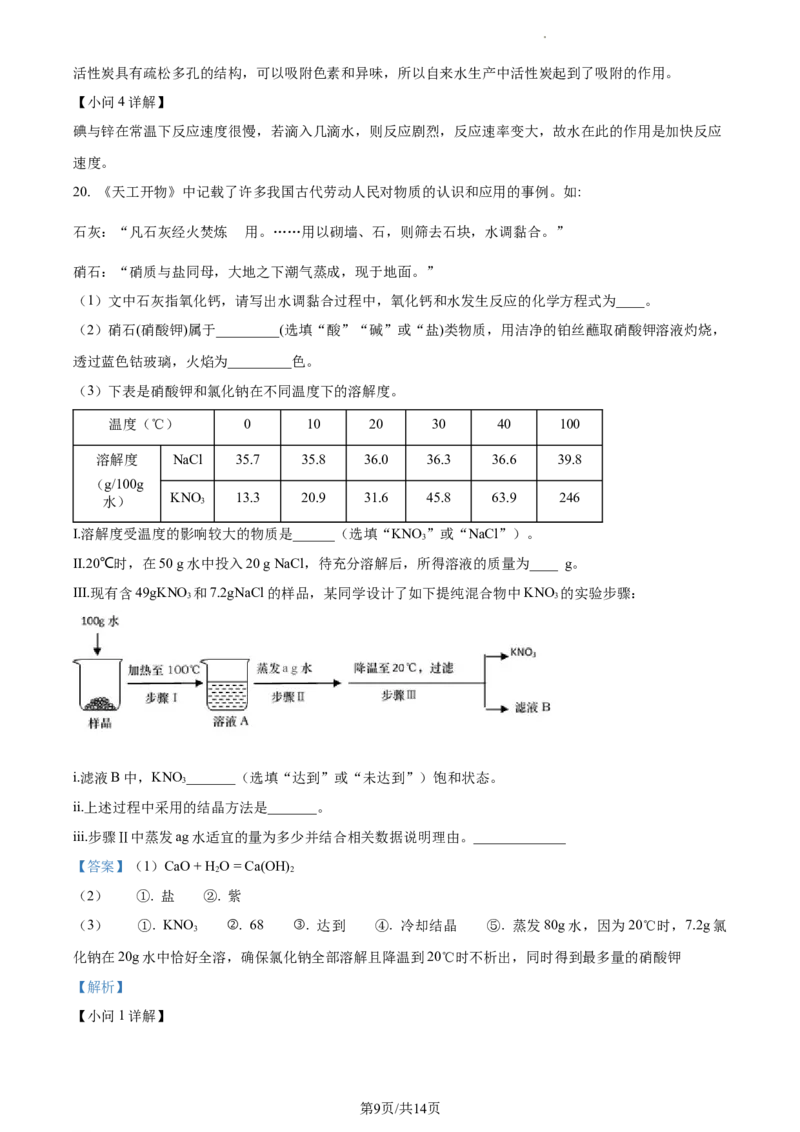
III.现有含49gKNO 和7.2gNaCl的样品,某同学设计了如下提纯混合物中KNO 的实验步骤:
3 3
i.滤液B中,KNO_______(选填“达到”或“未达到”)饱和状态。
3
ii.上述过程中采用的结晶方法是_______。
iii.步骤Ⅱ中蒸发ag水适宜的量为多少并结合相关数据说明理由。_____________
【答案】(1)CaO + H O = Ca(OH)
2 2
(2) ①. 盐 ②. 紫
(3) ①. KNO ②. 68 ③. 达到 ④. 冷却结晶 ⑤. 蒸发80g水,因为20℃时,7.2g氯
3
化钠在20g水中恰好全溶,确保氯化钠全部溶解且降温到20℃时不析出,同时得到最多量的硝酸钾
【解析】
【小问1详解】
第9页/共14页
学科网(北京)股份有限公司氧化钙和水发生反应生成氢氧化钙,化学方程式为CaO + H O = Ca(OH) ;
2 2
【小问2详解】
硝酸钾由硝酸根离子和钾离子构成,属于盐;钾离子的焰色反应火焰颜色是紫色;
【小问3详解】
I、从表中看出,硝酸钾的溶解度随温度的升高变化更大,故填KNO;
3
II、20℃时,氯化钠溶解度为36.0g,50g水可溶解18.0g氯化钠,故所得溶液的质量为50g+18.0g=68g;
III i、步骤三后得到硝酸钾固体和滤液,故滤液B中硝酸钾是饱和的;
ii、图中是先采用高温水溶解更多质量的硝酸钾,再冷却,使得硝酸钾溶解度下降、结晶出固体,采用的
结晶方法是冷却结晶;
iii、因为20℃时,7.2g氯化钠在20g水中恰好全部溶解,为确保氯化钠全部溶解且降温到20℃时不析出,
同时得到最多量的硝酸钾,可采用蒸发80g水。
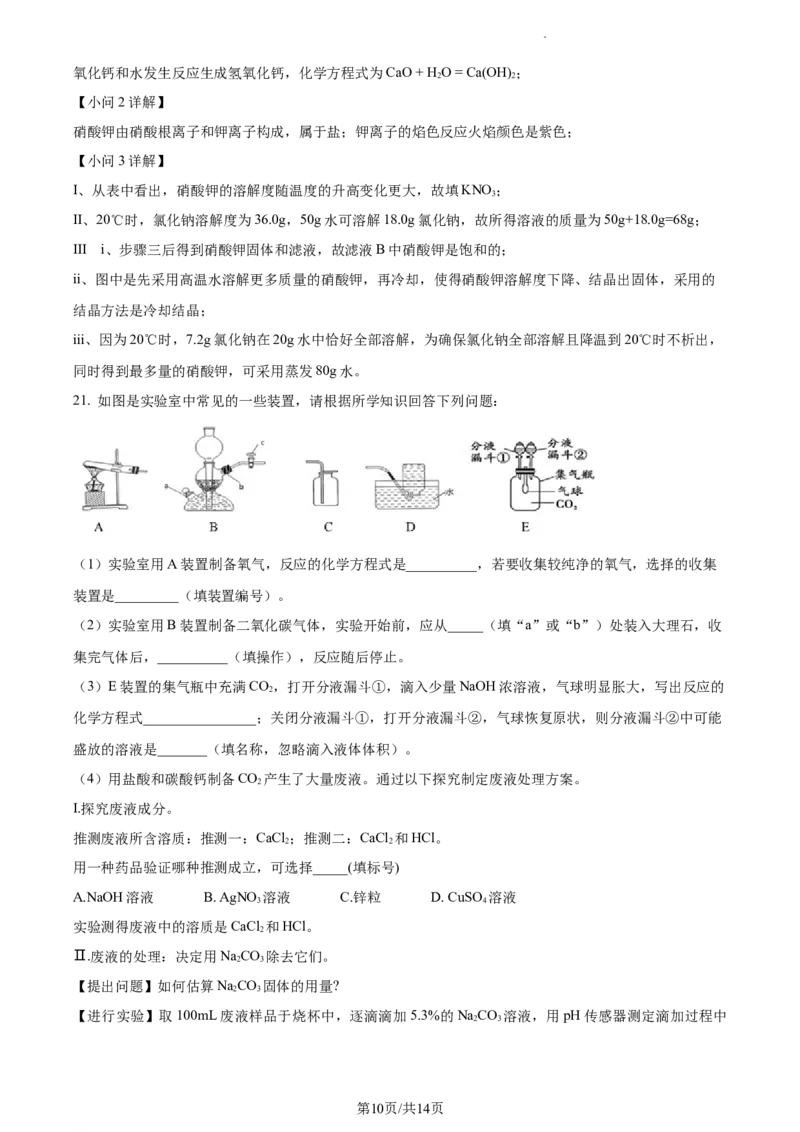
21. 如图是实验室中常见的一些装置,请根据所学知识回答下列问题:
(1)实验室用A装置制备氧气,反应的化学方程式是__________,若要收集较纯净的氧气,选择的收集
装置是_________(填装置编号)。
(2)实验室用B装置制备二氧化碳气体,实验开始前,应从_____(填“a”或“b”)处装入大理石,收
集完气体后,__________(填操作),反应随后停止。
(3)E装置的集气瓶中充满CO,打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出反应的
2
化学方程式________________;关闭分液漏斗①,打开分液漏斗②,气球恢复原状,则分液漏斗②中可能
盛放的溶液是_______(填名称,忽略滴入液体体积)。
(4)用盐酸和碳酸钙制备CO 产生了大量废液。通过以下探究制定废液处理方案。
2
I.探究废液成分。
推测废液所含溶质:推测一:CaCl ;推测二:CaCl 和HCl。
2 2
用一种药品验证哪种推测成立,可选择_____(填标号)
A.NaOH溶液 B. AgNO 溶液 C.锌粒 D. CuSO 溶液
3 4
实验测得废液中的溶质是CaCl 和HCl。
2
Ⅱ.废液的处理:决定用NaCO 除去它们。
2 3
【提出问题】如何估算NaCO 固体的用量?
2 3
【进行实验】取100mL废液样品于烧杯中,逐滴滴加5.3%的NaCO 溶液,用pH传感器测定滴加过程中
2 3
第10页/共14页
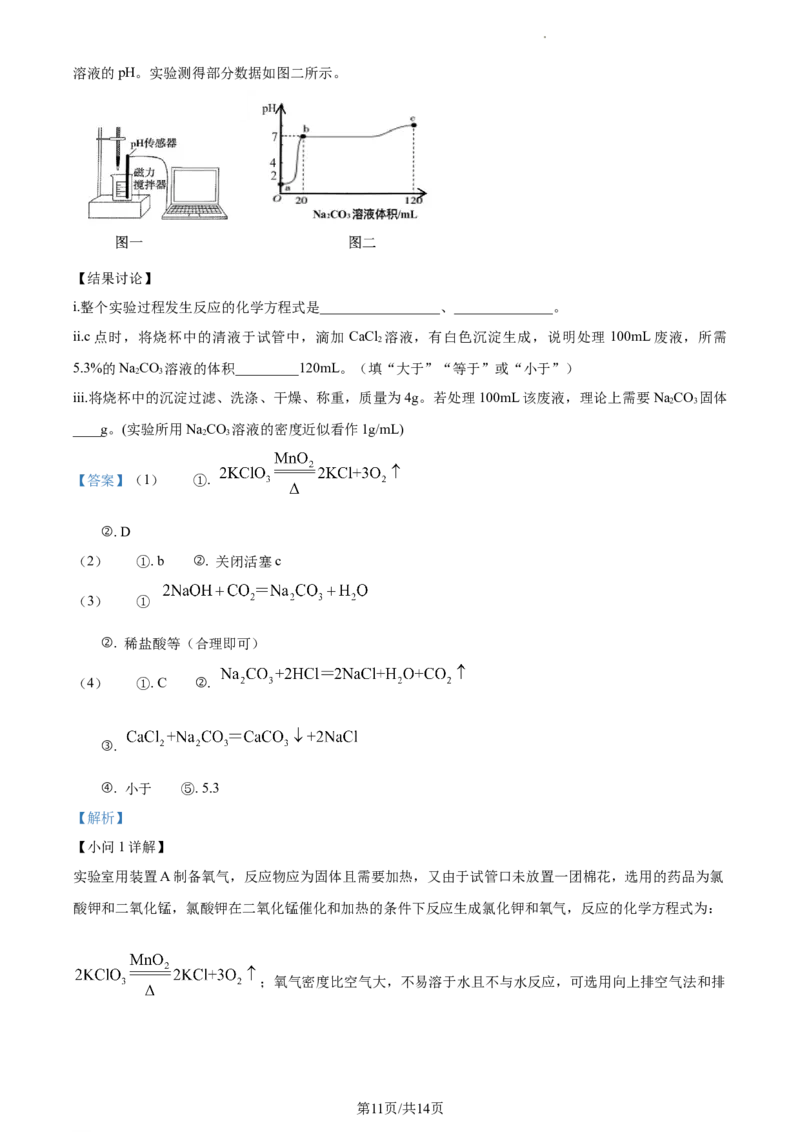
学科网(北京)股份有限公司溶液的pH。实验测得部分数据如图二所示。
【结果讨论】
i.整个实验过程发生反应的化学方程式是_________________、______________。
ii.c点时,将烧杯中的清液于试管中,滴加 CaCl 溶液,有白色沉淀生成,说明处理 100mL废液,所需
2
5.3%的NaCO 溶液的体积_________120mL。(填“大于”“等于”或“小于”)
2 3
iii.将烧杯中的沉淀过滤、洗涤、干燥、称重,质量为4g。若处理100mL该废液,理论上需要NaCO 固体
2 3
____g。(实验所用NaCO 溶液的密度近似看作1g/mL)
2 3
【答案】(1) ①.
②. D
(2) ①. b ②. 关闭活塞c
.
(3) ①
②. 稀盐酸等(合理即可)
(4) ①. C ②.
③.
④. 小于 ⑤. 5.3
【解析】
【小问1详解】
实验室用装置A制备氧气,反应物应为固体且需要加热,又由于试管口未放置一团棉花,选用的药品为氯
酸钾和二氧化锰,氯酸钾在二氧化锰催化和加热的条件下反应生成氯化钾和氧气,反应的化学方程式为:
;氧气密度比空气大,不易溶于水且不与水反应,可选用向上排空气法和排
第11页/共14页
学科网(北京)股份有限公司水法收集,排水法收集的气体更纯净,因此收集装置选D;
【小问2详解】
用装置B制备二氧化碳,实验开始前,应从b处装入大理石,从长颈漏斗上端加入稀盐酸,反应物一接触
立即产生气体,收集完气体后,关闭活塞c,装置B中压强增大,将稀盐酸“压”回长颈漏斗中,反应物
分离,反应随后停止;
【小问3详解】
E装置的集气瓶中充满CO,打开分液漏斗①,滴入少量NaOH浓溶液,二氧化碳与氢氧化钠溶液反应生
2
成碳酸钠和水,集气瓶中压强减小,气球明显胀大,涉及反应的化学方程式为:
;关闭分液漏斗①,打开分液漏斗②,气球恢复原状,说明分液漏斗②
中盛放的液体能与碳酸钠反应生成气体,则分液漏斗②中可能盛放的溶液是稀盐酸或稀硫酸等(合理即
可);
【小问4详解】
I.要验证推测一或推测二成立,即验证HCl是否存在即可;
A、氢氧化钠溶液能与氯化氢反应,但现象不明显,无法判断HCl是否存在,故A错误;
B、AgNO 溶液能与氯化钙和氯化氢反应生成白色氯化银沉淀,无法判断HCl是否存在,故B错误;
3
C、锌粒能与HCl反应产生气泡,不与氯化钙反应,若加入锌粒产生气泡说明推测二正确,若不产生气泡
说明推测一正确,故C正确;
D、CuSO 溶液不与氯化钙和氯化氢反应,无法判断HCl是否存在,故D错误;
4
故选C;
Ⅱ.[结果讨论]
i.由于实验测得废液中的溶质是CaCl 和HCl,加入的碳酸钠先与HCl反应生成氯化钠、水和二氧化碳,此
2
阶段溶液pH逐渐升高至7,,再与氯化钙反应生成碳酸钙和氯化钠此阶段溶液pH=7保持不变,反应的化学
方程式分别为: 、 ;当碳
酸钠过量后溶液的pH>7;
ii.c点时,将烧杯中的清液于试管中,滴加CaCl 溶液,有白色沉淀生成,说明碳酸钠过量,说明处理
2
100mL废液,所需5.3%的NaCO 溶液的体积小于120mL;
2 3
iii.设生成4g碳酸钙沉淀需要碳酸钠的质量为x
碳酸钠溶液的体积为: ;
第12页/共14页
学科网(北京)股份有限公司即80mL碳酸钠溶液中含有4.24g碳酸钠,则20mL碳酸钠溶液中含有 碳酸钠;则处理
100mL废液需要碳酸钠固体的质量为 ;
答:理论上需要NaCO 固体5.3g。
2 3
第13页/共14页
学科网(北京)股份有限公司第14页/共14页
学科网(北京)股份有限公司