文档内容
2023 学年第二学期九年级质量调研
综合测试样卷
考生注意:
1.试卷第1~20题为物理部分,第21~41题为化学部分,第42题开始为跨学科案例分析部分。
2.试卷满分135分。考试时间120分钟。
3.按要求在答题纸上作答,在试卷、草稿纸上答题一律无效。
化学部分
可能用到的相对原子质量:H-1 O-16 Fe-56 Cu-64 Ag-108
一、选择题(共20分)第21-34题,每题均只有一个正确选项。
1. 保存珍贵文物可用空气中含量最多的气体,该气体是
.
A 氮气 B. 氧气 C. 二氧化碳 D. 稀有气体
2. 下列物质在氧气中燃烧,能生成黑色固体物质的是
A. 红磷 B. 木炭 C. 镁条 D. 铁丝
3. 一氧化二氮(N O)在手术中常用作麻醉剂,其中氮元素的化合价为
2
A. -2 B. -1 C. +1 D. +2
4. 属于绿色能源的是
A. 煤 B. 石油 C. 天然气 D. 氢气
5. 溶液溶质为气体的是
A. 食盐水 B. 硝酸钾溶液 C. 盐酸 D. 澄清石灰水
6. 焰色反应火焰呈黄色的是
A. NaNO B. KOH C. CuSO D. BaCl
3 4 2
7. 山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,涂抹厨房中的下列某物质(括号内数值为pH )能明
显缓解不适,该物质是
A. 食醋(2.8-3.8) B. 食盐水(7.0) C. 鸡蛋清(7.6~8) D. 肥皂水(9-10)
8. 物质俗名正确的是
A. 氢氧化钠—纯碱 B. 汞—水银
C. 氧化钙—消石灰 D. 硫酸铜—胆矾
9. 碱性锌锰电池性能优越,其组成物质包括锌粉、氢氧化钾、二氧化锰、石墨等,这些物质的类别不包括
A. 酸 B. 碱
C. 单质 D. 氧化物
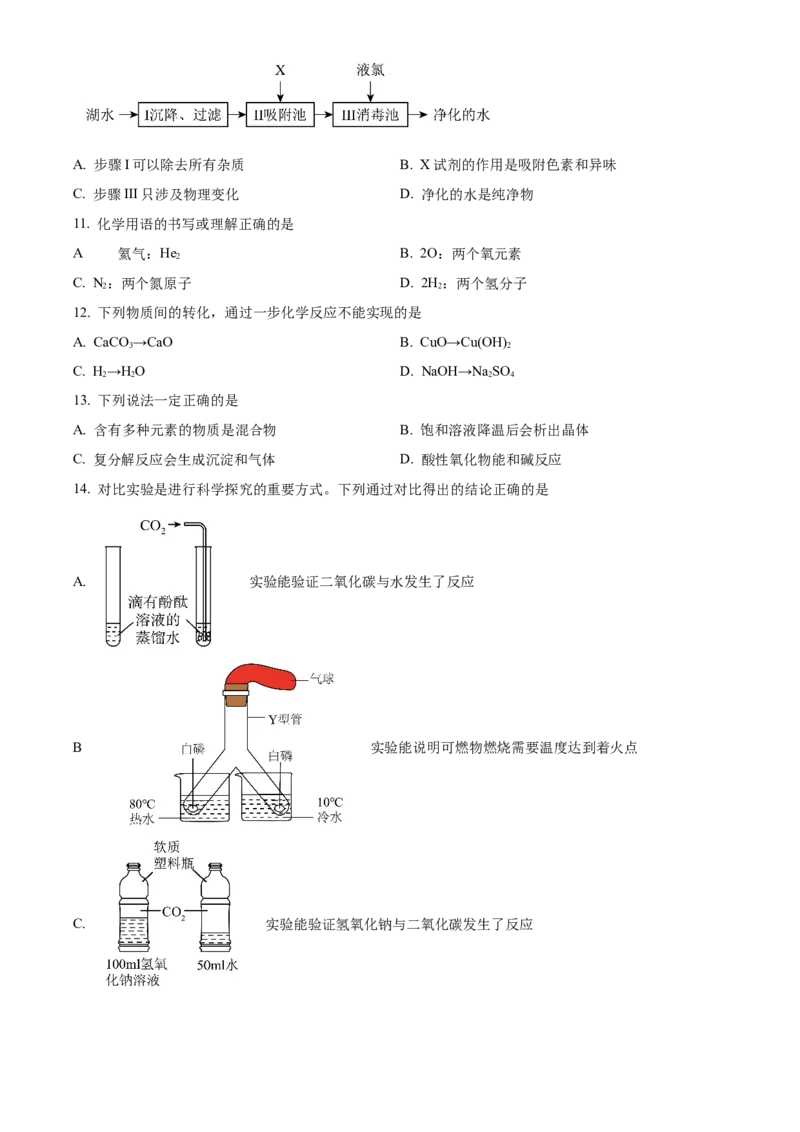
10. 水净化的主要步骤如图所示,有关说法正确的是A. 步骤I可以除去所有杂质 B. X试剂的作用是吸附色素和异味
C. 步骤III只涉及物理变化 D. 净化的水是纯净物
11. 化学用语的书写或理解正确的是
.
A 氦气:He B. 2O:两个氧元素
2
C. N:两个氮原子 D. 2H:两个氢分子
2 2
12. 下列物质间的转化,通过一步化学反应不能实现的是
A. CaCO →CaO B. CuO→Cu(OH)
3 2
C. H→HO D. NaOH→Na SO
2 2 2 4
13. 下列说法一定正确的是
A. 含有多种元素的物质是混合物 B. 饱和溶液降温后会析出晶体
C. 复分解反应会生成沉淀和气体 D. 酸性氧化物能和碱反应
14. 对比实验是进行科学探究的重要方式。下列通过对比得出的结论正确的是
A. 实验能验证二氧化碳与水发生了反应
B 实验能说明可燃物燃烧需要温度达到着火点
.
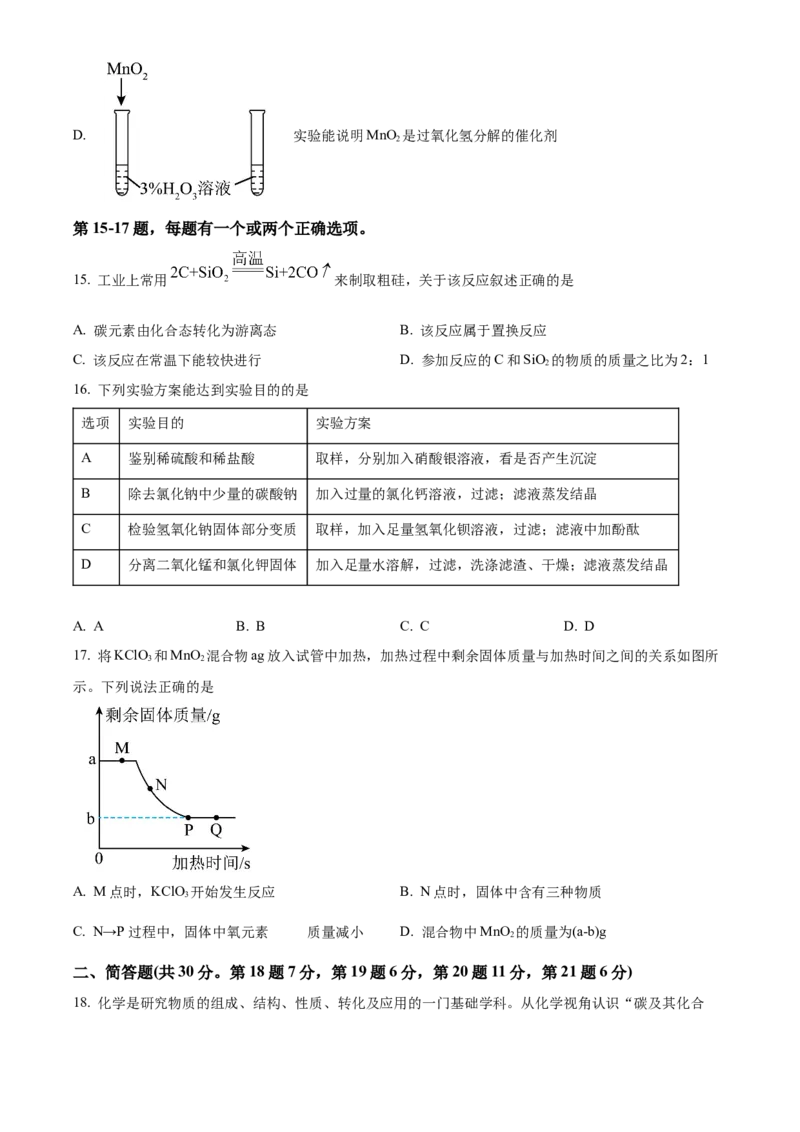
C. 实验能验证氢氧化钠与二氧化碳发生了反应D. 实验能说明MnO 是过氧化氢分解的催化剂
2
第15-17题,每题有一个或两个正确选项。
15. 工业上常用 来制取粗硅,关于该反应叙述正确的是
A. 碳元素由化合态转化为游离态 B. 该反应属于置换反应
C. 该反应在常温下能较快进行 D. 参加反应的C和SiO 的物质的质量之比为2:1
2
16. 下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 鉴别稀硫酸和稀盐酸 取样,分别加入硝酸银溶液,看是否产生沉淀
B 除去氯化钠中少量的碳酸钠 加入过量的氯化钙溶液,过滤;滤液蒸发结晶
C 检验氢氧化钠固体部分变质 取样,加入足量氢氧化钡溶液,过滤;滤液中加酚酞
D 分离二氧化锰和氯化钾固体 加入足量水溶解,过滤,洗涤滤渣、干燥;滤液蒸发结晶
A. A B. B C. C D. D
17. 将KClO 和MnO 混合物ag放入试管中加热,加热过程中剩余固体质量与加热时间之间的关系如图所
3 2
示。下列说法正确的是
A. M点时,KClO 开始发生反应 B. N点时,固体中含有三种物质
3
的
C. N→P过程中,固体中氧元素 质量减小 D. 混合物中MnO 的质量为(a-b)g
2
二、简答题(共30分。第18题7分,第19题6分,第20题11分,第21题6分)
18. 化学是研究物质的组成、结构、性质、转化及应用的一门基础学科。从化学视角认识“碳及其化合物”,回答下列问题。
(1)组成角度:CO和CO 均由___________元素组成。
2
(2)结构角度:CO和CO 分子构成不同,1molCO中约含___________个氧原子。
2
(3)性质角度:CO具有可燃性,可以作燃料,CO 不可燃也不助燃,可以用于___________。
2
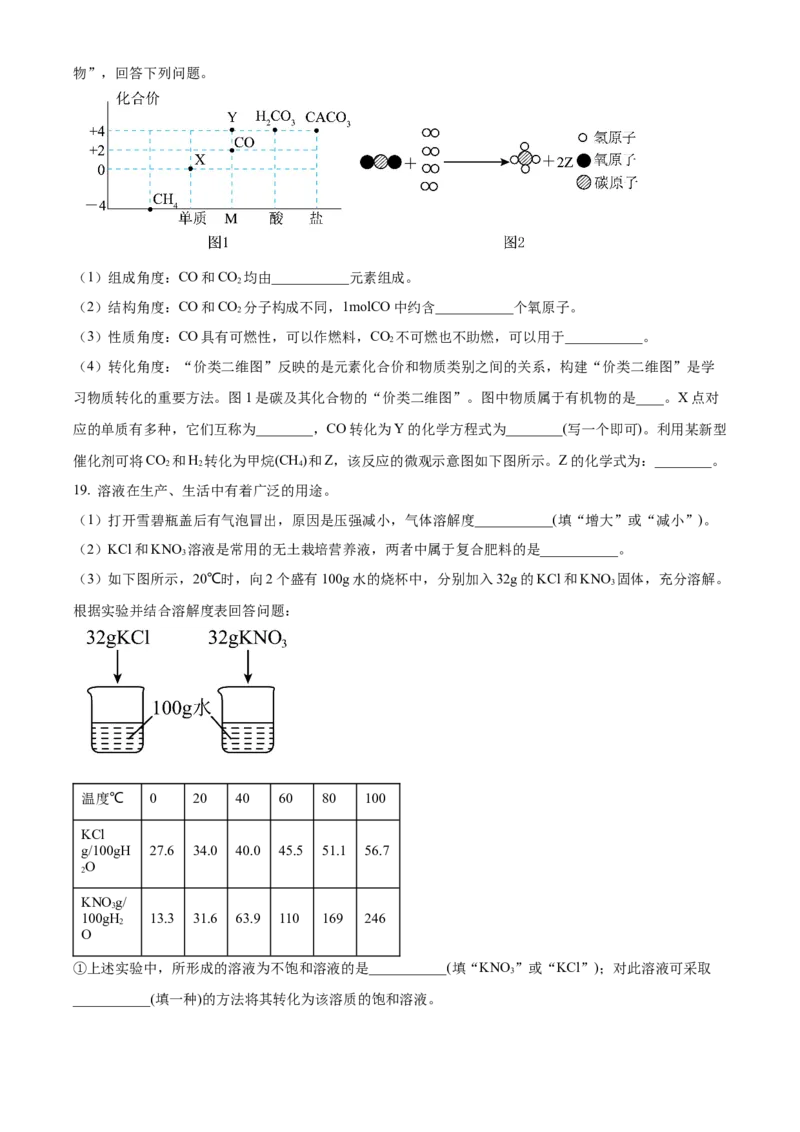
(4)转化角度:“价类二维图”反映的是元素化合价和物质类别之间的关系,构建“价类二维图”是学
习物质转化的重要方法。图1是碳及其化合物的“价类二维图”。图中物质属于有机物的是____。X点对
应的单质有多种,它们互称为________,CO转化为Y的化学方程式为________(写一个即可)。利用某新型
催化剂可将CO 和H 转化为甲烷(CH)和Z,该反应的微观示意图如下图所示。Z的化学式为:________。
2 2 4
19. 溶液在生产、生活中有着广泛的用途。
(1)打开雪碧瓶盖后有气泡冒出,原因是压强减小,气体溶解度___________(填“增大”或“减小”)。
(2)KCl和KNO 溶液是常用的无土栽培营养液,两者中属于复合肥料的是___________。
3
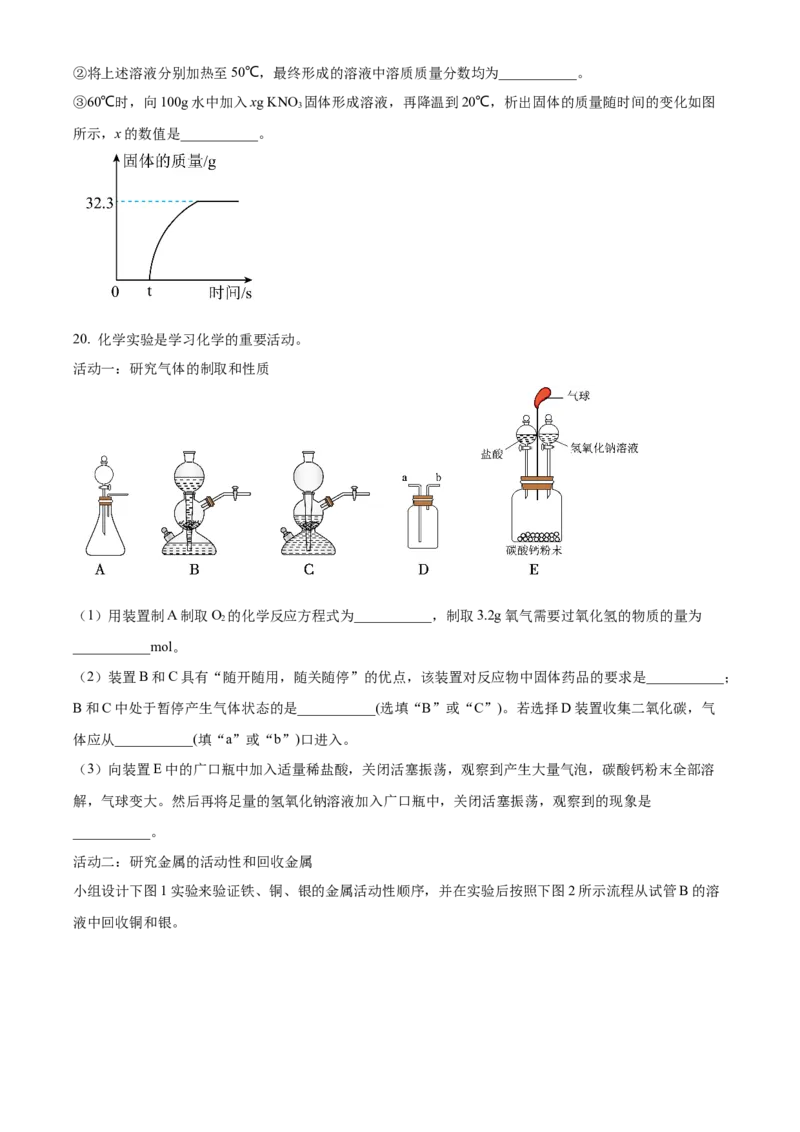
(3)如下图所示,20℃时,向2个盛有100g水的烧杯中,分别加入32g的KCl和KNO 固体,充分溶解。
3
根据实验并结合溶解度表回答问题:
温度℃ 0 20 40 60 80 100
KCl
g/100gH 27.6 34.0 40.0 45.5 51.1 56.7
O
2
KNOg/
3
100gH 13.3 31.6 63.9 110 169 246
2
O
①上述实验中,所形成的溶液为不饱和溶液的是___________(填“KNO”或“KCl”);对此溶液可采取
3
___________(填一种)的方法将其转化为该溶质的饱和溶液。②将上述溶液分别加热至50℃,最终形成的溶液中溶质质量分数均为___________。
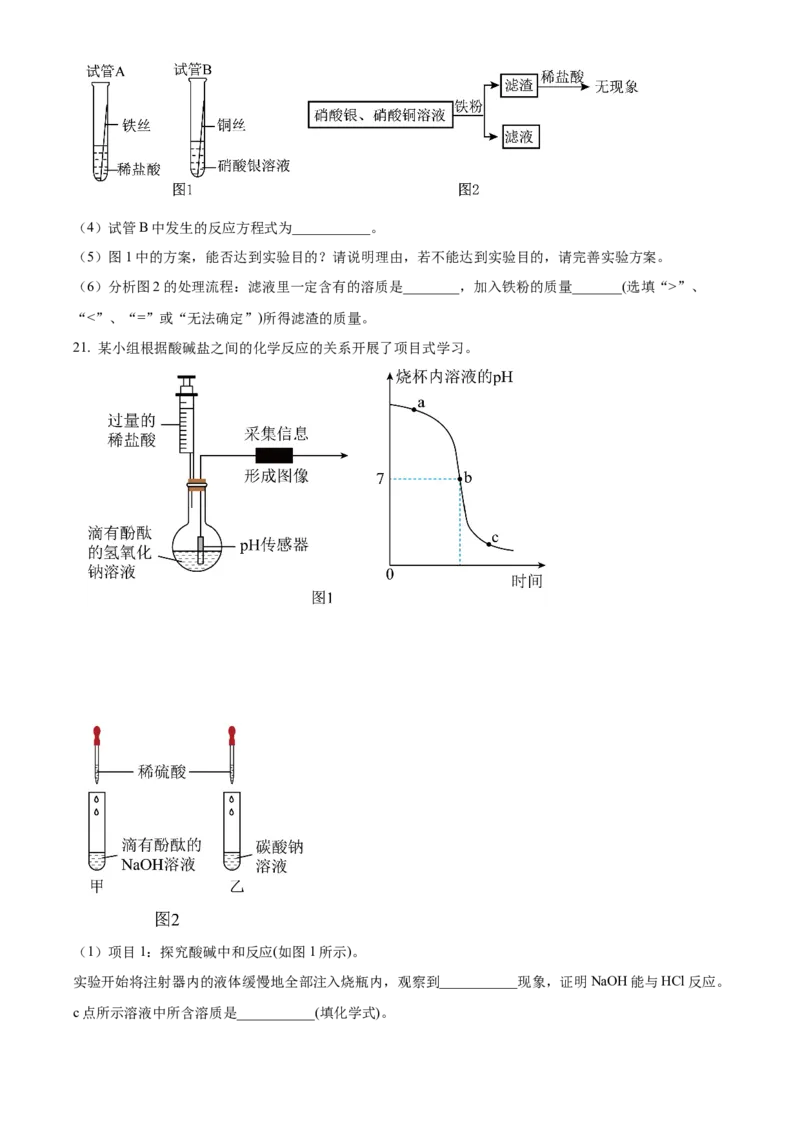
③60℃时,向100g水中加入xg KNO 固体形成溶液,再降温到20℃,析出固体的质量随时间的变化如图
3
所示,x的数值是___________。
20. 化学实验是学习化学的重要活动。
活动一:研究气体的制取和性质
(1)用装置制A制取O 的化学反应方程式为___________,制取3.2g氧气需要过氧化氢的物质的量为
2
___________mol。
(2)装置B和C具有“随开随用,随关随停”的优点,该装置对反应物中固体药品的要求是___________;
B和C中处于暂停产生气体状态的是___________(选填“B”或“C”)。若选择D装置收集二氧化碳,气
体应从___________(填“a”或“b”)口进入。
(3)向装置E中的广口瓶中加入适量稀盐酸,关闭活塞振荡,观察到产生大量气泡,碳酸钙粉末全部溶
解,气球变大。然后再将足量的氢氧化钠溶液加入广口瓶中,关闭活塞振荡,观察到的现象是
___________。
活动二:研究金属的活动性和回收金属
小组设计下图1实验来验证铁、铜、银的金属活动性顺序,并在实验后按照下图2所示流程从试管B的溶
液中回收铜和银。(4)试管B中发生的反应方程式为___________。
(5)图1中的方案,能否达到实验目的?请说明理由,若不能达到实验目的,请完善实验方案。
(6)分析图2的处理流程:滤液里一定含有的溶质是________,加入铁粉的质量_______(选填“>”、
“<”、“=”或“无法确定”)所得滤渣的质量。
21. 某小组根据酸碱盐之间的化学反应的关系开展了项目式学习。
(1)项目1:探究酸碱中和反应(如图1所示)。
实验开始将注射器内的液体缓慢地全部注入烧瓶内,观察到___________现象,证明NaOH能与HCl反应。
c点所示溶液中所含溶质是___________(填化学式)。(2)项目2:探究酸碱盐之间反应(如图2所示)。
把甲、乙反应后的溶液倒入同一烧杯中发现溶液显红色,决定继续对烧杯内溶液中溶质成分进行探究。
【提出问题】反应后所得溶液中溶质 的成分是什么?
【提出猜想】烧杯内溶液中的溶质成分可能有:
猜想一:NaSO 、NaCO 猜想二:___________。
2 4 2 3
猜想三:NaSO 、NaOH、NaCO 猜想四:NaSO 、HSO
2 4 2 3 2 4 2 4
【实验分析】通过分析,大家认为猜想四不成立,原因是___________。
【实验探究】同学们对剩余的几种猜想继续探究(提示:BaCl 溶液呈中性)
2
实验操作 实验现象及结论
①取烧杯中的溶液于试管中,加入过量的
___________,说明猜想一不成立
BaCl 溶液
2
②过滤,再向沉淀中加入___________。 沉淀部分溶解有气泡产生,说明猜想三成立