文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
2022 学年第二学期高三年级学业质量调研
化学学科试卷
考生注意:
1.本考试设试卷和答题纸两部分,所有答题必须涂或写在答题纸上;做在试卷上一律不得分。
2.答题前,考生务必在答题纸上将学校、姓名及考生号填写清楚,并在规定的区域填涂相关
信息。答题时客观题用2B铅笔涂写,主观题用黑色水笔填写。
3.答题纸与试卷在试题编号上是一一对应的,答题时应特别注意,不能错位。
可能用到的相对原子质量:H-1 C-12 O-16 S-32 N-14 Na-23
一、选择题(本题共40分,每小题2分,每题只有一个正确选项)。
1. 下列贡献与中国科学家有关的是
A. 发现青蒿素 B. 发明合成氨技术
C. 提出电子云模型 D. 提出元素周期律
2. 下列有关化学用语的表述正确的是
A. 乙烯的结构简式:CHCH B. 乙酸的分子式:CHCOOH
2 2 3
C. 铝离子的结构示意图: D. OH—的电子式:
3. 下列关于石油的说法正确的是
A. 石油主要含有碳、氢两种元素 B. 石油属于可再生矿物能源
C. 石油裂化属于物理变化 D. 石油分馏属于化学变化
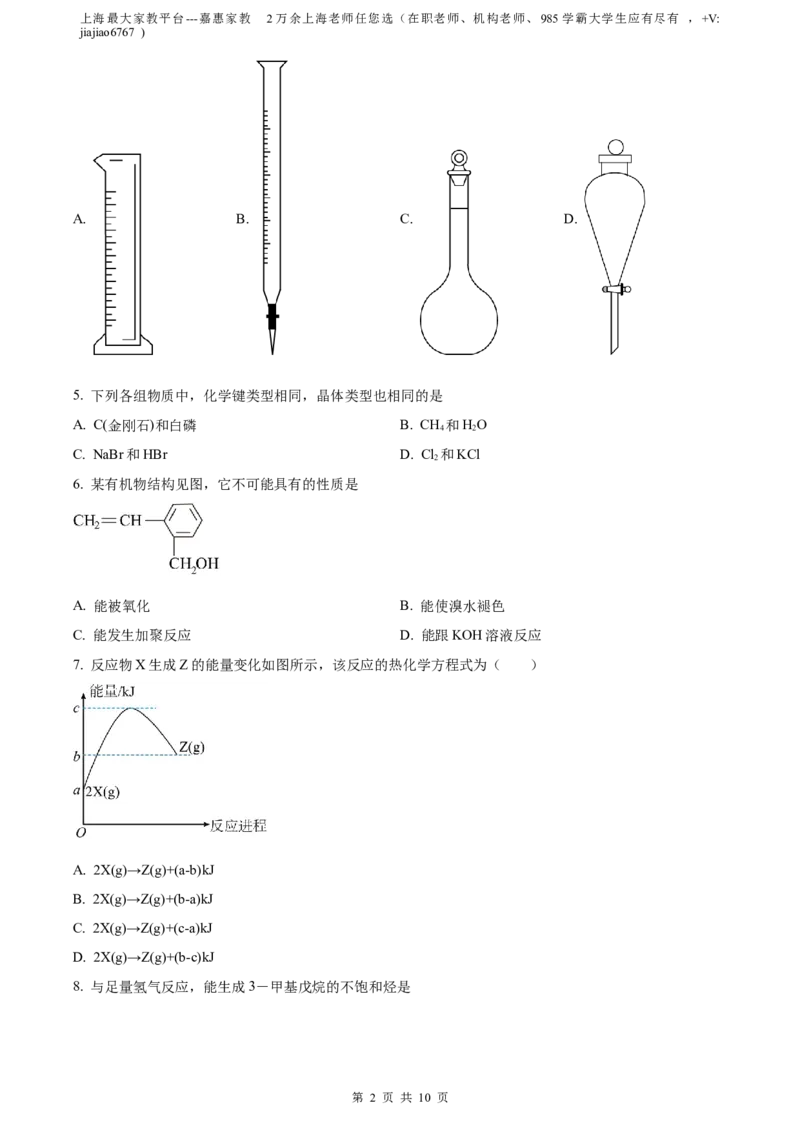
4. 下列玻璃仪器上有标明“0”刻度的是
第 1 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. B. C. D.
5. 下列各组物质中,化学键类型相同,晶体类型也相同的是
A. C(金刚石)和白磷 B. CH 和HO
4 2
C. NaBr和HBr D. Cl 和KCl
2
6. 某有机物结构见图,它不可能具有的性质是
A. 能被氧化 B. 能使溴水褪色
C. 能发生加聚反应 D. 能跟KOH溶液反应
7. 反应物X生成Z的能量变化如图所示,该反应的热化学方程式为( )
A. 2X(g)→Z(g)+(a-b)kJ
B. 2X(g)→Z(g)+(b-a)kJ
C. 2X(g)→Z(g)+(c-a)kJ
D. 2X(g)→Z(g)+(b-c)kJ
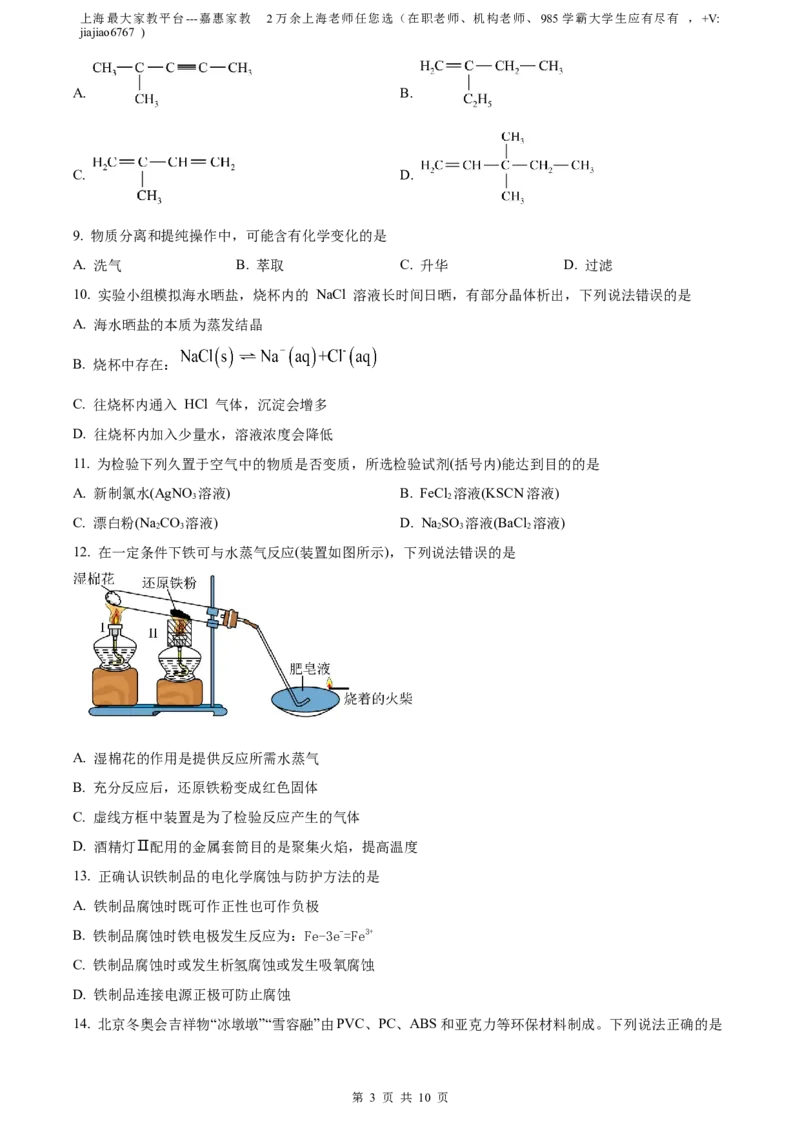
8. 与足量氢气反应,能生成3-甲基戊烷的不饱和烃是
第 2 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. B.
C. D.
9. 物质分离和提纯操作中,可能含有化学变化的是
A. 洗气 B. 萃取 C. 升华 D. 过滤
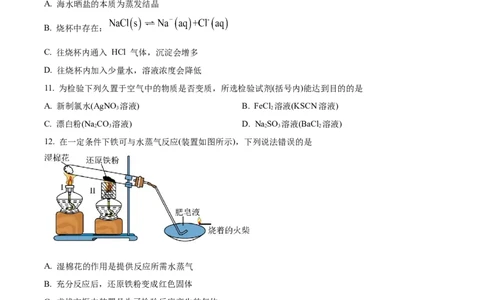
10. 实验小组模拟海水晒盐,烧杯内的 NaCl 溶液长时间日晒,有部分晶体析出,下列说法错误的是
A. 海水晒盐的本质为蒸发结晶
B. 烧杯中存在:
C. 往烧杯内通入 HCl 气体,沉淀会增多
D. 往烧杯内加入少量水,溶液浓度会降低
11. 为检验下列久置于空气中的物质是否变质,所选检验试剂(括号内)能达到目的的是
A. 新制氯水(AgNO 溶液) B. FeCl 溶液(KSCN溶液)
3 2
C. 漂白粉(Na CO 溶液) D. NaSO 溶液(BaCl 溶液)
2 3 2 3 2
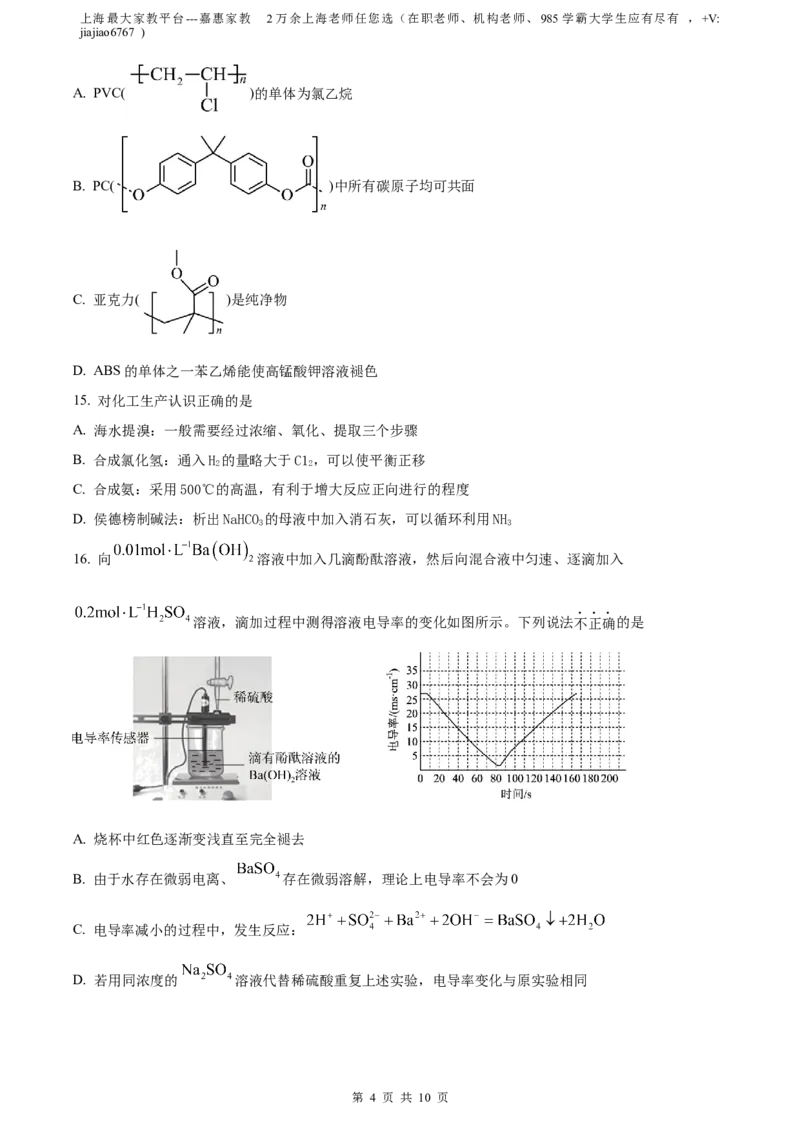
12. 在一定条件下铁可与水蒸气反应(装置如图所示),下列说法错误的是
A. 湿棉花的作用是提供反应所需水蒸气
B. 充分反应后,还原铁粉变成红色固体
C. 虚线方框中装置是为了检验反应产生的气体
D. 酒精灯Ⅱ配用的金属套筒目的是聚集火焰,提高温度
13. 正确认识铁制品的电化学腐蚀与防护方法的是
A. 铁制品腐蚀时既可作正性也可作负极
B. 铁制品腐蚀时铁电极发生反应为:Fe-3e-=Fe3+
C. 铁制品腐蚀时或发生析氢腐蚀或发生吸氧腐蚀
D. 铁制品连接电源正极可防止腐蚀
14. 北京冬奥会吉祥物“冰墩墩”“雪容融”由PVC、PC、ABS和亚克力等环保材料制成。下列说法正确的是
第 3 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. PVC( )的单体为氯乙烷
B. PC( )中所有碳原子均可共面
C. 亚克力( )是纯净物
D. ABS的单体之一苯乙烯能使高锰酸钾溶液褪色
15. 对化工生产认识正确的是
A. 海水提溴:一般需要经过浓缩、氧化、提取三个步骤
B. 合成氯化氢:通入H 的量略大于C1,可以使平衡正移
2 2
C. 合成氨:采用500℃的高温,有利于增大反应正向进行的程度
D. 侯德榜制碱法:析出NaHCO 的母液中加入消石灰,可以循环利用NH
3 3
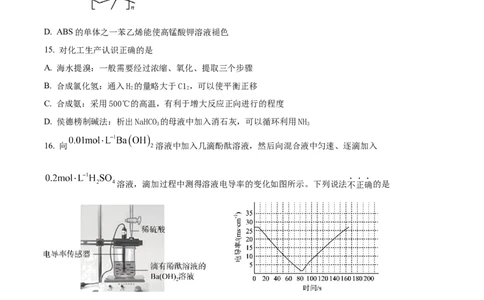
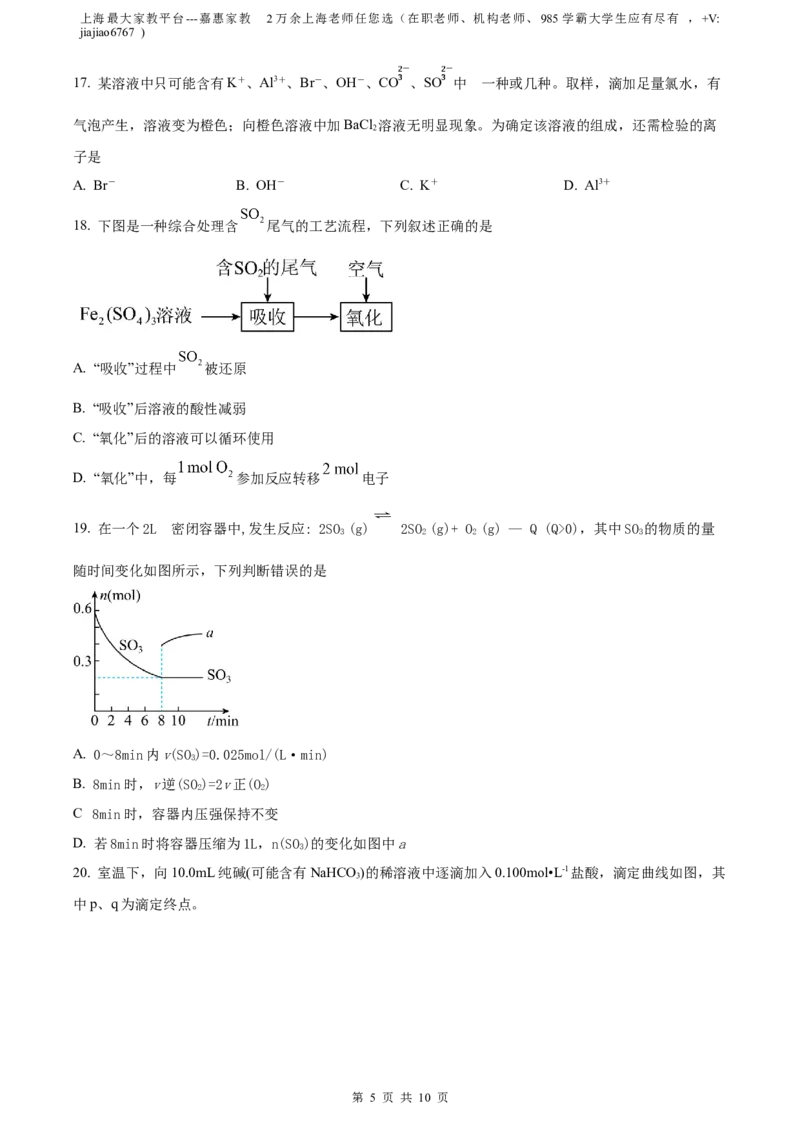
16. 向 溶液中加入几滴酚酞溶液,然后向混合液中匀速、逐滴加入
溶液,滴加过程中测得溶液电导率的变化如图所示。下列说法不正确的是
A. 烧杯中红色逐渐变浅直至完全褪去
B. 由于水存在微弱电离、 存在微弱溶解,理论上电导率不会为0
C. 电导率减小的过程中,发生反应:
D. 若用同浓度的 溶液代替稀硫酸重复上述实验,电导率变化与原实验相同
第 4 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
的
17. 某溶液中只可能含有K+、Al3+、Br-、OH-、CO 、SO 中 一种或几种。取样,滴加足量氯水,有
气泡产生,溶液变为橙色;向橙色溶液中加BaCl 溶液无明显现象。为确定该溶液的组成,还需检验的离
2
子是
A. Br- B. OH- C. K+ D. Al3+
18. 下图是一种综合处理含 尾气的工艺流程,下列叙述正确的是
A. “吸收”过程中 被还原
B. “吸收”后溶液的酸性减弱
C. “氧化”后的溶液可以循环使用
D. “氧化”中,每 参加反应转移 电子
的
19. 在一个2L 密闭容器中,发生反应: 2SO (g) 2SO (g)+ O (g) — Q (Q>0),其中SO 的物质的量
3 2 2 3
随时间变化如图所示,下列判断错误的是
A. 0~8min内v(SO)=0.025mol/(L·min)
3
B. 8min时,v逆(SO)=2v正(O)
2 2
.
C 8min时,容器内压强保持不变
D. 若8min时将容器压缩为1L,n(SO)的变化如图中a
3
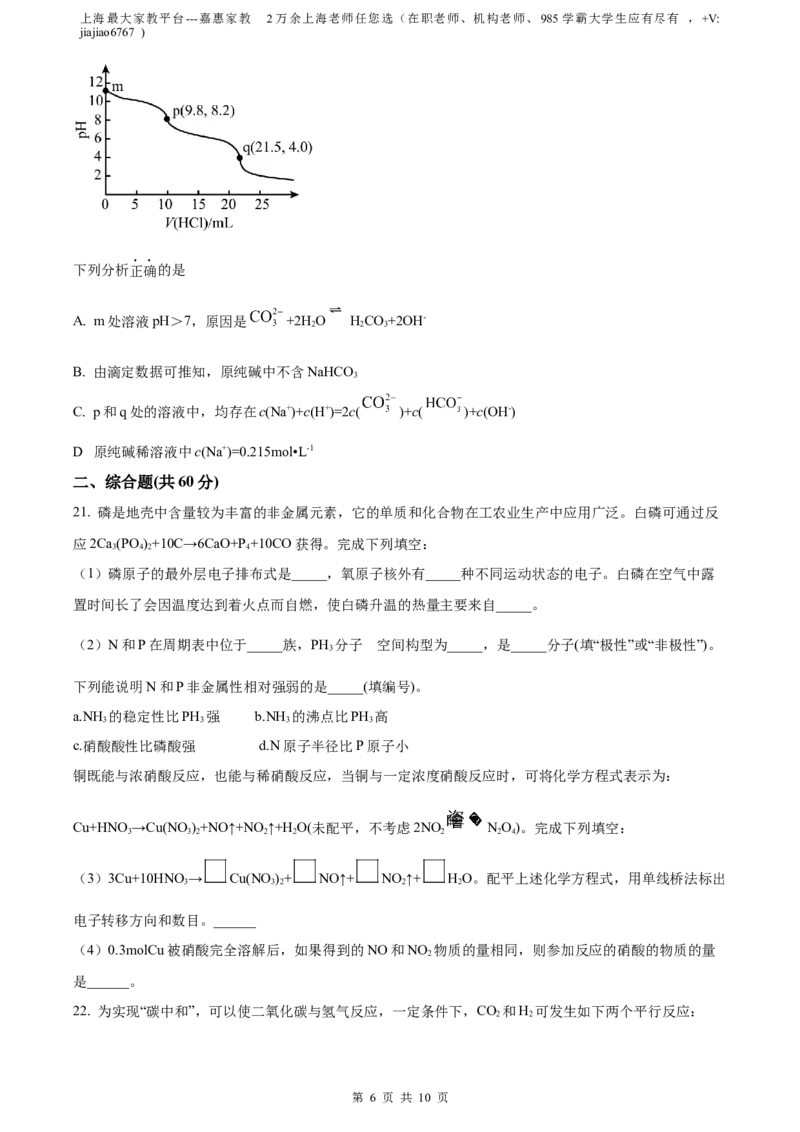
20. 室温下,向10.0mL纯碱(可能含有NaHCO )的稀溶液中逐滴加入0.100mol•L-1盐酸,滴定曲线如图,其
3
中p、q为滴定终点。
第 5 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
下列分析正确的是
A. m处溶液pH>7,原因是 +2H O HCO+2OH-
2 2 3
B. 由滴定数据可推知,原纯碱中不含NaHCO
3
C. p和q处的溶液中,均存在c(Na+)+c(H+)=2c( )+c( )+c(OH-)
.
D 原纯碱稀溶液中c(Na+)=0.215mol•L-1
二、综合题(共60分)
21. 磷是地壳中含量较为丰富的非金属元素,它的单质和化合物在工农业生产中应用广泛。白磷可通过反
应2Ca (PO )+10C→6CaO+P +10CO获得。完成下列填空:
3 4 2 4
(1)磷原子的最外层电子排布式是_____,氧原子核外有_____种不同运动状态的电子。白磷在空气中露
置时间长了会因温度达到着火点而自燃,使白磷升温的热量主要来自_____。
的
(2)N和P在周期表中位于_____族,PH 分子 空间构型为_____,是_____分子(填“极性”或“非极性”)。
3
下列能说明N和P非金属性相对强弱的是_____(填编号)。
a.NH 的稳定性比PH 强 b.NH 的沸点比PH 高
3 3 3 3
c.硝酸酸性比磷酸强 d.N原子半径比P原子小
铜既能与浓硝酸反应,也能与稀硝酸反应,当铜与一定浓度硝酸反应时,可将化学方程式表示为:
Cu+HNO →Cu(NO )+NO↑+NO ↑+H O(未配平,不考虑2NO NO)。完成下列填空:
3 3 2 2 2 2 2 4
(3)3Cu+10HNO → Cu(NO )+ NO↑+ NO ↑+ HO。配平上述化学方程式,用单线桥法标出
3 3 2 2 2
电子转移方向和数目。______
(4)0.3molCu被硝酸完全溶解后,如果得到的NO和NO 物质的量相同,则参加反应的硝酸的物质的量
2
是______。
22. 为实现“碳中和”,可以使二氧化碳与氢气反应,一定条件下,CO 和H 可发生如下两个平行反应:
2 2
第 6 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
i.CO (g)+H(g) CO(g)+HO(g)-42kJ
2 2 2
ii.CO(g)+3H(g) CHOH(g)+H O(g)+49.6kJ
2 2 3 2
(1)为了提高CHOH的产率,理论上应采用的措施是(填编号)______。
3
A. 低温低压 B. 高温低压 C. 高温高压 D. 低温高压
(2)保持温度533K,压强3MPa,按投料比 = 向密闭容器中充入CO 和H,反应相同时间测得
2 2
不同催化剂下CO 转化率和CHOH选择性的相关实验数据如表所示(已知CHOH选择性:转化的CO 中生
2 3 3 2
成CHOH的百分比)。
3
催化剂 CO 转化率 CHOH选择性
2 3
cat.1 21.9% 67.3%
cat.2 36.1% 100.0%
上述条件下,使用cat.2作催化剂,下列说法能判断反应ii达到平衡状态的是______(填编号)
A. 气体压强不再变化
B. 气体平均相对分子质量不再变化
C. CHOH和HO的物质的量之比为1:1
3 2
D. CO 和H 的物质的量之比不再变化
2 2
(3)一定条件下,向0.5L恒容密闭容器中充入1molCO 和3molH ,只发生上述反应ii,达平衡时,H 的
2 2 2
转化率为80%,则该温度下的平衡常数K=______(保留两位小数)。
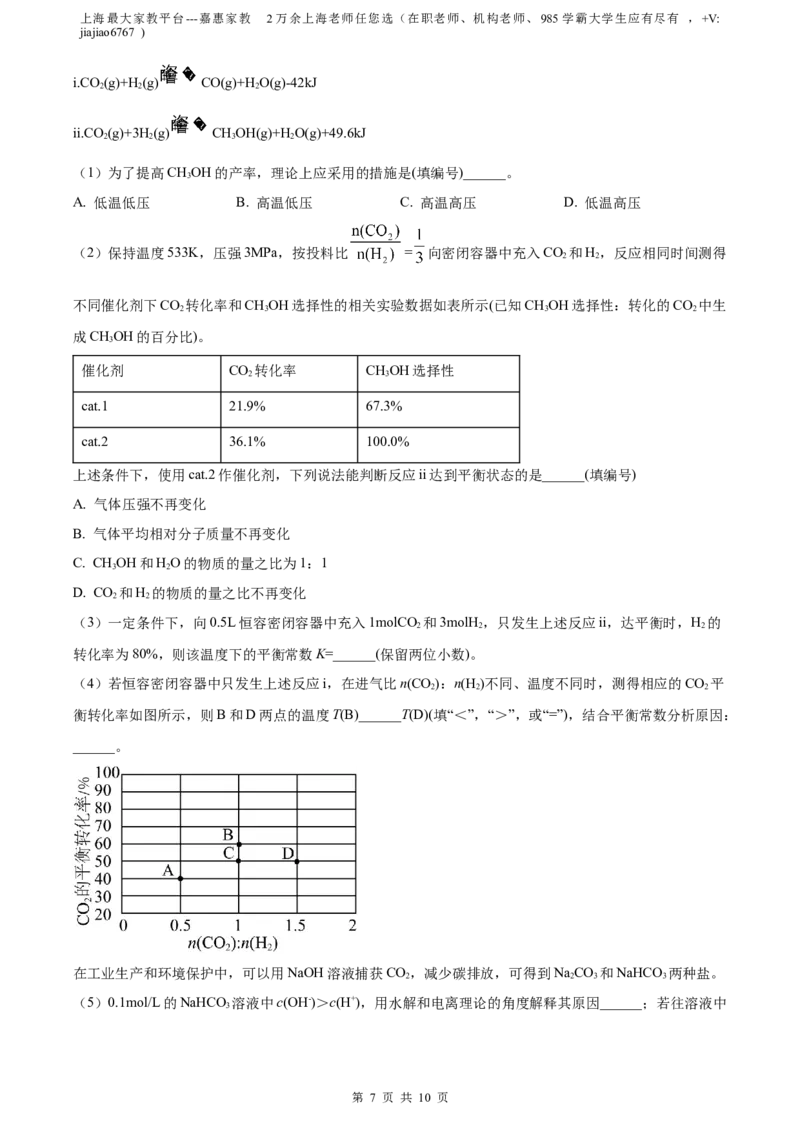
(4)若恒容密闭容器中只发生上述反应i,在进气比n(CO):n(H )不同、温度不同时,测得相应的CO 平
2 2 2
衡转化率如图所示,则B和D两点的温度T(B)______T(D)(填“<”,“>”,或“=”),结合平衡常数分析原因:
______。
在工业生产和环境保护中,可以用NaOH溶液捕获CO,减少碳排放,可得到NaCO 和NaHCO 两种盐。
2 2 3 3
(5)0.1mol/L的NaHCO 溶液中c(OH-)>c(H+),用水解和电离理论的角度解释其原因______;若往溶液中
3
第 7 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
加入氨水至中性,则c(Na+)______c( )+c( )+c(H CO)(填“>”、“﹤”或“=”)。
2 3
(6)往0.1mol/L的NaCO 溶液加入少量NaCO 固体,完全溶解后溶液中c(Na+):c(CO )的比值
2 3 2 3
______(填“变大”、“变小”或“保持不变”)。
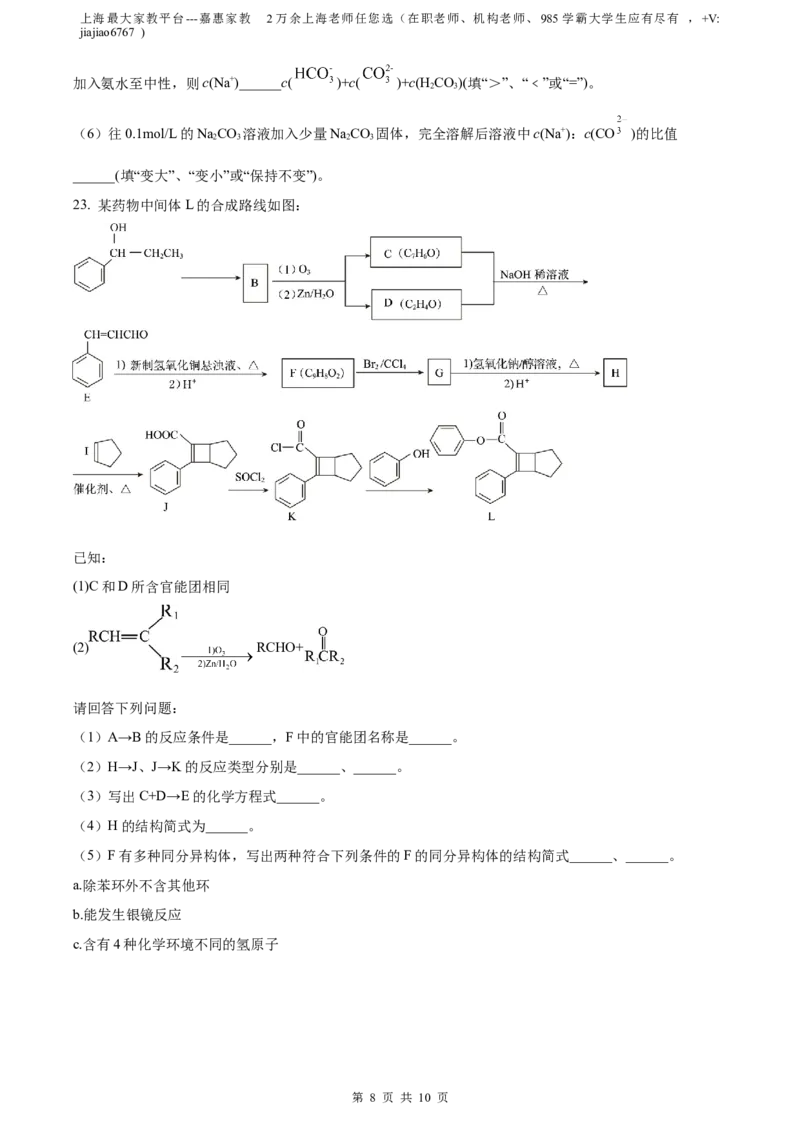
23. 某药物中间体L的合成路线如图:
已知:
(1)C和D所含官能团相同
(2) RCHO+
请回答下列问题:
(1)A→B的反应条件是______,F中的官能团名称是______。
(2)H→J、J→K的反应类型分别是______、______。
(3)写出C+D→E的化学方程式______。
(4)H的结构简式为______。
(5)F有多种同分异构体,写出两种符合下列条件的F的同分异构体的结构简式______、______。
a.除苯环外不含其他环
b.能发生银镜反应
c.含有4种化学环境不同的氢原子
第 8 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(6)结合题目所给信息,设计由CH=CH 和OHCCHO合成 的合成路线(用流程图表示,无机试
2 2
剂、有机溶剂任选)______。
(合成路线常用的表示方式为:A B…… 目标产物)
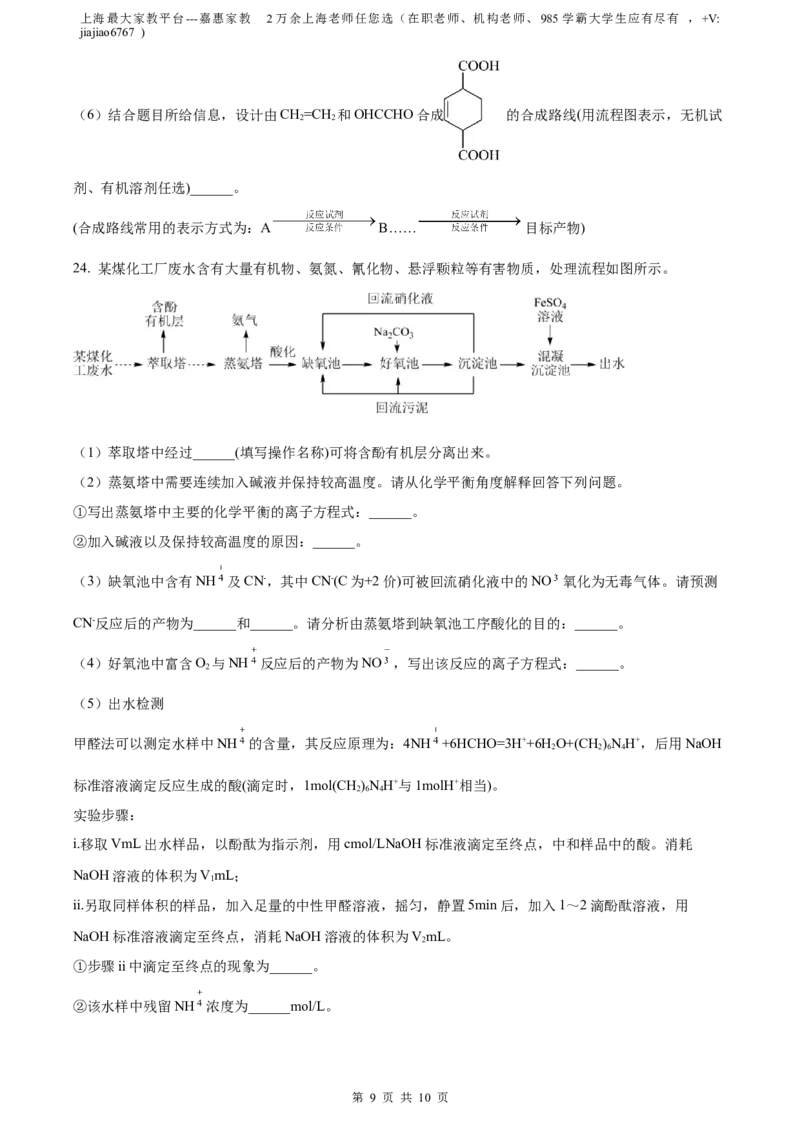
24. 某煤化工厂废水含有大量有机物、氨氮、氰化物、悬浮颗粒等有害物质,处理流程如图所示。
(1)萃取塔中经过______(填写操作名称)可将含酚有机层分离出来。
(2)蒸氨塔中需要连续加入碱液并保持较高温度。请从化学平衡角度解释回答下列问题。
①写出蒸氨塔中主要的化学平衡的离子方程式:______。
②加入碱液以及保持较高温度的原因:______。
(3)缺氧池中含有NH 及CN-,其中CN-(C为+2价)可被回流硝化液中的NO 氧化为无毒气体。请预测
CN-反应后的产物为______和______。请分析由蒸氨塔到缺氧池工序酸化的目的:______。
(4)好氧池中富含O 与NH 反应后的产物为NO ,写出该反应的离子方程式:______。
2
(5)出水检测
甲醛法可以测定水样中NH 的含量,其反应原理为:4NH +6HCHO=3H++6H O+(CH)NH+,后用NaOH
2 2 6 4
标准溶液滴定反应生成的酸(滴定时,1mol(CH )NH+与1molH+相当)。
2 6 4
实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸。消耗
NaOH溶液的体积为VmL;
1
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用
NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为VmL。
2
①步骤ii中滴定至终点的现象为______。
②该水样中残留NH 浓度为______mol/L。
第 9 页 共 10 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 10 页 共 10 页