文档内容
江门市 2025 年普通高中高一调研测试(一)
化学
本试卷8页,20小题,满分100分。考试时间75分钟。
注意事项:
1.答题前,务必将自己的姓名、准考证号填写在答题卡规定的位置上。
2.做选择题时,必须用2B铅笔将答题卷上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其它答案标号。
3.答非选择题时,必须用黑色字迹钢笔或签字笔,将答案写在答题卡规定的位置上。
4.所有题目必须在答题卡上作答,在试题卷上作答无效。
5.考试结束后,将答题卡交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56
一、选择题:本题共16小题,第1~10题每小题2分;第11~16题每小题4分,共44分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
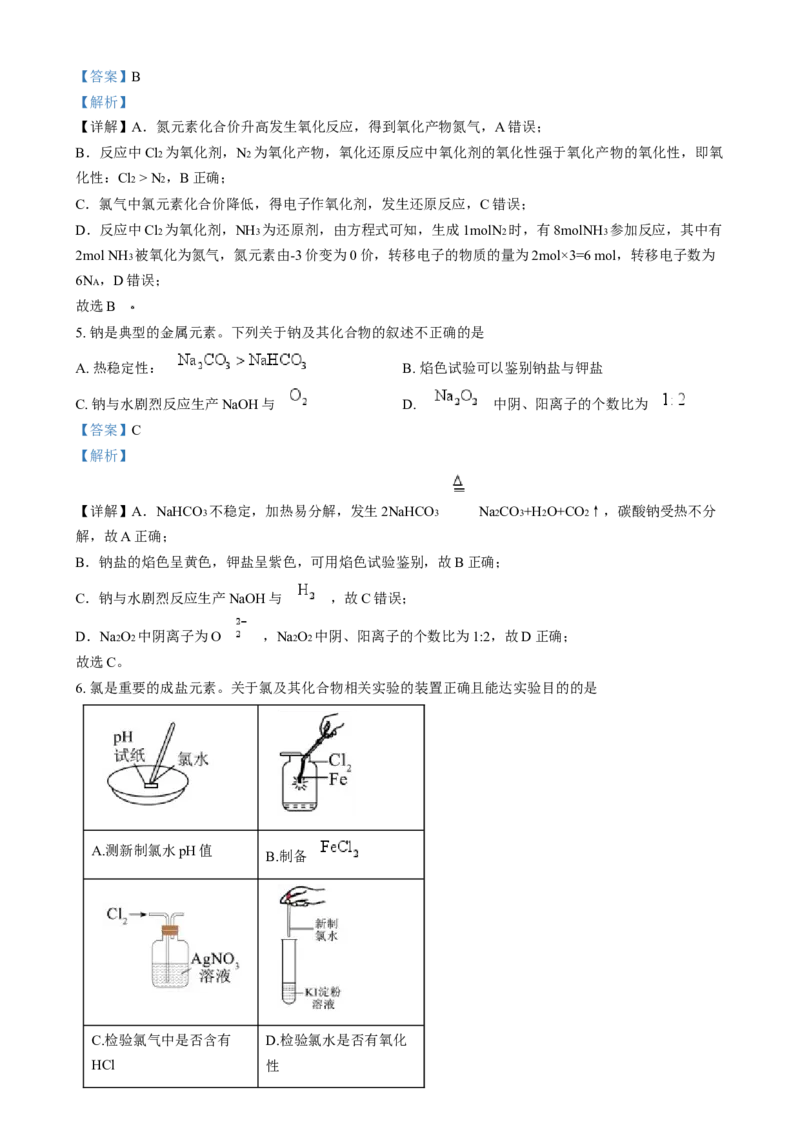
1. 梅花的纹样在中国艺术中被广泛运用。下列文物的主要材质属于金属材料的是
A.金质梅花型饰品 B.梅花砖雕
D.青花冰梅纹
C.梅花春燕纹碗
罐
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.金质梅花型饰品为黄金制品,属于金属材料,A正确;
B.梅花砖雕属于无机非金属材料,B错误;
C.梅花春燕纹碗为硅酸盐制品,属于无机非金属材料,C错误;
D.青花冰梅纹罐属于陶瓷,其主要材质是硅酸盐,属于无机非金属材料,D错误;
故选A。
2. 用激光笔照射蓝色钴玻璃,可以看到一条光亮的“通路”。下列说法正确的是A. 蓝色钴玻璃是纯净物 B. 蓝色钴玻璃是气溶胶
C. 该现象源于“丁达尔效应” D. 该现象出现时,蓝色钴玻璃发生了化学变化
【答案】C
【解析】
【详解】A.用激光笔照射蓝色钴玻璃,可以看到一条光亮的“通路”,说明蓝色钴玻璃为胶体,属于混
合物,A错误;
B.蓝色钴玻璃是固溶胶,B错误;
C.光束通过胶体时,光线能够发生散射作用而产生丁达尔效应,而通入其它分散系时不能产生丁达尔效
应,所以该现象源于“丁达尔效应”,C正确;
D.丁达尔效应为一种物理现象,不是化学变化,D错误;
故选C。
3. 生活中处处蕴含化学原理。下列相关场景中发生反应的离子方程式书写正确的是
A. 用覆铜板制作印刷电路板:
B. 用小苏打治疗胃酸过多:
C. 用食醋检验牙膏中的碳酸钙:
D. 用漂白粉漂洗衣服:
【答案】D
【解析】
【详解】A.该反应不满足电荷守恒和得失电子守恒,正确的离子方程式为:
,故A错误;
B.小苏打为碳酸氢钠, 不能拆,正确的离子方程式为: ,
故B错误;
C.醋酸为弱酸,应写化学式,正确的离子方程式为:
,故C错误;
D.漂白粉的有效成分次氯酸钙能与水、二氧化碳反应生成HClO,增强漂白能力,离子方程式为:
,故D正确;
故选D。
4. 化工厂常用浓氨水检验氯气管道是否漏气,原理为: 。关于该反应
下列说法正确的是
A. 还原产物为 B. 氧化性:
C. 发生了氧化反应 D. 消耗8mol 时,转移电子数为【答案】B
【解析】
【详解】A.氮元素化合价升高发生氧化反应,得到氧化产物氮气,A错误;
B.反应中Cl2 为氧化剂,N2 为氧化产物,氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,即氧
化性:Cl2 > N2 ,B正确;
C.氯气中氯元素化合价降低,得电子作氧化剂,发生还原反应,C错误;
D.反应中Cl2 为氧化剂,NH3 为还原剂,由方程式可知,生成1molN2 时,有8molNH3 参加反应,其中有
2mol NH3 被氧化为氮气,氮元素由-3价变为0价,转移电子的物质的量为2mol×3=6 mol,转移电子数为
6NA ,D错误;
故选B
5. 钠是典型的金属元素。下列关于钠及其化合物的叙述不正确的是
A. 热稳定性: B. 焰色试验可以鉴别钠盐与钾盐
C. 钠与水剧烈反应生产NaOH与 D. 中阴、阳离子的个数比为
【答案】C
【解析】
【详解】A.NaHCO3 不稳定,加热易分解,发生2NaHCO3 Na2CO3+H2O+CO2 ↑,碳酸钠受热不分
解,故A正确;
B.钠盐的焰色呈黄色,钾盐呈紫色,可用焰色试验鉴别,故B正确;
C.钠与水剧烈反应生产NaOH与 ,故C错误;
D.Na2O2 中阴离子为O ,Na2O2 中阴、阳离子的个数比为1:2,故D正确;
故选C。
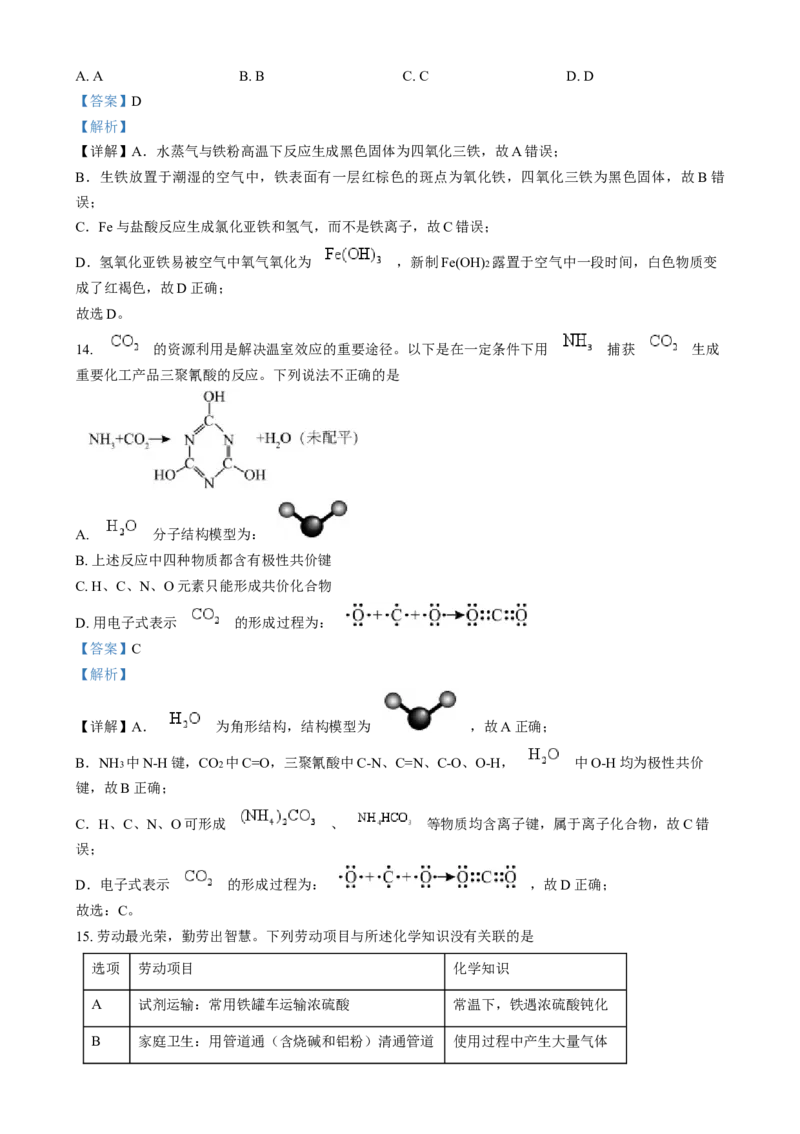
6. 氯是重要的成盐元素。关于氯及其化合物相关实验的装置正确且能达实验目的的是
A.测新制氯水pH值
B.制备
C.检验氯气中是否含有 D.检验氯水是否有氧化
HCl 性A A B. B C. C D. D
【答案】D
【解析】
【详解】A.新制氯水具有漂白性,能漂白pH试纸,故无法使用pH试纸测新制氯水的pH,实验不能达
到预期目的,A错误;
B.铁和氯气反应生成氯化铁,而非氯化亚铁,B错误;
C.氯气和水反应生成HCl和次氯酸,HCl和硝酸银生成氯化银沉淀,干扰氯气中是否含有HCl的检验,
C错误;
D.新制氯水中氯气氧化碘离子生成碘单质,使得淀粉溶液变蓝色,说明氯水具有氧化性,D正确;
故选D。
7. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 1.7g的 中含有的电子数为
B. 溶液中 的数目为
C. 0.1mol 中完全燃烧生成2.24LHCl
D. 与足量 反应生成1mol 时转移 电子
【答案】A
【解析】
【详解】A.1个 中含有10个电子,1.7g的 为0.1mol,含有1mol电子,电子数为
,故A正确;
B.未说明溶液的体积,无法计算 溶液中 的数目,故B错误;
C.没有说明气体所处状态,不能确定生成HCl的体积,故C错误;
D. ,则 与足量 反应生成1mol 时转移
2mol电子,为2 电子,故D错误;
故选A。
8. 小明血液检查的部分指标如下表。若其血液总体积为5.0L,则血液中含甘油三脂(设甘油三脂的平均
相对分子质量为840)的质量为
序号 项目名称 检查结果 单位 参考值
1 甘油三脂 1.50 0.45-1.70
2 总胆固醇 4.65 2.85-5.703 葡萄糖 5.1 3.9-6.1
A. 630g B. 126g C. 6.3g D. 12.6g
【答案】C
【解析】
【详解】甘油三脂的浓度为1.50 ,血液总体积为5.0L,甘油三脂的物质的量为1.50
×5.0L=7.5mmol=7.5×10-3mol,质量为7.5×10-3mol×840g/mol=6.3g,故C正确;
故选:C。
9. 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实
验,其中结论正确的是
A. 若滴加KSCN溶液,溶液变红,说明铁粉变质
B. 若滴加KSCN溶液,溶液未变红,说明铁粉未变质
C. 若依次滴加氯水,KSCN溶液,溶液变红,说明铁粉全部变质
D. 若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质
【答案】A
【解析】
【详解】A.滴加KSCN溶液,溶液变红,说明溶液中含有Fe3+ ,故还原铁粉即Fe变质,故A选项正
确;
B.滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+ ,但溶液中可能含Fe2+ ,不能说明铁粉未变质,
故B选项错误;
C.滴加氯水时可能把溶液中存在的Fe2+ 氧化成了Fe3+ ,再滴加硫氰化钾溶液,溶液变红,则不能说明铁
粉全部变质,故C选项错误;
D.若先滴加KSCN溶液,溶液未变红,说明溶液中不含Fe3+ ,再滴加氯水,溶液变红说明溶液中存在
Fe2+ ,被氯水氧化成了Fe3+ ,但不能说明铁粉全部变质,故D选项错误。
故选A选项。
10. 合金的使用对于促进生产发展,改善人类生活发挥了巨大作用。下列关于合金的说法中正确的是
A. 稀土金属可用于生产合金 B. 我国使用最早的合金是钢
C. 生铁的含碳量比钢的含碳量低 D. 合金的熔点一定比各金属成分的低
【答案】A
【解析】
【详解】A.稀土金属可以用于生产合金,能够提高合金的性能,A正确;
B.我国使用最早的合金是青铜,B错误;
C.生铁的含碳量为2%~4%,钢的含碳量为0.03%~0.2%,生铁的含碳量比钢的含碳量高,C错误;
D.合金的熔点大多数情况下,比各成分金属的低,但是汞与其它金属形成合金时,合金的熔点大于汞,
D错误;
故选A。
11. 化学实验安全不容忽视。下列操作不符合化学实验安全要求的是
A. 在通风橱中进行氯气的制备实验B. 切取大块的钠放入盛有水的烧杯中,观察反应现象
C. 不慎将碱沾到皮肤上,先用大量水冲洗,再涂上1%的硼酸
D. 把蘸取浓盐酸的棉花放进氨气集气瓶中密封,观察反应现象
【答案】B
【解析】
【详解】A.氯气有毒,制备氯气应在通风橱中进行,以防引起中毒,故A正确;
B.钠与水反应剧烈且放出热量,若用大块钠放入烧杯中会有爆炸的危险,故B错误;
C.碱液沾到皮肤上,应立即用大量水冲洗,然后涂上1%的硼酸中和残留的碱,故C正确;
D.浓盐酸易挥发,用蘸取浓盐酸的棉花放进氨气集气瓶中,可观察氨气与HCl反应的现象,故D正确;
故选:B。
12. 氮化镓(GaN)是一种第三代半导体材料,有良好的电学特性,近年智能手机的快速充电器就使用了
氮化镓材料,镓的原子结构示意图如下。下列说法不正确的是
A. 的结构式为 B. 和 互为同素异形体
C. 一个 原子中含有39个中子 D. 镓位于元素周期表的第四周期第ⅢA族
【答案】B
【解析】
【详解】A.N2 的结构式为N≡N,A正确;
B. N和 N为同种元素的不同核素,互为同位素,不互为同素异形体,B错误;
C.一个 70Ga原子中含有中子数为70-31=39,C正确;
D.镓为31号,在元素周期表中位于铝的下方,即位于元素周期表的第四周期第ⅢA族,D正确;
故答案为:B。
13. 通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正
确的是
选项 操作、现象 解释
A 水蒸气与铁粉高温下反应生成黑色固体 反应生成了FeO
红棕色的斑点的主要成分是
B 生铁长时间放置于潮湿的空气中,表面出现红棕色的斑点
C 向盐酸中加入少量铁粉,铁粉溶解 Fe被氧化为
被氧化成
D
新制 露置于空气中,最终变成了红褐色沉淀A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.水蒸气与铁粉高温下反应生成黑色固体为四氧化三铁,故A错误;
B.生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点为氧化铁,四氧化三铁为黑色固体,故B错
误;
C.Fe与盐酸反应生成氯化亚铁和氢气,而不是铁离子,故C错误;
D.氢氧化亚铁易被空气中氧气氧化为 ,新制Fe(OH)2 露置于空气中一段时间,白色物质变
成了红褐色,故D正确;
故选D。
14. 的资源利用是解决温室效应的重要途径。以下是在一定条件下用 捕获 生成
重要化工产品三聚氰酸的反应。下列说法不正确的是
A. 分子结构模型为:
B. 上述反应中四种物质都含有极性共价键
C. H、C、N、O元素只能形成共价化合物
D. 用电子式表示 的形成过程为:
【答案】C
【解析】
【详解】A. 为角形结构,结构模型为 ,故A正确;
B.NH3 中N-H键,CO2 中C=O,三聚氰酸中C-N、C=N、C-O、O-H, 中O-H均为极性共价
键,故B正确;
C.H、C、N、O可形成 、 等物质均含离子键,属于离子化合物,故C错
误;
D.电子式表示 的形成过程为: ,故D正确;
故选:C。
15. 劳动最光荣,勤劳出智慧。下列劳动项目与所述化学知识没有关联的是
选项 劳动项目 化学知识
A 试剂运输:常用铁罐车运输浓硫酸 常温下,铁遇浓硫酸钝化
B 家庭卫生:用管道通(含烧碱和铝粉)清通管道 使用过程中产生大量气体C 泳池消毒:用漂粉精作游泳池的消毒剂
具有氧化性
固体溶于水
D 帮厨活动:加入小苏打做膨松剂
吸热
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.常温下,铁遇浓硫酸钝化,可防止内部的铁继续反应,因此可用铁罐车运输浓硫酸,故 A不
选;
B.烧碱和铝粉可以发生反应: ,利用产生的氢
气清通管道,故B不选;
C.漂粉精主要成分是 ,其中的 具有强氧化性,可以作游泳池的消毒剂,故C不
选;
D.小苏打做膨松剂是利用碳酸氢钠受热分解生成碳酸钠、二氧化碳和水的原理,方程式为:
,和碳酸氢钠固体溶于水吸热无关,故D选;
答案选D。
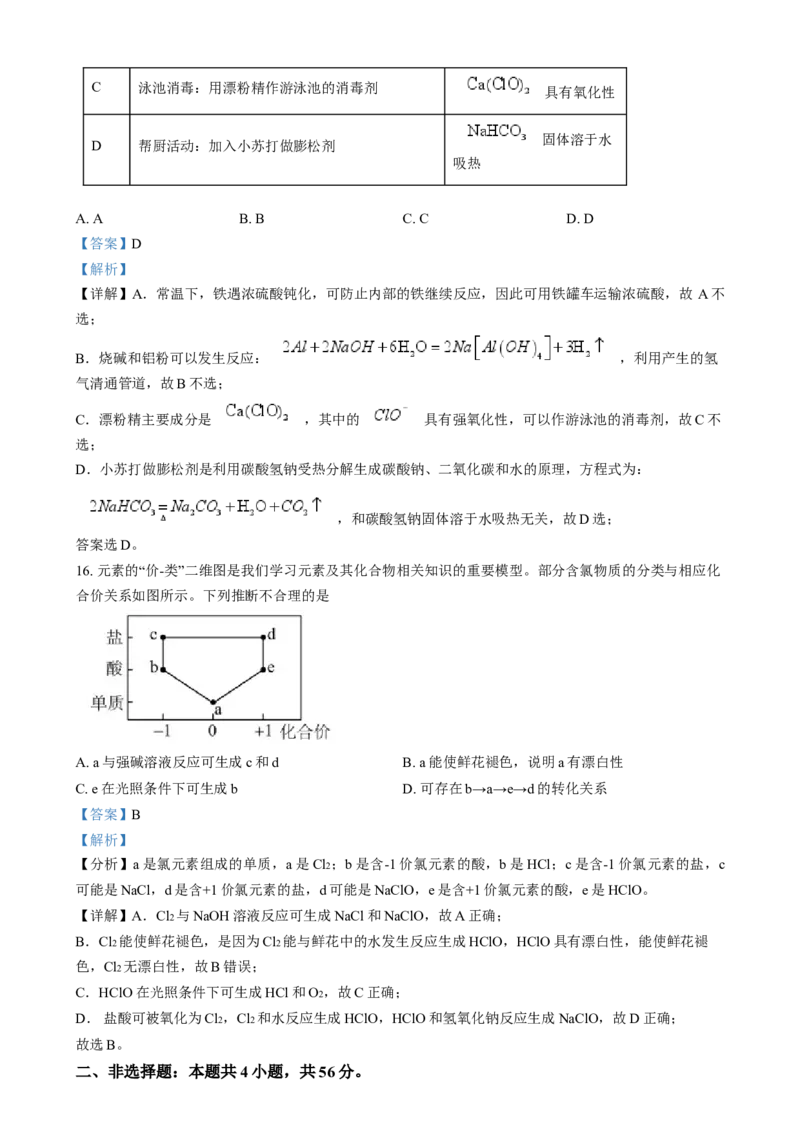
16. 元素的“价-类”二维图是我们学习元素及其化合物相关知识的重要模型。部分含氯物质的分类与相应化
合价关系如图所示。下列推断不合理的是
A. a与强碱溶液反应可生成c和d B. a能使鲜花褪色,说明a有漂白性
C. e在光照条件下可生成b D. 可存在b→a→e→d的转化关系
【答案】B
【解析】
【分析】a是氯元素组成的单质,a是Cl2 ;b是含-1价氯元素的酸,b是HCl;c是含-1价氯元素的盐,c
可能是NaCl,d是含+1价氯元素的盐,d可能是NaClO,e是含+1价氯元素的酸,e是HClO。
【详解】A.Cl2 与NaOH溶液反应可生成NaCl和NaClO,故A正确;
B.Cl2 能使鲜花褪色,是因为Cl2 能与鲜花中的水发生反应生成HClO,HClO具有漂白性,能使鲜花褪
色,Cl2 无漂白性,故B错误;
C.HClO在光照条件下可生成HCl和O2 ,故C正确;
D. 盐酸可被氧化为Cl2 ,Cl2 和水反应生成HClO,HClO和氢氧化钠反应生成NaClO,故D正确;
故选B。
二、非选择题:本题共4小题,共56分。17. 莫高窟的壁画是中华民族宝库里璀璨的明珠,了解壁画颜料成分对保护壁画有重要意义。研究表明,
颜料部分成分组成的元素在周期表中的位置如下所示:
综合上述材料,回答下列问题:
(1)陆游在诗中写到:“螺青点出莫山色,石绿染成春浦潮”。其中石绿中含有的铜(Cu)位于________
A. 第三周期第ⅠB族 B. 第四周期第ⅥB族 C. 第三周期第11列 D. 第四周期第11列
(2)元素最高价氧化物的水化物的性质是研究元素性质的重要依据。Si、C最高价氧化物的水化物酸性
大小顺序为________(用水化物化学式表示);Na和Al最高价氧化物的水化物之间反应的离子方程式为
________。
(3)微粒半径大小影响其化学性质。上述元素中原子半径最大的是________(填元素符号);O、Na、
A1简单离子的半径大小顺序为________(用离子符号表示)。
(4)S和Cl是典型的非金属元素。将 通入 溶液中,产生黄色沉淀,该反应的化学方程
式为________。
(5)各元素的原子之间通过化学键形成丰富的物质。
上述周期表中元素组成的化合物含共价键的是________
①
A.KCl B.CaO C. D.NaOH
写出HClO的电子式________。
②
【答案】(1)D (2) . H2CO3>H2SiO3 .
(3) . K . O2->Na+① >A13+
②
① ②
(4)
(5) . CD .
【解析】
① ②
【小问1详解】
Cu为29号元素,位于第四周期第ⅠB族,周期表中第11列位置,故D正确;
【小问2详解】
元素非金属性越强,最高价氧化物的水化物的酸性越强,非金属性:C>Si;则酸性:H2CO3>H2SiO3 ;Na
和Al最高价氧化物的水化物分别为NaOH和Al(OH)3 ,两这发生反应生成四羟基合铝酸钠,反应离子方
程式为: ;
【小问3详解】
电子层数越多原子半径越大,电子层数相同时,核电荷数越大原子半径越小,则上述元素中原子半径最大
的为K;O2- 、Na+ 、A13+ 核外电子排布相同,核电荷数ONa+>A13+ ;
【小问4详解】
将 通入 溶液中,产生S单质,反应方程式为: ;【小问5详解】
①A.KCl中只含离子键;
B.CaO只含离子键;
C. 中只含共价键;
D.NaOH中既含离子键也含共价键;
故选:CD。
②HClO的电子式: 。
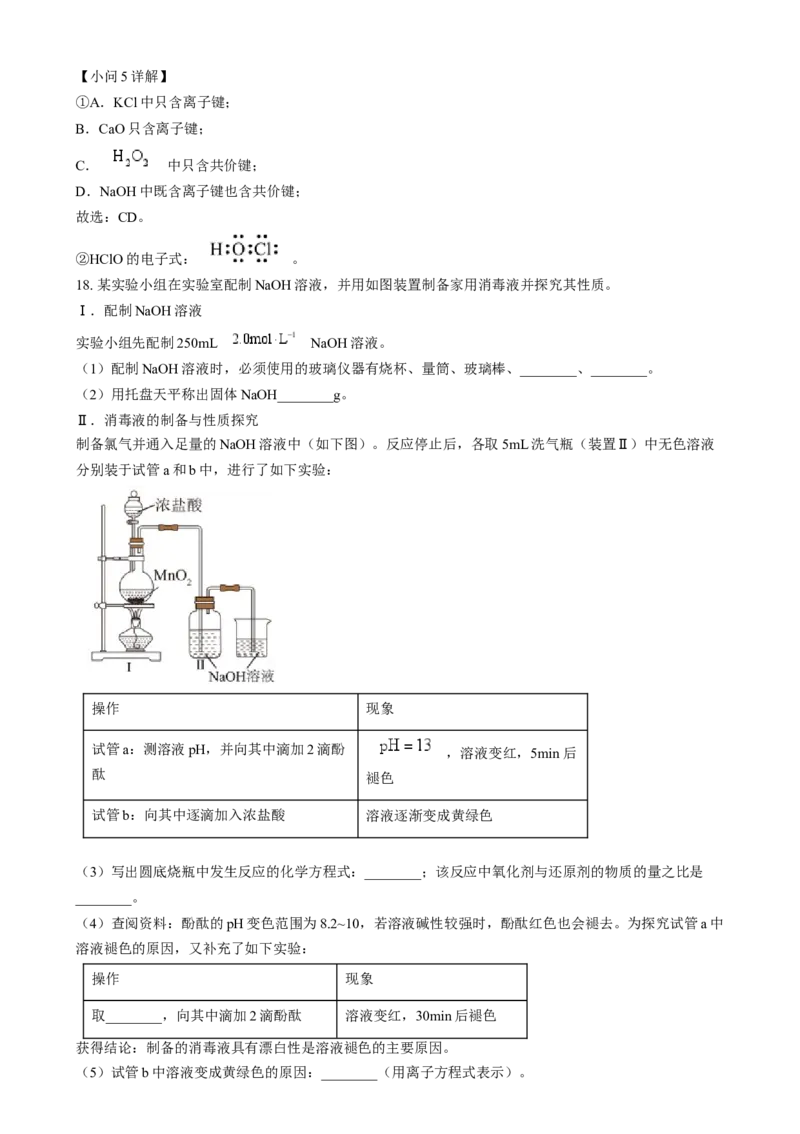
18. 某实验小组在实验室配制NaOH溶液,并用如图装置制备家用消毒液并探究其性质。
Ⅰ.配制NaOH溶液
实验小组先配制250mL NaOH溶液。
(1)配制NaOH溶液时,必须使用的玻璃仪器有烧杯、量筒、玻璃棒、________、________。
(2)用托盘天平称出固体NaOH________g。
Ⅱ.消毒液的制备与性质探究
制备氯气并通入足量的NaOH溶液中(如下图)。反应停止后,各取5mL洗气瓶(装置Ⅱ)中无色溶液
分别装于试管a和b中,进行了如下实验:
操作 现象
试管a:测溶液pH,并向其中滴加2滴酚 ,溶液变红,5min后
酞 褪色
试管b:向其中逐滴加入浓盐酸 溶液逐渐变成黄绿色
(3)写出圆底烧瓶中发生反应的化学方程式:________;该反应中氧化剂与还原剂的物质的量之比是
________。
(4)查阅资料:酚酞的pH变色范围为8.2~10,若溶液碱性较强时,酚酞红色也会褪去。为探究试管a中
溶液褪色的原因,又补充了如下实验:
操作 现象
取________,向其中滴加2滴酚酞 溶液变红,30min后褪色
获得结论:制备的消毒液具有漂白性是溶液褪色的主要原因。
(5)试管b中溶液变成黄绿色的原因:________(用离子方程式表示)。(6)基于(5)中的反应,有同学认为本实验把装置Ⅰ中产生的气体直接通入装置Ⅱ制备消毒液,会降低
消毒液中NaClO的浓度,可采取的改进措施是________。
【答案】(1) . 胶头滴管 . 250mL容量瓶
① ②
(2)20.0 (3) . . 1 2
(4)5mL,pH=13的NaOH溶液
① ② ∶
(5)2H++ ClO-+Cl-=Cl2↑+ H2O
(6)在装置I和II之间添加一个盛有饱和食盐水的洗气瓶,除去氯气中的氯化氢
【解析】
【分析】制备家用消毒液,并探究其性质:装置Ⅰ:盐酸和二氧化锰在加热条件下反应生成氯气、氯化锰
和水, ,装置Ⅱ:氯气和氢氧化钠反应:
Cl2+2NaOH=NaClO+NaCl+H2O,制得消毒液,氯气有毒,尾气需用氢氧化钠溶液吸收,据此分析作答。
【小问1详解】
配制250mL NaOH溶液时,必须使用的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
250mL容量瓶;
【小问2详解】
要完成本实验,应称出NaOH的质量是2.0mol/L×0.250L×40g/mol=20.0g;
【小问3详解】
圆底烧瓶中二氧化锰和浓盐酸在加热的条件下生成氯气,化学反应方程式为
;该反应中,二氧化锰是氧化剂,盐酸中只有一半是还
原剂,则该反应中氧化剂与还原剂的物质的量之比是1 2;
【小问4详解】
∶
根据资料可知,酚酞在强碱性溶液中红色会褪去,则为了验证溶液褪色的原因,需要补充碱性溶液使酚酞
褪色的对比实验,在这一过程中要注意物质的体积和浓度要与原溶液相同,所以应取5mL,pH=13的
NaOH溶液;
【小问5详解】
溶液变成黄绿色的原因为ClO- 与 Cl- 在酸性条件下发生氧化还原反应生成了氯气,离子方程式为2H++ ClO-
+Cl-=Cl2↑+ H2O;
【小问6详解】
装置Ⅰ中反应生成的氯气中含有氯化氢,一是会消耗氢氧化钠,基于(5)中的反应,所以HCl也可以提
供氢离子使溶液中的ClO- 与 Cl- 反应,从而降低消毒液中NaClO的浓度,则可采取的改进措施是在装置I
和II之间添加一个盛有饱和食盐水的洗气瓶,除去氯气中的氯化氢。
19. 亚氯酸钠( )是一种杀菌漂白剂,可用于棉纺漂白、食品消毒等。制备无水
晶体的其中一种生产工艺如下:已知:① 沸点为11 ,且浓度过高时易发生分解爆炸;
℃
② 在温度高于60 时易分解生成 和NaCl。
℃
(1) 中氯元素的化合价是________。
(2) 发生器发生反应: ,该反应的氧化剂
为________。通入的空气并不参与反应,其目的是________。
(3)工业上常选用试剂A加入吸收塔中。结合流程信息,试剂A是________。
a. b. c. d.
(4)吸收塔工作时需控制温度在10 以下,其目的是________。
℃
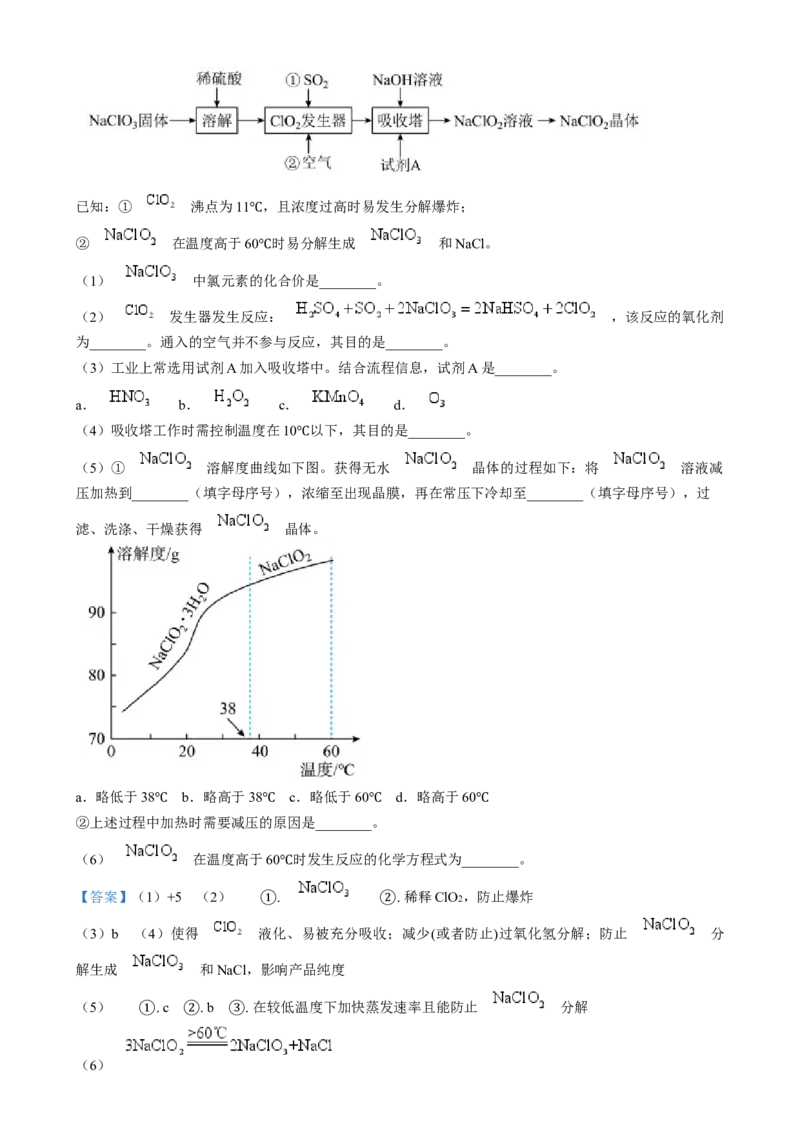
(5)① 溶解度曲线如下图。获得无水 晶体的过程如下:将 溶液减
压加热到________(填字母序号),浓缩至出现晶膜,再在常压下冷却至________(填字母序号),过
滤、洗涤、干燥获得 晶体。
a.略低于38 b.略高于38 c.略低于60 d.略高于60
②上述过程中加热时需要减压的原因是________。
℃ ℃ ℃ ℃
(6) 在温度高于60 时发生反应的化学方程式为________。
℃
【答案】(1)+5 (2) . . 稀释ClO2 ,防止爆炸
① ②
(3)b (4)使得 液化、易被充分吸收;减少(或者防止)过氧化氢分解;防止 分
解生成 和NaCl,影响产品纯度
(5) . c . b . 在较低温度下加快蒸发速率且能防止 分解
① ② ③
(6)【解析】
【分析】NaClO3 固体中加入稀硫酸溶解,向溶液中通入 SO2 和空气混合气,NaClO3 被SO2 还原生成
ClO2 ,ClO2 浓度过高时易发生分解爆炸,空气的作用是将 ClO2 稀释,防止发生爆炸,然后在碱性条件下
用过氧化氢还原,得到NaClO2 溶液,并从溶液得到NaClO2 晶体。
【小问1详解】
中钠氧分别为+1、-2,结合化合物中元素化合价代数和为零,氯元素的化合价是+5;
【小问2详解】
反应中氯化合价由+5降低为+4,发生还原反应,则 为氧化剂;已知, 沸点为
11 ,且浓度过高时易发生分解爆炸,通入的空气并不参与反应,其目的是:稀释ClO2 ,防止爆炸;
【小问3详解】
℃
“吸收塔” 中的作用是将产生的 反应转化为 ,氯化合价从+4降低到+3被还原,则需
加入还原剂,硝酸、臭氧、高锰酸钾均为常用氧化剂,过氧化氢中氧化合价可以升高,能做还原剂,故选
b;
【小问4详解】
沸点为11 ,且过氧化氢不稳定受热易分解,另根据信息, 在温度高于60 时易
分解生成 ℃ 和NaCl,则“吸收塔”中需要控制温度在10 以下的原因是使得 液化℃、易
被充分吸收;减少(或者防止)过氧化氢分解;防止 分℃解生成 和NaCl,影响产品
纯度;
【小问5详解】
①由 的溶解度曲线可以看出,温度低于38 时,会生成NaClO2•3H2O,所以温度应控制在
38 以上,则从 溶液中获得 晶℃体的操作是:将 溶液加热温度至略
低℃于60 蒸发浓缩、冷却至略高于38 结晶,过滤、洗涤、干燥获得 晶体。故选c、b;
℃ ℃
② 在温度高于60 时易分解,则蒸发过程中温度不能过高,而加热时进行减压可以在较低温
度下加快蒸发速率且能防止 ℃ 分解;
【小问6详解】
在温度高于60 时分解生成 和NaCl,氯化合价部分升高为+5、部分降低为-1,
℃
结合电子守恒,发生反应的化学方程式为 。
20. Ⅰ.经检测某工厂的酸性废水中所含离子种类及其浓度如下表所示:
离子
浓度/(mol/L)(1) ________mol/L。
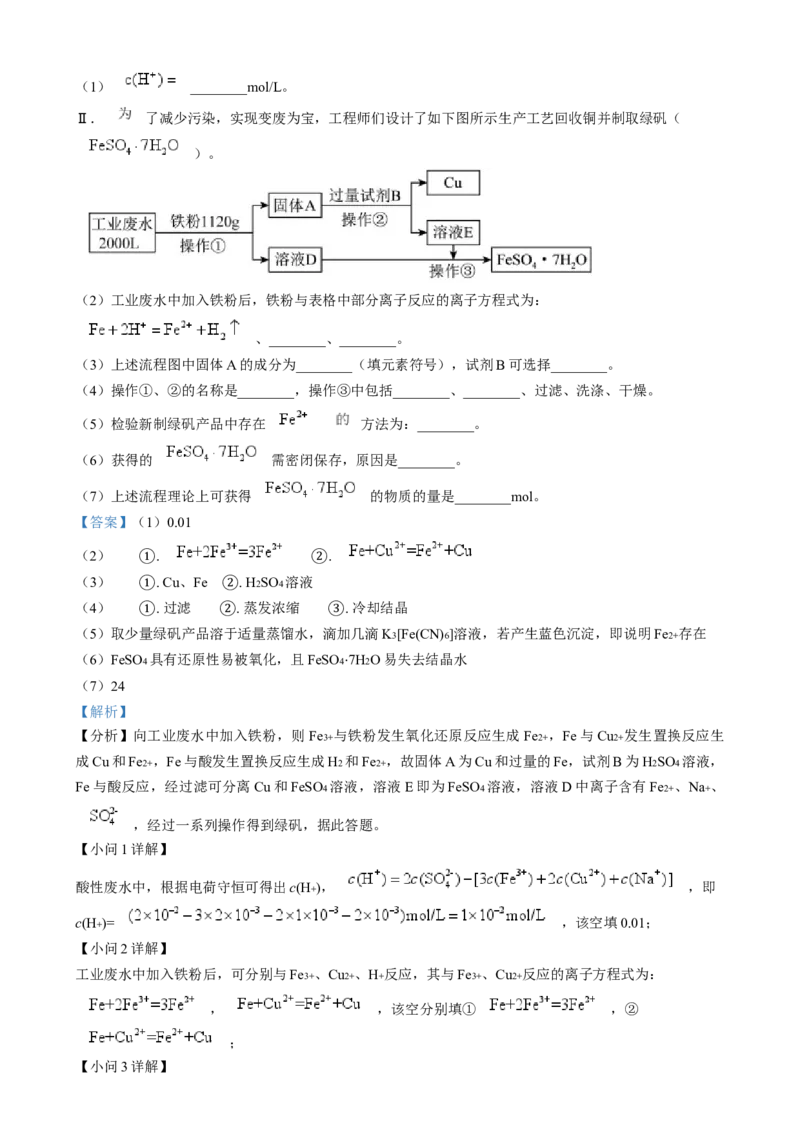
Ⅱ. 了减少污染,实现变废为宝,工程师们设计了如下图所示生产工艺回收铜并制取绿矾(
)。
(2)工业废水中加入铁粉后,铁粉与表格中部分离子反应的离子方程式为:
、________、________。
(3)上述流程图中固体A的成分为________(填元素符号),试剂B可选择________。
(4)操作①、②的名称是________,操作③中包括________、________、过滤、洗涤、干燥。
(5)检验新制绿矾产品中存在 方法为:________。
(6)获得的 需密闭保存,原因是________。
(7)上述流程理论上可获得 的物质的量是________mol。
【答案】(1)0.01
(2) . .
(3)
①
. Cu、Fe . H2SO4 溶液
②
(4) . 过滤 . 蒸发浓缩 . 冷却结晶
① ②
(5)取少
①
量绿矾产品溶
②
于适量蒸馏水,滴
③
加几滴K3[Fe(CN)6]溶液,若产生蓝色沉淀,即说明Fe2+ 存在
(6)FeSO4 具有还原性易被氧化,且FeSO47H2O易失去结晶水
(7)24
⋅
【解析】
【分析】向工业废水中加入铁粉,则Fe3+ 与铁粉发生氧化还原反应生成Fe2+ ,Fe与Cu2+ 发生置换反应生
成Cu和Fe2+ ,Fe与酸发生置换反应生成H2 和Fe2+ ,故固体A为Cu和过量的Fe,试剂B为H2SO4 溶液,
Fe与酸反应,经过滤可分离Cu和FeSO4 溶液,溶液E即为FeSO4 溶液,溶液D中离子含有Fe2+ 、Na+ 、
,经过一系列操作得到绿矾,据此答题。
【小问1详解】
酸性废水中,根据电荷守恒可得出c(H+), ,即
c(H+)= ,该空填0.01;
【小问2详解】
工业废水中加入铁粉后,可分别与Fe3+ 、Cu2+ 、H+ 反应,其与Fe3+ 、Cu2+ 反应的离子方程式为:
, ,该空分别填① ,②
;
【小问3详解】据分析可知,固体A为Cu和Fe,试剂B为H2SO4 溶液,该空分别填①Cu、Fe,②H2SO4 溶液;
【小问4详解】
根据流程图可知,操作①、②可分离固体和溶液,故该操作为过滤,而由FeSO4 溶液得到绿矾晶体需经过
蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,故该空分别为①过滤,②蒸发浓缩,③冷却结晶;
【小问5详解】
根据Fe2+ 的特征检验方法,取少量绿矾产品溶于适量蒸馏水,滴加几滴K3[Fe(CN)6]溶液,若产生蓝色沉
淀,即说明Fe2+ 存在,该空填取少量绿矾产品溶于适量蒸馏水,滴加几滴K3[Fe(CN)6]溶液,若产生蓝色
沉淀,即说明Fe2+ 存在;
【小问6详解】
FeSO47H2O需要密封保存,一方面由于Fe2+ 易被氧气氧化成Fe3+ ,另一方面明矾易风化而失去结晶水,
故
⋅
该空填FeSO4 具有还原性易被氧化,且FeSO47H2O易失去结晶水;
【小问7详解】
⋅
根据物质守恒,理论上废水中的Fe3+ 和过量铁粉均参与反应,最终生成FeSO4 ,n(Fe3+)=
,n(Fe)= ,故
n(FeSO4)=n(FeSO47H2O)=4mol+20mol=24mol。
⋅