文档内容
高一化学试卷(一) C.氯原子的结构示意图:
(本试卷满分100分,考试时间75分钟)
D.SO 的水溶液能导电,因此SO 属于电解质
2 2
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写
4.下列反应的离子方程式书写不正确的是 ( )
在试卷和答题卡规定的位置上。
A.铁与稀硫酸:2Fe+6H+2Fe2++3H↑
2
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需
B.稀盐酸与氢氧化钡溶液:H++OH-HO
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字 2
C.铜与硝酸银溶液:Cu+2Ag+Cu2++2Ag
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5
D.氧化钠与稀盐酸:Na
2
O+2H+2Na++H
2
O
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符 5.下列各物质的性质和用途都正确且有因果关系的是 ( )
合题目要求。
选项 性质 用途
1.对下列各组物质的分类正确的是 ( ) A NaCO 溶液显碱性 可以用来治疗胃酸过多
2 3
A.混合物:钢铁、液氯、硬铝 B NaHCO 3 受热易分解产生气体 可用作膨松剂
C HClO是弱酸 可用作有色物质的漂白剂
B.强酸:碳酸、硝酸、硫酸
D NaO 受热易分解 可用于潜水艇里的供氧剂
2 2
C.碱性氧化物:氧化钠、过氧化钠、氧化铜
D.电解质:醋酸、熔融氯化钠、过氧化钠 6.下列各选项中的两个反应,可用同一个离子方程式表示的是 ( )
2.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含一定量
选项 Ⅰ Ⅱ
的FeSO 和Fe(SO)溶液混合,再滴入稍过量的 NaOH溶液,随后加入油酸钠溶液,即可 A Ba(OH)溶液与过量NaHCO 溶液混合 NaOH溶液与过量NaHCO 溶液混合
4 2 4 3 2 3 3
生成黑色的、分散质粒子直径在5.5~36nm的磁流体。下列说法中正确的是 ( ) B 少量CO 通入澄清石灰水中 过量CO 通入澄清石灰水中
2 2
C KOH溶液与稀硝酸混合 Fe(OH)与稀硝酸混合
A.该分散系能产生丁达尔效应 2
D NaCO 溶液与过量HSO 溶液混合 少量KCO 溶液与HCl溶液混合
2 3 2 4 2 3
B.所得的分散系属于悬浊液
C.该磁流体的制备过程为物理变化 7.下列有关氯气的叙述中,正确的是 ( )
D.该分散系中的粒子做有规律的运动 A.氯气可使湿的红布褪色,所以氯气具有漂白性
3.已知反应:SO +Cl+2HOHSO +2HCl,相关化学用语正确的是 ( ) B.氯气是有毒气体,遇到氯气泄漏应向低处逃生
2 2 2 2 4
A.SO 是酸性氧化物 C.在通常情况下,氯气可以和任何金属直接化合
2
B.HSO 的电离方程式:HSO H++SO2- D.氯气经过降温加压转变为液氯后仍然是纯净物
2 4 2 4 4
高一化学试卷(一) 第1页 (共8页) 高一化学试卷(一) 第2页 (共8页)
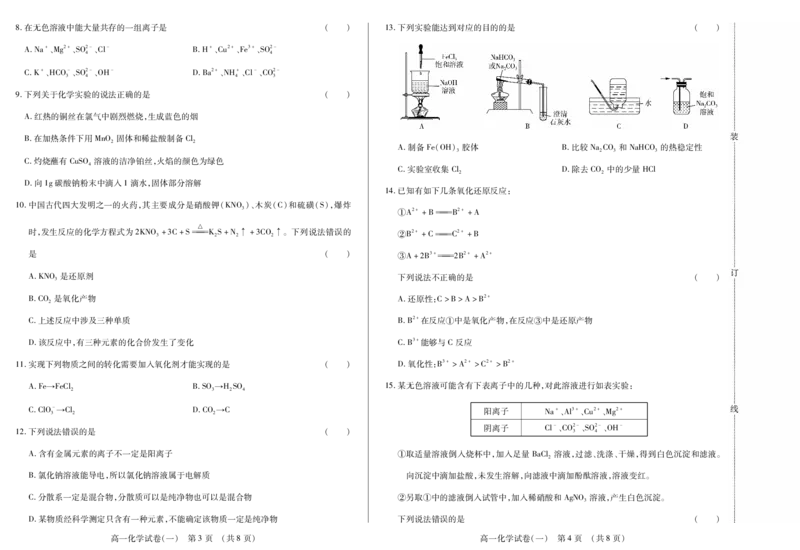
书书书8.在无色溶液中能大量共存的一组离子是 ( ) 13.下列实验能达到对应的目的的是 ( )
A.Na+、Mg2+、SO2-、Cl- B.H+、Cu2+、Fe3+、SO2-
4 4
C.K+、HCO-、SO2-、OH- D.Ba2+、NH+、Cl-、CO2-
3 4 4 3
9.下列关于化学实验的说法正确的是 ( )
A.红热的铜丝在氯气中剧烈燃烧,生成蓝色的烟
B.在加热条件下用MnO 固体和稀盐酸制备Cl
2 2
A.制备Fe(OH)胶体 B.比较NaCO 和NaHCO 的热稳定性
3 2 3 3
C.灼烧蘸有CuSO 溶液的洁净铂丝,火焰的颜色为绿色
4
C.实验室收集Cl D.除去CO 中的少量HCl
2 2
D.向1g碳酸钠粉末中滴入1滴水,固体部分溶解
14.已知有如下几条氧化还原反应:
10.中国古代四大发明之一的火药,其主要成分是硝酸钾(KNO)、木炭(C)和硫磺(S),爆炸
3 ①A2++BB2++A
△
时,发生反应的化学方程式为2KNO
3
+3C+SK
2
S+N
2
↑ +3CO
2
↑。下列说法错误的 ②B2++CC2++B
是 ( ) ③A+2B3+2B2++A2+
A.KNO 是还原剂 下列说法不正确的是 ( )
3
B.CO 是氧化产物 A.还原性:C>B>A>B2+
2
C.上述反应中涉及三种单质 B.B2+在反应①中是氧化产物,在反应③中是还原产物
D.该反应中,有三种元素的化合价发生了变化 C.B3+能够与C反应
11.实现下列物质之间的转化需要加入氧化剂才能实现的是 ( ) D.氧化性:B3+>A2+>C2+>B2+
A.Fe→FeCl B.SO→HSO 15.某无色溶液可能含有下表离子中的几种,对此溶液进行如表实验:
2 3 2 4
C.ClO
3
-→Cl
2
D.CO
2
→C 阳离子 Na+、Al3+、Cu2+、Mg2+
阴离子 Cl-、CO2-、SO2-、OH-
12.下列说法错误的是 ( ) 3 4
A.含有金属元素的离子不一定是阳离子 ①取适量溶液倒入烧杯中,加入足量 BaCl溶液,过滤、洗涤、干燥,得到白色沉淀和滤液。
2
B.氯化钠溶液能导电,所以氯化钠溶液属于电解质 向沉淀中滴加盐酸,未发生溶解,向滤液中滴加酚酞溶液,溶液变红。
C.分散系一定是混合物,分散质可以是纯净物也可以是混合物 ②另取①中的滤液倒入试管中,加入稀硝酸和AgNO 溶液,产生白色沉淀。
3
D.某物质经科学测定只含有一种元素,不能确定该物质一定是纯净物 下列说法错误的是 ( )
高一化学试卷(一) 第3页 (共8页) 高一化学试卷(一) 第4页 (共8页)A.无需实验即可判断溶液中肯定不存在Cu2+ (5)Ca(OH)在水溶液里的电离方程式为: 。
2
B.加入足量BaCl溶液,发生反应的离子方程式为Ba2++SO2-BaSO↓
2 4 4 (6)丁工厂排出的废液里含有的污染物是 。
C.溶液中一定不存在Al3+、Cu2+、Mg2+、CO2-
3
(7)在M处取出的河水中,含有的离子主要是 。
D.溶液中一定存在Na+、SO2-、Cl-、OH-
4
(8)丙处主要发生的反应的离子方程式为: 。
二、非选择题:本题共4小题,共55分。
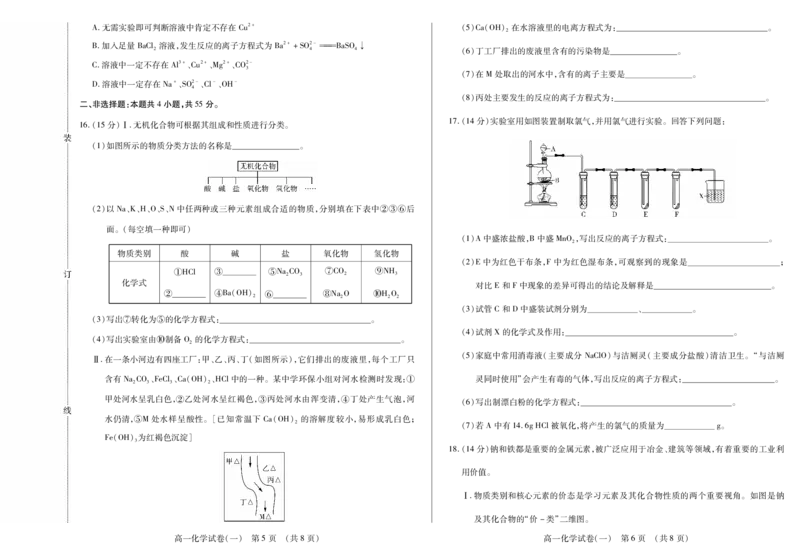
17.(14分)实验室用如图装置制取氯气,并用氯气进行实验。回答下列问题:
16.(15分)Ⅰ.无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法的名称是 。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后
面。(每空填一种即可)
(1)A中盛浓盐酸,B中盛MnO,写出反应的离子方程式: 。
2
物质类别 酸 碱 盐 氧化物 氢化物
(2)E中为红色干布条,F中为红色湿布条,可观察到的现象是 ;
①HCl ③ ⑤NaCO ⑦CO ⑨NH
2 3 2 3
化学式
对比E和F中现象的差异可得出的结论及解释是 。
② ④Ba(OH) ⑥ ⑧NaO ⑩HO
2 2 2 2
(3)试管C和D中盛装试剂分别为 、 。
(3)写出⑦转化为⑤的化学方程式: 。
(4)试剂X的化学式及作用: 。
(4)写出实验室由⑩制备O 的化学方程式: 。
2
(5)家庭中常用消毒液(主要成分 NaClO)与洁厕灵(主要成分盐酸)清洁卫生。“与洁厕
Ⅱ.在一条小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只
含有NaCO、FeCl、Ca(OH)、HCl中的一种。某中学环保小组对河水检测时发现:① 灵同时使用”会产生有毒的气体,写出反应的离子方程式: 。
2 3 3 2
甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河
(6)写出制漂白粉的化学方程式: 。
水仍清,⑤M处水样呈酸性。[已知常温下 Ca(OH) 的溶解度较小,易形成乳白色;
2 (7)若A中有14.6gHCl被氧化,将产生的氯气的质量为 g。
Fe(OH)为红褐色沉淀]
3
18.(14分)钠和铁都是重要的金属元素,被广泛应用于冶金、建筑等领域,有着重要的工业利
用价值。
Ⅰ.物质类别和核心元素的价态是学习元素及其化合物性质的两个重要视角。如图是钠
及其化合物的“价-类”二维图。
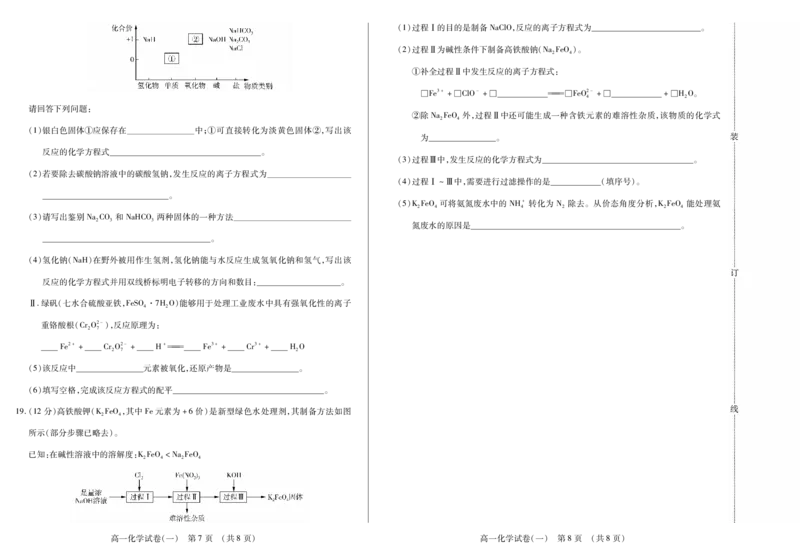
高一化学试卷(一) 第5页 (共8页) 高一化学试卷(一) 第6页 (共8页)(1)过程Ⅰ的目的是制备NaClO,反应的离子方程式为 。
(2)过程Ⅱ为碱性条件下制备高铁酸钠(NaFeO)。
2 4
①补全过程Ⅱ中发生反应的离子方程式:
□Fe3++□ClO-+□ □FeO2-+□ +□HO。
4 2
请回答下列问题:
②除NaFeO 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式
2 4
(1)银白色固体①应保存在 中;①可直接转化为淡黄色固体②,写出该
为 。
反应的化学方程式 。
(3)过程Ⅲ中,发生反应的化学方程式为 。
(2)若要除去碳酸钠溶液中的碳酸氢钠,发生反应的离子方程式为
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是 (填序号)。
。
(5)KFeO 可将氨氮废水中的NH+转化为 N 除去。从价态角度分析,KFeO 能处理氨
2 4 4 2 2 4
(3)请写出鉴别NaCO 和NaHCO 两种固体的一种方法
2 3 3
氮废水的原因是 。
。
(4)氢化钠(NaH)在野外被用作生氢剂,氢化钠能与水反应生成氢氧化钠和氢气,写出该
反应的化学方程式并用双线桥标明电子转移的方向和数目: 。
Ⅱ.绿矾(七水合硫酸亚铁,FeSO·7HO)能够用于处理工业废水中具有强氧化性的离子
4 2
重铬酸根(CrO2-),反应原理为:
2 7
Fe2++ CrO2-+ H+ Fe3++ Cr3++ HO
2 7 2
(5)该反应中 元素被氧化,还原产物是 。
(6)填写空格,完成该反应方程式的配平 。
19.(12分)高铁酸钾(KFeO,其中Fe元素为+6价)是新型绿色水处理剂,其制备方法如图
2 4
所示(部分步骤已略去)。
已知:在碱性溶液中的溶解度:KFeO <NaFeO
2 4 2 4
高一化学试卷(一) 第7页 (共8页) 高一化学试卷(一) 第8页 (共8页)