文档内容
机密★启用前
2023年河北省普通高中学业水平选择性考试
化学
题目1:
答案: D
解析: 粗盐提纯需经溶解、过滤除杂、蒸发结晶步骤,无需蒸馏操作。蒸馏常用于分离沸点差异较大的
液态混合物,与粗盐固相提纯无关。
题目2:
答案: B
解析: 氢氧化钠溶液会与玻璃成分二氧化硅反应生成硅酸钠,导致磨口玻璃塞粘连。应使用橡胶塞的广
口瓶保存。浓硝酸需避光保存,金属钠需隔绝空气保存,乙醇与高锰酸钾因氧化还原性质需分柜存放。
题目3:
答案: C
解析: 聚丙烯由丙烯通过加聚反应合成。聚乳酸具生物相容性可用于医疗,聚丙烯酰胺含酰胺基可水解,
聚丙烯腈由丙烯腈加聚制得。
题目4:
答案: B
解析: pH=2的HCl溶液中H⁺浓度为0.01 mol/L,1 L含H⁺数目为0.01N_A。NaH与H₂O反应生成H₂时,
H由-1价和+1价归中至0价,每生成1 mol H₂转移1 mol电子。碳原子质子数恒为6,中子数因同位素而
异;C_nH_{2n}可能是烯烃或环烷烃,后者无双键。
题目5:
答案: A
解析: Z易形成分子间氢键,熔点高于易形成分子内氢键的Y。X含酯基可水解;Y、Z均含酚羟基可与
Br₂取代;三者分子式相同(C₁₂H₁₀O₂),互为同分异构体。
题目6:
答案: A
第1页/共9页
学科网(北京)股份有限公司解析: CH₄无孤对电子,其价层电子对模型与空间构型均为正四面体。SO₂与OF₂虽均为V形,但中心原
子杂化方式不同(sp² vs sp³)。氢键有方向性而范德华力无;CCl₄仅含σ键不含π键。
题目7:
答案: C
解析: 碱金属熔点取决于金属键强度,锂离子半径最小故金属键最强。He替代H₂因惰性稳定;BF₃与
NH₃因B空轨道与N孤电子对成键;N原子无d轨道无法形成五氟化物。
题目8:
答案: A
解析: 由原子满足稀有气体构型及Z电子数为Q一半,推知W(H)、X(C)、Y(N)、Z(O)、Q(S)。稳定性:
H₂O > H₂S;第一电离能:N > C;C与S未成对电子数均为2;原子半径:O > H。
题目9:
答案: C
解析: SO₂使品红褪色因形成无色加合物,属非氧化还原褪色。Cl₂氧化I⁻、CO₂与苯酚钠生成苯酚、NH₃
水溶液呈碱性均符合对应结论。
题目10:
答案: C
解析: 由K_sp(MgF₂)=10^{-10.3} < K_sp(CaF₂)=10^{-8.3},当Ca²⁺、Mg²⁺浓度接近时,MgF₂先沉淀。酸
浸时Mn₂O₃氧化HCl生成Cl₂;pH=5-6时Al(OH)₃、Fe(OH)₃沉淀;沉淀工序离子方程式正确。
题目11:
答案: B
解析: 晶胞含4个Zr、8个O,化学式为ZrO₂。密度计算式应为 NA(a×10−10)34×91+8×16=NA
a3492×1030g/cm3。Zr原子最短距离为面对角线一半,p点平移后q点位⋅ 于xy面面心。
题目12:
答案: D
解析: 升温使反应③(活化能更高)的平衡逆向移动,c(Z)减小。0~2 min内X生成量因部分转化实际小
于0.16 mol/L;减压使反应②逆向移动,Y产率降低;平衡时2k₃c(Z)=k₂c²(X),若k₂=k₃则2c(Z)=c²(X)。
第2页/共9页
学科网(北京)股份有限公司题目13:
答案: B
解析: 充电时外电源正极应连接a电极(MnO₂/Mn²⁺氧化反应)。b电极充电时还原,放电时SO₄²⁻由①区
迁向②区,a电极反应为MnO₂还原。
题目14:
答案: D
解析: 由斜率关系得Ag₃X中x=3、K_sp=10^{-16},Ag_yY中y=1、K_sp=10^{-10}。J点加AgNO₃使
c(Ag⁺)↑,c(X³⁻)/c(Y⁻)↓。T点起始后Ag_yY沉淀,平衡时c(X³⁻)+c(Y⁻)>2c(Ag⁺)。
二、非选择题:本题共4题,共58分。
15. 配合物 在分析化学中用于 的鉴定,其制备装置示意图(夹持
装置等略)及步骤如下:
①向三颈烧瓶中加入 和 热蒸馏水,搅拌溶解。
②磁力搅拌下加入 ,从仪器a加入50%醋酸 。冷却至室温后,再从仪器b
缓慢滴入30%双氧水 。待反应结束,滤去固体。
③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
的
已知:i.乙醇、乙醚 沸点分别是 ;
第3页/共9页
学科网(北京)股份有限公司ii. 的溶解度数据如下表。
温度/℃ 20 30 40 50
溶解度/ 84.5 91.6 98.4 104.1
回答下列问题:
(1)仪器a的名称是_______,使用前应_______。
(2) 中钴的化合价是_______,制备该配合物的化学方程式为_______。
(3)步骤①中,用热蒸馏水的目的是_______。
(4)步骤③中,用乙醚洗涤固体产品的作用是_______。
(5)已知: (亮黄色)足量 与
产品反应生成 亮黄色沉淀,产品纯度为_______%。
(6)实验室检验样品中钾元素的常用方法是:将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色
相同时,用铂丝蘸取样品在外焰上灼烧,_______。
【答案】(1) ①. 分液漏斗 ②. 检漏
( 2 ) ① . ②.
(3)增加 的溶解度
(4)加速产品干燥 (5)80.0
(6)透过蓝色钻玻璃观察火焰的颜色,若呈紫色则含钾元素
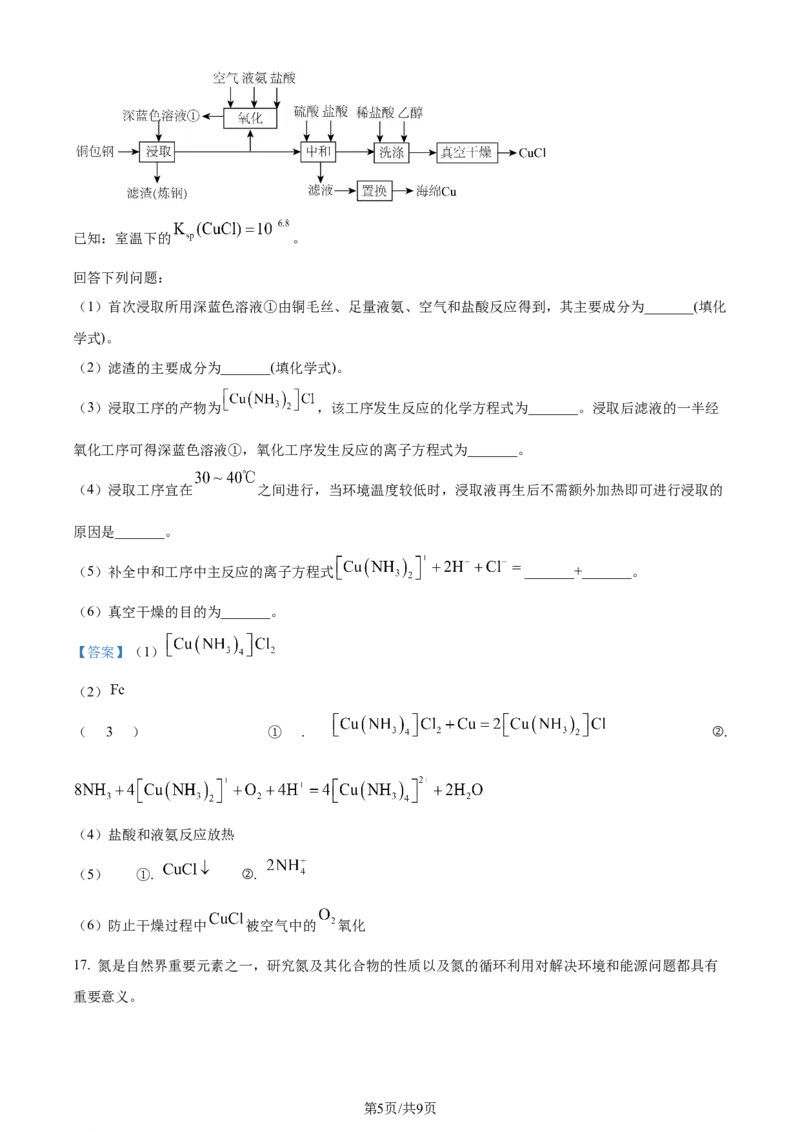
16. 闭环循环有利于提高资源利用率和实现绿色化学的目标。利用氨法浸取可实现废弃物铜包钢的有效分
离,同时得到的 可用于催化、医药、冶金等重要领域。工艺流程如下:
第4页/共9页
学科网(北京)股份有限公司已知:室温下的 。
回答下列问题:
(1)首次浸取所用深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分为_______(填化
学式)。
(2)滤渣的主要成分为_______(填化学式)。
(3)浸取工序的产物为 ,该工序发生反应的化学方程式为_______。浸取后滤液的一半经
氧化工序可得深蓝色溶液①,氧化工序发生反应的离子方程式为_______。
(4)浸取工序宜在 之间进行,当环境温度较低时,浸取液再生后不需额外加热即可进行浸取的
原因是_______。
(5)补全中和工序中主反应的离子方程式 _______+_______。
(6)真空干燥的目的为_______。
【答案】(1)
(2)
( 3 ) ① . ②.
(4)盐酸和液氨反应放热
(5) ①. ②.
(6)防止干燥过程中 被空气中的 氧化
17. 氮是自然界重要元素之一,研究氮及其化合物的性质以及氮的循环利用对解决环境和能源问题都具有
重要意义。
第5页/共9页
学科网(北京)股份有限公司已知: 物质中的化学键断裂时所需能量如下表。
物质
能量/ 945 498 631
回答下列问题:
(1)恒温下,将 空气( 和 的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为 的
恒容密闭容器中,假设体系中只存在如下两个反应:
i
ii
① _______ 。
②以下操作可以降低上述平衡体系中 浓度的有_______(填标号)。
A.缩小体积 B.升高温度 C.移除 D.降低 浓度
③若上述平衡体系中 ,则 _______
_______(写出含a、b、V的计算式)。
(2)氢气催化还原 作为一种高效环保的脱硝技术备受关注。高温下氢气还原 反应的速率方程为
为速率常数。在一定温度下改变体系中各物质浓度,测定结果如下表。
组
号
1 0.10 0.10 r
2 0.10 0.20
3 0.20 0.10
4 0.05 0.30 ?
表中第4组的反应速率为_______ 。(写出含r的表达式)
第6页/共9页
学科网(北京)股份有限公司(3)①以空气中的氮气为原料电解合成氨时, 在_______(填“阴”或“阳”)极上发生反应,产生 。
②氨燃料电池和氢燃料电池产生相同电量时,理论上消耗 和 的质量比为 ,则在碱性介质中氨
燃料电池负极的电极反应式为_______。
③我国科学家研究了水溶液中三种催化剂(a、b、c)上 电还原为 (图1)和 电还原为 (图2)反
应历程中的能量变化,则三种催化剂对 电还原为 的催化活性由强到弱的顺序为_______(用字母
a、b、c排序)。
【答案】(1) ①. 181 ②. CD ③. ④.
(2)
(3) ①. 阴 ②. ③. bac
18. 2,5-二羟基对苯二甲酸 是一种重要的化工原料,广泛用于合成高性能有机颜料及光敏聚合
物;作为钠离子电池的正、负电极材料也表现出优异的性能。利用生物质资源合成 的路线如下:
第7页/共9页
学科网(北京)股份有限公司已知:
回答下列问题:
(1) 的反应类型为_______。
(2)C的结构简式为_______。
(3)D的化学名称为_______。
(4) 的化学方程式为_______。
(5)写出一种能同时满足下列条件的G的同分异构体的结构简式_______。
(a)核磁共振氢谱有两组峰,且峰面积比为 ;
(b)红外光谱中存在 吸收峰,但没有 吸收峰;
(c)可与 水溶液反应,反应液酸化后可与 溶液发生显色反应。
(6)阿伏苯宗是防晒霜的添加剂之一。试以碘甲烷 、对羟基苯乙酮( )和对叔
丁基甲苯[ ]为原料,设计阿伏苯宗的合成路线_______。(无机试剂和三个碳以下的
有机试剂任选)
第8页/共9页
学科网(北京)股份有限公司【答案】(1)加成反应(或还原反应)
(2)CHOOCCH CHCOOH
3 2 2
(3)丁二酸二甲酯 (4) +4NaOH
+2CH OH+2H O
3 2
( 5 ) ( 6 )
第9页/共9页
学科网(北京)股份有限公司