文档内容
第 06 讲 影响化学反应速率的因素
知识导航
小杨老师 15521324728 侵权必究
温故知新
影响化学反应速率的因素可以分为内因和外因。
内因:_______________是决定化学反应速率的重要因素。
杨sir化学,侵权必究
外因:__________、__________、__________、__________、固体表面积等。
那么,如何定性与定量研究影响化学反应速率的因素呢?
知识精讲
小杨老师 15521324728 侵权必究
思考与交流:浓度、温度、催化剂等因素如何影响化学反应速率?
实验探究——定性研究影响化学反应速率的因素
杨sir化学,侵权必究
【实验仪器】烧杯、试管、量筒、试管架、胶头滴管、温度计、秒表。
【实验药品】0.1 mol/L NaSO 溶液、0.1 mol/L HSO 溶液、0.5 mol/L HSO 溶液、5% HO 溶液、
2 2 3 2 4 2 4 2 2
1mol/L FeCl 溶液、蒸馏水、热水。
3
【实验设计】
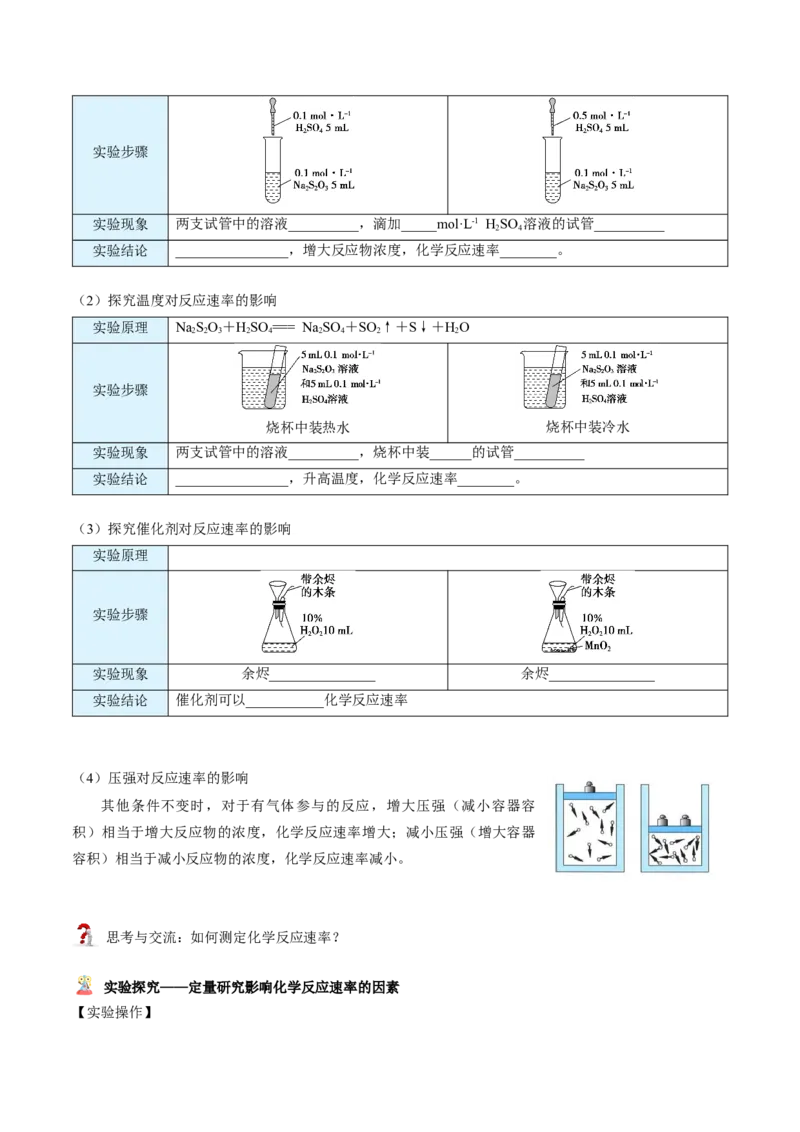
(1)探究浓度对反应速率的影响
实验原理 NaSO+HSO ===____________________________________
2 2 3 2 4实验步骤
实验现象 两支试管中的溶液__________,滴加_____mol·L-1 HSO 溶液的试管__________
2 4
实验结论 ________________,增大反应物浓度,化学反应速率________。
杨sir化学,侵权必究
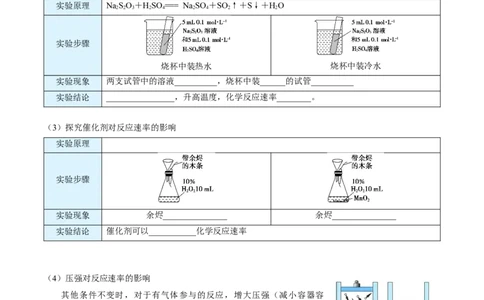
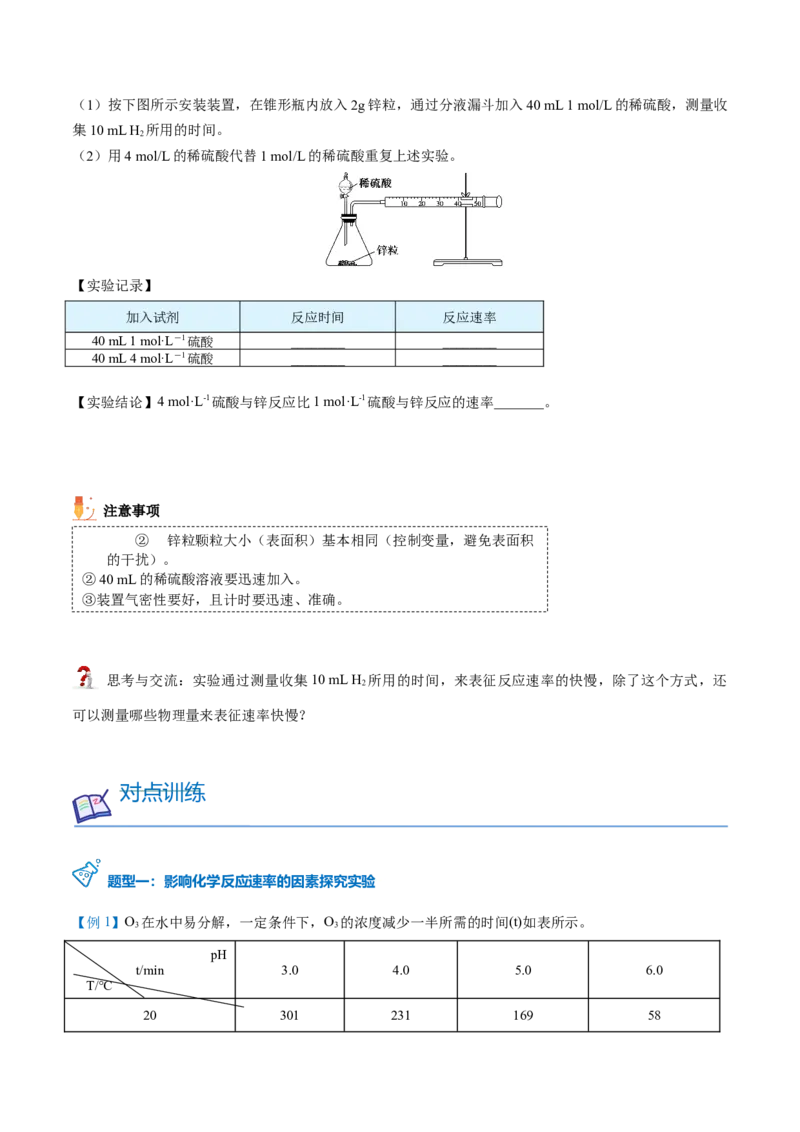
(2)探究温度对反应速率的影响
实验原理 NaSO+HSO === Na SO +SO ↑+S↓+HO
2 2 3 2 4 2 4 2 2
实验步骤
烧杯中装热水 烧杯中装冷水
实验现象 两支试管中的溶液__________,烧杯中装______的试管__________
实验结论 ________________,升高温度,化学反应速率________。
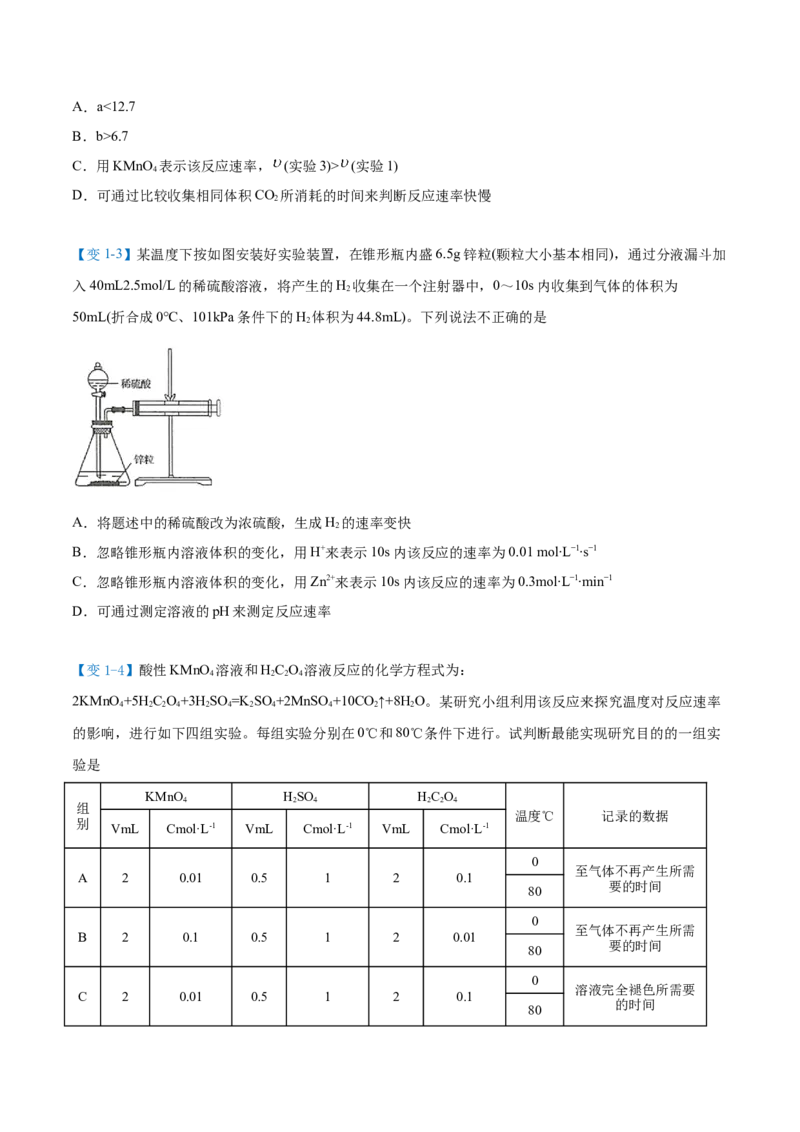
(3)探究催化剂对反应速率的影响
杨sir化学,侵权必究
实验原理
实验步骤
实验现象 余烬_______________ 余烬_______________
实验结论 催化剂可以___________化学反应速率
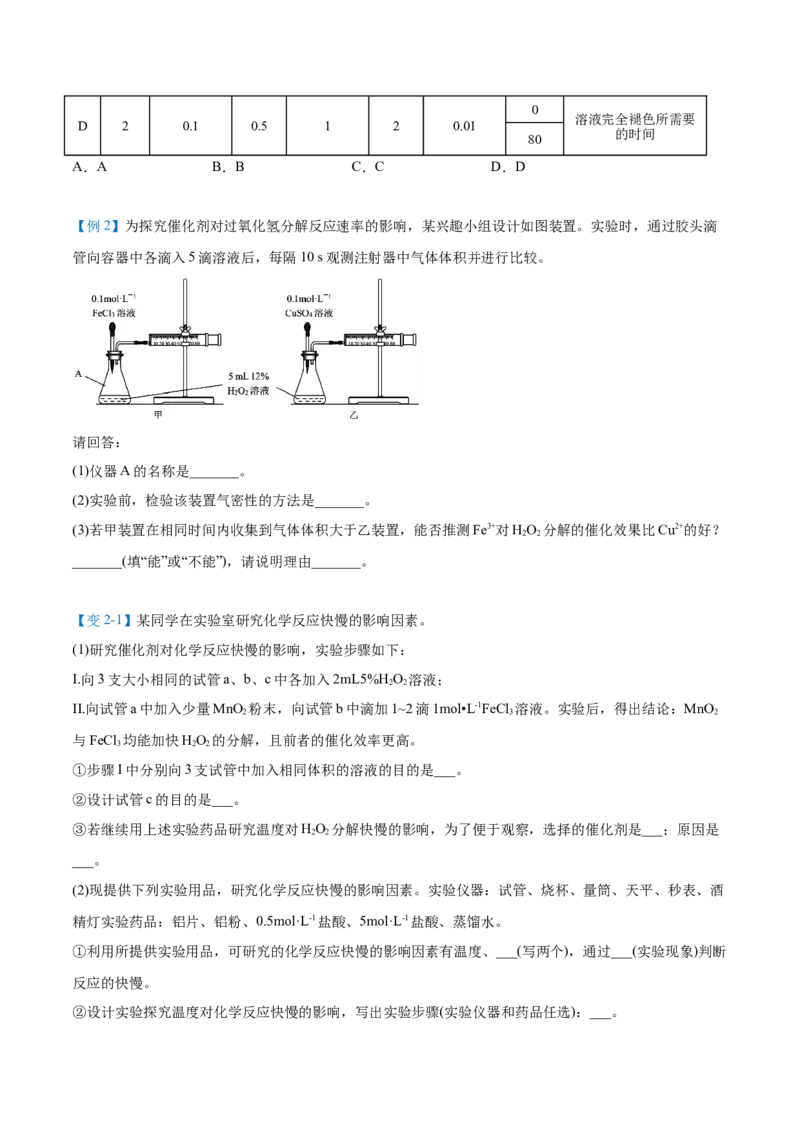
(4)压强对反应速率的影响
其他条件不变时,对于有气体参与的反应,增大压强(减小容器容
积)相当于增大反应物的浓度,化学反应速率增大;减小压强(增大容器
容积)相当于减小反应物的浓度,化学反应速率减小。
杨sir化学,侵权必究
思考与交流:如何测定化学反应速率?
实验探究——定量研究影响化学反应速率的因素
【实验操作】
杨sir化学,侵权必究(1)按下图所示安装装置,在锥形瓶内放入2g锌粒,通过分液漏斗加入40 mL 1 mol/L的稀硫酸,测量收
集10 mL H 所用的时间。
2
(2)用4 mol/L的稀硫酸代替1 mol/L的稀硫酸重复上述实验。
【实验记录】
加入试剂 反应时间 反应速率
40 mL 1 mol·L-1硫酸 ________ ________
40 mL 4 mol·L-1硫酸 ________ ________
【实验结论】4 mol·L-1硫酸与锌反应比1 mol·L-1硫酸与锌反应的速率_______。
杨sir化学,侵权必究
注意事项
② 锌粒颗粒大小(表面积)基本相同(控制变量,避免表面积
的干扰)。
②40 mL的稀硫酸溶液要迅速加入。
杨sir化学,侵权必究
③装置气密性要好,且计时要迅速、准确。
思考与交流:实验通过测量收集10 mL H 所用的时间,来表征反应速率的快慢,除了这个方式,还
2
可以测量哪些物理量来表征速率快慢?
对点训练
小杨老师 15521324728 侵权必究
题型一:影响化学反应速率的因素探究实验
杨sir化学,侵权必究
【例1】O 在水中易分解,一定条件下,O 的浓度减少一半所需的时间(t)如表所示。
3 3
pH
t/min 3.0 4.0 5.0 6.0
T/℃
20 301 231 169 5830 158 108 48 15
50 31 26 15 7
已知:O 的起始浓度为0.0216mol·L—1。
3
下列说法正确的是
A.pH增大能加速O 分解,表明对O 分解起催化作用的是H+
3 3
B.在30℃、pH=4.0条件下,O 的分解速率为1.67×10—6mol(L·s)—1
3
C.根据表中数据可知,O 的分解速率随温度升高而增大,随pH增大而减小
3 杨sir化学,侵权必究
D.根据表中数据的递变规律,推测O 在下列条件下分解速率的大小关系为40℃、pH=3.0>30℃、pH=7.0
3
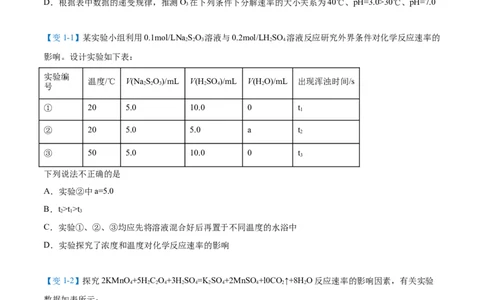
【变1-1】某实验小组利用0.1mol/LNa SO 溶液与0.2mol/LH SO 溶液反应研究外界条件对化学反应速率的
2 2 3 2 4
影响。设计实验如下表:
实验编
温度/℃ V(Na SO)/mL V(H SO )/mL V(H O)/mL 出现浑浊时间/s
号 2 2 3 2 4 2
① 20 5.0 10.0 0 t
1
② 20 5.0 5.0 a t
2
③ 50 5.0 10.0 0 t
3
下列说法不正确的是
A.实验②中a=5.0
B.t>t>t
2 1 3
C.实验①、②、③均应先将溶液混合好后再置于不同温度的水浴中
D.实验探究了浓度和温度对化学反应速率的影响
【变1-2】探究2KMnO +5H C O+3H SO =K SO +2MnSO +l0CO ↑+8H O反应速率的影响因素,有关实验
4 2 2 4 2 4 2 4 4 2 2
数据如表所示:
酸性KMn0 溶液 HCO 溶液 KMn0 溶液
实验 温度 催化剂 4 2 2 4 4
褪色平均时
编号 ℃ 用量g
体积(mL) 浓度(mol·L-1) 体积(mL) 浓度(mol·L-1) 间(min)
1 25 0.5 4 0.1 8 0.2 12.7
2 80 0.5 4 0.1 8 0.2 a
3 25 0.5 4 0.01 8 0.2 6.7
4 25 0 4 0.01 8 0.2 b
下列说法不正确的是A.a<12.7
B.b>6.7
C.用KMnO 表示该反应速率, (实验3)> (实验1)
4 杨sir化学,侵权必究
D.可通过比较收集相同体积CO 所消耗的时间来判断反应速率快慢
2
【变1-3】某温度下按如图安装好实验装置,在锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液漏斗加
入40mL2.5mol/L的稀硫酸溶液,将产生的H 收集在一个注射器中,0~10s内收集到气体的体积为
2
50mL(折合成0℃、101kPa条件下的H 体积为44.8mL)。下列说法不正确的是
2
A.将题述中的稀硫酸改为浓硫酸,生成H 的速率变快
2 杨sir化学,侵权必究
B.忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率为0.01 mol∙L−1∙s−1
C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率为0.3mol∙L−1∙min−1
D.可通过测定溶液的pH来测定反应速率
【变1-4】酸性KMnO 溶液和HC O 溶液反应的化学方程式为:
4 2 2 4 杨sir化学,侵权必究
2KMnO +5H C O+3H SO =K SO +2MnSO +10CO ↑+8H O。某研究小组利用该反应来探究温度对反应速率
4 2 2 4 2 4 2 4 4 2 2
的影响,进行如下四组实验。每组实验分别在0℃和80℃条件下进行。试判断最能实现研究目的的一组实
验是
KMnO HSO HCO
4 2 4 2 2 4
组
温度℃ 记录的数据
别
VmL Cmol·L-1 VmL Cmol·L-1 VmL Cmol·L-1
0
至气体不再产生所需
A 2 0.01 0.5 1 2 0.1
要的时间
80
0
至气体不再产生所需
B 2 0.1 0.5 1 2 0.01
要的时间
80
0
溶液完全褪色所需要
C 2 0.01 0.5 1 2 0.1
的时间
800
溶液完全褪色所需要
D 2 0.1 0.5 1 2 0.01
的时间
80
A.A B.B C.C D.D
【例2】为探究催化剂对过氧化氢分解反应速率的影响,某兴趣小组设计如图装置。实验时,通过胶头滴
管向容器中各滴入5滴溶液后,每隔10 s观测注射器中气体体积并进行比较。
请回答:
(1)仪器A的名称是_______。
(2)实验前,检验该装置气密性的方法是_______。
(3)若甲装置在相同时间内收集到气体体积大于乙装置,能否推测Fe3+对HO 分解的催化效果比Cu2+的好?
2 2
_______(填“能”或“不能”),请说明理由_______。
【变2-1】某同学在实验室研究化学反应快慢的影响因素。
(1)研究催化剂对化学反应快慢的影响,实验步骤如下:
I.向3支大小相同的试管a、b、c中各加入2mL5%H O 溶液;
2 2
II.向试管a中加入少量MnO 粉末,向试管b中滴加1~2滴1mol•L-1FeCl 溶液。实验后,得出结论:MnO
2 3 2
与FeCl 均能加快HO 的分解,且前者的催化效率更高。
3 2 2 杨sir化学,侵权必究
①步骤I中分别向3支试管中加入相同体积的溶液的目的是___。
②设计试管c的目的是___。
③若继续用上述实验药品研究温度对HO 分解快慢的影响,为了便于观察,选择的催化剂是___;原因是
2 2
___。
(2)现提供下列实验用品,研究化学反应快慢的影响因素。实验仪器:试管、烧杯、量筒、天平、秒表、酒
精灯实验药品:铝片、铝粉、0.5mol·L-1盐酸、5mol·L-1盐酸、蒸馏水。
①利用所提供实验用品,可研究的化学反应快慢的影响因素有温度、___(写两个),通过___(实验现象)判断
反应的快慢。
②设计实验探究温度对化学反应快慢的影响,写出实验步骤(实验仪器和药品任选):___。【变2-2】在生活中,需要对化学反应的速率和化学反应的限度进行研究,以便控制化学反应。
Ⅰ.某实验小组以HO 分解为例,研究浓度、催化剂、温度对反应速率的影响。按照如下方案完成实验。
2 2
项目 反应物 催化剂 温度
① 10mL10%H O 溶液 无 25℃
2 2
② 10mL20%H O 溶液 无 25℃
2 2
③ 10mL20%H O 溶液 无 40℃
2 2
④ 10mL20%H O 溶液 1~2滴0.1mol•L-1FeCl 溶液 40℃
2 2 3
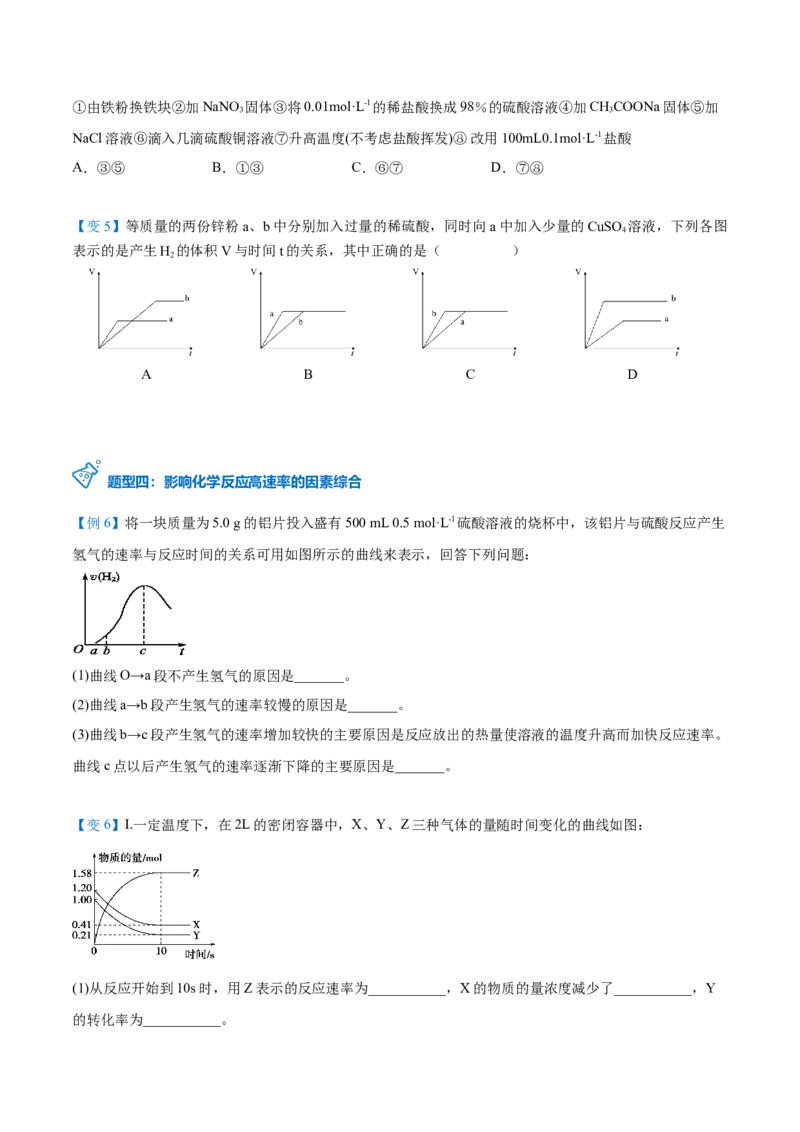
通过实验得到氧气的体积与时间的关系如图甲所示,回答下列问题:
(1)代表实验①的曲线是__。
(2)对比实验③和④的目的是_。
(3)通过上面对比实验,所得的实验结论是__。
Ⅱ.一定温度下,在体积为2L的恒容密闭容器中充入1molN 和3molH ,一定条件下发生反应N(g)+3H(g)
2 2 2 2
2NH (g),测得其中N 的物质的量随时间变化如图乙所示。回答下列问题:
3 2 杨sir化学,侵权必究
(4)从开始反应到t 时刻,氨的平均反应速率为___________。
2
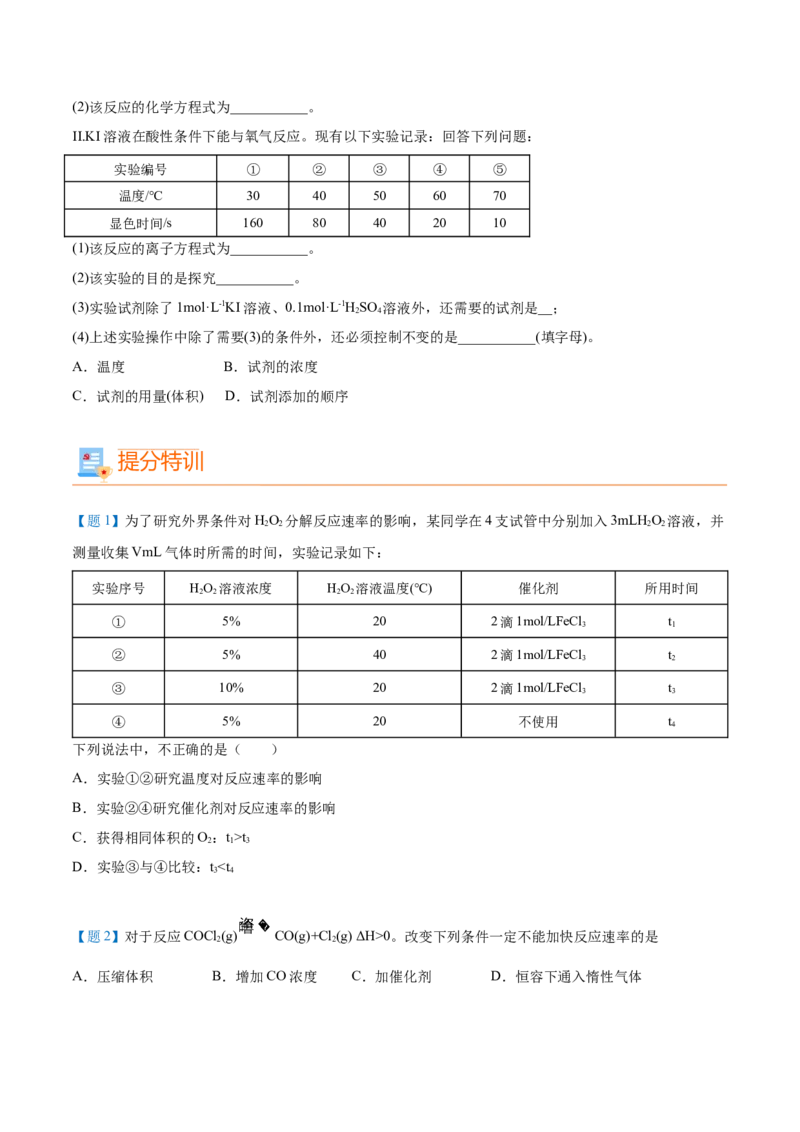
【变2-3】某学生设计如图Ⅰ装置,测定2mol·L-1的硫酸分别与锌粒、锌粉反应的速率。请回答:
(1)图Ⅰ装置中盛放硫酸的仪器名称是___。
(2)按照图Ⅰ装置实验时,已限定了两次实验时间均为10min,还需要测定的另一个数据是___。
(3)实验结束后,得到的结论是____。
杨sir化学,侵权必究(4)该学生又将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却室温后,该生准备读取滴定管上液
面所处的刻度数时,发现滴定管中液面高于干燥管中液面,应首先采取的操作是___。
(5)探究一定质量的锌粒与足量的2mol·L-1稀硫酸反应时,能减慢反应速率,又不影响氢气体积的条件是
___。
A.加入一定量的醋酸钠固体 B.加入一定量的硫酸铜
C.加入一定KNO 溶液 D.加入一定体积的NaSO 溶液
3 2 4
题型二:化学反应速率的影响因素
杨sir化学,侵权必究
【例3】下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
A.Cu能与浓硝酸反应,但不能与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C. 与 在常温、常压下不反应,放电时可反应
D.Fe与浓盐酸反应比与稀盐酸反应快
【变3】亚氯酸盐(如NaClO)可作漂白剂,在常温、不见光条件下可保存一年,在酸性下反应:
2
,开始时,反应非常慢,一段时间后,反应速率变快。对于该反应速率
变快的原因,下列猜测最合理的是
A.ClO-起催化作用 B.H+起催化作用
C.Cl-起催化作用 D.ClO 的逸出
2
【例4】在一密闭容器中充入1 mol H 和1 mol I ,压强为p(Pa),并在一定温度下使其发生反应:H(g)+
2 2 2
I g)=2HI(g)
2(
(1)保持容器容积不变,向其中充入1 mol H ,反应速率_________。
2 杨sir化学,侵权必究
(2)升高温度,反应速率________。
(3)扩大容器体积,反应速率______。
(4)保持容器内气体压强不变,向其中充入1 mol H (g)和1 mol I (g),反应速率________。
2 2
(5)保持容器体积不变,向其中充入1 mol N ,反应速率________。
2
(6)保持容器内气体压强不变,向其中充入1 mol N ,反应速率________。
2【变4-1】在某一密闭容器中,充入一定物质的量的N 和H,发生反应
2 2
,反应达到平衡后,下列条件的改变一定可以加快正反应速率的是
A.充入少量稀有气体 B.升高温度
C.及时移除产物 D.增大容器体积
【变4-2】对于100 mL1 mol·L-1盐酸与铁片的反应,采取下列措施:①升高温度;②改用100 mL3 mol·L-1
盐酸;③多用300 mL1 mol·L-1盐酸;④用等量铁粉代替铁片;⑤改用98%的硫酸。其中能使反应速率加快
的是
A.①③④ B.①②④ C.①②③④ D.①②③⑤
杨sir化学,侵权必究
【变4-3】下列说法正确的是
①增加水的量或升高温度,都可以加快镁跟水的反应速率。
②增加硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率。
③在可变体积的容器中进行 反应,充入氮气化学反应速率一定不改变。
④对于反应 ,加入KCl固体,逆反应速率瞬时增大,随
后正反应速率增大
A.①② B.①④ C.②④ D.无
【变4-4】反应3Fe(s)+4HO(g) Fe O(s)+4H(g)在一容积可变的密闭容器中进行,下列条件的改变
2 3 4 2
能使反应速率加快的是
①增加铁的量 ②将容器的体积缩小一半 ③保持体积不变,充入N 使体系压强增大 ④保持体积不变,
2
充入水蒸气使体系压强增大
A.①④ B.②③ C.③④ D.②④
题型三:化学反应速率与反应产量
杨sir化学,侵权必究
【例5】少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H 的
2
量,可以使用如下方法中的①由铁粉换铁块②加NaNO 固体③将0.01mol·L-1的稀盐酸换成98%的硫酸溶液④加CHCOONa固体⑤加
3 3
NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1mol·L-1盐酸
A.③⑤ B.①③ C.⑥⑦ D.⑦⑧
【变5】等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加入少量的CuSO 溶液,下列各图
4
表示的是产生H 的体积V与时间t的关系,其中正确的是( )
2
A B C D
题型四:影响化学反应高速率的因素综合
杨sir化学,侵权必究
【例6】将一块质量为5.0 g的铝片投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生
氢气的速率与反应时间的关系可用如图所示的曲线来表示,回答下列问题:
(1)曲线O→a段不产生氢气的原因是_______。
(2)曲线a→b段产生氢气的速率较慢的原因是_______。
(3)曲线b→c段产生氢气的速率增加较快的主要原因是反应放出的热量使溶液的温度升高而加快反应速率。
曲线c点以后产生氢气的速率逐渐下降的主要原因是_______。
【变6】I.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图:
(1)从反应开始到10s时,用Z表示的反应速率为___________,X的物质的量浓度减少了___________,Y
的转化率为___________。(2)该反应的化学方程式为___________。
II.KI溶液在酸性条件下能与氧气反应。现有以下实验记录:回答下列问题:
实验编号 ① ② ③ ④ ⑤
温度/℃ 30 40 50 60 70
显色时间/s 160 80 40 20 10
(1)该反应的离子方程式为___________。
杨sir化学,侵权必究
(2)该实验的目的是探究___________。
(3)实验试剂除了1mol·L-1KI溶液、0.1mol·L-1HSO 溶液外,还需要的试剂是__;
2 4
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是___________(填字母)。
A.温度 B.试剂的浓度
C.试剂的用量(体积) D.试剂添加的顺序
提分特训
小杨老师 15521324728 侵权必究
【题1】为了研究外界条件对HO 分解反应速率的影响,某同学在4支试管中分别加入3mLH O 溶液,并
2 2 2 2
测量收集VmL气体时所需的时间,实验记录如下:
实验序号 HO 溶液浓度 HO 溶液温度(℃) 催化剂 所用时间
2 2 2 2
① 5% 20 2滴1mol/LFeCl t
3 1
② 5% 40 2滴1mol/LFeCl t
3 2
③ 10% 20 2滴1mol/LFeCl t
3 3
④ 5% 20 不使用 t
4
下列说法中,不正确的是( )
A.实验①②研究温度对反应速率的影响
B.实验②④研究催化剂对反应速率的影响
杨sir化学,侵权必究
C.获得相同体积的O:t>t
2 1 3
D.实验③与④比较:t0。改变下列条件一定不能加快反应速率的是
2 2
A.压缩体积 B.增加CO浓度 C.加催化剂 D.恒容下通入惰性气体【题3】100mL6mol/LH SO 跟过量的锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气
2 4
的总量。可向反应物中加入适量的
A.碳酸钠(固体) B.水 C.硫酸铜溶液 D.硫酸铵(固体)
【题4】某同学设计实验探究镁与铵盐溶液的反应,仔细分析以下记录后,所得结论正确的是
实验编号 ① ② ③ ④
溶液种类
m( )/g 0.48 0.48 0.48 0.48
V(溶液)/mL 100 100 100 100
有气体产生,并产 有气体产生,并产生 有气体产生,并产 几乎看不到现
实验现象
生白色沉淀 白色沉淀 生白色沉淀 象
6h时 433 255 347 12
A.实验中产生的气体仅为 ,沉淀为
B.由实验①②可得,溶液中阴离子的浓度或种类对产生 的速率有影响
杨sir化学,侵权必究
C.由实验①③可得,溶液中 越大,反应速率越快
D.由实验①~④可得,溶液的 越小,产生 的速率越快
【题5】(1)在下列事实中,什么因素影响了化学反应的速率?
①石灰石煅烧时要粉碎成细小的矿粒_______;
②熔化的KClO 放出气泡很慢,撒入少量MnO ,则很快产生气体_______;
3 2
③同样大小的石灰石分别在0.1mol·L-1的盐酸和1mol·L-1的盐酸中反应速率不同_______;
④夏天的食品易霉变,冬天就不易发生该现象_______;
杨sir化学,侵权必究
(2)依据实验数据,写出下列反应的热化学方程式。
①1molC H(g)与适量O(g)反应,生成CO(g)和HO(1),放出1411kJ热量_______。
2 4 2 2 2
②2molAl(s)与适量O(g)发生反应,生成Al O(s),放出1669.8kJ热量_______。
2 2 3
③若适量的N 和O 完全反应,每生成23gNO 需要吸收16.95kJ热量,则表示该反应的热化学方程式为
2 2 2
_______。
④在25℃、101kPa时,4gH 在足量O 中完全燃烧生成HO(1)放出571.6kJ的热量,则表示H 燃烧热的热
2 2 2 2化学方程式为_______。
【题6】某小组拟用酸性KMnO 溶液与HC O 溶液的反应(此反应为放热反应)来探究“条件对化学反应速
4 2 2 4
率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20mol/
LHC O 溶液、0.010mol/LKMnO 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。
2 2 4 4
V(0.010mol/L酸
物理量编 V(0.20mol/LHCO V(蒸馏
2 2 4 性KMnO 溶液)/ m(MnSO)/g T/℃ 乙
号 溶液)/mL 水)/mL 4 4
mL
① 2.0 0 4.0 0 50
② 2.0 0 4.0 0 25
③ 1.5 a 4.0 0 25
④ 2.0 0 4.0 0.1 25
已知:2KMnO +5HC O+3HSO =KSO +2MnSO +10CO↑+8HO,回答下列问题:
4 2 2 4 2 4 2 4 4 2 2 杨sir化学,侵权必究
(1)KMnO 溶液用___________酸化(填名称);写出上述反应的离子方程式:___________;
4
(2)上述实验①②是探究___________对化学反应速率的影响;上述实验②④是探究___________对化学反
应速率的影响。
(3)若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;表格中的“乙”填写t/s,其
测量的是___________。
【题7】氧化剂 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验
小组以 分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成
实验。
实验编号 温度(℃) 反应物 催化剂
① 20 25 3% 溶液 无
② 20 25 5% 溶液 无
③ 20 25 5% 溶液 0.1g
④ 20 25 5% 溶液 1~2滴1 溶液
⑤ 30 25 5% 溶液 0.1g
(1)实验①和②的目的是___________。同学甲在进行实验①和②时并没有观察到明显现象。资料显示,通
常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是___________(写出一种即可)。杨sir化学,侵权必究
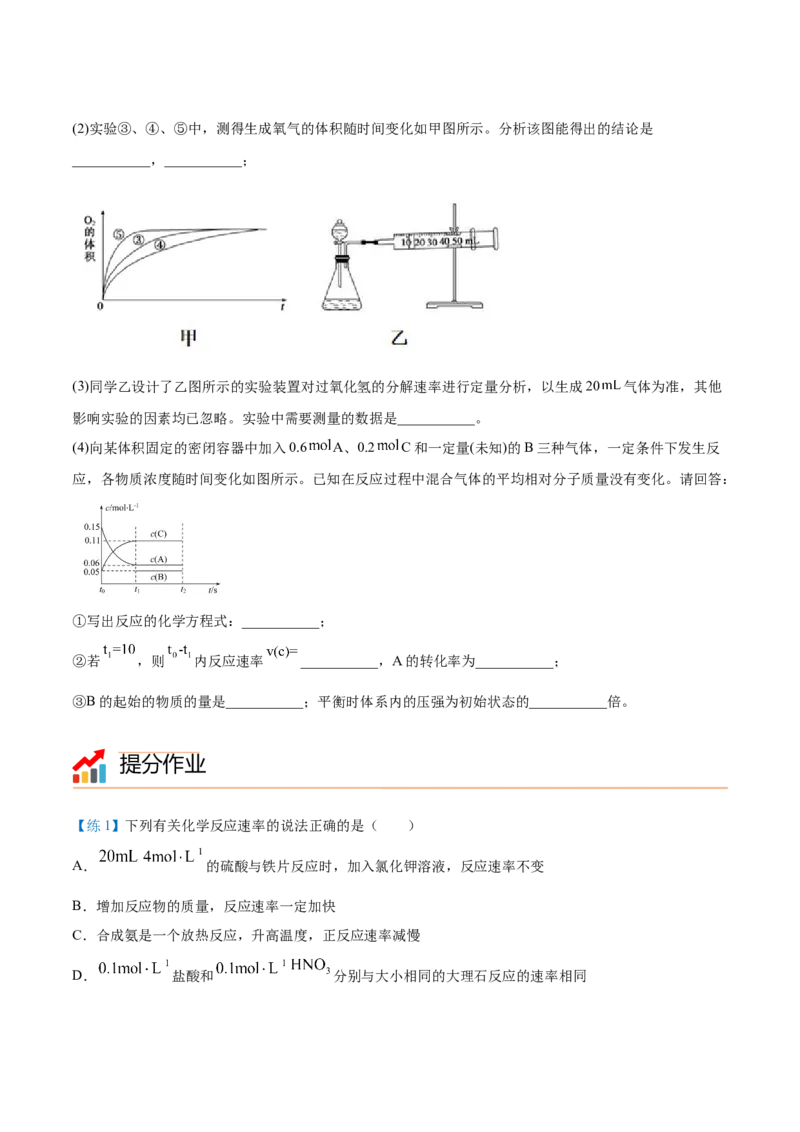
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。分析该图能得出的结论是
___________,___________;
(3)同学乙设计了乙图所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20 气体为准,其他
影响实验的因素均已忽略。实验中需要测量的数据是___________。
(4)向某体积固定的密闭容器中加入0.6 A、0.2 C和一定量(未知)的B三种气体,一定条件下发生反
应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①写出反应的化学方程式:___________;
杨sir化学,侵权必究
②若 ,则 内反应速率 ___________,A的转化率为___________;
③B的起始的物质的量是___________;平衡时体系内的压强为初始状态的___________倍。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列有关化学反应速率的说法正确的是( )
A. 的硫酸与铁片反应时,加入氯化钾溶液,反应速率不变
B.增加反应物的质量,反应速率一定加快
杨sir化学,侵权必究
C.合成氨是一个放热反应,升高温度,正反应速率减慢
D. 盐酸和 分别与大小相同的大理石反应的速率相同【练2】反应3Fe(s)+4HO(g) Fe O(s)+4H(g)在一容积可变的密闭容器中进行,下列条件的改变能
2 3 4 2
使反应速率加快的是
①增加铁的量 ②将容器的体积缩小一半 ③保持体积不变,充入N 使体系压强增大 ④保持体积不变,
2
充入水蒸气使体系压强增大
A.①④ B.②③ C.③④ D.②④
【练3】一定温度下,将1 mol A和2 mol B放入5 L的密闭容器中发生如下反应:A(s)+2B(g) C(g) + 2
D(g) △H<0,经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述正确的是
A.加入少量A,反应速率加快
B.在5 min内该反应用C的浓度改变量表示的反应速率为 0.02mol/(L·min)
C.保持体积不变,向容器充入一定量氦气,压强增大,反应速率加快
D.升高温度,正反应速率减小,逆反应速率加快
杨sir化学,侵权必究
【练4】用足量的铁片与一定量的稀硫酸反应制氢气,下列措施既能使氢气的生成速率加快,又不影响氢
气的产量的是
A.滴入适量NaSO 溶液 B.不用稀硫酸,改用98%的浓硫酸
2 4
C.加入少量碳酸钠固体 D.不用铁片,改用等质量的铁粉
【练5】对利用甲烷消除NO 污染进行研究,CH+2NO=====N+CO +2H O。在2L密闭容器中,控制不同
2 4 2 2 2 2
温度,分别加入0.50molCH 和1.2nolNO ,测得n(CH)随时间变化的有关实验数据见表。
4 2 4
时间/min
组别 温度 0 10 20 40 50
n/mol
① T n(CH) 0.50 0.35 0.25 0.10 0.10
1 4
② T n(CH) 0.50 0.30 0.18 … 0.15
2 4
下列说法不正确的是
A.组别①中,0~10min内,CO 的生成速率为0.0075mol·L-1·min-1
2
B.0~20min内,NO 的降解速率①>②
2 杨sir化学,侵权必究
C.40min时,表格中T 对应的数据为0.15
2
D.由实验数据可知实验控制的温度T