文档内容
第 06 讲 铵盐
知识导航
知识精讲
一、铵盐的概念及物理性质
1.概念:铵盐是由铵根离子(NH+)和酸根离子组成的化合物。
4
2.物理性质:铵盐是白色或无色固体,易溶于水。
二、铵盐的化学性质
1.受热分解,如NH Cl:__________________________;NH HCO :_____________________________。
4 4 3
2.与碱反应生成NH ·HO或放出NH
3 2 3
(1)(NH )SO 与NaOH固体共热:___________________________________________。
4 2 4
(2)铵盐溶液与碱液混合,不加热:___________________________________________。
(3)铵盐溶液与碱液混合,并加热:___________________________________________。
【答案】1. NHCl ===== NH ↑+ HCl↑ NH HCO ===== NH ↑+ H O + CO ↑
4 3 4 3 3 2 2
2.(1)(NH )SO + 2NaOH ===== NaSO + 2NH ↑+ 2H O
4 2 4 2 4 3 2
(2) + OH- === NH ·HO (3) + OH- ===== NH ↑+ H O
NH+ 3 2 NH+ 3 2
4 4
资料卡片——铵盐受热分解
大多数铵盐受热分解产生NH ,但有些例外,如NH NO ===== NO↑+ 2H O
3 4 3 2 2三、铵根离子的检验
【答案】湿润的红色石蕊试纸 浓盐酸
四、氨气的实验室制法
1.加热NH Cl和Ca(OH)
4 2
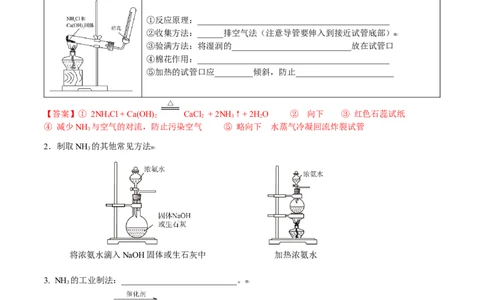
实验装置 反应原理、常见问题
①反应原理:_____________________________________________
②收集方法:______排空气法(注意导管要伸入到接近试管底部)
③验满方法:将湿润的____________________________放在试管口
④棉花作用:_____________________________________________
⑤加热的试管口应_________倾斜,防止_______________________
△
【答案】① 2NH
4
Cl + Ca(OH)
2
CaCl
2
+ 2NH
3
↑+ 2H
2
O ② 向下 ③ 红色石蕊试纸
④ 减少NH 与空气的对流,防止污染空气 ⑤ 略向下 水蒸气冷凝回流炸裂试管
3
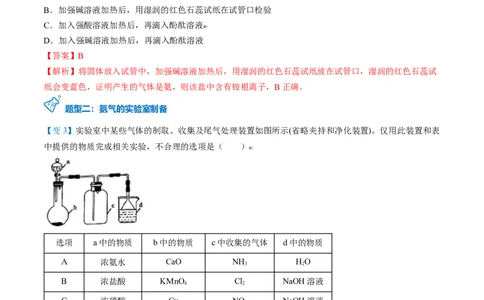
2.制取NH 的其他常见方法
3
将浓氨水滴入NaOH固体或生石灰中 加热浓氨水
3. NH 的工业制法:___________________________。
3
【答案】N + 3H 2NH
2 2 3
对点训练
题型一:铵盐的性质
【变1-1】下列不属于铵盐的共同性质的是( )A.易溶于水 B.与苛性钠共热产生NH
3
C.都是晶体 D.受热分解都产生NH
3
【答案】D
【解析】
【详解】
铵盐都是易溶于水的白色晶体,铵盐都能与碱反应,如与苛性钠反应生成氨气,铵盐都能受热分解,但不
一定有氨气产生,如:NH NO NO↑+2HO,故选D。
4 3 2 2
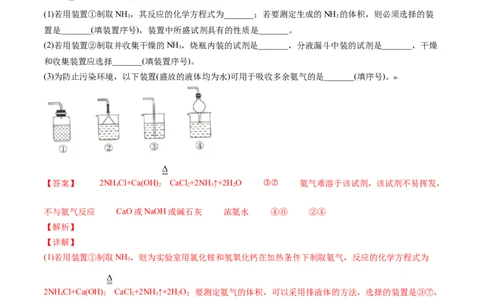
【例2】检验铵盐的一般方法是将待测物取少许置于试管中,然后( )
A.加水溶解后,再滴入酚酞溶液
B.加强碱溶液加热后,用湿润的红色石蕊试纸在试管口检验
C.加入强酸溶液加热后,再滴入酚酞溶液
D.加入强碱溶液加热后,再滴入酚酞溶液
【答案】B
【解析】将固体放入试管中,加强碱溶液加热后,用湿润的红色石蕊试纸放在试管口,湿润的红色石蕊试
纸会变蓝色,证明产生的气体是氨,则该盐中含有铵根离子,B正确。
题型二:氨气的实验室制备
【变3】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表
中提供的物质完成相关实验,不合理的选项是( )
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO NH HO
3 2
B 浓盐酸 KMnO Cl NaOH溶液
4 2
C 浓硝酸 Cu NO NaOH溶液
2
D 浓硫酸 NaSO SO NaOH溶液
2 3 2
【答案】A
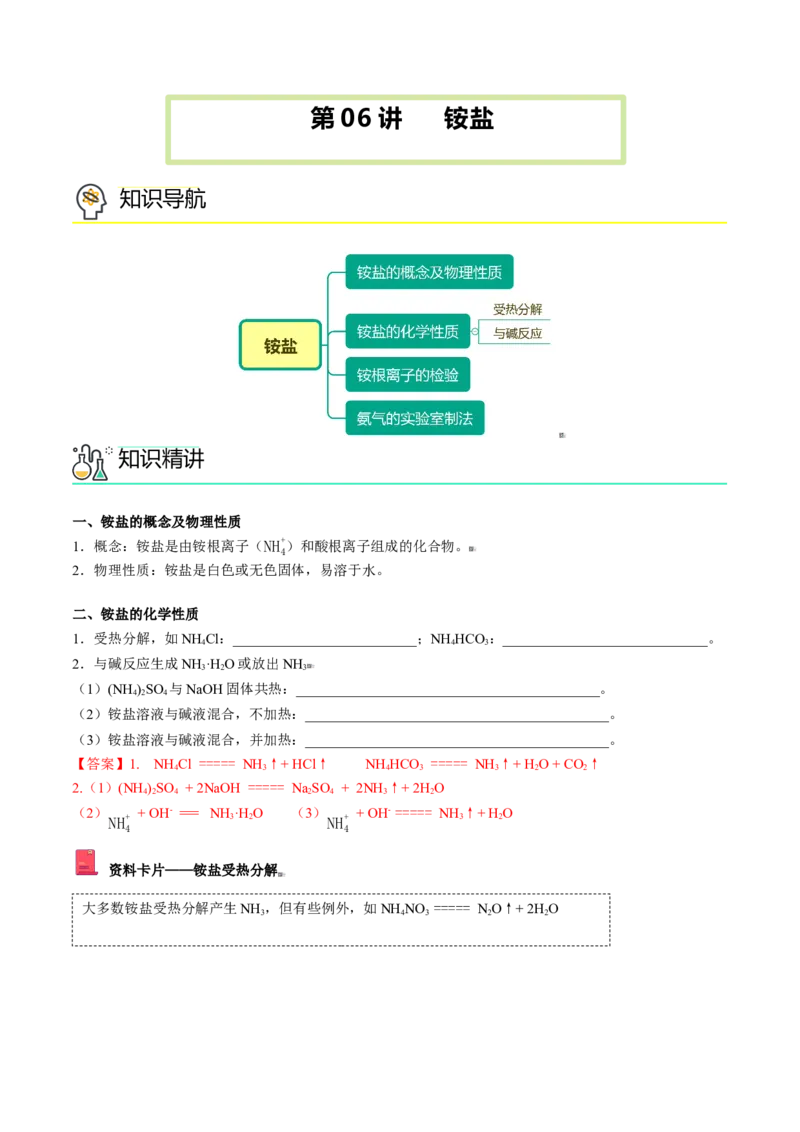
【例4】某同学用下列装置(固定、加热仪器和橡胶管已略去)进行有关氨气制取的实验。回答下列问题:(1)若用装置①制取NH ,其反应的化学方程式为_______;若要测定生成的NH 的体积,则必须选择的装
3 3
置是_______(填装置序号),装置中所盛试剂具有的性质是_______。
(2)若用装置②制取并收集干燥的NH ,烧瓶内装的试剂是_______,分液漏斗中装的试剂是_______,干燥
3
和收集装置应选择_______(填装置序号)。
(3)为防止污染环境,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_______(填序号)。
【答案】 2NH Cl+Ca(OH) CaCl +2NH↑+2H O ③⑦ 氨气难溶于该试剂,该试剂不易挥发,
4 2 2 3 2
不与氨气反应 CaO或NaOH或碱石灰 浓氨水 ④⑥ ②④
【解析】
【详解】
(1)若用装置①制取NH ,则为实验室用氯化铵和氢氧化钙在加热条件下制取氨气,反应的化学方程式为
3
2NH Cl+Ca(OH) CaCl +2NH↑+2H O;要测定氨气的体积,可以采用排液体的方法,选择的装置是③⑦,
4 2 2 3 2
在液体选择上氨气和该液体不能反应,氨气不能溶于该液体,该液体不易挥发;
(2)若用装置②制取并收集干燥的NH ,是固体和液体不加热制备气体的方法,可以利用浓氨水滴入碱石灰
3
中得到氨气,烧瓶中装入的试剂是CaO或NaOH或碱石灰,分液漏斗中是浓氨水;氨气极易溶于水,常温
下氨气和空气中的成分不反应,且氨气密度小于空气,所以可以采用向下排空气法收集,氨气是碱性气体,
应用碱石灰干燥,则应选择装置④⑥;
(3)因为氨气极易溶于水,吸收多余氨气的装置必须能够防止倒吸,则应选择装置②④。
【变4】氮元素的单质和常见的化合物在工农业生产中用途广泛。Ⅰ.(1)常用作食品袋中填充气的是__;常用作制冷剂的化合物是__,该物质在空气中与HCl相遇有白烟生成,
产生该现象的反应的化学方程式是__。
(2)铵盐大多在农业上用作化肥。工业制备氨气的化学方程式为__。
Ⅱ.某同学用下列装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究。回答下列问题:
(1)若用装置①制取并收集干燥的NH ,其反应的化学方程式为__。若要测定生成的NH 的体积,则必须选
3 3
择的装置是__(填序号),装置中所盛试剂具有的性质是__。
(2)若用装置②制取并收集干燥的NH ,烧瓶内的试剂是__,分液漏斗中的试剂是__,收集装置应选择__
3
(填序号)。
(3)已知氨气极易溶于水,而难溶于有机溶剂。下列装置中不适用于氨气的尾气吸收的是__(填序号)。
【答案】 氮气 氨气 NH +HCl=NH Cl
3 4
③⑦ 氨气难溶于该试剂,该试剂不易挥发,不与氨
气反应 CaO或NaOH或碱石灰 浓氨水 ⑥ A
【解析】
【分析】
I.(1)氮气化学性质稳定,氨气易液化,白烟是NH Cl固体。
4
(2)工业合成氨是氢气和氮气反应。
Ⅱ.(1)若用装置①制取NH ,则实验室用氯化铵和氢氧化钙在加热条件下制取氨气。
3
(2)若用装置2制取并收集干燥的NH ,可以利用浓氨水滴入碱石灰中得到氨气。
3
(3)根据防倒吸原理进行分析。
【详解】
I.(1)氮气化学性质稳定,常用作食品袋中填充气,氨气易液化,液氨汽化时吸收大量热,常作制冷剂,白
烟是NH Cl固体,氨气和氯化氢反应生成氯化铵的化学方程式为 ;故答案为:
4
。(2)工业合成氨的化学方程式为 ;故答案为: 。
Ⅱ.(1)若用装置①制取NH ,则实验室用氯化铵和氢氧化钙在加热条件下制取氨气,反应的化学方程式为
3
;要测定氨气的体积,可以采用排液法测量,要求氨气和该
液体不能反应、氨气不能溶于该液体、该液体不能挥发,必须选择的装置是③⑦;故答案为:
;③⑦;氨气难溶于该试剂,该试剂不易挥发,不与氨气反
应。
(2)若用装置②制取并收集干燥的NH ,可以利用浓氨水滴入碱石灰中得到氨气,分液漏斗中是浓氨水;氨
3
气极易溶于水,常温下,氨气和空气中成分不反应,且氨气密度小于空气,所以可以采用向下排空气法收
集,选择装置⑥;故答案为:CaO或NaOH或碱石灰;浓氨水;⑥。
(3)氨气通过导管直接通入水中,不能防止倒吸,故A符合题意;使用倒置的漏斗,可以防止倒吸,可用于
吸收氨气,故B不符合题意;四氯化碳不能和氨气反应,也不溶解氨气,该装置可以防止倒吸,可用于吸
收氨气,故C不符合题意;球形干燥管可以防止倒吸,可用于吸收氨气,故D不符合题意;综上所述,答
案为A。
【点睛】
化学制备实验是常考题型,主要考查实验室制取气体的方法,利用装置选择不同的实验药品及分析收集装
置。
【例5】有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为 ),某小组在实验室对该反
应进行探究,并对岩脑砂进行元素测定。
[岩脑砂的制备]
(1)写出实验室装置A中发生反应的化学方程式:_______。
(2)装置C的仪器名称是_______。
(3)为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:_______→ef←_______(用小写字
母和箭头表示,箭头方向与气流方向一致)。
(4)证明氨气和氯气反应有 生成,需要的检验试剂中除了蒸馏水、稀硝酸、红色石蕊试纸外,还需要
_______、_______。[岩脑砂中元素的测定]
准确称取a g岩脑砂,与足量氧化铜混合加热(反应: ),利用
下列装置测定岩脑砂中氮元素和氯元素的物质的量之比。
(5)装置H中盛装的试剂作用是_______。
(6)若装置I增重b g,利用装置K测得气体体积为V L(已知常温常压下气体摩尔体积为 ),则岩
脑砂中 _______(用含b、V的代数式表示,不必化简),若取消J装置(其它装置均正确),
比正常值_______(填“偏高”、“偏低”或“无影响”)。
【答案】(1)
(2)(球形)干燥管
(3) a→dc hg←ji←b
(4) NaOH溶液 溶液
(5)吸收混合气体中的水蒸气,防止对HCl测定造成干扰,减小实验误差
(6) 偏低
【解析】
【分析】
由题给实验装置图可知,装置A中氯化铵固体与氢氧化钙固体共热反应制备氨气,装置C为中盛有的碱石
灰用于干燥氨气,装置B中二氧化锰与浓盐酸共热反应制备氯气,浓盐酸具有挥发性,制得的氯气中混有
氯化氢和水蒸气,装置F中盛有的饱和食盐水用于除去氯化氢气体,装置E中盛有的浓硫酸用于干燥氯气,
装置D用于探究干燥氨气与干燥氯气常温下反应生成氯化铵,为了使氨气和氯气在D中充分混合,密度比
空气小的氨气应从e口通入,则实验装置的连接顺序为A、C、D、E、F、B,各装置的接口连接顺序为
a→dc→ef←hg←ji←b,该实验设计缺少尾气处理装置和氮气收集装置。
(1)
由分析可知,装置A中发生的反应为氯化铵固体与氢氧化钙固体共热反应生成氯化钙、氨气和水,反应的化学方程式为 ,故答案为:
;
(2)
由装置图可知,装置C为球形干燥管,故答案为:(球形)干燥管;
(3)
由分析可知,为了使氨气和氯气在D中充分混合,实验装置的连接顺序为A、C、D、E、F、B,各装置的
接口连接顺序为a→dc→ef←hg←ji←b,故答案为:a→dc;hg←ji←b;
(4)
证明氨气和氯气反应有氯化铵生成,应检验用蒸馏水溶解得到的溶液中是否存在铵根离子和氯离子,检验
铵根离子需要试剂为氢氧化钠溶液和红色石蕊试纸,检验氯离子需要试剂为稀硝酸和硝酸银溶液,则缺少
的试剂为氢氧化钠溶液和硝酸银溶液,故答案为:NaOH溶液; 溶液;
(5)
由实验装置图可知,装置H中盛有的浓硫酸用于吸收反应生成的水蒸气,防止对装置I中盛有的碱石灰吸
收测定反应生成氯化氢造成干扰,导致实验误差,故答案为:吸收混合气体中的水蒸气,防止对HCl测定
造成干扰,减小实验误差;
(6)
装置I增重的质量为氯化氢的质量,由原子个数守恒可知,岩脑砂中氯原子的物质的量为 =
mol,装置K测得气体体积为反应生成氮气的体积,由氮原子个数守恒可知,岩脑砂中氮原子的物质的量
为 ×2= mol,则氮原子和氯原子的物质的量比为 : ,若取消J装置,装置I会吸收
装置K中产生的水蒸气,导致测得氯化氢的质量偏大,使得氮原子和氯原子的物质的量比偏低,故答案为:
: ;偏低。
提分特训
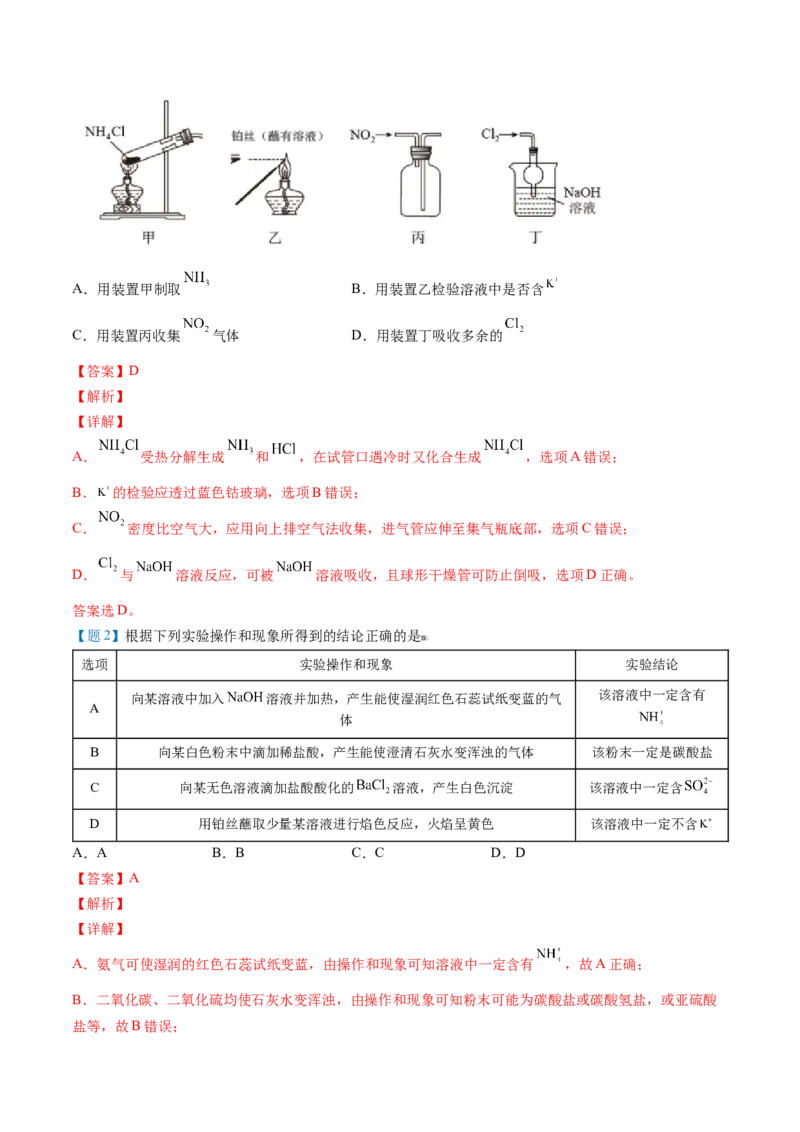
【题1】下列装置能达到实验目的的是A.用装置甲制取 B.用装置乙检验溶液中是否含
C.用装置丙收集 气体 D.用装置丁吸收多余的
【答案】D
【解析】
【详解】
A. 受热分解生成 和 ,在试管口遇冷时又化合生成 ,选项A错误;
B. 的检验应透过蓝色钴玻璃,选项B错误;
C. 密度比空气大,应用向上排空气法收集,进气管应伸至集气瓶底部,选项C错误;
D. 与 溶液反应,可被 溶液吸收,且球形干燥管可防止倒吸,选项D正确。
答案选D。
【题2】根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 实验结论
向某溶液中加入 溶液并加热,产生能使湿润红色石蕊试纸变蓝的气 该溶液中一定含有
A
体
B 向某白色粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体 该粉末一定是碳酸盐
C 向某无色溶液滴加盐酸酸化的 溶液,产生白色沉淀 该溶液中一定含
D 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色 该溶液中一定不含
A.A B.B C.C D.D
【答案】A
【解析】
【详解】
A.氨气可使湿润的红色石蕊试纸变蓝,由操作和现象可知溶液中一定含有 ,故A正确;
B.二氧化碳、二氧化硫均使石灰水变浑浊,由操作和现象可知粉末可能为碳酸盐或碳酸氢盐,或亚硫酸
盐等,故B错误;C.白色沉淀也可能是氯化银,不能说明溶液中一定含有硫酸根离子,故C错误;
D.观察K的焰色反应需要透过蓝色的钴玻璃,由操作和现象可知溶液中一定含Na+,不能确定是否含
K+,故D错误;
故选A。
【题3】能正确表示下列变化的离子方程式是
A.KHSO 溶液中滴入Ba(OH) 溶液至中性:H++ +Ba2++OH- = BaSO↓+H O
4 2 4 2
B.CuC1 溶液与过量氨水反应:Cu2++2NH ·H O=Cu(OH) ↓+2
2 3 2 2
C.KMnO 溶液滴入KOH溶液中微热,得到透明的绿色溶液KMnO :4 +4OH- 4
4 2 4
+O ↑+2H O
2 2
D.NH Al(SO ) 溶液中滴入少量NaOH溶液: +OHˉ= NH·H O
4 4 2 3 2
【答案】C
【解析】
【详解】
A.KHSO 溶液中滴入Ba(OH) 溶液至中性,反应生成硫酸钡沉淀、硫酸钾和水,反应的离子方程式为:
4 2
2H++ +Ba2++2OH- = BaSO↓+2H O,选项A错误;
4 2
B.CuC1 溶液与过量氨水反应生成四氨合硫酸铜和水,反应的离子方程式为:Cu2++
2
4NH ·H O=[Cu(NH )]2++4H O,选项B错误;
3 2 3 4 2
C.KMnO 溶液滴入KOH溶液中微热,得到透明的绿色溶液KMnO ,同时生成氧气和水,反应的离子方
4 2 4
程式为:4 +4OH- 4 +O ↑+2H O,选项C正确;
2 2
D.NH Al(SO ) 溶液中滴入少量NaOH溶液,氢氧根离子先与铝离子反应生成氢氧化铝,反应的离子方程
4 4 2
式为: Al3++3OHˉ= Al(OH) ↓,选项D错误;
3
答案选C。
【题4】实验室制取少量干燥的氨气涉及下列装置,其中正确的是
A. 是氨气发生装置B. 是氨气发生装置
C. 是氨气吸收装置
D. 是氨气收集、检验装置
【答案】B
【解析】
【详解】
A.NH Cl固体受热分解生成的NH 和HCl在试管口遇冷会重新化合生成NH Cl,故A错误;
4 3 4
B.将浓氨水滴到生石灰固体上时,生石灰与水反应放热会导致NH 逸出,此为氨气的发生装置,故B正
3
确;
C.NH 极易溶于水,为防止倒吸,倒置的漏斗口刚接触水面即可,不能浸于水中,故C错误;
3
D.收集NH 时,为防止NH 与空气形成对流使收集的NH 不纯,通常在导管口放置棉花团,故D错误;
3 3 3
答案选B。
提分作业
【练1】以下物质不可以直接通过化学反应转化的是
A.NH Cl→NH B.NH →NO C.S→SO D.Cu→SO
4 3 3 3 2
【答案】C
【详解】
A.NH Cl直接受热分解可生成NH ,A不符合题意;
4 3
B.NH 在催化剂高温的条件下可被氧气直接氧化为NO,B不符合题意;
3
C.S不能直接发生化学反应生成SO ,S与O 反应先生成SO ,SO 再被氧化生成SO ,C符合题意;
3 2 2 2 3
D.Cu跟浓硫酸直接加热可发生反应生成SO ,D不符合题意;
2
答案选C。
【练2】下列说法中正确的是( )
A.所有铵盐受热均可以分解,产物均有NH
3B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH
4
Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH+OH- =====NH
3
↑+H
2
O
D.NH Cl和NaCl的固体混合物可用升华法分离
4
【答案】C
【解析】A项,有的铵盐受热分解产生氨(如NH Cl),有的铵盐受热分解不产生氨(如硝酸铵);D项,可用
4
加热法分离NH Cl和某些固体(不分解、不升华的固体)的混合物,但其过程为先受热分解,再降温化合,
4
而不是升华。
【练3】为了检验某固体物质中是否含有 ,你认为下列试纸或试剂一定用不到的是
①蒸馏水 ② 溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀盐酸
A.①⑤ B.④⑤ C.①③ D.①④⑤
【答案】B
【解析】
【详解】
检验一般是取少量样品与碱液混合于试管中,加热,将用蒸馏水润湿的红色石蕊试纸靠近试管口,看
试纸是否变蓝;也可将蘸有浓盐酸的玻璃棒靠近试管口,看是否有白烟生成;因此④、⑤一定用不到,答
案选B。
【练4】下列离子方程式书写正确的是( )
A.实验室用氯化铵和熟石灰制氨:
B.NaOH溶液与 溶液混合加热:
C.氨水中加入盐酸:
D.氨水中加入氯化铁溶液:
【答案】C
【解析】
【详解】
A.该反应属于固体间的加热反应,不能写成离子形式,A错误;
B.加热条件下 应分解为 和 ,B错误;
C.符合反应原理及离子方程式书写要求,C正确;
D.一水合氨是弱碱,不能完全电离,向氨水中滴加 溶液应生成 沉淀,离子方程式应为 ,D错误;
答案选C。
【练5】实验室用下图装置(夹持装置已略去)制备NH ,并研究其性质。其中,a、b为湿润的红色石蕊试纸,
3
下列关于NH 性质实验的说法中,不正确的是
3
A.装置乙中,b先变蓝,a后变蓝 B.装置丙中,产生大量白烟
C.装置丁中,试剂可以是水 D.装置丁具有防止倒吸的作用
【答案】A
【详解】
A.由于NH 的密度比空气的小,故装置乙中,a先变蓝,b后变蓝甚至不变蓝,A错误;
3
B.浓盐酸具有挥发性,NH +HCl=NH Cl,产生NH Cl小颗粒,即装置丙中,产生大量白烟,B正确;
3 4 4
C.NH 极易溶于水,可以用水来吸收多余的NH ,装置丁中,试剂可以是水,C正确;
3 3
D.装置丁中的干燥管能够起到防止倒吸的作用,D正确;
故答案为:A。
【练6】某化学实验小组用如图装置制取、收集纯净干燥的氨,并探究氨的有关性质。
回答下列问题:
(1)开始实验之前要进行的操作是_____________________________________________。
(2)写出利用装置Ⅰ制取氨的化学方程式:_____________________________________。
(3)按照a、f、e、b、c、d的顺序将仪器连接,装置Ⅲ中倒置漏斗的作用是______________,装置Ⅳ中仪器
的名称为____________,盛装的试剂为________。
(4)向NH 的水溶液中滴加1~2滴酚酞溶液,溶液颜色由无色变________色,说明溶液显________性,写
3
出其电离方程式:______________________________________________。
【答案】(1)检验装置气密性 (2)2NH Cl+Ca(OH) CaCl +2HO+2NH ↑ (3)防止倒吸 球形干燥管
4 2===== 2 2 3
碱石灰 (4)红 碱 NH · H O NH+OH-
3 2倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育