文档内容
第06讲 分子结构的测定 多样的分子空间结构 价层电子对互斥模型
考点导航
知识精讲
知识点一:
一、分子结构的测定
1.早年的科学家主要靠对物质的化学性质进行系统总结得出规律后推测分子的结构。
2.如今,科学家应用红外光谱、晶体X射线衍射等现代仪器和方法测定分子的结构。
3.红外光谱工作原理
(1)原理:红外线透过分子时,分子会吸收跟它的某些化学键的 相同的红外线,再记录到谱图上
呈现吸收峰。通过和已有谱图库比对,或通过量子化学计算,可以分析出分子中含有何种 或官
能团的信息。
【答案】振动频率 化学键
(2)红外光谱仪原理示意图
微点拨
用红外光谱仪测定化学键或官能团信息。用质谱法测定分子的相对分子质量,在质谱图中质荷比最
大的数据代表所测物质的相对分子质量。
【即学即练1】1.经过X射线衍射实验等发现, 中存在 离子,下列粒子的VSEPR模型与空间结构都与 相同的是
A. B. C. D.
【答案】C
【解析】 可以看作I·I ,价层电子对数为2+ =4,VSEPR模型为四面体形,空间构型为V形,据
此分析;
的VSEPR模型为四面体形,空间构型为V形;
A.SO 的价层电子对数为2+ =3,VSEPR模型为平面三角形,空间构型为V形,与 不符,故A不
2
符合题意;
B.O 可以看作O·O ,价层电子对数为2+ =3,VSEPR模型为平面三角形,空间构型为V形,与 不
3 2
符,故B不符合题意;
C.OF 的价层电子对数为2+ =4,VSEPR模型为四面体形,空间构型为V形,与 相符,故C符合题
2
意;
D.NH 的价层电子对数为3+ =4,VSEPR模型为四面体形,空间构型为三角锥形,与 不符,故D
3
不符合题意;
答案为C。
2.经X—射线衍射测得化合物R的晶体结构,R代表 (五氮阴离子盐),其局部结构
如图所示。从结构角度分析,R中两种阳离子的不同之处是
A.中心原子的杂化轨道类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型【答案】C
【解析】R中的两种阳离子为H O+、 ;
3
A.H O+中O原子上的孤电子对数为 =1,σ键电子对数为3,价层电子对数为4,O为sp3杂
3
化, 中N原子上的孤电子对数为 =0,σ键电子对数为4,价层电子对数为4,N为sp3杂
化,中心原子的杂化类型均为sp3杂化,A项不符合题意;
B.中心原子的价层电子对数都为4,B项不符合题意;
C.H O+、 中中心原子的价层电子对数都为4,VSEPR模型都为四面体形,由于H O+中O原子上有1对
3 3
孤电子对, 中N原子上没有孤电子对,故H O+的立体结构为三角锥形,而 的立体结构为正四面
3
体形,两者的立体结构不同,C项符合题意;
D.H O+、 中都只存在σ键,D项不符合题意;
3
答案选C。
3.现代化学常用的测定分子的相对分子质量的方法是
A.质谱法 B.晶体 射线衍射法
C.核磁共振氢谱法 D.红外光谱法
【答案】A
【解析】现代化学常用质谱法测定分子的相对分子质量,故选A。
4.物质III(2, 二氢苯并呋喃)是一种重要的精细化工原料。其合成的部分流程如下:
下列叙述正确的是
A.III的核磁共振氢谱图显示有6种不同环境的氢原子,它是一种芳香烃,难溶于水
B.III与足量 加成所得产物分子中有2个手性碳原子C.I中所有原子可能位于同一平面内,氧原子为 杂化,碳原子为 杂化
D.II有弱酸性,但不能使紫色石蕊溶液变红,可与碳酸钠溶液反应,但没有气泡产生
【答案】B
【解析】A.III的结构不对称,III的核磁共振氢谱显示有6种不同化学环境的氢原子,该分子中含有C、
H、O三种元素且含有苯环,该分子不属于芳香烃,属于芳香族化合物,没有亲水基,只有憎水基,故不
易溶于水,A错误;
B.III与足量的H 加成后产物的结构简式为: ,两个环连接的碳原子为手性碳原子,共2
2
个手性碳原子,B正确;
C.I中亚甲基具有甲烷结构特点,故所有原子不可能位于同一平面内,亚甲基上的碳原子、氧原子的价层
电子对数均为4,则杂化方式均为sp3杂化,苯环上的碳原子杂化方式为sp2杂化,C错误;
D.II中含醇羟基,不含羧基和酚羟基,该物质无酸性,不能使紫色石蕊试液变红,不能与碳酸钠溶液反应,
D错误;
故选B。
知识点二:
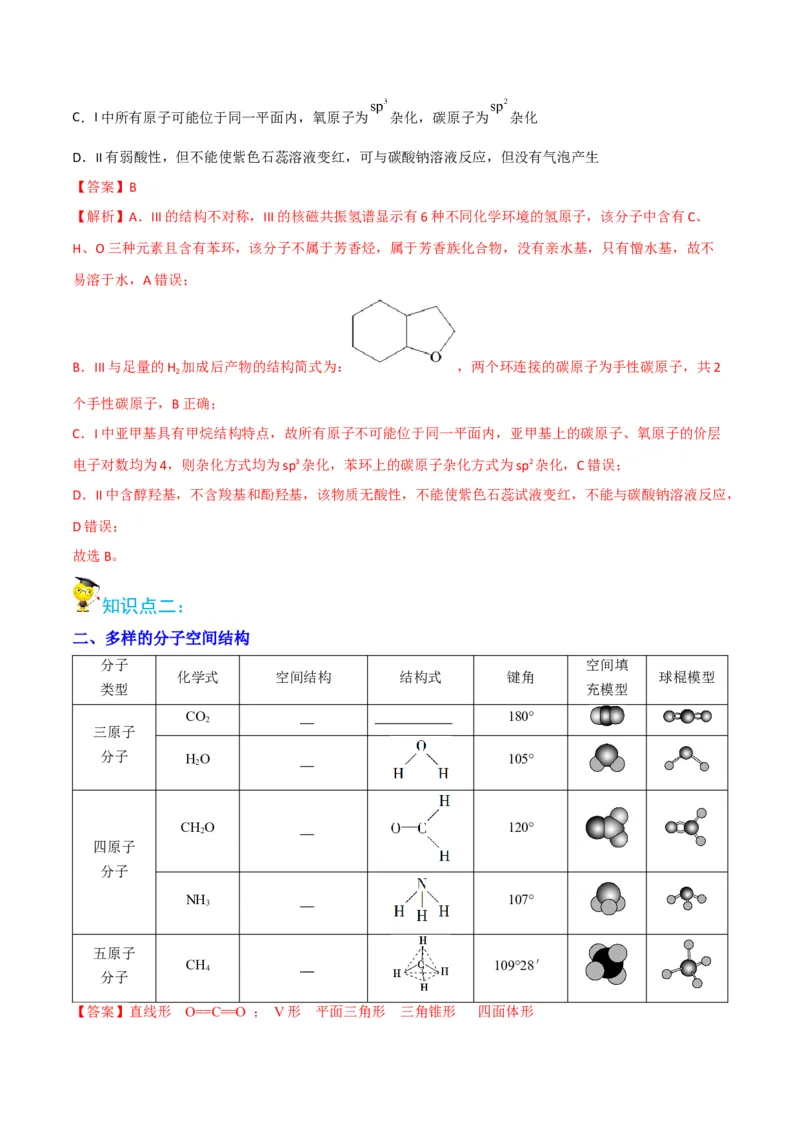
二、多样的分子空间结构
分子 空间填
化学式 空间结构 结构式 键角 球棍模型
类型 充模型
CO 180°
2
三原子
分子 HO 105°
2
CHO 120°
2
四原子
分子
NH 107°
3
五原子
CH 109°28′
4
分子
【答案】直线形 O==C==O ; V形 平面三角形 三角锥形 四面体形【即学即练2】
1.下列有关分子空间结构的说法正确的是
A.HClO、BF 、NCl 分子中所有原子的最外层电子都满足了8电子稳定结构
3 3
B.P 和CCl 都是正四面体形分子且键角都为109°28′
4 4
C.分子中键角的大小:BeCl >SO >NH >CCl
2 3 3 4
D.BeF 分子中,中心原子Be的价层电子对数等于2,其空间结构为直线形,成键电子对数等于2,没有孤
2
电子对
【答案】D
【解析】A.HClO中H原子的最外层电子数为1+1=2,不满足8电子稳定结构,BF 中B元素化合价为+
3
3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构;F元素化合价为−1,F原子最外层
电子数为7,所以1+7=8,F原子满足8电子结构,NCl 中P元素化合价为+3,N原子最外层电子数为
3
5,所以3+5=8,N原子满足8电子结构;Cl元素化合价为−1,Cl原子最外层电子数为7,所以1+7=8,
Cl原子满足8电子结构,故A错误;
B.P 是四原子的正四面体,键角是60°,而CH 是五原子的正四面体键角都为109°28′,故B错误;
4 4
C.BeCl 中Be形成2个σ键,无孤电子对,为sp杂化,键角为180°;SO 中S原子是sp2杂化,分子为平面
2 3
正三角形构型,键角为120°;NH 中N形成3个σ键,孤电子对数= ,为sp3杂化,为三角锥形,
3
键角大约为107°;CCl 中C形成4个σ键,无孤电子对,为sp3杂化,为正四面体,键角为109°28′,分子中
4
键角的大小:BeCl >SO >CCl >NH ,故C错误;
2 3 4 3
D.BeF 分子中,铍原子含有两个共价单键,不含孤电子对,所以价层电子对数是2,中心原子以sp杂化
2
轨道成键,价层电子对个数是2且不含孤电子对,为直线形结构,故D正确;
故答案选D。
2.下列各组粒子的空间结构相同的是
①NH 和H O;②NH 和H O+;③NH 和H O+;④O 和SO ;⑤CO 和BeCl 。
3 2 3 3 3 3 2 2 2
A.全部 B.①②③⑤ C.③④⑤ D.②⑤
【答案】C
【解析】根据价层电子对互斥理论确定微粒空间构型,价层电子对个数=σ键+孤电子对个数,孤电子对个
数= ×(a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子
最多能接受的电子数。①NH 中价层电子对个数=3+ ×(5-3)=4且含有一个孤电子对,所以为三角锥形,H O中价层电子对个数
3 2
=2+ ×(6-2)=4且含有两个孤电子对,所以为V形结构,二者空间构型不同,故①错误;
②NH +中价层电子对个数是4且不含孤电子对,为正四面体形结构;H O+中O原子价层电子对个数=3+
4 3
(6-1-3×1)=4且含有一个孤电子对,所以为三角锥形结构,二者空间构型不同,故②错误;
③NH 为三角锥形结构、H O+中O原子价层电子对个数=3+ (6-1-3×1)=4且含有一个孤电子对,所以为
3 3
三角锥形结构,所以二者空间构型相同,故③正确;
④O 、SO 中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故④正确;
3 2
⑤CO 分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+ (4-2×2)=2,二氧化碳是直线型结构,
2
BeCl 分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+ (2-2×1)=2,BeCl 是直线型结构,CO
2 2 2
和BeCl 分子都是直线型分子,故⑤正确;
2
答案选C。
1.下列分子或离子的空间结构相同的是
A.BeCl 和SO
2 2
B.BF 和PCl
3 3
C. 和
D.SO3和ClO
【答案】C
【解析】A. 分子中中心原子σ键数为2,孤电子对数为 ,空间结构为直线形,SO 分子中
2
中心原子σ键数为2,孤电子对数为 ,空间结构为V形,故A错误;
B. 分子中中心原子σ键数为3,孤电子对数为 ,空间结构为平面三角形, 分子中中心
原子σ键数为3,孤电子对数为 ,空间结构为三角锥形,故B错误;C. 中中心原子原子σ键数为4,孤电子对数为 ,空间结构为正四面体形, 中中心
原子σ键数为4,孤电子对数为 ,空间结构为正四面体形,故C正确;
D. 分子中中心原子σ键数为3,孤电子对数为 ,空间结构为平面三角形, 中中心原子σ
键数为3,孤电子对数为 ,空间结构为三角锥形,故D错误;
故答案选C。
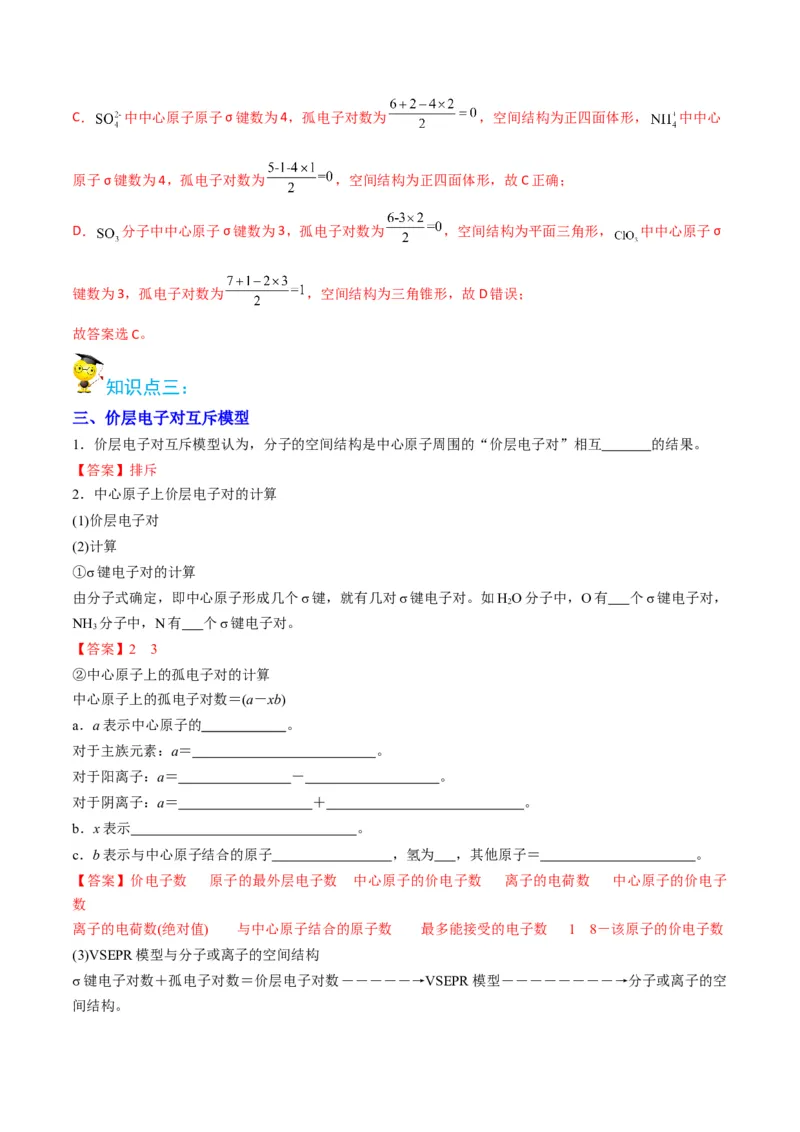
知识点三:
三、价层电子对互斥模型
1.价层电子对互斥模型认为,分子的空间结构是中心原子周围的“价层电子对”相互 的结果。
【答案】排斥
2.中心原子上价层电子对的计算
(1)价层电子对
(2)计算
①σ键电子对的计算
由分子式确定,即中心原子形成几个σ键,就有几对σ键电子对。如HO分子中,O有 个σ键电子对,
2
NH 分子中,N有 个σ键电子对。
3
【答案】2 3
②中心原子上的孤电子对的计算
中心原子上的孤电子对数=(a-xb)
a.a表示中心原子的 。
对于主族元素:a= 。
对于阳离子:a= - 。
对于阴离子:a= + 。
b.x表示 。
c.b表示与中心原子结合的原子 ,氢为 ,其他原子= 。
【答案】价电子数 原子的最外层电子数 中心原子的价电子数 离子的电荷数 中心原子的价电子
数
离子的电荷数(绝对值) 与中心原子结合的原子数 最多能接受的电子数 1 8-该原子的价电子数
(3)VSEPR模型与分子或离子的空间结构
σ键电子对数+孤电子对数=价层电子对数―――――→VSEPR模型――――――――→分子或离子的空
间结构。价层电子对 VSEPR 分子或离子的空间结
分子或离子 孤电子对数
数 模型名称 构名称
CO 0 2 直线形 直线形
2
SO 1 3 平面三角形 V形
2
CO 0 3 平面三角形 平面三角形
HO 2 4 四面体形 V形
2
NH 1 4 四面体形 三角锥形
3
CH 0 4 正四面体形 正四面体形
4
【即学即练3】
1.关于价层电子对互斥理论说法错误的是
A.价层电子对包括σ键电子对和中心原子上的孤电子对
B.分子中键角越大,价层电子对相互排斥力越小,分子越稳定
C.用该理论预测H S和BF 的空间结构为V形和平面三角形
2 3
D.该理论一定能预测出多中心原子的分子、离子或原子团的空间构型
【答案】D
【解析】A.价层电子对包括σ键电子对和中心原子上的孤电子对,不包含π键中的电子对,A正确;
B.分子中键角越大,价层电子对之间的距离越小,相互排斥力越小,则分子越稳定,B正确;
C.H S中S原子价层电子对数为:2+ =4,且含有2个孤电子对,分子呈V形结构;BF 中B原子价层
2 3
电子对数为:3+ =3,且不含孤电子对,分子呈平面三角形结构,C正确;
D.该理论不能预测所有分子或离子的空间构型,如:许多过渡金属化合物的几何构型不能用VSEPR模型
理论解释,D错误;
故合理选项是D。
2.用 模型可以判断许多分子或离子的空间结构,有时也能用来推测键角大小,下列判断正确的是
A. 分子中三个共价键的键能、键长、键角都相等
B. 、 、 键角由大到小的顺序为
C. 分子的键角是
D. 、 都是三角锥形的分子【答案】A
【解析】A. 是三角锥形的分子,其结构类似于氨气,分子中三个共价键的键能、键长、键角都相等,
A正确;
B. 、 、 中中心原子都是 杂化,都有1个孤电子对, 分子的中心原子 的电负性最
大,成键电子对距离中心原子最近,键角最大,键角由大到小的顺序为 ,B错误;
C. 是直线形分子,键角是 ,C错误;
D. 是三角锥形的分子, 分子中中心原子的价层电子对数 ,没有孤电子对,
是三角双锥形结构,D错误;
故选A。
3.下表中各粒子的 键电子对数、孤电子对数、和空间结构全部正确的是
粒子符
键电子对数 孤电子对数 空间结构
号
A 2 1 V形
B 2 2 直线形
C 3 1 平面三角形
D 4 0 正四面体
A.A B.B C.C D.D
【答案】D
【解析】A. 的 键电子对数为2,孤电子对对数为 个,采取sp3杂化则空间构型为V形,
故A错误;
B. 的 键电子对数为2,孤电子对对数为 ,采取sp杂化则空间构型为直线形,故B错
误;
C. 的 键电子对数为3,孤电子对对数为 ,采取sp3杂化则空间构型为三角锥形,故C错误;
D. 的 键电子对数为4,孤电子对对数为 ,采取sp3杂化则空间构型为正四面体,故
D正确;
故选D选项。
易错精析
BCl 的价层电子
3
1.对数、价层电子对空间结构、分子空间结构是怎样的?
【细剖精析】
BCl 的价层电子对数有3对,价层电子对空间结构为平面三角形,分子空间结构为平面三角形。
3
2.NF 的价层电子对、价层电子对空间结构、分子空间结构是怎样的?
3
【细剖精析】
NF 的价层电子对为4对,价层电子对空间结构为四面体形,分子空间结构为三角锥形。
3
3.通过(1)、(2)两例分析价层电子对的空间结构与分子的空间结构一定相同吗?二者之间有何规律存在?
【细剖精析】
价层电子对的空间结构与分子的空间结构不一定一致,分子的空间结构指的是成键电子对的空间结构,不
包括孤电子对(未用于形成共价键的电子对)。两者是否一致取决于中心原子上有无孤电子对,当中心原子
上无孤电子对时,两者的空间结构一致;当中心原子上有孤电子对时,两者的空间结构不一致。
4.四原子分子都为平面三角形或三角锥形吗?
【细剖精析】
不是。HO 分子的构型类似于一本打开的书,两个氧原子在两页书的交接处,两个 H原子分别在翻开的书
2 2
的两页上,如图1所示:
再如白磷(P )分子为正四面体形,如图2所示。
4
5.五原子分子都是正四面体结构吗?
【细剖精析】
不是,如CHCl、CHCl 、CHCl 等,虽为四面体结构,但由于碳原子所连的四个原子不相同,四个原子
3 2 2 3
电子云的排斥力不同,使四个键的键角不全相等,所以并不是正四面体结构。
6.应用价层电子对互斥模型如何将分子分类?
【细剖精析】应用价层电子对互斥模型将分子分成两大类:一类是中心原子上的价电子都用于形成共价键,如 CO 、
2
CHO、CH 等分子中的C原子,它们的立体构型可应用中心原子周围的原子数来预测;一类是中心原子上
2 4
有孤电子对(未用于形成共价键的电子对)的分子,如HO和NH 中心原子上的孤电子对也要占据中心原子
2 3
周围的空间,并参与互相排斥,因而HO分子呈V形,NH 分子呈三角锥形。
2 3
7.如何确定CO和NH的中心原子的孤电子对数?
【细剖精析】
阳离子:a为中心原子的价电子数减去离子的电荷数(绝对值),故NH中中心原子为N,a=5-1,b=1,x
=4,所以中心原子孤电子对数=(a-xb)=(4-4×1)=0。
阴离子:a为中心原子的价电子数加上离子的电荷数(绝对值),故CO中中心原子为C,a=4+2,b=2,x
=3,所以中心原子孤电子对数=(a-xb)= (6-3×2)=0。
8.分析CH===CH 和CH≡CH的中心原子的轨道杂化情况和成键情况。
2 2
【细剖精析】
在乙烯分子中C原子由一个s轨道和两个p轨道进行杂化,组成三个等同的sp2杂化轨道,sp2轨道彼此成
120°角。乙烯中的两个碳原子各用一个sp2轨道重叠形成一个C-C σ键外,又各以两个sp2轨道分别和两个
氢原子的1s轨道重叠,形成四个σ键,这样形成的五个键在同一平面上,每个C原子还剩下一个p轨道,
它们垂直于这五个σ键所在的平面,形成π键。在乙炔分子中碳原子由一个2s轨道和一个2p轨道杂化,
组成两个sp杂化轨道。两个sp杂化轨道夹角为180°,在乙炔分子中,两个碳原子各以一个sp轨道互相重
叠,形成一个C-C σ键,每一个碳原子又各以一个sp轨道分别与一个氢原子形成σ键,此外每个碳原子
还有两个互相垂直的未杂化的p轨道,它们与另一个碳的两个p轨道两两重叠形成两个π键。
9.在BF、BeF 分子中B、Be原子各用哪几个原子轨道参与杂化?形成什么类型的杂化轨道?
3 2
【细剖精析】
B原子参与杂化的原子轨道是一个2s轨道和两个2p轨道,形成三个sp2杂化轨道。Be原子参与杂化的原子
轨道是一个2s轨道和一个2p轨道,形成两个sp杂化轨道。
能力拓展
1.利用价层电子对互斥模型判断分子或离子的空间结构解题思路
说明:(1)若AB 型分子中,A与B之间通过两对或三对电子(即通过双键或三键)结合而成,则价层电子对
n
互斥模型把双键或三键作为一对电子对看待。
(2)价层电子对之间相互排斥作用大小的一般规律:孤电子对-孤电子对>孤电子对-成键电子对>成键电子对-成键电子对。随着孤电子对数目的增多,成键电子对与成键电子对之间的斥力减小,键角也减小。
如CH、NH 和HO分子中的键角依次减小。
4 3 2
2.用价层电子对互斥模型推测分子或离子的空间结构时的常见错误
1计算阴、阳离子的中心原子的价层电子对数时未考虑离子所带电荷而计算错误。
2由电子式或路易斯结构式判断中心原子价层电子对数时未将双键或三键当作一对价层电子对计算。
3不能准确区分和判断孤电子对和成键电子对。判断AB 型分子中孤电子对数的简单方法为孤电子对数=
n
价层电子对数-n。
4误将VSEPR模型当作分子或离子的空间结构。
5错误地利用相似性规律判断分子或离子的空间结构。
分层提分
题组A 基础过关练
1.六氟化硫分子空间结构呈正八面体形(如图所示),下列有关SF 的推测正确的是
6
A.六氟化硫是由极性键形成的极性分子
B.六氟化硫中各原子均达到8电子稳定结构
C.六氟化硫中心原子的价层电子对数为4
D.六氟化硫分子中的S-F键都是σ键,且键长、键能均相等
【答案】D
【解析】A.S和F属于不同原子,形成的是极性键,但分子是正八面体构型,正负电荷中心重合,是非极
性分子,A错误;
B.S原子的最外层有6个电子,在这个分子中,S形成了6个共价键,最外层不是8电子稳定结构,B错误;
C.六氟化硫中心原子的价层电子对数 ,C错误;
D.SF 中S和F中间都是单键(σ键),分子是正八面体构型,分子中心的硫原子到氟原子的距离都相等,化
6
学键都相同,故键长、键能都相等,D正确;
故选D。2.下列粒子的VSEPR模型为四面体、且其空间结构为V形的是
A. B. C. D.SF
2
【答案】D
【解析】A.二氧化硫分子中硫原子的价层电子对数为3,VSEPR模型为平面三角形,孤对电子对数为1,
分子的空间结构为V形,故A错误;
B.甲烷分子中碳原子的价层电子对数4,VSEPR模型为正四面体形,孤对电子对数为0,分子的空间结构
为正四面体形,故B错误;
C.水合氢离子中氧原子的价层电子对数为4,VSEPR模型为四面体形,孤对电子对数为1,分子的空间结
构为三角锥形,故C错误;
D.二氟化硫分子中硫原子的价层电子对数为4,VSEPR模型为四面体形,孤对电子对数为2,分子的空间
结构为V形,故D正确;
故选D。
3.利用价电子对互斥理论可推测分子结构中键角的大小,下列判断正确的是
A.苯的键角为109.5° B. 的键角为180°
C. 的键角比 的键角大 D.HCOOH分子中,H-C-O的键角为120°
【答案】C
【解析】A.苯中的C均为sp2杂化,为平面六边形结构,键角为120°,A错误;
B.根据价层电子对互斥理论,GeBr 的价层电子对数为2+ ×(4-2×1)=3,孤电子对数为1,为V形结构,由
2
于孤电子对斥力较大,键角小于120°,B错误;
C.根据价层电子对互斥理论,PH 的价层电子对数为3+ ×(5-3×1)=4, H S的价层电子对数为2+ ×(6-
3 2
2×1)=4,VSEPR模型为四面体形,H S的孤电子对数为2对,PH 为1对,孤电子对斥力较大,因此H S的键
2 3 2
角较小,C正确;
D.HCOOH中由于C=O双键的存在,C为sp2杂化,为平面三角形,由于羰基O的孤电子对的排斥作用,H-
C-O的键角略大于120°,D错误;
故选C。
4.下列分子或离子中,中心原子含有孤电子对的是
A.PCl B.NO C.SiCl D.PbCl
5 4 2【答案】D
【解析】分子中孤电子对个数= (中心原子价电子数-配原子个数×配原子形成稳定结构需要的电子数),
阳离子中孤电子对个数= (中心原子价电子数-电荷数-配原子个数×配原子形成稳定结构需要的电子数),
阴离子中孤电子对个数= (中心原子价电子数+电荷数-配原子个数×配原子形成稳定结构需要的电子数)。
A.PCl 中心原子碳原子孤电子对个数= (5-5×1)=0,没有孤对电子,故A不选;
5
B.NO 中心原子碳原子孤电子对个数= (5+1-3×2)=0,没有孤对电子,故B不选;
C.SiCl 中心原子碳原子孤电子对个数= (4-4×1)=0,没有孤对电子,故C不选;
4
D.PbCl 中心原子碳原子孤电子对个数= (4-2×1)=1,有孤对电子,故D选;
2
故选D。
5.用VSEPR模型预测下列分子或离子的立体结构,其中正确的是
A.CH 与CH Cl 均为正四面体 B.BeCl 与SO 为直线形
4 2 2 2 2
C.BF 与PCl 为三角锥形 D.NO 与CO 为平面三角形
3 3
【答案】D
【解析】A.CH 分子中价层电子对个数= ,采用sp3杂化,不含孤电子对,所以其空间构
4
型为正四面体,CH Cl 分子中价层电子对个数= ,采用sp3杂化,不含孤电子对,有H和
2 2
Cl,所以其空间构型为四面体,A错误;
B.BeCl 分子中价层电子对个数= ,采用sp杂化,且不含孤电子对,所以其空间构型为
2
直线型结构,SO 分子中价层电子对个数= ,采用sp2杂化,含1个孤电子对,所以其空
2
间构型为V形结构,B错误;
C.BF 分子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,所以其空间构型为平
3面三角形结构,PCl 分子中价层电子对个数= ,采用sp3杂化,且含1个孤电子对,所以其
3
空间构型为三角锥形结构,C错误;
D. 离子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,所以其空间构型
为平面三角形结构, 离子中价层电子对个数= ,采用sp2杂化,且不含孤电子对,
所以其空间构型为平面三角形结构,D正确;
故选D。
6.用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下
列判断正确的是
A.SO 、CS 、HCN都是直线形的分子
2 2
B.H O键角为120°,O 键角为180°
2 3
C.PCl 、NH 、GaCl 都是三角锥形的分子
3 3 3
D.HCHO、AlCl 、SO 都是平面三角形的粒子
3 3
【答案】D
【解析】A.SO 有2个 键,孤电子对数为 ,根据夹层电子对互斥理论可知SO 为sp2杂化,分子
2 2
为平面三角形;同理可知CS 为sp杂化,分子为直线型; HCN为sp杂化,分子为直线型,故A错误;
2
B.H O中心原子的价层电子对数为2+ ,所以采取的是sp3杂化,为V形结构,键角小于120°,
2
臭氧分子的空间结构与水分子的相似,其分子有极性,但很微弱,则其键角小于120°,故B错误;
C.PCl 和NH 是sp3杂化,分子空间构型为三角锥形,GaCl 有3个 键,孤电子对数为 ,为sp2杂化,
3 3 3
分子为平面三角形,故C错误;
D.HCHO含羰基、AlCl 中心原子的价层电子对数为3+ 、SO 中心原子的价层电子对数为3+
3 3
,则均采取sp2杂化,都是平面三角形的粒子,故D正确;
故答案为D。
7.依据价层电子对互斥理论,下列分子或离子的VSEPR模型相同的是
A. 、 B. 、C. 、 D. 、
【答案】A
【解析】A. 的成键数为2,孤对电子数为 =2,中心I原子的杂化轨道类型为sp3,VSEPR模型
是正四面体形, 中硫原子含有的孤对电子对数是 =0,属于sp3杂化,VSEPR模型是正四面
体形,A选;
B.OF 分子中O原子价层电子对数=2+ =4且含有2个孤电子对,VSEPR模型为四面体形,BeCl 分子
2 2
中,中心Be原子发生sp杂化,VSEPR模型为直线形,B不选;
C. 价层电子对数是3+ =3,且不含孤电子对,所以为平面三角形结构; 中S原子价层
电子对个数=3+ =4,为四面体结构,C不选;
D.BF 中心原子B的价层电子对数3,其杂化方式为sp2杂化,VSEPR构型为平面三角形,PCl 中心原子P
3 3
的价层电子对数4,其杂化方式为sp3杂化,VSEPR构型为四面体形,D不选;
故选:A。
8.用价层电子对互斥模型推测下列分子或离子的空间结构。
分子或离
VSEPR模型名称 空间结构名称
子
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
【答案】 直线形 直线形 四面体形 V形 四面体形
三角锥形 正四面体形 正四面体形 四面体形 三角锥形
【解析】二氯化铍分子中铍原子的价层电子对数为2,孤对电子对数为0,分子的VSEPR模型为直线形,空
间结构为直线形;二氯化硫分子中硫原子的价层电子对数为4,孤对电子对数为2,分子的VSEPR模型为四面体形,空间结构为V形;三氟化磷分子中磷原子的价层电子对数为4,孤对电子对数为1,分子的VSEPR
模型为四面体形,空间结构为三角锥形;铵根离子中氮原子的价层电子对数为4,孤对电子对数为0,离子
的VSEPR模型和空间结构都为正四面体形;亚硫酸根离子中硫原子的价层电子对数为4,孤对电子对数为
1,离子的VSEPR模型为正四面体形,空间结构为三角锥形,故答案为:直线形;直线形;四面体形;V形;
四面体形;三角锥形;正四面体形;正四面体形;四面体形;三角锥形。
题组B 能力提升练
1.下列分子构型为正四面体且键角为109°28′的是
①P ②NH ③CCl ④CH ⑤H S ⑥CO
4 3 4 4 2 2
A.③④ B.⑤⑥ C.①③④ D.②③④
【答案】A
【解析】①P 分子构型为正四面体、键角为60°;
4
②NH 分子中的氮原子sp3杂化,有一个杂化轨道容纳弧对电子对,所以构型为三角锥;
3
③CCl 分子中碳原子sp3杂化,没有弧对电子对,所以构型为正四面体且键角为109°28′;
4
④CH 分子中碳原子sp3杂化,没有弧对电子对,所以构型为正四面体且键角为109°28′;
4
⑤H S分子中硫原子sp3杂化,有两对弧对电子对,所以构型为V形;
2
⑥CO 分子中碳原子sp杂化,所以构型为直线形,
2
所以③④正确,答案选A。
2.下列分子的中心原子的价层电子对数是3的是
A. B. C. D.
【答案】B
【解析】水分子中氧原子、甲烷分子中碳原子和氨分子中氮原子的价层电子对数都为4,三氟化硼分子中
硼原子的价层电子对数为3,故选B。
17.下列离子的VSEPR模型与其空间结构一致的是
A. B. C. D.
【答案】B
【解析】A.亚硫酸根离子中硫原子的价层电子对数为4,孤对电子对数为1,离子的VSEPR模型为正四面
体形,空间结构为三角锥形,所以离子的空间结构模型与空间结构不一致,故A错误;
B.高氯酸根离子中氯原子的价层电子对数为4,孤对电子对数为0,离子的VSEPR模型和空间结构都为正
四面体形,所以离子的空间结构模型与空间结构一致,故B正确;C.亚硝酸根离子中氮原子的价层电子对数为3,孤对电子对数为1,离子的VSEPR模型为三角锥形,空间
结构为V形,所以离子的空间结构模型与空间结构不一致,故C错误;
D.氯酸根离子中氯原子的价层电子对数为4,孤对电子对数为1,离子的VSEPR模型为正四面体形,空间
结构为三角锥形,所以离子的空间结构模型与空间结构不一致,故D错误;
故选B。
3.下列分子或离子中,键角由大到小排列正确的是
① ②NH ③H O④BF ⑤CO
3 2 3 2
A.⑤④①②③ B.⑤①④②③
C.④①②⑤③ D.③②④①⑤
【答案】A
【解析】① 为正四面体,键角为109°28′;
②NH 分子中N原子价层电子对个数是4且含有一个孤电子对,其空间构型是三角锥形,键角约为107°;
3
③H O为V形,键角约为105°;
2
④BF 中心原子的价电子都用来形成共价键,所以价层电子对数为3,为平面三角形,键角为120°;
3
⑤CO 中心原子的价电子都用来形成共价键,所以价层电子对数为2,为直线形,键角为180°;
2
所以键角由大到小排列顺序是⑤④①②③;故选:A。
4.用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下
列判断正确的是
A.CS 是V形的分子
2
B.BF 键角为120°,H O键角大于120°
3 2
C.CH O、 都是平面三角形的分子
2
D.PCl 、PCl 都是三角锥形的分子
3 5
【答案】C
【解析】A.CS 的结构式为S=C=S,C原子价层电子对个数为2+ =2+0=2,无孤电子对,根据价层电
2
子对互斥理论判断CS 的空间构型为直线形,A错误;
2
B.BF 分子中中,B原子价层电子对个数为3+ =3+0=3,无孤对电子,根据价层电子对互斥理论判断
3
BF 的空间构型为平面正三角形,键角为120°;H O分子中,O原子价层电子对个数为2+ =2+2=4,且
3 2含2个孤电子对,所以O原子采用sp3杂化,H O的空间构型为V形,键角小于120°;B错误;
2
C.CH O分子中,C原子形成3个σ键,C原子采用sp2杂化,CH O的空间构型为平面三角形; 中,N
2 2
原子形成3个σ键,孤对电子数为 =0,N原子采用sp2杂化, 的空间构型为平面三角形;C正
确;
D.PCl 分子中,P原子价层电子对个数为3+ =3+1=4,含有一个孤电子对,根据价层电子对互斥理论
3
判断PCl 的空间构型三角锥形;PCl 分子中,P原子价层电子对个数为5+ =5+0=5,不含孤电子对,根
3 5
据价层电子对互斥理论判断PCl 的空间构型为三角双锥形;D错误;
5
故选C。
5.用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型或推测键角大小,下列判断正确的
是
A.SO 的分子构型类似CO 为直线形 B.SO 是三角锥形分子
2 2 3
C.BF 的键角为120° D.PCl 是平面三角形分子
3 3
【答案】C
【解析】A.SO 中中心原子S周围的价层电子对数为:2+ =3,其分子构型为V形,CO 中中心原
2 2
子S周围的价层电子对数为:2+ =2,即其空间构型为直线形,A错误;B.SO 中中心原子S周围的
3
价层电子对数为:3+ =3,空间构型是平面三角形,B错误;
C.BF 中中心原子B周围的价层电子对数为:3+ =3,空间构型是平面三角形,故其键角为120°,
3
C正确;
D.PCl 中中心原子P周围的价层电子对数为:3+ =4,则其空间构型是三角锥形,D错误;
3
故答案为:C。
6.用短线“−”表示共用电子对,用“∙∙”表示未成键孤电子对的式子叫路易斯结构式。R分子路易斯结构式可以表示为 ,下列叙述错误的是
A.R与BF 的空间结构相同 B.键角: 109°28′
3
C.R可以是PH 或AsH D.R分子的中心原子上的价层电子对数为4
3 3
【答案】A
【解析】A.R的空间结构为三角锥形,BF 中心原子价层电子对数为3+0=3,其空间结构是平面三角形,因
3
此其空间结构不相同,故A错误;
B. 都为三角锥形,键角小于109°28′,而N电负性大,吸引电子能力比P强,因此NH 共用电子
3
对之间的排斥力比PH 共用电子对之间的排斥力大,其键角大,所以键角: 109°28′,故B正确;
3
C. 可能为NH ,根据第VA族电子特点得到R可以是PH 或AsH ,故C正确;
3 3 3
D.R分子的中心原子上的价层电子对数为 ,故D正确。
综上所述,答案为A。
7.回答下列问题
(1)利用 模型推测分子或离子的空间结构。
:___________; (共价分子):___________。
(2)按要求写出由第二周期非金属元素的原子构成的中性分子的化学式。
平面三角形分子:___________,三角锥形分子:___________,正四面体形分子:___________。
【答案】(1) 正四面体形 平面三角形
(2)
【解析】中心原子价层电子对个数=σ键个数+孤电子对个数;σ键个数=配原子个数,孤电子对个数=,a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数;据
此确定VSEPR模型,实际空间构型要去掉孤电子对。
(1)利用 模型推测分子或离子的空间结构。
中的中心原子价层电子对数是4,没有孤电子对,空间结构为正四面体形。 分子中心原子价层
电子对数是3,没有孤电子对,空间结构是平面三角形。
(2)第二周期非金属元素有硼、碳、氮、氧、氟,按要求写出由第二周期非金属元素的原子构成的中性
分子的化学式:
平面三角形分子:BF (中心原子价层电子对数是3,没有孤电子对),三角锥形分子:NF (中心原子价层电子
3 3
对数是4,有1对孤电子对),正四面体形分子:CF (中心原子价层电子对数是4,没有孤电子对)。
4
8.根据所学知识填空:
(1)三原子分子常见的空间结构有__________形(如 )和__________形(如 )。
(2)四原子分子常见的空间结构有___________形和___________形,如甲醛( )分子呈___________
形,键角约为___________;氨分子呈___________形,键角为___________;需要注意的是白磷分子呈
___________形,键角为___________。
(3)五原子分子最常见的空间结构为___________形,如常见的 键角是___________。
【答案】(1) 直线
(2) 平面三角 三角锥 平面三角 三角锥
正四面体
(3) 四面体
【解析】中心原子价层电子对个数=σ键个数+孤电子对个数;σ键个数=配原子个数,孤电子对个数=
,a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数;据
此确定VSEPR模型,实际空间构型要去掉孤电子对。
(1)三原子分子常见的空间结构有V形或直线形。 分子中,中心原子孤电子对数 、价电
子对数2+0=2,则其空间构型为直线形,H O分子中,中心原子孤电子对数= 、价层电子对数
2=2+2=4,故空间构型为V形。
(2)四原子分子常见的空间结构有平面三角形和三角锥形,如甲醛 分子呈平面三角形,键角约为
120°;氨分子呈三角锥形,键角为107°;需要注意的是白磷分子呈正四面体形形,键角为60°。
(3)五原子分子最常见的空间结构为四面体形,如常见的 呈正四面体、键角是 。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育