文档内容
第 07 讲 杂化轨道理论简介
考点导航
知识精讲
知识点一:1.用杂化轨道理论解释甲烷分子的形成
在形成CH 分子时,碳原子的一个 轨道和三个轨道发生混杂,形成4个能量相等的 杂化轨道。4个
4
杂化轨道分别与4个H原子的1s轨道重叠形成4个C—H 键,所以4个C—H是等同的。
2.杂化轨道的形成及其特点
3.杂化轨道类型及其空间结构
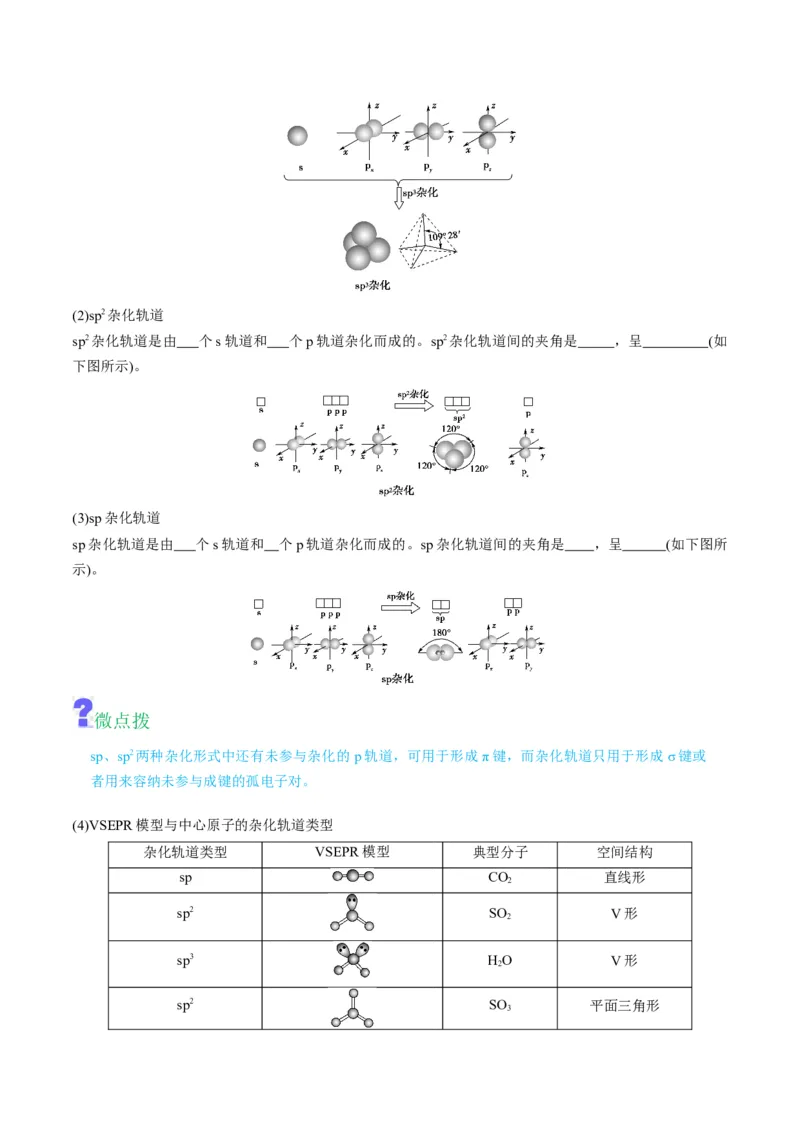
(1)sp3杂化轨道
sp3杂化轨道是由 个s轨道和 个p轨道杂化形成的。sp3杂化轨道间的夹角是109°28′,空间结构为
(如下图所示)。(2)sp2杂化轨道
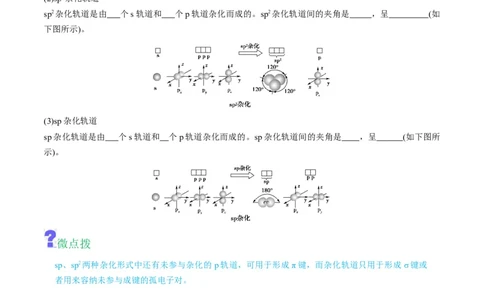
sp2杂化轨道是由 个s轨道和 个p轨道杂化而成的。sp2杂化轨道间的夹角是 ,呈 (如
下图所示)。
(3)sp杂化轨道
sp杂化轨道是由 个s轨道和 个p轨道杂化而成的。sp杂化轨道间的夹角是 ,呈 (如下图所
示)。
微点拨
sp、sp2两种杂化形式中还有未参与杂化的 p轨道,可用于形成π键,而杂化轨道只用于形成σ键或
者用来容纳未参与成键的孤电子对。
(4)VSEPR模型与中心原子的杂化轨道类型
杂化轨道类型 VSEPR模型 典型分子 空间结构
sp CO 直线形
2
sp2 SO V形
2
sp3 HO V形
2
sp2 SO 平面三角形
3sp3 NH 三角锥形
3
sp3 CH 正四面体形
4
【即学即练1】
1.下列关于杂化轨道的说法错误的是
A.所有原子轨道都参与杂化形成杂化轨道
B.同一原子中能量相近的原子轨道参与杂化
C.杂化轨道能量集中,有利于牢固成键
D.杂化轨道可用于形成 键
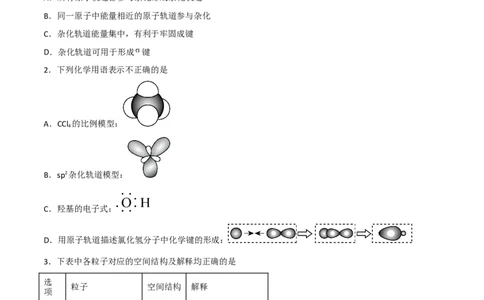
2.下列化学用语表示不正确的是
A.CCl 的比例模型:
4
B.sp2杂化轨道模型:
C.羟基的电子式:
D.用原子轨道描述氯化氢分子中化学键的形成:
3.下表中各粒子对应的空间结构及解释均正确的是
选
粒子 空间结构 解释
项
A 氨基负离子(NH ) 直线形 N原子采取sp杂化
B 二氧化硫(SO ) V形 S原子采取sp3杂化
2
C 碳酸根离子(CO ) 三角锥形 C原子采取sp3杂化
D 乙炔(C H ) 直线形 C原子采取sp杂化
2 2
A.A B.B C.C D.D4.列关于σ键和π键的说法中,不正确的是
A.σ键由原子轨道“头碰头”重叠形成
B.N 分子中的π键为p-p π键,π键不能绕键轴旋转
2
C.NH 分子中的σ键为s-s σ键
3
D.p轨道和p轨道之间既能形成π键,又能形成σ键
易错精析
1.写出碳原子的价电子排布式,这些价电子的能量是否相同?
【细剖精析】
2.碳原子的2s电子的能量与2p电子的能量是否有很大的差别?
【细剖精析】
3.碳原子的2s轨道电子能进入2p轨道吗?
【细剖精析】
能力拓展
1.杂化轨道理论要点
(1)只有能量相近的原子轨道才能杂化。
(2)杂化轨道数目和参与杂化的原子轨道数目相等,杂化轨道能量相同。
(3)杂化改变原有轨道的形状和伸展方向,使原子形成的共价键更牢固。
(4)杂化轨道为使相互间的排斥力最小,故在空间取最大夹角分布,不同的杂化轨道伸展方向不同。
(5)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对。
(6)未参与杂化的p轨道可用于形成π键。
2.中心原子杂化轨道类型的判断
(1)利用价层电子对互斥模型、杂化轨道理论判断分子构型的思路:
价层电子对――→杂化轨道数――→杂化类型――→杂化轨道构型。
(2)根据杂化轨道之间的夹角判断:若杂化轨道之间的夹角为 109°28′,则中心原子发生sp3杂化;若杂化
轨道之间的夹角为120°,则中心原子发生sp2杂化;若杂化轨道之间的夹角为180°,则中心原子发生sp杂
化。
(3)有机物中碳原子杂化类型的判断:饱和碳原子采取sp3杂化,连接双键的碳原子采取sp2杂化,连接三键
的碳原子采取sp杂化。
3.根据分子的空间结构判断中心原子杂化轨道类型的方法
1若分子的空间结构为正四面体形或三角锥形,则分子的中心原子采取sp3杂化。
2若分子的空间结构为平面三角形,则分子的中心原子采取sp2杂化。
3若分子的空间结构为直线形,则分子的中心原子采取sp杂化。4若分子的空间结构为V形,则分子的中心原子采取sp2杂化或sp3杂化。
分层提分
题组A 基础过关练
1.下列有关杂化轨道的说法不正确的是
A.四面体形、三角锥形、V形分子的结构可以用 杂化轨道解释
B. 、 、sp杂化轨道的夹角分别为109°28'、120°、180°
C.杂化轨道全部参加形成化学键
D.杂化前后的轨道数不变,但轨道的形状发生了改变
2.下列关于杂化轨道的叙述中,不正确的是
A.苯分子中所有碳原子均采取sp2杂化成键
B.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对
C.SO 和C H 分子中的中心原子S和C是通过sp2杂化轨道成键
2 2 4
D.中心原子通过sp3杂化轨道成键时,该分子一定为四面体结构
3.下列各项叙述中,正确的是
A. 、 的中心原子的杂化方式均为sp3
B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个
C.乙炔分子中σ键与π键的数目之比为3∶2
D.H O分子的VSEPR模型为V形
2
4.关于原子轨道的说法正确的是
A.sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道杂化形成的一组能量相同的新轨道
B.CH 分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道杂化而形成的
4
C.凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体
D.凡AB 型的共价化合物,其中心原子A均采用sp杂化轨道成键
2
5.s轨道与s轨道重叠形成的共价键可用符号表示为σs-s,p轨道与p轨道以“头碰头”方式重叠形成的共
价键可用符号表示为σp-p,请你指出下列分子中含有σs-sp2键的是
A.N B.C H C.C H D.HCl
2 2 4 2 2
6.下列粒子的中心原子的杂化轨道类型和粒子的空间结构不正确的是A. 中P原子为sp3杂化,分子空间结构为三角锥形
B. 中O原子为sp杂化,分子空间结构为直线形
C. 中N原子为sp3杂化,分子空间结构为正四面体形
D. 中S原子为sp2杂化,分子空间结构为V形
7.从微粒结构角度分析,下列说法错误的是
A.N 的空间结构为直线形,中心原子的杂化方式为sp
B.H CO 中C原子的杂化方式为sp2
2 3
C.S O (S O 相当于SO 中一个氧被硫替代)中心原子S的杂化方式为sp3
2 2
D.三氧化硫有单分子气体和三聚分子固体( )两种存在形式,两种形式中S原子
的杂化轨道类型相同
8.如图是甲烷分子中C原子 杂化轨道电子云图:
(1)甲烷分子中C-H键的键角为_______。
(2)乙烯和乙炔的电子式分别为_______、_______,请你比较乙烯和乙炔分子中“ ”和“ ”的键
长大小:_______。乙炔和乙烯一样都能和溴水发生加成反应并使溴水褪色,请你预测在同浓度同体积的
溴水中分别通入乙烯和乙炔时,_______(选填“乙烯”或“乙炔”)使溴水褪色的时间短;同温同压下,使等体积等浓度的溴水正好褪色,消耗的_______(选填“乙烯”或“乙炔”)少。
(3)苯分子中C原子以sp2杂化轨道成键,6个C原子中每个C原子的2s轨道和其中2个 轨道形成3个sp2
杂化轨道,其中1个sp2杂化轨道与1个H原子形成1个 键、另外2个sp2杂化轨道分别与另外2个C原子
的sp2杂化轨道形成2个 键而形成1个六元环,而每个C原子未参与杂化的另1个sp2轨道均垂直于这个
六元环所处的平面且相互之间“肩并肩”重叠形成1个“大 键”,如图:
请你猜想:
①苯分子中每个碳碳键的键长是否相等?_______;
②苯分子中碳碳键的键长与C-C键、C=C键、 键的键长相比,处于_______的键长之间。
题组B 能力提升练
1.近日科学家在Science杂志首次报道了具有半导体特性的18个原子纯碳环分子(如图所示)。下列说法正
确的是
A.该分子中碳杂化方式有sp、 两种
B.该分子可能要比苯更加稳定
C.该分子属于有机物
D.该分子具有半导体的功能,可以使类似的直碳链成为分子级电子元件
2.下列各组微粒,中心原子均采用sp2杂化方式的
A.NH ,PCl ,CO ,CO B.SO ,NO ,COCl ,BF
3 3 2 3 2 3
C.SO ,ClO ,PO ,BF D.BeCl ,NCl ,NO ,ClO
3 2 3
3.下列有关多原子分子中中心原子杂化的说法正确的是A.同一元素的原子在不同的分子中杂化方式相同
B.杂化轨道用于解释分子的立体构型,杂化轨道数目等于价层电子对数目
C.若分子中含有同一元素的多个原子,则在该分子中此原子的杂化方式完全相同
D.杂化轨道用于形成 键、容纳孤电子对和肩并肩形成 键
4.描述共价键的三个重要参数是键能、键长和键角。下列说法正确的是
A.在 分子中, 键的键长是C原子半径和S原子半径之和
B. 分子为正四面体结构,键角为
C.键能:
D. 型分子中的键角均为
【答案】B
【解析】A.键长是成键两原子的原子半径之和,二硫化碳分子中碳硫双键的键长比碳原子和硫原子的原
子半径之和要小,故A错误;
B.白磷分子的空间构型为正四面体形,键角为60°,故B正确;
C.查阅课本资料可知,氮氮三键的键能为946kJ/mol,而氮氮单键的键能为193kJ/mol,故氮气分子中含有
的氮氮三键的键能比氮氮单键的3倍要大,故C错误;
D.若AB 分子中A原子的价层电子对数为3,孤对电子对数为0,空间构型为平面三角形,分子中的键角
3
均为120°,故D错误;
故选B。
5. 的结构式为 ,下列有关 的说法错误的是
A.四个原子在一条直线上 B.S原子有两对孤电子对
C.S原子的杂化方式为 D. 分子中既有极性键又有非极性键
6.下列说法中正确的是
A.P 和CH 都是正四面体形分子,且键角都为109°28'
4 4
B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
C.s电子与s电子间形成的键一定是σ键,p电子与p电子间形成的键一定是π键
D.p轨道电子能量一定高于s轨道电子能量
7.下列说法正确的是A.Na+的电子排布式为1s22s22p63s1
B.SO 分子的立体构型是V形
2
C.HF的分子间作用力大于HCl,故HF比HCl更稳定
D.有机物CH =CH-CH 中杂化类型有sp3 和sp2,其中有一个π键,2个σ键
2 3
8. 原子在形成 分子时, 、 轨道和1个 轨道参与形成 杂化, 的空间构型为三角双锥
形(如下图所示)。下列关于 分子的说法不正确的是
A. 分子中价电子对数为5
B. 分子中没有形成 键
C. 分子中所有的 键角都相等
D. 分子中 原子也采用 杂化
9.H、C、N、O、S是重要的非金属元素,请按要求回答下列问题:
(1)C元素的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发
展水平的标志。有关该氢化物分子的说法正确的是_______。(填序号)。
a.该氢化物分子中C原子采用 杂化 b.6个原子不在同一平面上
c.只含有4个 键和1个 键 d.分子既含有极性键又含有非极性键
(2)相同条件下 与 分子在水中的溶解度较大的是_______(写分子式),理由是_______。 中的O
—C—O键角_______(填“>”“<”或“=”) 中的O—S—O键角。(3)已知(CN) 是直线形分子,且有对称性,则(CN) 分子的结构式为_______;其中 键与 键的个数比为
2 2
_______。
10.请依据相关化学知识与原理完成下列各题。
(1)下列一组微粒中键角按由大到小的顺序排列为___________(填编号)。
①HCN ② ③ ④ ⑤
(2) 、 、 、 中,Cl都是以 杂化轨道方式与O原子成键,将它们的立体构型填入表格
中:
离子
立体构型 ______ ______ ______ ______
(3)S单质的常见形式为 ,其环状结构如图所示,S原子采用的轨道杂化方式是___________杂化。
(4)肼 分子可视为 分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。 分
子中氮原子轨道的杂化类型是___________杂化, 中的六个原子___________(填“在”或“不在”)同
一个平面上。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育