文档内容
第 07 讲 活化能
知识导航
小杨老师 15521324728 侵权必究
课前引入
2 mol H 和1 mol O 混合于一个洁净的容器内,已知常温常压下,每个氢分子和氧分子自身或它们
2 2
之间每秒钟平均碰撞2.355×1010次,如果每一次碰撞都能够引发反应,试想会有什么样的现象?
如果每一次碰撞都能引发反应,整个容器中的氢气和氧气将在极短的时间内全部变成水。
杨sir化学,侵权必究
然而事实并非如此,为什么呢?
知识精讲
小杨老师 15521324728 侵权必究
一、基元反应与反应历程
1. 基元反应:大多数化学反应并不是经过简单碰撞就能完成的,而往往经过多个反应步骤才能实现。每一
步反应都称为基元反应。基元反应发生的先决条件是反应物的分子必须发生碰撞。
杨sir化学,侵权必究
2. 自由基:带有单电子的原子或原子团叫自由基,如 I·自由基、O·自由基。自由基反应活性很强,寿命
极短。
举个例子——碘化氢的分解
总反应:2HI ==== H + I
2 2 杨sir化学,侵权必究
实际上是经过下列两步基元反应完成的:2HI → H + 2I· 2I·→ I
2 2
3. 反应历程:与某化学反应有关的一组基元反应反映了该反应的反应历程,反应历程又称反应机理。说明
② 反应不同,反应历程也不相同。
②同一反应,在不同条件下,反应历程也可能不同。
杨sir化学,侵权必究
③反应历程的差别造成了化学反应速率的不同。
④对于由多个基元反应组成的化学反应,其反应的快慢由最慢的一步基元反应决定。
二、有效碰撞理论
1.有效碰撞的概念:能发生化学反应的碰撞称为有效碰撞。
2.有效碰撞必须满足的条件:
杨sir化学,侵权必究
(1)分子具有足够的_______;(即_____分子)
(2)分子在碰撞时具有合适的_______。
3.有效碰撞与反应速率的关系:有效碰撞的频率越高,则反应速率_______。
【答案】能量 活化 取向 越快
三、活化分子与活化能
1. 活化分子:具有足够能量、能够发生_________的分子。
【答案】有效碰撞
说明
对于某一化学反应来说,在一定条件下,反应物分子中活化分子的百分数是一定的。
2. 活化能:活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能。
E:正反应的活化能
1 杨sir化学,侵权必究
E:活化分子变成生成物分子放出的能量(逆反应的活化能)
2
E﹣E:反应热(△H)
1 2
催化剂的作用:降低反应的活化能。
杨sir化学,侵权必究四、有效碰撞理论对影响化学反应速率因素的解释
浓度 压强
反应物浓度增大 → 反应物中活化分子百分数____ 增大压强(压缩体积) → 反应物中活化分子百分
→ 单位体积内分子总数_____ → 活化分子总数 数______ → 单位体积内活化分子总数______ →
______ → 单位时间内有效碰撞次数______ → 反 单位时间内有效碰撞次数______ → 反应速率
应速率______;反之,反应速率_______。 ______;反之,反应速率_______。
温度 催化剂
升高温度 → 活化分子百分数______ → 单位体积 加入催化剂 → 活化分子百分数______ → 单位体
内分子总数______ → 活化分子总数______ → 单 积内活化分子总数______ → 单位时间内有效碰撞
位时间内有效碰撞次数______ → 反应速率 次数______ → 反应速率______;反之,反应速率
______;反之,反应速率_______。 _______。
【答案】不变;增多;增多;增多;增大;减慢
不变;增多;增多;增大;减慢
增大;不变;增多;增多;增大;减慢
增大;增多;增多;增大;减慢
及时小练
下列说法中正确的是__________
①活化分子间的碰撞不一定能发生化学反应
杨sir化学,侵权必究
②普通分子间的碰撞可能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④加入反应物,活化分子百分数不变,化学反应速率可能不变
⑤催化剂能增大活化分子百分数,从而成千成万倍地增大化学反应速率
⑥有气体参加的化学反应,若增大压强(缩小反应容器的体积),可增大活化分子的百分数,从而使反
应速率增大
【答案】①③④⑤
五、化学反应的速率常数和速率方程
1. 化学反应速率通常指一定时间内反应的平均速率。
杨sir化学,侵权必究
2. 在化学反应进程中,未达平衡时,瞬时反应速率一般是不断变化的。
3. 对于基元反应,化学反应速率通常与各反应物浓度的幂之积成正比。
4. 速率常数和速率方程
对于反应: aA + bB + … → 产物
速率方程为 v = k·cx(A)·cy(B)·… ,式中的 k 称为速率常数。对点训练
小杨老师 15521324728 侵权必究
题型一:有效碰撞理论
杨sir化学,侵权必究
【例1】下列说法正确的是
A.活化分子的每一次碰撞都能够发生化学反应
B.能够发生有效碰撞的分子叫做活化分子
C.反应物用量增加后,有效碰撞次数增多,反应速率增大
D.催化剂能提高活化分子的活化能,从而加快反应速率
【答案】B
【详解】
A.发生有效碰撞才反应,所以活化分子的碰撞不一定反应,还与取向有关,故A错误;
B.分子发生有效碰撞时发生化学反应,此时的分子为活化分子,故B正确;
C.反应物为纯固体或液体,用量增加,反应速率不变,反应物用量增加不一定反应速率加快,故C错误;
D.加入催化剂可降低活化能,提高活化分子的百分数,反应速率增大,故D错误;
故选B。
【变1-1】下列说法正确的是
A.活化能接近于零的反应,当反应物相互接触时,反应瞬间完成
杨sir化学,侵权必究
B.温度和压强都是通过增大活化分子百分数来加快化学反应速率
C.人们把能够发生有效碰撞的分子叫做活化分子,把活化分子具有的能量叫活化能
D.活化能的大小不仅意味着一般分子成为活化分子的难易,也会对化学反应前后的能量变化产生影响
【答案】A
【详解】
A.活化能接近于零的反应,由于不需要活化能的推动,所以当反应物相互接触时反应瞬间完成,A正确;
B.压强不能改变活化分子百分数,增大压强是通过增大单位体积内活化分子数来加快化学反应速率的,B
错误;
C.我们把能够发生化学反应的碰撞叫做有效碰撞,能够发生有效碰撞的分子叫做活化分子,活化分子具
有的平均能量与反应物分子具有的平均能量之差叫做反应的活化能,C错误;
D.活化能越大,一般分子成为活化分子越难,活化能越小,一般分子成为活化分子越易,活化能的大小
意味着一般分子成为活化分子的难易程度,化学反应前后的能量变化取决于反应物总能量与生成物总能量
的相对大小,与活化能无关,D错误;答案选A。
【变1-2】在有气体参加的反应中,能使反应物中活化分子总数和活化分子百分数都增大的措施有
①增大反应物浓度 ②增大压强 ③升高温度 ④加入催化剂
A.①② B.②④ C.①③ D.③④
【答案】D
【详解】
①增大反应物浓度,单位体积内活化分子数目增加,活化分子百分数不变;
③增大压强,单位体积内活化分子数目增加,活化分子百分数不变;
③升高温度,分子吸收能量,原来不是活化分子变为活化分子,活化分子数目增加,活化分子百分数增大;
④加入催化剂,降低反应所需活化能,原来不是活化分子变为活化分子,活化分子数目增加,活化分子百
分数增大;因此③④正确;
综上所述,答案为D。
【变1-3】对于水煤气转换反应 ,下列条件的改变,能增大活化分
子百分数的是
A.降低温度 B.增大反应物浓度
C.恒容条件下,充入稀有气体 D.使用催化剂
杨sir化学,侵权必究
【答案】D
【分析】
根据活化分子百分数= ,升高温度和使用催化剂能提高活化分子百分数,因为升高温度,一些
普通分子的能量升高,变为活化分子,活化分子数增多,使用催化剂能降低反应的活化能,从而使一些普
通分子相对的成为活化分子,提高活化分子数。
【详解】
A.降低温度,分子能量降低,活化分子数减少,因此活化分子百分数减小,故A不选;
B.增大反应物浓度,单位体积内活化分子数增多,但活化分子百分数不变,故B不选;
C.恒容条件下,充入稀有气体,反应物浓度不变,因此活化分子百分数不变,故C不选;
D.使用催化剂能降低反应的活化能,活化分子数增多,进而提高活化分子百分数,故D选;
故选D。
【变1-4】下列关于化学反应速率的说法正确的是
①恒温时,增大压强,化学反应速率一定加快②其他条件不变,温度越高,化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应
速率增大
⑥增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多
⑦催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率
A.②⑥ B.②④ C.②③⑤⑦ D.①②④⑤
【答案】B
【详解】
①恒温时,增大压强,如没有气体参加反应,化学反应速率不加快,故错误;
②其他条件不变,温度越高,增大活化分子百分数,化学反应速率越快,故正确;
③使用催化剂不能改变反应热,故错误;
④升高温度能增大了反应物分子中活化分子的百分数,使化学反应速率增大,故正确;
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),活化分子百分数不变,增加的是单位
体积内活化分子数,故错误;
⑥增大反应物浓度,活化分子的百分数不变,增加的是单位体积内活化分子数,故错误;
⑦催化剂通过参与反应,降低活化能,增大活化分子的百分数,从而增大反应速率,故错误。
②④符合题意,故答案选B。
题型二:基元反应与反应历程
杨sir化学,侵权必究
【例2】对于反应 ,科学家根据光谱研究提出如下反应历程:
第一步 :快反应;
第二步: 慢反应;
第三步: 快反应。
上述反应中可近似认为第二步反应不影响第一步反应的平衡,下列叙述正确的是
A.该反应的速率由第二步反应决定
B.反应的中间产物有NO、NO和H
2 2 2 2C.第三步反应中NO与H 的每一次碰撞都是有效碰撞
2 2
D.若第一步反应的 ,则升高温度,正反应速率减小,逆反应速率增大
【答案】A
【详解】
A.总反应速率由慢反应决定,所以该反应的速率由第二步反应决定,故A正确;
B.NO、H 是反应物,反应的中间产物有NO、NO,故B错误;
2 2 2 2
C.只有少数分子的碰撞能发生化学反应,能引发化学反应的碰撞称之为有效碰撞,第三步反应中NO与
2
H 的碰撞不都是有效碰撞,故C错误;
2
D.升高温度,正逆反应速率均增大,故D错误;
选A。
【变2】对于反应2NO(g)+2H(g)→N (g)+2HO(g),科学家根据光谱学研究提出如下反应历程:
2 2 2
第一步:2NO NO 快速平衡
2 2
第二步:N
2
O 2⇌+H
2
→N
2
O+H
2
O慢反应
第三步:NO+H→N+HO快反应
2 2 2 2 杨sir化学,侵权必究
其中可近似认为第二步反应不影响第一步的平衡。下列叙述正确的是
A.若第一步反应△H<0,则升高温度,v 减小,v 增大
正 逆
B.第二步反应的活化能大于第三步的活化能
C.第三步反应中NO与H 的每一次碰撞都是有效碰撞
2 2
D.反应的中间产物只有NO
2 2
【答案】B
【详解】
A.不管△H<0,还是△H>0,升高温度,v 和v 均增大,A选项错误;
正 逆
B.第二步反应为慢反应,第三步反应为快反应,则第二步反应的活化能大于第三步的活化能,B选项正
确;
C.根据有效碰撞理论可知,任何化学反应的发生都需要有效碰撞,但每一次碰撞不一定是有效碰撞,C
选项错误;
D.反应的中间产物有NO 和NO,D选项错误;
2 2 2
答案选B。
【点睛】
化学反应速率与温度有关,温度升高,活化分子数增多,无论是正反应速率还是逆反应速率都会加快,与
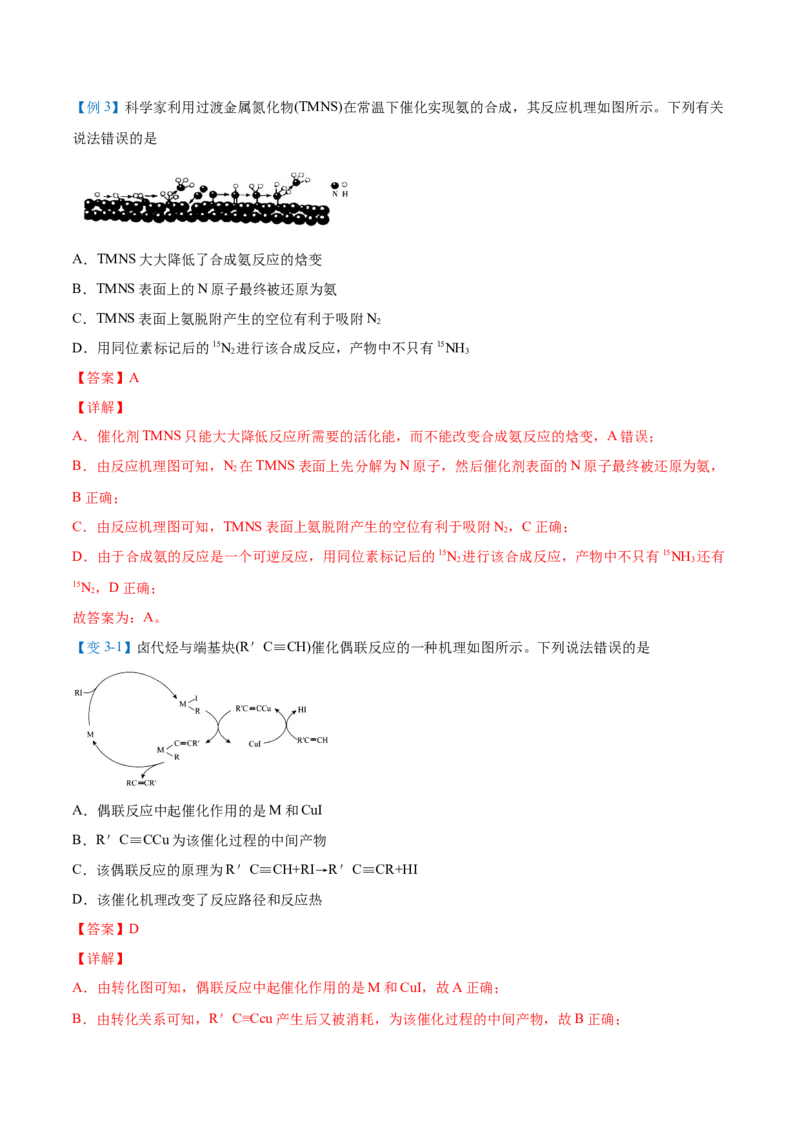
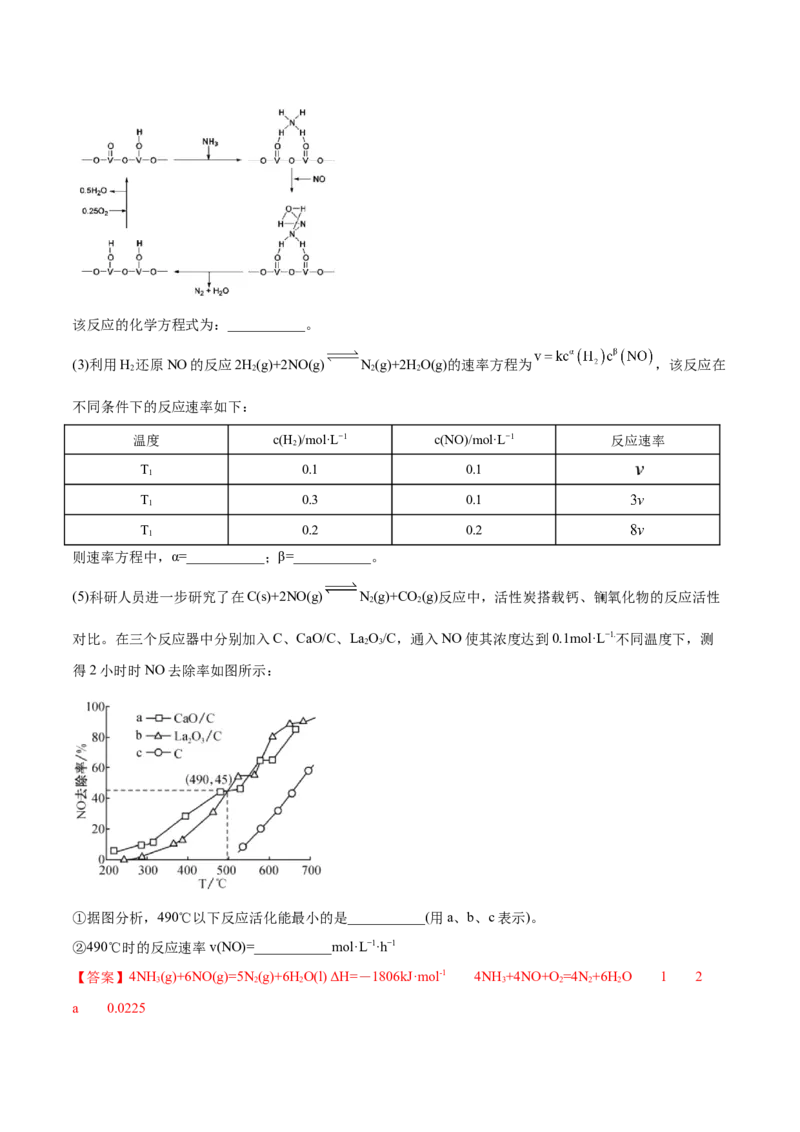
平衡移动没有必然联系。【例3】科学家利用过渡金属氮化物(TMNS)在常温下催化实现氨的合成,其反应机理如图所示。下列有关
说法错误的是
A.TMNS大大降低了合成氨反应的焓变
B.TMNS表面上的N原子最终被还原为氨
C.TMNS表面上氨脱附产生的空位有利于吸附N
2
D.用同位素标记后的15N 进行该合成反应,产物中不只有15NH
2 3
【答案】A
【详解】
A.催化剂TMNS只能大大降低反应所需要的活化能,而不能改变合成氨反应的焓变,A错误;
B.由反应机理图可知,N 在TMNS表面上先分解为N原子,然后催化剂表面的N原子最终被还原为氨,
2
B正确;
C.由反应机理图可知,TMNS表面上氨脱附产生的空位有利于吸附N,C正确;
2
D.由于合成氨的反应是一个可逆反应,用同位素标记后的15N 进行该合成反应,产物中不只有15NH 还有
2 3
15N,D正确;
2
故答案为:A。
【变3-1】卤代烃与端基炔(R'C≡CH)催化偶联反应的一种机理如图所示。下列说法错误的是
A.偶联反应中起催化作用的是M和CuI
B.R'C≡CCu为该催化过程的中间产物
杨sir化学,侵权必究
C.该偶联反应的原理为R'C≡CH+RI→R'C≡CR+HI
D.该催化机理改变了反应路径和反应热
【答案】D
【详解】
A.由转化图可知,偶联反应中起催化作用的是M和CuI,故A正确;
B.由转化关系可知,R'C≡Ccu产生后又被消耗,为该催化过程的中间产物,故B正确;C.由流程可知,转化图中右侧存在反应R'C≡CH+CuI→R'C≡CCu+HI,故C正确;
D.催化剂改变反应路径,不改变反应热,故D错误。
故选:D。
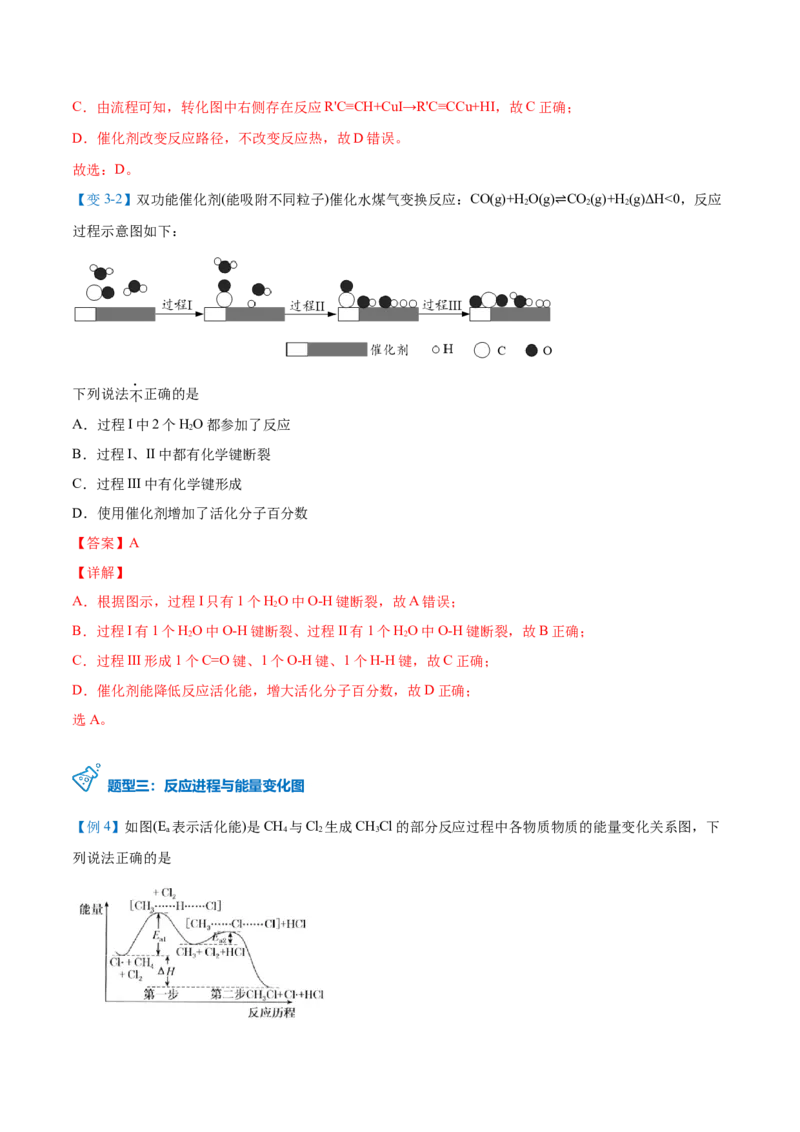
【变3-2】双功能催化剂(能吸附不同粒子)催化水煤气变换反应:CO(g)+HO(g) CO(g)+H(g)ΔH<0,反应
2 2 2
过程示意图如下: ⇌
下列说法不正确的是
A.过程I中2个HO都参加了反应
2
B.过程I、II中都有化学键断裂
C.过程III中有化学键形成
D.使用催化剂增加了活化分子百分数
【答案】A
【详解】
A.根据图示,过程I只有1个HO中O-H键断裂,故A错误;
2
B.过程I有1个HO中O-H键断裂、过程II有1个HO中O-H键断裂,故B正确;
2 2
C.过程III形成1个C=O键、1个O-H键、1个H-H键,故C正确;
D.催化剂能降低反应活化能,增大活化分子百分数,故D正确;
选A。
题型三:反应进程与能量变化图
杨sir化学,侵权必究
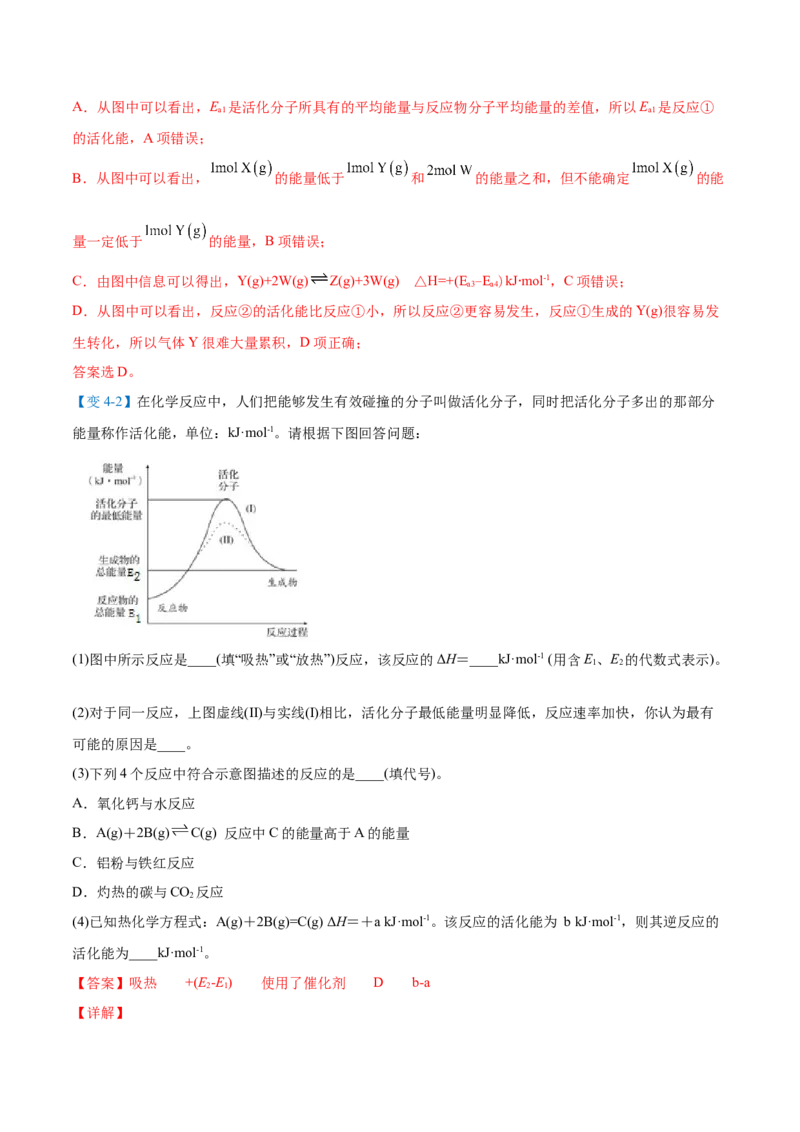
【例4】如图(E 表示活化能)是CH 与Cl 生成CHCl的部分反应过程中各物质物质的能量变化关系图,下
a 4 2 3
列说法正确的是A.Cl·可由Cl 在高温条件下生成,是CH 与Cl 反应的催化剂
2 4 2
B.升高温度,活化分子的百分数不变,但反应速率加快
C.增大Cl 的浓度,可提高反应速率,但不影响 H的大小
2
D.第一步反应的速率大于第二步反应 △
【答案】C
【分析】
CH 与Cl 生成CHCl的反应方程式为:CH+Cl CHCl+HCl。
4 2 3 4 2 3
【详解】
A.Cl·由Cl 在光照条件下生成,是CH 与Cl 反应的“中间体”,而不是反应的催化剂,选项A错误;
2 4 2
B.E 、E 分别为第一步反应、第二步反应所需活化能,升高温度,反应所需活化能不变,即E 、E 不
a1 a2 a1 a2
变,但活化分子的百分数增多,反应速率加快,选项B错误;
C.Cl 是该反应的反应物,增大反应物的浓度,反应速率增大,而反应的 H和反应的途径无关,只与反
2
应的始态和终态有关,即增大氯气的浓度不影响 H的大小,选项C正确;△
D.第一步反应所需活化能E
a1
大于第二步反应所△需活化能E
a2
,第一步反应单位体积内活化分子百分数低
于第二步反应,故第二步反应速率更大,选项D错误。
答案选C。
【变4-1】已知X转化为Z和W分步进行:① ,② ,其反应
过程能量变化如图所示,下列说法正确的是
A. 是反应①的活化能
杨sir化学,侵权必究
B. 的能量一定低于 的能量
C.
D.反应②更容易发生,气体Y很难大量存在
【答案】D
【详解】A.从图中可以看出,E 是活化分子所具有的平均能量与反应物分子平均能量的差值,所以E 是反应①
a1 a1
的活化能,A项错误;
B.从图中可以看出, 的能量低于 和 的能量之和,但不能确定 的能
量一定低于 的能量,B项错误;
C.由图中信息可以得出,Y(g)+2W(g) Z(g)+3W(g) △H=+(E -E )kJmol-1,C项错误;
a3 a4
D.从图中可以看出,反应②的活化能比反应①小,所以反应②更容易发∙生,反应①生成的Y(g)很容易发
生转化,所以气体Y很难大量累积,D项正确;
答案选D。
【变4-2】在化学反应中,人们把能够发生有效碰撞的分子叫做活化分子,同时把活化分子多出的那部分
能量称作活化能,单位:kJ·mol-1。请根据下图回答问题:
(1)图中所示反应是____(填“吸热”或“放热”)反应,该反应的ΔH=____kJ·mol-1 (用含E、E 的代数式表示)。
1 2
杨sir化学,侵权必究
(2)对于同一反应,上图虚线(Ⅱ)与实线(Ⅰ)相比,活化分子最低能量明显降低,反应速率加快,你认为最有
可能的原因是____。
(3)下列4个反应中符合示意图描述的反应的是____(填代号)。
A.氧化钙与水反应
B.A(g)+2B(g) C(g) 反应中C的能量高于A的能量
C.铝粉与铁红反应
D.灼热的碳与CO 反应
2 杨sir化学,侵权必究
(4)已知热化学方程式:A(g)+2B(g)=C(g) ΔH=+a kJ·mol-1。该反应的活化能为 b kJ·mol-1,则其逆反应的
活化能为____kJ·mol-1。
【答案】吸热 +(E-E) 使用了催化剂 D b-a
2 1
【详解】(1)图示反应的生成物能量大于反应物能量,所以为吸热反应;焓变=反应物能量-生成物能量=+(E-E)
2 1
kJ·mol-1;
(2)催化剂可以降低反应的活化能从而使反应速率加快,所以最可能的原因是使用了催化剂;
(3)A.氧化钙与水的反应为放热反应,故A不符合题意;
B.虽然C的能量高于A,但B的能量不确定,所以无法确定该反应吸热还是放热,故B不符合题意;
C.铝粉与铁红反应为铝热反应,为放热反应,故C不符合题意;
D.灼热的碳与CO 反应为吸热反应,故D符合题意;
2
综上所述答案为D;
(4)焓变=正反应活化能-逆反应活化能,所以逆反应活化能为(b-a) kJ·mol-1。
【例5】金属插入CH 的C-H键形成高氧化态过渡金属化合物的反应频繁出现在光分解作用、金属有机化
4
学等领域,如图是CH 与Zr形成过渡金属化合物的过程。下列说法不正确的是
4
A.整个反应快慢,由 CH— Zr···H →状态2反应决定
2 2
B.CH—Zr···H→CH —Zr···H ΔH=+8.32 kJ • mol-1
3 2 2
C.在中间产物中 CH—Zr···H状态最稳定
3
D.Zr +CH→CH—Zr···H 活化能为201. 84 kJ • mol-1
4 3
【答案】D
【详解】
A.反应速率取决于反应活化能的大小,活化能越大的那步反应的反应速率越小,整个反应的反应速率由
其决定,由图可知,CH﹣Zr···H→状态2反应的活化能最大,反应速率最慢,所以整个反应快慢,由CH
2 2 2
﹣Zr···H→状态2反应决定,故A正确;
2
B.由图可知,CH—Zr···H→CH —Zr···H 的 H=-106.15kJ/mol﹣(-114.47)kJ/mol═+8.32kJ/mol,故B正
3 2 2
确; △
C.由图可知,CH﹣Zr···H状态时具有的内能最低,所以CH﹣Zr…H状态最稳定,故C正确;
3 3D.由图可知,Zr+CH →CH─Zr···H 活化能为95.69kJ/mol,故D错误;
4 3
故选:D。
【变5】甲醇与SO 在有水条件下生成硫酸氢甲酯的反应部分历程如图所示。CHOH(g)+SO (g)
3 3 3
CHOSO H(g),其中粒子间的静电作用力用“…”表示。下列说法错误的是
3 3
A.水合CHOH分子比水合SO 分子更稳定
3 3 杨sir化学,侵权必究
B.反应历程中最大能垒(活化能)为6.62eV
C.d到f转化的实质为质子转移
D.在反应过程中,水起催化作用
【答案】A
【详解】
A.据图可知d为水合CHOH分子,c为水合SO 分子,c的能量更低,所以水合SO 分子更稳定,A错误;
3 3 3
B.据图可知反应历程中最大能垒(活化能)为3.66eV-(-2.96eV)=6.62eV,B正确;
C.据图可知d到f的过程中甲醇中的氢原子转移到水分子中,水分子中的氢原子转移到CHOSO H分子中,
3 3
实质为质子转移,C正确;
D.反应前后水未发生变化,形成的水合分子降低了能垒,为该反应的催化剂,D正确;
综上所述答案为A。
题型四:速率方程与速率常数
杨sir化学,侵权必究
【例6】已知 的速率方程 [ 为速率常数,只受温度影响]该反
应可认为经过以下反应历程:
第一步: 快速平衡
第二步: 快速平衡第三步: 慢反应
杨sir化学,侵权必究
下列说法正确的是
A.第一步反应和第二步反应的活化能较高
B. 、 分别增大相同的倍数,对总反应速率的影响程度相同
C.该总反应的速率主要取决于第三步反应
D.压缩容器体积,会使体系中活化分子百分数增加
【答案】C
【详解】
A.第一步反应和第二步反应反应速率较大,则反应的活化能越小,故A错误;
B.速率方程 ,可知若c(CO)、c((Cl )分别增大相同的倍数,对总反应速率的影响程度
2
不同,故B错误;
C.第三步反应较慢,则总反应的速率主要取决于第三步反应,故C正确;
D.压缩容器体积,增大气体的压强,使单位体积内活化分子数增加,但不能使活化分子百分数增加,故
D错误。
故选:C。
【变6】已知Cl(g)+CO(g)⇌COCl (g)的速率方程 [k为速率常数,只受温度影响],该反
2 2
应可认为经过以下反应历程:
第一步:Cl⇌2Cl 快速平衡
2
第二步:Cl+CO⇌COCl 快速平衡
第三步:COCl+Cl →COCl +Cl 慢反应
2 2
下列说法正确的是
A.第一步反应和第二步反应的活化能较高
B.c(CO)、c(Cl )分别增大相同的倍数,对总反应速率的影响程度相同
2
C.该总反应的速率主要取决于第三步反应
D.第三步反应的有效碰撞频率较大
杨sir化学,侵权必究
【答案】C
【详解】
A.第一步、第二步快速平衡,说明第一步反应和第二步反应的活化能较低,故A错误;B.c(CO)、c(Cl )分别增大相同的倍数,根据速率方程 ,得出它们对总反应速率的影响
2
程度不相同,c(Cl )影响程度大,故B错误;
2
C.第三步是慢反应,因此该总反应的速率主要取决于第三步反应,故C正确;
D.第三步是慢反应,说明第三步反应的有效碰撞频率较小,故D错误。
综上所述,答案为C。
【例7】某学习小组为了探究 反应速率(v)与反应物浓度的关系,在20℃进行
实验,所得的数据如表:
实验编号
① ② ③ ④ ⑤
相关数据
0.008 0.008 0.004 0.008 0.004
0.001 0.001 0.001 0.002 0.002
0.10 0.20 0.20 0.10 0.40
4.8×10−8 4.8×10−8
下列结论不正确的是
A.若温度升高到40℃,则反应速率增大
B.实验①④,探究的是 对反应速率的影响
C.若该反应速率方程为 (k为常数),则p=1
D.实验⑤中,
【答案】C
【详解】
A.由于温度升高,反应速率增大,故A正确;
B.实验①④中只有 不同,探究的是 对反应速率的影响,故B正确;
C.根据表中数据可判断②、③中,氢离子浓度增大1倍,速率增大到原来的4倍,故p=2,故C错误;
D.根据①②中数据可知n=1,同理根据①④中数据可判断m=1,③、⑤中氢离子浓度相同, 和
浓度关系是⑤中的二者浓度都比③中的增大一倍,速率增大4倍,因此 mol•L-1•s-1,故D正确;
故选C。
【变7-1】一定条件下,反应 的速率方程为 ,某温度下,
该反应在不同浓度下的反应速率如下:
反应速率
0.1 0.1 2 v
0.1 0.4 2 8v
0.2 0.4 2 16v
0.4 0.1 4 2v
0.2 0.1 x 4v
根据表中的测定结果,下列结论错误的是
A.表中x的值为1
杨sir化学,侵权必究
B.α、β、γ的值分别为1、2、-1
C.反应体系的三种物质中,Br (g)的浓度对反应速率影响最大
2
D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低
【答案】B
【分析】
v=kcα(H )cβ(Br)cγ(HBr),对比第一组和第二组数据知, =8,所以β= ,对比第二组和第三组数据知,
2 2
,所以α=1;对比第一组、第四组数据,将β= ,α=1带入得 =2,解得γ=-1。
【详解】
A.对比第四、第五组数据得 = ,解得x=1,A正确;
B.根据分析可知α、β、γ的值分别为1、 、-1,B错误;
C.根据分析可知c(Br)的指数的绝对值最大,对反应速率影响最大,C正确;
D.由于γ=-1,增大HBr(g)浓度,cγ(HBr)c减小,在反应体系中保持其他物质浓度不变,会使反应速率降
低,D正确;
综上所述答案为B。【变7-2】CO是一种常用的还原剂。一定条件下,反应 的速率方程为
(k为速率常数,只与温度、催化剂有关,与浓度无关)。某温度下,该反应在不同浓度
下反应速率如下表所示:
反应速率
① 0.10 0.10 v
② 0.20 0.10
③ 0.20 0.20
(1)根据表中测定结果,下列推断正确的是_______(填字母)。
杨sir化学,侵权必究
A.a=1、b=2 B.a=1、b=1 C.a=2、b=2 D.a=2、b=1
(2)改变下列一个条件,反应速率增大的是_______(填字母)。
A.降温 B.缩小体积 C.加入催化剂 D.减压
【答案】B BC
【详解】
(1)速率方程为 ,根据①②中数据,v: =k×(0.10)a×(0.10)b:k×(0.20)a×(0.10)b,解之得
a=1;根据②③中数据, : = k×(0.20)a×(0.10)b:k×(0.20)a×(0.20)b,解之得b=1;故选B。
(2)反应 ,缩小体积,增大浓度,反应速率加快;加入催化剂,反应速
率增大,而降温(活化分子数百分数减小)和减压(相等于减小物质的浓度)均使反应速率减慢,故选
BC。
【例8】汽车尾气中的CO、NO 是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化
x
物﹐防止空气污染。回答下列问题:
(1)已知:N(g)+O(g)=2NO(g) ΔH=+180kJ·mol−1
2 2
4NH (g)+5O(g)=4NO(g)+6H O(l) ΔH=-906kJ·mol−1
3 2 2
请写出NH 将NO转化成无毒物质的热化学方程式:___________。
3
(2)工业上一种除去NO的一种反应机理如图所示:该反应的化学方程式为:___________。
杨sir化学,侵权必究
(3)利用H 还原NO的反应2H(g)+2NO(g) N(g)+2HO(g)的速率方程为 ,该反应在
2 2 2 2
不同条件下的反应速率如下:
温度 c(H)/mol·L−1 c(NO)/mol·L−1 反应速率
2
T 0.1 0.1
1
T 0.3 0.1
1
T 0.2 0.2
1
则速率方程中,α=___________;β=___________。
(5)科研人员进一步研究了在C(s)+2NO(g) N(g)+CO (g)反应中,活性炭搭载钙、镧氧化物的反应活性
2 2
对比。在三个反应器中分别加入C、CaO/C、LaO/C,通入NO使其浓度达到0.1mol·L−1.不同温度下,测
2 3
得2小时时NO去除率如图所示:
①据图分析,490℃以下反应活化能最小的是___________(用a、b、c表示)。
②490℃时的反应速率v(NO)=___________mol·L−1·h−1
【答案】4NH (g)+6NO(g)=5N (g)+6HO(l) ΔH=-1806kJ·mol-1 4NH +4NO+O=4N +6H O 1 2
3 2 2 3 2 2 2
a 0.0225【详解】
(1)①N(g)+O(g)=2NO(g) ΔH=+180kJ·mol−1
2 2 1
②4NH (g)+5O(g)=4NO(g)+6H O(l) ΔH =-906kJ·mol−1
3 2 2 2
根据盖斯定律有②-5×①得4NH (g)+6NO(g)=6H O(l)+5N(g) ΔH=ΔH -5ΔH =-906kJ·mol−1-5×(+180kJ·mol−1)=
3 2 2 2 1
-1806kJ·mol-1,即4NH (g)+6NO(g)=5N (g)+6HO(l) ΔH=-1806kJ·mol-1;
3 2 2
(2)由图可知反应物为NO、O 和NH ,生成物为N 和HO,则该反应的化学方程式为
2 3 2 2
4NH +4NO+O=4N +6H O;
3 2 2 2
(3)由表中数据可得:① ,② ③ ,联立三式可解得α=1;
β=2;
(5)①活化能越小,反应越容易发生,反应速率越快,相同条件下NO去除率越大,因此490℃以下反应活
化能最小的是a;
②490℃时,2h时NO的去除率为45%,则NO浓度减小量为0.1mol/L×45%=0.045mol/L,反应速率
v(NO)=0.045mol/L÷2h=0.0225mol·L−1·h−1;
提分特训
小杨老师 15521324728 侵权必究
【题1】下列说法中错误的是
A.对有气体参加的化学反应,减小容器体积、体系压强增大,可使单位体积内活化分子数增加,因而反
应速率增大
B.活化分子之间发生的碰撞一定为有效碰撞
杨sir化学,侵权必究
C.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而增大化学反应的速率
【答案】B
【详解】
A.有气体参加的反应,减小容器体积,可增大单位体积内的活化分子数,分子的碰撞次数增多,反应速
率加快,A正确;
B.活化分子发生碰撞时,只有一部分碰撞为有效碰撞,能够发生化学反应,B错误;
C.升高温度,体系的能量增大,活化分子的数目增多,活化分子的百分数增大,反应速率增大,C正确;
D.加入适宜的催化剂,可降低反应的活化能,从而增大活化分子的百分数,加快化学反应的速率,D正
确;故选B。
【题2】下列关于可逆反应2SO (g) + O(g) 2SO (g) △H< 0 的说法中正确的是
2 2 3
A.活化分子之间的碰撞一定是有效碰撞
杨sir化学,侵权必究
B.增大反应物的浓度,可使单位体积内活化分子百分数增多,反应速率加快
C.升高反应体系温度,可使单位体积内活化分子增多,反应速率加快
D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加,反应速率加快
【答案】D
【详解】
A.活化分子之间的碰撞不一定均是有效碰撞,故A错误;
B.增大反应物的浓度,可使单位体积内活化分子数增多,增快速率,故B错误;
C.升高反应体系温度,活化分子百分数增加,反应速率增大,故C错误;
D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加,反应速率加快,故D正确;
故选D。
【题3】NO催化O 分解的反应机理如下:
3
第一步:
第二步:
第三步:
总反应:
其能量与反应历程的关系如图所示。下列叙述正确的是
A.三步反应的 均小于0
B.第一步反应的速率最快反应历程
C.第二步反应断裂的化学键只有共价键
杨sir化学,侵权必究D.NO改变了总反应的反应历程和焓变
【答案】C
【详解】
A.由反应历程图可知,第一步和第二步反应均为吸热反应, 大于0,A错误;
B.由反应历程图可知,第一步反应的活化能最大,第一步为速率最慢的反应历程,B错误;
C.第三步反应为: ,反应断裂的化学键只有共价键,C正确;
D.NO为该反应的催化剂,只能改变总反应的反应历程,不能改变总反应的焓变,D错误;
答案为:C。
【题4】在催化剂作用下,有机物DMO(CH OOC-COOCH )与H 反应能够转化为EG,其反应过程如图所
3 3 2
示。
下列说法正确的是
A.Cu纳米颗粒在反应过程中不参与化学反应
B.Cu纳米颗粒在反应过程中能够降低反应的活化能
C.DMO在反应过程中,吸收能量断裂C-O、C-H键
D.温度越高,Cu纳米颗粒的催化效果越好
【答案】B
【分析】
由图可知,DMO和H 反应获得EG的反应机理为:催化剂Cu纳米颗粒将H 解离成H原子,H原子与
2 2
DMO反应生成EG和CHOH。
3
【详解】
A.由图示可知,Cu纳米颗粒吸附H 后形成H—Cu—H过渡态,然后转化为Cu和H原子,故Cu参与了
2
化学反应,A错误;
B.Cu纳米颗粒反应前后不变,故作催化剂,催化剂能降低反应的活化能,B正确;
C.由图示知,CHOOC-COOCH 反应后转化为CHOH和HOCH -CHOH,故DMO中C—O与C=O发生
3 3 3 2 2
断裂,C—H未断裂,C错误;D.催化剂活性受温度影响,温度过高过低都会使催化剂活性下降,D错误;
故答案选B。
【题5】利用 和 合成甲醇: ,反应的历程如下图所示。下
杨sir化学,侵权必究
列说法正确的是
A.合成甲醇反应为放热反应
B. 活化能为
C.副产物有 、 ,其中 相对较多
D.合成甲醇反应历程中速率较慢的是
【答案】D
【详解】
A.由图可知,生成物总能量高于反应物总能量,该反应为吸热反应,A项错误;
B. 活化能为 ,B项错误;
C.由图可知,副产物有 、 ,由于活化能越大,反应速率越慢,故 相对较多,C项错误;
D.活化能越大,反应速率越慢,故合成甲醇反应历程中速率较慢的是 ,D项正
确;
答案选D。
【题6】亚硝酰氯在有机合成中有重要应用。 的反应历程如图所示。下列说法
错误的是A.催化剂能提高反应物的相对能量
杨sir化学,侵权必究
B.相对曲线Ⅱ,曲线Ⅰ表示加入催化剂
C.曲线Ⅱ的正反应活化能为
D. ,
【答案】A
【详解】
A.催化剂降低“过渡态”物质的相对能量,使活化能降低,A错误;
B.曲线I表示加入催化剂,B正确;
C.正反应活化能等于过渡态相对能量与反应物相对能量之差, ,
C正确;
D.反应热等于产物总能量与反应物总能量之差等于 ,D正确;
故答案为:A。
【题7】某反应 的速率方程为 ,其半衰期(当剩余反应物恰好
是起始的一半时所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示:
0.25 0.050 1.4
0.50 0.050 2.8
1.00 0.050 5.6
0.50 0.100 2.8
下列说法正确的是
A.速率方程中的 、
B.该反应的速率常数
杨sir化学,侵权必究C.增大反应物浓度,k增大导致反应的瞬时速率加快
D.在过量的B存在时,反应掉87.5%的A所需的时间是375min
【答案】D
【详解】
A.将第一组数据和第二组数据代入 可得 ,则m=1,将第二组数据和
第四组数据代入 可得 ,则n=0,A错误;
B.由A选项的分析可知,m=1,n=0,则 ,代入第一组数据可得, ,B错误;
C.增大反应物的浓度,增大了速率,并没有改变瞬时速率常数k(只受温度影响),C错误;
D.存在过量的B时,反应掉87.5%的A可以看作经历3个半衰期,即50%+25%+12.5%,因此所需的时间
为 ,D正确;
故选D。
【题8】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,
这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用
kJ/mol表示。请认真观察如图,然后回答问题:
(1)图中所示反应是____(填“吸热”或“放热”)反应,该反应的ΔH=____(用含E、E 的代数式表示)。
1 2
(2)下列4个反应中,符合示意图描述的反应的是____(填代号)。
A.盐酸与NaOH反应
杨sir化学,侵权必究
B.Na与HO反应生成H
2 2
C.铝热反应
D.灼热的炭与水蒸气反应生成CO和H
2(3)已知热化学方程式:H(g)+ O(g)=HO(g) ΔH=-241.8 kJ/mol。该反应的活化能为167.2 kJ/mol,则其
2 2 2
逆反应的活化能为____。
【答案】放热 -(E-E) kJ/mol C 409 kJ/mol
1 2
【分析】
(1)依据图象分析反应物的总能量大于生成物的总能量,反应放热;反应的焓变=生成物的总能量-反应物的
总能量;
(2)由于反应物的总能量低于活化分子的最低能量,因此反应需要加热,而且该反应为放热反应;
(3)该反应是放热反应,反应的焓变=正反应的活化能-逆反应的活化能。
【详解】
(1)据图可知,反应物的总能量高于生成物的总能量,该反应是放热反应,ΔH=-(E-E) kJ/mol,故答案为:
1 2
放热;-(E-E) kJ/mol;
1 2
(2)由于反应物的总能量低于活化分子的最低能量,因此反应需要加热,而且该反应为放热反应,故C项
正确,故答案为C;
(3)在反应H(g)+ O(g)=HO(g) ΔH=-241.8 kJ/mol中,反应的焓变=正反应的活化能-逆反应的活化
2 2 2
能,-241.8 kJ/mol=167.2kJ/mol-逆反应的活化能,则逆反应的活化能=(241.8+167.2) kJ/mol=409 kJ/mol;故
答案为:409 kJ/mol。
【点睛】
本题考查了化学反应的能量变化与反应的焓变关系的分析判断,本题利用图象的形式,旨在考查对“化学
反应中的能量变化”的判断与有关化学反应中“活化能”的计算,读懂图象,焓变和活化能计算方法的理
解是解答关键。
提分作业
小杨老师 15521324728 侵权必究
【练1】下列说法正确的是
A.一定条件下,增大反应物的量会加快化学反应速率
B.增大压强,一定会加快化学反应速率
C.催化剂参与了化学反应降低了活化能,从而加快化学反应速率
D.活化分子间的碰撞叫做有效碰撞
【答案】C【详解】
A.一定条件下,增大反应物的浓度会加快化学反应速率,若加入固体物质,反应物浓度不变,反应速率
不变,故A错误;
B.对于没有气体参与的反应,增大压强,化学反应速率不变,故B错误;
C.催化剂参与了化学反应降低了活化能,从而加快化学反应速率,故C正确;
D.能引发化学反应的分子间碰撞称之为有效碰撞,活化分子只有在碰撞方向正确时的碰撞才是有效碰撞,
故D错误;
选C。
【练2】下列说法正确的是
A.增大反应物的质量,活化分子百分数增大,反应速率增大
杨sir化学,侵权必究
B.升高温度,活化分子百分数增大,反应速率增大
C.增大压强,活化分子百分数增大,反应速率增大
D.使用催化剂,分子能量提高,活化分子百分数增大,反应速率增大
【答案】B
【详解】
A.增大反应物的质量,反应物浓度增大,单位体积内活化分子百分数增大,从而增大有效碰撞几率,反应
速率增大,故A错误;
B.升高温度,活化分子百分增大数,有效碰撞几率增大,反应速率增大,故B正确;
C.增大压强,相当于反应物浓度增大,单位体积内活化分子百分数增大,从而增大有效碰撞几率,反应速
率增大,故C错误;
D.使用催化剂,降低反应活化能,活化分子百分数增大,有效碰撞几率增大,反应速率增大,故D错误;
故选B。
【练3】下列说法正确的是
①活化分子间的碰撞一定能发生化学反应;
②普通分子有时也能发生有效碰撞;
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数;
杨sir化学,侵权必究
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多;
⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大;
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
A.①②⑤ B.③④⑥ C.③④⑤ D.②③④
【答案】B
【详解】①活化分子间的碰撞不一定能发生化学反应,有效碰撞才能发生化学反应,①错误;
②发生有效碰撞有两个条件即具有足够的能量成为活化分子,具有正确的取向,故普通分子有时不能发生
有效碰撞,②错误;
③升高温度会加快反应速率,原因是提高了分子自身的能量,使部分普通分子转化为活化分子,故增加了
活化分子的数目,从而增加有效碰撞次数,③正确;
④增大反应物浓度会加快反应速率的原因是单位体积内分子数目增多,活化分子百分数不变,故单位体积
内的活化分子数目增多,故单位体积内的有效碰撞的次数增多,④正确;
⑤使用催化剂能提高反应速率,原因是降低反应所需要的活化能,使部分普通分子转化为活化分子,使有
效碰撞频率增大,⑤错误;
⑥化学反应的实质是旧化学键的断裂和新化学键的形成,碰撞理论认为活化分子有合适取向时的有效碰撞
是化学反应发生的前提,⑥正确;
综上所述,③④⑥正确,故答案为:B。
【练4】已知反应SO (aq)+2I-(aq) 2SO (aq)+I (aq),若向该溶液中加入含Fe3+的某溶液,反应机理
2 2
如图所示。下列有关该反应的说法错误的是
①2Fe3+(aq)+2I-(aq) I(aq)+2Fe2+(aq)
2
②2Fe2+(aq)+S O (aq)=2Fe3+(aq)+2SO (aq)
2
A.反应①和反应②相比,反应②更容易发生
B.Fe3+是该反应的催化剂
C.增大Fe3+的浓度,能够加快反应速率
D.若不加Fe3+,正反应的活化能比逆反应的活化能大
【答案】D
【详解】
A.反应②比反应①活化能低,反应②更容易发生,故A正确;
B. 在反应①中被消耗生成中间产物 ,在反应②中 消耗又生成了 , 是该反应的催化剂,故B正确;
C.增大 的浓度,能够加快反应①的速率,反应①决定整个反应的快慢,故C正确;
D.无论是否加 ,该反应为放热反应,正反应的活化能比逆反应的活化能小,故D错误。
故答案为:D
【练5】甲硫醇是一种重要的原料和化工试剂,硫化氢与甲醇合成甲硫醇的催化过程如图。下列说法不正
确的是
A.CHSH为共价化合物
3
B.该过程中断裂了O—H键、S—H键和C—S键
杨sir化学,侵权必究
C.该催化剂可降低该反应的活化能
D.该过程的总反应为HS+CHOH CHSH+H O
2 3 3 2
【答案】B
【详解】
A.CHSH的组成元素都是非金属元素,非金属元素的原子之间都是以共价键结合,因此该化合物为共价
3
化合物,A正确;
B.通过催化过程可以看出:硫化氢加入催化剂后,硫化氢中的氢硫键断开,形成巯基和氢原子,加入甲
醇后,甲醇分子吸附在催化剂表面,氢氧键断开,巯基取代羟基的位置形成甲硫醇和水,该过程中断裂O
—H键、S—H键、C—O键,形成了C—S键,B错误;
C.该催化剂可改变反应途径,降低该反应的活化能,使反应在较低的温度下进行,C正确;
D.根据图示可知:反应物是HS、CHOH,生成物是CHSH、HO,反应在催化剂存在条件下进行,故
2 3 3 2
反应方程式为:HS+CHOH CHSH+H O,D正确;
2 3 3 2
故合理选项是B。【练6】某学习小组为了探究BrO-+5Br-+6H+=3Br +3H O反应速率(v)与反应物浓度的关系,在20℃进
3 2 2
行实验,所得的数据如下表:
实验编号
① ② ③ ④ ⑤
相关数据
c(H+)/ mol · L-1 0.008 0.008 0.004 0.008 0.004
c(BrO-)/ mol· L-1 0.001 0.001 0.001 0.002 0.002
3
c(Br-)/ mol· L-1 0.10 0.20 0.20 0.10 0.40
v / mol· L-1· s-1 2.4×10-8 4.8×10-8 1.2×10-8 4.8×10-8 v
1
下列结论不正确的是( )
A.若温度升高到40℃,则反应速率增大
杨sir化学,侵权必究
B.实验②、④,探究的是c(BrO-)对反应速率的影响
3
C.若该反应速率方程为v ="k" ca(BrO -)cb(Br-)cc(H+)(k为常数),则c =2
3
D.实验⑤中,v =4.8×10-8
1
【答案】B
【解析】
试题分析:A、温度升高,化学反应速率增大,故说法正确;B、②和④对比,BrO-和Br-浓度都不一样,
3
因此探究的是BrO-和Br-对反应速率的影响,故说法错误;B、①和②代入数值,求出c=2,故说法正确;
3
D、根据表格②④数据的对比,求出v=4.8×10-8,故说法正确。
1
考点:考查影响化学反应速率的因素等知识。
【练7】汽车尾气中的氮氧化物是城市空气的主要污染物之一,如何降低汽车尾气污染已成为环保领域的
热点。
回答下列问题:
(1)科技工作者用甲烷将氮氧化物还原为 N 和 HO,涉及的反应如下:
2 2
CH(g)+4NO (g) =4NO(g)+CO(g)+2HO(g) ΔH=-574 kJ/mol
4 2 2 2 1
CH(g)+2NO (g) =CO (g)+2HO(g)+N(g) ΔH =-867 kJ/mol
4 2 2 2 2 2
则 CH(g)还原 NO(g)生成 N(g)的热化学方程式为___________。
4 2
(2)使用氢能源可以减少汽车尾气中有害气体的排放。利用甲醇与水蒸气反应可以制备氢气:CHOH(g)+
3
HO(g) =CO (g)+3H(g) ΔH,该反应过程中的能量变化如图:
2 2 2①ΔH___________0(填“>”“=”或“<”)。
杨sir化学,侵权必究
②途径(Ⅰ)的活化能 E=___________。
③途径(Ⅰ)变为途径(Ⅱ):改变的条件是___________,反应热(ΔH)___________(填“增大”“减小”或
“不变”)。
【答案】CH(g)+4NO(g) =2N(g)+CO(g)+2HO(g) ΔH=-1160 kJ/mol > E-E 加入催化剂
4 2 2 2 4 1
不变
【分析】
(1)利用盖斯定律书写CH(g)还原 NO(g)生成 N(g)的热化学方程式;
4 2
(2) ①反应物分子的能量小于生成物分子的能量;
②活化能是指分子从常态转变为容易发生化学反应的活跃状态所需要的能量;
③催化剂能降低反应的活化能;
【详解】
(1)①CH(g)+4NO (g) =4NO(g)+CO(g)+2HO(g) ΔH=-574 kJ/mol
4 2 2 2 1
②CH(g)+2NO (g) =CO (g)+2HO(g)+N(g) ΔH =-867 kJ/mol
4 2 2 2 2 2
根据盖斯定律,②×2-①得CH(g)还原 NO(g)生成 N(g)的热化学方程式为CH(g)+4NO(g) =2N(g)+
4 2 4 2
CO(g)+2HO(g) ΔH=-1160 kJ/mol;
2 2
(2) ①根据图示,反应物分子的能量小于生成物分子的能量,所以ΔH>0;
②活化能是指分子从常态转变为容易发生化学反应的活跃状态所需要的能量,根据图示,途径(Ⅰ)的活化能
E= E -E ;
4 1
③途径(Ⅰ)比途径(Ⅱ)的活化能高,途径(Ⅰ)变为途径(Ⅱ)改变的条件是加入催化剂;反应热只与反应体系的始
态和终态有关,所以ΔH不变。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育