文档内容
第 07 讲 常见的氧化剂与还原剂、氧化还原规律
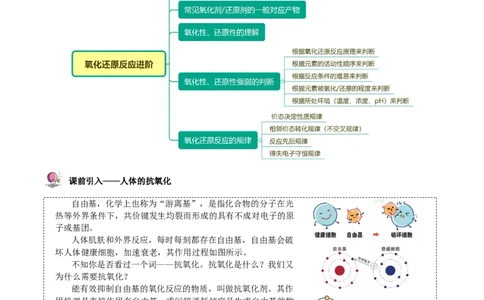
知识导航
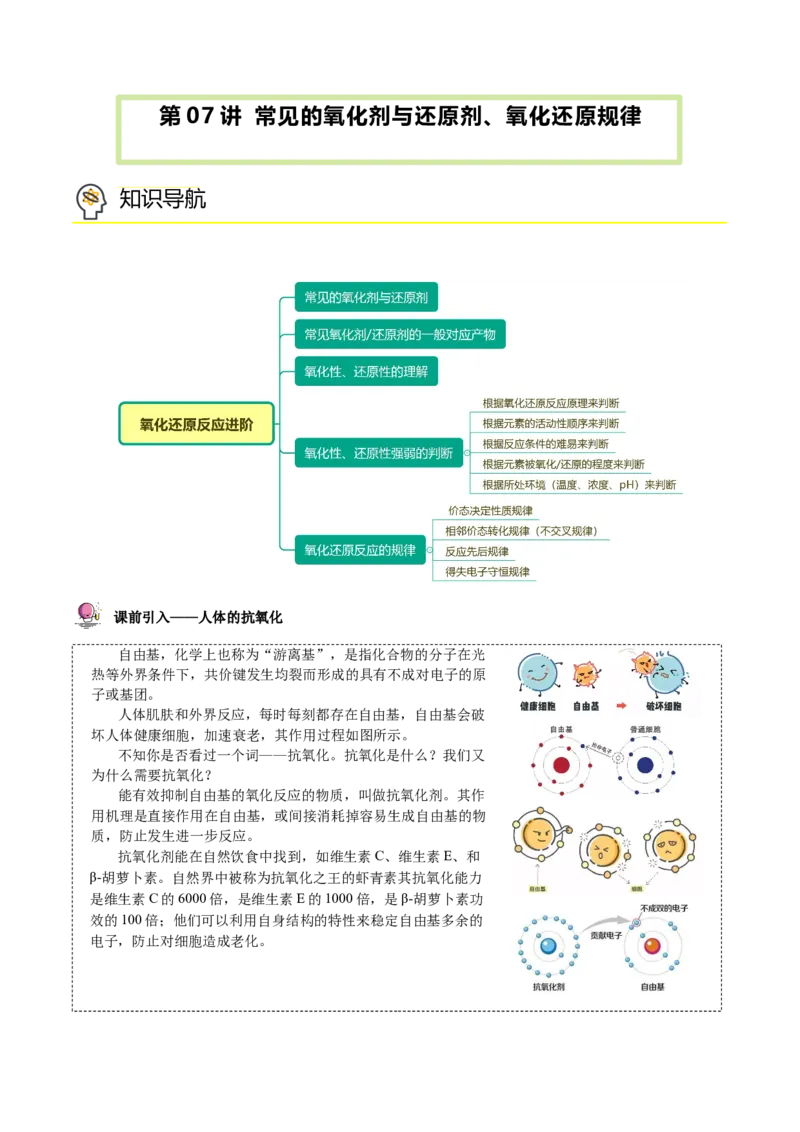
课前引入——人体的抗氧化
自由基,化学上也称为“游离基”,是指化合物的分子在光
热等外界条件下,共价键发生均裂而形成的具有不成对电子的原
子或基团。
人体肌肤和外界反应,每时每刻都存在自由基,自由基会破
坏人体健康细胞,加速衰老,其作用过程如图所示。
不知你是否看过一个词——抗氧化。抗氧化是什么?我们又
为什么需要抗氧化?
能有效抑制自由基的氧化反应的物质,叫做抗氧化剂。其作
用机理是直接作用在自由基,或间接消耗掉容易生成自由基的物
质,防止发生进一步反应。
抗氧化剂能在自然饮食中找到,如维生素C、维生素E、和
β-胡萝卜素。自然界中被称为抗氧化之王的虾青素其抗氧化能力
是维生素C的6000倍,是维生素E的1000倍,是β-胡萝卜素功
效的100倍;他们可以利用自身结构的特性来稳定自由基多余的
电子,防止对细胞造成老化。知识精讲
一、常见的氧化剂与还原剂
常见的氧化剂 常见的还原剂
活泼的非金属单质 Cl、O 活泼的金属单质 Al、Fe、Zn
2 2
高价态化合物 浓硫酸、KMnO、HNO、FeCl 低价态化合物 CO、SO、KI
4 3 3 2
过氧化物 Na
2
O
2
、H
2
O
2
某些非金属单质 C、H
2
、S
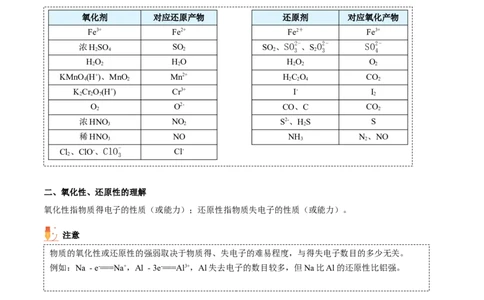
资料卡片——常见的氧化剂/还原剂及其一般对应产物
氧化剂 对应还原产物 还原剂 对应氧化产物
Fe3+ Fe2+ Fe2+ Fe3+
浓HSO SO SO 、SO2-、S O2- SO2-
2 4 2 2 3 2 3 4
HO HO HO O
2 2 2 2 2 2
KMnO (H+)、MnO Mn2+ HC O CO
4 2 2 2 4 2
KCr O(H+) Cr3+ I- I
2 2 7 2
O O2- CO、C CO
2 2
浓HNO NO S2-、HS S
3 2 2
稀HNO NO NH N、NO
3 3 2
Cl、ClO-、ClO- Cl-
2 3
二、氧化性、还原性的理解
氧化性指物质得电子的性质(或能力);还原性指物质失电子的性质(或能力)。
注意
物质的氧化性或还原性的强弱取决于物质得、失电子的难易程度,与得失电子数目的多少无关。
例如:Na - e-===Na+,Al - 3e-===Al3+,Al失去电子的数目较多,但Na比Al的还原性比铝强。
三、氧化性、还原性强弱的判断
1.根据氧化还原反应原理来判断
(1)氧化性强弱:氧化剂>氧化产物。(2)还原性强弱:还原剂>还原产物。
2.根据元素的活动性顺序来判断
(1)金属单质越活泼,其还原性越强;非金属单质越活泼,其氧化性越强。
(2)“单强离弱”——金属单质还原性越强,其阳离子的氧化性越弱;非金属单质的氧化性越强,其阴
离子的还原性越弱。
3. 根据反应条件的难易来判断
反应的条件越简单,反应就越容易发生,说明物质氧化性(或还原性)越强。
举个例子
2KMnO + 16HCl(浓) === 2KCl + 2MnCl + 8HO+ 5Cl↑
4 2 2 2
MnO + 4HCl(浓) ===== MnCl + 2HO+ Cl↑
2 2 2 2
O + 4HCl(浓) ===== 2Cl+2HO
2 2 2
氧化性:_____________________________
4. 根据元素被氧化/还原的程度来判断
某还原剂被不同氧化剂氧化时,元素化合价升得越高,说明氧化剂的氧化性越强。
举个例子
2Fe + 3Cl ===== 2FeCl Fe + S ===== FeS 氧化性:__________
2 3
Cu + 2Fe3+ ==== Cu2+ + 2Fe2+ 3Zn + 2Fe3+ ==== 3Zn2+ + 2Fe 还原性:__________
5. 根据所处环境(温度、浓度、pH)来判断同一物质在不同的条件下,其氧化性/还原性会有所不同。
(1)温度:①氧化性:浓硫酸(热)>浓硫酸(冷); ②还原性:浓盐酸(热)>浓盐酸(冷)。
(2)浓度:HNO(浓) > HNO(稀)
3 3
(3)pH:①中性环境中 不显氧化性,酸性环境中 显强氧化性;
NO- NO-
3 3
②KMnO (酸性)>KMnO (中性)>KMnO (碱性)
4 4 4
四、氧化还原反应的规律
1. 价态决定性质规律
(1)处于最高价态的元素 → 只有 性;
(2)处于最低价态的元素 → 只有 性;
(3)处于中间价态的元素 → 性。
补充说明
一般来说,同种元素价态越高,氧化性越强;价态越低,还原性越强。
如氧化性:Fe3+ > Fe2+ > Fe,SO > SO;(特例:HClO <HClO < HClO < HClO)
3 2 4 3 2
还原性:HS > S > SO 。
2 2
思考与交流:下面两种双线桥的画法,哪种是正确的?
2. 相邻价态转化规律(不交叉规律)
同种元素不同价态之间发生氧化还原反应,元素的化合价只向中间靠拢,不出现交叉。即:高价要降低,
低价要升高,它们最多变为同一价态,不可能发生交叉现象。
3. 反应先后规律
(1)当一种氧化剂遇到几种还原剂,若均能反应,先跟还原性强的反应。
(2)当一种还原剂遇到几种氧化剂,若均能反应,先跟氧化性强的反应。
及时小练
在含有Cu(NO )、Mg(NO)、AgNO 的溶液中加入过量锌粉,反应的先后顺序是?
3 2 3 2 34. 得失电子守恒规律
氧化还原反应中,氧化剂得电子总数等于还原剂失电子总数。
对点训练
题型一:氧化还原基本概念辨析
【例1】(2019·罗平县第二中学高一期末)下列说法正确的是
A.金属单质在反应中只能作还原剂,非金属单质只能作氧化剂
B.氧化还原反应中一定存在电子的转移
C.某元素从化合态到游离态,该元素一定被还原
D.失电子多的金属还原性强
题型二:常见的氧化剂/还原剂
【例2】(2021·浙江)ClO 是一种高效消毒剂,可通过以下反应制得:
2
2KClO+H C O+H SO =2ClO +K SO +2CO +2H O,其中还原剂是
3 2 2 4 2 4 2 2 4 2 2
A.KClO B.HC O C.ClO D.CO
3 2 2 4 2 2
【变2-1】在氧化还原反应中,下列各组物质均可用作氧化剂的是( )
A.F-、I-、S2- B.Fe3+、 、
MnO- NO-
4 3
C. 、Mg D.Cl、Fe3+、Al
ClO- 2
4
【变2-2】(2021·全国高三开学考试)人体正常的血红蛋白中应含Fe2+,若误食亚硝酸盐,则导致血红蛋
白中Fe2+转化为高铁血红蛋白而中毒,服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe2+氧化为Fe3+ D.亚硝酸盐被氧化
题型三:氧化还原规律【例3】(2021·四川雅安·高一期末)已知锰元素的最高化合价为+7价,下列对KMnO 推测或判断错误的
4
是
A.物质分类属于盐 B.在反应中易表现氧化性
C.在反应中易表现还原性 D.可用于实验室制O
2
【变3-1】硫元素在下列物质中,只有还原性的是( )
A.NaS B.S C.SO D.HSO
2 2 2 4
【变3-2】下列粒子不具有还原性和只具有还原性的依次是( )
A.Fe2+、Fe B.CO、CO C.S、S2- D.Na+、Na
2
【例4】(2022·浙江高三专题练习)根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是
I+SO+2H O=HSO +2HI;2FeCl +Cl=2FeCl ;2FeCl +2HI=2FeCl +2HCl+I
2 2 2 2 4 2 2 3 3 2 2
A.I->Fe2+>Cl->SO B.Cl->Fe2+>SO I-
2 2>
C.Fe2+>I->Cl->SO D.SO >I->Fe2+>Cl-
2 2
【变4-1】(2021·四川省武胜烈面中学校高一开学考试)已知有如下反应∶ ①ClO +5Cl-
+6H+=3Cl↑+3H O,②2FeCl +2KI=2FeCl +2KCl+I ③2FeCl +Cl=2FeCl 。下列各微粒氧化能力由强到弱的
2 2 3 2 2 2 2 3
顺序正确的是
A.ClO >Cl>Fe3+>I B.Cl>ClO >I >Fe3+
2 2 2 2
C.ClO >Cl>I >Fe3+ D.ClO >Fe3+ >Cl>I
2 2 2 2
【变4-2】(2020·石家庄市第十中学高一月考)已知Co O 在酸性溶液中易被还原成Co2+,Co O、Cl、
2 3 2 3 2
FeCl 、I 氧化性依次减弱。下列反应在水溶液中不可能发生的是
3 2
A.3Cl+6FeI =4FeI +2FeCl
2 2 3 3
B.3Cl+2FeI = 2FeCl +2I
2 2 3 2
C.Co O+6HCl =2CoCl +Cl↑+3H O
2 3 2 2 2
D.2Fe3++2I-=2Fe2++I
2【变4-3】(2021·济宁市实验中学高三开学考试)已知三个氧化还原反应:①2FeCl +2KI=2FeCl +2KCl
3 2
+I,②2FeCl +Cl=2FeCl ,③2KMnO +16HCl(浓)= 2KCl+2MnCl +8HO+5Cl↑。若某溶液中有Fe2
2 2 2 3 4 2 2 2
+、I-、Cl-共存,要将I-氧化除去而不氧化Fe2+和Cl-,则可加入的试剂是
A.Cl B.KMnO C.FeCl D.HCl
2 4 3
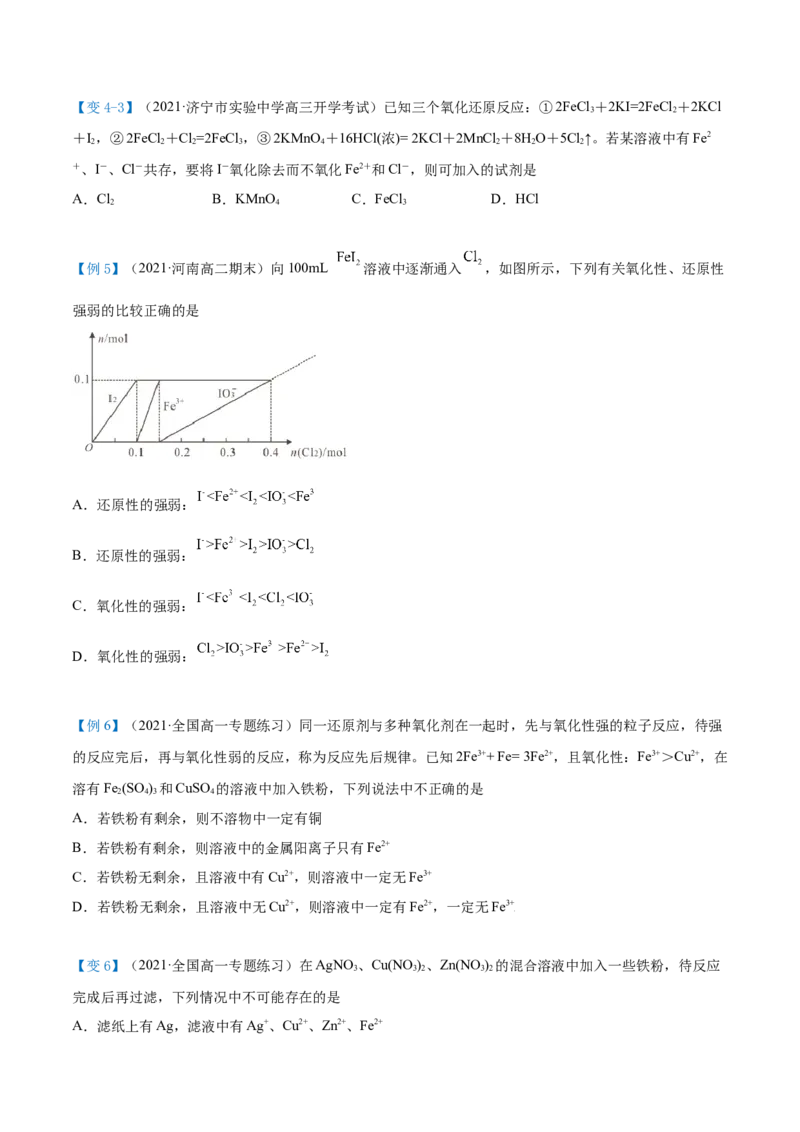
【例5】(2021·河南高二期末)向100mL 溶液中逐渐通入 ,如图所示,下列有关氧化性、还原性
强弱的比较正确的是
A.还原性的强弱:
B.还原性的强弱:
C.氧化性的强弱:
D.氧化性的强弱:
【例6】(2021·全国高一专题练习)同一还原剂与多种氧化剂在一起时,先与氧化性强的粒子反应,待强
的反应完后,再与氧化性弱的反应,称为反应先后规律。已知2Fe3++ Fe= 3Fe2+,且氧化性:Fe3+>Cu2+,在
溶有Fe (SO ) 和CuSO 的溶液中加入铁粉,下列说法中不正确的是
2 4 3 4
A.若铁粉有剩余,则不溶物中一定有铜
B.若铁粉有剩余,则溶液中的金属阳离子只有Fe2+
C.若铁粉无剩余,且溶液中有Cu2+,则溶液中一定无Fe3+
D.若铁粉无剩余,且溶液中无Cu2+,则溶液中一定有Fe2+,一定无Fe3+
【变6】(2021·全国高一专题练习)在AgNO、Cu(NO )、Zn(NO ) 的混合溶液中加入一些铁粉,待反应
3 3 2 3 2
完成后再过滤,下列情况中不可能存在的是
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+B.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+、Zn2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+
D.滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+
【例7】(2022·全国高三专题练习)在常温下,发生下列几种反应:
①
②
③
根据上述反应,下列结论判断错误的是
A.溶液中可发生反应:
B. 在①、③反应中为还原剂
C.氧化性强弱的顺序为:
D. 是 的还原产物
【变7-1】(2021·全国高一课时练习)已知:①2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
②6FeCl +3Br =4FeCl +2FeBr
2 2 3 3
③Cl+2KBr=Br +2KCl。根据上述反应,判断下列结论错误的是
2 2
A.溶液中可发生反应:2FeCl +Cl=2FeCl
2 2 3
B.少量KMnO 溶液加入HBr和HCl的混合溶液中:HBr先被氧化
4
C.氧化性强弱顺序为:KMnO >Cl>FeCl >Br
4 2 3 2
D.反应①中,MnCl 是KMnO 的还原产物
2 4
【变7-2】(2021·罗平县第二中学高一期末)已知下述三个实验均能发生化学反应:
①将铜丝放入氯化铁溶液中
②将光亮铁钉放入硫酸铜溶液中
③向硫酸亚铁溶液中滴入几滴双氧水
下列判断正确的是A.实验①中发生的是置换反应 B.实验②中硫酸铜作还原剂
C.实验③中体现Fe2+的氧化性 D.上述实验证明还原性Fe>Cu>Fe2+
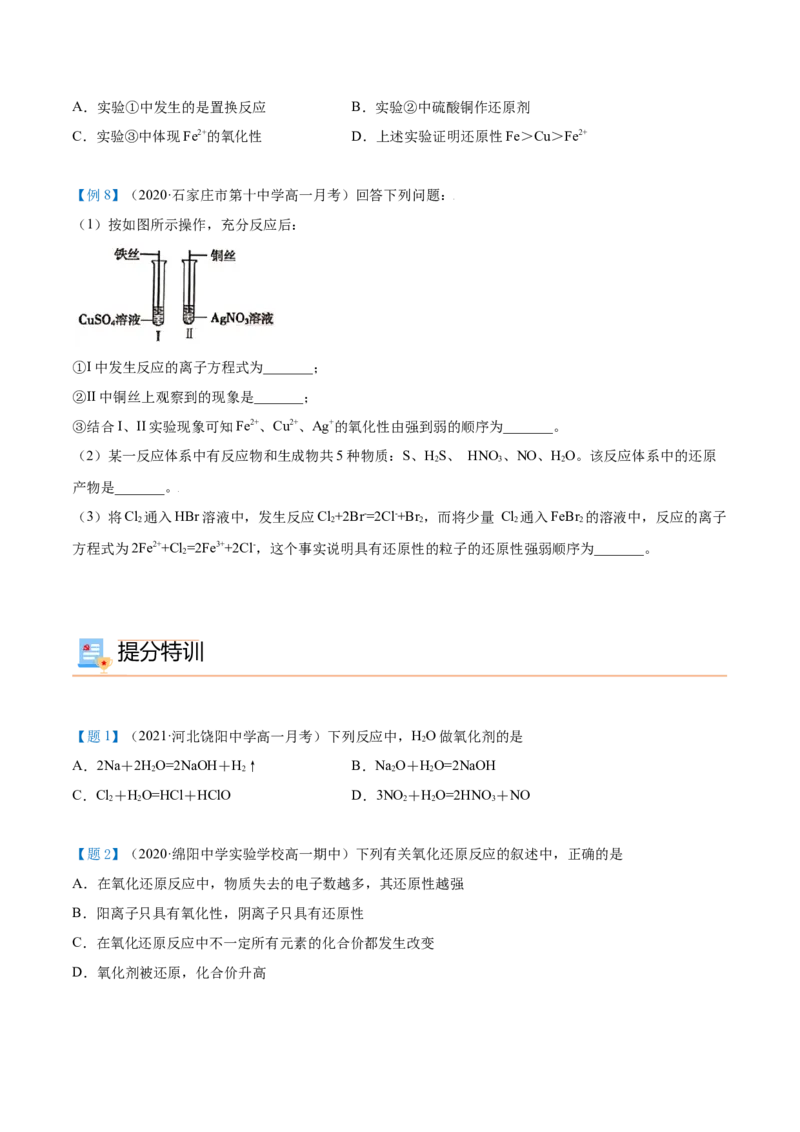
【例8】(2020·石家庄市第十中学高一月考)回答下列问题:
(1)按如图所示操作,充分反应后:
①I中发生反应的离子方程式为_______;
②II中铜丝上观察到的现象是_______;
③结合I、II实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______。
(2)某一反应体系中有反应物和生成物共5种物质:S、HS、 HNO、NO、HO。该反应体系中的还原
2 3 2
产物是_______。
(3)将Cl 通入HBr溶液中,发生反应Cl+2Br-=2Cl-+Br ,而将少量 Cl 通入FeBr 的溶液中,反应的离子
2 2 2 2 2
方程式为2Fe2++Cl=2Fe3++2Cl-,这个事实说明具有还原性的粒子的还原性强弱顺序为_______。
2
提分特训
【题1】(2021·河北饶阳中学高一月考)下列反应中,HO做氧化剂的是
2
A.2Na+2HO=2NaOH+H↑ B.NaO+HO=2NaOH
2 2 2 2
C.Cl+HO=HCl+HClO D.3NO +HO=2HNO +NO
2 2 2 2 3
【题2】(2020·绵阳中学实验学校高一期中)下列有关氧化还原反应的叙述中,正确的是
A.在氧化还原反应中,物质失去的电子数越多,其还原性越强
B.阳离子只具有氧化性,阴离子只具有还原性
C.在氧化还原反应中不一定所有元素的化合价都发生改变
D.氧化剂被还原,化合价升高【题3】(2020·石家庄市第十中学高一月考)根据下列各反应,判断有关物质还原性由强到弱的顺序是
①HSO +I +H O=2HI+HSO
2 3 2 2 2 4
②2FeCl +2HI=2FeCl +2HCl+I
3 2 2
③3FeCl +4HNO =2FeCl +NO↑+2HO+Fe(NO )
2 3 3 2 3 3
A.HSO >HI>FeCl >NO
2 3 2
B.NO>FeCl >HSO >HI
2 2 3
C.I>FeCl >HSO >NO
2 2 2 3
D.FeCl >HI>HSO >NO
2 2 3
【题4】在KClO + 6HCl(浓) === KCl + 3Cl ↑+ 3H O的反应中,被氧化的氯与被还原的氯的原子个数比
3 2 2
为( )
A.1∶6 B.6∶1 C.1∶5 D.5∶1
【题5】(2020·石家庄市第十中学高一月考)NO既是医学上的一种麻醉剂,又是一种常见的温室气体。
2
制取NO的方法有很多,例如:
2
①NH NO =N O↑+2HO
4 3 2 2
②KSO +2NO=KSO +N O
2 3 2 4 2
③2NH +2O =N O+3HO
3 2 2 2
④2NaNO +(NH)SO =2N O↑+Na SO +4H O
3 4 2 4 2 2 4 2
下列说法中正确的是
A.反应①中NH NO 既是氧化剂又是还原剂,HO是氧化产物
4 3 2
B.反应②中KSO 是还原剂,NO是氧化产物
2 3 2
C.反应③中每生成1个NO,转移8个电子
2
D.反应④中NaNO 是还原剂,NO既是氧化产物又是还原产物
3 2
【题6】(2022·全国)根据表中信息,判断下列叙述中正确的是
序号 氧化剂 还原剂 其他反应物 氧化产物 还原产物
① Cl FeBr - Cl-
2 2
② KClO 浓盐酸 - Cl
3 2
③ KMnO HO HSO O Mn2+
4 2 2 2 4 2
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO>Fe3+>Cl>Br
3 2 2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-D.表中③组反应的离子方程式为2MnO +3HO+6H+=2Mn2++4O↑+6HO
2 2 2 2
【题7】(2021·陕西榆林·高一期末)已知反应:① ;② ;③
。下列说法不正确的是
A.氧化性:
B.还原性:
C.反应①中氧化剂与还原剂的质量之比为
D.反应③中被氧化的元素与被还原的元素的质量之比为
【题8】(2021·全国高一课时练习)有下列三个在溶液中发生的氧化还原反应:
①2FeCl +2KI=2FeCl +2KCl+I
3 2 2
②2FeCl +Cl=2FeCl
2 2 3
③KCr O+14HCl=2KCl+2CrCl +7H O+3Cl ↑
2 2 7 3 2 2
请根据上述反应分析推断后回答下列问题:
(1)FeCl 、I、Cl、KCr O 的氧化性由强到弱依次是___________。
3 2 2 2 2 7
(2)Cr O 、I-在强酸性溶液中能否大量共存?___________(填“能”或“不能”),理由是___________。
2
(3)在酸性溶液中存在大量的I-,则Cr O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________。
2
(4)+6价铬的化合物毒性较大,常用NaHSO 将酸性废液中的Cr O 还原成Cr3+,反应的离子方程式为
3 2
___________。
提分作业
【练1】(2021·浙江高一月考)下列反应中,HCl只作氧化剂的是
A.CuO+2HCl=CuCl +H O B.Zn+2HCl=ZnCl +H ↑
2 2 2 2C.2HCl H↑+Cl↑ D.4HC1+O 2Cl+2H O
2 2 2 2 2
【练2】(2021·湖南娄底市·娄底一中高一期中)可用反应2Al+WO Al O+W制取高熔点的钨,该
3 2 3
反应的氧化剂是
A.Al B.WO C.Al O D.W
3 2 3
【练3】(2021·河北师大附中高一月考)已知氧化性:Cl>Br >Fe3+>I 。判断下列化学方程式一定不正确
2 2 2
的是
A.2FeCl +2KI=2FeCl +2KCl+I B.6FeCl +3Br =4FeCl +2FeBr
3 2 2 2 2 3 3
C.FeCl +Br =FeBr +Cl D.FeI+Cl=FeCl +I
2 2 2 2 2 2 2 2
【练4】(2021·浙江高一月考)已知:①向MnO 晶体滴加浓盐酸,加热产生黄绿色气体:②向FeCl 溶液
2 2
中通入少量实验①产生的气体,溶液变黄色。下列判断正确的为
A.上述实验证明氧化性: MnO >Cl> Fe3+
2 2
B.上述实验中, 有一个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
【练5】(2021·全国高一课时练习)一定条件下,KClO 与I 按下式反应:2KClO+I=2KIO+Cl,则下
3 2 3 2 3 2
列推断正确的是
A.该反应属于复分解反应 B.还原产物为Cl,氧化产物为KIO
2 3
C.还原性KClO>I D.氧化性I>KClO
3 2 2 3
【练6】(2021·全国高一课时练习)PbO 、KMnO 、Cl、FeCl 、CuCl 的氧化性依次减弱。下列反应在水
2 4 2 3 2
溶液中不可能发生的是
A.Cu+2Fe3+=Cu2++2Fe2+ B.10Cl-+2MnO +16H+=2Mn2++5Cl↑+8HO
2 2
C.2Fe2++Cl=2Fe3++2Cl- D.5Pb2++2MnO +2HO=5PbO +2Mn2++4H+
2 2 2【练7】(2020·石家庄市第十中学高一月考)现有①KMnO 、②H、③O、④Cl、⑤CO、⑥A1 6种物
4 2 2 2
质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲药品柜中,常用的还原剂放入乙药品柜中。
(1)甲药品柜中有_______。(均填序号)
(2)由Fe Fe O,Fe O Fe可知,欲实现I反应过程应从_______(填“甲”或“乙”)药品柜中找物
3 4 2 3
质。
(3)请将Fe、Fe O、CO、CO 4种物质填入下面的横线上,组成一个配平了的化学方程式。并用双线桥
2 3 2
法标出电子转移的方向和数目_______。关注更新免费领取,淘宝唯一每月更新店铺:知二教育