文档内容
第 06 讲 氧化还原反应基础
知识导航
课前引入
初中时学过氧化反应、还原反应。你还记得它们的定义吗?
2CuO+C=====2Cu+CO
2
↑,Fe
2
O
3
+3CO=====2Fe+3CO
2
物质 反应物 发生的反应(氧化反应或还原反应)
得氧物质
失氧物质
氧化反应和还原反应,是分开进行的吗?
请从元素化合价角度观察分析,上述化学方程式中有什么特征?
【答案】物质得到氧的反应叫做氧化反应 物质失去氧的反应叫做还原反应
C、CO 氧化反应 CuO、Fe O 还原反应
2 3在化学反应中,一种物质得到氧发生氧化反应,必然有一种物质失去氧发生还原反应。
元素化合价在反应前后发生了改变
知识精讲
一、氧化还原反应的定义
凡是有元素___________升降的化学反应称之为氧化还原反应。
【答案】化合价
二、氧化还原反应的特征
元素的化合价在反应前后发生了变化。
三、氧化反应、还原反应的定义(元素化合价角度)
1. 氧化反应:物质所含元素化合价________的反应叫做氧化反应。
2. 还原反应:物质所含元素化合价________的反应叫做还原反应。
【答案】升高 降低
思考与交流:氧化还原反应前后,元素化合价为什么会改变?
举个例子——氯化钠的形成
从原子结构来看,钠原子的最外电子层上有1个电子,氯原
子的最外电子层上有7个电子。当Na与Cl 反应时,钠原子失去
2
1个电子,带1个单位正电荷,成为钠离子(Na+);氯原子得到
1个电子,带1个单位负电荷,成为氯离子(Cl-),这样双方最
外电子层都达到了8个电子的稳定结构(如图)。
反应中钠元素的化合价从0价升高到+1价,Na被氧化;氯
元素的化合价从0价降低到-1价,Cl 被还原。在这个反应中,发
2
生了电子的得失,Na发生了氧化反应,Cl 发生了还原反应。
2
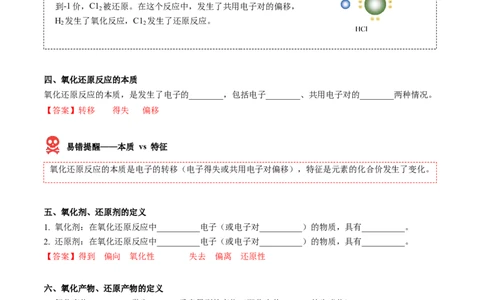
再举个例子——氯化氢的形成H 与Cl 的反应则与此不同。氢原子的最外电子层上有1个电
2 2
子,可获得1个电子而形成2个电子的稳定结构;氯原子的最外电
子层上有7个电子,也可获得1个电子而形成8个电子的稳定结
构。
在发生反应时,它们都未能把对方的电子夺取过来,而是双
方各以最外层的1个电子组成一个共用电子对,这个电子对受到两
个原子核的共同吸引,使双方最外电子层都达到稳定结构。
由于氯原子对共用电子对的吸引力比氢原子的稍强一些,所
以,共用电子对偏向于氯原子而偏离于氢原子。因此,氢元素的化
合价从0价升高到+1价,H 被氧化;氯元素的化合价从0价降低
2
到-1价,C1 被还原。在这个反应中,发生了共用电子对的偏移,
2
H 发生了氧化反应,C1 发生了还原反应。
2 2
四、氧化还原反应的本质
氧化还原反应的本质,是发生了电子的________,包括电子________、共用电子对的________两种情况。
【答案】转移 得失 偏移
易错提醒——本质 vs 特征
氧化还原反应的本质是电子的转移(电子得失或共用电子对偏移),特征是元素的化合价发生了变化。
五、氧化剂、还原剂的定义
1. 氧化剂:在氧化还原反应中__________电子(或电子对__________)的物质,具有__________。
2. 还原剂:在氧化还原反应中__________电子(或电子对__________)的物质,具有__________。
【答案】得到 偏向 氧化性 失去 偏离 还原性
六、氧化产物、还原产物的定义
1. 氧化产物:________发生_______反应得到的产物(即化合价_______的生成物)。
2. 还原产物:________发生_______反应得到的产物(即化合价_______的生成物)。
【答案】还原剂 氧化 升高 氧化剂 还原 降低
及时小练指出下列氧化还原反应的氧化剂、还原剂、氧化产物、还原产物:
反应 氧化剂 还原剂 氧化产物 还原产物
Fe+CuSO ===FeSO + Cu
4 4
Cl+2NaOH===NaCl+NaClO+HO
2 2
SO +2HS===2HO+3S↓
2 2 2
【答案】CuSO Fe FeSO Cu
4 4
Cl Cl NaClO NaCl
2 2
SO HS S S
2 2
思考与交流:观察上面几个反应,氧化剂与还原剂一定是不同物质吗?氧化产物与还原产物一定是不
同物质吗?
注意
在氧化还原反应中,氧化剂与还原剂可能是同一物质,氧化产物和还原产物也有可能是同一物质。
思考与交流:判断下列化学方程式是否氧化还原反应。
四大基本反应类型 化学方程式 是否氧化还原反应
2NO+O===2NO
2 2
化合反应
CaO + HO === Ca(OH)
2 2
2HO ===== 2H↑ + O↑
2 2 2
分解反应
CaCO ===== CaO + CO ↑
3 2
Fe + CuSO === FeSO + Cu
4 4
置换反应
Fe+2HCl===FeCl +H↑
2 2
NaOH + HCl === NaCl +HO
2
复分解反应
NaCl + AgNO === AgCl↓+NaNO
3 3
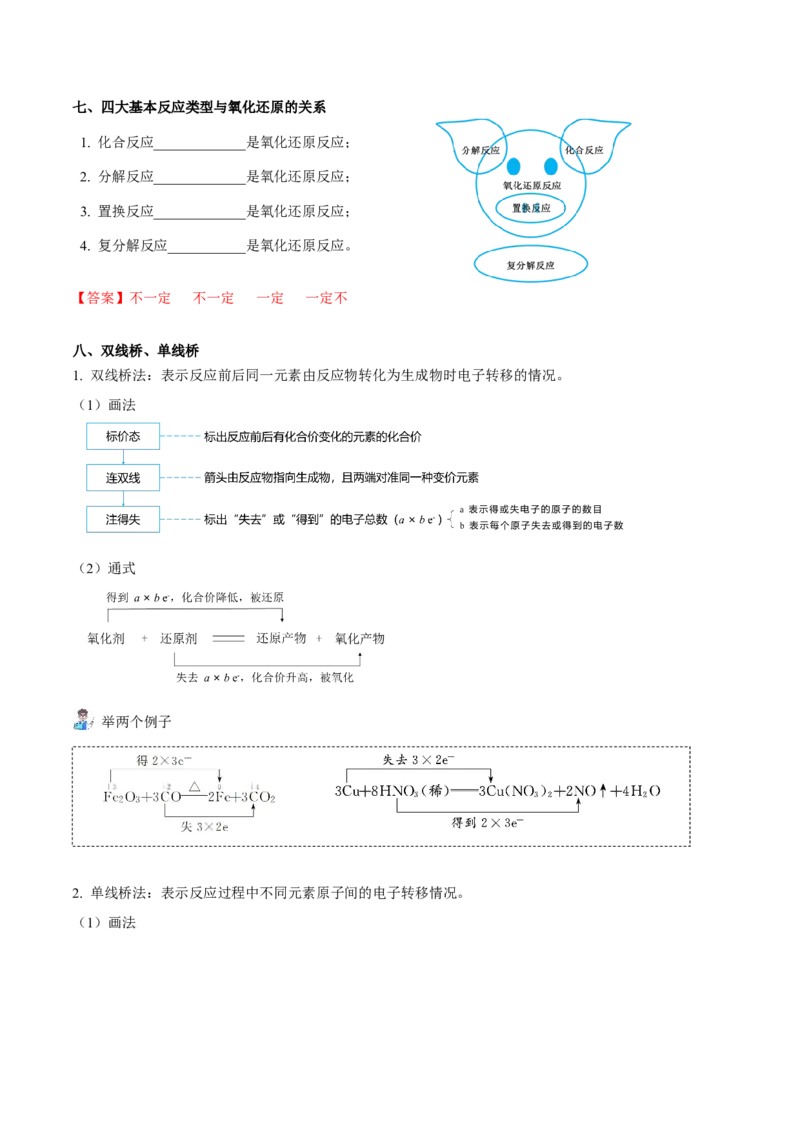
【答案】 √;×;√;×;√;√;×;×七、四大基本反应类型与氧化还原的关系
1. 化合反应_____________是氧化还原反应;
2. 分解反应_____________是氧化还原反应;
3. 置换反应_____________是氧化还原反应;
4. 复分解反应___________是氧化还原反应。
【答案】不一定 不一定 一定 一定不
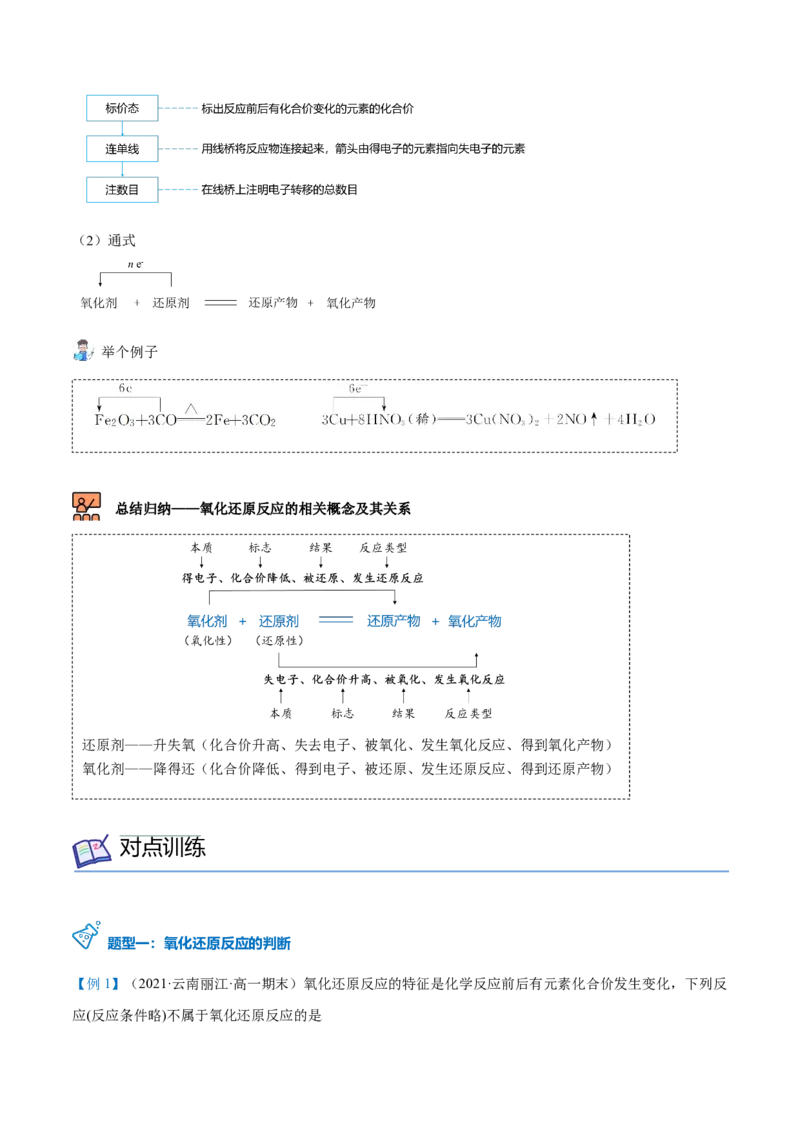
八、双线桥、单线桥
1. 双线桥法:表示反应前后同一元素由反应物转化为生成物时电子转移的情况。
(1)画法
(2)通式
举两个例子
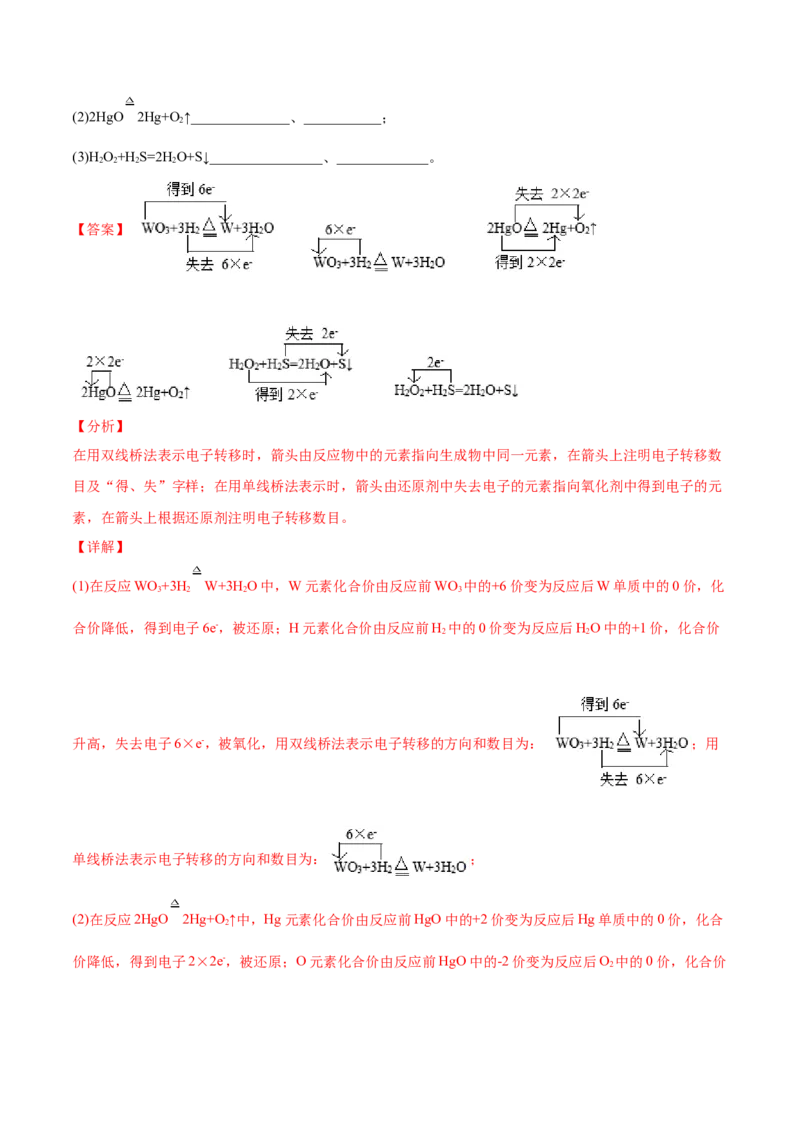
2. 单线桥法:表示反应过程中不同元素原子间的电子转移情况。
(1)画法(2)通式
举个例子
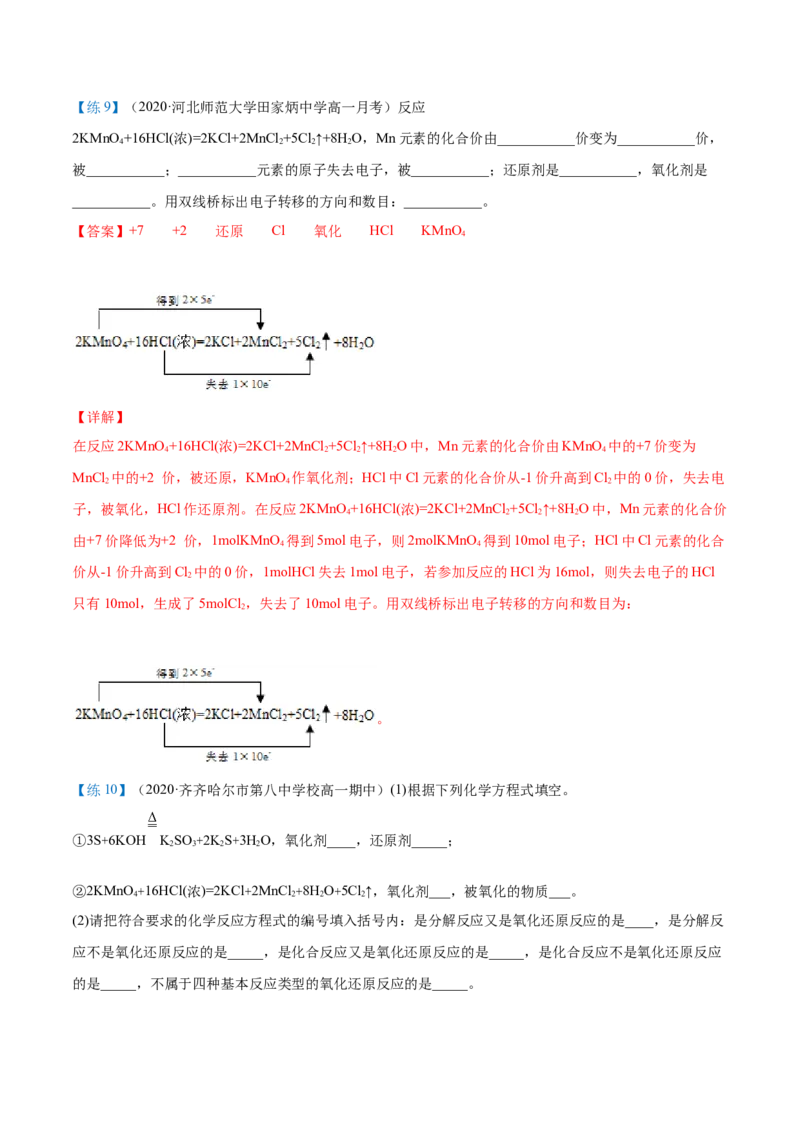
总结归纳——氧化还原反应的相关概念及其关系
还原剂——升失氧(化合价升高、失去电子、被氧化、发生氧化反应、得到氧化产物)
氧化剂——降得还(化合价降低、得到电子、被还原、发生还原反应、得到还原产物)
对点训练
题型一:氧化还原反应的判断
【例1】(2021·云南丽江·高一期末)氧化还原反应的特征是化学反应前后有元素化合价发生变化,下列反
应(反应条件略)不属于氧化还原反应的是A.H+Cl=2HCl B.CO+CuO=CO +Cu
2 2 2
C.HCl+NaOH=NaCl+H O D.C+CO =2CO
2 2
【答案】C
【分析】
有元素化合价发生变化的反应属于氧化还原反应。
【详解】
A. H+Cl=2HCl反应前后有H、Cl元素化合价发生变化,A不符合;
2 2
B. CO+CuO=CO +Cu反应前后有C、Cu元素化合价发生变化,B不符合;
2
C. HCl+NaOH=NaCl+H O反应前后没有元素化合价发生变化,C符合;
2
D. C+CO =2CO反应前后有C元素化合价发生变化,D不符合;
2
答案选C。
【变1-1】(2020·重庆复旦中学高一月考)下列反应既属于离子反应,又属于氧化还原反应的是
A.
B.
C.
D.
【答案】B
【分析】
反应过程中有化合价变化的反应是氧化还原反应,有离子参与的反应是离子反应。
【详解】
A.反应过程中没有离子参与反应,不是离子反应,A项错误;
B.反应过程中氧的化合价由—1价变为0价和+2价,而且生成氢氧化钠,有离子生成,所以既是离子反
应,也是氧化还原反应,B项正确;
C.反应中没有元素化合价变化,不是氧化还原反应,C项错误;
D,反应过程中没有离子参与反应,不是离子反应,D项错误。
答案为B。
【变1-2】(2021·全国高一课时练习)下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是A.NH Cl+NaOH NaCl+H O+NH ↑ B.CH+2O CO+2H O
4 2 3 4 2 2 2
C.2Al+Fe O Al O+2Fe D.3Cl+2Fe 2FeCl
2 3 2 3 2 3
【答案】B
【详解】
A.该反应属于复分解反应,没有化合价变化,不是氧化还原反应,故A不符合题意;
B.该反应不属于四种基本反应类型,且有元素化合价发生变化,属于氧化还原反应,故B符合题意;
C.该反应属于置换反应,是氧化还原反应,故C不符合题意;
D.该反应属于化合反应,是氧化还原反应,故D不符合题意。
综上所述,答案为B。
【变1-3】(2021·罗平县第二中学高一月考)下列反应中水既不是氧化剂又不是还原剂的氧化还原反应是
A.2NaO+2HO=4NaOH+O↑
2 2 2 2
B.NaH+HO=NaOH+H↑
2 2
C.2F+2HO=4HF+O
2 2 2
D.SO +HO=HSO
3 2 2 4
【答案】A
【详解】
A.2NaO+2HO=4NaOH+O↑,反应NaO 中O元素化合价发生变化,水中H、O元素化合价不变,所
2 2 2 2 2 2
以水既不是氧化剂也不是还原剂,故A符合题意;
B.该反应中HO中的H由+1价变为0价,所以水作氧化剂,故B不符合题意;
2
C.该反应水中O元素化合价由-2价变为0价,所以水作还原剂,故C不符合题意;
D.该反应元素的化合价均不变,不是氧化还原反应,故D不符合题意;
答案选A。
【变1-4】(2020·河北高一月考)氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属
于阴影部分的是A.Cl+2KBr=Br +2KCl
2 2
B.2NaHCO NaCO+ H O+CO↑
3 2 3 2 2
C.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
D.CH+2O CO +2H O
4 2 2 2
【答案】D
【分析】
阴影部分的区域属于氧化还原反应,但不属于四大反应类型。
【详解】
A.Cl+2KBr=Br +2KCl属于置换反应、氧化还原反应,故A不符合题意;
2 2
B.2NaHCO NaCO+ H O+CO↑属于分解反应、非氧化还原反应,故B不符合题意;
3 2 3 2 2
C.4Fe(OH) +O +2H O=4Fe(OH) 属于化合反应、氧化还原反应,故C不符合题意;
2 2 2 3
D.CH+2O CO +2H O属于氧化还原反应,但不属于四大反应类型,故D符合题意;
4 2 2 2
答案选D。
【变1-5】(2021·全国高一课时练习)化学反应按照不同的分类方法可以分为化合反应、分解反应、置换
反应、复分解反应,也可以分为氧化还原反应和非氧化还原反应。回答下列问题:
①CO+C 2CO
2
②2Fe+3Cl 2FeCl
2 3③C+HO(g) CO+H
2 2
④2HO 2H↑+O↑
2 2 2
⑤NaSO +BaCl =2NaCl+BaSO↓
2 4 2 4
⑥HO+HS=S↓+2HO
2 2 2 2
(1)既是氧化还原反应又是化合反应的为________(填序号,下同)。
(2)属于非氧化还原反应的为________。
(3)不属于四种基本反应类型的为________。
(4)属于置换反应的为________。
【答案】①② ⑤ ⑥ ③
【详解】
①为氧化还原反应和化合反应;②为氧化还原反应和化合反应;③为氧化还原反应和置换反应;④为氧化
还原反应和分解反应;⑤为非氧化还原反应和复分解反应;⑥为氧化还原反应,不属于四种基本反应类型,
据此解答;
(1)既是氧化还原反应又是化合反应的为①②;
(2)属于非氧化还原反应的为⑤;
(3)不属于四种基本反应类型的为⑥;
(4)属于置换反应的为③。
题型二:氧化还原反应中的概念辨析
【例2】(2021·张家口市宣化第一中学高一月考)下列说法正确的是
A.氧化还原反应中一定有氧元素参加
B.得电子的物质是氧化剂,失电子的物质是还原剂
C.在一个氧化还原反应中,有一种元素被氧化,必有另一种元素被还原
D.某元素从游离态变为化合态,该元素一定被氧化
【答案】B
【详解】
A.钠和氯气点燃条件下反应生成氯化钠,该氧化还原反应中没有O元素参加,故A错误;
B.得电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂,故B正确;C. 中被氧化、被还原的元素都是Cl元素,故C错误;
D.氢气在氯气中点燃反应生成氯化氢,反应中氯气被还原、氢气被氧化,故D错误;
综上所述,答案为B。
【变2-1】(2020·天水市田家炳中学)有关氧化还原反应的说法正确的是
A.还原剂失去电子 B.氧化剂被氧化
C.氧化剂与还原剂不能是同种物质 D.还原剂被氧化生成还原产物
【答案】A
【详解】
A.还原剂失去电子化合价升高,被氧化, 选项A正确;
B.氧化剂得电子化合价降低,被还原,选项B错误;
C.同种物质可能既失去电子也得到电子,则在氧化还原反应中,氧化剂与还原剂可能是同一种物质,如
氯气与水的反应,选项C错误;
D.还原剂被氧化生成氧化产物,选项D错误;
答案选A。
【变2-2】(2020·荆州市北门中学高一期中)下列关于氧化还原反应说法正确的是
A.有化合价升降的反应,不一定是氧化还原反应
B.某元素从化合态变成游离态,该元素一定被还原
C.有单质参加或生成的反应不一定是氧化还原反应
D.得电子越多,其氧化性越强
【答案】C
【详解】
A.氧化还原反应中一定有元素化合价的变化,为氧化还原反应的特征,故A错误;
B.某元素从化合态变成游离态,可能是由正价降为0价,该元素一定被还原,也可能是从负价升为0价,
该元素被氧化,故B错误;
C.有单质参加或生成的反应不一定是氧化还原反应,如氧气和臭氧的转化,故C正确;
D.氧化性是指得电子能力的强弱,与得电子的多少没有必然联系,故D错误;
故选C。
【点睛】
本题考查氧化还原反应,侧重氧化还原反应基本概念的考查,明确反应中元素的化合价变化是氧化还原反
应的特征、氧化还原反应的本质是有电子的转移、在氧化还原反应中得电子的反应物作氧化剂,被还原,
失电子的反应物作还原剂,被氧化,易错点C,注意一些特殊形式的反应。【变2-3】(2021·吉林延边二中高一月考)关于氧化还原反应,下列说法正确的是( )
①氧化剂发生氧化反应②氧化剂具有氧化性③某元素在反应中由化合物转化为单质,该元素一定被氧化④
物质所含元素化合价是否发生变化是判断氧化还原反应的依据⑤失电子越多的还原剂,其还原性越强
A.①②④ B.②④ C.②③④ D.②④⑤
【答案】B
【详解】
①氧化剂化合价降低得电子,发生还原反应,故错误;
②氧化剂在反应中元素的化合价降低,得电子,具有氧化性,故正确;
③某元素在反应中由化合物转化为单质,该元素的化合价可能升高,也可能降低,元素可能被氧化,如Cl
﹣→Cl,也可能被还原,如Cu2+→Cu,故错误;
2
④存在元素化合价变化的反应是氧化还原反应,所以物质所含元素化合价变化是判断氧化还原反应的依据,
故正确;
⑤还原性与失电子能力有关,与失电子数多少无关,越易失电子,还原性越强,故错误;综上所述,②④
正确;
故选B。
题型三:氧化还原反应中的概念关系
【例3】(2021·全国高一课时练习)下列反应中,划线的物质发生氧化反应的是
A.Cu+2FeCl =2FeCl +CuCl B.CO+C 2CO
3 2 2 2
C.Fe O+2Al Al O+2Fe D.CO+NaOH=NaHCO
2 3 2 3 2 3
【答案】C
【详解】
A.Cu+2FeCl =2FeCl +CuCl 反应中,氯化铁中的铁元素化合价由+3降低为+2,得电子,发生还原反应,
3 2 2
故A不符合题意;
B.CO+C 2CO反应中,二氧化碳中的碳元素化合价由+4降低为+2价,得电子,发生还原反应,故B
2
不符合题意;C.Fe O+2Al Al O+2Fe反应中,铝元素化合价由0价升高为+3价,失电子,发生氧化反应,故C符
2 3 2 3
合题意;
D.CO+NaOH=NaHCO 该反应中元素化合价都未改变,不是氧化还原反应,故D不符合题意。
2 3
故选C。
【变3】(2021·全国高一课时练习)下列各反应中,氧化反应与还原反应在同种元素中进行的是
A.Cl+2NaOH=NaCl+NaClO+HO B.2KClO 2KCl+3O↑
2 2 3 2
C.2KMnO KMnO +MnO +O↑ D.2HO 2H↑+O↑
4 2 4 2 2 2 2 2
【答案】A
【详解】
A.一部分氯元素的化合价由0价升高到+1价,被氧化,同时还有一部分由0价降低到−1价,被还原,氧
化反应与还原反应均在氯元素中进行,选项A正确;
B.氯元素由+5价降低到−1价,被还原,氧元素由−2价升高到0价,被氧化,氧化反应与还原反应未在同
种元素中进行,选项B错误;
C.锰元素由+7价降低到+4价,被还原,氧元素由-2价升高到0价,被氧化,氧化反应与还原反应未在同
种元素中进行,选项C错误;
D.氢元素由+1价降低到0价,被还原,氧元素由−2价升高到0价,被氧化,氧化反应与还原反应未在同
种元素中进行,选项D错误。
答案选A。
【例4】(2020·嘉祥县第一中学高一月考)下列变化中,必须需要加入合适的氧化剂才能实现的是
A.KClO→O B.FeCl →FeCl C.CaCO →CO D.CuO→Cu
3 2 2 3 3 2
【答案】B
【详解】
A.KClO 受热分解生成O,反应过程中KClO 既做氧化剂又做还原剂,不需要加入氧化剂,故A不符合
3 2 3
题意;
B.铁元素由+2价变为+3价,被氧化,必须要加入氧化剂,故B符合题意;
C.CaCO 和盐酸反应可生成CO,属于非氧化还原反应,不需要加入氧化剂,故C不符合题意;
3 2
D.铜由+2价变为0价,被还原,必须要加入还原剂,故D不符合题意;答案选B。
【变4】下列转化过程中必须加入还原剂的是
A.N→NH B.Fe2+→Fe3+ C.NaSO →SO D.HO→HO
2 3 2 3 2 2 2 2
【答案】A
【分析】
在转化过程中需加入还原剂则其自身应作为氧化剂,元素的化合价应降低且自身不能发生歧化反应。
【详解】
A.N元素的化合价降低,为氧化剂,必须加入还原剂才能实现,A符合题意;
B.Fe元素的化合价升高,为还原剂,需加氧化剂才能实现,B不符合题意;
C.S元素的化合价不变,无需加还原剂也能实现,C不符合题意;
D.O元素的化合价降低,为氧化剂,应加还原剂才能实现或者发生歧化反应也能实现,D不符合题意;
故答案选A。
【例5】(2021·内蒙古包头·)宋代著名法医学家宋慈所著的《洗冤集录》中有“银针验毒”的记载。“银
针验毒”的原理是 ,下列有关该反应的说法正确的是
A. 发生氧化反应,是还原剂 B. 被氧化,是氧化剂
C.Ag发生氧化反应,是还原剂 D. 是还原产物
【答案】C
【详解】
A. 中的H元素、S元素的化合价都没有变化,则 既不是氧化剂也不是还原剂,没有发生氧化或
还原反应,故A错误;
B.氧元素由0价降低为-2价,化合价降低, 被还原,是氧化剂,故B错误;
C.银元素化合价由0价升高到+1价,化合价升高,发生氧化反应,是还原剂,故C正确;
D.Ag元素在反应中化合价升高,则Ag S为氧化产物,故D错误;
2
故选C。
【变5-1】(2021·江西九江·高一期末)除去FeCl 溶液中混有的少量FeCl ,可以向此溶液中通入过量的氯
3 2
气,发生如下反应:2FeCl +Cl=2FeCl 。对于该反应说法正确的是
2 2 3
A.属于氧化还原反应 B.属于复分解反应
C.Cl 作还原剂 D.Fe2+被还原
2【答案】A
【详解】
A.2FeCl +Cl=2FeCl 反应中铁、氯元素化合价有变化,属于氧化还原反应,故A正确;
2 2 3
B.2FeCl +Cl=2FeCl 是两种物质生成一种物质,属于化合反应,故B错误;
2 2 3
C.2FeCl +Cl=2FeCl 反应,Cl 中氯元素化合价降低,Cl 作氧化剂,故C错误;
2 2 3 2 2
D.2FeCl +Cl=2FeCl 反应,Fe元素化合价升高,Fe2+被氧化,故D错误;
2 2 3
选A。
【变5-2】(2021·青铜峡市高级中学高二开学考试)LiH是一种氢气发生剂,用于军事或其他需氢气的场
合。反应为:LiH+H O=LiOH+H ↑在这个反应中,说法正确的是
2 2
A.水是氧化剂,LiH是还原性 B.LiH是氧化剂,水是还原剂
C.LiH既是氧化剂又是还原剂 D.该反应是非氧化还原反应,不存在氧化剂和还原性
【答案】A
【详解】
A.LiH中H为-1价、化合价升高,HO中H为+1价、化合价降低,因此水是氧化剂,LiH是还原性,故
2
A正确;
B.根据A分析得到LiH是还原剂,水是氧化剂,故B错误;
C.根据A分析得到LiH是还原剂,故C错误;
D.该反应LiH中H化合价升高,HO中H化合价降低,是氧化还原反应,故D错误。
2
综上所述,答案为A。
【变5-3】(2020·临猗县临晋中学)氧化还原反应反应是重要的化学反应类型,仔细思考回答下列问题,
下列有水参与的反应①2Na+2HO=2NaOH+H↑ ②2NaO+2HO=4NaOH+O↑ ③NaO+
2 2 2 2 2 2 2
HO=2NaOH ④2HO 2H↑+O↑ ⑤2F+2HO=4HF+O
2 2 2 2 2 2 2
(1)其中不属于氧化还原反应的是____________(填编号)。
(2)在这些氧化还原反应中,水只作氧化剂的反应是_________(填编号);水只作还原剂的反应是______
(填编号);水既作氧化剂,又作还原剂是_______(填编号);水既不作氧化剂,又不作还原剂是
________(填编号)。
(3)根据你的理解,氧化还原反应的实质是____________
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得失或共用电子对的偏移 D.化合价的改变(4)请你运用所学知识分析3NO +HO= 2HNO +NO是否属于氧化还原反应?_____(填“是”或“不
2 2 3
是”),若是,这个反应的氧化剂是______,氧化产物是_________。
【答案】③ ① ⑤ ④ ② C 是 NO HNO
2 3
【分析】
有电子转移的化学反应是氧化还原反应,其特征是反应前后有元素化合价的变化,在化学反应中得电子化
合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂。
【详解】
①反应2Na+2HO=2NaOH+H ↑中,钠失电子作还原剂,水得电子作氧化剂,此反应是氧化还原反应;
2 2
②反应2NaO+2H O=4NaOH+O ↑中,过氧化钠既失电子又得电子,则过氧化钠既是氧化剂又是还原剂,
2 2 2 2
水中各元素的化合价都不变,则水既不是氧化剂又不是还原剂,但该反应是氧化还原反应;
③反应NaO+HO=2NaOH中各元素的化合价都不变,则不是氧化还原反应;
2 2
④反应2HO 2H↑+O ↑中氢元素得电子、氧元素失电子,则水既是氧化剂又是还原剂,此反应是氧化
2 2 2
还原反应;
⑤反应2F+2H O=4HF+O 中氟气得电子作氧化剂,水失电子作还原剂,是氧化还原反应;
2 2 2
(1)其中不属于氧化还原反应的是③;
(2)在这些氧化还原反应中,水只作氧化剂的反应是①;水只作还原剂的反应是⑤;水既作氧化剂,又作还
原剂是④;水既不作氧化剂,又不作还原剂是②;
(3)氧化还原反应的实质是电子转移,即电子的得失或共用电子对的偏移,故答案为C;
(4)反应3NO +H O=2HNO +NO中,二氧化氮中的N元素化合价是+4价,NO中N元素的化合价是+2价,
2 2 3
HNO 中N元素化合价是+5价,则该反应NO 中N元素部分化合价升高,部分化合价降低,故此反应是氧
3 2
化还原反应,且氧化剂和还原剂都是NO ,氧化产物为HNO。
2 3
【点睛】
考查氧化还原反应的判断,准确理解氧化还原反应的基本概念是解题关键,特别注意氧化还原反应的本质
是电子转移,而不是化合价的升降。
题型四:画双线桥与单线桥
【例6】(2020·平遥县综合职业技术学校)用双线桥法和单线桥法表示电子转移的方向和数目。
(1)WO+3H W+3H O_____________、_____________;
3 2 2(2)2HgO 2Hg+O↑______________、___________;
2
(3)H O+H S=2HO+S↓________________、_____________。
2 2 2 2
【答案】
【分析】
在用双线桥法表示电子转移时,箭头由反应物中的元素指向生成物中同一元素,在箭头上注明电子转移数
目及“得、失”字样;在用单线桥法表示时,箭头由还原剂中失去电子的元素指向氧化剂中得到电子的元
素,在箭头上根据还原剂注明电子转移数目。
【详解】
(1)在反应WO+3H W+3H O中,W元素化合价由反应前WO 中的+6价变为反应后W单质中的0价,化
3 2 2 3
合价降低,得到电子6e-,被还原;H元素化合价由反应前H 中的0价变为反应后HO中的+1价,化合价
2 2
升高,失去电子6×e-,被氧化,用双线桥法表示电子转移的方向和数目为: ;用
单线桥法表示电子转移的方向和数目为: ;
(2)在反应2HgO 2Hg+O↑中,Hg元素化合价由反应前HgO中的+2价变为反应后Hg单质中的0价,化合
2
价降低,得到电子2×2e-,被还原;O元素化合价由反应前HgO中的-2价变为反应后O 中的0价,化合价
2升高,失去电子2×2e-,被氧化,用双线桥法表示电子转移的方向和数目为: ;用单
线桥法表示电子转移的方向和数目为: ;
(3)在反应 HO+H S=2HO+S↓中,O元素化合价由反应前HO 中的-1价变为反应后HO中的-2价,化合
2 2 2 2 2 2 2
价降低,得到电子2×e-,被还原;S元素化合价由反应前HS中的-2价变为反应后S单质中的0价,化合
2
价升高,失去电子2e-,被氧化,用双线桥法表示电子转移的方向和数目为: ;用单
线桥法表示电子转移的方向和数目为 。
【点睛】
氧化还原反应中电子转移可以用双线桥法表示,也可以用单线桥法表示。双线桥法表示的是同一元素在反
应前后元素的化合价的变化及电子转移,既要注明电子转移数目,也要注明电子的“得、失”字样;而单
线桥法表示的是不同元素的原子之间的电子转移情况,箭头是由还原剂中失去电子的元素指向氧化剂中得
到电子的元素,因此只需注明电子转移数目,不必注明电子的“得、失”字样。
题型五:氧化还原反应综合训练
【例7】(2021·河北)一种借用 的转化,消除NH 、NO气体污染的途径如图所示。下列说
3
法正确的是A.反应①是一个非氧化还原反应
B.该过程的总反应可能为
C.利用上述转化有利于缓解温室效应
D.反应②中N 只是氧化产物
2
【答案】B
【详解】
A.反应①过程中有氧气生成,O元素的化合价在反应过程中发生变化,是一个氧化还原反应,故A错误;
B.由图示中的转化关系可知,该过程的总反应可能为 ,故B正确;
C.温室效应主要由二氧化碳引起的,上述转化过程中没有二氧化碳参与转化,不能改变大气中二氧化碳
的含量,不能缓解温室效应,故C错误;
D.由图示可知,反应②中反应物NH 、NO中的N元素化合价分别由-3价、+2价变为0价,氮元素的化
3
合价既升高又降低,则N 既是氧化产物又是还原产物,故D错误;
2
答案选B。
【例8】(2020·石家庄市第二十四中学高一月考)根据反应8NH +3Cl=6NHCl+N ,回答下列问题。
3 2 4 2
(1)氧化剂___________,还原剂___________;
(2)氧化产物___________,还原产物___________;
(3)用单线桥的方法表示该反应的电子转移情况___________。
(4)用双线桥的方法表示该反应的电子转移情况。___________。
(5)当有8个NH 分子参加反时,转移的电子个数为___________。
3
【答案】
(1) Cl NH
2 3
(2) N NH Cl
2 4(3)
(4)
(5)6
【分析】
该反应NH 中N元素化合价由-3价变为0价,化合价升高,所以氨气是还原剂,N 是氧化产物,氯气中氯
3 2
元素化合价由0价变为-1价,化合价降低,所以Cl 是氧化剂,NH Cl是还原产物。
2 4
(1)根据分析氧化剂为Cl,还原剂为NH ;
2 3
(2)根据分析氧化产物为N,还原产物为NH Cl;
2 4
(3)N元素化合价由-3价变为0价,化合价升高,每个氮原子失去3个电子,但只有两个氮原子化合价升
高,即失去6个电子,氯元素化合价由0价变为-1价,化合价降低,得到电子,用单线桥表示为:
;
(4)N元素化合价由-3价变为0价,化合价升高,每个氮原子失去3个电子,但只有两个氮原子化合价升
高,氯元素化合价由0价变为-1价,化合价降低,得到电子,用双线桥表示为: ;
(5)当有8个NH 参加反应时,化合价变化的NH 只有2个,N元素化合价由-3价变为0价,所以转移的
3 3
电子数目为6个。提分特训
【题1】(2021·西藏昌都市第三高级中学高一期末)下列反应进行分类时,既属于氧化还原反应又属于化
合反应的是
A.Zn+HSO =ZnSO +H↑ B.CaO+HO=Ca(OH)
2 4 4 2 2 2
C.2K(ClO) =2KCl+O↑ D.Cl +2FeCl = 2FeCl
3 2 2 2 3
【答案】D
【详解】
A.Zn+HSO =ZnSO +H↑反应中,锌失电子,硫酸得电子,是氧化还原反应,同时该反应还是置换反应,
2 4 4 2
不是化合反应,故A不选;
B.CaO+H O═Ca(OH) 符合“多变一”的形式,符合化合反应的特征,属于化合反应,但反应中没有元素化
2 2
合价的变化,不属于氧化还原反应,故B不选;
C.2K(ClO) =2KCl+O↑是分解反应,Cl、O元素的化合价发生变化,属于氧化还原反应,故C不选;
3 2
D.Cl+2FeCl =2FeCl 中Cl、Fe元素的化合价变化,属于氧化还原反应,且属于化合反应,故D选;
2 2 3
故选D。
【题2】下列说法正确的是
A.氧化还原反应一定有氧元素参加
B.氧化剂本身发生氧化反应
C.氧化反应一定先于还原反应发生
D.氧化还原反应一定有电子转移
【答案】D
【详解】
A.氧化还原反应中不一定有氧元素参加,如Cu与氯化铁的反应等,故A错误;
B.氧化剂在反应中被还原,发生还原反应,故B错误;
C.氧化反应与还原反应同时发生,不存在先后反应的顺序,故C错误;
D.氧化还原反应的本质是有电子的转移,故D正确;
故选D。
【题3】(2021·四川绵阳中学高一期中)下列有关氧化还原反应的叙述正确的是
A.金属单质在氧化还原反应中只能作还原剂,非金属单质只能作氧化剂
B.化合物中某元素处于最高价,则该元素只能被还原C.失电子越多的还原剂,其还原性越强
D.在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原
【答案】B
【详解】
A.金属无负价,金属单质化合价只能升高,只能作还原剂,但非金属有正价、有负价,非金属单质化合
价可升可降,既可作氧化剂也可作还原剂,A错误;
B.元素处于最高价,化合价只能降低,只能被还原,B正确;
C.还原性的强弱与失电子的数目无关,只与失电子的难易程度有关,C错误;
D.氧化还原反应中,可能同一种元素既被氧化,又被还原,D错误;
故选B。
【题4】(2020·湘南中学高二期中)从海水中可以提取溴的反应为2Br-+Cl=2Cl-+Br ,下列说法正确的是
2 2
A.溴元素化合价不变 B.Br 是还原剂
2
C.该反应不是氧化还原反应 D.该反应为置换反应
【答案】D
【分析】
在反应2Br-+Cl=2Cl-+Br 中,Cl元素的化合价从0价降低到-1价,Br元素的化合价从-1价升高到0价,由
2 2
此分析。
【详解】
A.根据分析,Br元素的化合价从-1价升高到0价,溴的化合价发生了变化,故A不符合题意;
B.根据分析,溴元素的化合价从-1价升高到0价,得到Br ,Br 是氧化产物,故B不符合题意;
2 2
C.根据分析,该化学反应有化合价的变化,属于氧化还原反应,故C不符合题意;
D.该反应为单质和化合物反应生成另一种单质和化合物的反应,属于置换反应,故D符合题意;
答案选D。
【题5】(2020·福建省泰宁第一中学高一月考)下列变化过程属于氧化反应的是。
A.HCl→H B.Mg→Mg2+
2
C.Cl-→AgCl D.CuO→Cu
【答案】B
【详解】
A.HCl→H 中氢元素化合价降低,得到电子,发生还原反应,A不选;
2
B.Mg→Mg2+中镁元素化合价升高,失去电子,发生氧化反应,B选;
C.Cl-→AgCl中元素的化合价均没有发生变化,不是氧化还原反应,C不选;D.CuO→Cu中铜元素化合价降低,得到电子,发生还原反应,D不选;
答案选B。
【题6】(2020·盘锦市第二高级中学高一月考)氧化还原反应中,水的作用可以是氧化剂、还原剂、既是
氧化剂又是还原剂、既不是氧化剂也不是还原剂等。下列反应与C+HO(g) CO+H 相比较,水的作
2 2
用相同的是( )
A.3Fe+4HO(g) Fe O+4H B.NaO+HO=2NaOH
2 3 4 2 2 2
C.2F+2HO=4HF+O D.3NO +HO=2HNO +NO
2 2 2 2 2 3
【答案】A
【分析】
反应C+HO(g) CO+H 水中H元素化合价下降做氧化剂,以此分析。
2 2
【详解】
A.该反应中水中H元素化合价下降做氧化剂,与反应C+HO(g) CO+H 中水的作用相同,故A正确;
2 2
B.该反应没有化合价的变化,为非氧化还原反应,故B错误;
C. .该反应中水中O元素化合价升高做还原剂,与反应C+HO(g) CO+H 中水的作用不同,故C错误;
2 2
D. 该反应中水中没有元素化合价有变化,既不做还原剂也不做氧化剂,与反应C+HO(g) CO+H 中
2 2
水的作用不同,故D错误。
故答案选:A。
【题7】(2021·河南)化学反应按照不同的分类方法,可以分为四大基本反应类型,离子反应和非离子反
应,氧化还原反应和非氧化还原反应等。回答下列问题:①2NaO+2CO=2Na CO+O ②2Mg+CO 2MgO+C
2 2 2 2 3 2 2
③AlCl +4NaOH=NaAlO +3NaCl+2HO ④Cl+2KI=2KCl+I
3 2 2 2 2
(1)上述反应中的单质被氧化的是___________(填序号,下同)。
(2)上述反应中无电子转移的是___________。
(3)上述反应中,属于氧化还原反应且不属于四大基本反应类型的是___________。
(4)写出一个满足下列条件的化学方程式,并用单线桥标出电子转移的方向和数目___________。
①是分解反应 ②是氧化还原反应 ③产物中有单质
【答案】② ③ ①
【详解】
(1)②2Mg+CO 2MgO+C,镁单质化合价升高,被氧化符合题意;
2
(2)③AlCl +4NaOH=NaAlO +3NaCl+2HO,反应中没有元素化合价发生变化,是非氧化还原反应,无电
3 2 2
子转移;
(3)①2Na O+2CO=2Na CO+O,氧元素化合价既有升又有降,属于氧化还原反应,且不属于四大基本反
2 2 2 2 3 2
应类型;
(4) ,由一种物质生成多种物质,是化合反应,并且有元素化合价变化
属氧化还原反应,还有单质生成,完全符合要求。
【题8】(2021·河北武强中学高一月考)(一)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也
永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:
2KNO+C+S=KS+2NO ↑+CO ↑。其中被还原的元素是_____,被氧化的元素是_____,氧化剂是_____,还
3 2 2 2
原剂是______
(二)已知铜在常温下能被稀HNO 溶解,反应为3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO。
3 3 3 2 2
(1)请将上述反应改写成离子方程式:______。
(2)氧化剂是______,还原剂是_______。(3)用双线桥法标出该反应的电子转移情况:_______。
(4)在参加反应的硝酸中,起氧化作用的HNO 与起酸性作用的HNO 的质量比为______。
3 3
【答案】N、S C KNO、S C 3Cu+8H++2 =3Cu2++2NO↑+4HO HNO Cu
3 2 3
1:3
【分析】
根据化合价的变化判断氧化还原反应中的对应项,化合价升高的元素是被氧化,所含元素的物质是还原剂;
降低的元素是被还原,所含元素的反应物是氧化剂;化合价的变化值即是得电子数、失电子数、转移电子
数。
【详解】
(一)根据元素的化合价变化判断:N元素由+5价降到+4价,S元素由0价降到-2价,故N、S元素被还原,
C元素的化合价由0价升为+4价,被氧化。含N、S元素的反应物做氧化剂,即是KNO、S,含化合价升
3
高的反应物做还原剂,是C;
(二)(1)根据单质、氧化物不能改写为离子,得出离子方程式为:3Cu+8H++2 =3Cu2+
+2NO↑+4HO;
2
(2)元素N由+5价变为+2价,故含氮的硝酸做氧化剂,Cu元素化合价由0升为+2价,Cu做为还原剂;
(3) 根据双线桥法的规则:
(4)根据变价元素N由+5价变为+2价有2个N,没有发生变化N有6个,故起氧化作用的HNO 与起酸性作
3
用的HNO 的质量比为1:3;
3
【点睛】
转移电子数等于化合价的升高总数等于化合价的降低总数,根据化合价的变化判断对应项。
【题9】(2020·广东)(1)分别用双线桥法标明下列反应的电子转移的方向和数目:① __________。
② __________。
(2)分别单线桥法标明下列反应的电子转移的方向和数目:
① __________。
② __________。
(3)写出下列反应的离子方程式。
① 和 溶液反应:__________。
② 溶液和 溶液反应:_________。
(4)写出 的电离方程式:_________。
【答案】
Fe+2Ag+=Fe2++2Ag Cu2++2OH-=Cu(OH) ↓ Fe (SO )=2Fe3++3
2 2 4 3
【详解】
(1)①在该反应中,Fe元素化合价由反应前Fe单质中0价变为反应后FeSO 中的+2价,化合价升高,失去
4
2e-;Cu元素的由反应前CuSO +2价变为反应后Cu中的0价,化合价降低,得到2e-,用双线桥法表示电
4
子转移为: ;
②在该反应中只有NaO 中的-1价的O元素的化合价发生变化。一部分失去电子变为反应后O 中的0价,
2 2 2一部分得到电子,变为反应后NaCO 中的-2价,电子转移数目为2×e-,用双线桥法表示电子转移为:
2 3
;
(2)①在该反应中,H元素化合价由反应前H 中的0价变为反应后HO中的+1价,化合价升高,失去电子
2 2
2×e-;Cu元素的由反应前CuO中的+2价变为反应后Cu中的0价,化合价降低2,得到2e-,用单线桥法表
示电子转移为: ;
②在该反应中,Na元素化合价由反应前Na单质中的0价变为反应后NaCl中的+1价,化合价升高,失去
电子2×e-;Cl元素的由反应前Cl 中的0价变为反应后NaCl中的-1价,化合价降低,得到2×e-,用单线桥
2
法表示电子转移为: ;
(3)①由于金属活动性Fe>Ag,所以Fe和AgNO 溶液发生反应,产生Fe(NO )、Ag,反应的离子方程式
3 3 2
为:Fe+2Ag+=Fe2++2Ag;
②CuSO 与NaOH溶液发生复分解反应产生Cu(OH) 、NaSO ,该反应的离子方程式为:Cu2++2OH-
4 2 2 4
=Cu(OH) ↓;
2
(3)Fe (SO ) 是盐,在水溶液中电离产生Fe3+、 ,物质电离方程式为:Fe (SO )=2Fe3++3 。
2 4 3 2 4 3
【题10】(2020·河北石家庄二中高一月考)回答下列问题
(1)根据反应8NH +3Cl=6NHCl+N
3 2 4 2
①氧化剂是___________还原剂是___________
②氧化剂与还原剂的质量之比为 ___________。
③当生成28gN 时被氧化的物质为 ___________g。
2
(2)高铁酸钠(Na FeO)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取: 2Fe(OH) +
2 4 3
4NaOH+3NaClO =2Na FeO+ 3NaCl+5H O
2 4 2
①该反应中氧化剂是 ___________(用化学式表示,下同),___________元素被氧化,还原产物为
___________。②用双线桥在方程式中标出电子转移的情况:___________
(3)化合价是学习氧化还原反应的基础。写出以下几种物质中加点元素的化合价。
H 2C2 O 4 ___________ NH 4 NO 3 ___________
【答案】
(1) Cl NH 213:34 34
2 3
(2) NaClO Fe NaCl
(3) +3 -3
【分析】
(1)
①在反应8NH +3Cl=6NHCl+N 中,氯元素的化合价从0价降低到-1价,得到电子,Cl 作氧化剂,氮元素
3 2 4 2 2
的化合价从-3价升高到0价,失去电子,NH 作还原剂。②当3mol氯气发生反应时,得到6mol电子,所
3
以参加反应的8mol氨气中只有2mol失去电子,所以氧化剂和还原剂的质量比为3mol×71g/
mol:2mol×17g/mol=213:34。③根据反应方程式和②的分析可知,当生成28g氮气时,被氧化的氨气为
34g。
(2)
①在2Fe(OH) + 4NaOH+3NaClO =2Na FeO+ 3NaCl+5H O中,氯元素的化合价从+1价降低到-1价,得到电
3 2 4 2
子,NaClO作氧化剂,被还原为NaCl,故NaCl是还原产物。铁元素的化合价从+3价升高到+6价,失去电
子,Fe元素被氧化。②在该反应中,铁元素的化合价从+3价升高到+6价,1mol Fe(OH) 失去3mol电子,
3
则2mol Fe(OH) 失去6mol电子;氯元素的化合价从+1价降低到-1价,1molNaClO得到2mol电子,则
3
3molNaClO得到6mol电子,用双线桥在方程式中标出电子转移的情况为:
。
(3)
在H 2C2 O 4 中,根据正负化合价代数和为0的原则,H为+1价,O为-2价,所以C为+3价。在NH 4 NO 3 中,中H为+1价,所以N为-3价。
提分作业
【练1】(2021·河南)下列反应中,属于氧化还原反应的是
A.
B.
C.
D.
【答案】D
【详解】
在题目涉及的反应中, 、 、
三个中元素化合价都不发生变化,因此反应属于非氧化还原反应;而
在反应 中Fe、O元素化合价发生了变化,因此该反应属于氧化还原反应,
故合理选项是D。
【练2】(2021·全国高一课时练习)下列反应属于氧化还原反应,且水既不作氧化剂又不作还原剂的是
A.2F+2H O=4HF+O
2 2 2
B.2NaO+2H O=4NaOH+O ↑
2 2 2 2
C.2HO+2Na=2NaOH+H ↑
2 2
D.2HO O↑+2H ↑
2 2 2
【答案】B【详解】
A.在反应2F+2HO=4HF+O 中,O元素化合价由-2价变为反应后O 中的0价,化合价升高,失去电子
2 2 2 2
被氧化,所以该反应属于氧化还原反应,HO作还原剂,A不符合题意;
2
B.在反应2NaO+2H O=4NaOH+O ↑中,只有NaO 中的O元素化合价部分升高变为O 的0价,部分降
2 2 2 2 2 2 2
低变为NaOH中的-2价,而HO的组成元素化合价不变,所以该反应属于氧化还原反应,且水既不作氧化
2
剂又不作还原剂,B符合题意;
C.在反应2HO+2Na=2NaOH+H ↑中,H元素的化合价由反应前HO的+1价变为反应后H 中的0价,化
2 2 2 2
合价降低,得到电子,被还原,所以该反应为氧化还原反应,HO为氧化剂,C不符合题意;
2
D.在该反应中水的组成元素H、O元素化合价都发生了变化,因此该反应属于氧化还原反应,水既作氧
化剂,又作还原剂,D不符合题意;
故合理选项是B。
【练3】(2020·镇江市实验高级中学高一期中)有关氧化还原反应的说法正确的是
A.在氧化还原反应中,金属单质只体现还原性,金属阳离子只体现氧化性
B.物质所含元素化合价变化是判断氧化还原反应的依据
C.在一个氧化还原反应中,有一种元素被氧化,必有另一种元素被还原
D.某元素在反应中由化合物转化为单质,该元素一定被氧化
【答案】B
【详解】
A.金属单质的最低化合价为0价,所以在化学反应中只体现还原性;变价金属阳离子既有氧化性又有还
原性,如 ,故A不选;
B.氧化还原反应的标志就是元素化合价的变化,故选B;
C.在一个氧化还原反应中,一种元素既可能被氧化有可能被还原,如 与 生成 和 中
O元素即氧化又被还原,故C不选;
D.某元素在反应中由化合物转化为单质,该元素即可被氧化有可能被还原,如 转化为Cu则Cu被还
原, 转化为 则C罗被氧化。
答案选B
【练4】(2020·盘锦市第二高级中学高一月考)周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环
惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu (OH) CO(碱式碳酸铜)。铜在潮湿的空气中生锈的
2 2 3化学反应为:2Cu+O +CO +H O=Cu (OH) CO。下列有关该反应的说法正确的是( )
2 2 2 2 2 3
A.该反应不是氧化还原反应
B.该反应中氧元素和碳元素化合价发生变化,所以是氧化还原反应
C.该反应中铜得电子,O 失电子,所以是氧化还原反应
2
D.该反应是氧化还原反应,变价的只有两种元素
【答案】D
【分析】
在反应2Cu+O +CO +H O=Cu (OH) CO 中,铜元素的化合价由0价变成+2价,失去电子,被氧化,氧元素
2 2 2 2 2 3
的化合价由0价变成-2价,得到电子,被还原,其余元素的化合价都没有发生变化,据此分析解答。
【详解】
A.在该反应中,铜元素的化合价由0价变成+2价,失去电子,被氧化,氧元素的化合价由0价变成-2价,
得到电子被还原,故该反应属于氧化还原反应,故A错误;
B.该反应中氧元素和铜元素化合价发生变化,碳元素化合价没有发生变化,是氧化还原反应,故B错误
C.根据分析,该反应中铜失电子,O 得电子,故C错误;
2
D.该反应是氧化还原反应,化合价发生改变的只有铜、氧两种元素,故D正确;
答案选D。
【练5】(宁夏回族自治区中卫市海原县第一中学2020-2021学年高一上学期第二次月考化学试题)下列变
化中,属于氧化反应的是
A.HNO→NO B.NaO→NaOH C.Fe→FeCl D.CO→C
3 2 3 2
【答案】C
【详解】
A.HNO→NO中氮元素的化合价降低,发生还原反应,故A不选;
3
B.NaO→NaOH中元素化合价没有发生变化,故B不选;
2
C.Fe→FeCl 中铁元素的化合价升高,发生氧化反应,故C选;
3
D.CO→C中碳元素的化合价降低,发生还原反应,故D不选;
2
故选:C。
【练6】(2021·务川仡佬族苗族自治县汇佳中学高一月考)下列变化中需要加入还原剂才能实现的是(
)
A.SO →SO B.H→HO
2 2 2
C.CO→CO D.Cl→Cl-
2 2
【答案】C【详解】
A.SO →SO 中硫元素化合价升高,则需要加入氧化剂才能实现,故A错误;
2
B.H→HO中氢元素化合价升高则需要加入氧化剂才能实现,所以B错误;
2 2
C.CO→CO中碳元素化合价降低,则需要加入还原剂才能实现,故C正确;
2
D.Cl→Cl-中氯元素的化合价降低,和氢氧化钠的反应中氯气既作氧化剂又作还原剂,所以加入氢氧化钠
2
也能实现,故D错误;
答案选C。
【练7】(2021·浙江高一月考)下列变化过程中,必须加入氧化剂才能实现的是
A.H→NaH B.HO→O C.NaClO→Cl D.CH→CO
2 2 2 2 2 4 2
【答案】D
【详解】
A.H→NaH中氢元素化合价降低,得到电子,必须加入还原剂才能实现,A不选;
2
B.HO→O 中可以利用双氧水的分解实现,B不选;
2 2 2
C.NaClO→Cl 中氯元素的化合价降低,得到电子,必须加入还原剂才能实现,C不选;
2
D.CH→CO 中碳元素的化合价升高,失去电子,必须加入氧化剂才能实现,D选;
4 2
答案选D。
【练8】(2021·三亚华侨学校高一开学考试)分析下列氧化还原反应,按要求填空
(1)C+2H SO (浓) CO↑+2SO↑+2H O氧化剂是_______(元素),化合价_______(填升高或降低),还原产物
2 4 2 2 2
是_______。
(2)NO+NO+2NaOH=2NaNO +H O还原剂是_______(物质),化合价_______(填升高或降低),氧化产物是
2 2 2
_______。
【答案】S 降低 SO NO 升高 NaNO
2 2
【详解】
(1) C+2H SO (浓) CO↑+2SO↑+2H O中,浓硫酸中S元素的化合价从 价降低到 价,2个S原子化合
2 4 2 2 2
价降低,化合价降低4价,所以浓硫酸是氧化剂,二氧化硫是还原产物;故答案为:S;降低;SO ;
2
(2) NO+NO +2NaOH=2NaNO +H O中NO中N的化合价从 价升高到 中的 价,化合价升高1价,
2 2 2
NO是还原剂, 是氧化产物;故答案为:NO;升高;NaNO 。
2【练9】(2020·河北师范大学田家炳中学高一月考)反应
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O,Mn元素的化合价由___________价变为___________价,
4 2 2 2
被___________;___________元素的原子失去电子,被___________;还原剂是___________,氧化剂是
___________。用双线桥标出电子转移的方向和数目:___________。
【答案】+7 +2 还原 Cl 氧化 HCl KMnO
4
【详解】
在反应2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O中,Mn元素的化合价由KMnO 中的+7价变为
4 2 2 2 4
MnCl 中的+2 价,被还原,KMnO 作氧化剂;HCl中Cl元素的化合价从-1价升高到Cl 中的0价,失去电
2 4 2
子,被氧化,HCl作还原剂。在反应2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O中,Mn元素的化合价
4 2 2 2
由+7价降低为+2 价,1molKMnO 得到5mol电子,则2molKMnO 得到10mol电子;HCl中Cl元素的化合
4 4
价从-1价升高到Cl 中的0价,1molHCl失去1mol电子,若参加反应的HCl为16mol,则失去电子的HCl
2
只有10mol,生成了5molCl ,失去了10mol电子。用双线桥标出电子转移的方向和数目为:
2
。
【练10】(2020·齐齐哈尔市第八中学校高一期中)(1)根据下列化学方程式填空。
①3S+6KOH KSO +2KS+3HO,氧化剂____,还原剂_____;
2 3 2 2
②2KMnO +16HCl(浓)=2KCl+2MnCl +8HO+5Cl↑,氧化剂___,被氧化的物质___。
4 2 2 2
(2)请把符合要求的化学反应方程式的编号填入括号内:是分解反应又是氧化还原反应的是____,是分解反
应不是氧化还原反应的是_____,是化合反应又是氧化还原反应的是_____,是化合反应不是氧化还原反应
的是_____,不属于四种基本反应类型的氧化还原反应的是_____。A.2KClO 2KCl+3O↑
3 2
B.2FeCl +Cl 2FeCl
2 2 3
C.NH HCO NH ↑+HO+CO↑
4 3 3 2 2
D.CaO+CO=CaCO
2 3
E.Cl +2NaOH=NaCl+NaClO+H O
2 2
(3)按要求分别用双线桥或单线桥标出下列反应中电子转移的情况。
①3NO +HO=2H++2 +NO(双线桥) _____。
2 2
②8NH +6NO 7N+12HO(单线桥) _____。
3 2 2 2
【答案】S S KMnO HCl A C B D E
4
【详解】
(1)①反应3S+6KOH KSO +2K S+3HO中S的化合价一部分从0价升高变为+4价发生氧化反应,一部分
2 3 2 2
从0价降低变为-2价发生还原反应,所以S单质既是氧化剂又是还原剂,答案:S;S;
②2KMnO +16HCl(浓)=2KCl+2MnCl +8H O+5Cl ↑反应中KMnO 中的Mn元素化合价由+7价降为+2价发生
4 2 2 2 4
还原反应,KMnO 是氧化剂;HCl中的Cl元素化合价由-1升高变为0价发生氧化反应,被氧化的物质是
4
HCl,答案:KMnO ;HCl;
4
(2)A.2KClO 2KCl+3O ↑属于分解反应,反应中元素Cl、O的化合价有变化,属于氧化还原反应;
3 2B.2FeCl +Cl 2FeCl 属于化合反应,反应中元素Fe、Cl的化合价有变化,属于氧化还原反应;
2 2 3
C.NHHCO NH ↑+H O+CO↑属于分解反应,反应中各元素的化合价没有变化,属于非氧化还原反应;
4 3 3 2 2
D.CaO+CO =CaCO 属于化合反应,反应中各元素的化合价没有变化,属于非氧化还原反应;
2 3
E.Cl +2NaOH=NaCl+NaClO+H O不属于四种基本反应类型,反应中元素Cl的化合价有变化,属于氧化还
2 2
原反应;
综上,是分解反应又是氧化还原反应的是A,是分解反应不是氧化还原反应的是C,是化合反应又是氧化
还原反应的是B,是化合反应不是氧化还原反应的是D,不属于四种基本反应类型的氧化还原反应的是
E,答案:A;C;B;D;E;
(3)①3NO +H O=2H++2 +NO中,NO 中的N元素的化合价一部分升高,一部分降低,3NO 参加反应
2 2 2 2
转移2mol电子,用双线桥表示为 ,答案: ;
②8NH +6NO 7N+12H O中,NH 中N元素化合价升高,NO 中N元素化合价降低,生成7N 转移
3 2 2 2 3 2 2
24mol电子,用单线桥表示为 ,答案:
。关注更新免费领取,淘宝唯一每月更新店铺:知二教育