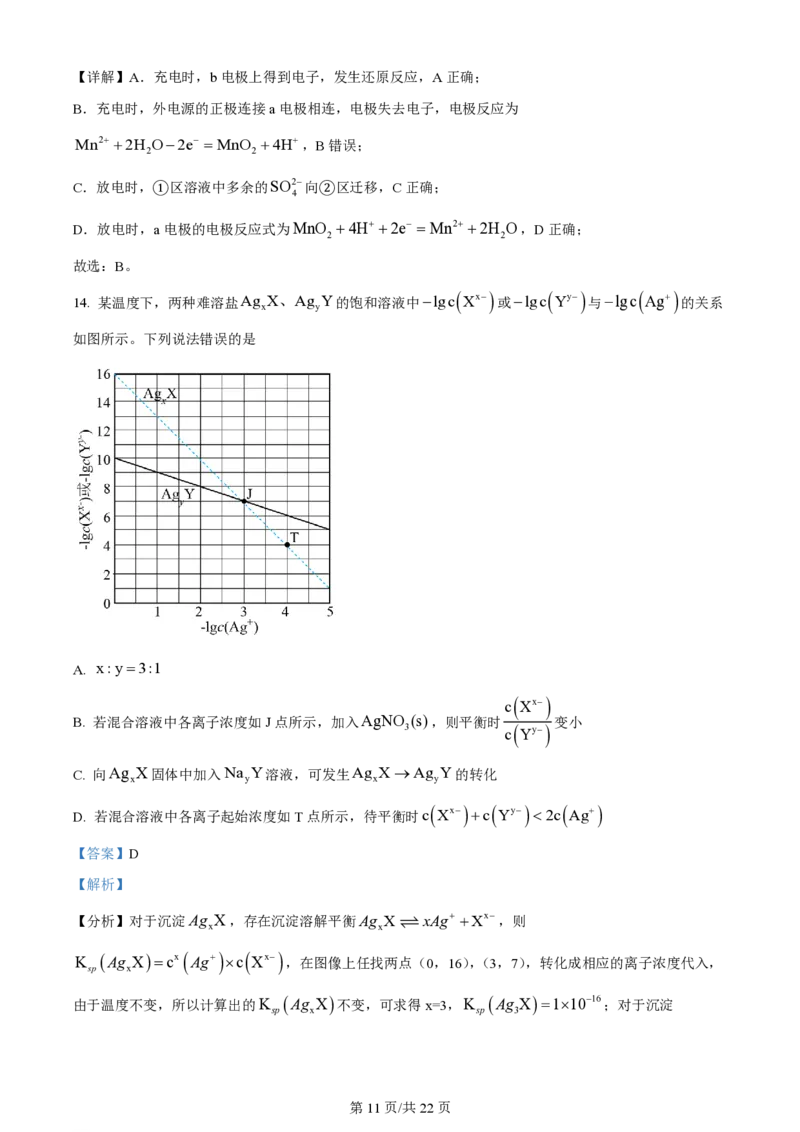
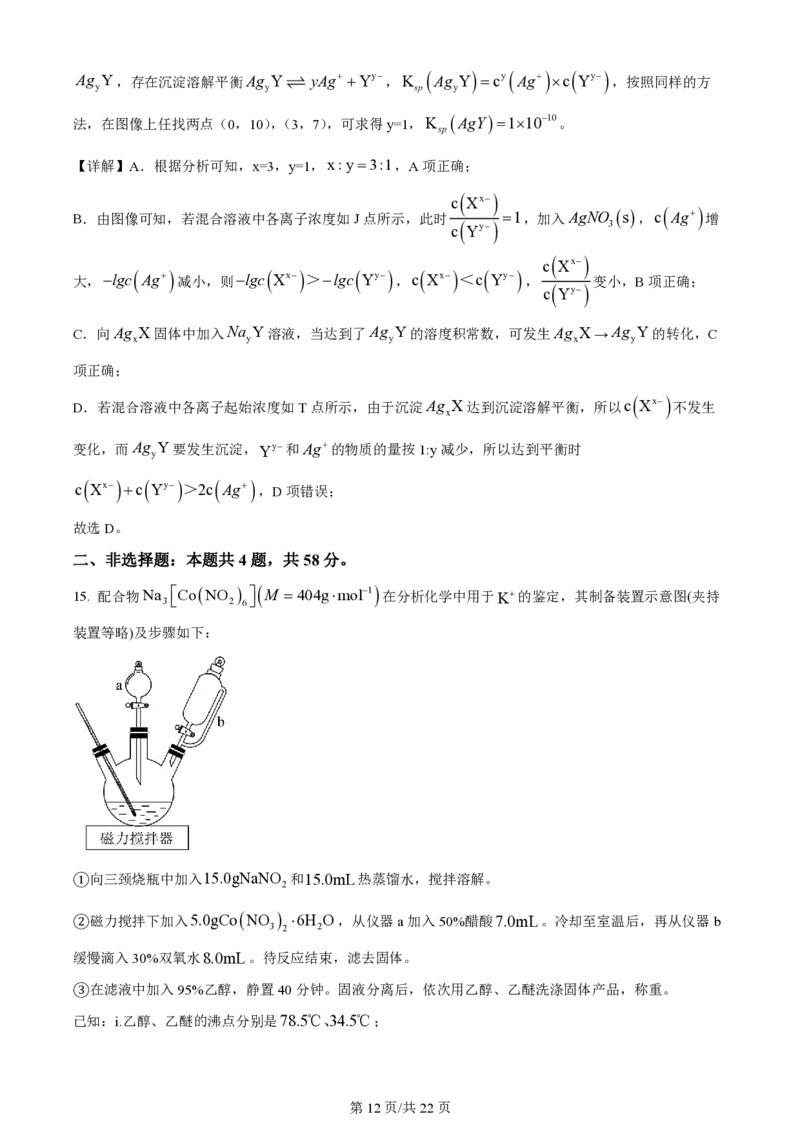
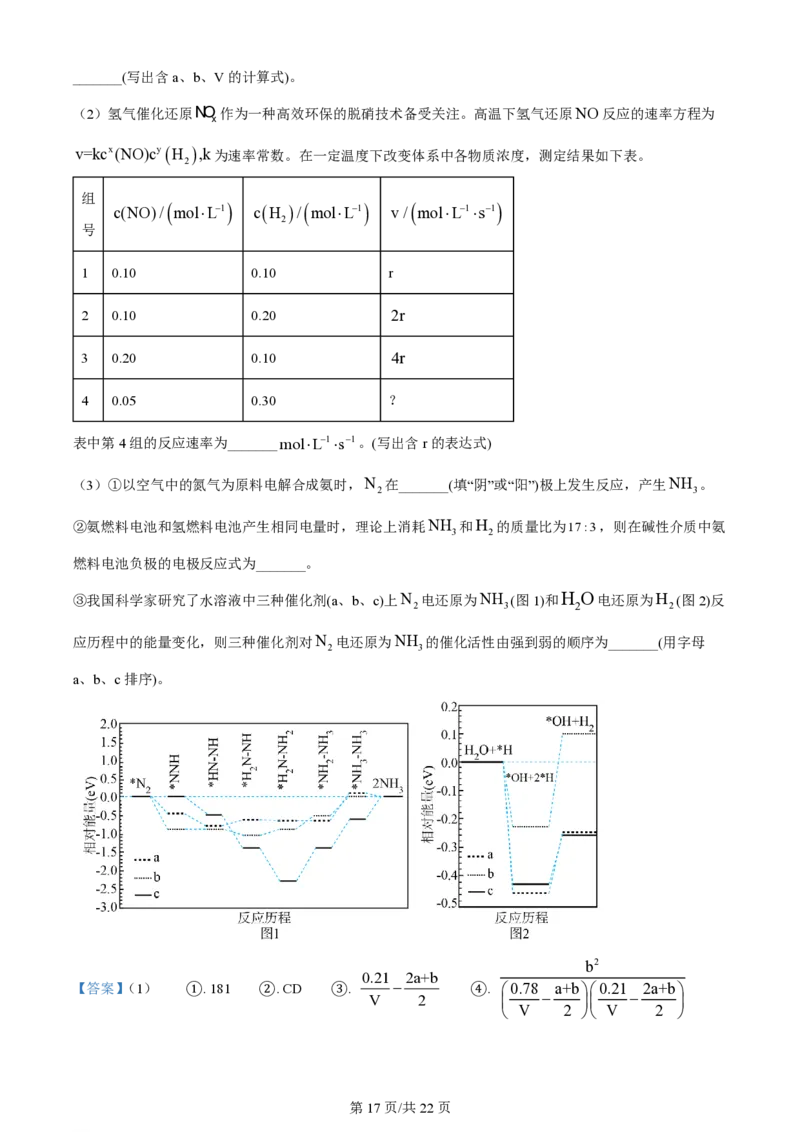
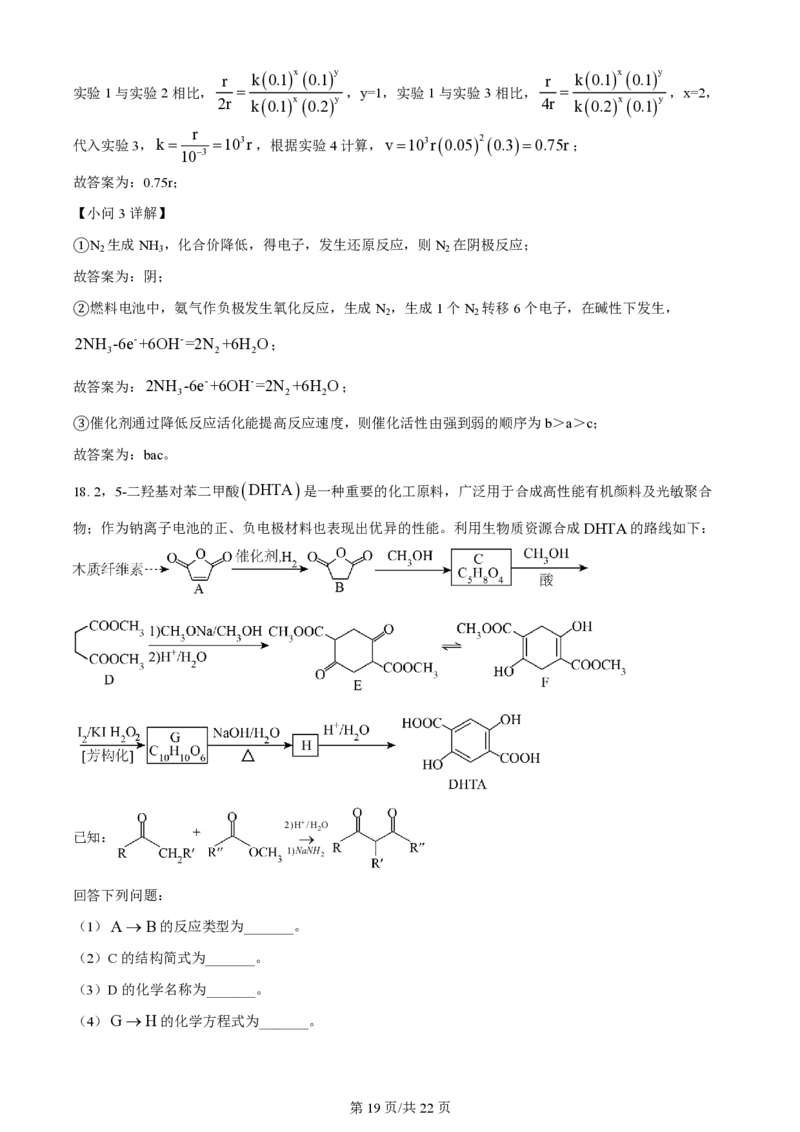
文档内容
机密★启用前
2023 年河北省普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改
动,用橡皮擦干净后,再选涂其他答案标号,回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
H1 N14 O16 Na23 K39 Co59 Zr91
可能用到的相对原子质量:
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 《本草纲目》中记载了粗食盐的一种制作过程:“取盐于池旁耕地沃以池水,每得南风急,则宿夕成
盐。”若将粗食盐在实验室提纯,不涉及的操作是
A. 溶解 B. 蒸发 C. 过滤 D. 蒸馏
【答案】D
【解析】
【详解】若将粗食盐在实验室提纯,需要将粗盐溶解,然后过滤除杂,接着蒸发结晶,不需要蒸馏,故
选:D。
2. 实验室根据化学试剂性质的不同采用不同的保存方法,下列说法错误的是
A. 浓硝酸保存在棕色试剂瓶中
B. 氢氧化钠溶液保存在带磨口玻璃塞的细口瓶中
C. 高锰酸钾和乙醇不能同时保存在同一药品柜中
D. 金属钠保存在煤油中
【答案】B
【解析】
【详解】A.浓硝酸见光易分解,少量浓硝酸保存在棕色细口瓶中,A正确;
B.氢氧化钠能与玻璃中的二氧化硅反应生成硅酸钠使玻璃粘连而打不开,故少量氢氧化钠溶液保存在带
橡胶塞的粗口试剂瓶中,B错误;
第1页/共22页
学科网(北京)股份有限公司C.乙醇具有挥发性,且乙醇可以和高锰酸钾发生氧化还原反应,所以乙醇和高锰酸钾不能同时保存在同
一个药品柜中,C正确;
D.金属钠的密度比煤油大且不与煤油反应,少量金属钠保存在煤油中,防止与空气中的氧气和水蒸气等
物质因接触而反应,D正确;
故答案选B。
3. 高分子材料在各个领域中得到广泛应用。下列说法错误的是
A. 聚乳酸可用于制造医用材料 B. 聚丙烯酰胺可发生水解反应
C. 聚丙烯可由丙烯通过缩聚反应合成 D. 聚丙烯腈纤维可由丙烯腈通过加聚反应合成
【答案】C
【解析】
【详解】A.聚乳酸具有良好的生物相容性和生物可吸收性,可以用于制造手术缝合线、药物缓释材料等
医用材料,A正确;
B.聚丙烯酰胺中含有酰胺基,可发生水解反应,B正确;
C.聚丙烯是由丙烯通过加聚反应合成的,C错误;
D.聚丙烯腈纤维是加聚产物,可由丙烯腈通过加聚反应合成,D正确;
故选C。
4. N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 1LpH=2的HCl溶液中含2N 个H+
A
B. 反应NaH+H O= NaOH+H 生成1molH ,转移N 个电子
2 2 2 A
C. 1mol6号元素的原子一定含有6N 个质子、6N 个中子
A A
D. 1mol组成为C H 的烃一定含有N 个双键
n 2n A
【答案】B
【解析】
【详解】A.pH=2即c H+ =10-2mol/L,故1LpH=2的HCl溶液中含H+的的数目为10-2N ,A错
A
误;
B.NaH+H O= NaOH+H 中H的化合价由-1和+1归中到0价,转移1个电子,故生成1molH ,
2 2 2
转移N 个电子,B正确;
A
C.6号元素为碳元素,碳定含有的质子数为6,但中子数却不一定为6,故1mol6号元素的原子一定含有
第2页/共22页
学科网(北京)股份有限公司6N 个质子、中子数不一定为6N ,C错误;
A A
D.通式C H 的有机物可能是单烯烃,也可能是环烷烃,为环烷烃时不含双键,D错误;
n 2n
故选B。
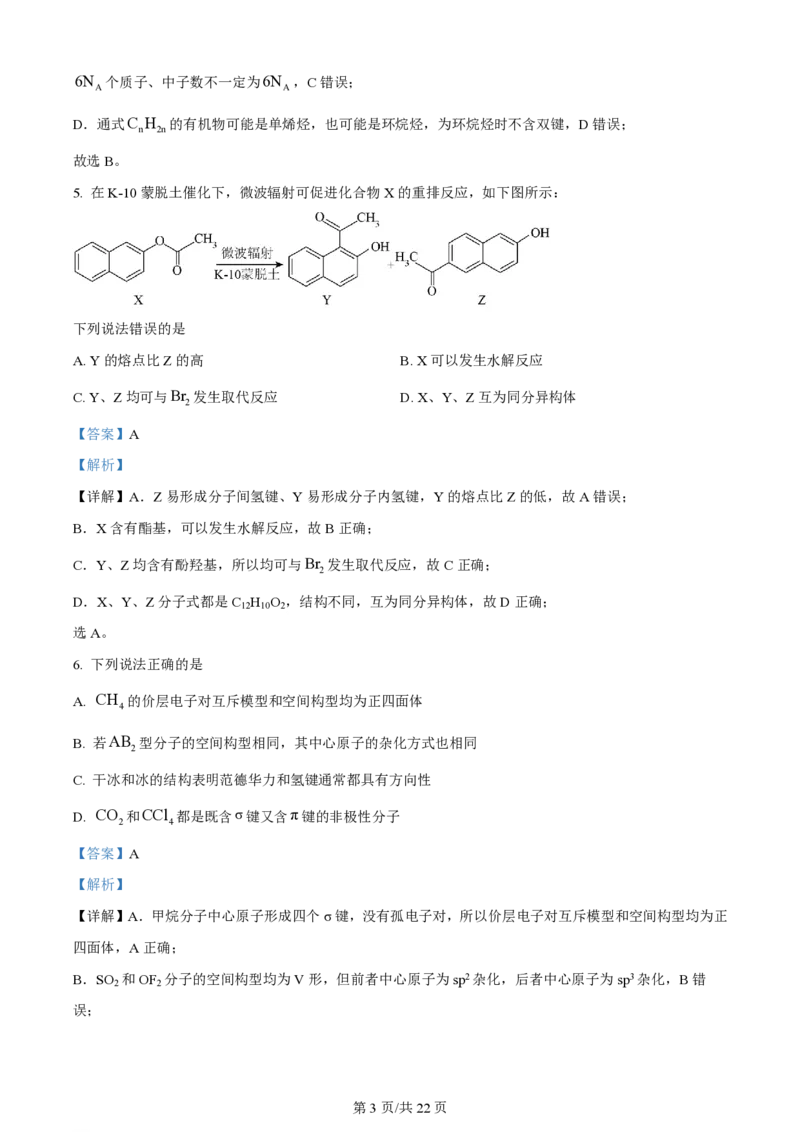
5. 在K-10蒙脱土催化下,微波辐射可促进化合物X的重排反应,如下图所示:
下列说法错误的是
A. Y的熔点比Z的高 B. X可以发生水解反应
C. Y、Z均可与Br 发生取代反应 D. X、Y、Z互为同分异构体
2
【答案】A
【解析】
【详解】A.Z易形成分子间氢键、Y易形成分子内氢键,Y的熔点比Z的低,故A错误;
B.X含有酯基,可以发生水解反应,故B正确;
C.Y、Z均含有酚羟基,所以均可与Br 发生取代反应,故C正确;
2
D.X、Y、Z分子式都是C H O ,结构不同,互为同分异构体,故D正确;
12 10 2
选A。
6. 下列说法正确的是
A. CH 的价层电子对互斥模型和空间构型均为正四面体
4
B. 若AB 型分子的空间构型相同,其中心原子的杂化方式也相同
2
C. 干冰和冰的结构表明范德华力和氢键通常都具有方向性
D. CO 和CCl 都是既含σ键又含π键的非极性分子
2 4
【答案】A
【解析】
【详解】A.甲烷分子中心原子形成四个σ键,没有孤电子对,所以价层电子对互斥模型和空间构型均为正
四面体,A正确;
B.SO 和OF 分子的空间构型均为V形,但前者中心原子为sp2杂化,后者中心原子为sp3杂化,B错
2 2
误;
第3页/共22页
学科网(北京)股份有限公司C.冰的结构是水分子通过氢键结合形成的有空隙的空间结构,表明了氢键通常具有方向性,干冰的结构
表现为分子密堆积,范德华力没有方向性,C错误;
D.CO 和CCl 都是极性键形成的非极性分子,CO 既含σ键又含π键而CCl 只含σ键不含π键,D错
2 4 2 4
误;
故选A。
7. 物质的结构决定其性质。下列实例与解释不相符的是
选项 实例 解释
A 用He替代H 填充探空气球更安全 He的电子构型稳定,不易得失电子
2
B BF 与NH 形成配合物 H N®BF BF 中的B有空轨道接受NH 中N的孤电子对
3 3 3 3 3 3
C 碱金属中Li的熔点最高 碱金属中Li的价电子数最少,金属键最强
D 不存在稳定的NF 分子 N原子价层只有4个原子轨道,不能形成5个N-F键
5
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.氢气具有可燃性,使用氢气填充气球存在一定的安全隐患,而相比之下,氦气是一种惰性气体,
不易燃烧或爆炸,因此使用电子构型稳定,不易得失电子的氦气填充气球更加安全可靠,故A正确;
B.三氟化硼分子中硼原子具有空轨道,能与氨分子中具有孤对电子的氮原子形成配位键,所以三氟化硼
能与氨分子形成配合物 H N®BF ,故B正确;
3 3
C.碱金属元素的价电子数相等,都为1,锂离子的离子半径在碱金属中最小,形成的金属键最强,所以
碱金属中锂的熔点最高,故C错误;
D.氮原子价层只有4个原子轨道,3个不成对电子,由共价键的饱和性可知,氮原子不能形成5个氮氟
键, 所以不存在稳定的五氟化氮分子,故D正确;
故选C。
8.
下图所示化合物是制备某些药物的中间体,其中W、X、Y、Z、Q均为短周期元素,且原子序数依次
增大,分子中的所有原子均满足稀有气体的稳定电子构型,Z原子的电子数是Q的一半。下列说法正确的
是
第4页/共22页
学科网(北京)股份有限公司A. 简单氢化物的稳定性:Z>Q B. 第一电离能:X>Y
C. 基态原子的未成对电子数:X>Q D. 原子半径:Z<W
【答案】A
【解析】
【分析】由W、X、Y、Z、Q均为短周期元素,且原子序数依次增大,分子中的所有原子均满足稀有气
体的稳定电子构型,Z原子的电子数是Q的一半,图中W含有1个化学键,原子序数最小,故W为H,X
含有4个共价键,故X为C,Z和Q都含2个共价键,且Z原子的电子数是Q的一半,故Z为O,Q为
S,Y含3个共价键,而且原子序数介于C和O之间,故Y为N,据此回答
【详解】A.非金属性:O>S,故简单氢化物的稳定性:Z(O)>Q(S),A正确;
B.同一周期从左到右第一电离能呈现增大的趋势,故第一电离能:Y(N)>X(C),B错误;
C.基态原子中C的未成对电子数为2个,S的未成对电子数也为2个,故基态原子的未成对电子数:
X(C)=Q(S),C错误;
D.原子半径为O>H,故原子半径:Z(O)>W(H),D错误;
故选A。
9. 由下列实验操作及现象,不能得出相应结论的是
选项 实验操作及现象 结论
A Cl 通入淀粉-KI溶液中,溶液变蓝 氧化性:Cl >I
2 2 2
B CO 通入苯酚钠溶液中,溶液变浑浊 酸性:碳酸>苯酚
2
C SO 通入品红溶液中,溶液褪色 SO 具有氧化性
2 2
D NH 通入滴有酚酞溶液的水中,溶液变红 氨水显碱性
3
A. A B. B C. C D. D
第5页/共22页
学科网(北京)股份有限公司【答案】C
【解析】
【详解】A.试纸变蓝是因为Cl 和KI反应生成I ,反应的化学方程式为Cl +2KI =I +2KCl,该反应
2 2 2 2
氧化性Cl >I ,A正确;
2 2
B.CO 通入苯酚钠溶液中生成苯酚微溶物,C H ONa+CO +H O=C H OH +NaHCO ,B正确;
2 6 5 2 2 6 5 3
C.SO 通入品红溶液,生成无色物质,不属于因氧化性褪色,C错误;
2
D.NH 3 与水反应NH 3 +H 2 O ƒ NH 3 ·H 2 O,溶液呈碱性,使酚酞变红,D正确;
故答案为:C。
10. 一种以锰尘(主要成分为Mn O ,杂质为铝、镁、钙、铁的氧化物)为原料制备高纯MnCO 的清洁生
2 3 3
产新工艺流程如下:
已知:室温下相关物质的K 如下表。
sp
Al(OH) Mg(OH) Ca(OH) Fe(OH) Fe(OH) Mn(OH) MgF CaF
3 2 2 2 3 2 2 2
10-32.9 10-11.3 10-5.3 10-16.3 10-38.6 10-12.7 10-10.3 10-8.3
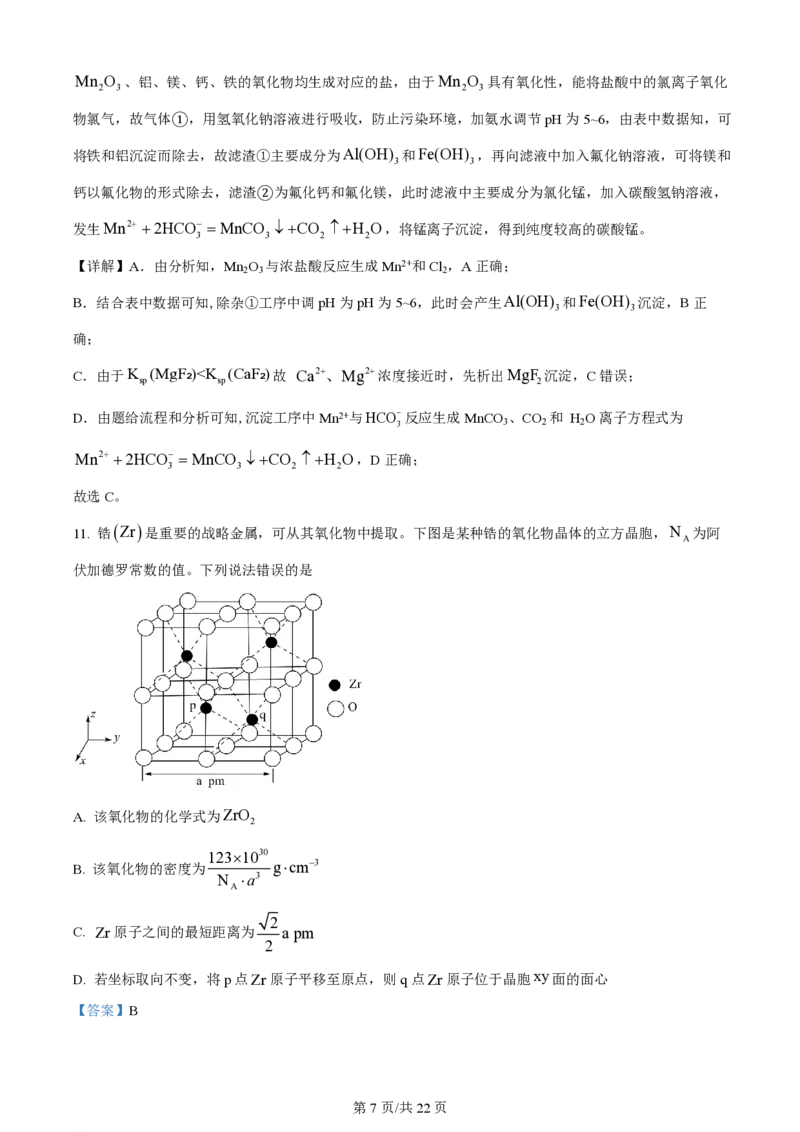
下列说法错误的是
A. 酸浸工序中产生的气体①为氯气
B. 滤渣①主要成分为Al(OH) 和Fe(OH)
3 3
C. 除杂②工序中逐渐加入NaF溶液时,若Ca2+、Mg2+浓度接近,则CaF 先析出
2
D. 沉淀工序中发生反应的离子方程式为Mn2+ +2HCO- =MnCO ¯+CO +H O
3 3 2 2
【答案】C
【解析】
【分析】由图知锰尘(主要成分为Mn O ,杂质为铝、镁、钙、铁的氧化物)加入浓盐酸进行酸浸,
2 3
第6页/共22页
学科网(北京)股份有限公司Mn O 、铝、镁、钙、铁的氧化物均生成对应的盐,由于Mn O 具有氧化性,能将盐酸中的氯离子氧化
2 3 2 3
物氯气,故气体①,用氢氧化钠溶液进行吸收,防止污染环境,加氨水调节pH为5~6,由表中数据知,可
将铁和铝沉淀而除去,故滤渣①主要成分为Al(OH) 和Fe(OH) ,再向滤液中加入氟化钠溶液,可将镁和
3 3
钙以氟化物的形式除去,滤渣②为氟化钙和氟化镁,此时滤液中主要成分为氯化锰,加入碳酸氢钠溶液,
发生Mn2+ +2HCO- =MnCO ¯+CO +H O,将锰离子沉淀,得到纯度较高的碳酸锰。
3 3 2 2
【详解】A.由分析知,Mn O 与浓盐酸反应生成Mn2+和Cl ,A正确;
2 3 2
B.结合表中数据可知,除杂①工序中调pH为pH为5~6,此时会产生Al(OH) 和Fe(OH) 沉淀,B正
3 3
确;
C.由于K (MgF₂)