文档内容
2024 年普通高等学校招生全国统一考试(甲卷)
理科综合能力测试
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,并将自己的姓名、准考证
号、座位号填写在本试卷上。
2.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑;如需
改动,用橡皮擦干净后,再选涂其他答案标号。涂写在本试卷上无效。
3.作答非选择题时,将答案书写在答题卡上,书写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Zn 65 Pb 207
一、选择题:本题共 13小题,每小题 6分,共 78分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 人类对能源的利用经历了柴薪、煤炭和石油时期,现正向新能源方向高质量发展。下列有关能源的叙述
错误的是
A. 木材与煤均含有碳元素 B. 石油裂化可生产汽油
C. 燃料电池将热能转化为电能 D. 太阳能光解水可制氢
2. 下列过程对应的离子方程式正确的是
A. 用氢氟酸刻蚀玻璃:SiO2-+4F-+6H+=SiF +3H O
3 4 2
B. 用三氯化铁溶液刻制覆铜电路板:2Fe3++3Cu=3Cu2++2Fe
C. 用硫代硫酸钠溶液脱氯:S O2-+2Cl +3H O=2SO2-+4Cl-+6H+
2 3 2 2 3
D. 用碳酸钠溶液浸泡锅炉水垢中的硫酸钙:CaSO +CO2-=CaCO +SO2-
4 3 3 4
3. 我国化学工作者开发了一种回收利用聚乳酸(PLA)高分子材料的方法,其转化路线如下所示。
下列叙述错误的是
A. PLA在碱性条件下可发生降解反应
B. MP的化学名称是丙酸甲酯
第1页/共9页
学科网(北京)股份有限公司C. MP的同分异构体中含羧基的有3种
D. MMA可加聚生成高分子
4. 四瓶无色溶液NH NO、Na CO、Ba(OH) 、AlCl ,它们之间的反应关系如图所示。其中a、b、
4 3 2 3 2 3
c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是
A. a呈弱碱性
B. f可溶于过量的b中
C. c中通入过量的e可得到无色溶液
D. b和d反应生成的沉淀不溶于稀硝酸
5. W、X、Y、Z为原子序数依次增大的短周期元素。W和X原子序数之和等于Y-的核外电子数,化合物
W+ZY - 可用作化学电源的电解质。下列叙述正确的是
6
A. X和Z属于同一主族
B. 非属性:X>Y>Z
C. 气态氢化物的稳定性:Z>Y
D. 原子半径:Y>X>W
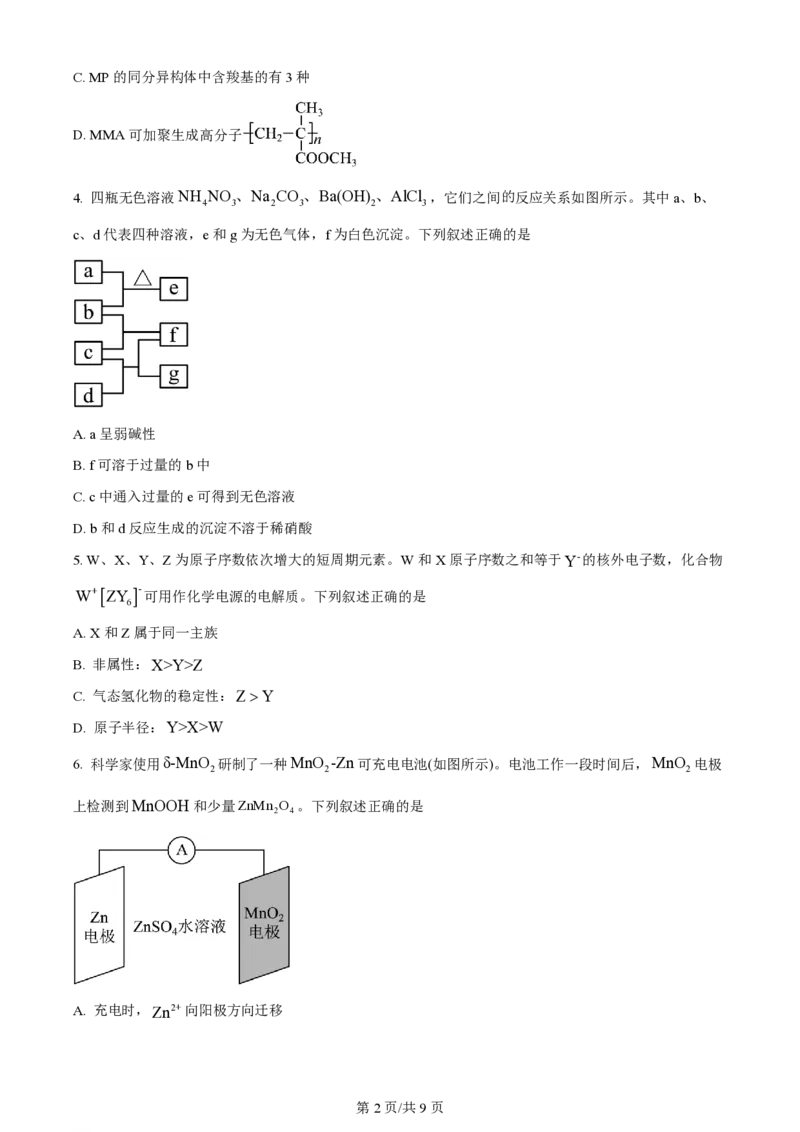
6. 科学家使用δ-MnO 研制了一种MnO -Zn可充电电池(如图所示)。电池工作一段时间后,MnO 电极
2 2 2
上检测到MnOOH和少量ZnMn O 。下列叙述正确的是
2 4
A. 充电时,Zn2+向阳极方向迁移
第2页/共9页
学科网(北京)股份有限公司B. 充电时,会发生反应Zn+2MnO =ZnMn O
2 2 4
C. 放电时,正极反应有MnO +H O+e-=MnOOH+OH-
2 2
D. 放电时,Zn电极质量减少0.65g,MnO 电极生成了0.020mol MnOOH
2
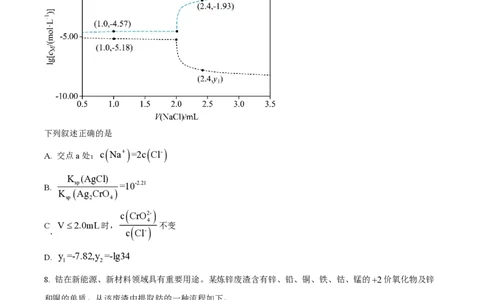
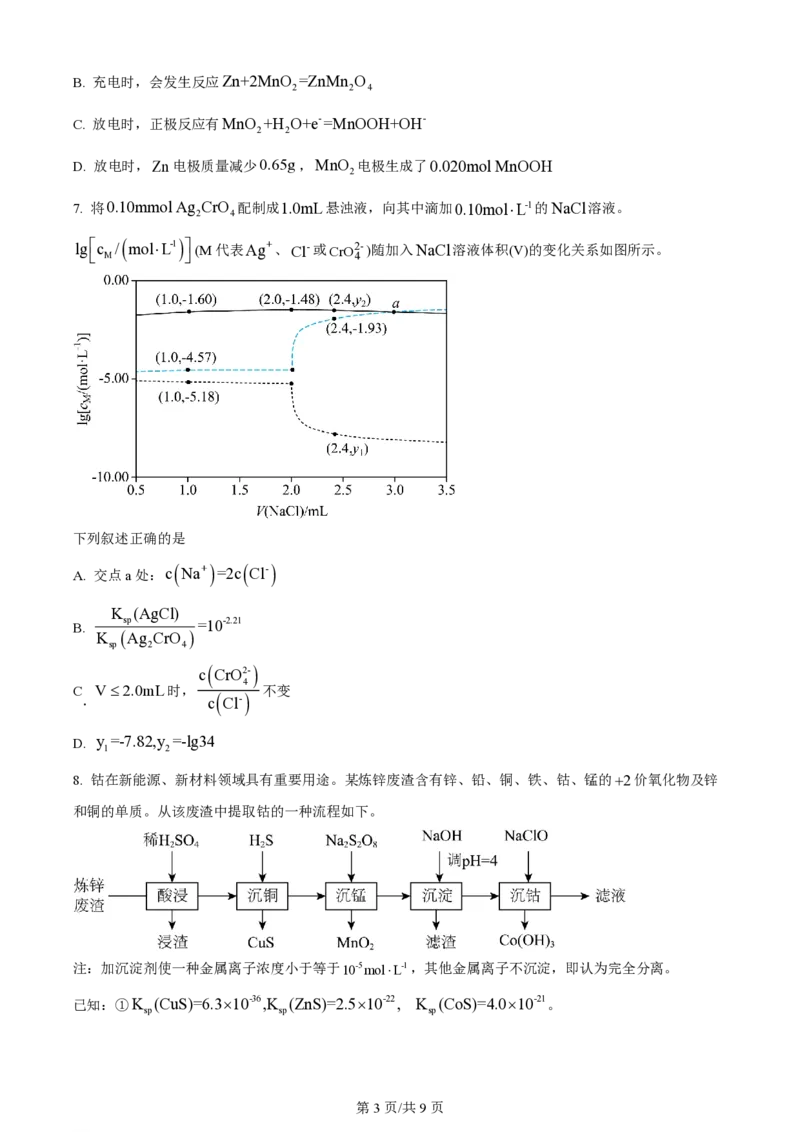
7. 将0.10mmol Ag CrO 配制成1.0mL悬浊液,向其中滴加0.10mol×L-1的NaCl溶液。
2 4
lgéc / mol×L-1ù (M代表Ag+、Cl-或CrO 2-)随加入NaCl溶液体积(V)的变化关系如图所示。
ë M û 4
下列叙述正确的是
A. 交点a处:c
Na+
=2c
Cl-
K (AgCl)
B.
sp =10-2.21
K Ag CrO
sp 2 4
c
CrO2-
4
C V£2.0mL时, 不变
.
c
Cl-
D. y =-7.82,y =-lg34
1 2
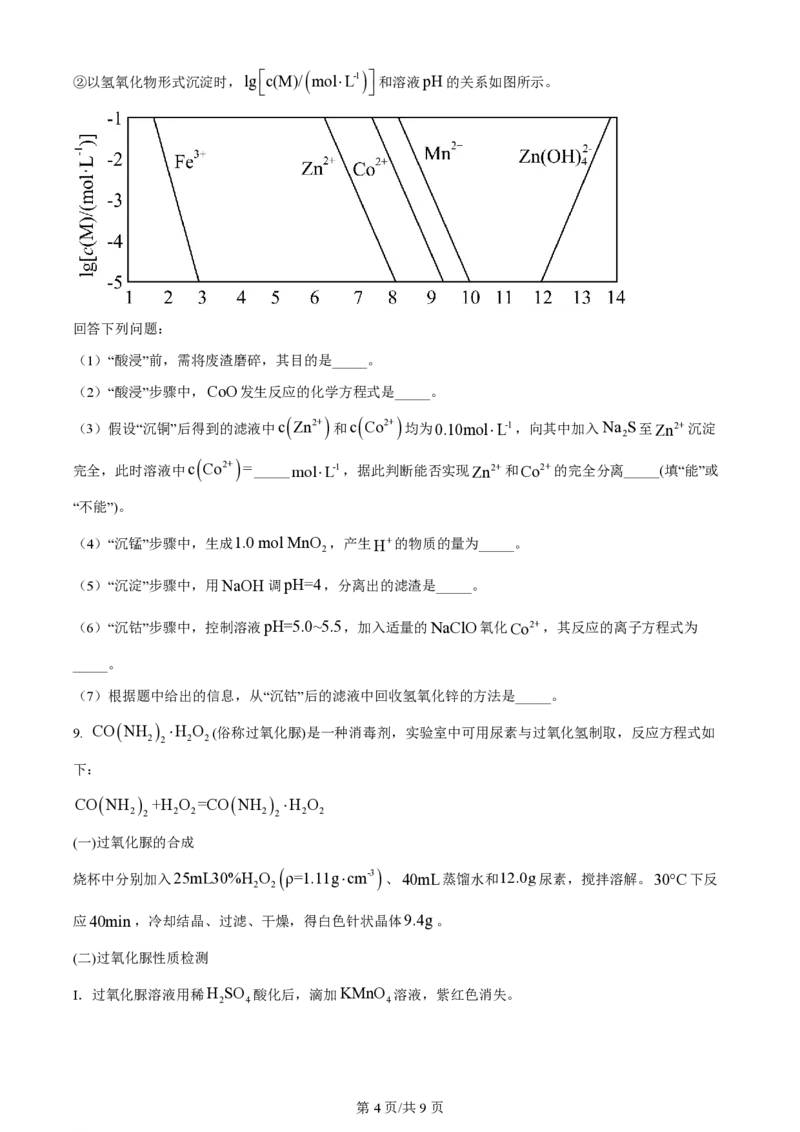
8. 钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的+2价氧化物及锌
和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于10-5mol×L-1,其他金属离子不沉淀,即认为完全分离。
已知:①K (CuS)=6.3´10-36,K (ZnS)=2.5´10-22, K (CoS)=4.0´10-21。
sp sp sp
第3页/共9页
学科网(北京)股份有限公司②以氢氧化物形式沉淀时,lgéc(M)/ mol×L-1ù和溶液pH的关系如图所示。
ë û
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是_____。
(2)“酸浸”步骤中,CoO发生反应的化学方程式是_____。
(3)假设“沉铜”后得到的滤液中c
Zn2+
和c
Co2+
均为0.10mol×L-1,向其中加入Na S至Zn2+沉淀
2
完全,此时溶液中c
Co2+
=_____mol×L-1,据此判断能否实现Zn2+和Co2+的完全分离_____(填“能”或
“不能”)。
(4)“沉锰”步骤中,生成1.0 mol MnO ,产生H+的物质的量为_____。
2
(5)“沉淀”步骤中,用NaOH调pH=4,分离出的滤渣是_____。
(6)“沉钴”步骤中,控制溶液pH=5.0~5.5,加入适量的NaClO氧化Co2+,其反应的离子方程式为
_____。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是_____。
9. CONH ×H O (俗称过氧化脲)是一种消毒剂,实验室中可用尿素与过氧化氢制取,反应方程式如
2 2 2 2
下:
CONH +H O =CONH ×H O
2 2 2 2 2 2 2 2
(一)过氧化脲的合成
烧杯中分别加入25mL30%H O
ρ=1.11g×cm-3
、40mL蒸馏水和12.0g尿素,搅拌溶解。30°C下反
2 2
应40min,冷却结晶、过滤、干燥,得白色针状晶体9.4g。
(二)过氧化脲性质检测
I.过氧化脲溶液用稀H SO 酸化后,滴加KMnO 溶液,紫红色消失。
2 4 4
第4页/共9页
学科网(北京)股份有限公司Ⅱ.过氧化脲溶液用稀H SO 酸化后,加入KI溶液和四氯化碳,振荡,静置。
2 4
(三)产品纯度测定
溶液配制:称取一定量产品,用蒸馏水溶解后配制成100mL溶液。
滴定分析:量取25.00mL过氧化脲溶液至锥形瓶中,加入一定量稀H SO ,用准确浓度的KMnO 溶液
2 4 4
滴定至微红色,记录滴定体积,计算纯度。
回答下列问题:
(1)过滤中使用到的玻璃仪器有_____(写出两种即可)。
(2)过氧化脲的产率为_____。
(3)性质检测Ⅱ中的现象为_____。性质检则I和Ⅱ分别说明过氧化脲具有的性质是_____。
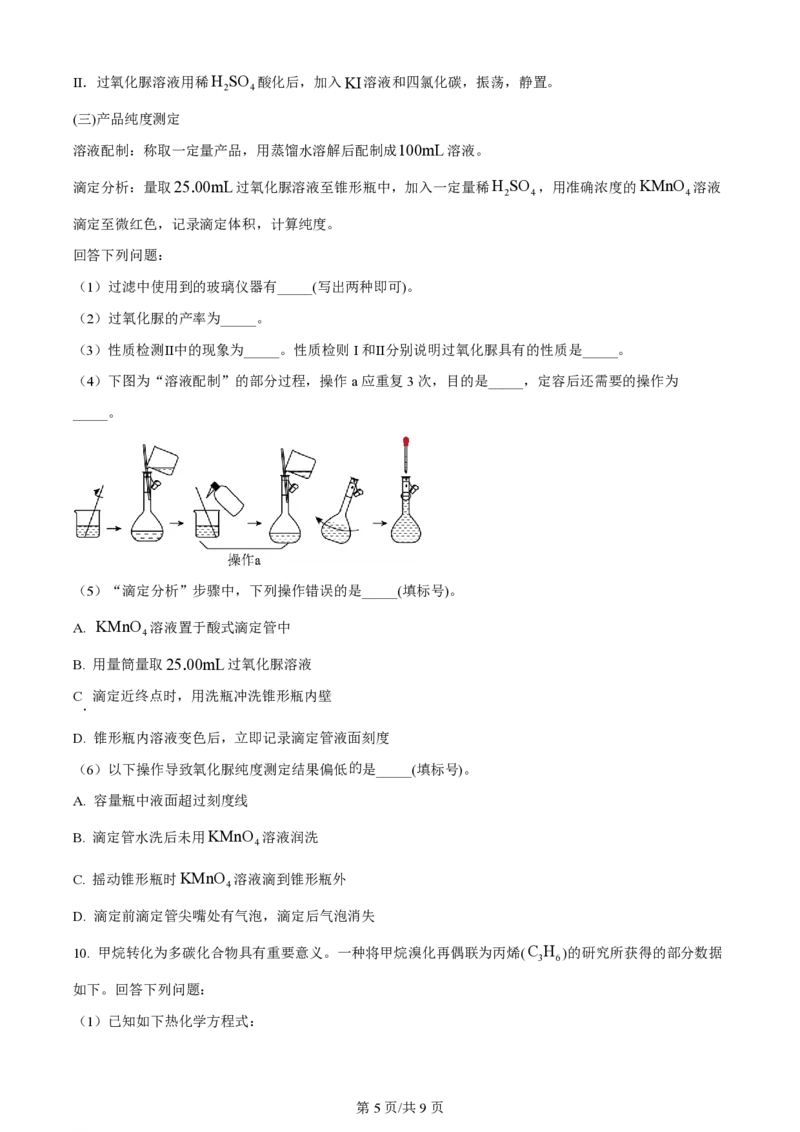
(4)下图为“溶液配制”的部分过程,操作a应重复3次,目的是_____,定容后还需要的操作为
_____。
(5)“滴定分析”步骤中,下列操作错误的是_____(填标号)。
A. KMnO 溶液置于酸式滴定管中
4
B. 用量筒量取25.00mL过氧化脲溶液
C 滴定近终点时,用洗瓶冲洗锥形瓶内壁
.
D. 锥形瓶内溶液变色后,立即记录滴定管液面刻度
(6)以下操作导致氧化脲纯度测定结果偏低的是_____(填标号)。
A. 容量瓶中液面超过刻度线
B. 滴定管水洗后未用KMnO 溶液润洗
4
C. 摇动锥形瓶时KMnO 溶液滴到锥形瓶外
4
D. 滴定前滴定管尖嘴处有气泡,滴定后气泡消失
10. 甲烷转化为多碳化合物具有重要意义。一种将甲烷溴化再偶联为丙烯(C H )的研究所获得的部分数据
3 6
如下。回答下列问题:
(1)已知如下热化学方程式:
第5页/共9页
学科网(北京)股份有限公司CH (g)+Br (g)=CH Br(g)+HBr(g) ΔH =-29kJ×mol-1
4 2 3 1
3CH Br(g)=C H (g)+3HBr(g) ΔH =+20kJ×mol-1
3 3 6 2
计算反应3CH (g)+3Br (g)=C H (g)+6HBr(g)的ΔH=_____kJ×mol-1。
4 2 3 6
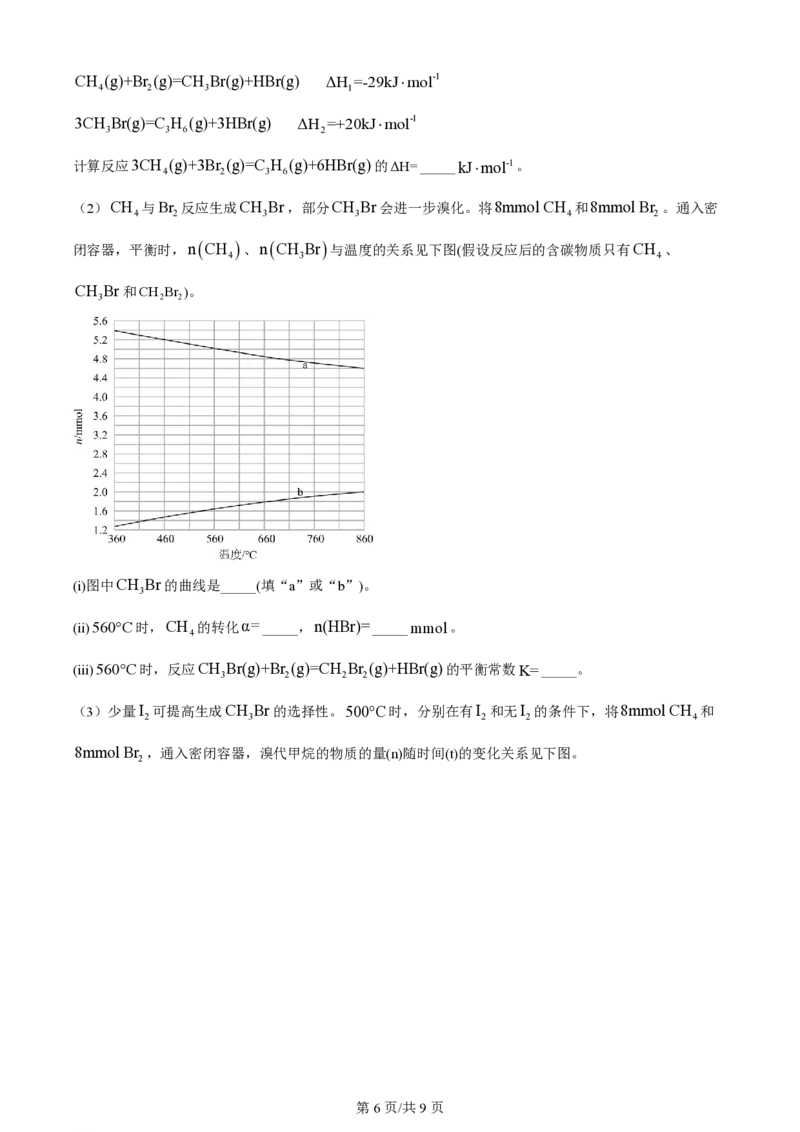
(2)CH 与Br 反应生成CH Br,部分CH Br会进一步溴化。将8mmol CH 和8mmol Br 。通入密
4 2 3 3 4 2
闭容器,平衡时,nCH 、nCH Br 与温度的关系见下图(假设反应后的含碳物质只有CH 、
4 3 4
CH Br和CH Br )。
3 2 2
(i)图中CH Br的曲线是_____(填“a”或“b”)。
3
(ii)560°C时,CH 的转化α=_____,n(HBr)=_____mmol。
4
(iii)560°C时,反应CH Br(g)+Br (g)=CH Br (g)+HBr(g)的平衡常数K=_____。
3 2 2 2
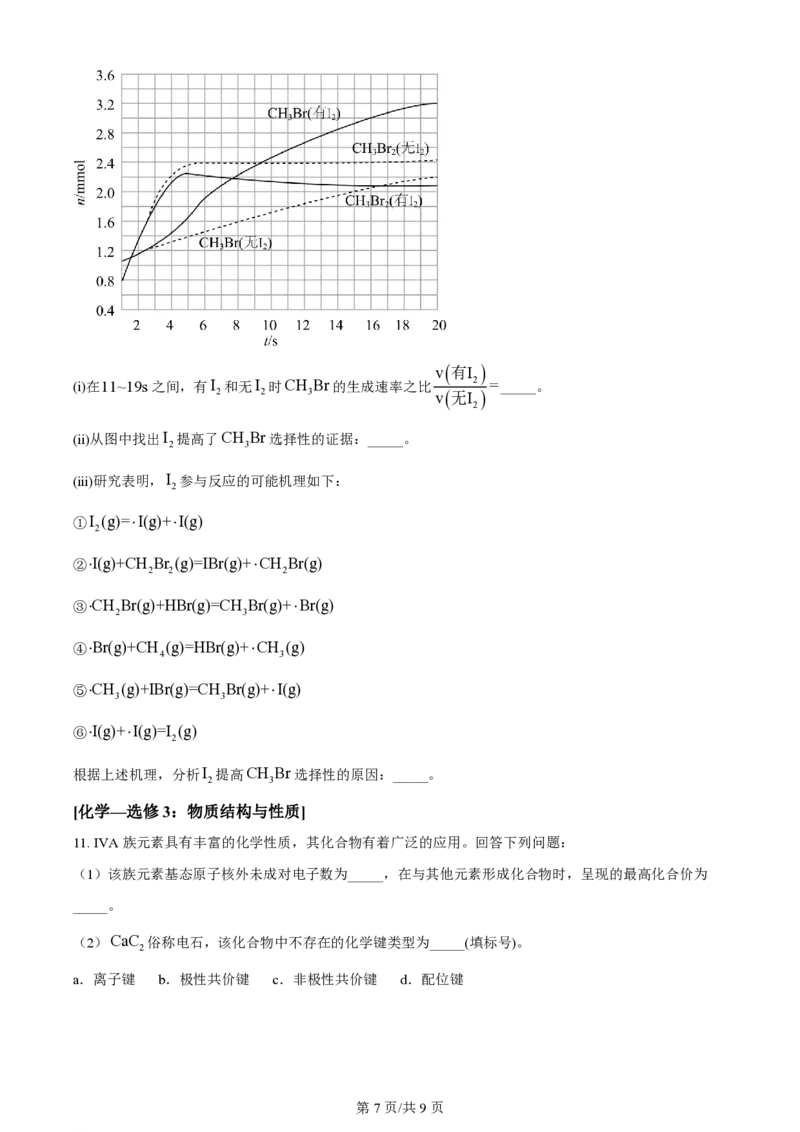
(3)少量I 可提高生成CH Br的选择性。500°C时,分别在有I 和无I 的条件下,将8mmol CH 和
2 3 2 2 4
8mmol Br ,通入密闭容器,溴代甲烷的物质的量(n)随时间(t)的变化关系见下图。
2
第6页/共9页
学科网(北京)股份有限公司v有I
(i)在11~19s之间,有I 和无I 时CH Br的生成速率之比 2 =_____。
2 2 3 v无I
2
(ii)从图中找出I 提高了CH Br选择性的证据:_____。
2 3
(ⅲ)研究表明,I 参与反应的可能机理如下:
2
①I (g)=×I(g)+×I(g)
2
②×I(g)+CH Br (g)=IBr(g)+×CH Br(g)
2 2 2
③×CH Br(g)+HBr(g)=CH Br(g)+×Br(g)
2 3
④×Br(g)+CH (g)=HBr(g)+×CH (g)
4 3
⑤×CH (g)+IBr(g)=CH Br(g)+×I(g)
3 3
⑥×I(g)+×I(g)=I (g)
2
根据上述机理,分析I 提高CH Br选择性的原因:_____。
2 3
[化学—选修 3:物质结构与性质]
11. ⅣA族元素具有丰富的化学性质,其化合物有着广泛的应用。回答下列问题:
(1)该族元素基态原子核外未成对电子数为_____,在与其他元素形成化合物时,呈现的最高化合价为
_____。
(2)CaC 俗称电石,该化合物中不存在的化学键类型为_____(填标号)。
2
a.离子键 b.极性共价键 c.非极性共价键 d.配位键
第7页/共9页
学科网(北京)股份有限公司(3)一种光刻胶薄膜成分为聚甲基硅烷 ,其中电负性最大的元素是_____,硅原子的杂化轨道类
型为_____。
(4)早在青铜器时代,人类就认识了锡。锡的卤化物熔点数据如下表,结合变化规律说明原因:_____。
物质 SnF SnCl SnBr SnI
4 4 4 4
熔点/°C 442 -34 29 143
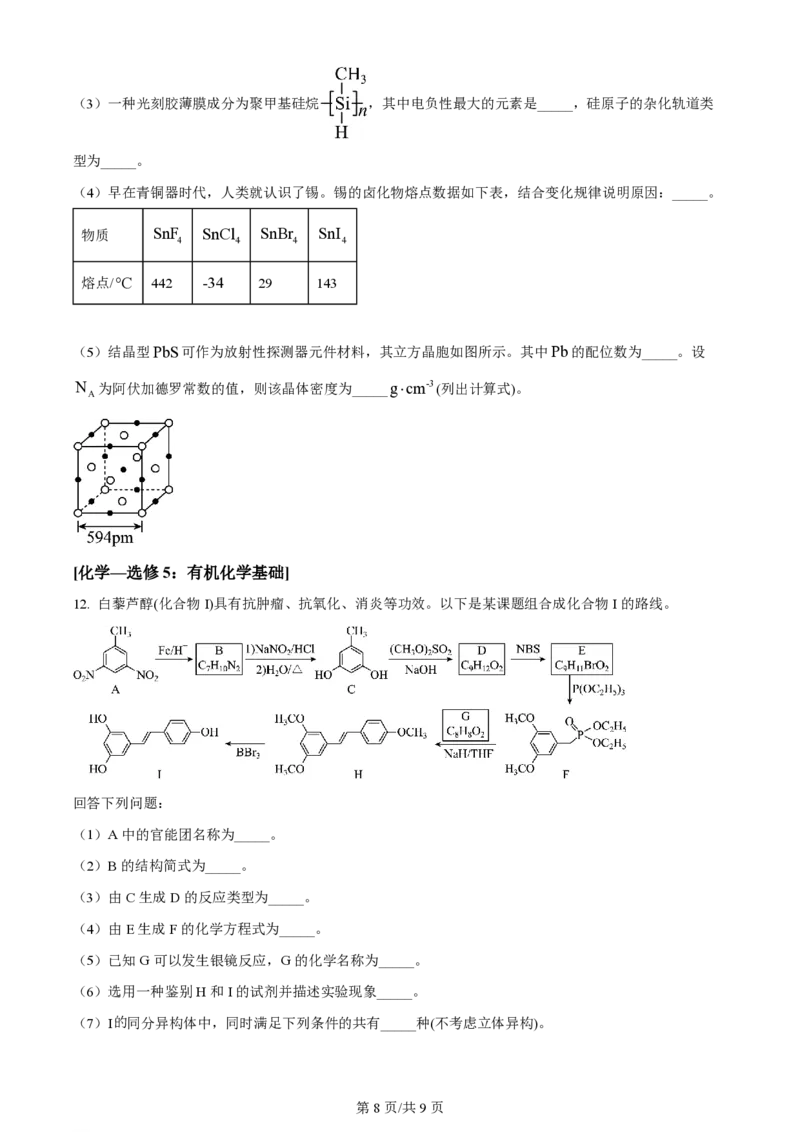
(5)结晶型PbS可作为放射性探测器元件材料,其立方晶胞如图所示。其中Pb的配位数为_____。设
N 为阿伏加德罗常数的值,则该晶体密度为_____g×cm-3(列出计算式)。
A
[化学—选修 5:有机化学基础]
12. 白藜芦醇(化合物I)具有抗肿瘤、抗氧化、消炎等功效。以下是某课题组合成化合物I的路线。
回答下列问题:
(1)A中的官能团名称为_____。
(2)B的结构简式为_____。
(3)由C生成D的反应类型为_____。
(4)由E生成F的化学方程式为_____。
(5)已知G可以发生银镜反应,G的化学名称为_____。
(6)选用一种鉴别H和I的试剂并描述实验现象_____。
(7)I的同分异构体中,同时满足下列条件的共有_____种(不考虑立体异构)。
第8页/共9页
学科网(北京)股份有限公司①含有手性碳(连有4个不同的原子或基团的碳为手性碳);
②含有两个苯环;③含有两个酚羟基;④可发生银镜反应。
第9页/共9页
学科网(北京)股份有限公司