文档内容
2024 年普通高等学校招生全国统一考试
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 K 39 Mn 55 Fe 56
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 《天工开物》记载:软浆车榨蔗汁,一石(dàn)汁下石灰五合,取汁煎糖,冷凝成黑沙,黄泥水淋下成白
糖。下列说法错误的是
A. 石灰可中和蔗汁中的酸性物质 B. “冷凝成黑沙”是结晶过程
C. “黄泥水淋下”的目的是脱色 D. “白糖”的主要成分是葡萄糖
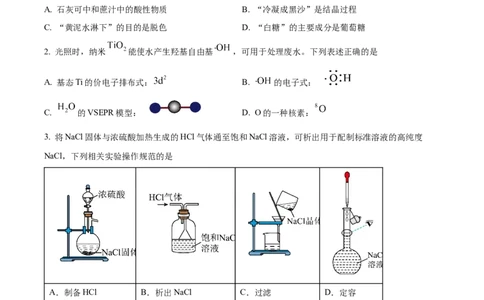
2. 光照时,纳米 能使水产生羟基自由基 ,可用于处理废水。下列表述正确的是
A. 基态Ti的价电子排布式: B. 的电子式:
C. 的VSEPR模型: D. O的一种核素:
3. 将NaCl固体与浓硫酸加热生成的HCl气体通至饱和NaCl溶液,可析出用于配制标准溶液的高纯度
NaCl,下列相关实验操作规范的是
A.制备HCl B.析出NaCl C.过滤 D.定容
A. A B. B C. C D. D
4. 6-硝基胡椒酸是合成心血管药物奥索利酸的中间体,其合成路线中的某一步如下:
第1页/共11页
学科网(北京)股份有限公司下列有关X和Y的说法正确的是
A. 所含官能团的个数相等 B. 都能发生加聚反应
C. 二者中的所有原子共平面 D. 均能溶于碱性水溶液
5. 白磷 是不溶于水的固体,在空气中易自燃。下列有关白磷的说法错误的是
A. 分子中每个 原子的孤电子对数均为1
B. 常保存于水中,说明白磷密度大于
C. 难溶于水,是因为水是极性分子, 是非极性分子
D. 熔点低,是因为 分子内的 键弱
6. 化学与生活息息相关。下列离子方程式书写正确的是
A. 用 溶液处理水垢中的
B. 明矾用于净水:
C. 抗酸药中的 可治疗胃酸过多:
D. 用酸化的KI淀粉溶液检验加碘盐中的
7. 如图所示的铼配合物离子能电催化还原 。短周期元素 的原子序数依次增大。标准
状况下,WY和 是等密度的无色气体, 是黄绿色气体。下列说法错误的是
A. 第一电离能: B. 图中X原子的杂化方式为
C. 元素以原子的形态与 配位 D. Y的电负性大于 中的化学键是极性键
8. 某小组对 和 的性质进行探究:
第2页/共11页
学科网(北京)股份有限公司Ⅰ.向少量蒸馏水里滴加2滴 溶液,再滴加2滴KSCN溶液。
Ⅱ.向少量蒸馏水里滴加2滴 溶液,再滴加2滴KSCN溶液。
下列说法正确的是
A. 实验Ⅰ中继续加入少量 固体,溶液颜色变浅
B. 实验Ⅱ中溶液呈红色
C. KSCN能区分 和
D. 焰色试验不能区分 和
9. 某新型钠离子二次电池(如图)用溶解了NaPF 的二甲氧基乙烷作电解质溶液。放电时嵌入PbSe中的Na
6
变成Na+后脱嵌。下列说法错误的是
A. 外电路通过1mol电子时,理论上两电极质量变化的差值为23g
B. 充电时,阳极电极反应为:
C. 放电一段时间后,电解质溶液中的Na+浓度基本保持不变
D. 电解质溶液不能用NaPF 的水溶液替换
6
10. 烯烃进行加成反应的一种机理如下:
此外,已知实验测得 与 进行加成反应的活化能依次减
小。下列说法错误的是
A. 乙烯与HCl反应的中间体为
第3页/共11页
学科网(北京)股份有限公司B. 乙烯与氯水反应无 生成
C. 卤化氢与乙烯反应的活性:
D. 烯烃双键碳上连接的甲基越多,与 的反应越容易
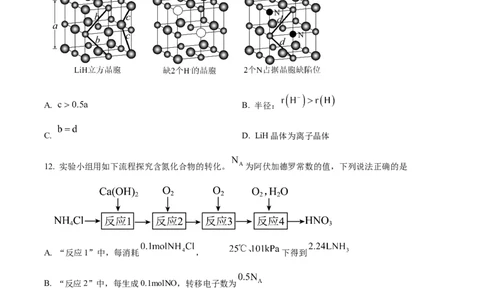
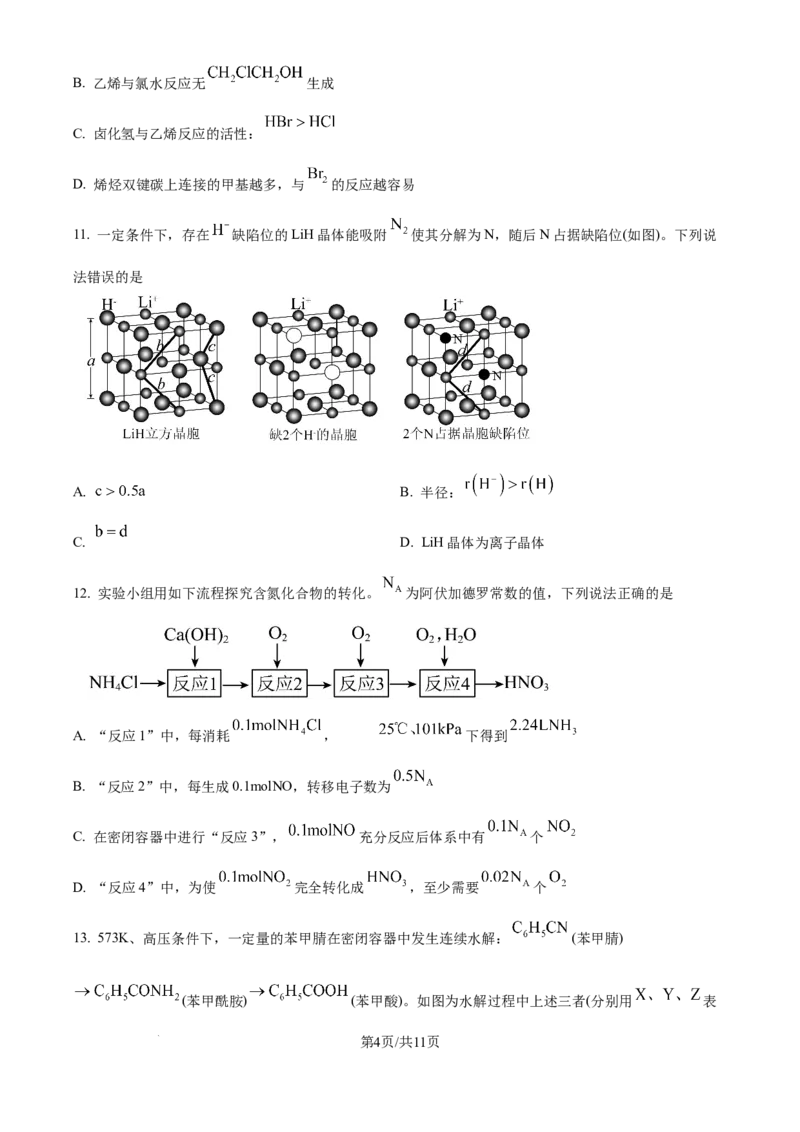
11. 一定条件下,存在 缺陷位的LiH晶体能吸附 使其分解为N,随后N占据缺陷位(如图)。下列说
法错误的是
A. B. 半径:
C. D. LiH晶体为离子晶体
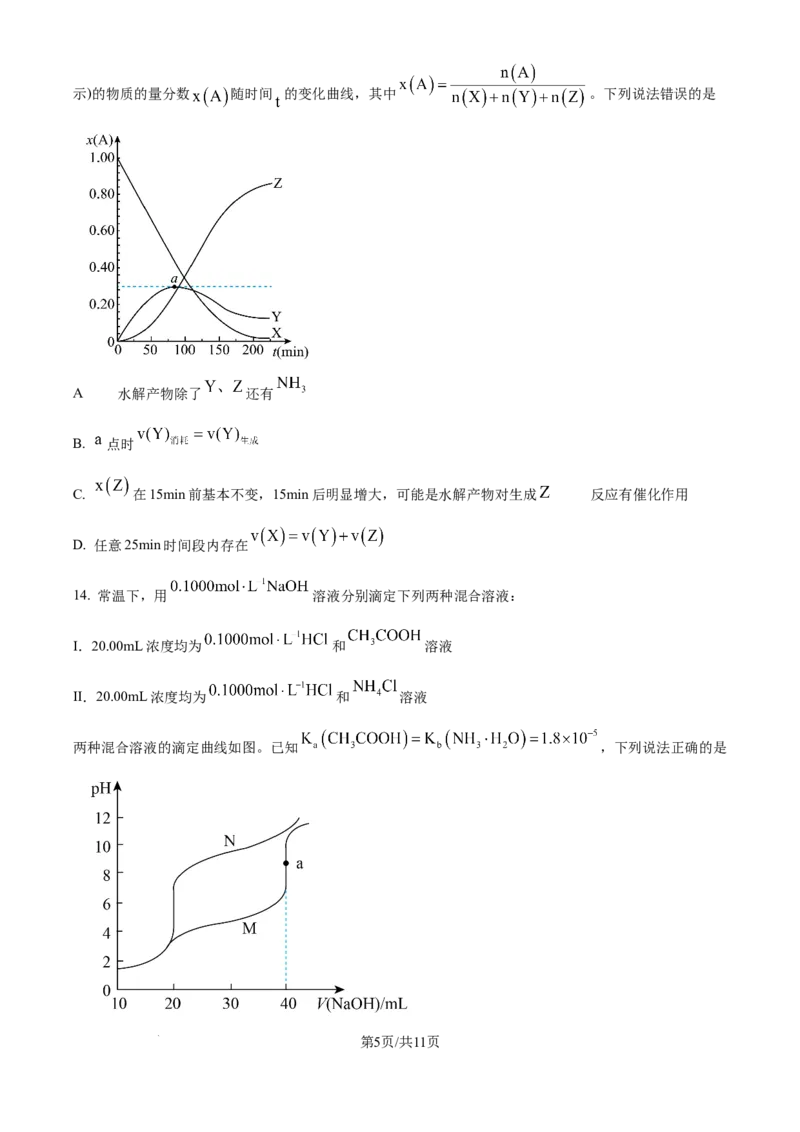
12. 实验小组用如下流程探究含氮化合物的转化。 为阿伏加德罗常数的值,下列说法正确的是
在
A. “反应1”中,每消耗 , 下得到
B. “反应2”中,每生成0.1molNO,转移电子数为
C. 在密闭容器中进行“反应3”, 充分反应后体系中有 个
D. “反应4”中,为使 完全转化成 ,至少需要 个
13. 573K、高压条件下,一定量的苯甲腈在密闭容器中发生连续水解: (苯甲腈)
(苯甲酰胺) (苯甲酸)。如图为水解过程中上述三者(分别用 表
第4页/共11页
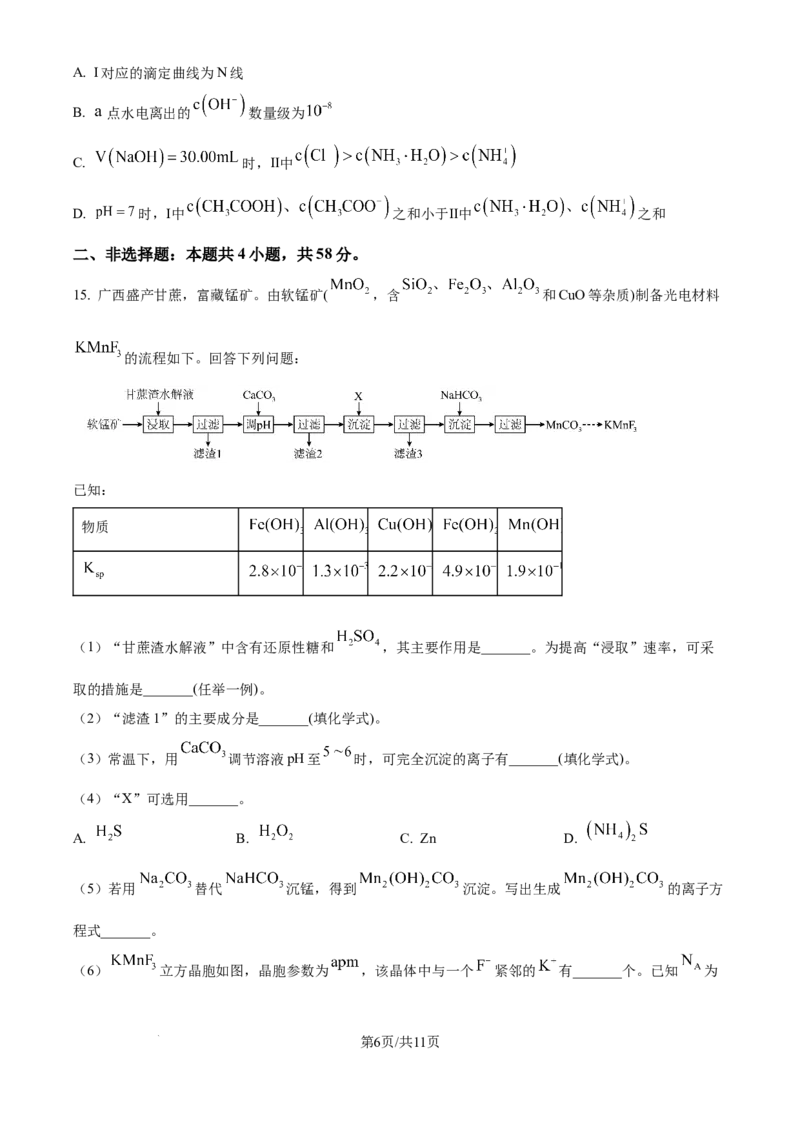
学科网(北京)股份有限公司示)的物质的量分数 随时间 的变化曲线,其中 。下列说法错误的是
.
A 水解产物除了 还有
B. 点时
C. 在15min前基本不变,15min后明显增大,可能是水解产物对生成 的反应有催化作用
D. 任意25min时间段内存在
14. 常温下,用 溶液分别滴定下列两种混合溶液:
Ⅰ.20.00mL浓度均为 和 溶液
Ⅱ.20.00mL浓度均为 和 溶液
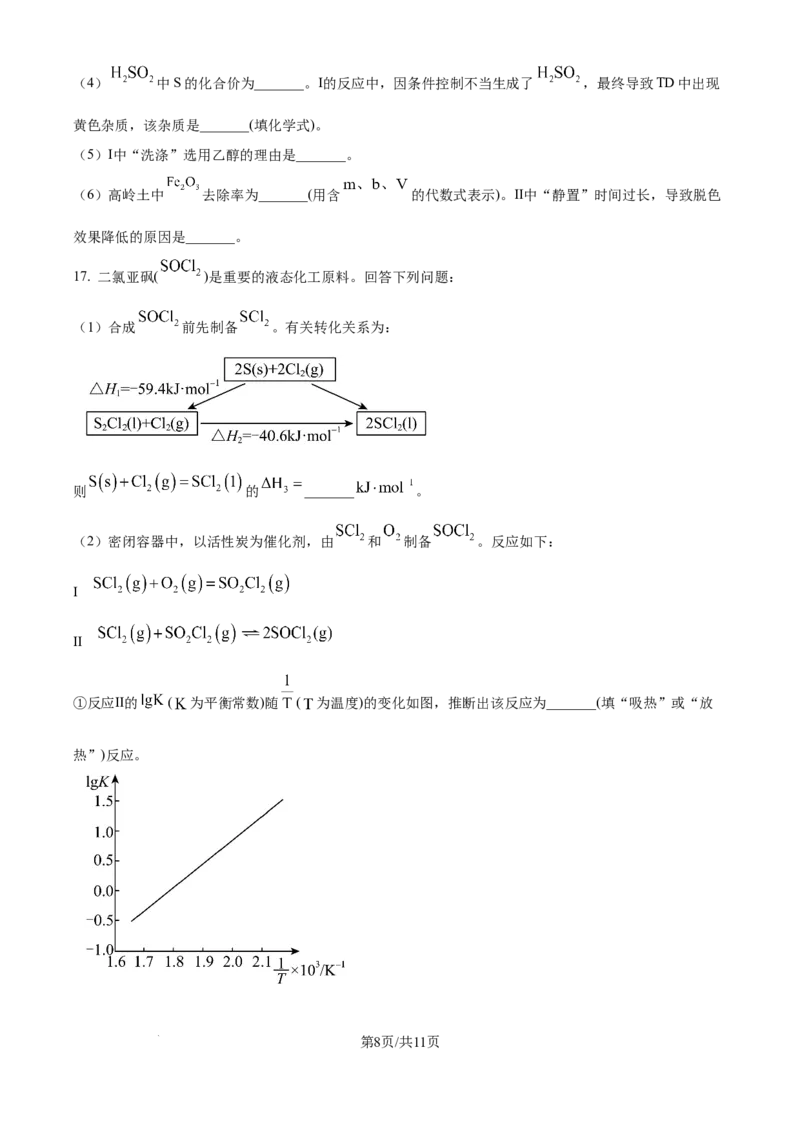
两种混合溶液的滴定曲线如图。已知 ,下列说法正确的是
第5页/共11页
学科网(北京)股份有限公司A. Ⅰ对应的滴定曲线为N线
B. 点水电离出的 数量级为
C. 时,Ⅱ中
D. 时,Ⅰ中 之和小于Ⅱ中 之和
二、非选择题:本题共4小题,共58分。
15. 广西盛产甘蔗,富藏锰矿。由软锰矿( ,含 和CuO等杂质)制备光电材料
的流程如下。回答下列问题:
已知:
物质
(1)“甘蔗渣水解液”中含有还原性糖和 ,其主要作用是_______。为提高“浸取”速率,可采
取的措施是_______(任举一例)。
(2)“滤渣1”的主要成分是_______(填化学式)。
(3)常温下,用 调节溶液pH至 时,可完全沉淀的离子有_______(填化学式)。
(4)“X”可选用_______。
A. B. C. Zn D.
(5)若用 替代 沉锰,得到 沉淀。写出生成 的离子方
程式_______。
(6) 立方晶胞如图,晶胞参数为 ,该晶体中与一个 紧邻的 有_______个。已知 为
第6页/共11页
学科网(北京)股份有限公司阿伏加德罗常数的值,晶体密度为_______ (用含 的代数式表示)。
16. 二氧化硫脲 (TD)是还原性漂白剂,可溶于水,难溶于乙醇,在受热或碱性条件下易
水解: 。其制备与应用探究如下:
Ⅰ.由硫脲 制备TD
按如图装置,在三颈烧瓶中加入硫脲和水,溶解,冷却至5℃后,滴入 溶液,控制温度低于10℃和
进行反应。反应完成后,结晶、过滤、洗涤、干燥后得到产品TD。
Ⅱ.用TD进行高岭土原矿脱色(去除 )探究
将 高岭土原矿( 质量分数为 )制成悬浊液,加入TD,在一定条件下充分反应,静置,分离
出上层清液 ,用分光光度法测得该清液中 浓度为 ,计算 的去除率。
回答下列问题:
(1)仪器 的名称是_______。
(2)Ⅰ中控制“温度低于10℃和 ”的目的是_______。
(3)写出制备TD的化学方程式_______。
第7页/共11页
学科网(北京)股份有限公司(4) 中S的化合价为_______。Ⅰ的反应中,因条件控制不当生成了 ,最终导致TD中出现
黄色杂质,该杂质是_______(填化学式)。
(5)Ⅰ中“洗涤”选用乙醇的理由是_______。
(6)高岭土中 去除率为_______(用含 的代数式表示)。Ⅱ中“静置”时间过长,导致脱色
效果降低的原因是_______。
17. 二氯亚砜( )是重要的液态化工原料。回答下列问题:
(1)合成 前先制备 。有关转化关系为:
则 的 _______ 。
(2)密闭容器中,以活性炭为催化剂,由 和 制备 。反应如下:
Ⅰ
Ⅱ
①反应Ⅱ的 ( 为平衡常数)随 ( 为温度)的变化如图,推断出该反应为_______(填“吸热”或“放
热”)反应。
第8页/共11页
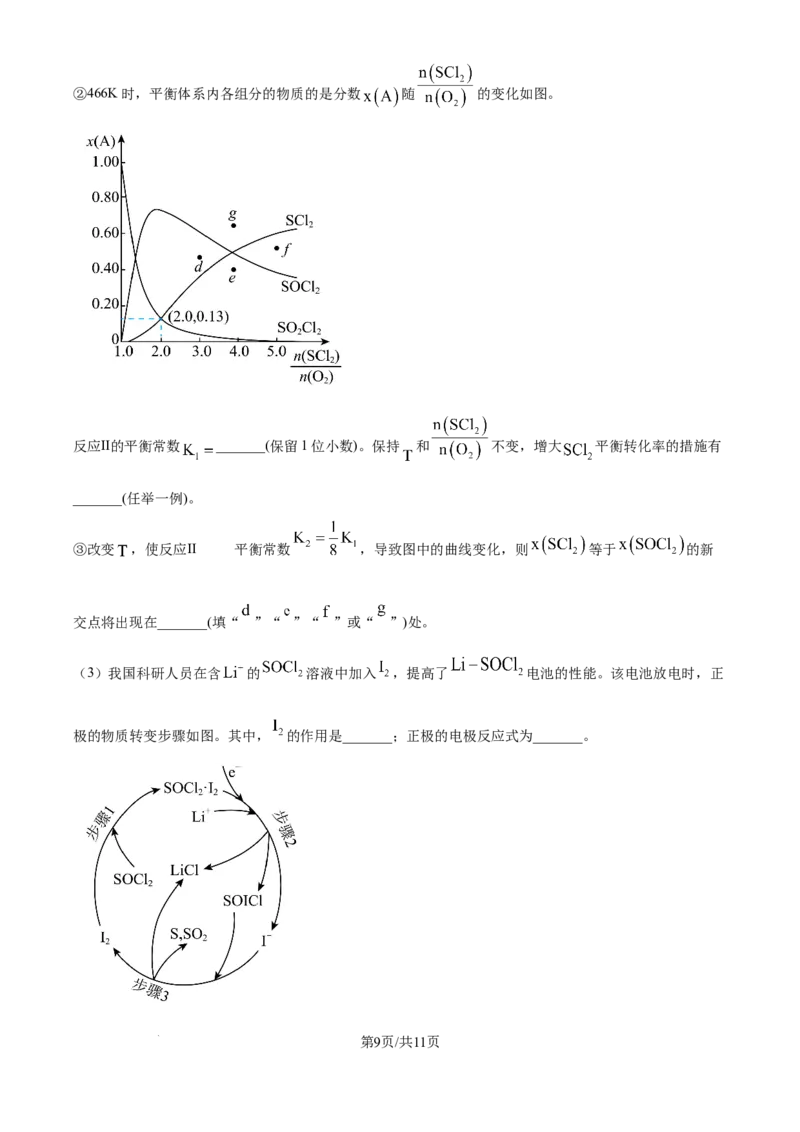
学科网(北京)股份有限公司②466K时,平衡体系内各组分的物质的是分数 随 的变化如图。
反应Ⅱ的平衡常数 _______(保留1位小数)。保持 和 不变,增大 平衡转化率的措施有
_______(任举一例)。
③改变 ,使反应Ⅱ 的平衡常数 ,导致图中的曲线变化,则 等于 的新
交点将出现在_______(填“ ”“ ”“ ”或“ ”)处。
(3)我国科研人员在含 的 溶液中加入 ,提高了 电池的性能。该电池放电时,正
极的物质转变步骤如图。其中, 的作用是_______;正极的电极反应式为_______。
第9页/共11页
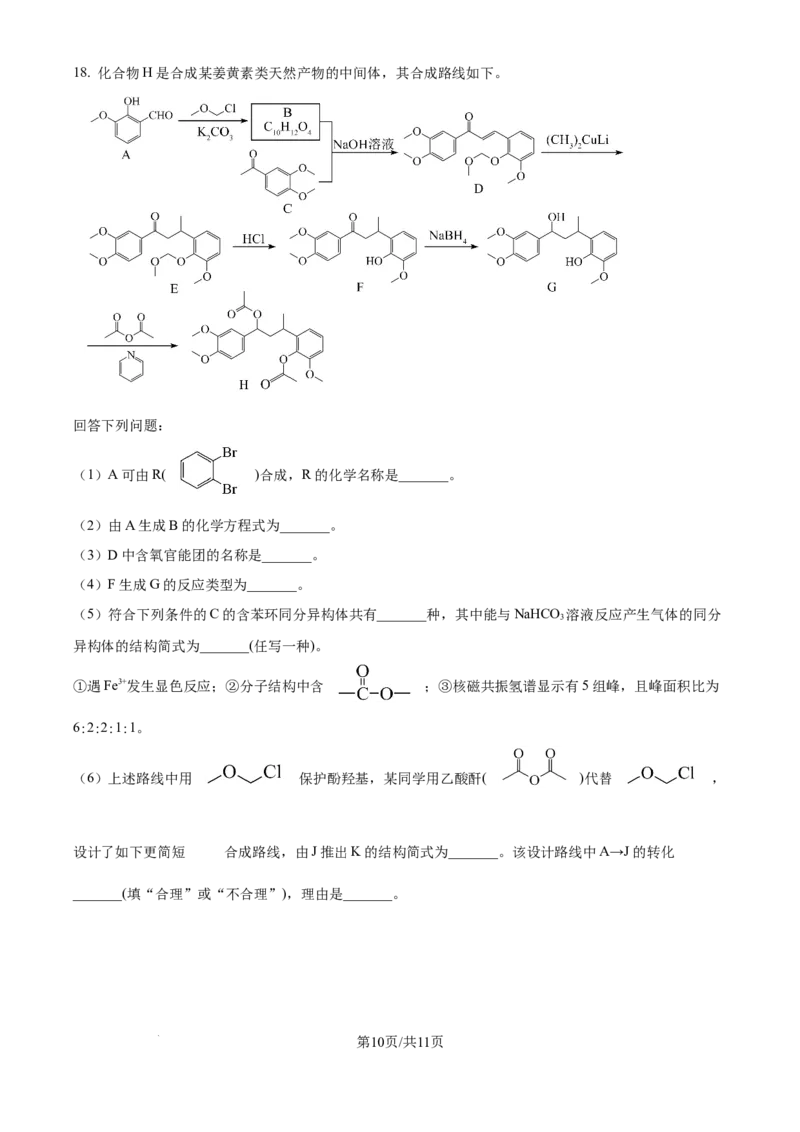
学科网(北京)股份有限公司18. 化合物H是合成某姜黄素类天然产物的中间体,其合成路线如下。
回答下列问题:
(1)A可由R( )合成,R的化学名称是_______。
(2)由A生成B的化学方程式为_______。
(3)D中含氧官能团的名称是_______。
(4)F生成G的反应类型为_______。
(5)符合下列条件的C的含苯环同分异构体共有_______种,其中能与NaHCO 溶液反应产生气体的同分
3
异构体的结构简式为_______(任写一种)。
①遇Fe3+发生显色反应;②分子结构中含 ;③核磁共振氢谱显示有5组峰,且峰面积比为
6:2:2:1:1。
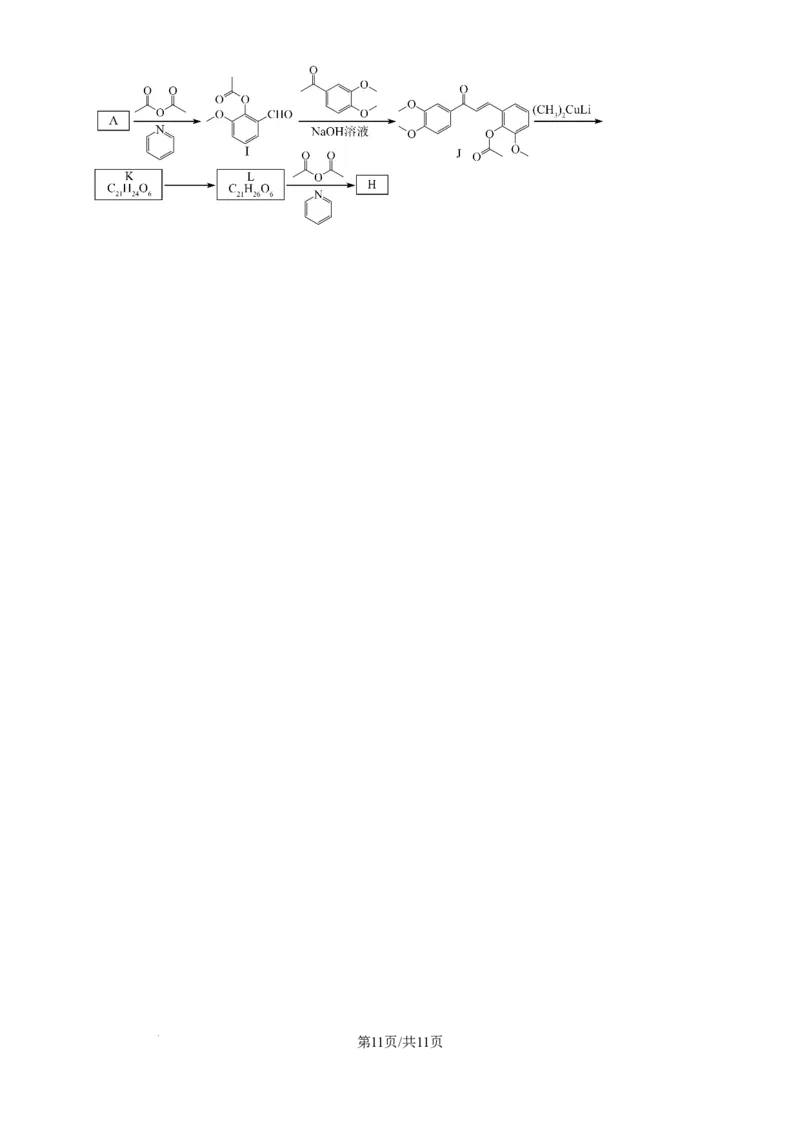
(6)上述路线中用 保护酚羟基,某同学用乙酸酐( )代替 ,
的
设计了如下更简短 合成路线,由J推出K的结构简式为_______。该设计路线中A→J的转化
_______(填“合理”或“不合理”),理由是_______。
第10页/共11页
学科网(北京)股份有限公司第11页/共11页
学科网(北京)股份有限公司