【2026版三维高考设计高中化学人教版培优讲义word电子版第6讲物质的量浓度
课标要求
1.了解物质的量浓度的概念。
2.掌握有关物质的量浓度的计算。
3.掌握一定物质的量浓度溶液配制的操作并能正确地进行误差分析。

考点一物质的量浓度

物质的量浓度
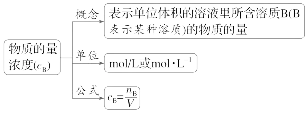

判断正误(正确的打“√”,错误的打“×”)。
(1)1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl。()
(2)1 L水中溶解5.85 g NaCl所形成的溶液的物质的量浓度为0.1 mol·L-1。()
(3)31 g Na2O溶于水,配成1 L溶液,c(Na2O)=0.5 mol·L-1。()
(4)1 L 0.5 mol·L-1CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1。()

|
一 |
物质的量浓度的理解与计算 |
1.下列溶液中,溶质的物质的量浓度不是1 mol·L-1的是()
A.28.6 g Na2CO3·10H2O固体溶解在水中配成100 mL溶液
B.将39 g Na2O2溶于水并配成1 L的溶液
C.将100 mL 0.5 mol·L-1的NaOH溶液加热蒸发掉50 g水的溶液
D.标准状况下,将22.4 L 氯化氢气体溶于水配成1 L溶液
2.某同学购买了一瓶“84”消毒液,包装说明如下:
|
主要成分:25% NaClO、1 000 mL、密度1.19 g·cm-3 使用方法:稀释100倍(体积比)后使用 注意事项:密封保存,易吸收空气中的CO2变质 |
根据以上信息和相关知识判断,下列分析不正确的是()
A.该“84”消毒液的物质的量浓度为4.0 mol·L-1
B.一瓶“84”消毒液能吸收空气中44.8 L的CO2而变质
C.取100 mL该“84”消毒液稀释100倍后用以消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.参阅该“84”消毒液的包装,欲用NaClO固体配制500 mL含25% NaClO的消毒液,需要称量的NaClO固体质量为149 g

溶质质量分数与物质的量浓度的换算公式:c=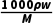 (式中ρ为溶液的密度,w为溶质的质量分数,M为溶质的摩尔质量)。
(式中ρ为溶液的密度,w为溶质的质量分数,M为溶质的摩尔质量)。
|
二 |
溶液的稀释与混合 |
3.V mL Al2(SO4)3溶液中含有Al3+m g,取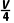 mL该溶液用水稀释至4V mL,则S
mL该溶液用水稀释至4V mL,则S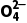 物质的量浓度为()
物质的量浓度为()
A.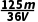 mol·L-1
mol·L-1
B.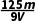 mol·L-1
mol·L-1
C.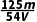 mol·L-1
mol·L-1
D.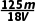 mol·L-1
mol·L-1
4.小艾同学配制的植物营养液中存在Zn2+、K+、N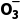 、S
、S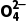 四种离子,其中K+、N
四种离子,其中K+、N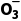 、S
、S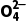 的物质的量浓度分别为0.3 mol·L-1、0.2 mol·L-1、0.4 mol·L-1,则Zn2+的物质的量浓度为()
的物质的量浓度分别为0.3 mol·L-1、0.2 mol·L-1、0.4 mol·L-1,则Zn2+的物质的量浓度为()
A.0.5 mol·L-1B.0.7 mol·L-1
C.0.35 mol·L-1D.0.9 mol·L-1

任何电解质溶液中均存在电荷守恒,即溶液中阳离子所带正电荷总数与阴离子所带负电荷总数相等。混合溶液中某一离子浓度的计算可借助电荷守恒进行求解。
考点二配制一定物质的量浓度的溶液

1.容量瓶的构造与使用
(1)构造
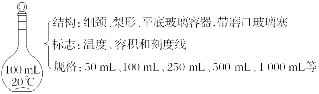
(2)查漏操作

2.一定物质的量浓度溶液的配制过程
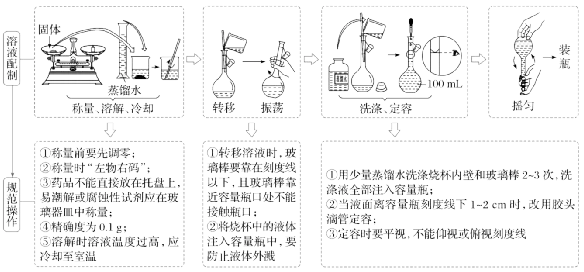

判断正误(正确的打“√”,错误的打“×”)。
(1)向容量瓶中转移液体时,引流用的玻璃棒可以接触容量瓶内壁。()
(2)用NaCl固体配制0.5 mol·L-1的溶液,所用的仪器只有:烧杯、玻璃棒、胶头滴管、容量瓶。()
(3)NaOH在烧杯里刚完全溶解时,立即将溶液转移到容量瓶。()
(4)用量筒量取20 mL 0.500 0 mol·L-1 H2SO4溶液于烧杯中,加水80 mL,配制成0.100 0 mol·L-1 H2SO4溶液。()
(5)配制480 mL 1 mol ·L-1的NaOH溶液,应用托盘天平称量NaOH固体19.2 g,选用500 mL容量瓶。()

|
一 |
溶液配制过程中的仪器使用与操作 |
1.用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是()
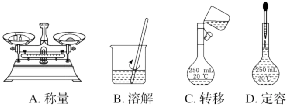
2.配制100 mL 1.00 mol·L-1NaOH溶液的操作如下。下列说法不正确的是()
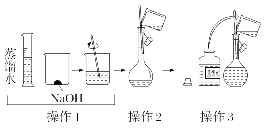
A.操作1前称取NaOH的质量为4.0 g
B.操作2前NaOH溶液需恢复至室温
C.若操作4俯视刻度线定容,则所配制溶液的浓度偏大
D.操作5后液面下降,需补充少量水至刻度线

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




