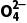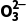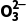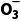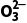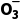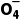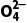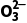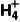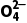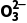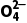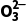【2026版三维高考设计高中化学人教版培优讲义word电子版第10讲物质的检验、鉴别与推断
课标要求
1.了解常见离子、常见气体的检验方法,能根据实验现象进行物质推断。
2.了解常见物质的鉴别方法与鉴别实验方案的评价。

考点一常见离子与气体的检验

1.常见阳离子的检验
(1)Fe3+的检验
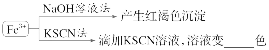
(2)Fe2+的检验
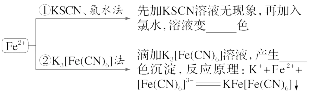
(3)N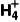 的检验
的检验
N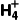
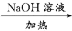 的气体
的气体
(4)焰色试验法检验
|
金属元素 |
锂 |
钠 |
钾 |
铜 |
钡 |
钙 |
|
焰色 |
紫红色 |
色 |
色(透过蓝色钴玻璃观察) |
色 |
黄绿色 |
砖红色 |
2.常见阴离子的检验
根据离子性质不同而在实验中所表现出的现象不同,可以把检验阴离子的方法归纳为三种类型:Ⅰ.生成沉淀;Ⅱ.生成气体;Ⅲ.显现特殊颜色。
(1)生成沉淀
|
阴离子 |
试剂 |
实验现象(证据) |
|
Cl-Br-I- |
AgNO3溶液和 稀硝酸 |
产生色沉淀→Cl- 产生色沉淀→Br- 产生色沉淀→I- |
|
S |
稀盐酸和BaCl2 溶液 |
先加稀盐酸无明显现象,再加BaCl2溶液产生色沉淀 |
|
C |
CaCl2溶液和 稀盐酸 |
先加CaCl2溶液产生色沉淀,再加稀盐酸沉淀 ,并产生无色无味的气体 |
【提醒】 检验S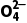 时不能用硝酸代替盐酸,也不能用Ba(NO3)2代替BaCl2溶液,原因是N
时不能用硝酸代替盐酸,也不能用Ba(NO3)2代替BaCl2溶液,原因是N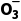 在酸性条件下具有强氧化性,能将S
在酸性条件下具有强氧化性,能将S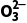 氧化成S
氧化成S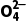 S
S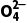 的检验。
的检验。
(2)生成气体
|
阴离子 |
试剂 |
实验现象(证据) |
|
C |
稀盐酸和澄清石灰水 |
加稀盐酸产生无色无味的气体,且该气体能使澄清石灰水 |
|
S |
稀硫酸和品红溶液 |
加稀硫酸产生刺激性气味的气体,且该气体能使品红溶液 |
(3)显现特殊颜色
①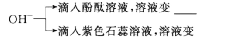
②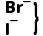
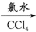 (下层)
(下层)
③I-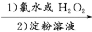
3.常见气体的检验
(1)酸性气体的检验
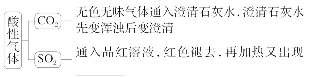
(2)碱性气体的检验
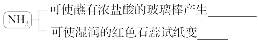
(3)还原性气体的检验
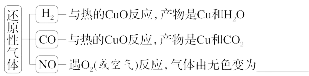
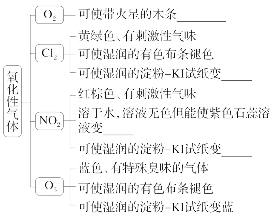
(4)氧化性气体的检验
4.离子推断的原则和方法
(1)定性推断四原则
|
肯定性 原则 |
根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住常见的有色离子:Fe2+、Fe3+、Cu2+、Mn |
|
互斥性 原则 |
在肯定某些离子存在的同时,结合离子共存规律,否定一些离子存在(要注意题目中的隐含条件,如酸性、碱性、指示剂的变化、与铝反应产生氢气、水的电离情况等) |
|
电中性 原则 |
溶液呈电中性,一定既有阳离子,又有阴离子,且溶液中正、负电荷总数相等(利用这一原则可确定一些隐含的离子) |
|
进出性 原则 |
通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验的干扰 |
(2)定量推断一关系
解与离子反应有关的定量推断类试题,需要掌握定量推断最后一种离子存在的方法;如果多种离子共存,且只有一种离子的物质的量未知,可以用电荷守恒关系来确定最后一种离子是否存在,即阳离子所带的正电荷总数等于阴离子所带的负电荷总数。

|
一 |
离子和气体的检验 |
1.下列实验有关离子检验的操作及现象与结论之间对应关系正确的是()
|
选项 |
操作及现象 |
结论 |
|
A |
向某溶液中加稀盐酸酸化的BaCl2溶液,有白色沉淀生成 |
该溶液中一定含S |
|
B |
向某溶液中加入过量盐酸,产生能使澄清石灰水变浑浊的气体 |
该溶液中一定含C |
|
C |
向某溶液中加入NaOH,产生能使湿润的蓝色石蕊试纸变红的气体 |
该溶液中含N |
|
D |
向某溶液中先滴加稀硝酸酸化,再滴加AgNO3溶液,产生白色沉淀 |
该溶液中含Cl- |
2.下列有关常见气体成分检验的结论正确的是()
|
选项 |
仪器或试剂 |
实验现象 |
结论 |
|
A |
湿润的红色石蕊试纸 |
试纸变蓝 |
一定含NH3 |
|
B |
灼热CuO |
黑色固体变为红色 |
一定含H2 |
|
C |
澄清石灰水 |
溶液中出现浑浊 |
一定含CO2 |
|
D |
湿润的淀粉-KI试纸 |
试纸变蓝 |
一定含Cl2 |

离子检验中常见干扰离子以及排除措施
|
待检离子 |
干扰离子 |
排除措施 |
|
Cl- |
S |
加过量的Ba(NO3)2溶液 |
|
C |
加稀硝酸酸化 |
|
|
OH- |
||
|
S |
C |
加盐酸酸化 |

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风