【2026版三维高考设计高中化学人教版培优讲义word电子版第9讲物质的分离和提纯
课标要求
1.初步学会物质分离、提纯等化学实验基础知识和基本技能。
2.能综合运用物质的不同性质对常见物质进行分离和提纯。
3.利用典型代表物的性质和反应,设计常见物质分离、提纯等简单任务的方案。

考点一分离、提纯的基本方法

1.物质的分离、提纯
|
分离 |
将混合物的各组分分开,获得几种纯净物的过程 |
|
提纯 |
将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂 |
2.分离、提纯常用的方法与装置
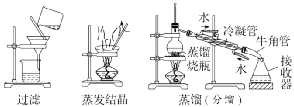
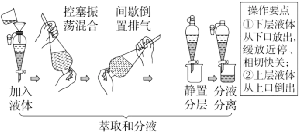
(1)从MgSO4溶液中得到MgSO4固体的实验操作包括、冷却结晶、、洗涤、干燥等一系列操作,在此过程中玻璃棒的作用是(填序号)。
①引流 ②搅拌加速溶解 ③搅拌使溶液受热均匀,防止暴沸
(2)过滤后,若滤液浑浊,需更换滤纸,重新过滤。浑浊的原因可能是。
(3)硫酸铝和硫酸铵的混合液经蒸发浓缩至溶液表面刚出现薄层晶体时即停止加热,然后冷却结晶,得到铵明矾晶体[NH4Al(SO4)2·12H2O]。溶液不能蒸干的原因是。
(4)分液时,分液漏斗中的液体很难滴下,可能的原因是。
3.结晶与重结晶的应用
图甲、图乙为一些物质的溶解度随温度变化的曲线。

(1)常温下,由NaCl稀溶液获取NaCl固体的方法是。
(2)常温下由KNO3稀溶液获取KNO3固体的方法是。
(3)NaCl固体中含少量KNO3,提纯NaCl固体的方式是。
(4)KNO3固体中含少量NaCl,提纯KNO3固体的方式是。
(5)图乙所示为Na2SO3的溶解度随温度的变化曲线。常温下由Na2SO3稀溶液获取Na2SO3固体的方法是
。

判断正误(正确的打“√”,错误的打“×”)。
(1)过滤时,为加快过滤速度,应用玻璃棒不断搅拌漏斗中的液体。()
(2)根据食用油和汽油的密度不同,可选用分液的方法分离。()
(3)用乙醇萃取出溴水中的溴,再用蒸馏的方法分离溴与乙醇。()
(4)在蒸馏过程中,若发现忘加沸石,应停止加热立即补加。()
(5)利用加热的方法分离NH4Cl和I2的固体混合物。()
(6)蒸发操作时,应使混合物中的水分完全蒸干后,再停止加热。()

|
一 |
分离、提纯中的实验装置与操作 |
1.下列实验中,所采取的分离方法与对应原理都正确的是()
|
选项 |
实验 |
分离方法 |
原理 |
|
A |
除去KCl中的MnO2 |
蒸发结晶 |
溶解度不同 |
|
B |
除去碘中的NaCl |
加热、升华 |
NaCl的熔点高,碘易升华 |
|
C |
分离KNO3和NaCl |
重结晶 |
KNO3的溶解度大于NaCl |
|
D |
分离食用油和汽油 |
分液 |
食用油和汽油的密度不同 |
2.下列叙述正确的是()
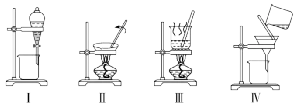
A.用装置Ⅰ分离乙酸乙酯与饱和碳酸钠溶液
B.用装置Ⅱ蒸干硫酸亚铁溶液制备FeSO4·7H2O
C.用装置Ⅲ将硫酸铜溶液蒸发浓缩、冷却结晶,得到胆矾晶体
D.用装置Ⅳ分离Cl2与KI溶液反应生成的碘
|
二 |
分离、提纯中的沉淀洗涤 |
3.从铝土矿(含有Fe2O3、SiO2等杂质)中提取氧化铝的流程如图所示:
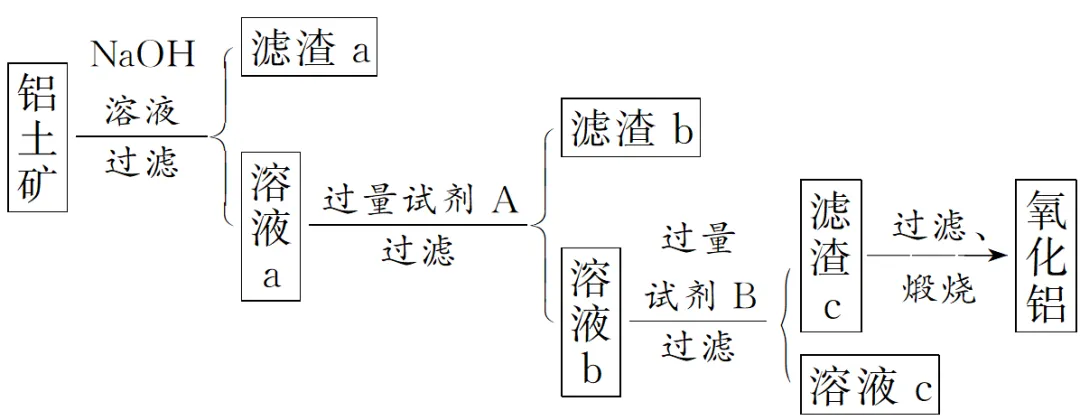
洗涤滤渣c的实验操作方法是。
4.二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]·2H2O}制备流程如下:
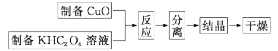
(已知:H2C2O4 CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)
制备CuO:CuSO4溶液中滴入NaOH溶液,加热煮沸、冷却、双层滤纸过滤、洗涤。
(1)用双层滤纸过滤的原因是。
(2)用蒸馏水洗涤氧化铜时,如何证明氧化铜已洗涤干净:。

(1)沉淀洗涤的答题规范
注洗涤液(沿玻璃棒向漏斗中注入洗涤液)
↓
标准(使洗涤液完全浸没沉淀或晶体)
↓
重复(待洗涤液自然流尽后,重复操作2~3次)
(2)判断沉淀是否洗净的答题规范
取样(取少量最后一次洗涤液于一洁净的试管中)
↓
加试剂[加入××试剂(必要时加热,如检验N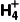 )]
)]
↓
现象(不产生××沉淀、溶液不变××色或不产生××气体)
↓
结论(说明沉淀已经洗涤干净)
考点二化学提纯法及其应用

1.除杂“四原则”
(1)不增,不得引入新的杂质。
(2)不减,尽量不减少被提纯和分离的物质。
(3)易分离,应使被提纯或分离的物质与其他物质易分离。
(4)易复原,被提纯物质转化后要易被复原。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/136tUpK67Q1V3PV2VsUIuPw?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




