文档内容
2016年苏州市中考化学试卷及答案
一、选择题(共25小题,每小题2分,满分50分)
1.2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”。下列做法
与之相违背的是( )
A.农作物的秸杆就地焚烧 B.社会公共场所严禁吸烟
C.积极开展绿化国土行动 D.工业废水处理达标后排放
2.下列化学用语中,既能表示一种元素,又能表示一种物质的是( )
A.H B.Cu C.CO D.HCl
2 2
3.下列属于物理变化的是( )
A.甘薯酿酒 B.石蜡熔化 C.烟花爆炸 D.食物腐败
4.下列物质属于混合物的是( )
A.氧气 B.氧化铜 C.硫酸钠 D.空气
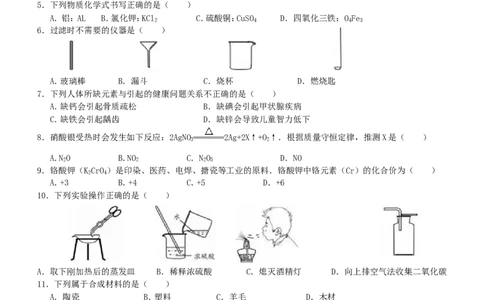
5.下列物质化学式书写正确的是( )
A.铝:AL B.氯化钾:KCl C.硫酸铜:CuSO D.四氧化三铁:O Fe
2 4 4 3
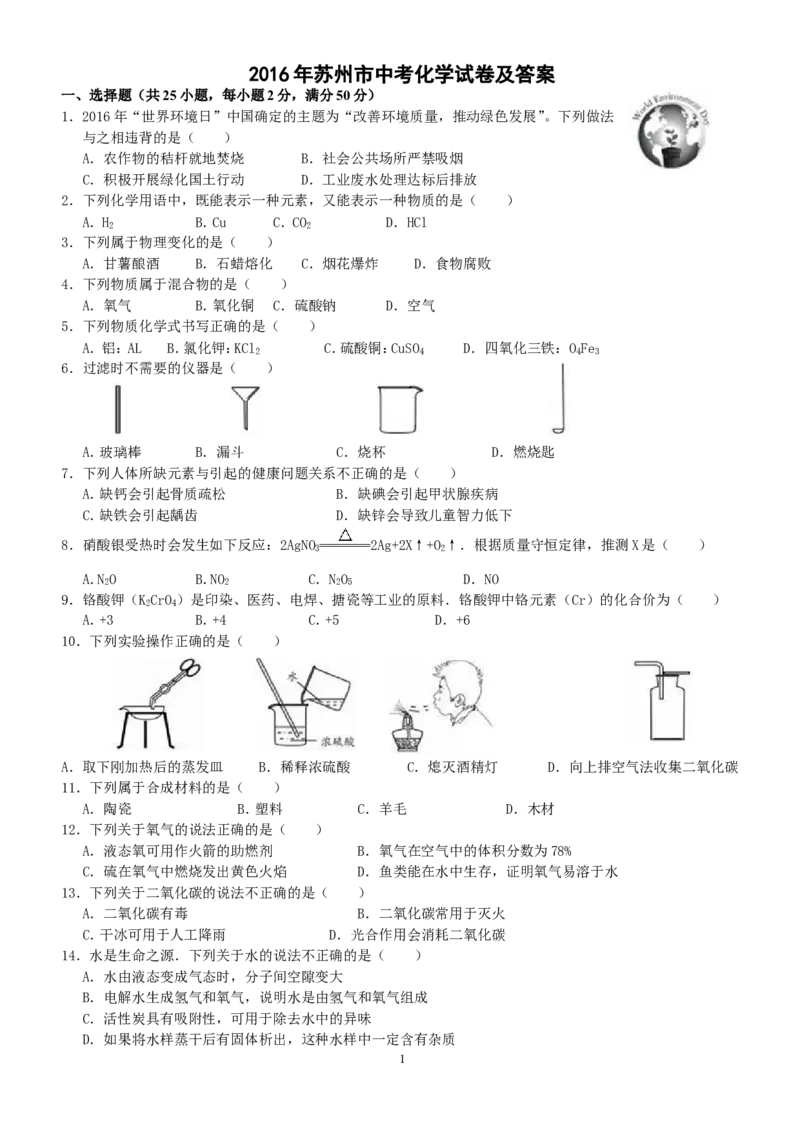
6.过滤时不需要的仪器是( )
A.玻璃棒 B.漏斗 C.烧杯 D.燃烧匙
7.下列人体所缺元素与引起的健康问题关系不正确的是( )
A.缺钙会引起骨质疏松 B.缺碘会引起甲状腺疾病
C.缺铁会引起龋齿 D.缺锌会导致儿童智力低下
8.硝酸银受热时会发生如下反应:2AgNO 2Ag+2X↑+O ↑.根据质量守恒定律,推测X是( )
3 2
A.N O B.NO C.N O D.NO
2 2 2 5
9.铬酸钾(K CrO )是印染、医药、电焊、搪瓷等工业的原料.铬酸钾中铬元素(Cr)的化合价为( )
2 4
A.+3 B.+4 C.+5 D.+6
10.下列实验操作正确的是( )
A.取下刚加热后的蒸发皿 B.稀释浓硫酸 C.熄灭酒精灯 D.向上排空气法收集二氧化碳
11.下列属于合成材料的是( )
A.陶瓷 B.塑料 C.羊毛 D.木材
12.下列关于氧气的说法正确的是( )
A.液态氧可用作火箭的助燃剂 B.氧气在空气中的体积分数为78%
C.硫在氧气中燃烧发出黄色火焰 D.鱼类能在水中生存,证明氧气易溶于水
13.下列关于二氧化碳的说法不正确的是( )
A.二氧化碳有毒 B.二氧化碳常用于灭火
C.干冰可用于人工降雨 D.光合作用会消耗二氧化碳
14.水是生命之源.下列关于水的说法不正确的是( )
A.水由液态变成气态时,分子间空隙变大
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成
C.活性炭具有吸附性,可用于除去水中的异味
D.如果将水样蒸干后有固体析出,这种水样中一定含有杂质
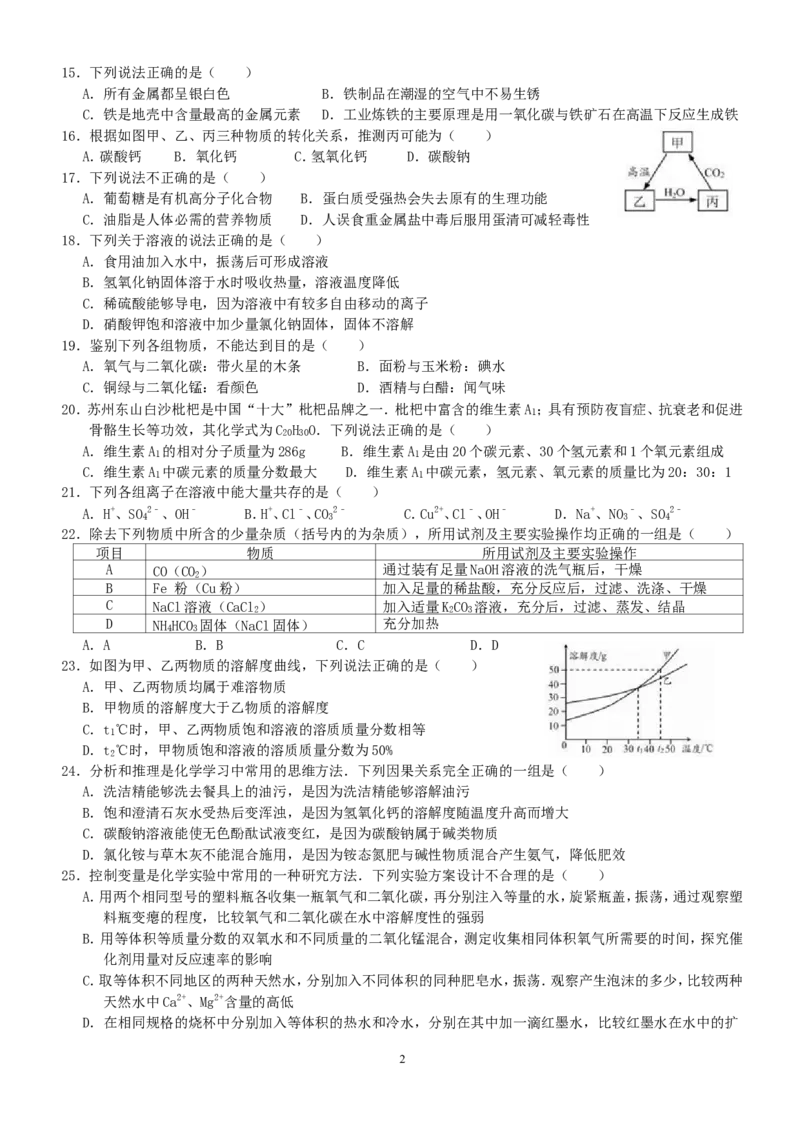
115.下列说法正确的是( )
A.所有金属都呈银白色 B.铁制品在潮湿的空气中不易生锈
C.铁是地壳中含量最高的金属元素 D.工业炼铁的主要原理是用一氧化碳与铁矿石在高温下反应生成铁
16.根据如图甲、乙、丙三种物质的转化关系,推测丙可能为( )
A.碳酸钙 B.氧化钙 C.氢氧化钙 D.碳酸钠
17.下列说法不正确的是( )
A.葡萄糖是有机高分子化合物 B.蛋白质受强热会失去原有的生理功能
C.油脂是人体必需的营养物质 D.人误食重金属盐中毒后服用蛋清可减轻毒性
18.下列关于溶液的说法正确的是( )
A.食用油加入水中,振荡后可形成溶液
B.氢氧化钠固体溶于水时吸收热量,溶液温度降低
C.稀硫酸能够导电,因为溶液中有较多自由移动的离子
D.硝酸钾饱和溶液中加少量氯化钠固体,固体不溶解
19.鉴别下列各组物质,不能达到目的是( )
A.氧气与二氧化碳:带火星的木条 B.面粉与玉米粉:碘水
C.铜绿与二氧化锰:看颜色 D.酒精与白醋:闻气味
20.苏州东山白沙枇杷是中国“十大”枇杷品牌之一.枇杷中富含的维生素A ;具有预防夜盲症、抗衰老和促进
1
骨骼生长等功效,其化学式为C H O.下列说法正确的是( )
20 30
A.维生素A 的相对分子质量为286g B.维生素A 是由20个碳元素、30个氢元素和1个氧元素组成
1 1
C.维生素A 中碳元素的质量分数最大 D.维生素A 中碳元素,氢元素、氧元素的质量比为20:30:1
1 1
21.下列各组离子在溶液中能大量共存的是( )
A.H+、SO 2﹣、OH﹣ B.H+、Cl﹣、CO 2﹣ C.Cu2+、Cl﹣、OH﹣ D.Na+、NO ﹣、SO 2﹣
4 3 3 4
22.除去下列物质中所含的少量杂质(括号内的为杂质),所用试剂及主要实验操作均正确的一组是( )
项目 物质 所用试剂及主要实验操作
A CO(CO ) 通过装有足量NaOH溶液的洗气瓶后,干燥
2
B Fe 粉(Cu粉) 加入足量的稀盐酸,充分反应后,过滤、洗涤、干燥
C NaCl溶液(CaCl ) 加入适量K CO 溶液,充分后,过滤、蒸发、结晶
2 2 3
D NH HCO 固体(NaCl固体) 充分加热
4 3
A.A B.B C.C D.D
23.如图为甲、乙两物质的溶解度曲线,下列说法正确的是( )
A.甲、乙两物质均属于难溶物质
B.甲物质的溶解度大于乙物质的溶解度
C.t ℃时,甲、乙两物质饱和溶液的溶质质量分数相等
1
D.t ℃时,甲物质饱和溶液的溶质质量分数为50%
2
24.分析和推理是化学学习中常用的思维方法.下列因果关系完全正确的一组是( )
A.洗洁精能够洗去餐具上的油污,是因为洗洁精能够溶解油污
B.饱和澄清石灰水受热后变浑浊,是因为氢氧化钙的溶解度随温度升高而增大
C.碳酸钠溶液能使无色酚酞试液变红,是因为碳酸钠属于碱类物质
D.氯化铵与草木灰不能混合施用,是因为铵态氮肥与碱性物质混合产生氨气,降低肥效
25.控制变量是化学实验中常用的一种研究方法.下列实验方案设计不合理的是( )
A.用两个相同型号的塑料瓶各收集一瓶氧气和二氧化碳,再分别注入等量的水,旋紧瓶盖,振荡,通过观察塑
料瓶变瘪的程度,比较氧气和二氧化碳在水中溶解度性的强弱
B.用等体积等质量分数的双氧水和不同质量的二氧化锰混合,测定收集相同体积氧气所需要的时间,探究催
化剂用量对反应速率的影响
C.取等体积不同地区的两种天然水,分别加入不同体积的同种肥皂水,振荡.观察产生泡沫的多少,比较两种
天然水中Ca2+、Mg2+含量的高低
D.在相同规格的烧杯中分别加入等体积的热水和冷水,分别在其中加一滴红墨水,比较红墨水在水中的扩
2散速率,探究温度对分子运动速率的影响
二、非选择题(共7小题,满分50分)
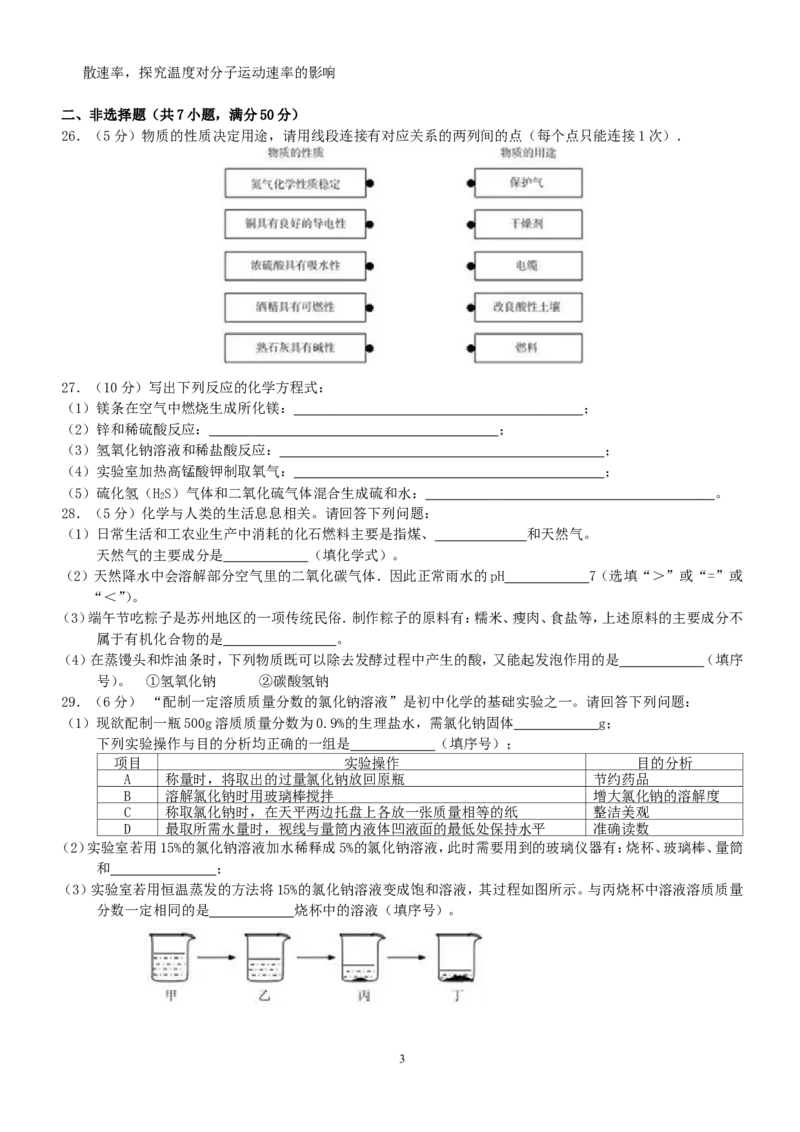
26.(5分)物质的性质决定用途,请用线段连接有对应关系的两列间的点(每个点只能连接1次).
27.(10分)写出下列反应的化学方程式:
(1)镁条在空气中燃烧生成所化镁: ;
(2)锌和稀硫酸反应: ;
(3)氢氧化钠溶液和稀盐酸反应: ;
(4)实验室加热高锰酸钾制取氧气: ;
(5)硫化氢(H S)气体和二氧化硫气体混合生成硫和水: 。
2
28.(5分)化学与人类的生活息息相关。请回答下列问题:
(1)日常生活和工农业生产中消耗的化石燃料主要是指煤、 和天然气。
天然气的主要成分是 (填化学式)。
(2)天然降水中会溶解部分空气里的二氧化碳气体.因此正常雨水的pH 7(选填“>”或“=”或
“<”)。
(3)端午节吃粽子是苏州地区的一项传统民俗.制作粽子的原料有:糯米、瘦肉、食盐等,上述原料的主要成分不
属于有机化合物的是 。
(4)在蒸馒头和炸油条时,下列物质既可以除去发酵过程中产生的酸,又能起发泡作用的是 (填序
号)。 ①氢氧化钠 ②碳酸氢钠
29.(6分) “配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500g溶质质量分数为0.9%的生理盐水,需氯化钠固体 g;
下列实验操作与目的分析均正确的一组是 (填序号);
项目 实验操作 目的分析
A 称量时,将取出的过量氯化钠放回原瓶 节约药品
B 溶解氯化钠时用玻璃棒搅拌 增大氯化钠的溶解度
C 称取氯化钠时,在天平两边托盘上各放一张质量相等的纸 整洁美观
D 最取所需水量时,视线与量筒内液体凹液面的最低处保持水平 准确读数
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有:烧杯、玻璃棒、量筒
和 ;
(3)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示。与丙烧杯中溶液溶质质量
分数一定相同的是 烧杯中的溶液(填序号)。
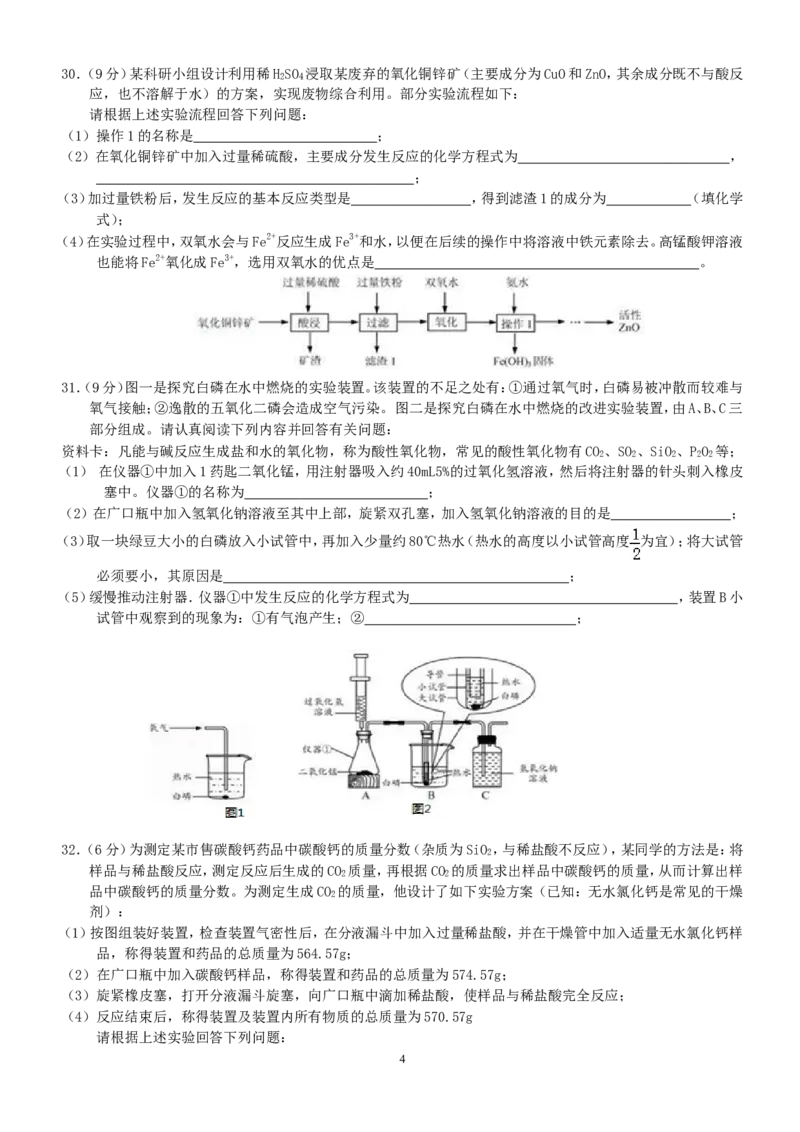
330.(9分)某科研小组设计利用稀H SO 浸取某废弃的氧化铜锌矿(主要成分为CuO和ZnO,其余成分既不与酸反
2 4
应,也不溶解于水)的方案,实现废物综合利用。部分实验流程如下:
请根据上述实验流程回答下列问题:
(1)操作1的名称是 ;
(2)在氧化铜锌矿中加入过量稀硫酸,主要成分发生反应的化学方程式为 ,
;
(3)加过量铁粉后,发生反应的基本反应类型是 ,得到滤渣1的成分为 (填化学
式);
(4)在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去。高锰酸钾溶液
也能将Fe2+氧化成Fe3+,选用双氧水的优点是 。
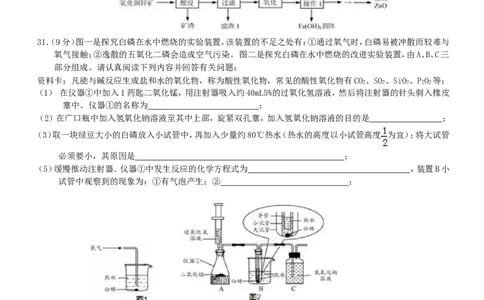
31.(9分)图一是探究白磷在水中燃烧的实验装置。该装置的不足之处有:①通过氧气时,白磷易被冲散而较难与
氧气接触;②逸散的五氧化二磷会造成空气污染。 图二是探究白磷在水中燃烧的改进实验装置,由A、B、C三
部分组成。请认真阅读下列内容并回答有关问题:
资料卡:凡能与碱反应生成盐和水的氧化物,称为酸性氧化物,常见的酸性氧化物有CO 、SO 、SiO 、P O 等;
2 2 2 2 2
(1) 在仪器①中加入1药匙二氧化锰,用注射器吸入约40mL5%的过氧化氢溶液,然后将注射器的针头刺入橡皮
塞中。仪器①的名称为 ;
(2)在广口瓶中加入氢氧化钠溶液至其中上部,旋紧双孔塞,加入氢氧化钠溶液的目的是 ;
(3)取一块绿豆大小的白磷放入小试管中,再加入少量约80℃热水(热水的高度以小试管高度 为宜);将大试管
必须要小,其原因是 ;
(5)缓慢推动注射器.仪器①中发生反应的化学方程式为 ,装置B小
试管中观察到的现象为:①有气泡产生;② ;
32.(6分)为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO ,与稀盐酸不反应),某同学的方法是:将
2
样品与稀盐酸反应,测定反应后生成的CO 质量,再根据CO 的质量求出样品中碳酸钙的质量,从而计算出样
2 2
品中碳酸钙的质量分数。为测定生成CO 的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥
2
剂):
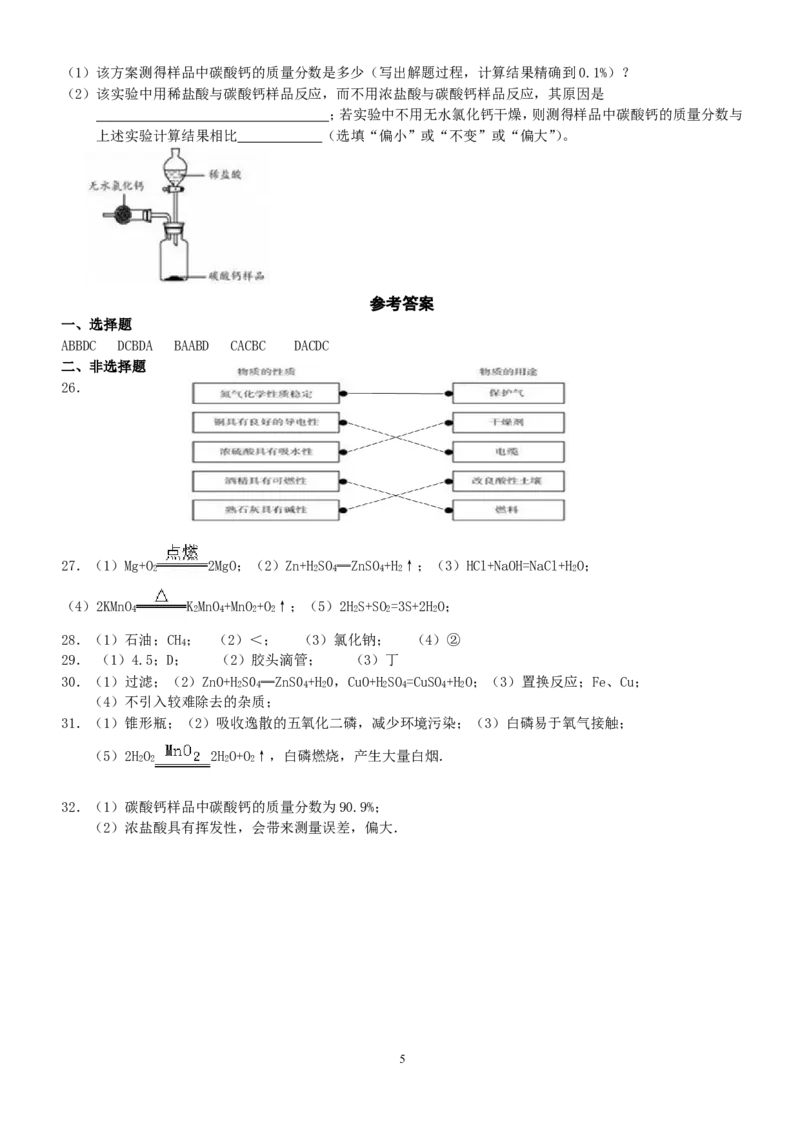
(1)按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样
品,称得装置和药品的总质量为564.57g;
(2)在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
(3)旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
(4)反应结束后,称得装置及装置内所有物质的总质量为570.57g
请根据上述实验回答下列问题:
4(1)该方案测得样品中碳酸钙的质量分数是多少(写出解题过程,计算结果精确到0.1%)?
(2)该实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应,其原因 是
;若实验中不用无水氯化钙干燥,则测得样品中碳酸钙的质量分数与
上述实验计算结果相比 (选填“偏小”或“不变”或“偏大”)。
参考答案
一、选择题
ABBDC DCBDA BAABD CACBC DACDC
二、非选择题
26.
27.(1)Mg+O 2MgO;(2)Zn+H SO ═ZnSO +H ↑;(3)HCl+NaOH=NaCl+H O;
2 2 4 4 2 2
(4)2KMnO K MnO +MnO +O ↑;(5)2H S+SO =3S+2H O;
4 2 4 2 2 2 2 2
28.(1)石油;CH ; (2)<; (3)氯化钠; (4)②
4
29. (1)4.5;D; (2)胶头滴管; (3)丁
30.(1)过滤;(2)ZnO+H S0 ═ZnS0 +H 0,CuO+H SO =CuSO +H O;(3)置换反应;Fe、Cu;
2 4 4 2 2 4 4 2
(4)不引入较难除去的杂质;
31.(1)锥形瓶;(2)吸收逸散的五氧化二磷,减少环境污染;(3)白磷易于氧气接触;
(5)2H O 2H O+O ↑,白磷燃烧,产生大量白烟.
2 2 2 2
32.(1)碳酸钙样品中碳酸钙的质量分数为90.9%;
(2)浓盐酸具有挥发性,会带来测量误差,偏大.
5