文档内容
2026 届高三考前模拟综合检测(化学)
可能用到的相对分子质量:H-1 O-16 S-32 Cl-35.5
一、单选题(本题共13题,每题3分,共39分。每题只有一个选项最符合题意)
1. 第19届杭州亚运会采用石墨烯纳米防滑涂层以增加地面防滑性。石墨烯属于
A. 有机材料 B. 无机非金属材料 C. 金属材料 D. 复合材料
2. 印刷电路板的碱性蚀刻液与NaOH溶液共热可发生反应:[Cu(NH )]2++2OH- CuO↓+4NH ↑+H O。下列
3 4 3 2
说法不正确的是
A. Cu属于d区元素 B. 1mol[Cu(NH)]2+中含16molσ键
3 4
.
C NH 分子所含键角大于HO D. 稳定性:NH <HO
3 2 3 2
3. 一种用于烧制陶瓷的黏土中含Al Si O(OH) 、CaMg(CO )、MgSO 等物质。下列说法正确的是
2 2 5 4 3 2 4
A. 离子半径:r(Na+)>r(Al3+)>r(O2–) B. 电负性:χ(O)>χ(C)>χ(Si)
C. 熔点:CaO>MgO D. 第一电离能:I(Si)>I (Al)>I (Mg)
1 1 1
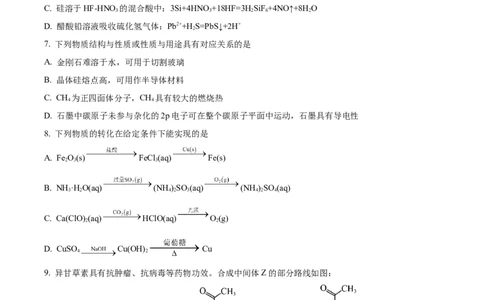
4. 在酸性条件下可发生反应: 。以 为原料制取 晶
体的实验操作或原理不能达到实验目的的是
A. 用装置甲制取含 的悬浊液 B. 用装置乙吸收挥发出的 气体
C. 用装置丙除去S和未反应的 D. 用装置丁蒸干溶液,获得
阅读下列材料,完成以下3个小题:
碳族元素及其化合物在自然界广泛存在且具有重要应用。甲烷具有较大燃烧热(890.3kJ·mol-1),是常见燃料;
HCS 是一种弱酸,在水中缓慢水解生成HCO;通过反应Ni(s)+4CO(g) Ni(CO) (g)可用于提纯Ni。Si、
2 3 2 3 4
Ge是重要半导体材料,硅可以溶于HF-HNO 的混合酸中生成HSiF;醋⇌酸铅(易溶于水,难电离)溶液可以
3 2 6
吸收硫化氢气体。的
5. 下列说法正确 是
A. 碳和硅的单质都属于分子晶体
B. CO 中的C原子与SiO 中的Si原子杂化方式相同
2 2
C. 配合物Ni(CO) 中配位键的形成由Ni提供空轨道
4
D. Ge原子基态核外电子排布式为[Ar]4s24p2
6. 下列化学反应表示不正确的是
A. 甲烷的燃烧:CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890.3kJ·mol-1
4 2 2 2
B. HCS 与水反应:HCS+3H O=HCO+3H S
2 3 2 3 2 2 3 2
C. 硅溶于HF-HNO 的混合酸中:3Si+4HNO +18HF=3HSiF+4NO↑+8HO
3 3 2 6 2
D. 醋酸铅溶液吸收硫化氢气体:Pb2++H S=PbS↓+2H+
2
7. 下列物质结构与性质或性质与用途具有对应关系的是
A. 金刚石难溶于水,可用于切割玻璃
B. 晶体硅熔点高,可用作半导体材料
C. CH 为正四面体分子,CH 具有较大的燃烧热
4 4
D. 石墨中碳原子未参与杂化的2p电子可在整个碳原子平面中运动,石墨具有导电性
8. 下列物质的转化在给定条件下能实现的是
A. Fe O(s) FeCl (aq) Fe(s)
2 3 3
B. NH ·H O(aq) (NH )SO (aq) (NH )SO (aq)
3 2 4 2 3 4 2 4
C. Ca(ClO) (aq) HClO(aq) O(g)
2 2
D. CuSO Cu(OH) Cu
4 2
9. 异甘草素具有抗肿瘤、抗病毒等药物功效。合成中间体Z的部分路线如图:
下列有关化合物X、Y和Z的说法正确的是
A. 1molZ中含有6mol碳氧σ键
B. X分子中的所有原子一定共平面
C. Y能发生加成、氧化和消去反应D. Z与足量的氢气加成后的产物分子中含有3个手性碳原子
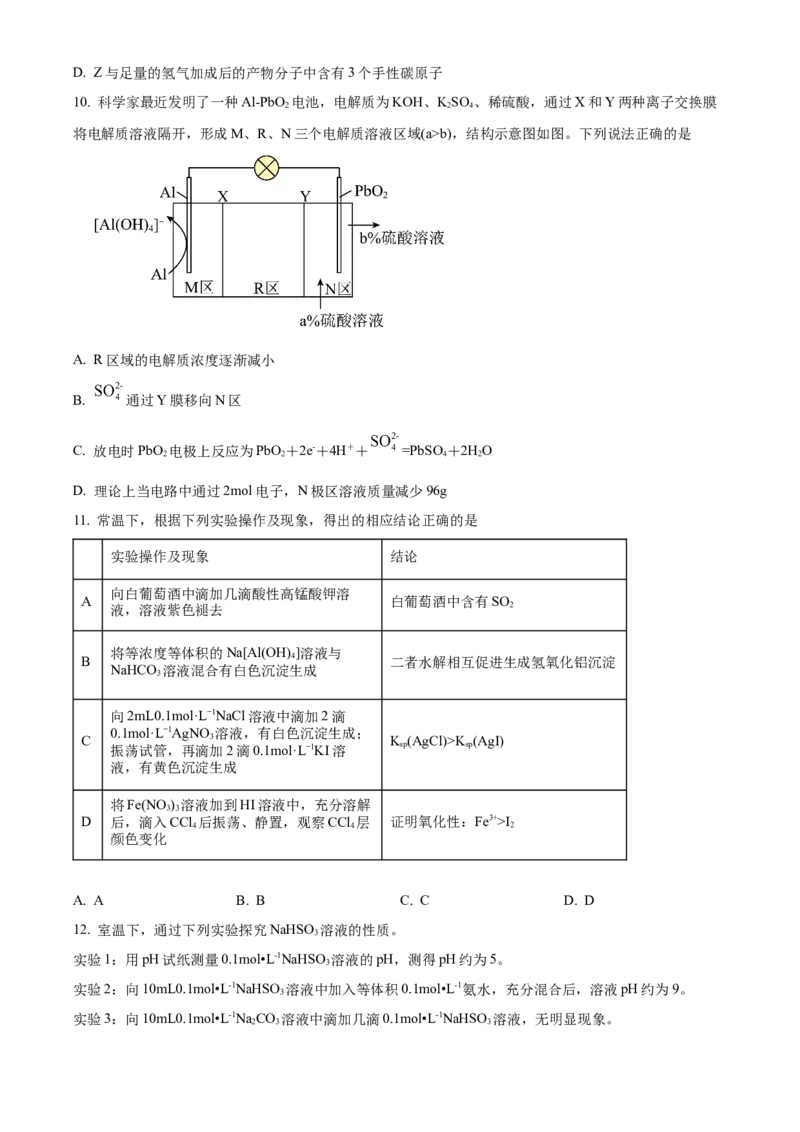
10. 科学家最近发明了一种Al-PbO 电池,电解质为KOH、KSO 、稀硫酸,通过X和Y两种离子交换膜
2 2 4
将电解质溶液隔开,形成M、R、N三个电解质溶液区域(a>b),结构示意图如图。下列说法正确的是
A. R区域的电解质浓度逐渐减小
B. 通过Y膜移向N区
C. 放电时PbO 电极上反应为PbO +2e-+4H++ =PbSO+2HO
2 2 4 2
D. 理论上当电路中通过2mol电子,N极区溶液质量减少96g
11. 常温下,根据下列实验操作及现象,得出的相应结论正确的是
实验操作及现象 结论
向白葡萄酒中滴加几滴酸性高锰酸钾溶
A 白葡萄酒中含有SO
液,溶液紫色褪去 2
将等浓度等体积的Na[Al(OH)]溶液与
B 4 二者水解相互促进生成氢氧化铝沉淀
NaHCO 溶液混合有白色沉淀生成
3
向2mL0.1mol·L−1NaCl溶液中滴加2滴
0.1mol·L−1AgNO 溶液,有白色沉淀生成;
C 3 K (AgCl)>K (AgI)
振荡试管,再滴加2滴0.1mol·L−1KI溶 sp sp
液,有黄色沉淀生成
将Fe(NO ) 溶液加到HI溶液中,充分溶解
3 3
D 后,滴入CCl 后振荡、静置,观察CCl 层 证明氧化性:Fe3+>I
4 4 2
颜色变化
A. A B. B C. C D. D
12. 室温下,通过下列实验探究NaHSO 溶液的性质。
3
实验1:用pH试纸测量0.1mol•L-1NaHSO 溶液的pH,测得pH约为5。
3
实验2:向10mL0.1mol•L-1NaHSO 溶液中加入等体积0.1mol•L-1氨水,充分混合后,溶液pH约为9。
3
实验3:向10mL0.1mol•L-1NaCO 溶液中滴加几滴0.1mol•L-1NaHSO 溶液,无明显现象。
2 3 3实验4:向10mL0.1mol•L-1NaHSO 溶液中加入过量Ba(OH) 溶液,产生白色沉淀。
3 2
下列有关说法正确的是
A. 由实验1可得出:
B. 实验2所得溶液中存在:
C. 由实验3可得出:K (H SO )<K (H CO)
a2 2 3 a1 2 3
D. 实验4反应后的上层清液中:
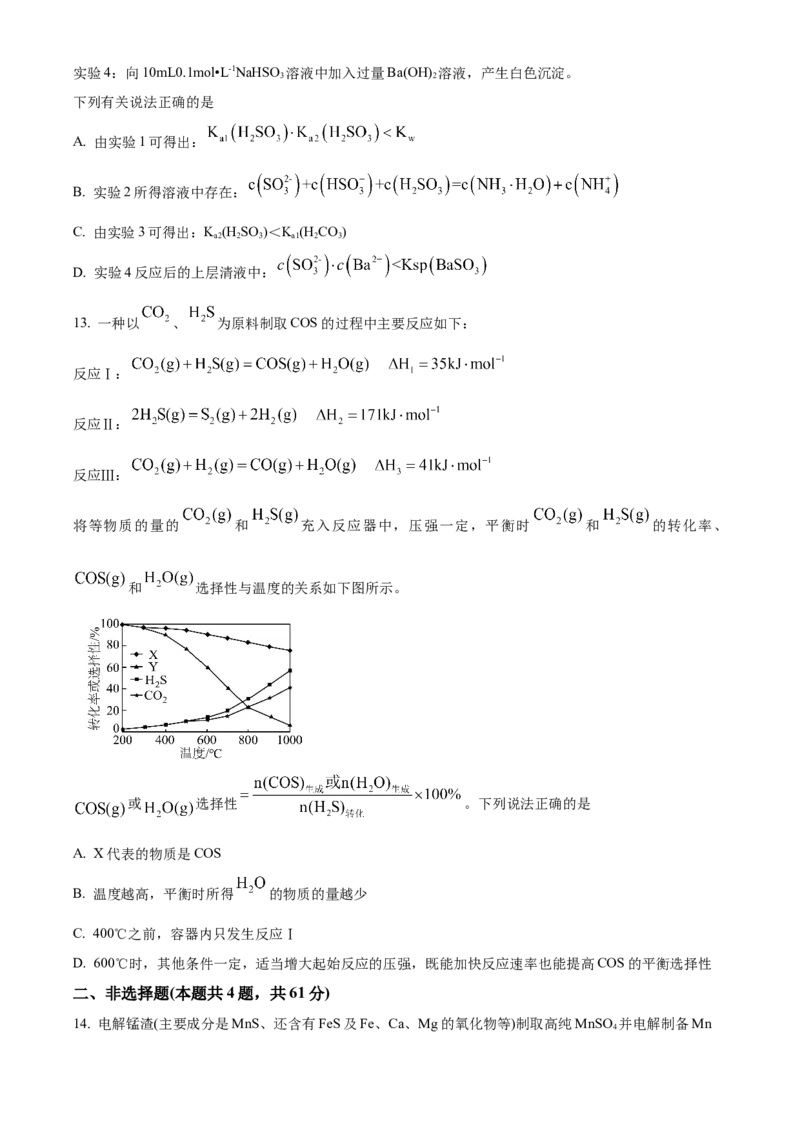
13. 一种以 、 为原料制取COS的过程中主要反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
将等物质的量的 和 充入反应器中,压强一定,平衡时 和 的转化率、
和 选择性与温度的关系如下图所示。
或 选择性 。下列说法正确的是
A. X代表的物质是COS
B. 温度越高,平衡时所得 的物质的量越少
C. 400℃之前,容器内只发生反应Ⅰ
D. 600℃时,其他条件一定,适当增大起始反应的压强,既能加快反应速率也能提高COS的平衡选择性
二、非选择题(本题共4题,共61分)
14. 电解锰渣(主要成分是MnS、还含有FeS及Fe、Ca、Mg的氧化物等)制取高纯MnSO 并电解制备Mn
4的流程如下:
(1)氧化酸浸。酸浸后浸出液中主要离子为Mn2+、H+、 、Fe3+、Ca2+、Mg2+。写出FeS酸浸时发生反
应的离子方程式_______。
(2)沉铁。常温下,Fe3+开始生成氢氧化物沉淀的pH=1.7,完全沉淀时pH=2.8(某离子浓度≤1×10-
5mol/L,认为该离子沉淀完全)。酸浸后的溶液调节pH至4后,溶液中残留的c(Fe3+)=_______mol·L-1。
(3)萃取与反萃取。向沉铁后的溶液加入某有机萃取剂HA,在不同pH下进行萃取可以实现Ca2+、
Mn2+的分离。萃取原理为M2++2HA⇌MA
2
+2H+(M2+表示Ca2+或Mn2+),过程如图。
已知:某温度下M2++2HA⇌MA
2
+2H+的平衡常数用K表示,且K(CaA
2
)>K(MnA
2
)。上述过程中前后调节
pH值大小为a_______b(填“>”或“<”)
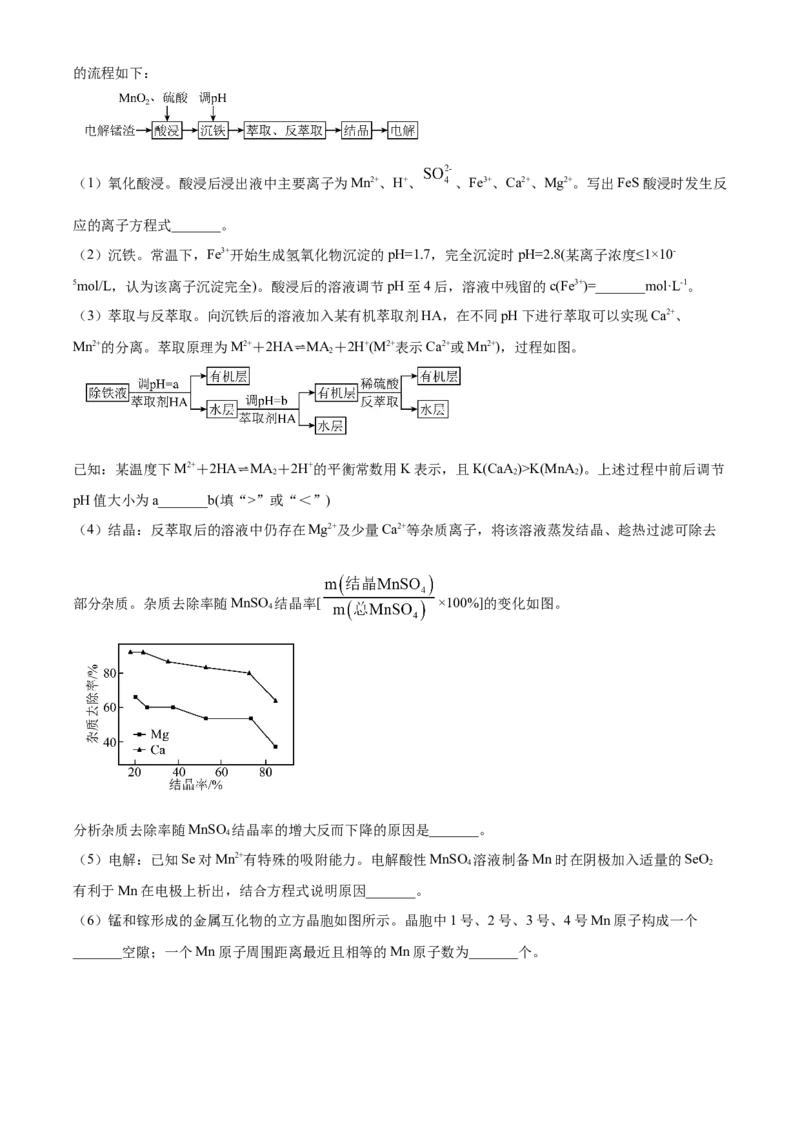
(4)结晶:反萃取后的溶液中仍存在Mg2+及少量Ca2+等杂质离子,将该溶液蒸发结晶、趁热过滤可除去
部分杂质。杂质去除率随MnSO 结晶率[ ×100%]的变化如图。
4
分析杂质去除率随MnSO 结晶率的增大反而下降的原因是_______。
4
(5)电解:已知Se对Mn2+有特殊的吸附能力。电解酸性MnSO 溶液制备Mn时在阴极加入适量的SeO
4 2
有利于Mn在电极上析出,结合方程式说明原因_______。
(6)锰和镓形成的金属互化物的立方晶胞如图所示。晶胞中1号、2号、3号、4号Mn原子构成一个
_______空隙;一个Mn原子周围距离最近且相等的Mn原子数为_______个。15. 化合物G 是一种药物合成中间体,人工合成路线如图:
(1)化合物D中的含氧官能团除羟基外,还有_______。
(2)A→B中生成的另一有机产物为_______。
(3)(C H)N有利于D→E的转化,原因是_______。
2 5 3
(4)写出同时满足下列条件 的一种同分异构体,_______。
除苯环外不含其它环状结构;含有3种不同化学环境的氢原子;含有2种官能团。
(5)请设计以 和乙炔为原料制备 的合成路线_______(无机试
剂和有机溶剂任用,合成路线示例见本题题干)。
16. 亚硫酰氯(SOCl )是一种无色或淡黄色液体(熔点-105℃,沸点79℃),有强烈刺激性气味,遇水剧烈反
2
应生成两种酸性气体,常用作脱水剂。
(1)实验室用SCl 、SO 与Cl 在活性炭催化加热条件下制取SOCl ,部分装置(夹持、加热装置略去)如图
2 2 2 2
所示。
①三颈烧瓶中发生反应的化学方程式为_______。②碱石灰的作用为_______。
(2)测定样品中SOCl 的纯度。准确称量2.55gSOCl 样品,将其完全溶解于300mLNaOH溶液中,发生反
2 2
应:SOCl +4NaOH=Na SO +2NaCl+2HO。将反应后的溶液稀释到500mL;取50mL稀释后的溶液于碘
2 2 3 2
量瓶,滴加盐酸至NaOH恰好完全反应;再加入50.00mL0.0500mol·L-1I 溶液充分反应,用
2
0.1000mol·L-1NaSO 溶液滴定过量的I(I+2NaSO=2NaI+NaSO)。平行滴定三次,反应消耗NaSO
2 2 3 2 2 2 2 3 2 4 6 2 2 3
溶液的平均体积为20.00mL。则样品中SOCl 的质量分数为_______(写出计算过程)。
2
(3)实验室常利用SOCl 和FeCl ·4H O混合加热制取无水FeCl ,但不使用SOCl 与FeCl ·6H O制取无水
2 2 2 2 2 3 2
FeCl ,其原因 是可能发生副反应导致产品不纯。
3
①SOCl 与FeCl ·6H O发生副反应的可能原因是_______。
2 3 2
②为验证副反应的可能性,请补充完整实验方案:取少量FeCl ·6H O于试管中,_______。则证明发生了
3 2
副反应。(实验中必须使用的试剂:SOCl 、NaOH溶液、K[Fe(CN) ]溶液)
2 3 6
17. 资源化利用具有重要意义。
(1)电催化制取甲烷。
①酸性条件下,向阴极通入 ,反应生成 的电极反应式为______。
②实际电解时,需控制pH约为7.当其他条件相同时,pH减小, 的产率降低,可能的原因是______。
(2)光催化制乙烯。 、 、三乙胺( )在催化剂作用下,光照一段时间可制得
。
①催化剂中含 。常温下,将 溶液和 溶液混合制备
。已知: , 、 、
。
反应 的平衡常数K的数值为______。
制备 时, 溶液与 溶液的混合方式为______。
②用同位素示踪法研究乙烯分子中C和H的来源。在其他条件相同时,三乙胺( 分别与下列三组试剂反应,得到乙烯的质谱中最大质荷比均为28。能证明C和H均来源于三乙胺的一组试剂是______(填
序号)。
A. 和 B. 和 C. 和
若以 代替三乙胺发生上述反应,生成的烯烃有乙烯和______(填结构简式)。
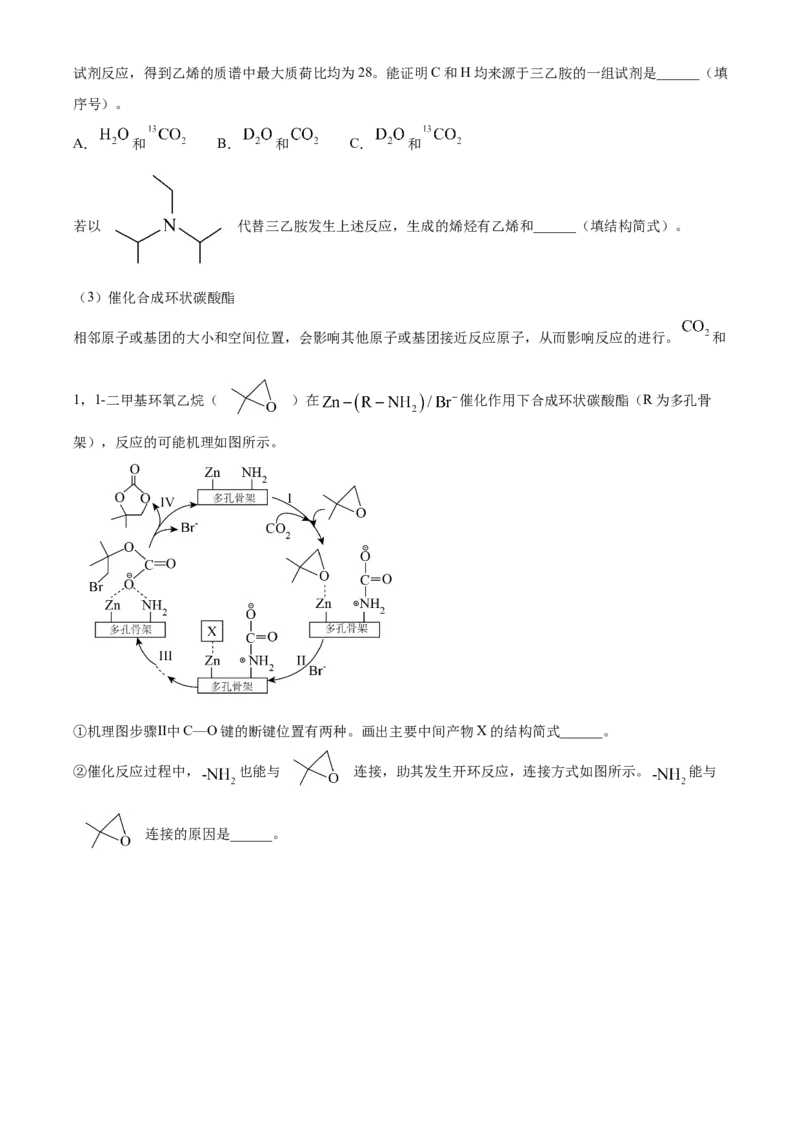
(3)催化合成环状碳酸酯 。
相邻原子或基团的大小和空间位置,会影响其他原子或基团接近反应原子,从而影响反应的进行。 和
1,1-二甲基环氧乙烷( )在 催化作用下合成环状碳酸酯(R为多孔骨
架),反应的可能机理如图所示。
①机理图步骤Ⅱ中C—O键的断键位置有两种。画出主要中间产物X的结构简式______。
②催化反应过程中, 也能与 连接,助其发生开环反应,连接方式如图所示。 能与
连接的原因是______。