文档内容
2026届高三九校联合模拟考试
化学科试题
本试卷满分100分,考试时间75分钟。
注意事项:
1.答卷前,考生务必将条形码粘贴在答题卡相应位置,并且把自己的姓名、准考证号
填写在答题卡上。
2.答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。答非选择题时,将答案写在答题卡相应
位置上。写在本试卷上无效。
3.考试结束后,只上交答题卡,试卷不回收。
4.可能用到的相对原子质量:H1 Li7 N14 O16 P31 Fe56
一.选择题(共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求)
1. 吉林省历史悠久,自古就有人类活动的迹象,是东北亚诸多民族活动的场所,为人类
留下了璀璨的文化。下列说法正确的是:
A.“黄龙府”为今农安,“农安辽塔”建筑用的青砖主要成分是Fe O
2 3
B. 农安左家山出土的“中华第一龙”——玉石龙,玉石属于合金
C. 公主岭被誉为“中国玉米之乡”,玉米中的主要成分——淀粉属于糖类
D. 辽源煤炭开采历史长达百年,煤的液化属于物理变化
2. 我国科学家在“液态阳光”(利用太阳能将CO₂转化为甲醇)研究上取得重大进展,其
关键反应之一为CO₂+3H₂→CH OH+H O。下列相关化学用语表述正确的是( )
3 2
A.CO 为含极性键的极性分子
2
B. 产物CH₃OH中碳原子的杂化方式:sp³
C. 产物H₂O的VSEPR模型:
D. 中间产物HCOOH(甲酸)分子中σ键与π键的数目之比为 3:1
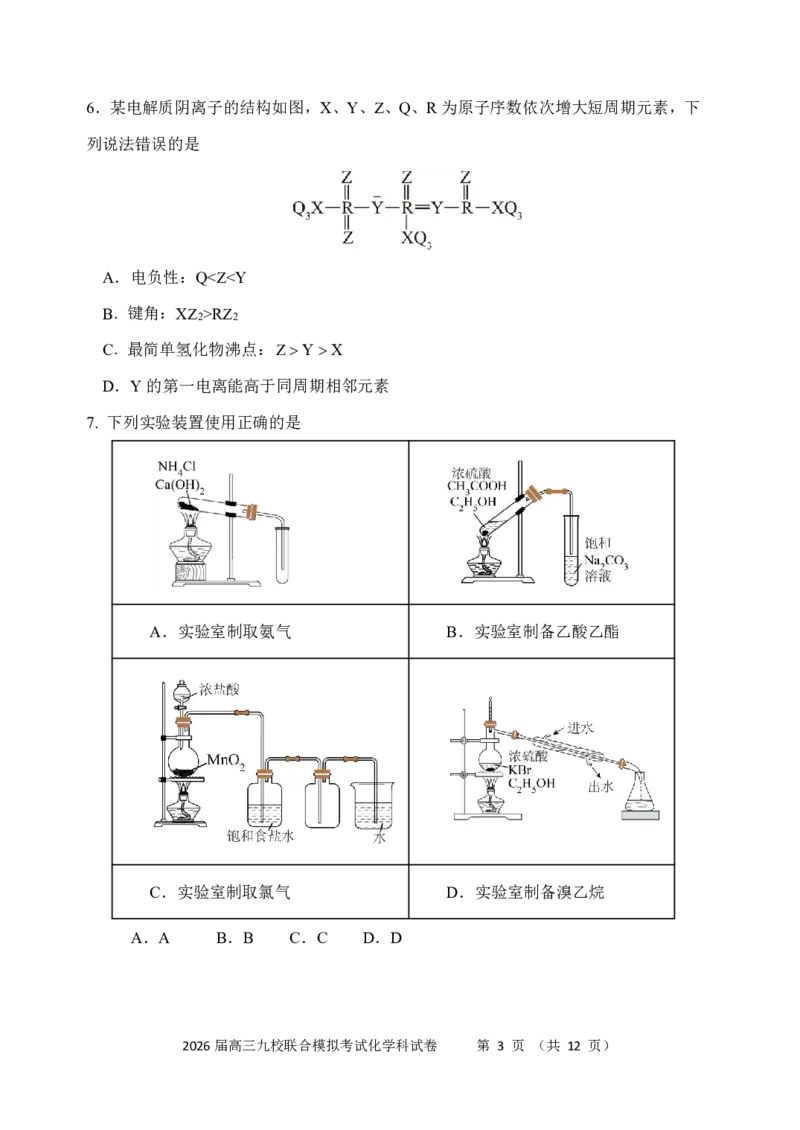
2026届高三九校联合模拟考试化学科试卷 第 1 页 (共 12 页)3. 下列反应的离子方程式书写正确的是
A. 用醋酸和淀粉-KI溶液检验加碘盐中的IO:IO 5I 6H 3I 3H O
3 3 2 2
B. 向NaClO溶液中通入少量SO :ClO SO H OSO2 Cl 2H
2 2 2 4
C. 向H 18O 中加入H SO 酸化的KMnO 溶液:
2 2 2 4 4
5H 18O +2MnO -+6H+===518O ↑+2Mn2++8H O
2 2 4 2 2
D.牺牲阳极法保护海水中钢闸门的正极反应:2H O+4e-===O ↑+4OH-
2 2
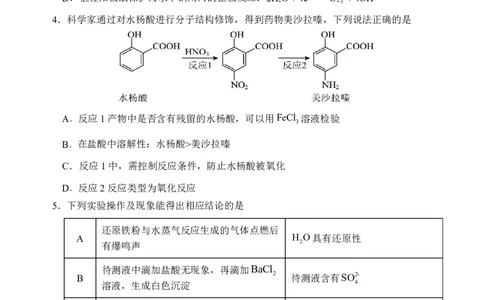
4.科学家通过对水杨酸进行分子结构修饰,得到药物美沙拉嗪,下列说法正确的是
A.反应1产物中是否含有残留的水杨酸,可以用FeCl 溶液检验
3
B.在盐酸中溶解性:水杨酸>美沙拉嗪
C.反应1中,需控制反应条件,防止水杨酸被氧化
D.反应2反应类型为氧化反应
5.下列实验操作及现象能得出相应结论的是
还原铁粉与水蒸气反应生成的气体点燃后
A H O具有还原性
有爆鸣声 2
待测液中滴加盐酸无现象,再滴加BaCl
B 2 待测液含有SO2-
溶液,生成白色沉淀 4
Mg(OH) 和Al(OH) 中均分别加入
2 3
C NaOH溶液和盐酸,Mg(OH) 只溶于盐 Mg(OH) 比Al(OH) 碱性弱
2 2 3
酸,Al(OH) 都能溶
3
K CrO 溶液中滴加NaOH溶液,溶液由 加入NaOH溶液,发生了氧化还原
2 2 7
D
橙色变为黄色 反应
A. A B.B C.C D.D
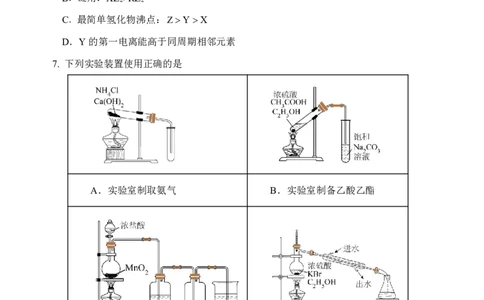
2026届高三九校联合模拟考试化学科试卷 第 2 页 (共 12 页)6.某电解质阴离子的结构如图,X、Y、Z、Q、R为原子序数依次增大短周期元素,下
列说法错误的是
A.电负性:QRZ
2 2
C.最简单氢化物沸点:ZYX
D.Y的第一电离能高于同周期相邻元素
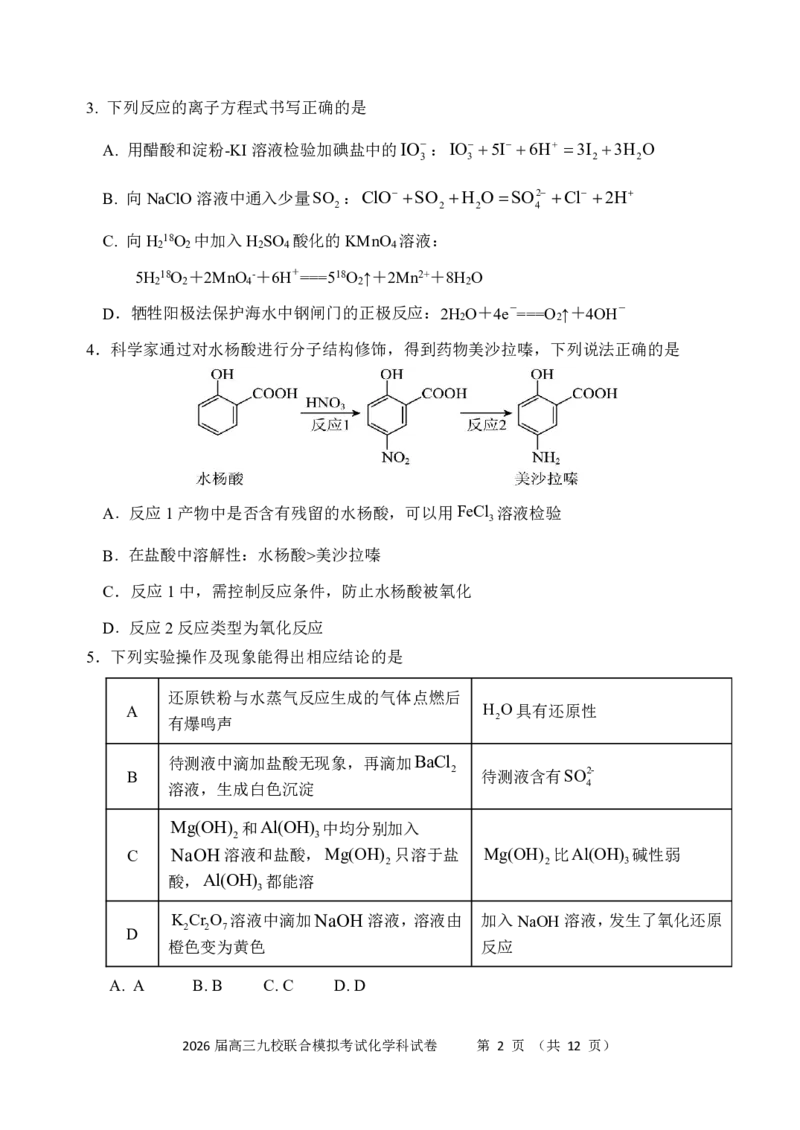
7. 下列实验装置使用正确的是
A.实验室制取氨气 B.实验室制备乙酸乙酯
C.实验室制取氯气 D.实验室制备溴乙烷
A.A B.B C.C D.D
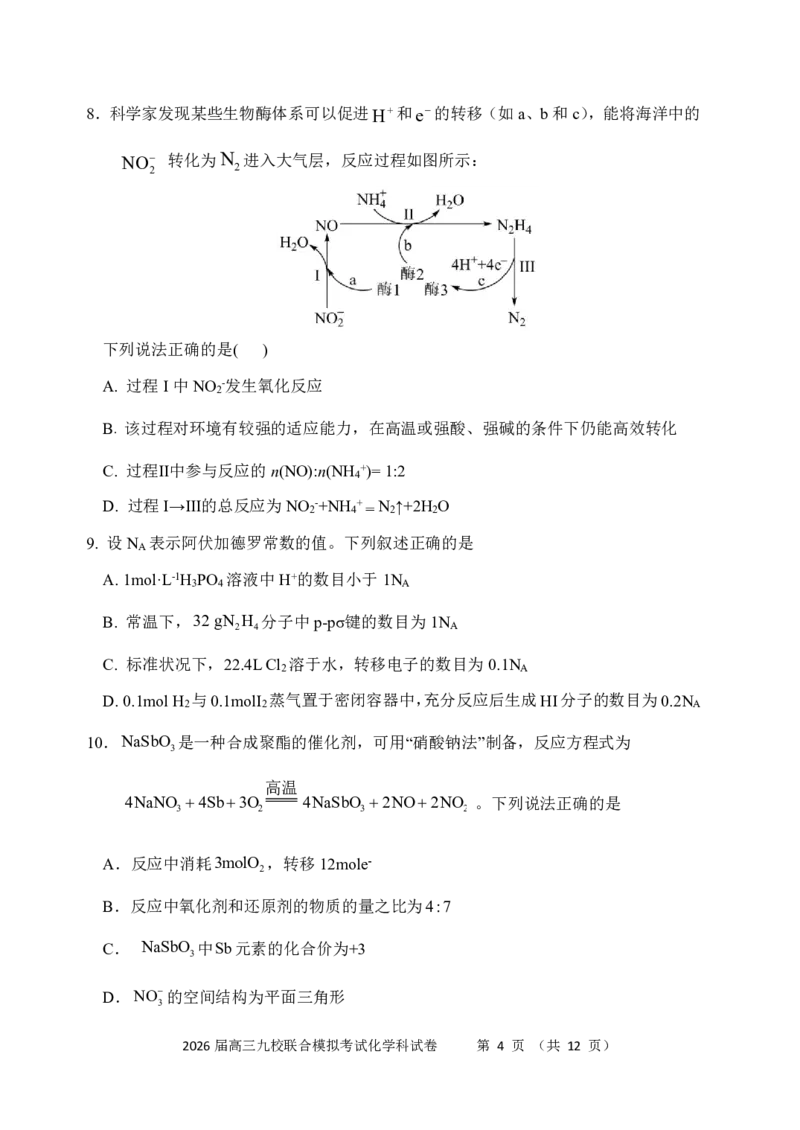
2026届高三九校联合模拟考试化学科试卷 第 3 页 (共 12 页)8.科学家发现某些生物酶体系可以促进H+和e的转移(如a、b和c),能将海洋中的
NO 转化为N 进入大气层,反应过程如图所示:
2 2
下列说法正确的是( )
A. 过程I中NO -发生氧化反应
2
B. 该过程对环境有较强的适应能力,在高温或强酸、强碱的条件下仍能高效转化
C. 过程Ⅱ中参与反应的n(NO):n(NH +)=1:2
4
D. 过程I→Ⅲ的总反应为NO
2
-+NH
4
+=N
2
↑+2H
2
O
9. 设N 表示阿伏加德罗常数的值。下列叙述正确的是
A
A.1mol·L-1H PO 溶液中H+的数目小于1N
3 4 A
B. 常温下,32 gN H 分子中p-pσ键的数目为1N
2 4 A
C. 标准状况下,22.4LCl 溶于水,转移电子的数目为0.1N
2 A
D.0.1molH 与0.1molI 蒸气置于密闭容器中,充分反应后生成HI分子的数目为0.2N
2 2 A
10.NaSbO 是一种合成聚酯的催化剂,可用“硝酸钠法”制备,反应方程式为
3
高温
4NaNO 4Sb3O 4NaSbO 2NO2NO 。下列说法正确的是
3 2 3 2
A.反应中消耗3molO ,转移12mole-
2
B.反应中氧化剂和还原剂的物质的量之比为4:7
C. NaSbO 中Sb元素的化合价为+3
3
D.NO的空间结构为平面三角形
3
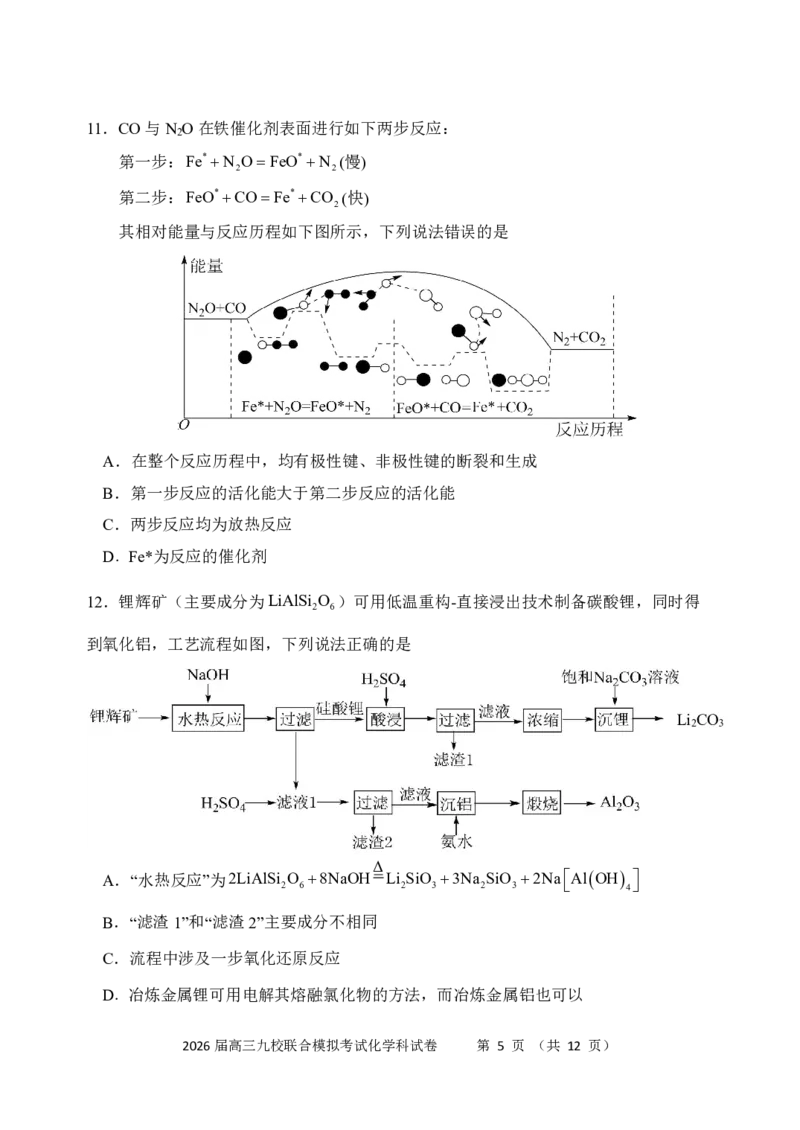
2026届高三九校联合模拟考试化学科试卷 第 4 页 (共 12 页)11.CO与N O在铁催化剂表面进行如下两步反应:
2
第一步:Fe*N OFeO*N (慢)
2 2
第二步:FeO*COFe*CO (快)
2
其相对能量与反应历程如下图所示,下列说法错误的是
A.在整个反应历程中,均有极性键、非极性键的断裂和生成
B.第一步反应的活化能大于第二步反应的活化能
C.两步反应均为放热反应
D.Fe*为反应的催化剂
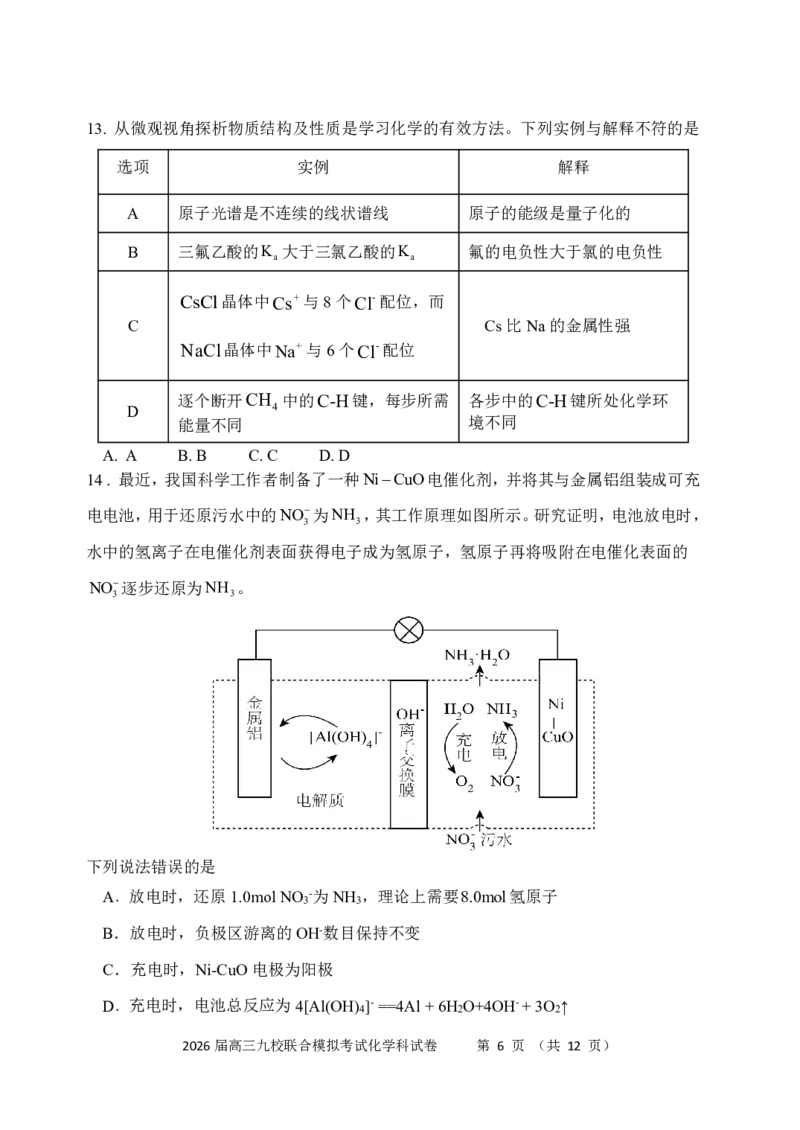
12.锂辉矿(主要成分为LiAlSi O )可用低温重构-直接浸出技术制备碳酸锂,同时得
2 6
到氧化铝,工艺流程如图,下列说法正确的是
Li CO
2 3
Δ
A.“水热反应”为2LiAlSi
2
O
6
8NaOH Li
2
SiO
3
3Na
2
SiO
3
2Na
AlOH
4
B.“滤渣1”和“滤渣2”主要成分不相同
C.流程中涉及一步氧化还原反应
D.冶炼金属锂可用电解其熔融氯化物的方法,而冶炼金属铝也可以
2026届高三九校联合模拟考试化学科试卷 第 5 页 (共 12 页)13. 从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是
选项 实例 解释
A 原子光谱是不连续的线状谱线 原子的能级是量子化的
B 三氟乙酸的K 大于三氯乙酸的K 氟的电负性大于氯的电负性
a a
CsCl晶体中Cs+与8个Cl-配位,而
C Cs比Na的金属性强
NaCl晶体中Na+与6个Cl-配位
逐个断开CH 中的C-H键,每步所需 各步中的C-H键所处化学环
D 4
能量不同 境不同
A. A B.B C.C D.D
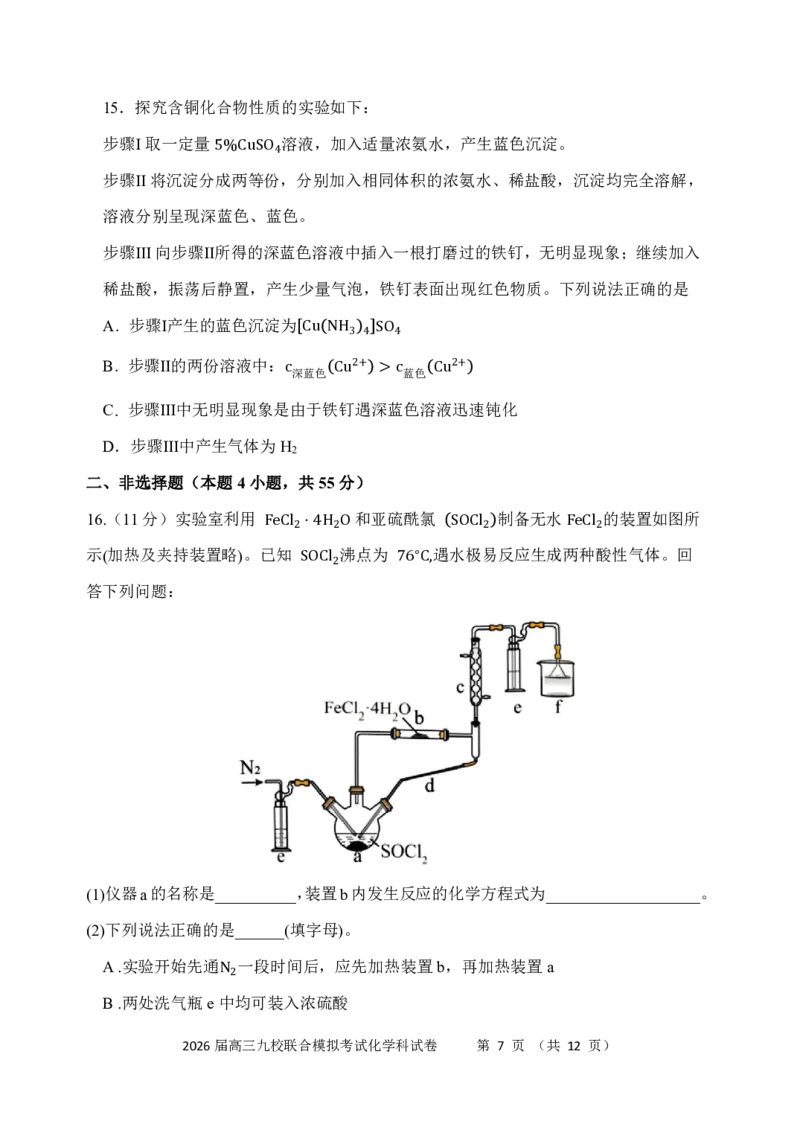
14. 最近,我国科学工作者制备了一种NiCuO电催化剂,并将其与金属铝组装成可充
电电池,用于还原污水中的NO为NH ,其工作原理如图所示。研究证明,电池放电时,
3 3
水中的氢离子在电催化剂表面获得电子成为氢原子,氢原子再将吸附在电催化表面的
NO逐步还原为NH 。
3 3
下列说法错误的是
A.放电时,还原1.0molNO -为NH ,理论上需要8.0mol氢原子
3 3
B.放电时,负极区游离的OH-数目保持不变
C.充电时,Ni-CuO电极为阳极
D.充电时,电池总反应为4[Al(OH) ]-==4Al+6H O+4OH-+3O ↑
4 2 2
2026届高三九校联合模拟考试化学科试卷 第 6 页 (共 12 页)15.探究含铜化合物性质的实验如下:
步骤Ⅰ取一定量 溶液,加入适量浓氨水,产生蓝色沉淀。
步骤Ⅱ将沉淀分5成%两Cu等SO份4,分别加入相同体积的浓氨水、稀盐酸,沉淀均完全溶解,
溶液分别呈现深蓝色、蓝色。
步骤Ⅲ向步骤Ⅱ所得的深蓝色溶液中插入一根打磨过的铁钉,无明显现象;继续加入
稀盐酸,振荡后静置,产生少量气泡,铁钉表面出现红色物质。下列说法正确的是
A.步骤Ⅰ产生的蓝色沉淀为
B.步骤Ⅱ的两份溶液中: Cu NH3 4 SO4
深蓝色 蓝色
2+ 2+
c Cu >c Cu
C.步骤Ⅲ中无明显现象是由于铁钉遇深蓝色溶液迅速钝化
D.步骤Ⅲ中产生气体为H
2
二、非选择题(本题4小题,共55分)
16.(11分)实验室利用 和亚硫酰氯 制备无水 的装置如图所
示(加热及夹持装置略)。已Fe知Cl2⋅4H2沸O 点为 遇水SO极Cl易2 反应生成两Fe种Cl酸2 性气体。回
∘
答下列问题: SOCl2 76 C,
(1)仪器a的名称是__________,装置b内发生反应的化学方程式为___________________。
(2)下列说法正确的是______(填字母)。
A.实验开始先通 一段时间后,应先加热装置b,再加热装置a
B.两处洗气瓶e中N2均可装入浓硫酸
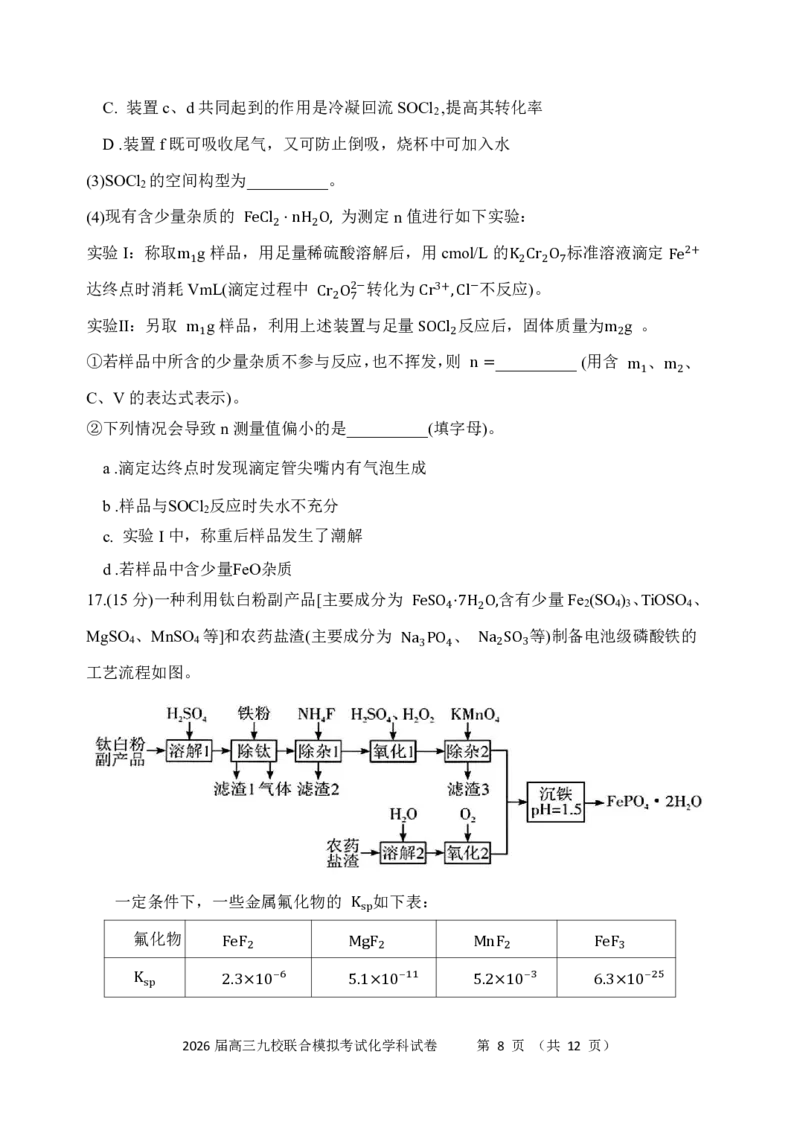
2026届高三九校联合模拟考试化学科试卷 第 7 页 (共 12 页)C. 装置c、d共同起到的作用是冷凝回流SOCl ,提高其转化率
2
D.装置f既可吸收尾气,又可防止倒吸,烧杯中可加入水
(3)SOCl 的空间构型为__________。
2
(4)现有含少量杂质的 为测定n值进行如下实验:
实验I:称取 g样品,Fe用Cl2足⋅量nH稀2O硫, 酸溶解后,用cmol/L的 标准溶液滴定
2+
达终点时消耗mV 1 mL(滴定过程中 转化为 不反K应2C)。r2O7 Fe
2− 3+ −
实验Ⅱ:另取 g样品,利用上述Cr装2O置7 与足量 Cr ,C反l应后,固体质量为 g 。
①若样品中所含m1的少量杂质不参与反应,也不挥S发O,C则l2 __________(用含m2 、 、
C、V的表达式表示)。 n= m1 m2
②下列情况会导致n测量值偏小的是__________(填字母)。
a.滴定达终点时发现滴定管尖嘴内有气泡生成
b.样品与SOCl 反应时失水不充分
2
c. 实验I中,称重后样品发生了潮解
d.若样品中含少量FeO杂质
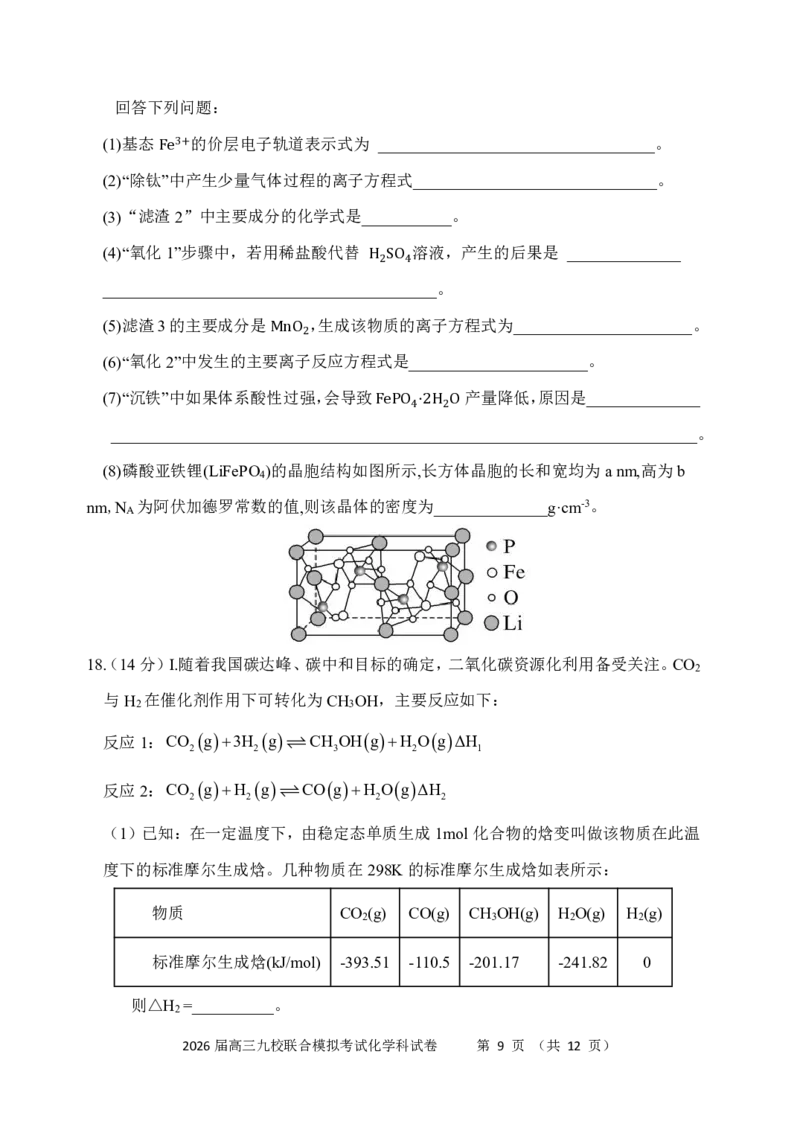
17.(15分)一种利用钛白粉副产品[主要成分为 含有少量Fe (SO ) 、TiOSO 、
2 4 3 4
MgSO 、MnSO 等]和农药盐渣(主要成分为 FeSO4⋅、7H2O, 等)制备电池级磷酸铁的
4 4
工艺流程如图。 Na3PO4 Na2SO3
一定条件下,一些金属氟化物的 如下表:
氟化物 Ksp
FeF₂ MgF₂ MnF₂ FeF₃
Ksp
2.3×10⁻⁶ 5.1×10⁻¹¹ 5.2×10⁻³ 6.3×10⁻²⁵
2026届高三九校联合模拟考试化学科试卷 第 8 页 (共 12 页)回答下列问题:
(1)基态 的价层电子轨道表示式为 __________________________________。
3+
(2)“除钛F”e中产生少量气体过程的离子方程式______________________________。
(3)“滤渣2”中主要成分的化学式是___________。
(4)“氧化1”步骤中,若用稀盐酸代替 溶液,产生的后果是 ______________
_________________________________H_ 2 _S_O__ 4 ___。
(5)滤渣3的主要成分是 ,生成该物质的离子方程式为______________________。
(6)“氧化2”中发生的主要M离nO子2反应方程式是______________________。
(7)“沉铁”中如果体系酸性过强,会导致 产量降低,原因是______________
_________________________________F_e_P_O_ 4 _⋅_2_H_ 2 _O______________________________。
(8)磷酸亚铁锂(LiFePO )的晶胞结构如图所示,长方体晶胞的长和宽均为anm,高为b
4
nm,N 为阿伏加德罗常数的值,则该晶体的密度为______________g·cm-3。
A
18.(14分)I.随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用备受关注。CO
2
与H 在催化剂作用下可转化为CH OH,主要反应如下:
2 3
反应1:CO g3H g CH OHgH OgΔH
2 2 3 2 1
反应2:CO gH g COgH OgΔH
2 2 2 2
(1)已知:在一定温度下,由稳定态单质生成1mol化合物的焓变叫做该物质在此温
度下的标准摩尔生成焓。几种物质在298K的标准摩尔生成焓如表所示:
物质 CO (g) CO(g) CH OH(g) H O(g) H (g)
2 3 2 2
标准摩尔生成焓(kJ/mol) -393.51 -110.5 -201.17 -241.82 0
则△H =__________。
2
2026届高三九校联合模拟考试化学科试卷 第 9 页 (共 12 页)II.铅酸电池是用途广泛并不断发展的化学电源。
(2)十九世纪,铅酸电池工作原理初步形成并延续至今。
铅酸电池工作原理:PbO +Pb+2H SO 放 电 2PbSO +2H O
2 2 4 充电 4 2
①充电时,阳极发生的电极反应为 ______________________________________。
②放电时,产生a库仑电量,则两电极质量变化之差为 __________g(用计算式表达
即可)。已知:转移1mol电子所产生的电量为96500库仑。
③铅酸电池储存过程中,存在化学能的缓慢消耗:PbO 电极在H SO 作用下产生的
2 2 4
O 可将Pb电极氧化。O 氧化Pb发生反应的化学方程式为 ________________________。
2 2
(3)随着铅酸电池广泛应用,需要回收废旧电池材料,实现资源的再利用。回收过程
中主要物质的转化关系示意图如下。
①将PbSO 等物质转化为Pb2+的过程中,步骤I加入NaOH溶液的目的是_______ 。
4
②步骤Ⅱ、Ⅲ中H O 和K S O 作用分别是____________________________________。
2 2 2 2 8
(4)铅酸电池使用过程中,负极因生成导电性差的大颗粒PbSO ,导致电极逐渐失活。
4
通过向负极添加石墨、多孔碳等碳材料,可提高铅酸电池性能。碳材料的作用有 ____(填
序号)。
a.增强负极导电性
b.增大负极材料比表面积,利于生成小颗粒PbSO
4
c.碳材料作还原剂,使PbO 被还原
2
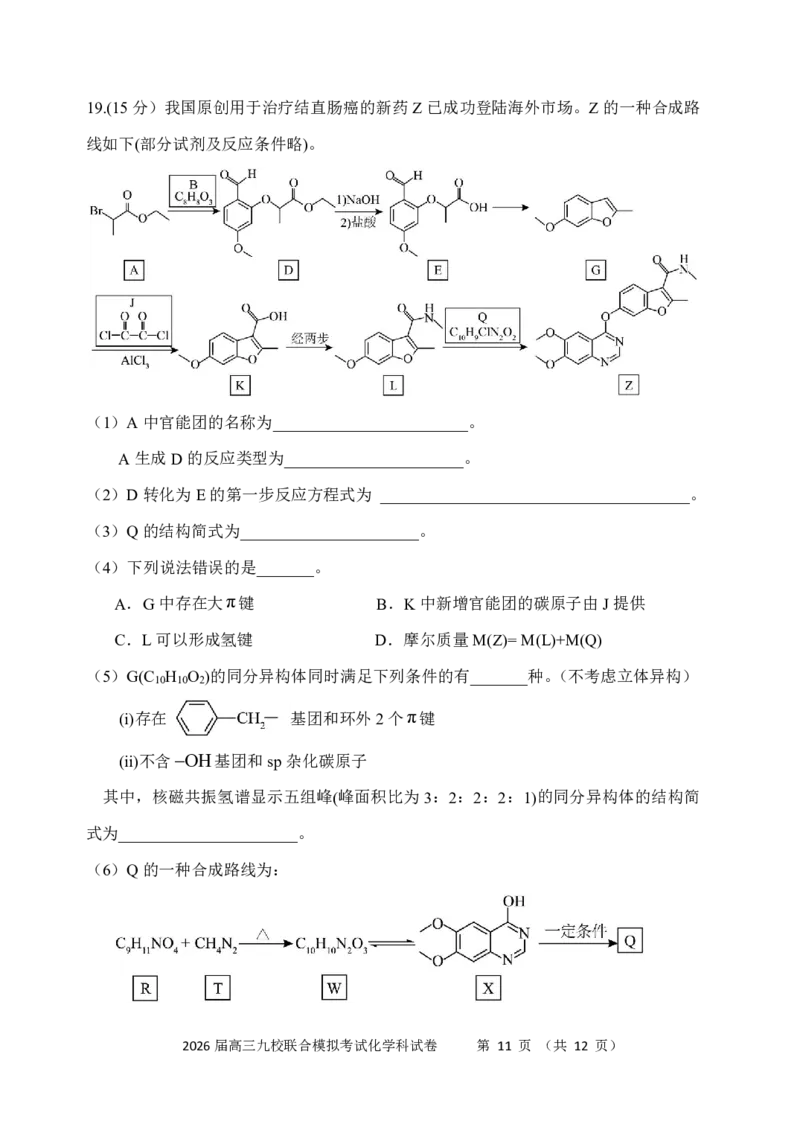
2026届高三九校联合模拟考试化学科试卷 第 10 页 (共 12 页)19.(15分)我国原创用于治疗结直肠癌的新药Z已成功登陆海外市场。Z的一种合成路
线如下(部分试剂及反应条件略)。
(1)A中官能团的名称为________________________。
A生成D的反应类型为______________________。
(2)D转化为E的第一步反应方程式为 ______________________________________。
(3)Q的结构简式为______________________。
(4)下列说法错误的是_______。
A.G中存在大π键 B.K中新增官能团的碳原子由J提供
C.L可以形成氢键 D.摩尔质量M(Z)=M(L)+M(Q)
(5)G(C H O )的同分异构体同时满足下列条件的有_______种。(不考虑立体异构)
10 10 2
(i)存在 基团和环外2个π键
(ii)不含OH基团和sp杂化碳原子
其中,核磁共振氢谱显示五组峰(峰面积比为3:2:2:2:1)的同分异构体的结构简
式为______________________。
(6)Q的一种合成路线为:
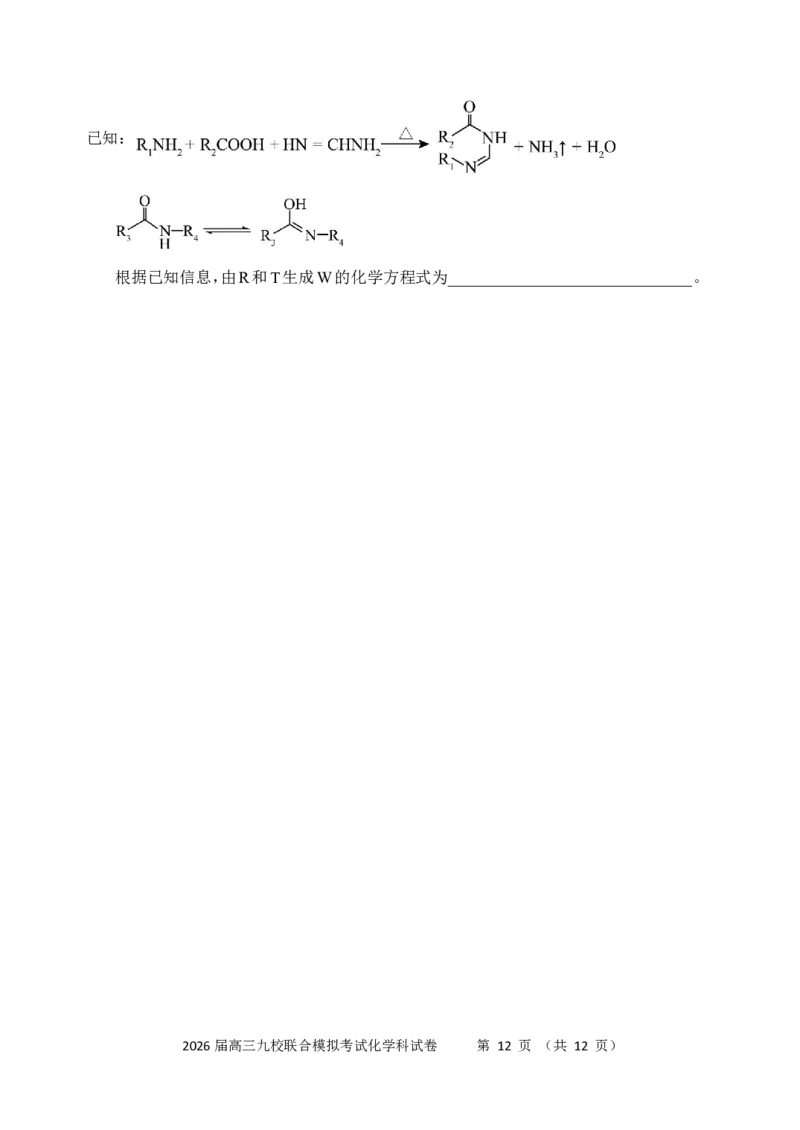
2026届高三九校联合模拟考试化学科试卷 第 11 页 (共 12 页)已知:
根据已知信息,由R和T生成W的化学方程式为______________________________。
2026届高三九校联合模拟考试化学科试卷 第 12 页 (共 12 页)2026 届高三九校联合模拟考试
化学科试题答案
一.选择题(共15小题,每小题 3分,共 45分。每小题只有一个选项符合题目要求)
1-5CBCCB 6-10ABDBD 11-15AACBD
二、非选择题(本题 4小题,共 55分)
16 题:(11分)
(1)三颈烧瓶 (1分,写错字不给分) FeCl ∙4H O+4SOCl (g) FeCl +4SO +8HCl (2分,
2 2 2 2 2
反应物和生成物均写对给1分,有错误不给分,系数配平和条件及气体(g)给1分)
(2)B C (2分,每个选项各1分,有错误选项不给分)
(3)三角锥形 (2分,有错字不给分)
1000m -m ( )
(4) ① 1 2 或 (2分,只要表达式正确就给分) ② bd (2
108cV
250 1− 2
分,每个选项各1分,有错误选
27
项
不给分)
17题: (15分)
(1) (1分)
(2) Fe+2H+ =Fe2++H ↑ (2分,反应物和生成物均写对给1分,有错误不给分,系数配
2
平和气体箭头给1分)
(3) MgF (2分)
2
(4) 盐酸与高锰酸钾溶液反应生成氯气,污染空气 (2分,答出氯气和答出污染各1分)
(5) 2MnO -+3Mn2++2H O=5MnO ↓+4H+ (2分,反应物和生成物均写对给1分,有错误
4 2 2
不给分,系数配平和沉淀箭头给1分)
(6)2SO 2-+O =2SO 2- (2分,反应物和生成物均写对给1分,有错误不给分,系数配
3 2 4
平给1分)
(7)溶液中氢离子浓度增大,磷元素主要以H PO 、H PO -、HPO 2-形式存在,使PO 3-
3 4 2 4 4 4
浓度降低(1分),生成FePO .2H O沉淀量少 (1分)
4 2
(8) (2分,只要表达式正确就给分)
23
6.32×10
18:(1 a 4 b 2 N 分 A )(每空 2分)
(1)+41.19 kJ/mol (数值算对给1分,“+”号和单位给1分)
(2) ① PbSO +2H O-2e-=PbO +SO 2-+4H+ (2分,反应物和生成物均写对给1分,有错
4 2 2 4
误不给分,系数配平给1分) ② 16 (2 分,表达式正确即可给分)
2026届高三九校联合模拟考试9化65学00科 × 试题答案 第 1 页 (共 2 页)③ 2Pb+O +2H SO =2PbSO +2H O (2分,反应物和生成物均写对给1分,有错误不给分,
2 2 4 4 2
系数配平给1分)
(3)① 使硫酸铅转化为氢氧化铅(1分),便于后续的溶解(1分)。
②H O 的作用为还原剂(1分),K S O 的作用为氧化剂 (1分)。
2 2 2 2 8
(4)ab (2 分,每个选项各1分,有错误选项不给分)
19(15分)
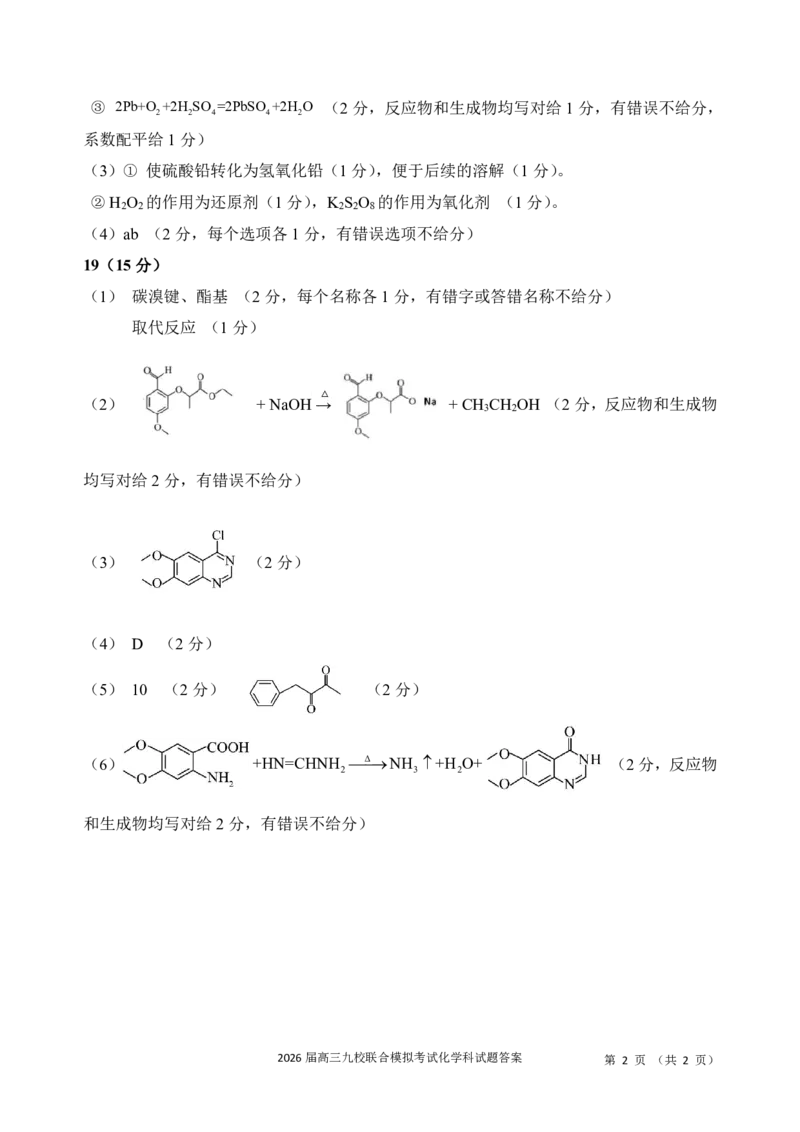
(1) 碳溴键、酯基 (2分,每个名称各1分,有错字或答错名称不给分)
取代反应 (1分)
△
(2) + NaOH→ + CH CH OH (2分,反应物和生成物
3 2
均写对给2分,有错误不给分)
(3) (2分)
(4) D (2分)
(5) 10 (2分) (2分)
(6) +HN=CHNH ΔNH +H O+ (2分,反应物
2 3 2
和生成物均写对给2分,有错误不给分)
2026届高三九校联合模拟考试化学科试题答案 第 2 页 (共 2 页)