文档内容
2025~2026 学年 12 月七校联合学情调研
高三化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 V 51 Mn 55 Fe 56
一、单项选择题:共 13 题,每题 3 分,共 39 分。每题只有一个选项最符合题
意。
1.下列工业生产中,不涉及氧化还原反应的是
A.工业合成氨 B. 接触法制硫酸 C. 侯德榜制碱法 D. 高炉炼铁
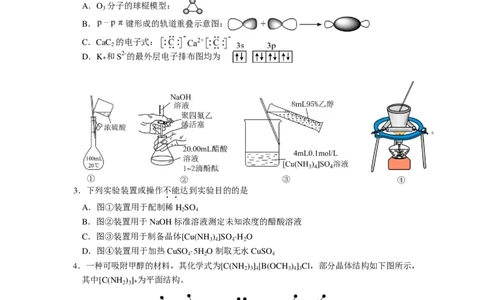
2.下列化学用语或图示表达正确的是
A.O 分子的球棍模型:
3
B. 键形成的轨道重叠示意图:
C.CaC 的电子式:
2
D.K+ 和 S2-的最外层电子排布图均为
3.下列实验装置或操作不能达到实验目的的是
A.图①装置用于配制稀 H SO
2 4
B.图②装置用于 NaOH 标准溶液测定未知浓度的醋酸溶液
C.图③装置用于制备晶体[Cu(NH ) ]SO ·H O
3 4 4 2
D.图④装置用于加热 CuSO ·5H O 制取无水 CuSO
4 2 4
4.一种可吸附甲醇的材料,其化学式为[C(NH ) ] [B(OCH ) ] Cl,部分晶体结构如下图所示,
2 3 4 3 4 3
其中[C(NH
2
)
3
]+ 为平面结构。
下列说法不正确的是
A.该晶体中存在 N-H…O 氢键 B.基态原子的第一电离能:
C.电负性:χ(B)<χ(C) D.晶体中 B、N 和 O 原子轨道的杂化类型相同
高三化学 第 1页(共 8 页)阅读下列材料,完成 5-7 题:
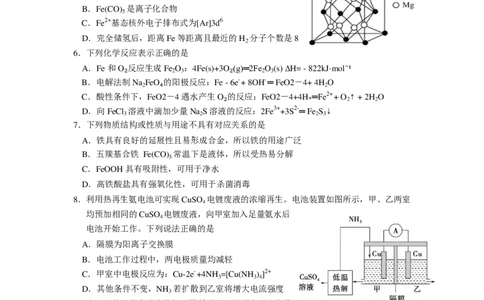
铁是用途广泛的金属。铁镁合金是储氢材料,其晶胞结构如下图所示,储氢后 H 分子
2
在晶胞的体心和棱心位置。五羰基合铁 [Fe(CO) ]常温下是液体,分解可得高纯铁。Fe(s)和
5
O (g)反应生成 1mol Fe O (s)放出 822kJ 的热量。FeCl 水解能生成有较强吸附能力的
2 2 3 3
FeOOH。向 Na S 溶液中滴加少量 FeCl 溶液会生成 Fe S 黑色沉淀,在酸性溶液中 Fe S
2 3 2 3 2 3
会发生氧化还原反应。以铁为阳极,氢氧化钠溶液为电解质溶液,进行电解可制得高铁酸钠
(Na FeO )。FeO 2-在酸性条件下氧化性很强,遇水产生 O 。
2 4 4 2
5.下列说法正确的是
A. Fe 与 Fe 为同一种核素
B.Fe(CO) 是离子化合物
5
C.Fe2+基态核外电子排布式为[Ar]3d6
D.完全储氢后,距离 Fe 等距离且最近的 H 分子个数是 8
2
6.下列化学反应表示正确的是
A.Fe 和 O 反应生成 Fe O :4Fe(s)+3O (g)═2Fe O (s) ΔH= - 822kJ·mol ¹
2 3 2 3
B.电解法制 Na FeO 的阳极反应:Fe - 6e- + 8OH- ═ FeO2-4+ 4H O
₂ 2 ₂ 2 ⁻
C.酸性条件下,FeO
₄
2-4 遇水产生 O 的反应:FeO2-4+4H+═Fe2+ + O
2
↑ + 2H
2
O
D.向 FeCl 溶液中滴加少量 Na S 溶液的反应:2Fe3++3S2-═ Fe S ↓
3 2 ₂ 2 3
7.下列物质结构或性质与用途不具有对应关系的是
A.铁具有良好的延展性且易形成合金,所以铁的用途广泛
B.五羰基合铁 Fe(CO) 常温下是液体,所以受热易分解
5
C.FeOOH 具有吸附性,可用于净水
D.高铁酸盐具有强氧化性,可用于杀菌消毒
8.利用热再生氨电池可实现 CuSO 电镀废液的浓缩再生。电池装置如图所示,甲、乙两室
4
均预加相同的 CuSO 电镀废液,向甲室加入足量氨水后
4
电池开始工作。下列说法正确的是
A.隔膜为阳离子交换膜
B.电池工作过程中,两电极质量均减轻
C.甲室中电极反应为:Cu-2e- +4NH =[Cu(NH ) ]2+
3 3 4
D.其他条件不变,NH 若扩散到乙室将增大电流强度
3
9.多巴胺的一种合成路线如下图所示,下列说法正确的是
A.甲和苯酚互为同系物
B.乙与足量的 H 完全加成后的产物中含有 3 个手性碳原子
2
C.丙分子中所有碳原子可能在同一个平面上
高三化学 第 2页(共 8 页)D.多巴胺可与碳酸钠溶液反应,产生气泡
10.用肼(N H )的水溶液处理核冷却系统内壁上的铁氧化物时,通常加入少量 CuSO ,反应
2 4 4
原理如图所示。下列说法正确的是
A.反应过程中只生成了极性键
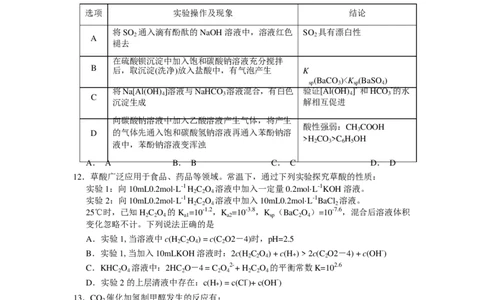
B.还原性:Fe2+H CO >C H OH
液中,苯酚钠溶液变浑浊 2 3 6 5
A. A B. B C. C D. D
12.草酸广泛应用于食品、药品等领域。常温下,通过下列实验探究草酸的性质:
实验 1:向 10mL0.2mol·L-1 H C O 溶液中加入一定量 0.2mol·L-1KOH 溶液。
2 2 4
实验 2:向 10mL0.2mol·L-1 H C O 溶液中加入 10mL0.2mol·L-1BaCl 溶液。
2 2 4 2
25℃时,已知 H C O 的 K =10-1.2,K =10-3.8,K (BaC O )=10-7.6,混合后溶液体积
2 2 4 a1 a2 sp 2 4
变化忽略不计。下列说法正确的是
A.实验 1,当溶液中 c(H C O ) = c(C O2-4)时,pH=2.5
2 2 4 2
B.实验 1,当加入 10mLKOH 溶液时:2c(H
2
C
2
O
4
) + c(H+) > 2c(C
2
O2-4) + c(OH-)
C.KHC O 溶液中:2HC O-4 = C O 2- + H C O 的平衡常数 K=102.6
2 4 2 2 4 2 2 4
D.实验 2 的上层清液中存在:c(H+) = c(Cl-)+ c(OH-)
13.CO 催化加氢制甲醇发生的反应有:
2
i.CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49.5 kJ·moL-1
2 2 3 2 1
ii.CO (g)+H (g) CO(g)+H O(g) ΔH = + 40.9 kJ·mol-1
2 2 ⇌ 2 2
iii.CO(g)+2H (g) CH OH(g) ΔH =-90.4 kJ·moL-1
2 ⇌ 3 3
将 CO
2
和 H
2
按 n(C⇌O
2
): n(H
2
)=1:3 通入密闭容器中发生反应,测得不同压强下 CO
2
的平
衡转化率以及相同压强下 CH OH、CO 选择性[CH OH 选择性= ]
3 3
随温度的变化如图所示。下列说法正确的是
高三化学 第 3页(共 8 页)A.相同压强下,从 0℃到 350℃,H O(g)的平
2
衡产率先降低后逐渐增大
B.CH OH 的选择性曲线为 b
3
C.P 、P 、P 由大到小的顺序为 P >P >P
1 2 3 3 2 1
D.P 、P 、P 三条曲线接近重合的原因是催
1 2 3
化剂失去活性
二、非选择题:共 4 题,共 61 分。
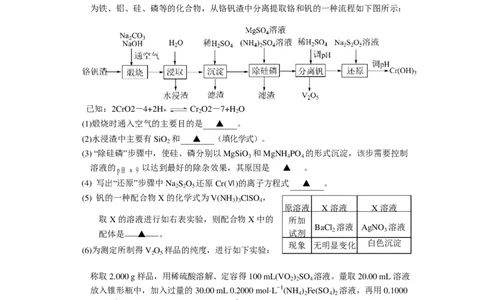
14.(16 分)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质
为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:2CrO2-4+2H+ Cr
2
O2-7+H
2
O
(1)煅烧时通入空气的主要目的是 ▲ 。
(2)水浸渣中主要有 SiO 和 ▲ (填化学式)。
2
(3) “除硅磷”步骤中,使硅、磷分别以 MgSiO 和 MgNH PO 的形式沉淀,该步需要控制
3 4 4
溶液的 以达到最好的除杂效果,其原因是 ▲ 。
(4) 写出“还原”步骤中 Na S O 还原 Cr(Ⅵ)的离子方程式 ▲ 。
2 2 5
(5) 钒的一种配合物 X 的化学式为 V(NH ) ClSO ,
3 3 4
原溶液 X 溶液 X 溶液
取 X 的溶液进行如右表实验,则配合物 X 中的 所加
BaCl 溶液 AgNO 溶液
配体是 ▲ 。 试剂 2 3
现象 无明显变化 白色沉淀
(6)为测定所制得 V O 样品的纯度,进行如下实验:
2 5
称取 2.000 g 样品,用稀硫酸溶解、定容得 100 mL(VO ) SO 溶液。量取 20.00 mL 溶液
2 2 4
放入锥形瓶中,加入过量的 30.00 mL 0.2000 mol·L−1(NH ) Fe(SO ) 溶液,再用 0.1000
4 2 4 2
mol·L−1 KMnO 标准溶液滴定过量的 Fe2+至终点,消耗标准溶液的体积为 8.00mL。计
4
算 V O 样品的纯度 ▲ (写出计算过程,杂质不参与反应)。实验过程中反应如下:
2 5
VO 2++Fe2++H+——VO2++Fe3++H
2
O(未配平);
MnO-4+Fe2++H+——Mn2++Fe3++H
2
O(未配平)。
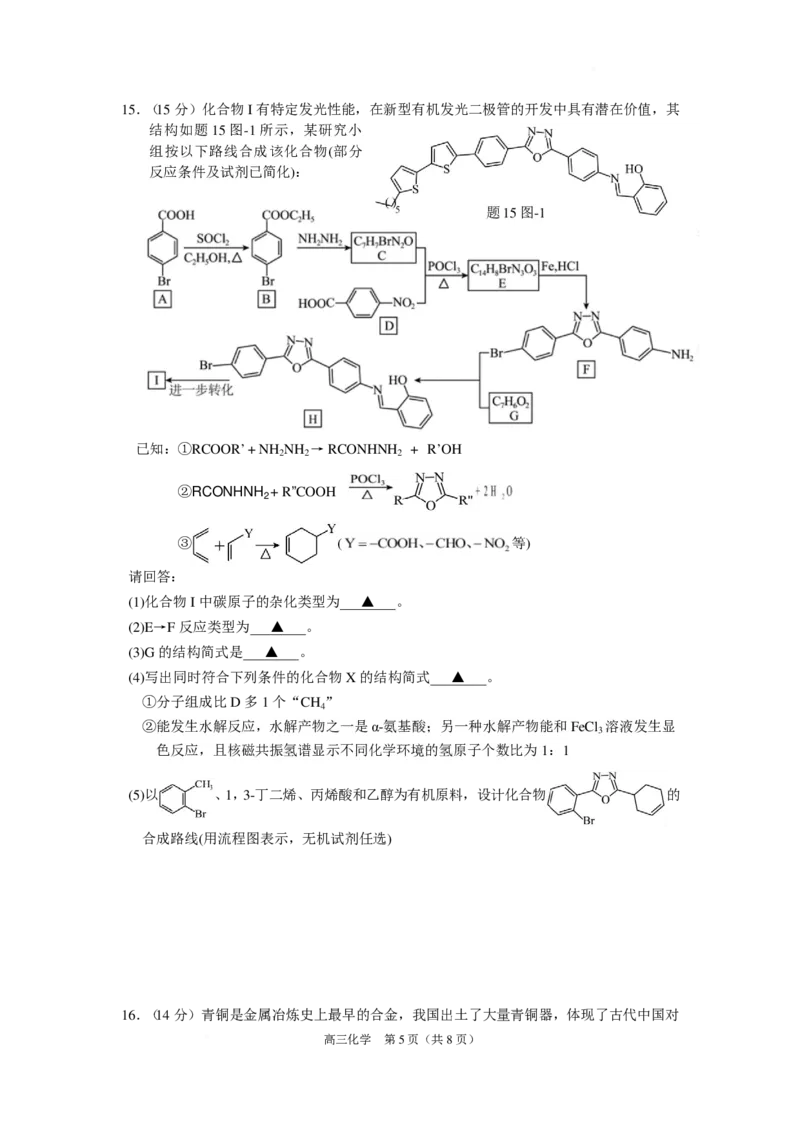
高三化学 第 4页(共 8 页)15.(15 分)化合物 I有 特定发光性能,在新型有机发光二极管的开发中具有潜在价值,其
结构如题 15 图-1 所示,某研究小
组按以下路线合成该化合物(部分
反应条件及试剂已简化):
题 15 图-1
已知:①RCOOR’ + NH NH → RCONHNH + R’OH
2 2 2
②RCONHNH + R”COOH
2
③ ( 等)
请回答:
(1)化合物 I 中碳原子的杂化类型为 ▲ 。
(2)E→F 反应类型为 ▲ 。
(3)G 的结构简式是 ▲ 。
(4)写出同时符合下列条件的化合物 X 的结构简式 ▲ 。
①分子组成比 D 多 1 个“CH ”
4
②能发生水解反应,水解产物之一是α-氨基酸;另一种水解产物能和 FeCl 溶液发生显
3
色反应,且核磁共振氢谱显示不同化学环境的氢原子个数比为 1:1
(5)以 、1,3-丁二烯、丙烯酸和乙醇为有机原料,设计化合物 的
合成路线(用流程图表示,无机试剂任选)
16.(14 分)青铜是金属冶炼史上最早的合金,我国出土了大量青铜器,体现了古代中国对
高三化学 第 5页(共 8 页)人类文明的巨大贡献。青铜器在埋藏过程中会逐渐生锈,其修复工作是文物保护的重要环
节。
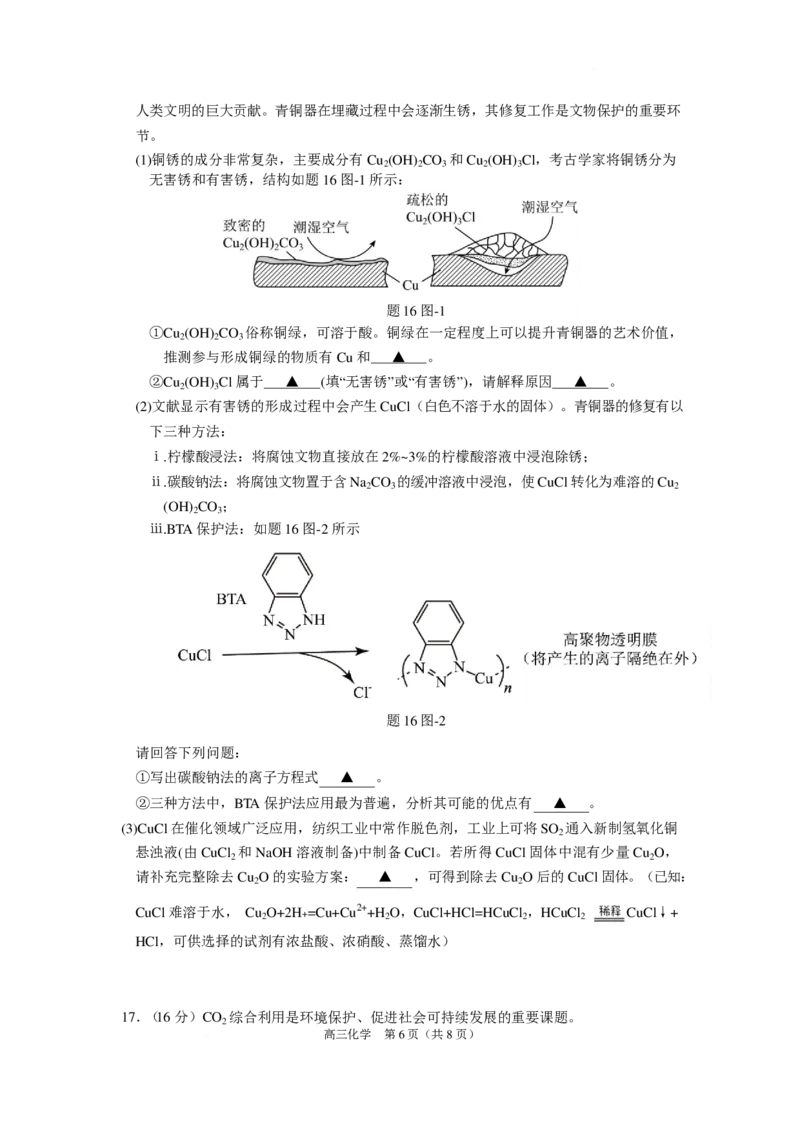
(1)铜锈的成分非常复杂,主要成分有 Cu (OH) CO 和 Cu (OH) Cl,考古学家将铜锈分为
2 2 3 2 3
无害锈和有害锈,结构如题 16 图-1 所示:
题 16 图-1
①Cu (OH) CO 俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,
2 2 3
推测参与形成铜绿的物质有 Cu 和 ▲ 。
②Cu (OH) Cl 属于 ▲ (填“无害锈”或“有害锈”),请解释原因 ▲ 。
2 3
(2)文献显示有害锈的形成过程中会产生 CuCl(白色不溶于水的固体)。青铜器的修复有以
下三种方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在 2%~3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:将腐蚀文物置于含 Na CO 的缓冲溶液中浸泡,使 CuCl 转化为难溶的 Cu
2 3 2
(OH) CO ;
2 3
ⅲ.BTA 保护法:如题 16 图-2 所示
题 16 图-2
请回答下列问题:
①写出碳酸钠法的离子方程式 ▲ 。
②三种方法中,BTA 保护法应用最为普遍,分析其可能的优点有 ▲ 。
(3)CuCl 在催化领域广泛应用,纺织工业中常作脱色剂,工业上可将 SO 通入新制氢氧化铜
2
悬浊液(由 CuCl 和 NaOH 溶液制备)中制备 CuCl。若所得 CuCl 固体中混有少量 Cu O,
2 2
请补充完整除去 Cu O 的实验方案: ▲ ,可得到除去 Cu O 后的 CuCl 固体。(已知:
2 2
CuCl 难溶于水, Cu
2
O+2H+=Cu+Cu2++H
2
O,CuCl+HCl=HCuCl
2
,HCuCl
2
CuCl↓+
HCl,可供选择的试剂有浓盐酸、浓硝酸、蒸馏水)
17.(16 分)CO 综合利用是环境保护、促进社会可持续发展的重要课题。
2
高三化学 第 6页(共 8 页)Ⅰ.电化学技术:采用电化学-化学串联催化策略可将 CO 高选择性合成 C H ,该流程
2 4 10
如题 17 图-1 所示:
题 17 图-1
(1)电解过程中 CO 生成 C H 的电极反应式 ▲ 。
2 2 4
(2)在反应器中,发生如下反应:
反应 i:2C H (g) C H (g) ΔH =-104.7 kJ/mol
2 4 4 8 1
反应 ii:2C H (g)+H (g) C H (g) ΔH =-230.7 kJ/mol
2 4 2 4 10 2
①计算反应 C H (g) +H (g) C H (g) 的ΔH= ▲ kJ/mol。
4 8 2 4 10
一定温度下,CO 、C H 和 H (体积比为 )按一定流速进入装有催化剂的恒容反应
2 2 4 2
器(入口压强为 )发生反应 i 和 ii.有 CO 存在时,反应 ii 的反应进程如题 17 图- 2
2
所示。随着 x 的增加,C H 的转化率和产物的选择性
2 4
(选择性 )如题 17 图-3 所示。
题 17 图-2 题 17 图-3
②根据 17-图 2,C H 的选择性大于 C H 的原因是 ▲ 。
4 10 4 8
③结合 17-图 3,当 时,混合气体以较低的流速经过恒容反应器时,反应近似达到平
衡,随着 x 的增大,C H 的转化率减小的原因是 ▲ 。
2 4
Ⅱ.等离子体技术
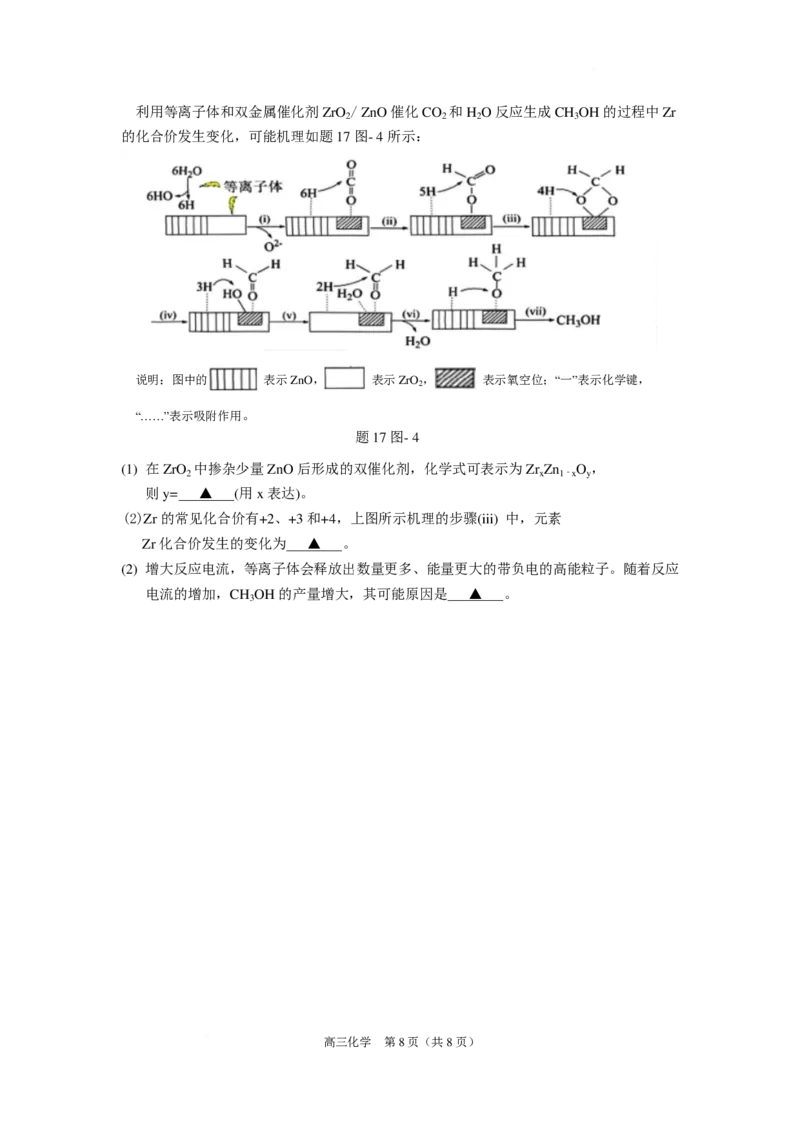
高三化学 第 7页(共 8 页)利用等离子体和双金属催化剂 ZrO / ZnO 催化 CO 和 H O 反应生成 CH OH 的过程中 Zr
2 2 2 3
的化合价发生变化,可能机理如题 17 图- 4 所示:
说明:图中的 表示 ZnO, 表示 ZrO, 表示氧空位;“一”表示化学键,
2
“……”表示吸附作用。
题 17 图- 4
(1) 在 ZrO 中掺杂少量 ZnO 后形成的双催化剂,化学式可表示为 Zr Zn O ,
2 x 1﹣x y
则 y= ▲ (用 x 表达)。
(2)Zr 的常见化合价有+2、+3 和+4,上图所示机理的步骤(iii) 中,元素
Zr 化合价发生的变化为 ▲ 。
(2) 增大反应电流,等离子体会释放出数量更多、能量更大的带负电的高能粒子。随着反应
电流的增加,CH OH 的产量增大,其可能原因是 ▲ 。
3
高三化学 第 8页(共 8 页)