文档内容
化
广元市 2025 年春季普通高中二年级期末教学质量监测
学试题
注意事项:
1.化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共 6 页;满分 100
分,考试时间 75 分钟。
2.答题前,考生务必将自己的姓名、座位号、考籍号等用 0.5 毫米的黑色墨水签字笔
填写在答题卡上。并检查条形码粘贴是否正确。
3.选择题使用 2B 铅笔填涂在答题卡对应题目标号的位置上;非选择题用 0.5 毫米的
黑色墨水签字笔书写在答题卡对应的框内,超出答题区域书写的答案无效;在草稿
纸、试题卷上答题无效。
4.考试结束后,将答题卡收回。
可能用到的相对原子质量:H—1 N—14 O—16 S—32 V—51 Mn—55 Fe—56 Cu—64
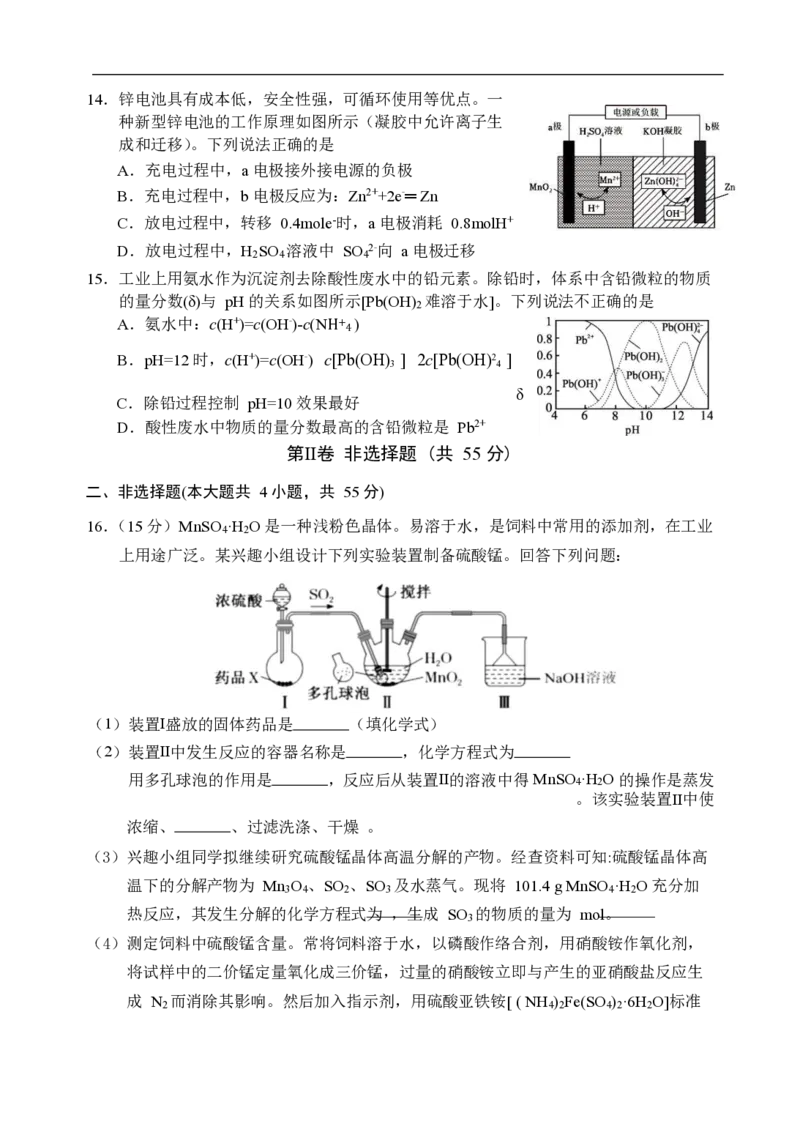
第Ⅰ卷 选择题(共 45 分)
一、选择题(本题包括 15 个小题,每小题 3 分,共 45 分。每小题只有一个最佳选项符
合题意)
1.为共同构建人与自然生命共同体,我国已将“碳达峰”和“碳中和”纳入生态文明建
设整体布局,“3060”双碳目标是我国对世界的庄严承诺,重点是推动以二氧化碳为
主的温室气体减排。下列措施与此目标不吻合的是
A.植树造林、节能减排
B.太阳能、潮汐能、风能、氢能等清洁能源逐步替代火力发电
C.研发二氧化碳加氢制甲醇的高效催化剂
D.燃煤中适当添加石灰石,减少污染气体排放
2.在①二氧化硅 ②碘 ③镁 ④蔗糖 ⑤冰等物质中,属于分子晶体的是
A.①②④ B.②③⑤ C.②④⑤ D.①②④⑤
3.化学与生活生产及科技密切相关。下列说法错误的是
A.杭州亚运会使用聚乳酸塑料代替聚乙烯塑料,可有效减少白色污染
B.月球探测器带回的月壤样品中含磷酸盐晶体,其结构可用 X 射线衍射仪测
定
C.医用口罩和防护服的主要原材料是聚丙烯(PP),它与聚乙烯互为同系物
D.2024 年 5 月 1 日,我国第三艘航母“福建舰”开展首次航行试验,相控阵雷达使
用的碳化硅属于无机非金属材料
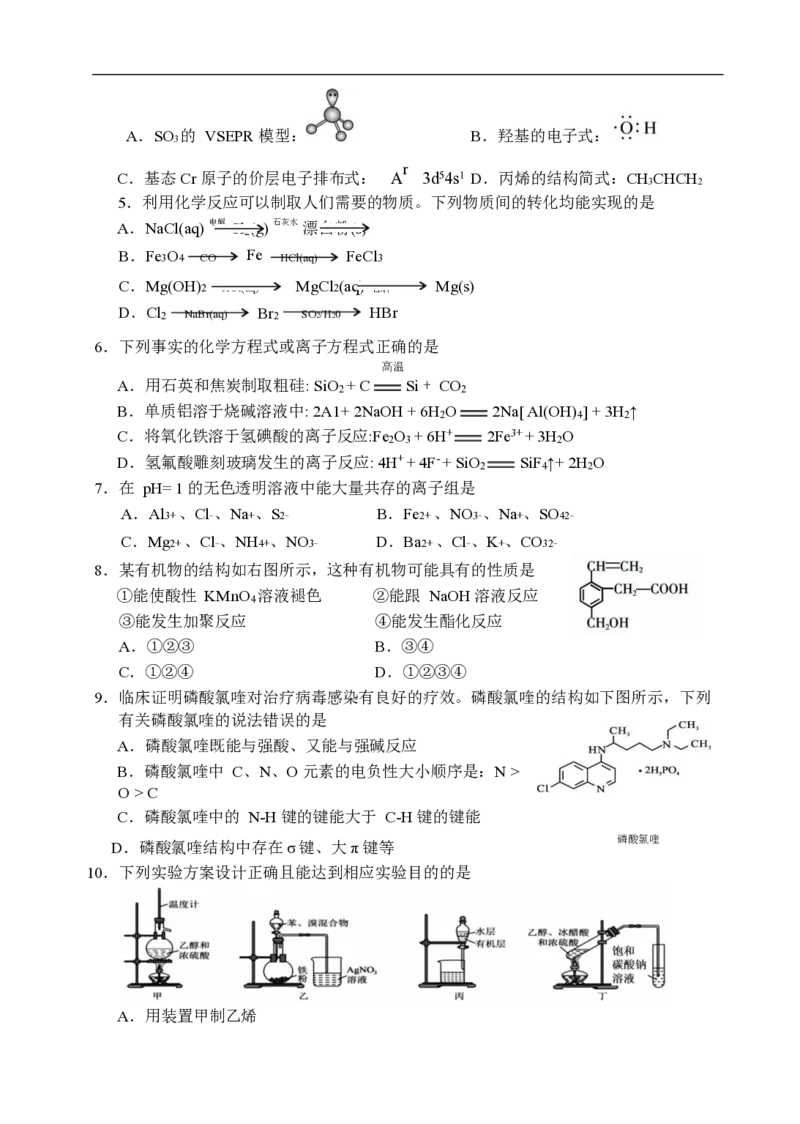
4.下列化学用语或图示表达正确的是A.SO 的 VSEPR 模型: B.羟基的电子式:
3
r
C.基态Cr 原子的价层电子排布式: A 3d54s1 D.丙烯的结构简式:CHCHCH
3 2
5.利用化学反应可以制取人们需要的物质。下列物质间的转化均能实现的是
A.NaCl(aq) 电解 Cl (g) 石灰水 漂白粉(s)
2
B.Fe3O4 CO Fe HCl(aq) FeCl3
C.Mg(OH)2 HCl(aq) MgCl2(aq) 电解 Mg(s)
D.Cl 2 NaBr(aq) Br 2 SO2/H20 HBr
6.下列事实的化学方程式或离子方程式正确的是
高温
A.用石英和焦炭制取粗硅: SiO + C Si + CO
2 2
B.单质铝溶于烧碱溶液中: 2A1+ 2NaOH + 6H O 2Na[ Al(OH) ] + 3H ↑
2 4 2
C.将氧化铁溶于氢碘酸的离子反应:Fe O + 6H+ 2Fe3+ + 3H O
2 3 2
D.氢氟酸雕刻玻璃发生的离子反应: 4H+ + 4F- + SiO SiF ↑+ 2H O
2 4 2
7.在 pH= 1 的无色透明溶液中能大量共存的离子组是
A.Al3+ 、Cl
-
、Na+ 、S2- B.Fe2+ 、NO3- 、Na+ 、SO42-
C.Mg2+ 、Cl
-
、NH4+ 、NO3- D.Ba2+ 、Cl
-
、K+ 、CO32-
8.某有机物的结构如右图所示,这种有机物可能具有的性质是
①能使酸性 KMnO 溶液褪色 ②能跟 NaOH 溶液反应
4
③能发生加聚反应 ④能发生酯化反应
A.①②③ B.③④
C.①②④ D.①②③④
9.临床证明磷酸氯喹对治疗病毒感染有良好的疗效。磷酸氯喹的结构如下图所示,下列
有关磷酸氯喹的说法错误的是
A.磷酸氯喹既能与强酸、又能与强碱反应
B.磷酸氯喹中 C、N、O 元素的电负性大小顺序是:N >
O > C
C.磷酸氯喹中的 N-H 键的键能大于 C-H 键的键能
磷酸氯喹
D.磷酸氯喹结构中存在σ键、大π键等
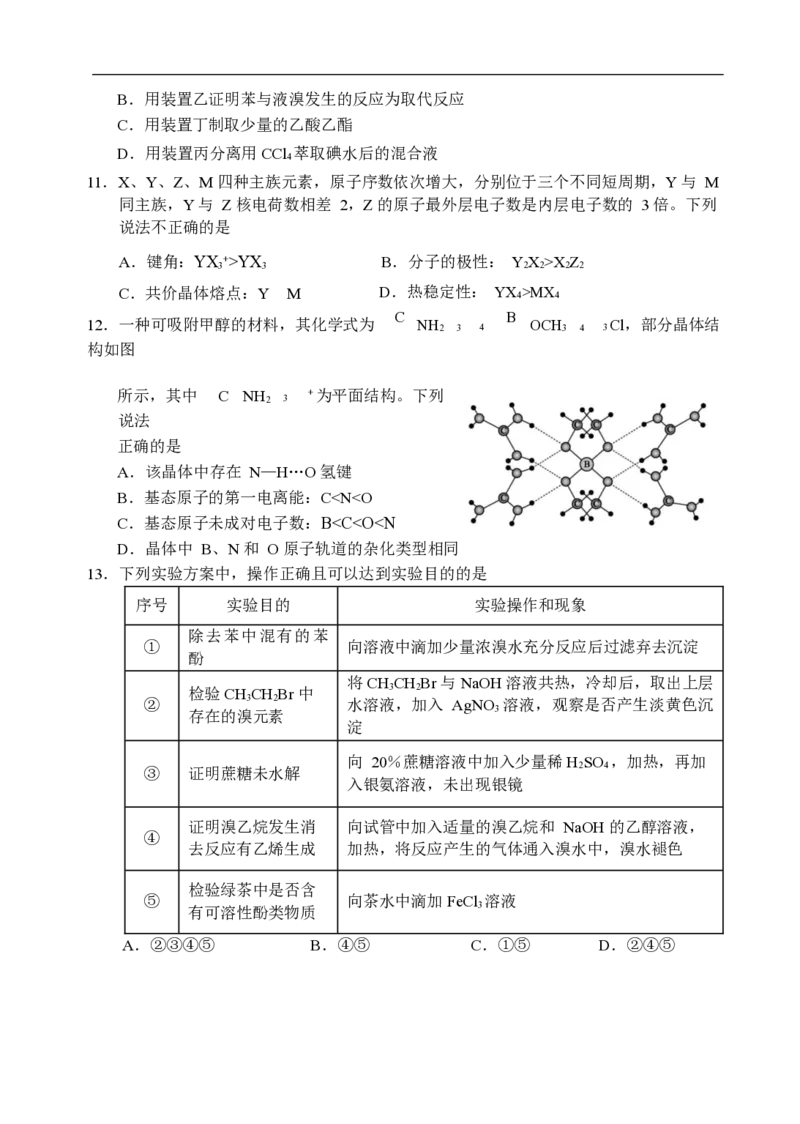
10.下列实验方案设计正确且能达到相应实验目的的是
A.用装置甲制乙烯B.用装置乙证明苯与液溴发生的反应为取代反应
C.用装置丁制取少量的乙酸乙酯
D.用装置丙分离用CCl 萃取碘水后的混合液
4
11.X、Y、Z、M 四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y 与 M
同主族,Y 与 Z 核电荷数相差 2,Z 的原子最外层电子数是内层电子数的 3 倍。下列
说法不正确的是
A.键角:YX+>YX B.分子的极性: YX>XZ
3 3 2 2 2 2
C.共价晶体熔点:Y M D.热稳定性: YX >MX
4 4
C B
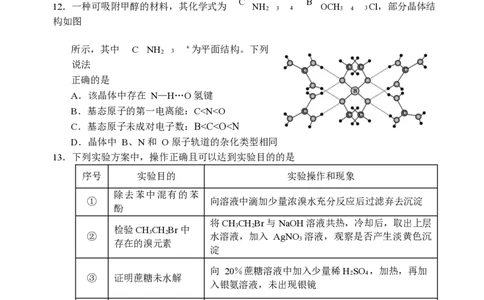
12.一种可吸附甲醇的材料,其化学式为 NH OCH Cl,部分晶体结
2 3 4 3 4 3
构如图
所示,其中 C NH + 为平面结构。下列
2 3
说法
正确的是
A.该晶体中存在 N—H…O 氢键
B.基态原子的第一电离能:Cp >p
1 2 3
n(H2)
=3,则平衡时,α(CO)小于 50% C.若在 p 和 316 ℃时,起始时
3n(CO)
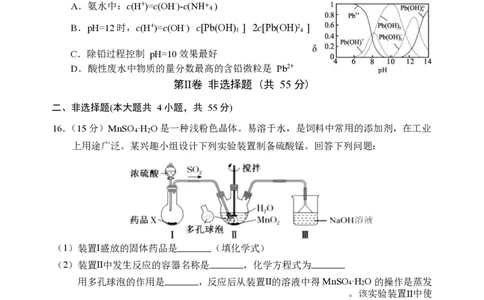
(3)CO 合成甲醇时,在不同温度下的平衡转化率与压
强的关系如图所示。实际生产条件控制在 250 ℃、
1.3×104 kPa 左右,选择此压强的理由是。
(4)高温时二甲醚蒸气发生分解反应:
CH OCH CH +CO+H 。迅速将二甲醚引入一个
3 3 4 2
504 ℃抽成真空的恒容瓶中,在不同时刻测定瓶内
压强 p 如下表:
总
t/min 0 10 20 30 40 50
p /kPa 50.0 78.0 92.0 99.0 100 100
总
该反应的平衡常数 K =_______(kPa)2。(用平衡分压代替平衡浓度计算,分压=总
p
压×物质的量分数)。
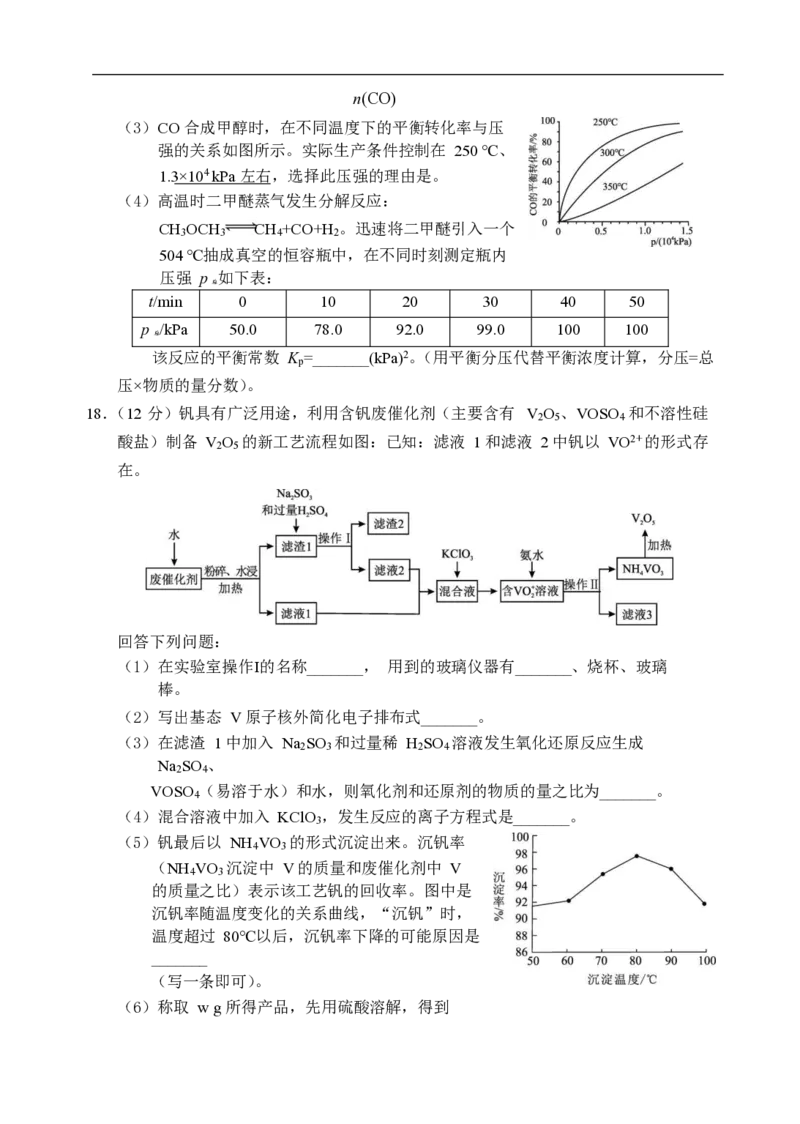
18.(12 分)钒具有广泛用途,利用含钒废催化剂(主要含有 V O 、VOSO 和不溶性硅
2 5 4
酸盐)制备 V O 的新工艺流程如图:已知:滤液 1 和滤液 2 中钒以 VO2+ 的形式存
2 5
在。
回答下列问题:
(1)在实验室操作Ⅰ的名称_______, 用到的玻璃仪器有_______、烧杯、玻璃
棒。
(2)写出基态 V 原子核外简化电子排布式_______。
(3)在滤渣 1 中加入 Na SO 和过量稀 H SO 溶液发生氧化还原反应生成
2 3 2 4
Na SO 、
2 4
VOSO (易溶于水)和水,则氧化剂和还原剂的物质的量之比为_______。
4
(4)混合溶液中加入 KClO ,发生反应的离子方程式是_______。
3
(5)钒最后以 NH VO 的形式沉淀出来。沉钒率
4 3
(NH VO 沉淀中 V 的质量和废催化剂中 V
4 3
的质量之比)表示该工艺钒的回收率。图中是
沉钒率随温度变化的关系曲线,“沉钒”时,
温度超过 80℃以后,沉钒率下降的可能原因是
_______
(写一条即可)。
(6)称取 w g 所得产品,先用硫酸溶解,得到(VO ) SO 溶液,再加入 a mL b mol·L-1 的(NH ) Fe(SO ) 溶液,充分反应后用 b
2 2 4 1 1 4 2 4 2 2
mol·L-1 酸性 KMnO 溶液滴定过量的(NH ) Fe(SO ) 至终点,消耗 KMnO 溶液
4 4 2 4 2 4
的体积为 a mL。假设杂质不参与反应,锰元素被还原为 Mn2+。求产品中 V O
2 2 5
的质量分数为_______ [已知 (VO ) SO 和 (NH ) Fe(SO ) 溶液反应的离子方程式
2 2 4 4 2 4 2
为 VO + + 2H+ + Fe2+ == VO2+ + Fe3+ + H O]
2 2
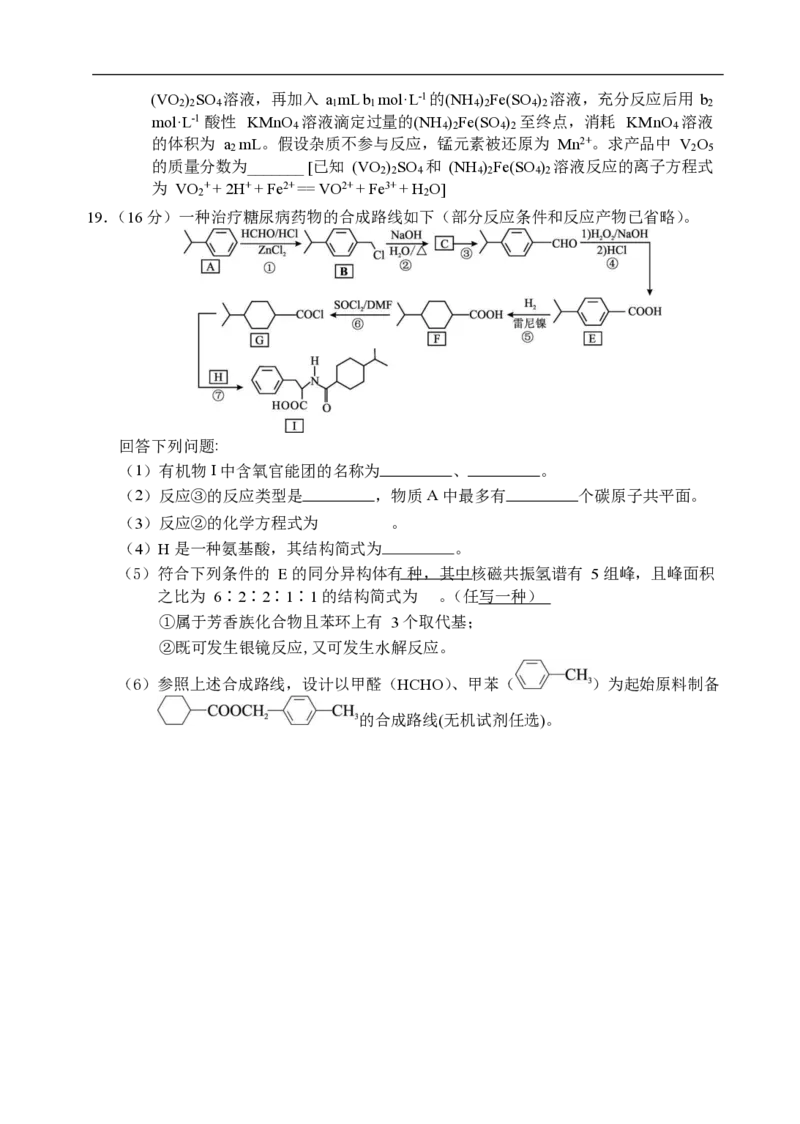
19.(16 分)一种治疗糖尿病药物的合成路线如下(部分反应条件和反应产物已省略)。
回答下列问题 :
( 1 )有 机物 I 中含氧官能团的名称为 、 。
( 2 )反 应 ③ 的反应类型是 ,物质 A 中最多有 个碳原子共平面。
(3)反应②的化学方程式为 。
(4)H 是一种氨基酸,其结构简式为 。
(5)符合下列条件的 E 的同分异构体有 种,其中核磁共振氢谱有 5 组峰,且峰面积
之比为 6∶2∶2∶1∶1 的结构简式为 。(任写一种)
①属于芳香族化合物且苯环上有 3 个取代基;
②既可发生银镜反应,又可发生水解反应。
(6)参照上述合成路线,设计以甲醛(HCHO)、甲苯( )为起始原料制备
的合成路线(无机试剂任选)。