文档内容
5.下列实验设计和操作均正确且能达到实验目的的是 ( )
高三化学试卷(一)
(本试卷满分100分,考试时间75分钟)
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写
在试卷和答题卡规定的位置上。
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字
A.用HCl标准溶液滴定NaOH溶液 B.验证氧化性:Cl>Fe3+>I
2 2
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。
C.制备并收集NO D.实验室制备氨气
2
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Si-28 Cl-35.5 6.可采用Deacon催化氧化法制成工业副产物HCl,实现氯资源的再利用。反应的热化学方程
Fe-56 Cu-64 Se-79 式:4HCl(g)+O(g) C u O 2Cl(g)+2HO(g) ΔH=-114.4kJ·mol-1。下图所示为该法
2 2 2
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符 的一种催化机理,下列说法不正确的是 ( )
合题目要求。
1.我国提出在2060年前完成“碳中和”的目标,下列有关低碳生活的说法不正确的是 ( )
A.使用氢气等清洁能源代替传统能源有利于“碳中和”
B.推广使用煤液化技术,可减少二氧化碳的排放
C.低碳生活不意味着禁止使用所有燃料
A.X为生成物Cl,W为生成物HO
2 2
D.在一定条件下将CO 2 还原为甲酸 B.反应制得1molCl 2 ,放出热量57.2kJ
高温 高温 C.升高温度,HCl被O 氧化制Cl的反应逆向移动
2.电石可通过如下反应制得:CaCO CaO+CO、CaO+3CCaC +CO。下列说法正确 2 2
3 2 2
D.图中转化涉及的反应中有三个属于氧化还原反应
的是 ( )
7.设N 为阿伏加德罗常数的值。下列说法正确的是 ( )
A.基态Ca2+的电子排布式:[Ar]4s2 B.CO2-的空间构型为四面体形 A
3 A.1mol[Cu(OH)]2-中所含σ键数目为4N
4 A
C.CaC的电子式为 D.二氧化碳晶体属于共价晶体
2 B.6gSiO 晶体中所含硅氧键数目为0.4N
2 A
3.化学使生活更美好。下列生产生活对应化学原理解释错误的是 ( ) C.标准状况下,4.48L氯仿中所含氯原子数目为0.6N
A
D.室温下,pH=13的KOH溶液中所含OH-数目为0.1N
选项 生活经验 化学原理 A
8.由实验操作和现象得出结论正确的是 ( )
A 明矾水去除青铜器上的铜锈 盐类水解产生的酸与碱式盐反应
选项 实验操作和现象 结论
B 锡纸装食盐水让银饰由黑变回银色 Sn未经过外电路直接把电子转移给Ag+
A 向0.1mol/LNaHSO 溶液中加入石蕊试液,变红色 K (HSO)>K (SO2-)
3 a2 2 3 h2 3
C 节日燃放的烟花在夜空下呈现多种色彩 原子核外电子跃迁会释放能量
向某溶液中加入稀盐酸,产生使澄清石灰水变浑浊
D 打霜后的萝卜白菜味道更甜美 淀粉水解产生葡萄糖 B 该溶液中含有CO2-或HCO-
的气体 3 3
4.硒(Se)在医药、催化、材料等领域有广泛应用,乙烷硒啉(Ethaselen)是一种抗癌新药,其结
34
将溴乙烷与NaOH乙醇溶液加热产生的气体通入 溴乙烷与NaOH的乙醇溶液发
构式如下图所示。关于硒及其化合物,下列说法不正确的是 ( ) C
酸性KMnO 溶液,溶液褪色 生了消去反应
A.Se原子在周期表中位于p区 4
B.乙烷硒啉分子中,C原子的杂化类型有sp2、sp3 室温下,用 pH试纸分别测定浓度为 0.1mol/L的
C.乙烷硒啉分子中有5种不同化学环境的氢原子 D HClO溶液和0.1mol/L的 HF溶液的 pH,前者的 HClO的酸性小于HF
D.键角大小:气态SeO <SeO2- pH大于后者
3 3
高三化学试卷(一) 第1页 (共8页) 高三化学试卷(一) 第2页 (共8页)
书书书9.短周期元素X、Y、Z、W的原子序数依次增大,Y、W同主族。甲、乙、丙分别是由以上四种元 13.利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响
素中的两种组成的化合物,丁是由以上三种元素组成的化合物;甲与乙摩尔质量相同,乙为 可忽略):
淡黄色固体,上述物质之间的转化关系如图所示(部分生成物省略),下列说法中一定正确
的是 ( )
A.图中有两个氧化还原反应
B.丁中含有离子键、共价键和配位键
C.摩尔质量:戊>丙,沸点:丙>戊
D.简单离子半径:W>Y>Z>X
下列说法正确的是 ( )
10.液氨的沸点-33.5℃,锂能与液氨反应,反应方程式为Li+nNH [e(NH)]-+Li+,
3 3 n A.“氧化”时,发生的化学方程式:4Ag+4NaClO+2HO4AgCl↓+4NaOH+O↑
2 2
[e(NH)]-是一种强还原剂,反应装置如图所示(夹持装置略)。下列说法不正确的是 ( )
3 n B.氨水的作用是调节溶液的pH
C.若“还原”工序利用原电池来实现,则N 是正极产物
2
D.“还原”时,每生成1molAg,理论上消耗0.5molNH·HO
2 4 2
14.Li、Fe、Se可形成一种新型超导材料,其晶胞结构如图所示。
A点分数坐标为(1,1,1),下列叙述不正确的是 ( )
A.图中“试剂A”“试剂B”均可以为碱石灰
A.该超导材料的化学式为LiFeSe
B.实验过程中可以通过调节分液漏斗的活塞,控制产生氨气的速率 2 2
C.图中“冷却溶剂”可以是冰水混合物 B.距离Se原子最近的Fe原子的个数为4
D.反应前锂片需打磨除去表面的氧化膜 (7+79×2+56×2)×2
C.晶胞晶体密度为 g/cm3
a2bN
11.下列关于物质的结构或性质的描述解释都正确的是 ( ) A
A.H—O—H键角:HO+<HO是由于HO+中O上孤电子对数比HO分中O上的少 1 1 1
3 2 3 2 D.B点分数坐标为( , , )
2 2 2
B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛存在分子间氢键
15.常温下,NaA溶液中HA、HA-、A2-的物质的量分数与pH的关系如下图。已知:A2-的物
C.电离能:P的第一电离能>S的第一电离能,是由于原子半径P>S 2 2
D.酸性:CHClCOOH>CHCOOH,是由于CHClCOOH的羧基中羟基极性更小 c(A2-)
2 3 2 质的量分数= 。下列表述不正确的是 ( )
c(HA)+c(HA-)+c(A2-)
12.一种兼具合成功能的新型锂电池工作原理如图。电解质为含Li有机溶液。放电过程中产 2
生(CFSO)NLi,充电过程中电解LiCl产生Cl。下列说法正确的是 ( )
3 2 2 2
A.0.1mol·L-1HA溶液中,c(HA)+c(HA-)+c(A2-)=0.1mol·L-1
2 2
A.交换膜为阴离子交换膜
B.在0.1mol·L-1NaHA溶液中,c(HA-)>c(A2-)>c(HA)
B.电解质溶液可替换为LiCl水溶液 2
C.理论上每生成1molCl,需消耗2molLi C.将等物质的量的NaHA、NaA溶于水中,所得溶液的pH为4.2
2 2
D.关闭S、打开S时总反应:6Li+N +4CFSOCl2(CFSO)NLi+4LiCl D.M点对应的pH为2.7
1 2 2 3 2 3 2 2
高三化学试卷(一) 第3页 (共8页) 高三化学试卷(一) 第4页 (共8页)二、非选择题:本题共4小题,共55分。 (2)以a为原料制备硝酸,第一步反应的化学方程式为 ;生产
16.(14分)以工业钛白副产品[主要成分 FeSO·7HO,少量 Al(SO) 和 CuO]、废硫酸和 中用a的水溶液吸收少量i,发生反应的离子方程式为 。
4 2 2 4 3
软锰矿(主要成分MnO 2 )为原料生产硫酸锰和碳酸锰流程如图: (3)常温下,在上述物质中选择试剂 (填名称)可除去铁制品表面的铜镀层。
(4)研究发现,空气中少量的NO 也能参与硫酸型酸雨的形成,反应过程如下:
2
①SO +NO SO +NO
2 2 3
②SO +HOHSO
3 2 2 4
已知:常温下,K[Al(OH)]=1×10-33。 ③2NO+O 2 2NO 2
sp 3
回答下列问题: NO 在上述过程中的作用,与 HSO 在下列变化中的作用相同的是 (填
2 2 4
(1)“共热”过程中MnO 参与反应的离子方程式为 。 序号)。
2
(2)“过滤Ⅰ”先加入适量废铁屑充分反应后再加入硫酸铵生成(NH)Fe(SO)(OH) A.潮湿的氯气通过盛有浓HSO 的洗气瓶
4 2 6 4 4 12 2 4
沉淀,生成沉淀的化学方程式为 ,加入“废铁屑”的
B.硫化氢通入浓HSO 中
2 4
目的为 。
C.蔗糖水解实验中加入稀硫酸
(3)“试剂X”可能为 (填标号)。
D.向盐酸中加入浓硫酸产生白雾
A.MnO B.MnO C.MnCO
2 3 (5)向含0.1molk的溶液中通入4.48LCl(标准状况下),硫元素恰好被氧化为 +6价,则
2
(4)“滤渣3”的主要成分为 (填化学式)。
k的化学式可能为 (填序号),反应的离子方程式为 。
(5)实验室中进行“系列操作”所用的玻璃仪器有 。
A.NaSO B.NaSO C.NaSO
2 3 2 2 5 2 2 6
(6)“滤液1”可循环到的操作单元为 。
18.(14分)CuCl在工业生产中有着重要应用。利用如图装置制备CuCl并测定产品纯度。
17.(13分)氮、硫及其化合物的“价—类”二维图如图所示。
已知:ⅰ.CuCl是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
ⅱ.浓的Na[CuCl]溶液为无色,加水稀释即析出CuCl白色固体。
2 3
回答下列问题:
请回答下列问题:
(1)生活中使用的天然气中往往添加少量 (填上述物质的化学式),用于警示 (1)①图中制取Cl的反应中,氧化剂和还原剂的物质的量之比为 。
2
天然气泄漏,保障使用安全。 ②装置B中发生反应的仪器名称为 。
高三化学试卷(一) 第5页 (共8页) 高三化学试卷(一) 第6页 (共8页)③C中可选用试剂 (填标号)。
已知:
A.NaSO 溶液 B.饱和食盐水
2 3
C.浓HSO D.FeCl溶液
2 4 2 回答下列问题:
(2)制备CuCl:打开分液漏斗旋塞与搅拌器,装置 B中依次发生反应的离子方程式为:①
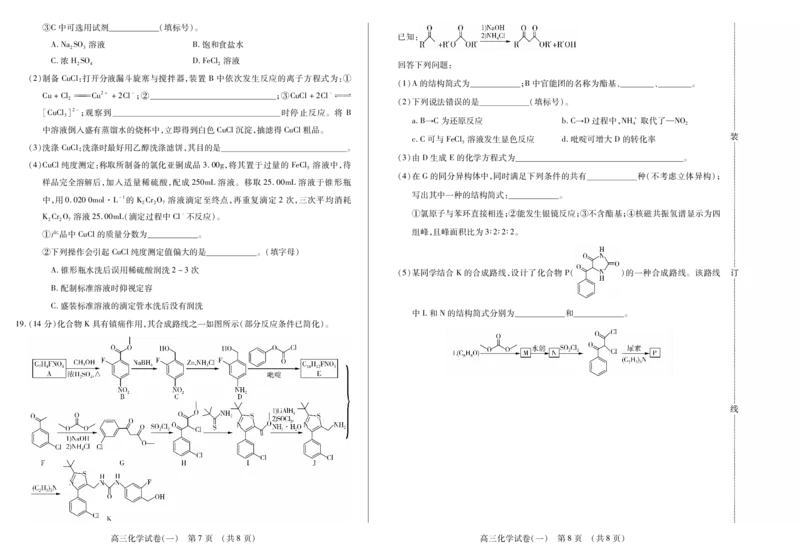
(1)A的结构简式为 ;B中官能团的名称为酯基、 、 。
Cu+ClCu2+ +2Cl-;② ;③CuCl+2Cl-幑幐
2 (2)下列说法错误的是 (填标号)。
[CuCl]2-;观察到 时停止反应。将 B
3 a.B→C为还原反应 b.C→D过程中,NH+取代了—NO
4 2
中溶液倒入盛有蒸馏水的烧杯中,立即得到白色CuCl沉淀,抽滤得CuCl粗品。
c.C可与FeCl溶液发生显色反应 d.吡啶可增大D的转化率
3
(3)洗涤CuCl:洗涤时最好用乙醇洗涤滤饼,其目的是 。
(3)由D生成E的化学方程式为 。
(4)CuCl纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的 FeCl溶液中,待
3
(4)在G的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构);
样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶
写出其中一种的结构简式: 。
中,用0.0200mol·L-1的 KCrO 溶液滴定至终点,再重复滴定2次,三次平均消耗
2 2 7
KCrO 溶液25.00mL(滴定过程中Cl-不反应)。 ①氯原子与苯环直接相连;②能发生银镜反应;③不含酯基;④核磁共振氢谱显示为四
2 2 7
①产品中CuCl的质量分数为 。 组峰,且峰面积比为3∶2∶2∶2。
②下列操作会引起CuCl纯度测定值偏大的是 。(填字母)
A.锥形瓶水洗后误用稀硫酸润洗2-3次
(5)某同学结合K的合成路线,设计了化合物 P( )的一种合成路线。该路线
B.配制标准溶液时仰视定容
C.盛装标准溶液的滴定管水洗后没有润洗
中L和N的结构简式分别为 和 。
19.(14分)化合物K具有镇痛作用,其合成路线之一如图所示(部分反应条件已简化)。
高三化学试卷(一) 第7页 (共8页) 高三化学试卷(一) 第8页 (共8页)