文档内容
成都市⽯室成⻜中学 学年上期⼗⼀⽉⽉考
2025-2026
⾼ 级 化学试卷
2023
试卷说明:
1.答题前,考⽣务必在答题卡上将⾃⼰的姓名、座位号、考号⽤0.5毫⽶⿊⾊签字笔填写清楚,考⽣考
试条形码由监考⽼师粘贴在答题卡上的“贴条形码区”。
2.选择题使⽤2B铅笔填涂在答题卡上对应题⽬标号的位置上,如需改动,⽤橡⽪擦擦⼲净后再填涂其
它答案;⾮选择题⽤0.5毫⽶⿊⾊签字笔在答题卡的对应区域内作答,超出答题区域答题的答案⽆效;在草
稿纸上、试卷上答题⽆效。
3.考试时间75分钟,满分100分,考试结束后由监考⽼师将答题卡收回。
可能⽤到的相对原⼦质量 H-1 N-14 O-16 Na-23 P-31
第 I 卷(选择题,共 45 分)
⼀、选择题(本题共15⼩题,每⼩题3分,共45分。每⼩题只有⼀项是符合题⽬要求)
1.化学与⼈类⽣产、⽣活密切相关。下列说法正确的是
A.聚苯⼄烯可⽤作包装材料,其属于可降解材料
B.纳⽶铁粉属于胶体,能⾼效去除⽔中的重⾦属离⼦
C.氟氯代烷化学性质稳定,排放到⼤⽓中不会造成污染
D.过氧碳酸钠(Na CO )具有强氧化性,可以漂⽩⾐物
2 4
2. 科学家通过核反应 发现氚 。下列说法正确的是
A. 表示⼀个质⼦ B. 的基态原⼦核外电⼦排布式为
C. 与 互为同位素 D. 的原⼦结构示意图为
3.我国某科研团队设计了⼀种新型共轭聚合分⼦反应器,实现CO 和硝酸盐的⾼效偶联。原理为
2
。下列叙述正确的是
A.CO 的电⼦式为
2
B. 的VESPR模型为平⾯三⻆形
C. 分⼦中含有6个σ键
D.C原⼦的电⼦排布由 能够形成原⼦吸收光谱
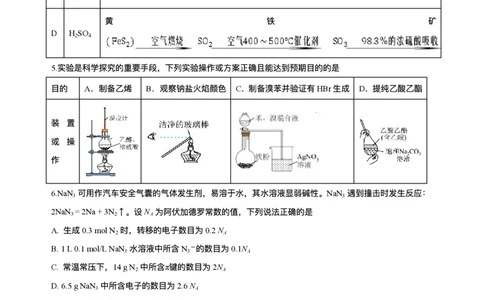
4.⼯业⽣产需综合考虑反应进⾏的可能性、原料来源、成本⾼低和绿⾊环保等多种因素。⼯业⽣产下列物质
学科⽹(北京)股份有限公司时,对应的转化过程符合要求的是
选
物质 转化过程
项
A Na CO NaCl溶液
2 3
B NaOH
C Al 铝⼟矿
⻩ 铁 矿
D H SO
2 4
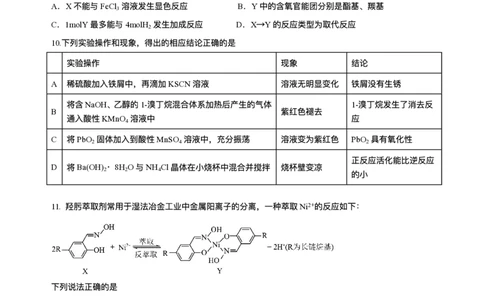
5.实验是科学探究的重要⼿段,下列实验操作或⽅案正确且能达到预期⽬的的是
⽬的 A.制备⼄烯 B.观察钠盐⽕焰颜⾊ C.制备溴苯并验证有HBr⽣成 D.提纯⼄酸⼄酯
装 置
或 操
作
6.NaN 可⽤作汽⻋安全⽓囊的⽓体发⽣剂,易溶于⽔,其⽔溶液显弱碱性。NaN 遇到撞击时发⽣反应:
3 3
2NaN =2Na+3N ↑。设N 为阿伏加德罗常数的值,下列说法正确的是
3 2 A
A. ⽣成0.3molN 时,转移的电⼦数⽬为0.2N
2 A
B.1L0.1mol/LNaN ⽔溶液中所含N -的数⽬为0.1N
3 3 A
C. 常温常压下,14gN 中所含π键的数⽬为2N
2 A
D.6.5gNaN 中所含电⼦的数⽬为2.6N
3 A
7.下列过程对应的离⼦⽅程式正确的是
A. ⽤稀HNO 溶解FeS固体:
3
B.Na S溶液在空⽓中氧化变质:
2
C. ⽤Na S O 溶液脱氯:
2 2 3
D.NaHCO 溶液中通⼊少量Cl :
3 2
8. 化合物XYZ W 为翡翠的主要成分,W、X、Y和Z为原⼦序数依次增⼤的短周期主族元素。基态W原
2 6
学科⽹(北京)股份有限公司⼦的价层电⼦排布式为nsnnp2n,Y的基态原⼦核外电⼦共占据7个原⼦轨道,Z的最⾼正化合价和最低负
化合价的绝对值相等。下列说法中正确的是
A. 简单离⼦半径:X>Y>W B.ZW 的空间构型为直线型
2
C.X和Y的第⼀电离能均⼩于同周期相邻元素 D.YCl 分⼦中所有原⼦均满⾜8e-结构
3
9. 化合物Z是合成药物⾮奈利酮的重要中间体,其合成路线如下,正确的是
A.X不能与FeCl 溶液发⽣显⾊反应 B.Y中的含氧官能团分别是酯基、羰基
3
C.1molY最多能与4molH 发⽣加成反应 D.X→Y的反应类型为取代反应
2
10.下列实验操作和现象,得出的相应结论正确的是
实验操作 现象 结论
A 稀硫酸加⼊铁屑中,再滴加KSCN溶液 溶液⽆明显变化 铁屑没有⽣锈
将含NaOH、⼄醇的1-溴丁烷混合体系加热后产⽣的⽓体 1-溴丁烷发⽣了消去反
B 紫红⾊褪去
通⼊酸性KMnO 溶液中 应
4
C 将PbO 固体加⼊到酸性MnSO 溶液中,充分振荡 溶液变为紫红⾊ PbO 具有氧化性
2 4 2
正反应活化能⽐逆反应
D 将Ba(OH) · 8H O与NH Cl晶体在⼩烧杯中混合并搅拌 烧杯壁变凉
2 2 4 的⼩
11. 羟肟萃取剂常⽤于湿法冶⾦⼯业中⾦属阳离⼦的分离,⼀种萃取Ni2+的反应如下:
下列说法正确的是
A.Y中N-Ni配位键中的电⼦由N的p轨道提供
B.Y可以通过氢键形成五元环结构
C. 向萃取后的有机相中加⼊合适的碱可实现反萃取
D. 冠醚识别Li+与上述原理相同
12. 铈(Ce,镧系元素)的氧化物是常⽤的催化剂,能⽤于汽⻋尾⽓的净化。两种铈的氧化物的⽴⽅晶胞结构
(晶胞参数均为anm)如图a和图b所示。图b晶胞中存在O缺陷,其中Ce的化合价有+3和+4。已知N 为
A
学科⽹(北京)股份有限公司阿伏加德罗常数的值,下列说法正确的是
A.Ce位于元素周期表的ds区
B.图a晶胞中与Ce最近的O的个数为4
C.图b晶胞中化合价为+3的Ce的数⽬为2
D.图a表示的晶体的摩尔体积为
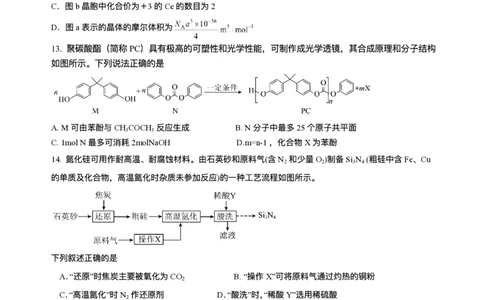
13. 聚碳酸酯(简称PC)具有极⾼的可塑性和光学性能,可制作成光学透镜,其合成原理和分⼦结构
如图所示。下列说法正确的是
A.M可由苯酚与CH COCH 反应⽣成 B.N分⼦中最多25个原⼦共平⾯
3 3
C.1molN最多可消耗2molNaOH D.m=n-1,化合物X为苯酚
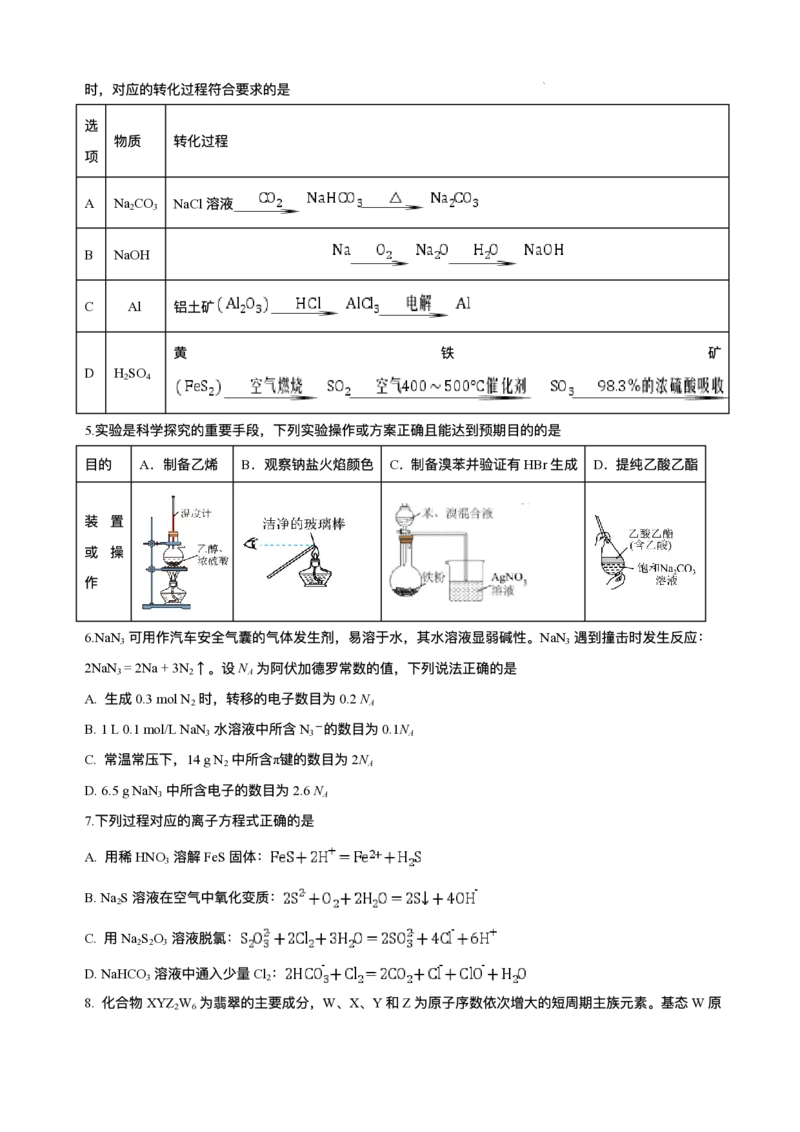
14. 氮化硅可⽤作耐⾼温、耐腐蚀材料。由⽯英砂和原料⽓(含N 和少量O )制备Si N (粗硅中含Fe、Cu
2 2 3 4
的单质及化合物,⾼温氮化时杂质未参加反应)的⼀种⼯艺流程如图所示。
下列叙述正确的是
A.“还原”时焦炭主要被氧化为CO B.“操作X”可将原料⽓通过灼热的铜粉
2
C.“⾼温氮化”时N 作还原剂 D.“酸洗”时,“稀酸Y”选⽤稀硫酸
2
15. 利⽤硼烷独特温和的化学选择性可还原羧酸﹐其机理如下:
下列说法错误的是
A.过程①的进⾏与硼原⼦的缺电⼦有关 B.整个过程中硼的杂化⽅式不发⽣改变
C.过程⑥的反应类型属于取代反应 D.根据上述机理猜测硼烷还可还原酯基
学科⽹(北京)股份有限公司第 II 卷(⾮选择题,共 55 分)
⼆、⾮选择题:本题共4题,共55分。
16.(15分)氮的化合物是重要的⼯业原料,也是⼤⽓和⽔质污染来源,研究氮的化合物的反应具有重要意义,
回答下列问题:
(1)N原⼦的价电⼦排布图
(2)饮⽤⽔中的NO -主要来⾃于NH +。已知在微⽣物作⽤下,NH +经过两步反应被氧化成NO -。两步反
3 4 4 3
应的能量变化示意图如下:
①试写出1molNH +(aq)全部氧化成NO -(aq)的热化学⽅程式是 。
4 3
②NH +中N 的杂化⽅式 ,NO +键⻆⼤于NO -的原因是
4 2 2
(3)联氨(⼜称为肼,分⼦式为N H )⼀种⾼能燃料,常备⽤于⽕箭、航天领域,通常⽤过量NH 与NaClO
2 4 3
溶液反应制得。
①肼的⽔溶液呈弱碱性,其电离⽅程式为
②请写出上述制备肼的化学⽅程式:
③肼(N H )、甲胺(CH NH )、羟胺(NH OH)碱性最强的是
2 4 3 2 2
(4)可利⽤如图电解装置将硝酸⼯业尾⽓中的NO转化为NH NO (假设两电
4 3
极均为惰性电极)。
①M电极上的电极反应式为 。 。
②若回收的NH NO 溶液中溶质的质量增加了40g,则通⼊的NH 在标准
4 3 3
状况下的体积为 L
17.(12分)某兴趣⼩组设计如图实验装置制备次磷酸钠(NaH PO )。
2 2
已知:①⽩磷(P )在空⽓中可⾃燃,与过量烧碱溶液混合,80~90℃⽣成NaH PO 和PH 。
4 2 2 3
②PH 是⼀种有强还原性的有毒⽓体,空⽓中可⾃燃,可与NaClO溶液反应⽣成NaH PO 。
3 2 2
学科⽹(北京)股份有限公司(1)仪器a的名称是 ,a中发⽣反应的化学⽅程式是 。
(2)检查装置⽓密性后,应先打开K通⼊N ⼀段时间,⽬的是 。
2
(3)下列有关说法正确的是 。
A.次磷酸(H PO )是三元酸
3 2
B.为加快反应速率,投料前应先在通⻛橱内将⽩磷碾成薄⽚状
C.d中所盛硫酸铜溶液,可⽤酸性⾼锰酸钾溶液代替
(4)①写出装置c中NaClO溶液在碱性环境中发⽣反应的离⼦⽅ 程
式 。 S(25℃) S(100℃)
②已知NaH PO 和NaCl的溶解度(S)如右表所示,从充分反应 NaCl 37 39 后
2 2
的装置c中获取NaH 2 PO 2 粗品的操作如下: NaH 2 PO 2 100 667
取c中溶液, ___________→_________→冷却结晶→过滤→洗涤→⼲燥→NaH PO 粗品。
2 2
(5)取产品mg配成250mL溶液,取25mL于锥形瓶中,然后⽤0.01mol·L-1KMnO 标准溶液滴定⾄终点(还
4
原产物是Mn2+,氧化产物是PO 3-),达到滴定终点时消耗VmL标准溶液,产品的纯度为 %
4
18.(13分)以⾚泥熔炼渣(主要成分为Fe O 、SiO 、CaO,少量Sc O )为原料分离稀⼟元素钪(Sc)的⼀种⼯
3 4 2 2 3
艺流程如下:
已知:①萃取剂为磷酸三丁酯、磷酸⼆丁酯和磺化煤油;②Sc3+的氧化性很弱。回答下列问题:
(1)稀⼟元素Y为第五周期Sc的同族元素,基态Y原⼦的d能级和s能级电⼦个数⽐
为 。
(2)“浸渣”的主要成分为 (填化学式)。
(3)“萃取”过程使⽤的萃取剂(C H O) PO的结构如图,与Sc3+配位的能
4 9 3
⼒:1号O原⼦
(填“>”“<”或“=”)2号O原⼦。
(4)“反萃取”的⽬的是分离Sc和Fe元素。向“萃取液”中加⼊NaOH,
学科⽹(北京)股份有限公司