文档内容
2025 年秋季高三年级期中考试
化学试卷
考试时间:2025年11月4日下午14:30-17:05 试卷满分:100分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Al-27 Cl-35.5 K-39
一、选择题:(本题共15小题,每小题3分,共45分,每小题只有一个选项符合题意。)
1. 九三阅兵体现了中国国防科技的进步,下列关于大阅兵中涉及到的化学知识错误的是( )
A.庆典用到的聚乳酸气球是一种可降解塑料
B.飞机表演时拉出的彩色烟带是焰色试验
C.新型战斗机机身采用碳纤维复合材料,可以减轻机体重量
D.战士佩戴的防弹头盔材料芳纶是一种高分子材料
2. 下列化学用语表达正确的是( )
A.CO2的价层电子对互斥模型:
3
B.基态S原子的价电子轨道表示式:
C.用电子式表示BeCl 的形成过程:
2
D.天然橡胶的结构简式
3. 下列有关物质性质与用途对应关系错误的是( )
A.单晶硅有半导体性能,可用于制造芯片 B.浓硫酸具有吸水性,可用作干燥剂
C.乙炔燃烧火焰温度高,可用于切割金属 D.SO 具有氧化性,可用作漂白剂
2
4. 钠及其化合物的部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.反应①生成的气体,每22.4L(标准状况)含原子的数目为N
A
B.反应②中2.3gNa完全反应生成的产物中含非极性键的数目为0.1N
A
C.反应③中1molNa O 与足量H O反应转移电子的数目为N
2 2 2 A
D.100mL1molL 1 NaClO溶液中,ClO 的数目为0.1N
A
5. 下列图示实验中,操作规范的是( )
A.用pH试纸测定 B.灼烧海带制海 D.用NaOH溶液滴定
C.收集二氧化碳气体
溶液pH 带灰 醋酸
2025年秋季高三年级期中考试 化学试卷(共8页)第1页6. 下列对物质性质的解释错误的是( )
性质 解释
A 原子光谱是不连续的线状谱线 原子的能级是量子化的
B 聚丙烯酸钠可用于制备高吸水性树脂
聚丙烯酸钠( )中含有亲水基团
C 沸点:H O>H S 电离能:O>S
2 2
D 离子液体可以作为新型电池电解质 离子液体具有导电性
A.A B.B C.C D.D
7.金性质稳定,常用作饰品,但金可以被王水溶解,其方程式为Au+HNO +4HCl=H[AuCl ]+NO↑+2H O。
3 4 2
下列有关说法不正确的是( )
A.NO ﹣的空间构型为平面三角形
3
B.反应中形成的化学键有配位键和极性键
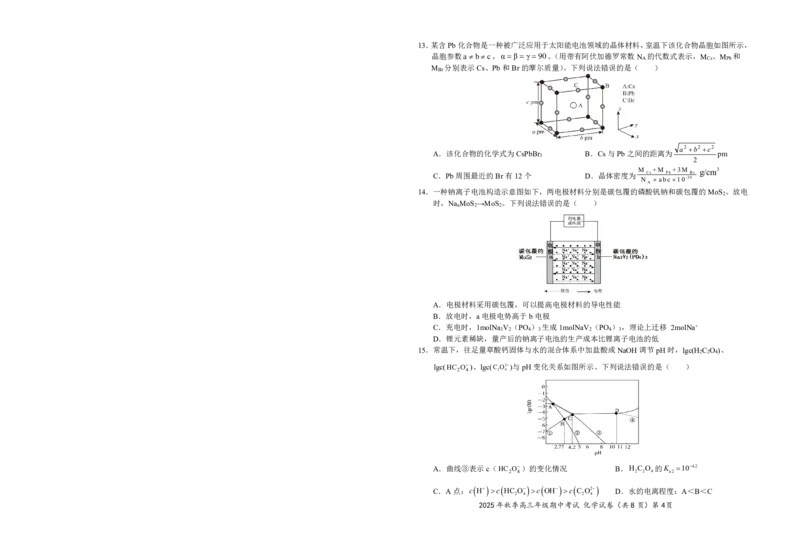
C.第二电离能:O”“<”或“=”),该反应在 (填
2
“高温”或“低温”)自发进行。
2025年秋季高三年级期中考试 化学试卷(共8页)第5页(2)一定温度下,CO、C H 和H (体积比为x:2:1)按一定流速进入装有催化剂Ni-NiO-SiO 的恒容
2 4 2 2
反应器(入口压强为100kPa)发生反应i和ii.有CO存在时,反应ii的反应进程如图1所示。随
转化为目的产物所消耗乙烯的量
着x的增加,C H 的转化率和产物的选择性(选择性 100%)如图
2 4 已转化的乙烯总量
2所示。
①根据图1,下列有关说法正确的是( )
A.生成C H 的决速步反应式C H +C H =C H
4 10 2 5 2 4 4 9
B.生成C H 比生成C H ,活化能较大,反应速率慢
4 8 4 10
C.C H 的选择性大于C H
4 10 4 8
D.*H不参与生成C H 的反应,对生成C H 反应的速率没有影响
4 8 4 8
②结合图2,当x2时,混合气体以较低的流速经过恒容反应器时,反应近似达到平衡,随着
x的增大,C H 的转化率 (填“增大、减小、不变”),原因是
2 4
;
③结合图2,当x2时,在该温度下达到平衡时,C H 的选择性为 ,容器内压强
4 8
为 kPa。
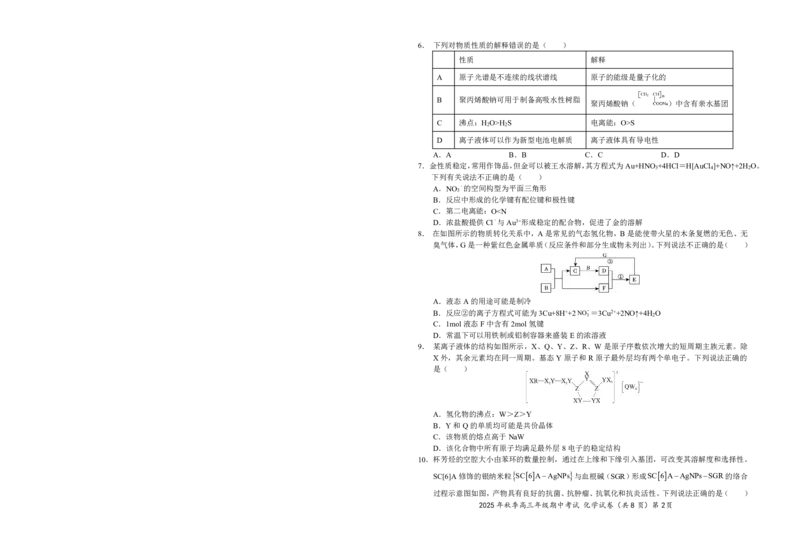
18.(14分)研究一个化学反应可从可行性、速率、平衡等角度考虑。某化学小组对MnO 和KBr在
2
酸性溶液中的反应展开了探究。
查阅资料:①Br 易挥发;该反应在25℃时正反应进行程度较大;②Br 与水反应的程度很小,
2 2
可忽略该反应对其浓度测定的干扰。③低浓度HBr挥发性很小,可忽略。
④I +2Na SO =2NaI+Na S O ;Na S O 和Na S O 溶液颜色均为无色。
2 2 2 3 2 4 6 2 2 3 2 4 6
2025年秋季高三年级期中考试 化学试卷(共8页)第6页(1)写出该反应的离子方程式为 ,该反应的平衡常数的
表达式为 。
(2)展开探究
甲同学:25℃,将0.200molL-1KBr溶液(pH1)与过量MnO 混合,密闭并搅拌,充分反应
2
后,溶液变为黄色,液面上方有淡黄色气体。
乙同学:25℃,将0.200molL-1KBr溶液(pH2)与过量MnO 混合,密闭并搅拌,反应时间
2
与甲相同,溶液变为淡黄色,液面上方未观察到黄色气体。
丙同学:25℃,将0.200molL-1KBr溶液(pH2)与过量MnO 混合,密闭并搅拌,充分反应
2
后,溶液变为淡黄色,液面上方未观察到黄色气体。
25℃时,用浓度较大的KBr溶液与过量MnO 反应,反应前后c(Br-)几乎不变,c(Mn2+)=
2
c(Br ),仅需测定平衡时溶液pH和cBr ,三人分别测定了反应后溶液的pH,取一定量反应
2 2
后溶液,加入过量KI固体,用Na S O 标准溶液滴定并进行了相关计算,滴定时选择较合适的
2 2 3
指示剂是 。
(3)甲计算所得K值小于丙的原因是因为:Br 挥发导致计算时所用 的浓度小于其在溶液中
2
实际浓度。乙通过控制合适pH,使生成cBr 较小,避免了Br 挥发,但计算所得K值也小
2 2
于丙的原因是因为:c
H
浓度小,反应相同时间, ,计算的K值偏
小。请解释丙实验液面上方未观察到黄色气体的原因是 。
(4)三人认为丙实验时间较长,经过讨论认为既要使反应更快的达到平衡状态,又要使Br 处于溶
2
解平衡且挥发最少的状态,可以 ,其他条件与丙相同,可以较准确测得该反
应一定条件下的平衡常数。
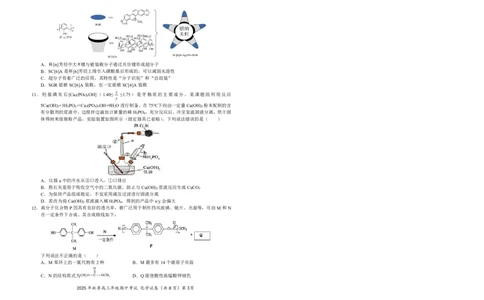
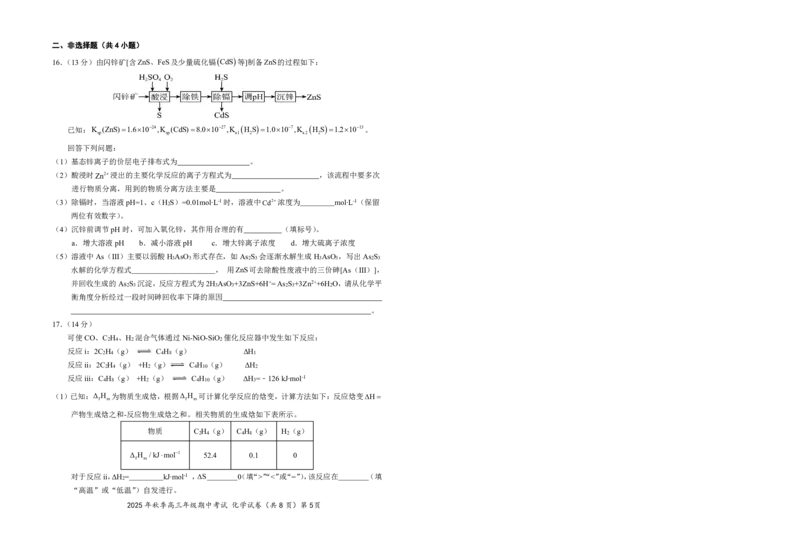
2025年秋季高三年级期中考试 化学试卷(共8页)第7页19.(14分)我国原创用于治疗结直肠癌的新药Z已成功登陆海外市场。Z的一种合成路线如下(部
分试剂及反应条件略)。
BB
CHO
8 8 3
A C D E
F
II
C HClNO
10 9 2 2
G H J
(1)B中含氧官能团有醚键、 、 (填名称),B的核磁共振氢谱有
组吸收峰。
(2)H生成J的反应类型为 ,J中氮原子的杂化方式为 。
(3)I的结构简式为 。
(4)已知 +HN=CHNH ΔNH +H O+ ,L的同分异构体
2 3 2
K
L
M发生取代反应可生成I,M的结构简式为 。请写出CH COOH、CH CH CH NH 、
3 3 2 2 2
HN=CHNH 在加热的条件下发生反应的化学方程式 。
2
2025年秋季高三年级期中考试 化学试卷(共8页)第8页