文档内容
2024 年重庆市普通高中学业水平选择性考试
高三第一次联合诊断检测 化学
化学测试卷共4页,满分100分。考试时间75分钟。
可能用到的相对原子质量:N-14 O-16 Na-23 Ca-40 Fe-56
一、选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项符合题目要求。
1. 百年变局,科技创新是“关键变量”。2023年中国科技取得新突破,下列材料属于无机半导体材料的是
A.“北斗卫星” B.“ 奋 斗 者 ” 潜 水器 C.“中国天眼(FAST)” D.“山东舰”
氮化镓芯片 钛合金外壳 合成树脂镜面 特种钢甲板
2. 下列离子方程式书写正确的是
A.NaHSO 水解:HSO-+H O H O++SO2-
3 3 2 3 3
B.CO 通入BaCl 溶液中:Ba2++CO +H O=BaCO ↓+2H+
2 2 2 2 3
C.Mg(HCO ) 溶液与足量NaOH溶液反应:Mg2++HCO-+OH-=MgCO ↓+H O
3 2 3 3 2
D.金属铝与NaOH溶液反应:2Al+2OH-+6H O=2[Al(OH) ]-+3H ↑
2 4 2
3. 已知反应CaSO +2NH +CO +H O=CaCO +(NH ) SO 可以制取硫酸铵晶体,下列说法正确的是
4 3 2 2 3 4 2 4
A.CO 的电子式为 O C O B.NH+的VSEPR模型为三角锥形
2 4
C.钙离子结构示意图为 +20288 D.(NH ) SO 由非金属元素组成,仅含共价键
4 2 4
4. 下列叙述正确的是
A.浓硝酸见光分解的产物有NO、O 、H O B.CaSO (s)加入饱和Na CO 溶液中可生成CaCO (s)
2 2 4 2 3 3
C.苏打不稳定,受热分解生成CO D.铜分别与Cl 和S粉在加热条件下反应生成CuCl 和CuS
2 2 2
5. 已知反应:Fe+6HNO (浓) Fe(NO ) +3NO ↑+3H O,N 为阿伏加德罗常数的值,若反应消耗了28g Fe
3 3 3 2 2 A
粉(HNO 足量)。下列说法正确的是
3
A.所得溶液中Fe3+数目为0.5N B.收集到的NO 分子数为1.5N
A 2 A
C.转移的电子数为1.5N D.生成的H O含共价键数为2N
A 2 A
6. 离子液体在化工领域具有广泛的应用前景。一种离子液体的结构如图所示,下列有关说法不正确的是
A.电负性:F>N>C>H
+
H C
B.第一电离能:I (N)>I (F)>I (C)>I (B) 3 CH
1 1 1 1 N 3 BF-
C.该化合物的离子键弱,熔点低 N 4
D.该化合物中N原子发生sp2和sp3杂化
7. 下列实验装置及操作能达到相应实验目的的是
温度计 玻璃搅拌器
镊子
2% AgNO
3
溶液
内筒 杯盖
隔热层 pH试纸 2%氨水
外壳
A.中和热测定 B.除去Fe(OH) 胶体中的NaCl溶液 C.测定溶液的pH D.配制银氨溶液
3
8. LK-99是一种将Pb (SO )O和Cu P 按1︰1比例在真空石英管中加热到 925℃后形成的铜掺杂改性铅磷灰石材
2 4 3
料,可表示为M Y (XW ) W。W、X为既不同周期也不同主族的短周期元素,M、Y为金属元素,M元素的
(10-x) x 4 6
原子与碳原子具有相同的最外层电子数。下列说法正确的是
A.简单氢化物的稳定性:X>W B.原子半径:Y>M>X
C.一定条件下,Y能与硫酸反应生成气体 D.X元素最高价氧化物对应的水化物属于强酸
第一次联合诊断检测(化学)参考答案 第1页 共9页9. 常温下,用0.1000mol·L-1的NaOH溶液滴定10.00mL等浓度的HCl溶液和用0.1000mol·L-1的CH COOH溶
3
液滴定10.00mL等浓度的NaOH溶液,滴定过程中溶液的导电能力如图所示。
下列说法不正确的是 导
电 a
A.a点的K w 等于b点的K w 能 b c ①
力
B.等浓度等体积的HCl溶液与NaOH溶液的导电能力不相同 d e
②
C.c点溶液中阴离子总浓度大于d点溶液中阴离子总浓度
0 10 20 V/mL
D.e点溶液中:c(H+)+c(CH COOH)=2c(OH-)+c(CH COO-)
3 3
10.光响应高分子材料在人工肌肉、微型机器人等领域有广泛的应用前景。我国科学家合成了一种光响应高分子M,
其合成路线如图,下列说法正确的是
O
催化剂 ( )( )
E + O
HO 酯化反应 m n
F G O O
一定条件
O O ( )
O 4 O
( ) N
O 4 O B
NN
B
M
H
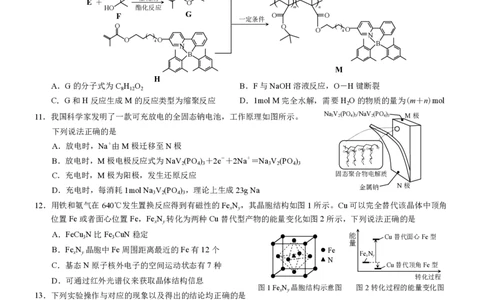
A.G的分子式为C H O B.F与NaOH溶液反应,O-H键断裂
8 12 2
C.G和H反应生成M的反应类型为缩聚反应 D.1mol M完全水解,需要H O的物质的量为(m+n)mol
2
11.我国科学家发明了一款可充放电的全固态钠电池,工作原理如图所示。 Na 3 V 2 (PO 4 ) 3 /NaV 2 (PO 4 ) 3 M极
下列说法正确的是
B A . . 放 放 电 电 时 时 , , M Na 极 +由 电 M 极 极 反 迁 应 移 式 至 为 N Na 极 V 2 (PO 4 ) 3 +2e-+2Na+=Na 3 V 2 (PO 4 ) 3 O [ O O ∞ O O O ∞ O O O ∞ O O O ∞ ] n
C.充电时,M极为阳极,发生还原反应 固态聚合物电解质
D.充电时,每消耗1mol Na V (PO ) ,理论上生成23g Na 金属钠 N极
3 2 4 3
12.用铁和氨气在640℃发生置换反应得到有磁性的Fe N,其晶胞结构如图1所示。Cu可以完全替代该晶体中顶角
x y
位置Fe或者面心位置Fe,FeN 转化为两种Cu替代型产物的能量变化如图2所示,下列说法正确的是
x y
A.FeCu 3 N比Fe 3 CuN稳定 能 Cu替代面心Fe型
量
B.FeN 晶胞中Fe周围距离最近的Fe有12个 Fe
x y FeN
x y
N
C.基态N原子核外电子的空间运动状态有7种 Cu替代顶角Fe型
转化过程
D.可通过红外光谱仪来获取晶体结构信息
图1 FeN 晶胞结构示意图 图2 转化过程的能量变化图
x y
13.下列实验操作与对应的现象以及得出的结论均正确的是
选项 实验操作 现象 结论
A 向Na SiO 溶液中加入稀盐酸 产生白色沉淀 非金属性:Cl>Si
2 3
B 向Na[Al(OH) ]溶液中滴加NaHCO 溶液 产生白色沉淀 结合H+的能力:[Al(OH) ]->CO2-
4 3 4 3
C 常温下用pH计测定0.1mol·L-1 NaHCO 3 NaHCO 3 (aq )为8.3, 水解平衡常数:
溶液和0.1mol·L-1 CH 3 COONa溶液的pH CH 3 COONa(aq)为8.9 K h (HCO- 3 )<K h (CH 3 COO-)
取一支试管加入1mL 2mol·L-1 NaOH
先生成白色沉淀,
D 溶液,先滴加1mL 0.5mol·L-1 MgCl K [Cu(OH) ]<K [Mg(OH) ]
2 sp 2 sp 2
后沉淀变为蓝色
溶液,再滴几滴1mol·L-1 CuCl 溶液
2
第一次联合诊断检测(化学)参考答案 第2页 共9页14.某温度下,在刚性密闭容器中模拟用FeO冶炼Fe涉及如下反应:①FeO(s)+CO(g) Fe(s)+CO (g) K =1,
2 p1
②FeO(s)+C(s) Fe(s)+CO(g),反应达到平衡时,测得容器内的压强为1600kPa。下列说法不正确的是
A.该温度下,反应②的平衡常数为800 kPa B.容器内气体密度不再发生变化时,反应①达到平衡
C.通入CO,再次达到平衡,容器内总压强不变 D.若温度不变,缩小容器体积,则CO的平衡分压增大
二、非选择题:本题共4小题,共58分。
15.(14分)工业上以菱锰矿(主要成分为MnCO ,含杂质CaCO 、FeCO 、NiCO )为原料制取金属锰的工艺流
3 3 3 3
程如下:
HSO MnO 稀氨水 (NH)S NH F
2 4 2 4 2 4
菱锰矿粉 酸浸 调pH 除杂1 除杂2 电解 Mn
滤渣1 滤渣2 滤渣3 滤渣4
已知常温下,溶度积常数(K )如下表:
sp
NiS MnS Mn(OH) Fe(OH) Ni(OH) Fe(OH)
2 3 2 2
1.0×10-24 2.5×10-10 1.9×10-13 2.8×10-39 5.5×10-16 4.8×10-17
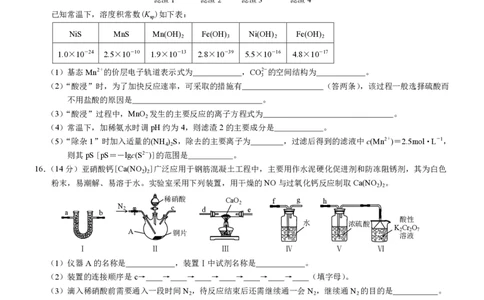
(1)基态Mn2+的价层电子轨道表示式为 ,CO2-的空间结构为 。
3
(2)“酸浸”时,为了加快反应速率,可采取的措施有 (答两条),该过程一般选择硫酸而
不用盐酸的原因是 。
(3)“酸浸”过程中,MnO 发生的主要反应的离子方程式为 。
2
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是 。
(5)“除杂1”时加入适量的(NH ) S,除去的主要离子为 ,过滤后得到的滤液中c(Mn2+)=2.5mol·L-1,
4 2
则其pS [pS=-lgc(S2-)]的范围是 。
16.(14分)亚硝酸钙[Ca(NO ) ]广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色
2 2
粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的NO与过氧化钙反应制取Ca(NO ) 。
2 2
稀硝酸 CaO f g h
2
a b
N 2 c d e
酸性
水 浓硫酸
KCrO
A 铜片 2
溶液
2 7
Ⅰ Ⅱ Ⅲ Ⅳ Ⅴ Ⅵ
(1)仪器A的名称是 ,装置Ⅰ中试剂名称是 。
(2)装置的连接顺序是c→ → → → → → → (填字母)。
(3)滴入稀硝酸前需要通入一段时间N ,待反应结束后还需继续通一会N ,继续通N 的目的是 。
2 2 2
(4)装置Ⅱ中滴入稀硝酸后,A中观察到的现象是 。
(5)装置Ⅴ的作用是 。
(6)装置Ⅵ中氮元素被氧化成+5价,则反应的离子方程式为 。
(7)测定所得亚硝酸钙产品中硝酸钙的含量,实验步骤如下:
足量NHCl 25.00mL a mol·L-1 b mol·L-1
4
足量Na
2
SO
4
溶液 饱和溶液 (NH
4
)
2
Fe(SO
4
)
2
和适量H
2
SO
4
K
2
Cr
2
O
7
标准液
称量mg
除Ca2+ 除NO- 还原NO- 滴定Fe2+
产品溶于水 2 3
N NO
2
①除去NO-时,需要煮沸3min,其反应的化学方程式为 。
2
②滴定时消耗标准液的体积为V mL,则所得产品中硝酸钙的质量分数为 。
第一次联合诊断检测(化学)参考答案 第3页 共9页17.(15分)综合利用二氧化碳可以缓解温室效应。
(1)利用二氧化碳催化氢化获得甲酸的部分反应历程如右图,该反应
历程的决速步骤是 (填序号),由中间产物T2到产物的
∆H= 。
(2)二氧化碳与氢气反应过程涉及的主要反应如下:
①CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49.5 kJ·mol-1
2 2 3 2 1
②CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ·mol-1
2 2 2 2
向2L恒容密闭容器中通入2mol CO (g)和2.24mol H (g)发生上述反应①和②,起始总压强为21.2MPa,实验
2 2
测得CO
2
的平衡转化率和平衡时CH
3
OH的选择性(转化的CO
2
中 100
X
100
80 80
生成CH
3
OH的百分比)随温度变化如右图。表示CH
3
OH选择性的
60 b Y 60
曲线是 (填“X”或“Y”),a、c两点中CH OH的产率最 40 40
3 a c
20 20
高的是 点,240℃时反应①的压强平衡常数K = (MPa)-2,
p 0 0
200 240 280 320 360
Y曲线如此变化的原因是 。
温度/℃
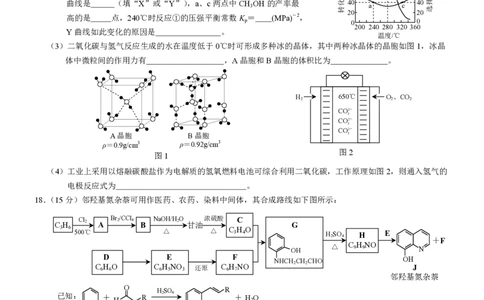
(3)二氧化碳与氢气反应生成的水在温度低于0℃时可形成多种冰的晶体,其中两种冰晶体的晶胞如图1,冰晶
体中微粒间的作用力有 ,A晶胞和B晶胞的体积比为 。
H 2 650℃ O 2 、CO 2
CO2-
3
CO2-
3
CO2-
A晶胞 B晶胞 3
ρ=0.9g/cm3 ρ=0.92g/cm3
图2
图1
(4)工业上采用以熔融碳酸盐作为电解质的氢氧燃料电池可综合利用二氧化碳,工作原理如图2,则通入氢气的
电极反应式为 。
18.(15分)邻羟基氮杂萘可用作医药、农药、染料中间体,其合成路线如下图所示:
C H Cl 2 A Br 2 /CCl 4 B NaOH/H 2 O 甘油 浓硫酸 C G
3 6 500℃ △ △ C 3 H 4 O H 2 SO 4 H E
+F
OH △ C 9 H 9 NO N
D E F
NHCHCHCHO OH
C 6 H 6 O C 6 H 5 NO 3 还原 C 6 H 7 NO 2 2 J
邻羟基氮杂萘
O HSO R
已知: + H R 2 △ 4 + H 2 O
(1)A的名称为 ,F中官能团名称是 ,B→甘油的反应类型是 。
(2)C能与银氨溶液发生银镜反应,其化学方程式为 。
(3)H+E→J的化学方程式为 。
(4)化合物G的同分异构体中能同时满足下列条件的有 种(不考虑立体异构)。
①能发生银镜反应 ②能与FeCl 溶液发生显色反应 ③含有-NH ④苯环上有两个取代基
3 2
(5)根据流程中的信息和已学知识,写出下列流程(Ar为芳基)中Y、Z的结构简式: 、 。
Ar H
NN
O H 2 SO 4 X
Y Z
N 还原 N △ N
NO NH Ar
2 2
X
第一次联合诊断检测(化学)参考答案 第4页 共9页
%/率化转 %/性择选
)lom/Jk(/量能对相
TS2(16.87)
④ TS3(11.53)
③ ⑤
TS1(2.34) T2(5.31) ⑥
①
②
反应物(0.00)
T1(-1.99) 产物(-2.38)
反应历程