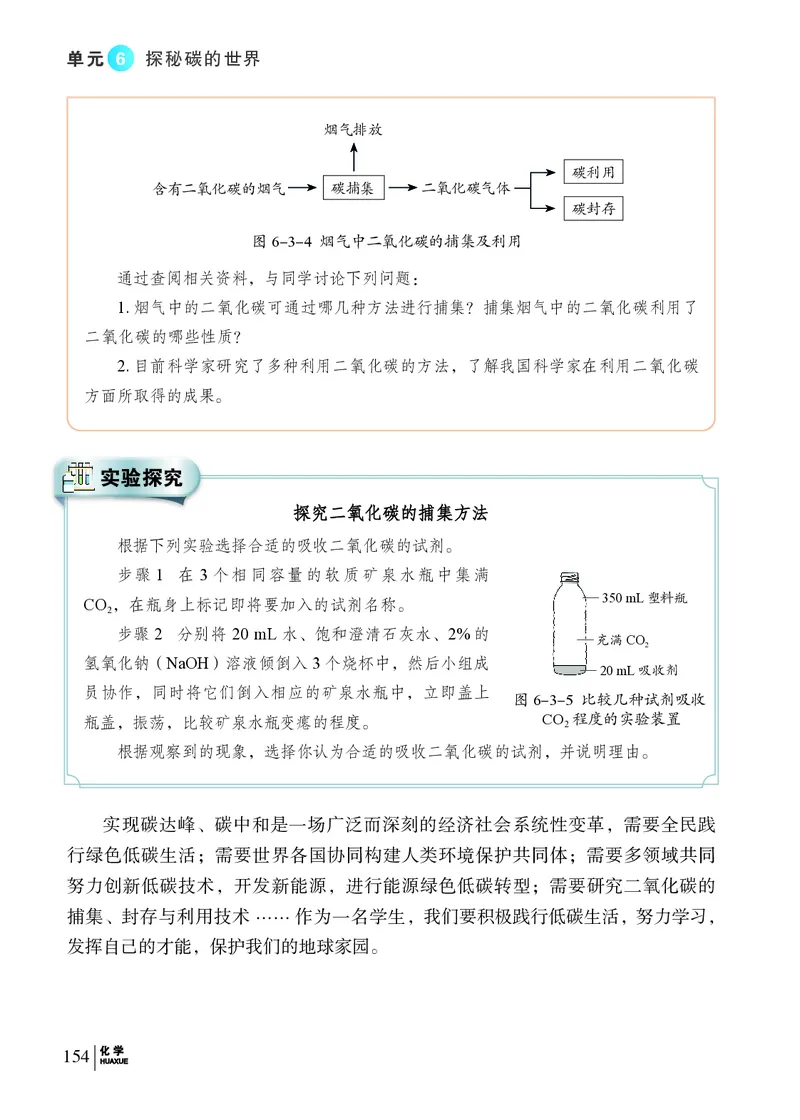
文档内容
义
务 义 务 教 育 教 科 书
教
育
教
科
书
化化 学学
化
九年级 上册
学
九
年
级
上
册
定价:10.95元
绿色印刷产品 价格投诉举报电话:12315义 务 教 育 教 科 书
化 学
九年级 上册
科 学 普 及 出 版 社
·北 京·图书在版编目(CIP)数据
义务教育教科书. 化学九年级 上册 / 北京市仁爱教
育研究所编著. -- 北京:科学普及出版社,2024. 8.
ISBN 978-7-110-10822-2
Ⅰ. G634
中国国家版本馆CIP数据核字第2024MK8232号
北京市仁爱教育研究所 编著
周 青
主 编
吕 琳
副 主 编
(按姓氏笔画排列)
编 者
王 峰 王伟群 杨玉琴 汪定用 唐 敏 曹旭琴 景崤壁
周 婷
责任编辑
北京市仁爱教育研究所
装帧设计
徐 飞
责任印制
科学普及出版社
出 版
中国科学技术出版社有限公司
发 行
北京市海淀区中关村南大街16号
地 址
100081
邮 编
010-62173865
发行电话
010-62173081
传 真
http://www.cspbooks.com.cn
网 址
787 mm×1092 mm 1/16
开 本
211千字
字 数
11.5 印张
印 张
2024 年 8 月第 1 版
版 次
2024 年 8 月第 1 次印刷
印 次
河北新华第二印刷有限责任公司
印 刷
ISBN 978-7-110-10822-2 / G·4397
书 号
10.95元
定 价
价格批准文号:冀发改价调【2022】1365号 冀发改价审【2024】122004
价格投诉举报电话:12315
(声明:我们已尽可能取得作品权利人的授权或许可,作品权利人如有关于报酬支付事宜可与我们联系。)
如有质量问题,影响阅读,请联系:
地址:北京市海淀区北四环西路68号左岸工社12层北京市仁爱教育研究所 邮编:100080
电话:4008100168 010-82676936
邮箱:editor@renai-edu.com前前言言
亲爱的同学们:
这学期我们将开始学习一门新的课程——化学。
打开上册化学课本,你会发现,课本中探讨的都是你熟悉的
情境和有趣的课题:呼吸的空气、物质的组成、燃料的燃烧、变
化的表示、碳世界的奥秘等,这些都与我们的生活息息相关。在
这些课题的学习中,你会更多地了解物质及其变化的奥秘,感受
化学的美妙与神奇,学会从化学视角观察世界、以化学思维思考
世界、用化学语言表达世界。
课本中不仅有丰富的化学知识,还有丰富多彩的图片,有功
能各异的学习栏目。“情境问题”能帮助你在已有的知识经验基
础上从化学的视角思考课题学习的内容;“化学史话”“阅读理
解” “交流讨论” “观察思考”“实验探究”“方法引导”等
栏目,能帮助你通过观察、思考、实验等学习化学知识、技能和
方法;“联系实际”“练习实践”“单元作业”“项目学习”“跨
学科实践活动”等栏目,能让你学会应用所学化学知识解决实际
问题;“单元小结”能引导你对所学知识进行整理归纳、复习
总结。
与其他科学课程一样,学习化学需要对物质世界充满好奇心
和探究欲,需要细心观察、积极思考、动手实验,需要联系生产、
生活实际来理解和解决与化学相关的问题。
我们深信,通过化学学习,你一定会增长智慧,增长为国家
作贡献的力量。目录
1
单元 走走进进化化学学世世界界
课题1 丰富多彩的物质世界…………………………… 2
课题2 化学通过实验研究物质………………………… 10
课题3 化学服务于人类社会发展……………………… 18
2
单元 探探析析空空气气之之谜谜
课题1 空气组成的探究………………………………… 28
课题2 氧气的性质与应用……………………………… 32
课题3 空气资源的保护………………………………… 42
3
单元 初初探探物物质质构构成成
课题1 探秘微观粒子特性……………………………… 52
课题2 认识原子结构…………………………………… 58
课题3 物质组成的表示………………………………… 65
4
单元 再再探探燃燃烧烧与与燃燃料料
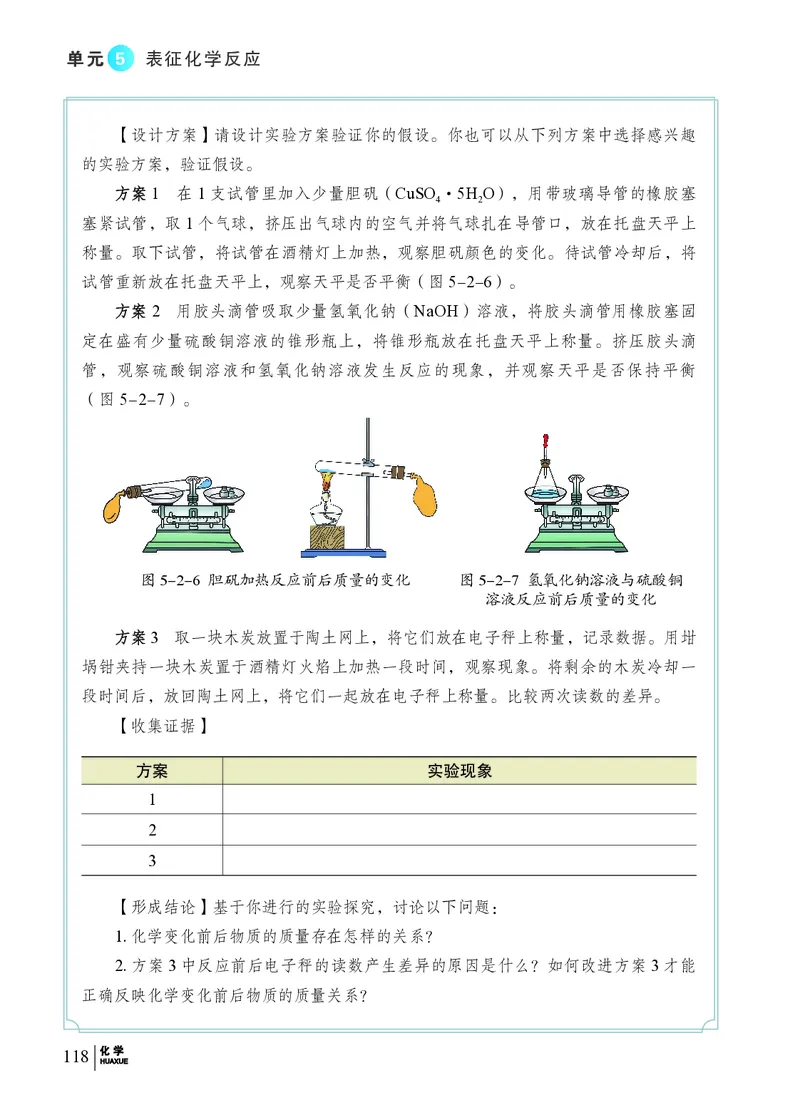
课题1 燃烧与灭火……………………………………… 80
课题2 化学反应中的能量变化………………………… 91
课题3 化石燃料的综合利用与新能源开发…………… 965
单元 表表征征化化学学反反应应
课题1 化学反应是有条件的……………………………108
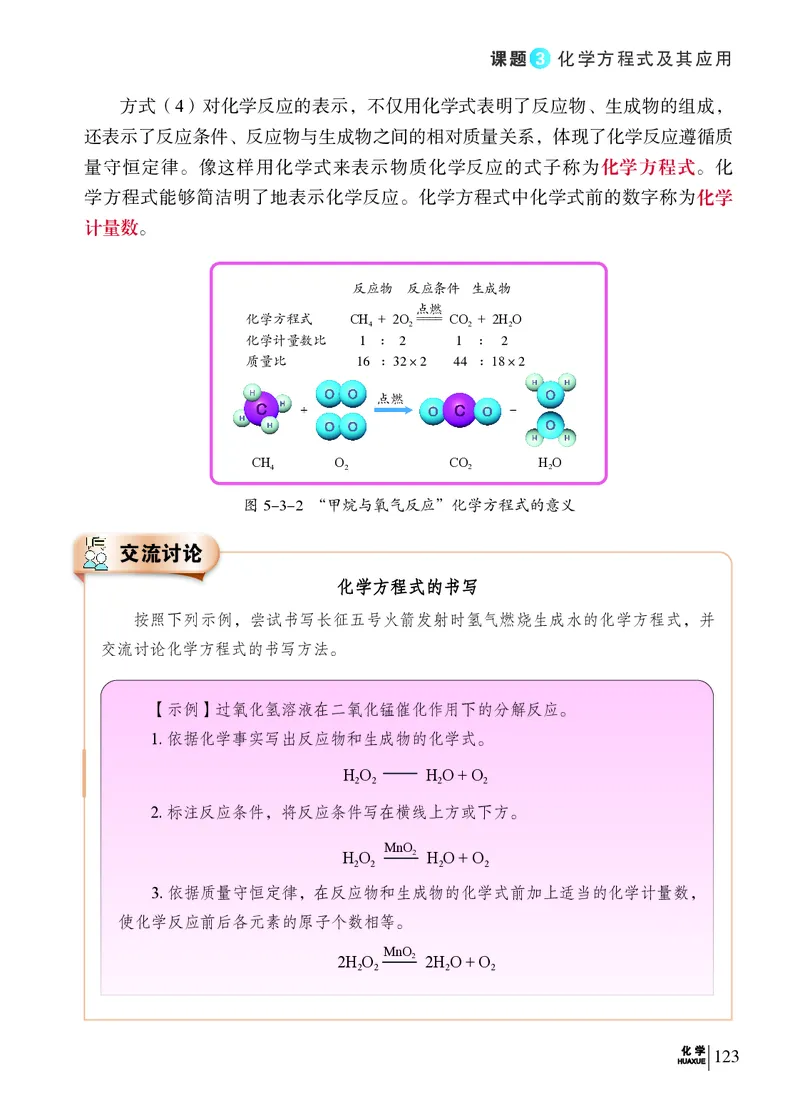
课题2 质量守恒定律……………………………………114
课题3 化学方程式及其应用……………………………122
6
单元 探探秘秘碳碳的的世世界界
课题1 神秘的碳家族……………………………………134
课题2 二氧化碳的性质与应用…………………………142
课题3 碳循环与碳中和…………………………………150
学 生
实 验
实验1 实验基本操作………………………………………………………………161
实验2 氧气的实验室制取与性质…………………………………………………163
实验3 燃烧条件的探究……………………………………………………………166
实验4 二氧化碳的实验室制取与性质……………………………………………168
跨 学 科
实 践 活 动
一、简易制氧器的制作 ……………………………………………………………… 171
二、基于碳中和理念设计低碳行动方案…………………………………………… 172附 录
附录1 化学实验规则………………………………………………………………174
附录2 中学化学实验常用仪器……………………………………………………175
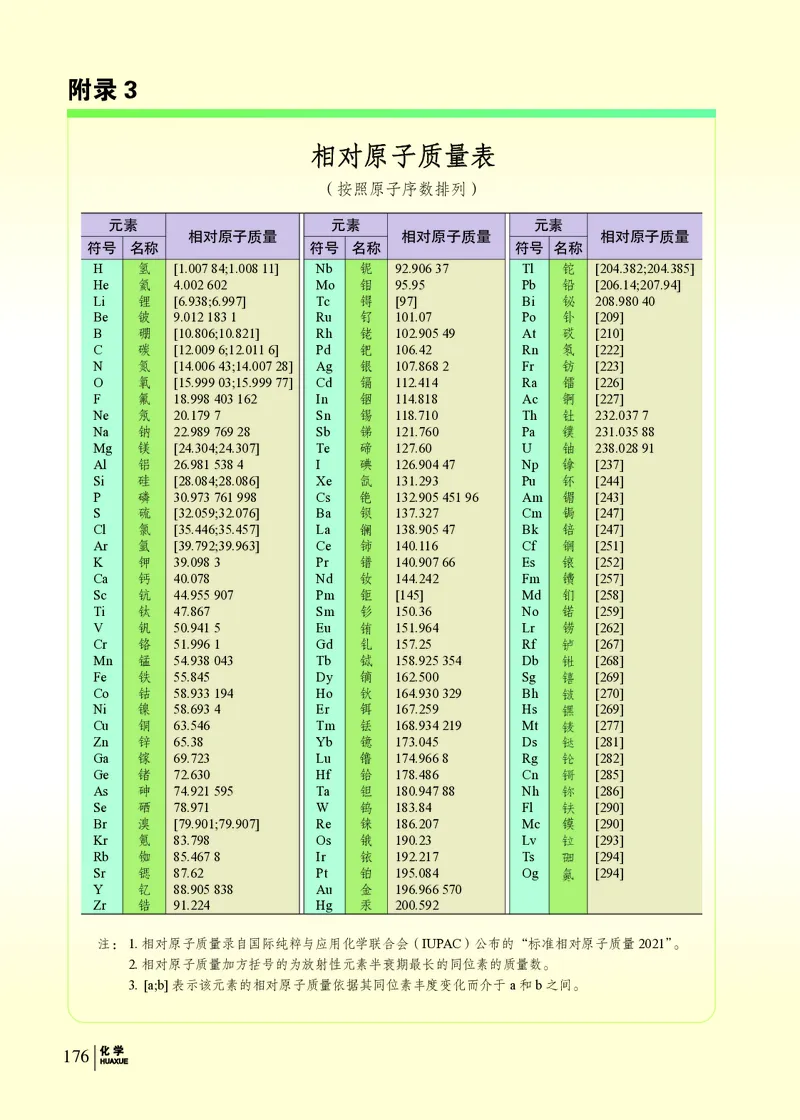
附录3 相对原子质量表……………………………………………………………176
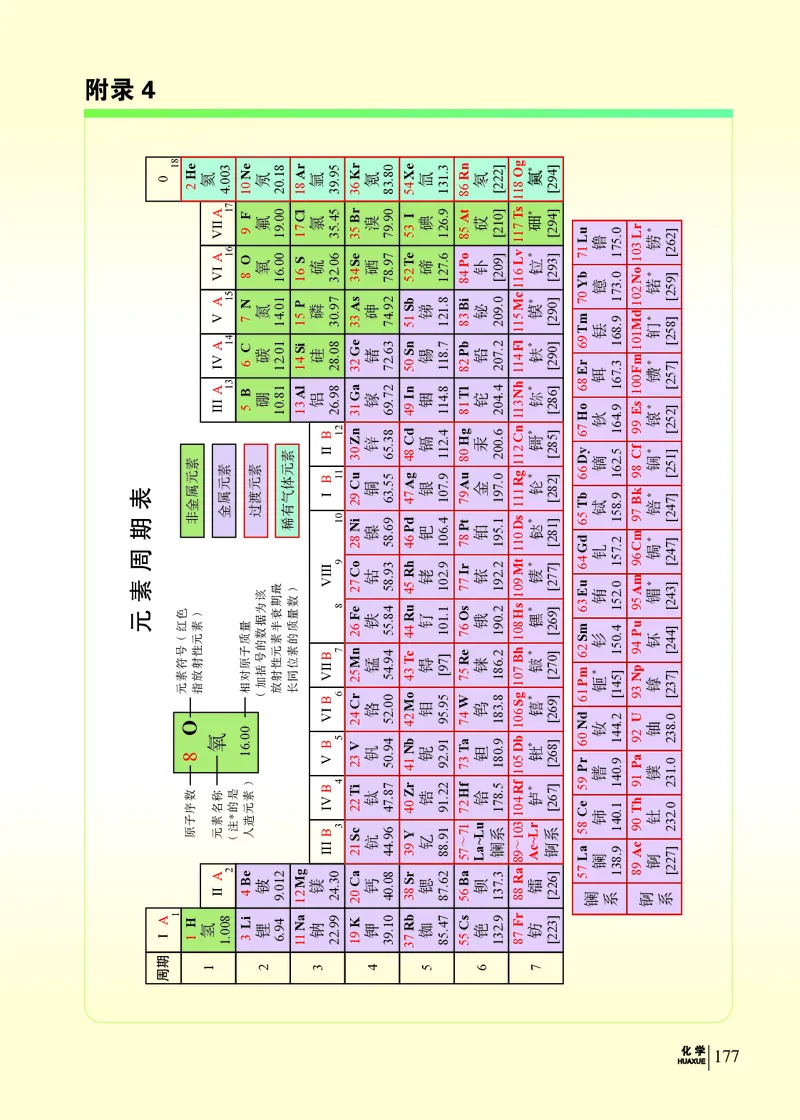
附录4 元素周期表…………………………………………………………………177单元 1 走进化学世界
课题 1 丰富多彩的物质世界
情境问题
世世界界是是由由物物质质组组成成的的
我们生活的世界,大到天体、小到尘埃都是由物质组成的。人类生活也离不开
物质,如我们呼吸的空气、喝的水、吃的食物等都是物质。
图1-1-1 世界由物质组成 图1-1-2 人类生活离不开物质
面对物质世界,你可能有许多的疑惑,在该课题中我们将共同探究:
1.如何认识纷繁多样的物质?
2. 物质是否会发生变化?
3. 物质的用途与其性质之间有怎样的关系?
一、组成世界的物质纷繁多样
在生活中,我们每时每刻都在与各种物品打交道,如餐具、衣服、桌椅、文具、
书本等,而这些物品都是由一些更为基本的物质制造出来的。如塑料文具和塑料餐
具由塑料制成,玻璃杯和玻璃窗由玻璃制成,衣服、被褥和书包由各种纤维制成等。
物质种类极其多样,既有大自然馈赠给人类的,也有人类通过化学方法创造出
来的。它们用途广泛,为人类构建了一个丰富多彩的世界。
目前人类发现和创造的物质数以亿计,它们的组成、性质和用途存在着差异。
如氧气由氧元素组成,常温下为气态,能支持燃烧;水由氧元素和氢元素组成,常
温下为液态,能灭火;铜由铜元素组成,常温下为紫红色固体,能导电,可用于制
作导线 ……
2 化化 学学
HHUUAAXXUUEE课题 1 丰富多彩的物质世界
在我们发现和接触到的物质中,有的仅由一种物质组成,如水、氧气、铜、
氮气等,这类物质称为纯净物;有的由两种或两种以上物质组成,如空气、牛奶、
盐水等,这类物质称为混合物。
交流讨论
物物质质的的初初步步分分类类
请列举你常接触或知道的物质的名称,尝试将你列举出的物质进行分类,并与
老师、同学交流讨论你的分类依据。
水存在固态、液态、 空气中含有氮气、 铅笔外层为油漆和木材, 电线里层为铜,外层
气态三种状态 氧气等物质 内部笔芯主要成分是石墨 为橡胶或塑料
图1-1-3 形形色色的物质
方法引导
物质的分类
分类是根据研究对象的共同点和差异点,将它们区
分为不同种类和层次的科学方法。通过分类,人们可以
分门别类地认识物质,提高认识物质的效率。
对物质进行分类时需要依据物质的某种属性进行
划分。如依据聚集状态将物质分为气态、液态、固态
物质;依据组成将物质分为纯净物和混合物;依据导 图1-1-4 分类在生活中的应用
电性将物质分为导体、半导体、绝缘体等。
化学根据物质的组成、性质、结构、用途等对物质进行分类,通过研究同一类
物质的共性和不同类物质的性质差异,帮助人们更好地认识丰富多彩的物质,以服
务于人类的生产和生活。
化化 学学 3
HHUUAAXXUUEE单元 1 走进化学世界
二、组成世界的物质不断变化
如果我们注意观察就会发现,在自然界以及我们的生产生活中,物质时刻发生
着各种变化。如暴露在空气中的钢铁会缓慢生锈,江河湖泊中的水总在不断蒸发,
塑料制品在使用过程中会不断老化等。
观察思考
物物质质的的变变化化是是多多样样的的
实实验验1 用镊子夹住一小块干冰放入蒸发皿中,观察现象,思考干冰发生的变化
有怎样的特点。
实实验验2 点燃 1 根蜡烛,观察燃烧过程中发生的现象,然后取 1 个冷而干燥的
烧杯和 1 个用澄清石灰水润湿内壁的烧杯,先后罩在火焰上方,观察烧杯内壁上有什
么现象发生,推测蜡烛燃烧后生成了什么物质。
图1-1-5 干冰的升华 图1-1-6 蜡烛的燃烧
在上述实验中,放置在空气中的干冰(固态二氧化碳)会升华,即由固态转变
为气态,并吸收周围的热量,使空气中的水蒸气凝结成小水滴而形成白雾。蜡烛燃
烧时发光、放热,燃烧中受热熔化的石蜡向下流淌时又逐渐凝固,燃烧后生成了水
以及能使澄清石灰水变浑浊的二氧化碳。可见,物质的变化是多样的。
根据物质变化的特征,可将物质变化分为物理变化和化学变化。有新物质生成
的变化为化学变化(又称化学反应),如蜡烛燃烧生成了二氧化碳和水。而没有新
物质生成的变化为物理变化,如干冰的升华、熔化的石蜡凝固等。
4 化化 学学
HHUUAAXXUUEE课题 1 丰富多彩的物质世界
联系实际
物物质质变变化化类类型型的的判判别别
1.观察图1-1-7,描述下列物质变化的现象,判断这些变化的类型,并将你思考
的结果填写在表格中。
树枝燃烧 铜棒拉成铜丝 冰凌生成与消融 铁钉生锈
图1-1-7 常见的物质变化
物质发生的变化 变化的现象 变化的类型
树枝燃烧
铜棒拉成铜丝
冰凌生成与消融
铁钉生锈
2.在日常生活中,物质的变化随处可见。请列举出你见过的物质变化的事例,并
进行分类。
物质变化是物理变化还是化学变化,关键在于变化中是否有新物质生成。如冰
凌生成与消融、铜棒拉成铜丝,都没有新物质生成,属于物理变化;树枝在空气中
燃烧有二氧化碳和水生成,铁与空气中的水和氧气发生反应生成铁锈,这些过程
中均有新物质生成,属于化学变化。
化学变化中,还经常伴随着许多奇妙的现象。
观察思考
化化学学变变化化伴伴随随的的现现象象
观察下列实验,尝试描述这些实验中发生的现象。
实实验验1 取 2 g 氧化钙放入烧杯中,加入适量水浸没氧化钙,将 1 支温度计插入
化化 学学 5
HHUUAAXXUUEE单元 1 走进化学世界
其中(图1-1-8),观察温度的变化,然后在烧杯中滴加几滴酚酞溶液(图1-1-9),
观察颜色的变化。
图1-1-8 氧化钙与水反应 图1-1-9 氢氧化钙使酚酞溶液变红
实实验验2 将棉手帕放入用酒精与水按体积比为1 ∶ 1配成的溶液里浸透,然后轻
挤出多余酒精溶液。用坩埚钳夹住手帕一角放到酒精灯上点燃,手帕燃着后离开酒
精灯,晃动手帕(图1-1-10),观察现象。
实实验验3 向 2 支试管中各加入 2 mL 硫酸铜溶液,然后向其中1 支试管中滴加氢
氧化钠溶液,向另1支试管中加入1根洁净的铁钉,观察现象(图 1-1-11)。
图1-1-10 “烧不坏”的手帕 图1-1-11 硫酸铜溶液分别与氢氧化钠溶液和铁反应
实实验验4 取2个集气瓶,向其中1个集气瓶中滴加一滴浓盐酸,向另1个集气瓶
中滴加一滴浓氨水,迅速用毛玻璃片盖住两个瓶口,然后将其中1个集气瓶倒放在另
1个集气瓶的瓶口上,抽出毛玻璃片,观察现象(图 1-1-12)。
图1-1-12 浓盐酸与浓氨水反应
6 化化 学学
HHUUAAXXUUEE课题 1 丰富多彩的物质世界
方法引导
实验观察方法
实验观察是获取实验信息的重要途径,是科学探究中获取证据的重要手段。
实验观察前,要明确观察目的,做好观察规划,然后通过“看”“听”“闻”“触
摸”等手段,甚至借助仪器设备,有目的、有计划地获取物质及其变化的信息,并记
录观察到的现象。
观察时要积极思考,尝试解释观察到的实验现象,分析产生现象的原因,并依据
观察到的现象进行推理,形成结论。
通过上述实验可以发现,物质发生化学变化时,除有新物质生成,还常伴随着
发光、放热、颜色变化、生成沉淀、放出气体等现象。如酒精燃烧时,能看到
火光;氧化钙与水反应会放出热量,生成的物质能使酚酞溶液变红;向硫酸铜溶液
中加入铁钉,可看到紫红色固体生成。
化学致力于研究物质的化学变化。通过研究化学变化,我们可以认识物质变化
的规律,并通过化学变化创造新的物质,服务于生活和社会的可持续发展。
三、组成世界的物质用途广泛
物质具有广泛的用途,物质的用途是由它们的性质决定的。如汽油具有可燃性,
可用作燃料;铜具有良好的导电性,可用作导线。
通常把物质在化学变化中表现出来的性质叫做物质的化学性质,如物质的可燃
性、腐蚀性、毒性等。物质不需要通过化学变化就能表现出来的性质叫做物质的物
理性质,如物质的颜色、气味、密度、硬度等。
交流讨论
物物质质的的用用途途与与性性质质
请按照表中示例,将你知道的物质的用途与其对应的性质填入表中,并与同学交
流讨论。
化化 学学 7
HHUUAAXXUUEE单元 1 走进化学世界
物质的用途 用途对应的物质性质 性质类型
汽油用作燃料
铝用于制作炊具
化学致力于研究物质的性质和用途,并通过化学变化创造出具有特殊性能和用
途的新物质,从而不断提高人类生活水平,推动人类社会不断进步。
拓展视野
从从造造纸纸术术到到植植物物纤纤维维制制品品
“造纸术”的发明是中国对世界文明的伟大贡献。早在西汉时期,我国劳动人
民就掌握了造纸的基本方法。东汉时期的蔡伦,进一步改进了造纸工艺,大大提高
了纸的质量,其造纸工艺流程(图 1-1-13)一直沿用至今。
古代造纸主要以树皮、麻头等物质为原料,这些原料中富含一种叫做植物纤
维的物质。植物纤维来源于农作物秸秆或其他植物的茎秆,是自然界中取之不尽、用
之不竭的可再生资源。如今,运用化学方法可将植物纤维制成一次性餐饮器具、可
降解容器、工艺品、建筑板材和工业包装材料等物品,这些物品使用后在自然环境中
可自然降解。植物纤维可制成多种新型绿色环保材料,用于替代部分塑料、玻璃、陶、
瓷等的使用。
①切麻 ②洗涤 ③浸灰水 ④蒸煮
⑧晒纸
⑤舂捣
⑦抄纸
⑥打浆 ⑨揭纸
图1-1-13 中国古代造纸工艺流程
8 化化 学学
HHUUAAXXUUEE课题 1 丰富多彩的物质世界
同学们,面对如此丰富多彩的物质世界,你一定还有许多问题,如怎样充分利
用大自然馈赠给我们的物质,怎样在利用物质的同时又避免对环境造成负面影响,
怎样根据人们的需求创造物质,等等。相信化学课程的学习,一定会激发起大家探
究物质的兴趣,帮助大家了解更多物质世界的奥秘!
练习实践
1. 下列变化中属于化学变化的是( )。
A . 冰川融化 B. 铜丝折弯 C. 纸张燃烧 D. 汽油挥发
2.下列变化中属于物理变化的是( )。
A .花生霉变 B.玉石雕刻 C.蜡烛燃烧 D.菜刀生锈
3.下列生产过程中不包含化学变化的是( )。
A. 烧制陶瓷 B. 造纸 C. 粉碎矿石 D. 粮食酿酒
4.下列物质中属于纯净物的是( )。
A.氧气 B.牛奶 C.海水 D.空气
5. 下列物质的用途与其化学性质相关的是( )。
A. 铜作导线 B. 铁制成炊具 C. 黄金压成金箔 D. 煤炭用作燃料
6. 从日常生活常见的变化中,分别举出3个属于物理变化和化学变化的例子。
7. 说出你所知道的物质的名称,尝试将它们分为纯净物和混合物两类。
8. 晶体硅是一种半导体材料。晶体硅太阳能电池具有能量转化效率高、稳定性好、
成本低等优点。常温常压下,晶体硅为银灰色固体,硬而有金属光泽,不溶于水;晶
体硅的密度为 2.33 g ·· cm-3,熔点为1 410 ℃,沸点为2 355 ℃;在450 ℃时硅能与氯
气发生反应生成四氯化硅,工业上常利用该反应对硅进行提纯。请根据上述信息总结
归纳硅的物理性质和化学性质。
化化 学学 9
HHUUAAXXUUEE单元 1 走进化学世界
课题 2 化学通过实验研究物质
情境问题
通通过过实实验验认认识识物物质质
化学上许多重大发现是科学家通过实验探究得到的。化学实验是学习化学极其重
要的方法。如通过实验,我们知道氧化钙能与水反应并放出热量,硫酸铜溶液能与铁
反应生成铜。那么,如何通过实验认识物质?
图1-2-1 通过实验认识物质及其变化
请与同学合作探究下列问题:
1.实验探究的一般过程是什么?
2.实验探究时要掌握哪些实验操作技能,遵守哪些规则?
一、实验探究的一般过程
化学发展的历史告诉我们,化学是一门以实验为基础的科学,化学上的许多
重大发现和发明创造都是通过实验得到的。化学家还通过实验检验理论和假说是否
正确。
化学史话
对对甲甲烷烷组组成成和和性性质质的的认认识识
古代劳动人民在生活实践中发现沼泽或淤泥中会产生一种气体。但直到18世纪,
科学家才通过实验确定了它的组成和基本性质。
10 化化 学学
HHUUAAXXUUEE课题 2 化学通过实验研究物质
1776 年,意大利科学家伏打用木棒搅动淤泥,并用倒转过来充满水的瓶子将这
种气体收集起来带到实验室。他点燃这种气体,发现它能够燃烧,火焰呈青蓝色。
1790 年,英国医生奥斯汀在实验室中进一步研究了这种物质,他发现这种气体的燃
烧产物是水和二氧化碳。他根据氢气燃烧生成水的事实,推测这种气体由碳元素和
氢元素组成,后来这种气体被命名为甲烷。
化学家通过实验探究物质时,都是基于一定的实验目的进行的。如为了研究甲
烷是否具有可燃性,化学家进行了甲烷燃烧的实验;为了认识甲烷的组成,化学家
进行了对甲烷燃烧产物分析的实验。通过实验认识物质时,通常需要借助一定的实
验仪器和设备,需要控制实验条件,需要在实验中观察实验现象和收集实验数据,
并依据收集到的信息进行分析和推理以得到有关物质组成、性质等方面的结论。
实验是学习化学的重要途径,我们可以像化学家一样通过实验来研究物质。
实验探究
铜铜片片加加热热产产物物的的实实验验探探究究
【提出问题】某小组同学将一小块光亮的铜片放在酒精灯火焰上加热,观察到铜
片表面有一层黑色物质。为此,他们提出了“铜片在空气中加热时表面的黑色物质是
什么”的问题。
【形成猜想】小组同学根据生活经验和小学阶段所学科学知识形成了如下猜想。
猜想 1:黑色物质是酒精灯中酒精燃烧时生成的炭黑。
猜想 2:黑色物质是铜与空气中的氧气反应的产物。
【设计方案】为验证猜想,小组同学设计了如下实验方案。
验证猜想1的方案:将铜片在不与酒精灯火焰接触的条件下加热,应观察不到铜
片表面有黑色物质生成。
验证猜想2的方案:将铜片在隔绝空气的条件下加热,应观察不到铜片表面有黑
色物质生成。
【实验探究】
实实验验1 将一小块光亮的铜片放置在试管中,在酒精灯火焰上加热试管(图1-2-2),
观察铜片表面的颜色变化,以此验证猜想1是否正确。
化化 学学 11
HHUUAAXXUUEE单元 1 走进化学世界
实实验验2 取两块相同的光亮铜片,将其中一块铜片用铝箔紧紧包裹,分别用坩埚
钳夹持两块铜片,在酒精灯火焰上加热(图1-2-3),观察比较两块铜片表面的颜色
变化,以此验证猜想2是否正确。
图1-2-2 铜片在试管中加热 图1-2-3 铜片在酒精灯火焰上加热
【形成结论】将观察到的实验现象填入下表中,并依据观察到的现象进行分析和
推理以得出结论。
实验 实验现象 实验结论
1
2
【反思评价】有的同学认为,上述实验还未能完全解答“黑色物质是什么”的
问题。要确定铜片在空气中加热生成的黑色物质的组成,需要将铜片表面的黑色物
质收集起来,再进行实验探究。
【表达交流】将上述实验探究过程中的探究思路、观察到的现象、形成的结论、
反思评价等撰写成实验报告,并与同学交流讨论。
从“铜片加热产物的实验探究”过程可以看出,化学实验探究包括提出问题、
形成猜想、设计实验方案、实施实验、获取证据、形成结论、反思评价及表达交流
等要素。
实验探究往往始于问题,提出问题后,人们会依据已有的知识和经验,对问题
解决的过程和结果提出猜想与假设,然后设计验证猜想与假设是否正确的实验方案。
在设计实验方案时,我们要对实验原理、仪器装置、试剂用量和实验操作步骤等进
行严谨的设计,并对可能观察到的现象和测量到的数据进行预测。在实验实施过程
12 化化 学学
HHUUAAXXUUEE课题 2 化学通过实验研究物质
中要规范操作,细心观察,及时、客观地记录实验现象和数据。实验结束后,我们
还要对获取到的证据进行分析和推理,得出合理的结论,并尝试应用得出的结论解
决实际问题。此外,实验探究过程中,我们还要不断对提出的猜想与假设、设计的
方案、获取的证据等进行反思评价。
化学实验探究是科学、严谨的创造性活动。在探究过程中,我们需要规范
操作、细心观察、积极思考、乐于合作、敢于质疑并勇于创新,这样才能充分发挥
实验探究在化学学习中的作用。
二、走进实验室学习化学实验操作技能和实验规则
化学实验室是进行实验的主要场所。我们需要了解实验室的基本设施,熟悉
化学实验的基本要求,并掌握实验基本操作技能。
观察思考
认认识识实实验验室室
在老师的带领下走进实验室,完成下列任务。
11..议议一一议议::仔细阅读实验室墙上的“化学实验规则”或查阅本书附录 1,与老师、
同学讨论实验安全要求和有关注意事项,思考需要遵守的准则和严格禁止的行为。
22..找找一一找找::查找实验室通风橱、电源开关、自来水总闸、灭火器、安全小药箱、
废液缸、垃圾桶等所在的位置,提出你对确保实验安全的想法。
33..认认一一认认::拿出实验台仪器柜里的仪器,查阅中学化学实验常用仪器(见附录 2),
认一认这些仪器的名称,并向老师请教常用化学实验仪器的使用方法。
图1-2-4 化学实验室 图1-2-5 常用化学实验仪器
化化 学学 13
HHUUAAXXUUEE单元 1 走进化学世界
进入实验室做化学实验,首先要确保安全。实验室
里所用的化学试剂有些有腐蚀性,有些有毒,因此,实验
前要仔细阅读试剂的使用规则。不能用手直接接触任何试
剂,更不能品尝试剂。有些试剂易燃、易爆,必须按照
要求存放和使用,以免发生危险。实验中要佩戴护目镜。
加热操作过程中,不要凑近被加热仪器,不要将试管口朝
向自己或他人。加热后,仪器不要直接放于桌面,可放在 图1-2-6 常见危险化学品标志
陶土网上。使用玻璃仪器时要避免划破皮肤。
为保证实验正常进行并顺利完成,我们必须遵守一定的规则:
1. 实验前,要进行充分的预习,明确实验目的,熟悉实验步骤,知晓实验安全
的有关事项。
2. 实验中,要节约试剂,严格按照实验规定的用量取用试剂。如果没有说明试
剂用量,一般应该按最少量取用,液体取 1 ~ 2 mL,固体只需铺满试管底部即可。
从试剂瓶中取出的使用后剩余的试剂,不要放回原瓶,也不要随意丢弃,更不能拿
出实验室,要放在指定的回收位置。实验中要规范地进行操作,边观察、边记录并
进行思考,尝试用自己学习到的化学知识对实验现象加以解释。
3. 实验结束时,要将废液倒入废液缸中统一处理,清洗好实验仪器,并将仪器
和试剂存放到指定位置。
4. 实验后,要按要求将本次实验的实验目的、实验步骤、实验现象、实验结论
及反思评价等撰写成实验报告。
为保证实验顺利进行,我们还必须掌握一定的化学实验基本操作技能。
实验探究
在在““硫硫酸酸铜铜与与氢氢氧氧化化钠钠反反应应””实实验验中中学学习习实实验验操操作作技技能能
完成下列实验内容,观察实验现象,学习实验基本操作技能,总结实验操作要点。
实实验验1 硫酸铜晶体的取用
用药匙取绿豆粒大的硫酸铜晶体放入纸槽(用小纸条折叠而成)中,小心送至横
放的试管底部,然后将试管缓慢竖立。如果试管口径较大,也可用药匙直接将少量硫
酸铜晶体送至横放的试管底部,然后缓慢竖直试管(图1-2-7)。
14 化化 学学
HHUUAAXXUUEE课题 2 化学通过实验研究物质
图1-2-7 固体试剂的取用
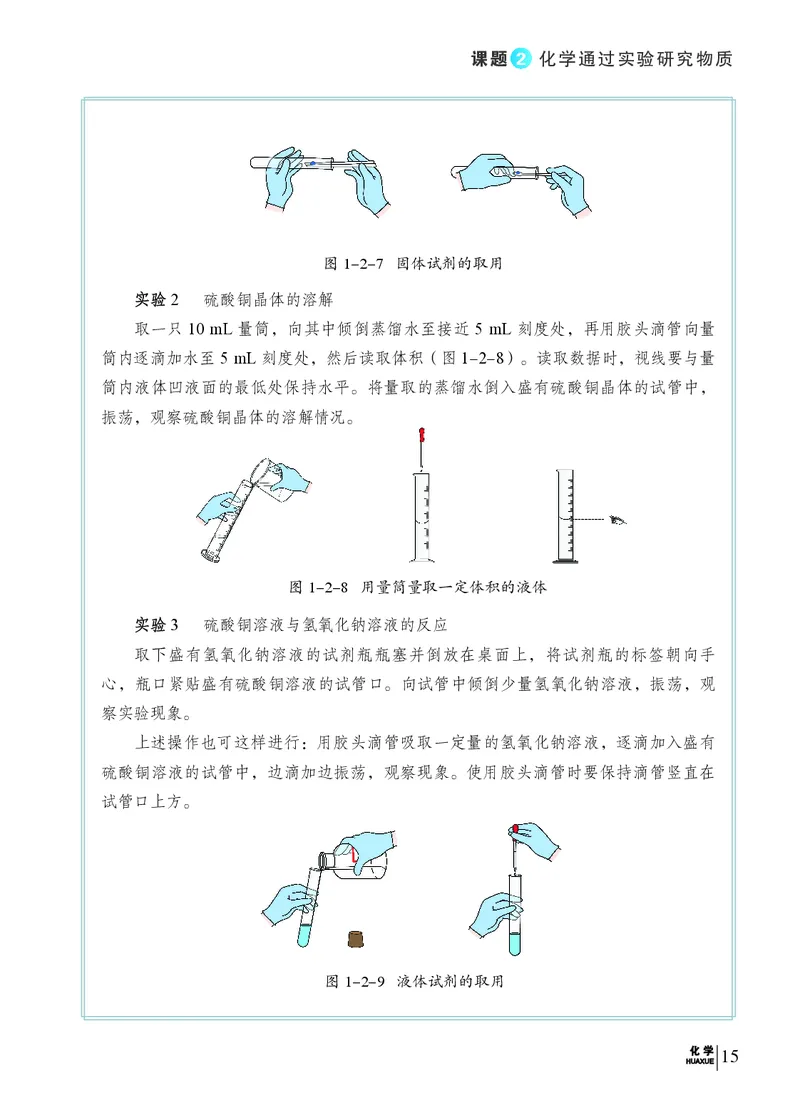
实实验验2 硫酸铜晶体的溶解
取一只10 mL 量筒,向其中倾倒蒸馏水至接近 5 mL 刻度处,再用胶头滴管向量
筒内逐滴加水至 5 mL 刻度处,然后读取体积(图1-2-8)。读取数据时,视线要与量
筒内液体凹液面的最低处保持水平。将量取的蒸馏水倒入盛有硫酸铜晶体的试管中,
振荡,观察硫酸铜晶体的溶解情况。
图1-2-8 用量筒量取一定体积的液体
实实验验3 硫酸铜溶液与氢氧化钠溶液的反应
取下盛有氢氧化钠溶液的试剂瓶瓶塞并倒放在桌面上,将试剂瓶的标签朝向手
心,瓶口紧贴盛有硫酸铜溶液的试管口。向试管中倾倒少量氢氧化钠溶液,振荡,观
察实验现象。
上述操作也可这样进行:用胶头滴管吸取一定量的氢氧化钠溶液,逐滴加入盛有
硫酸铜溶液的试管中,边滴加边振荡,观察现象。使用胶头滴管时要保持滴管竖直在
试管口上方。
图1-2-9 液体试剂的取用
化化 学学 15
HHUUAAXXUUEE单元 1 走进化学世界
实实验验4 加热硫酸铜溶液与氢氧化钠溶液反应的产物
加热前将试管上部的部分液体倾倒入废液缸中,被加热的液体体积不超过试
管容积的 1/3,然后用抹布将试管外壁的水珠擦干,用试管夹由下往上夹住试管
(夹在距试管口约 1/3 处),在酒精灯外焰上加热。为使液体均匀受热,加热开
始时要先将试管底部在火焰上来回缓慢移动,然后再集中加热。加热结束后,将
试管放在试管架上冷却,用灯帽盖灭酒精灯。如果中途需要在酒精灯中添加酒精,
一定要熄灭酒精灯后再进行,添加后的量不宜过多,酒精灯内酒精的量不要超过
酒精灯容量的 2/3(图 1-2-11)。
外焰
内焰
焰心
灯芯
酒精
图1-2-10 酒精灯的结构 图1-2-11 液体的加热与酒精灯的使用
实验完毕后,将试管中的废液倒入指定位置,然后通过多次注水、振荡的步骤进
行洗涤。如果试管内壁附有不易洗掉的物质,可使用试管刷在试管中转动或上下移动,
但要注意,不能用力过猛,以防损坏试管(图1-2-12)。洗净的仪器要放在指定位置。
打扫实验室后离开实验室,并撰写实验报告。
图1-2-12 试管的洗涤
实验过程中同学们还要注意养成良好的实验习惯、实事求是的态度和认真严谨
的作风,做到仔细观察,不轻易放过任何实验现象,不轻信现有结论,不迷信权威
观点,养成独立思考的习惯等。只有这样,我们才能逐步掌握化学实验的方法,才
能使实验成为我们学习化学和提高科学素养的重要手段。
16 化化 学学
HHUUAAXXUUEE课题 2 化学通过实验研究物质
练习实践
1.下列是探究铜绿(一种绿色粉末状固体)性质的有关实验操作,其中正确的
是( )。
A.取用铜绿 B.点燃酒精灯 C.加热铜绿 D.取用盐酸
2.下列实验操作正确的是( )。
A. 用嘴吹灭酒精灯火焰
B. 在实验室中用尝味道的方法鉴别食盐和蔗糖
C. 读取量筒中液体体积时,视线要与液体凹液面的最低处保持水平
D. 将未用完的剩余试剂倒入水池中
3. 某同学探究酒精燃烧的产物,观察到如下现象:
(1)把1个冷而干燥的烧杯罩在酒精灯火焰上方,观察到烧杯内壁出现水雾。
(2)用手靠近酒精灯火焰或触摸罩在酒精灯火焰上方的烧杯外壁,感觉到烫。
请写出你根据实验现象得出的结论。
4. 某同学用“闻气味”的方法区分酒精和白醋。你还能想到其他区分酒精和白醋
的方法吗?请给出你设计的简要探究方案。
5.丁烷是一种可以燃烧的气体,人们常将其压缩为液态作为打火机内的燃料使
用。若按下打火机的按钮而未使打火石产生火花,部分液态的丁烷气化,你会听到
嘶嘶的声音;若按下打火机的按钮并使打火石产生火花点燃丁烷,丁烷会在空气中
燃烧。请描述上述文字中涉及的变化,对其进行分类,并说明理由。
化化 学学 17
HHUUAAXXUUEE单元 1 走进化学世界
课题 3 化学服务于人类社会发展
情境问题
化化学学与与我我们们的的生生活活和和社社会会息息息息相相关关
环顾我们生活的世界,你会发现,无论是我们的衣食住行,还是环境保护、能源
利用、材料研制等,都离不开化学。
请与同学交流和讨论,谈一谈:
1.化学对提升人类生活质量作出了怎样的贡献?
2.化学如何促进人类社会的可持续发展?
一、化学提升了人类的生活质量
化学对人类生活的最大贡献,在于它为人类创造出了数量庞大、功能多样的物
质,满足了人类现代化生活的需要。
化学已经渗透到我们生活的各个方面。化学为我们的日常生活提供了多种多
样、性能优越的日用品,如用有机合成材料制造牙刷、脸盆等,用化学合成试剂
生产护肤品、洗涤剂和消毒用品等。化学为房屋建筑提供了种类繁多的材料,如
钢铁、水泥、玻璃、涂料、各种合金等。化学为我们使用的各种学习和运动用品,
如纸张、铅笔、墨水、运动服、球鞋、运动器材和塑胶跑道等提供了优质的材料
和制作的手段。
交流讨论
寻寻找找化化学学的的““足足迹迹””
请按照你一天的学习、生活顺序,列出你接触或使用到的物质。通过交流讨论
和查阅资料的方式,了解哪些物质是自然界中本来就有的,哪些是用化学方法人工
合成的,并讨论这些化学合成物质对人类生活产生的影响。
18 化化 学学
HHUUAAXXUUEE课题 3 化学服务于人类社会发展
洗漱 早餐 上学
学习 运动 劳动
图1-3-1 一天的生活
化学能将自然界的物质转化为应用价值更高的物质并为人类所用,如将木材转
变为纸张,将金属矿石转变为合金等。化学还能创造新物质,如以石油为原料,可
以制得合成塑料、合成纤维、合成橡胶、合成药物等(图 1-3-2)。化学犹如一
双神奇的手,为我们创造了一个神奇的物质世界。
化学还是解密人类
生命过程和保障生命健
康的重要手段。科学家
正通力合作,逐步揭示
建筑用塑料
生命的奥秘,指导人类
合成药物
合理膳食,研制更有效 汽油
的、副作用更小的药
品,以改善人类的生活
质量。
石油化工
合成纤维
合成洗涤剂
图1-3-2 以石油为原料获得的物质
化化 学学 19
HHUUAAXXUUEE单元 1 走进化学世界
化学史话
中中国国合合成成结结晶晶牛牛胰胰岛岛素素
由中国科学院上海生物化学研究所、中国科学院上海有机化学研究所以及北京大
学精干技术力量组成的研究团队,历经7年,于 1965 年人工合成了与天然牛胰岛素分
子结构相同并具有完整生物活性的蛋白质。这是世界上第一次人工合成具有完整生物
活性的蛋白质,标志着人类在揭示生命本质的征途上实现了里程碑式的飞跃。
化学使我们的日常交通更为便捷和环保。用石油化工
产品——沥青铺设的高速公路使我们的出行更加方便;电
动汽车耗能成本低廉且环保;我们可以乘坐飞机环游世
界,在不远的将来我们甚至可以乘坐宇宙飞船遨游太空。
无论是汽车、火车、飞机还是飞船的制造和运行,都离不
开化学家参与研究的各种新型材料和绿色能源。
由此可见,在我们的生活中,化学无处不在,化学使
我们的生活更美好。
图1-3-3 化学为人类出行提供方便
二、化学促进了社会的可持续发展
资源是人类社会发展的保障。化学在人类利用自然资源的过程中,发挥着极其
重要的作用。经过化学家的研究,一种天然物质往往被开发出多种多样的用途,极
大地丰富了我们的生活,促进了社会经济和文明的发展。但地球上的资源是有限的,
为此,化学家正在积极探索能够充分利用资源且不破坏生态环境的途径。
拓展视野
从从沙沙子子到到多多种种材材料料
通过化学反应,我们可将许多随处可见的物质转化为人类生产和生活中重要且具
有广泛应用的物质,以满足人类生产和生活的需求。
例如,一种看起来很不起眼的沙子,通过化学反应可制备成半导体材料、光导
纤维材料、硅橡胶等,还可以用于生产玻璃、水泥和水玻璃等建筑材料(图1-3-4)。
20 化化 学学
HHUUAAXXUUEE课题 3 化学服务于人类社会发展
半导体材料
光导纤维材料 玻璃
沙子
(二氧化硅)
硅橡胶 水玻璃
图1-3-4 从沙子到多种材料
材料是人类生存不可或缺的物质基础,是人类社会发展的基石。材料也是
历史学家划分时代的重要依据之一,如石器时代、青铜器时代等。而化学变化
是人类制备、合成材料的重要手段。目前,科学家致力于利用化学变化研制和
加工各式各样性能更加优良的新材料(图 1-3-5),如超导材料、耐超高温材料、
超硬材料、光学材料、磁性材料和生物材料等,以满足工农业生产的需求以及
网络通信、航空航天等高科技领域的需求。
磁悬浮列车中使用了超导材料 信息时代离不开硅晶片
我国“蛟龙号”载人潜水器采用 我国天宫空间站的建造采用了
了多种耐压、耐腐蚀的材料 耐超高温的材料
图1-3-5 化学为研制新材料作出贡献
化化 学学 21
HHUUAAXXUUEE单元 1 走进化学世界
人类面临着能源短缺的问题,化学家正在探索走出这一困境的方法和途径:
一方面,研究高效利用生物质能以及石油、煤炭、天然气等燃料的方法;另一
方面,开发新型的绿色能源,以帮助人类解决能源危机。
随着人类生产方式的改变、生活活动范围和需求的不断增大,气候变化、空
气污染、水体污染、土壤污染等环境问题使人类的生存环境受到了严峻的挑战。
为此,化学家正积极探求保护生态环境、治理污染的方法和途径(图 1-3-6)。
如研究实现碳中和的措施,帮助人类控制温室效应;研发“绿色新工艺”,实现
生产零排放、零污染;监控水质,对污水进行处理并循环使用;研制可降解塑料
和替代氯氟烃的新型制冷剂。
运用化学方法检测水质 通过化学反应处理污水
图1-3-6 化学参与环境治理
化学为人类的安居乐业、丰衣足食和健康长寿作出了重要的贡献,而且将进一
步为人类作出更大的贡献。让我们一起徜徉于化学世界,努力学好化学,为祖国
昌盛、民族富强、人类进步作出自己的贡献吧!
22 化化 学学
HHUUAAXXUUEE课题 3 化学服务于人类社会发展
练习实践
1.下面列出的是我国“国家最高科学技术奖”几位获奖者及他们的研究领域,其
中研究领域涉及优良导电材料开发的是( )。
A.闵恩泽,石油化工催化剂研究 B. 师昌绪,材料腐蚀与防护研究
C. 赵忠贤,高温超导材料研究 D. 张存浩,高能化学激光研究
2.请通过查阅资料或询问家长、老师等方式,了解下列物品使用了哪些化学合成
材料。
(1)尼龙绳。
(2)一次性注射器。
(3)气球。
(4)自行车轮胎。
3. 汽车尾气是城市空气污染源之一。科学家发明的汽车尾气净化器,能将一氧化
碳、一氧化氮等有毒废气转化为无害气体。汽车尾气净化器中发生的变化属于哪种变
化类型?请列举出一些其他利用该变化改善环境的事例。
4.大多数的人类活动,如驾驶汽车、使用食品包装袋等,都会消耗自然资源并产
生废弃物。根据消耗、再生和更新的时间关系,资源可以分为可再生资源和不可再生
资源。
(1)查阅资料,了解哪些是可再生资源,哪些是不可再生资源。
(2)有一种观点认为,技术进步在自然资源开发利用中具有重要作用,人类应当
通过发明新的技术、采用新的方法,最低限度地使用资源,最大限度地利用资源。
对此,你的看法如何?请通过具体的例子阐述你的观点。
5.阿司匹林是一种常用的解热镇痛药。请你通过查阅资料的方式,了解化学家研
制这种药物的过程,感受化学家不断进取、勇于创新的精神,并将你的感受写成 300
字的读后感。
化化 学学 23
HHUUAAXXUUEE单元小结
单元小结
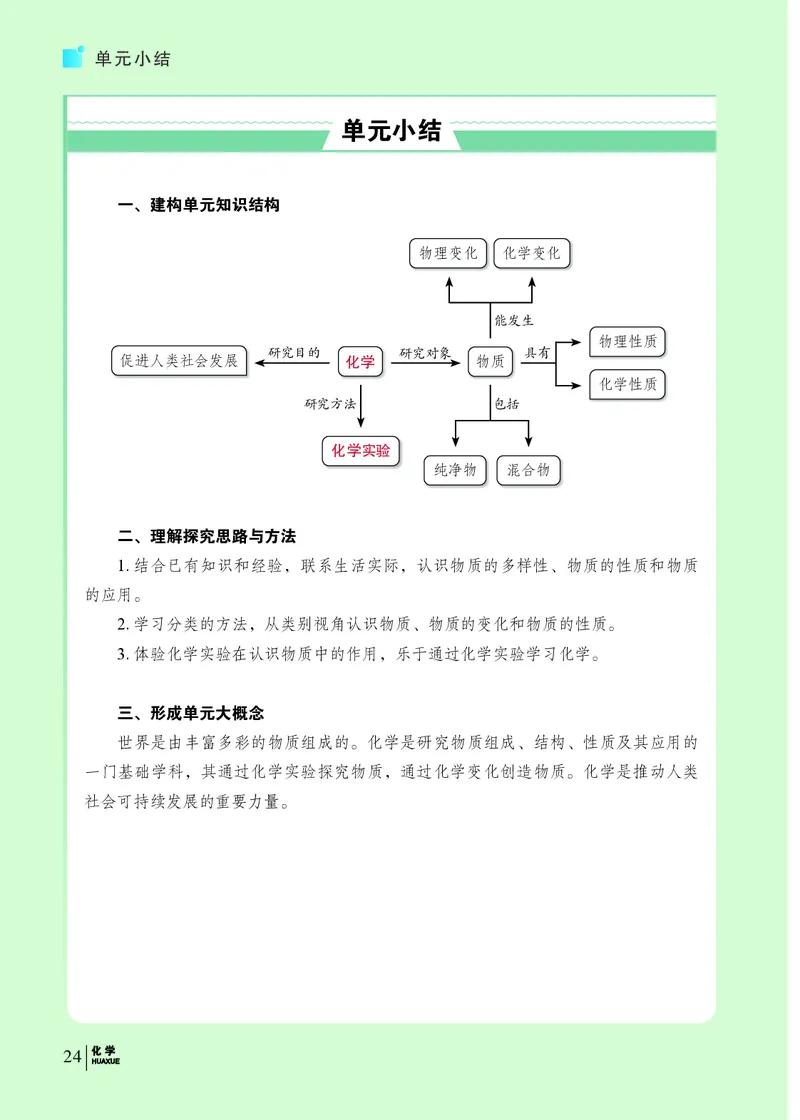
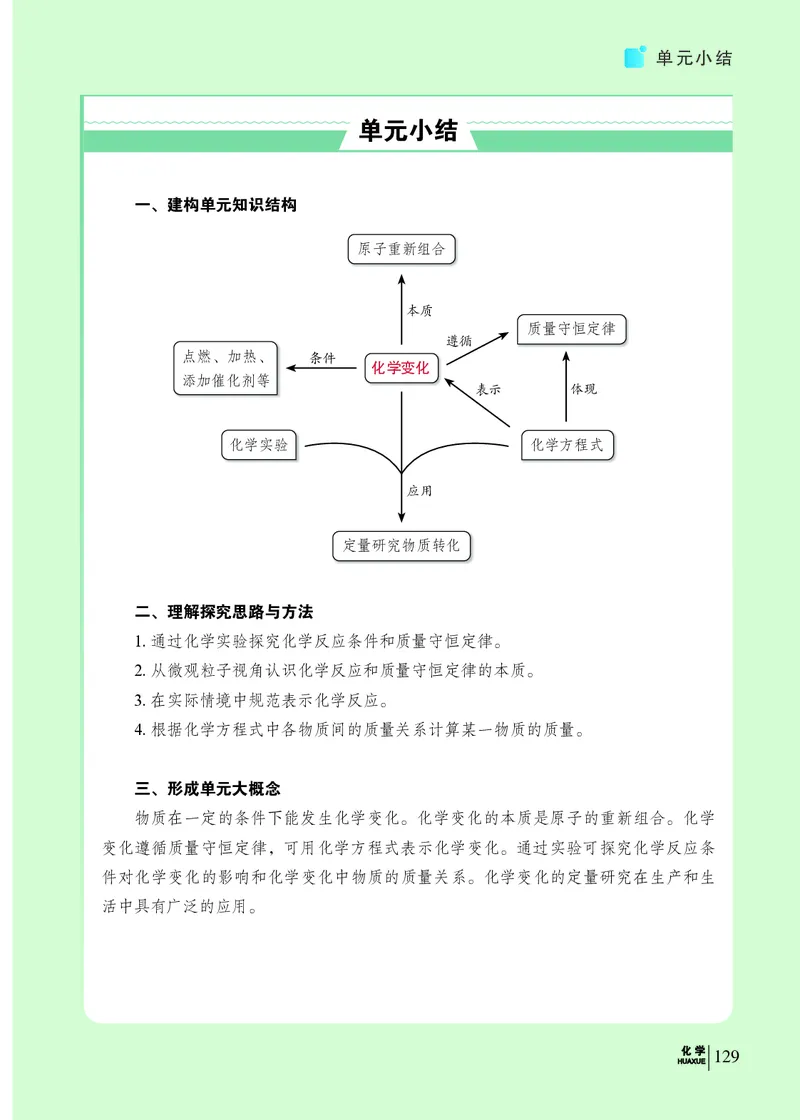
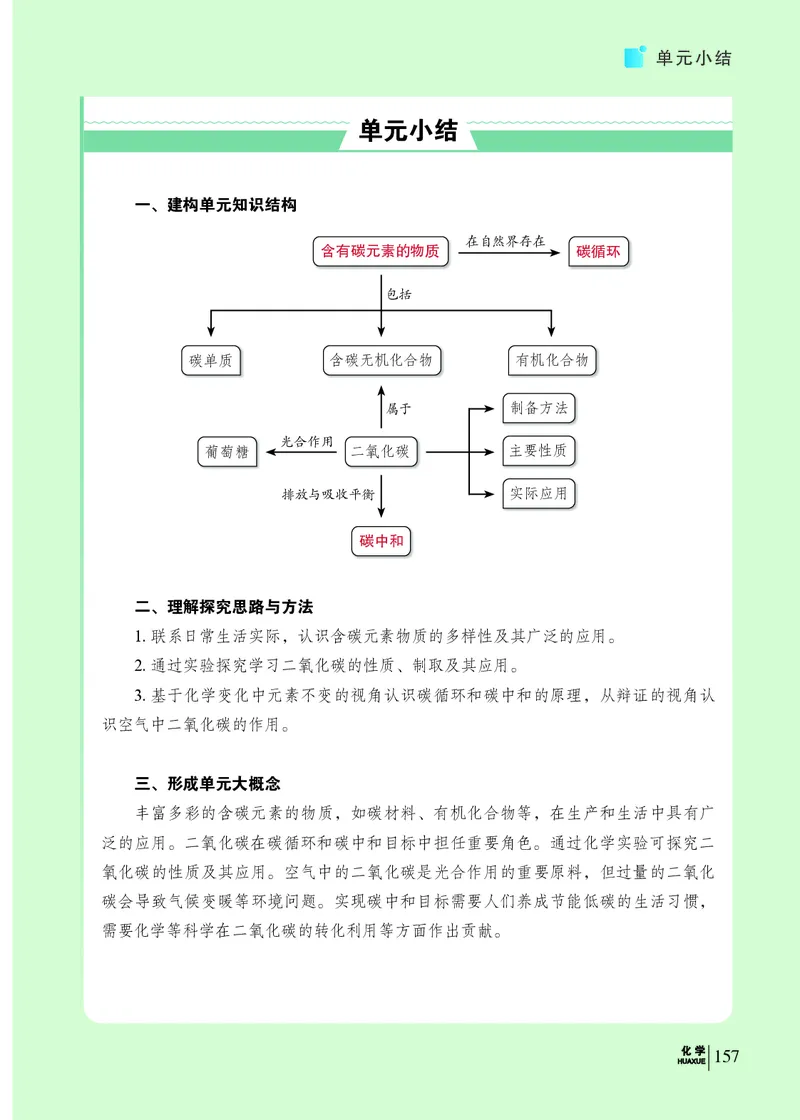
一、建构单元知识结构
物理变化 化学变化
能发生
物理性质
研究目的 研究对象 具有
促进人类社会发展 化学 物质
化学性质
研究方法 包括
化学实验
纯净物 混合物
二、理解探究思路与方法
1.结合已有知识和经验,联系生活实际,认识物质的多样性、物质的性质和物质
的应用。
2.学习分类的方法,从类别视角认识物质、物质的变化和物质的性质。
3.体验化学实验在认识物质中的作用,乐于通过化学实验学习化学。
三、形成单元大概念
世界是由丰富多彩的物质组成的。化学是研究物质组成、结构、性质及其应用的
一门基础学科,其通过化学实验探究物质,通过化学变化创造物质。化学是推动人类
社会可持续发展的重要力量。
24 化化 学学
HHUUAAXXUUEE单元作业
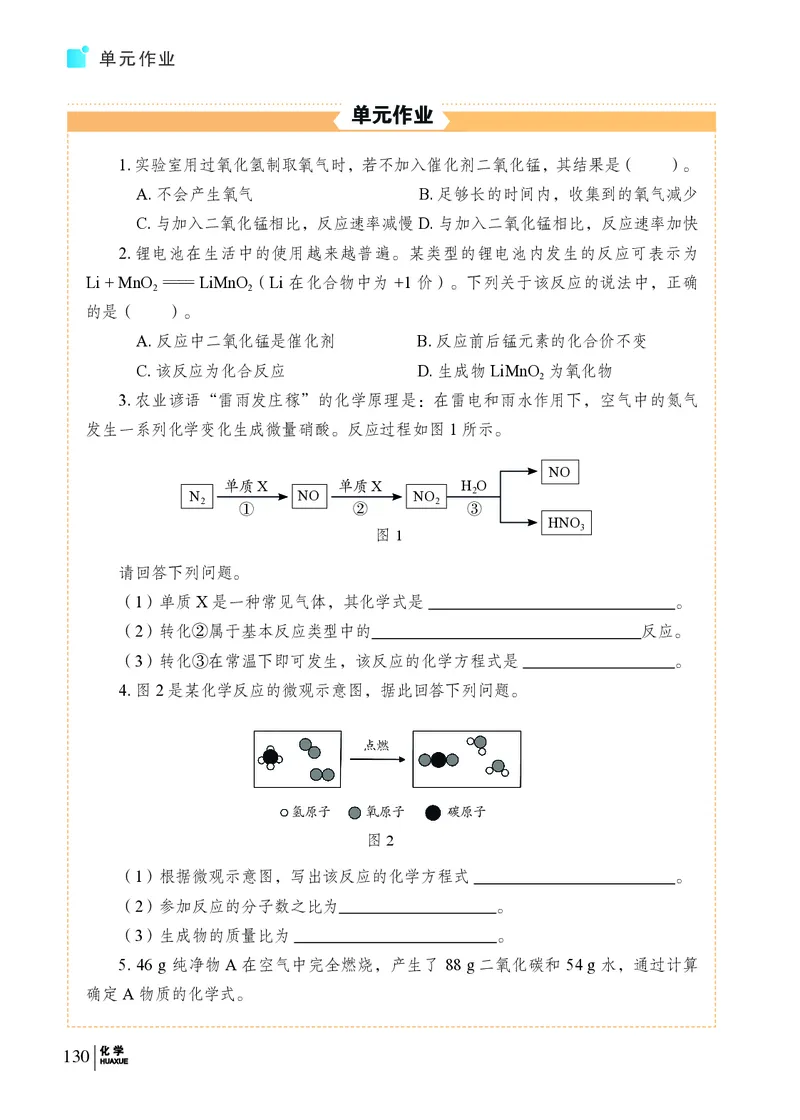
单元作业
1.下列物质属于纯净物的是( )。
A.铁粉 B.矿泉水 C.不锈钢 D.食醋
2.下列物质的用途主要与其化学性质有关的是( )。
A.用金刚石切割玻璃 B.用水清洗污泥
C.用铝合金制作炊具 D.用酒精作燃料
3.从下图中选择相关的仪器,将其编号填写在相应的空格处。
a b c d e f g h
(1)取用少量粉末状固体试剂应使用 。(2)滴加液体应使用的是 。
(3)存放液体试剂通常使用 。(4)木炭燃烧时夹持木炭需使用 。
(5)量取液体试剂应使用 。
4.下面列出了同学们在实验中的一些操作。判断下列操作是否规范。在规范的操
作后打“√”,在不规范的操作后打“×”,并对错误的操作进行纠正。
(1)给试管中的铜片加热时,试管口略朝上。 ( )
(2)酒精灯使用完毕后,未盖上灯帽。 ( )
(3)倾倒盐酸时试剂瓶上的标签未向着手心。 ( )
(4)点燃镁带时未在实验桌上放置陶土网。 ( )
5. 哪些现象可以帮助我们判断铁发生了锈蚀?
6.设计尽可能多的方案,以区分铁与铜、水与酒精两组物质。
7.加热铜绿(铜锈的主要成分)会生成黑色的氧化铜固体,并释放出二氧化碳和
水蒸气。请设计检验铜绿加热释放出的二氧化碳和水蒸气的方案。方案包括如下内容:
(1)探究目的或探究需要解决的问题。
(2)基于探究问题提出的假设。
(3)验证假设的实验方案,包括使用的仪器、试剂和实验步骤等。
(4)预测实验中可能观察到的现象。
(5)实验记录表和实验结果分析方法。
化化 学学 25
HHUUAAXXUUEE项目学习
项目学习
我我是是化化学学实实验验室室安安全全巡巡查查员员
项目背景
通过扮演化学实验室安全巡查员角色,进一步了解实验操作规则和安全要求,学
会分析、防范安全隐患问题,增强实验安全意识,掌握规范的操作技能。
项目建议方案
1. 讨论巡查计划。查阅关于实验室安全的法律法规资料,与老师和同学交流讨论
实验室安全规范要求和防范实验安全隐患的措施,确定安全巡查主要内容,设计安全
巡查记录表。
2. 总体巡查实验室。在老师的带领下走进实验室,详细察看实验室整体结构,查
找通风橱、电源开关、自来水总闸、灭火器、安全小药箱、废液缸、垃圾桶等的位置,
绘制实验室平面图。
3. 分项安全巡查。结合“化学实验规则”的内容,巡查小组同学分工合作,分别
巡查实验室消防设施、三废处理系统和实验安全保障措施等内容,做好巡查记录。
4. 巡查总结与反馈。小组内经过讨论后形成巡查报告,并在全班进行交流。
26 化化 学学
HHUUAAXXUUEE单元 2 探析空气之谜
课题 1 空气组成的探究
情境问题
生生命命离离不不开开空空气气
人类的生活离不开空气,生命体的呼吸、植物的光
合作用、化肥的生产等都需要空气。
你是否知道:
1.人类对空气的认识经历了哪些过程?
2.空气中有哪些成分?
图2-1-1 空气是宝贵的资源
3.如何测定空气中氧气的体积分数?
一、人类对空气的认识
人类对空气成分的探索经历了漫长而又复杂的过程。很久以前人们只知道燃烧
和呼吸都需要空气,并认为空气是单一成分的物质。到了 18 世纪,科学家通过对
燃烧现象和呼吸作用等的深入研究,才开始认识到空气是由多种成分组成的。
阅读理解
氧氧气气的的发发现现
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分
别通过实验制得了氧气。但受当时错误的“燃素学说”的影响,他
们仍然认为空气是单一成分的物质,氧气是“脱燃素的空气”,因
而没能真正认识空气的成分。
1774年,法国化学家拉瓦锡用金属燃烧实验证明,燃烧是物质
与空气中氧气作用的结果,并发现了金属燃烧后余下的“空气”不
图2-1-2 拉瓦锡
支持燃烧和呼吸,第一次明确提出空气是由氧气和氮气组成的。
拉瓦锡定量测定空气成分(图2-1-3)的实验过程主要为:
28 化化 学学
HHUUAAXXUUEE课题 1 空气组成的探究
曲颈甑
(1)将少量汞放在密闭容器中加热12
玻璃钟罩
天,发现部分汞变成红色粉末(氧化汞,
HgO),同时,空气体积减小了1/5左右。 氧化汞 汞槽
(2)对容器中剩余气体进行研究,发
现这部分气体不能供给呼吸,也不助燃(拉
瓦锡将这种气体称为氮气)。
图2-1-3 拉瓦锡研究空气组成的实验装置
(3)将生成的红色粉末收集起来,放
在另一个较小的容器中再加强热,得到汞(Hg)和氧气(O )。
2
(4)将氧化汞分解得到的氧气导入汞与空气加热反应后的剩余气体中,所得气体
和空气性质完全相同。
根据拉瓦锡定量测定空气成分的实验,你能得到哪些结论?
人类认识空气成分的过程是一个不断探索的过 其他组分1%
氧气21%
程。更精密的科学实验表明,空气是一种混合物,干
燥的空气中各组分的体积占空气总体积的体积分数大约
是:氮气 78%、氧气 21%、稀有气体 0.94%、二氧化碳
氮气78%
0.03%、其他气体和杂质0.03%。
图2-1-4 干燥空气的组分
化学史话
氩氩气气的的发发现现
1892年,英国物理学家瑞利研究气体密度时发现,
在 0 ℃、1.01×105 Pa 的条件下,从含氮的化合物中制
得的氮气的密度 (1.250 8 g ·· L-1) 比从空气中分离得到
的氮气的密度 (1.257 2 g ·· L-1) 总是低了 0.006 4 g ·· L-1。
这一差异似乎是微不足道的,然而瑞利并没有忽视这一微
小的差异,他不认为这是实验本身的“误差”,而是与英
图2-1-5 瑞利
国化学家拉姆塞合作,通过更加精密的实验进一步研究。
经过两年多的努力,他们终于发现在空气中还存在着一种“惰性”气体——氩气。氩
气是第一种被发现的稀有气体。
化化 学学 29
HHUUAAXXUUEE单元 2 探析空气之谜
二、空气中氧气体积分数的测定
空气是含有氮气、氧气等多种气体的混合物,人们可通过实验方法测定空气中
氧气的体积分数。
实验探究
测测定定空空气气中中氧氧气气的的体体积积分分数数
【实验目的】测定空气中氧气的体积分数。
【实验原理】在充满空气的密闭容器中,足量的红磷固体与空气中的氧气反应生
成五氧化二磷(P O )固体,而在该条件下氮气不与红磷反应。通过测量反应前后容
2 5
器中水的体积变化,可以确定空气中氧气的体积分数。
【实验探究】
步骤1 在图2-1-6所示的充满空气的集气瓶内加入少 燃烧匙
弹簧夹
量水,将集气瓶内水面以上容积划分为5等份,并做好标记。
连接好装置,检验装置的气密性。 红磷
步骤2 用弹簧夹夹紧乳胶管,在燃烧匙内装满红磷,
并放在酒精灯火焰上点燃,当红磷燃烧后迅速伸入集气瓶
水
内,塞紧橡胶塞,观察红磷燃烧的现象。
图2-1-6 空气中氧气含
步骤3 红磷燃烧结束,待集气瓶冷却至室温,打开
量的测定
弹簧夹,观察集气瓶中水位的变化情况。
【实验报告】
1.完成下列实验观察记录,并得出结论。
观察内容 实验现象 实验结论
红磷燃烧
集气瓶中水位变化
2.思考下列问题,与同学交流讨论你的想法。
(1)如果集气瓶中水位上升不足集气瓶内水面以上容积的 1/5,导致该现象的
原因可能是什么?
(2)还可以通过哪些实验粗略地测定空气中氧气的含量?
30 化化 学学
HHUUAAXXUUEE课题 1 空气组成的探究
在上述实验中,红磷(P)燃烧消耗了集气瓶内空气中的氧气(O ),生成了
2
白色的五氧化二磷(P O )固体,该反应的文字表达式为:
2 5
点燃
红磷 + 氧气 五氧化二磷
(P) (O ) (P O )
2 2 5
集气瓶内气体减少、气压下降,烧杯中的水被吸入集气瓶中,吸入的水的体积
等于瓶内空气中被消耗的氧气的体积。吸入的水的体积约为集气瓶内原来空气总体
积的 1/5,说明空气中氧气的体积约占空气总体积的 1/5。
练习实践
1. 下列说法中正确的是( )。
A. 洁净的空气是纯净物,被污染的空气是混合物
B. 干燥空气中氧气的质量分数约为 21%
C. 常温常压下,氮气、氧气和二氧化碳都是无色无味的气体
D. 空气中仅含有氮气、氧气和二氧化碳
2. 下列关于红磷燃烧法测定空气中氧气含量的实验分析中,错误的是( )。
A. 为了减少实验误差,应待大量白烟沉降和温度冷却到室温后再打开弹簧夹
B. 水倒流进燃烧装置中是装置内外的压强差导致的
C. 该实验说明空气中的氮气不与红磷发生反应
D. 实验中红磷的量不会影响测定结果
3.汽车受到剧烈碰撞后,车内安全气囊会瞬间释放一种气体,该气体是空气中含
量最多的一种成分,这种气体为( )。
A. 氧气 B. 氮气 C. 二氧化碳 D. 水蒸气
4. 根据下列事实说明空气中含有哪些物质。
(1)绿色植物能在太阳光作用下发生光合作用。
(2)燃着的蜡烛在充满空气的密闭玻璃瓶中燃烧一段时间后会熄灭。
(3)夏天,盛放冰水的玻璃杯外壁上常常附有一些小水珠。
化化 学学 31
HHUUAAXXUUEE单元 2 探析空气之谜
课题 2 氧气的性质与应用
情境问题
应应用用广广泛泛的的氧氧气气
地球上几乎所有生物的生存都离不开氧气,人类的生产和生活也需要氧气。
图2-2-1 广泛应用的氧气
请根据生产和生活中的应用实例,并结合实验探究等活动,与同学合作探究下列
问题:
1. 如何用实验方法探究氧气的性质?
2. 氧气在生产和生活中具有哪些应用?
3. 如何获得较纯的氧气?
一、性质活泼的氧气
氧气在人类的生产和生活中具有广泛的应用,氧气的广泛应用是由氧气的性质
决定的。氧气能和许多物质发生反应。
观察思考
认认识识氧氧气气的的性性质质
观察实验1与实验2中的实验现象,根据实验现象分析和总结氧气的性质,并与
同学交流讨论观察的结果和分析推理所得到的结论。
32 化化 学学
HHUUAAXXUUEE课题 2 氧气的性质与应用
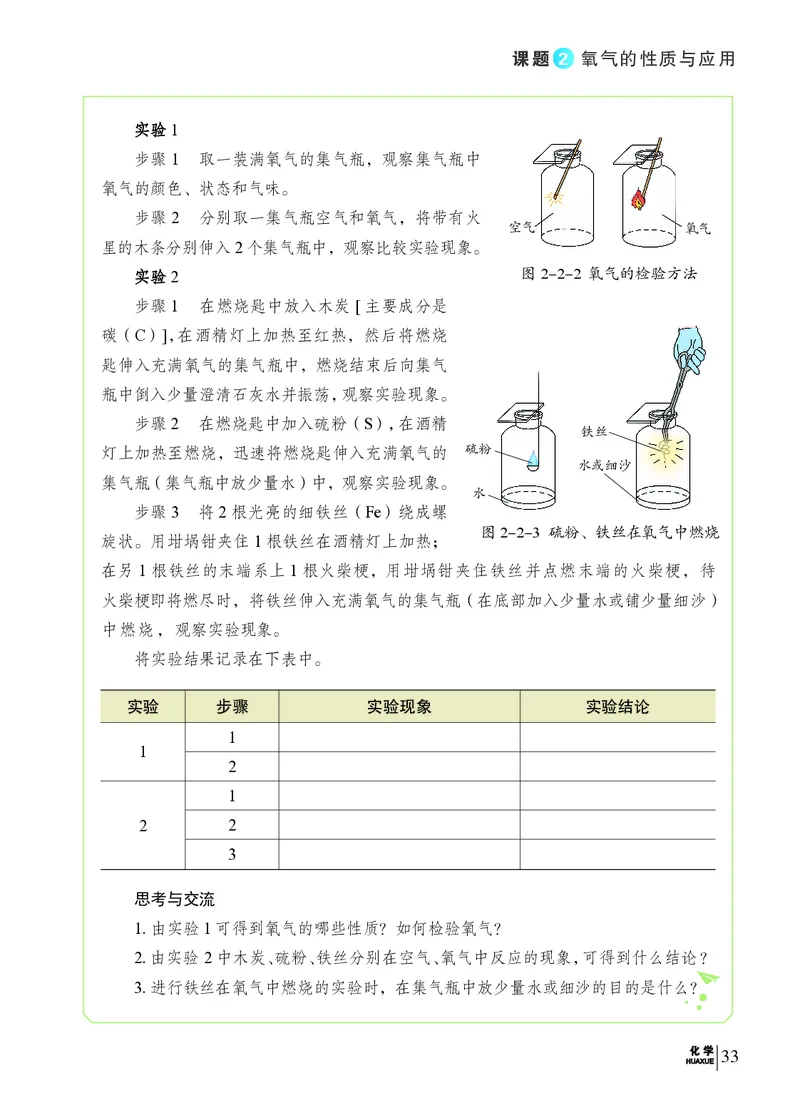
实实验验1
步骤1 取一装满氧气的集气瓶,观察集气瓶中
氧气的颜色、状态和气味。
步骤2 分别取一集气瓶空气和氧气,将带有火
空气 氧气
星的木条分别伸入2个集气瓶中,观察比较实验现象。
实实验验2 图2-2-2 氧气的检验方法
步骤1 在燃烧匙中放入木炭 [ 主要成分是
碳(C)],在酒精灯上加热至红热,然后将燃烧
匙伸入充满氧气的集气瓶中,燃烧结束后向集气
瓶中倒入少量澄清石灰水并振荡,观察实验现象。
步骤2 在燃烧匙中加入硫粉(S),在酒精
铁丝
灯上加热至燃烧,迅速将燃烧匙伸入充满氧气的 硫粉
水或细沙
集气瓶(集气瓶中放少量水)中,观察实验现象。
水
步骤3 将2根光亮的细铁丝(Fe)绕成螺
图2-2-3 硫粉、铁丝在氧气中燃烧
旋状。用坩埚钳夹住1根铁丝在酒精灯上加热;
在另1根铁丝的末端系上1根火柴梗,用坩埚钳夹住铁丝并点燃末端的火柴梗,待
火柴梗即将燃尽时,将铁丝伸入充满氧气的集气瓶(在底部加入少量水或铺少量细沙)
中燃烧,观察实验现象。
将实验结果记录在下表中。
实验 步骤 实验现象 实验结论
1
1
2
1
2 2
3
思考与交流
1.由实验1可得到氧气的哪些性质?如何检验氧气?
2.由实验 2 中木炭、硫粉、铁丝分别在空气、氧气中反应的现象,可得到什么结论?
3.进行铁丝在氧气中燃烧的实验时,在集气瓶中放少量水或细沙的目的是什么?
化化 学学 33
HHUUAAXXUUEE单元 2 探析空气之谜
方法引导
闻气味的操作方法
打开盛放试剂的试剂瓶瓶盖,或部分移开集气瓶上的毛玻璃
片,将集气瓶或试剂瓶的瓶口放在鼻子前下方约20 cm 处,用手
轻轻地在瓶口扇动,使极少量的气体进入鼻孔。注意:不能将鼻
子凑到集气瓶或试剂瓶的瓶口去闻气体的气味。
图2-2-4 闻气味的操作方法
通常状况下,氧气是无色无味的气体,标准状况下(0 ℃、1.01×105 Pa),氧气的
密度是 1.429 g ·· L-1,比空气的密度略大(标准状况下空气的密度是1.293 g ·· L-1)。
氧气不易溶于水,标准状况下 1 L 水中大约能溶解 30 mL 氧气;温度升高或气压降
低,氧气在水中溶解的量下降。在压强为 1.01×105 Pa、温度为-183 ℃时,氧气转
化为淡蓝色的液体;压强不变,温度为-218 ℃ 时,氧气转化为淡蓝色的雪花状
固体。
物质在空气中燃烧,实际上是物质与空气中的氧气发生反应。如碳与氧气反应
生成二氧化碳(CO ),二氧化碳能使澄清石灰水变浑浊。
2
点燃
碳 + 氧气 二氧化碳
(C)(O ) (CO )
2 2
二氧化碳 + 氢氧化钙 碳酸钙 + 水
(CO ) [Ca(OH) ] (CaCO )(H O)
2 2 3 2
硫与氧气反应生成具有刺激性气味的二氧化硫(SO )气体。
2
点燃
硫 + 氧气 二氧化硫
(S)(O ) (SO )
2 2
铁丝在空气中与氧气反应主要生成氧化铁(Fe O )固体,而铁丝在氧气中燃烧
2 3
生成黑色的四氧化三铁(Fe O )固体。
3 4
点燃
铁 + 氧气 四氧化三铁
(Fe)(O ) (Fe O )
2 3 4
34 化化 学学
HHUUAAXXUUEE课题 2 氧气的性质与应用
碳、硫、铁分别与氧气的反应有两个共同特点:一是它们都是物质与氧气
发生的反应,二是它们都是由两种物质生成一种新物质的反应。物质与氧气的
反应属于氧化反应,由两种或两种以上的物质生成一种新物质的反应称为化合
反应。
由上述反应可知,氧气是一种化学性质活泼的气体,能与许多物质发生反
应,反应过程中放出热量。物质在氧气中燃烧比在空气中更剧烈。某些在空
气中不易燃烧的物质,在氧气中却可以燃烧。
二、应用广泛的氧气
氧气在人类生活中扮演着极为重要的角色,在工业生产中也发挥着重要的作用。
氧气的用途与氧气的性质有关,因此可以从氧气的性质认识氧气的用途。
交流讨论
氧氧气气的的性性质质与与用用途途的的关关系系
请结合已有学习和生活经验,或通过与同学讨论、请教他人、查阅资料等方式,
说出氧气的具体用途,并将氧气的用途与对应的性质建立关联。
氧气的用途 氧气的性质
氧气的活泼性质决定了氧气的广泛用途。氧气可供给呼吸,因此人类生存、动
植物呼吸都离不开氧气,航天员在太空行走、潜水员在深海遨游、患者在医院急救
等特殊环境下,都必须携带或使用较高浓度的氧气。人们还常利用可燃物与空气中
的氧气反应放出的热量来取暖、加热食物等。燃料在纯氧中燃烧能快速提供更多的
热量、达到更高的温度,生产中也常用高纯度的氧气作助燃剂。高新科技领域和科
学研究中也经常会用到高纯度的氧气。
化化 学学 35
HHUUAAXXUUEE单元 2 探析空气之谜
太空行走
火 转
箭 炉
发 炼
射 钢
医 金
疗 属
急 切
救 割
深海潜水
图2-2-5 氧气的应用
三、氧气的获得
空气为人类正常生活提供了所需的氧气,但在医疗急救、科学研究、工业生产
和一些特殊环境下需要较为纯净的氧气。如何获得一定量纯净的氧气呢?
实验探究
实实验验室室制制取取少少量量的的氧氧气气
实实验验1 加热分解高锰酸钾制取氧气
步骤1 检验装置气密性。按图2-2-6所示,用手握紧试管,观察水中的导管口
是否有气泡冒出。如有气泡冒出,说明装置气密性良好;若没有上述现象,则说明装
置的气密性差,需要重新检查橡胶塞是否完好以及橡胶管、橡胶塞与玻璃导管的连接
处是否漏气。
图2-2-6 检验装置气密性
36 化化 学学
HHUUAAXXUUEE课题 2 氧气的性质与应用
步骤2 连接实验装置。按图 2-2-7 所示,向试管
高锰酸钾
中装入约 2 g 高锰酸钾,并在试管口放一团棉花,防止
加热时固体小颗粒进入导管。塞上带导气管的橡胶塞,
根据铁架台上酒精灯火焰的高度固定好试管,使试管口
略向下倾斜。将集气瓶中盛满水,用毛玻璃片盖住瓶口,
图2-2-7 加热分解高锰酸钾
将盛满水的集气瓶连同毛玻璃片一起倒立在盛水的水 制取氧气的装置
槽内。
步骤3 制取并用排水法收集氧气。加热试管,导管口会产生混有空气的气泡,
待气泡均匀、连续放出片刻后,把导管口伸入集气瓶中。当集气瓶中的水排完后,
在水面下用毛玻璃片盖住瓶口,小心地把集气瓶移出水槽,正放在桌上。
步骤4 检验氧气。将带火星的木条插入盛有氧气的集气瓶中,观察木条是否
复燃。
步骤5 结束实验。收集完需要的氧气后,先将导管移出水面,再熄灭酒精灯。
实实验验2 分解过氧化氢溶液制取氧气
按图2-2-8所示连接好实验装置,检验装置气密性 分液漏斗
过氧化氢溶液
后,将25 mL 5%的过氧化氢溶液装入分液漏斗中,在
锥形瓶
锥形瓶中放入少量二氧化锰以加快反应,打开分液漏斗
二氧化锰
上的活塞,使过氧化氢溶液缓慢滴下,用排水法收集并检
验氧气。
图2-2-8 分解过氧化氢溶液
与同学讨论下列问题: 制取氧气的装置
1.如何检验收集的氧气?
2.能否用向上排空气法收集氧气?
实验室通常用分解高锰酸钾(KMnO )或过氧化氢(H O )的方法制取氧气,
4 2 2
其化学反应可表示为:
加热
高锰酸钾 锰酸钾 + 二氧化锰 + 氧气
(KMnO ) (K MnO )(MnO )(O )
4 2 4 2 2
二氧化锰
过氧化氢 水 + 氧气
(H O ) (H O)(O )
2 2 2 2
化化 学学 37
HHUUAAXXUUEE单元 2 探析空气之谜
像高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气这样,由一种物质生成两种
或两种以上新物质的反应叫做分解反应。过氧化氢分解成水和氧气的反应也是分
解反应。
在分解过氧化氢制取氧气的反应中,二氧化锰能加快反应速率,但化学反应
前后本身的质量和化学性质都没有发生改变,化学上将这种物质称为催化剂。催
化剂在工业生产中具有重要的应用。
阅读理解
获获得得氧氧气气的的常常用用方方法法
通过分离空气获得氧气,是生产和生活中获得氧气的常用方法。
11.. 蒸蒸发发液液态态空空气气法法
蒸发液态空气法制取氧气,是工业上制取大量氧气的一种方法。其原理是将除尘
后的空气,经分子筛除去二氧化碳和水,再冷却至液态,根据液态氮(-196 ℃) 和
液态氧(-183 ℃)沸点的差异对二者进行分离,从而得到氧气。其流程如图 2-2-9
所示。
空气 过滤除尘 压缩 分子筛除杂 加压、降温 蒸发 氧气
水 、二氧化碳 氮气、稀有气体
图2-2-9 蒸发液态空气制取氧气的流程
为了便于贮存、运输和使用,通常把氧气加压到1.5 ×107 Pa,并贮存在蓝色的钢
瓶中。
22.. 分分子子筛筛吸吸附附法法
医用、家用制氧机多数是通过分子筛吸附法使空气中的氧气和氮气分离而获得氧
气的。在常温条件下,经过过滤的空气首先被压缩,再经冷却进入装有分子筛的
吸附塔,在加压时分子筛可吸附空气中的氮气,剩余未被吸收的氧气在气相中得
到富集,经过净化处理后可得到纯度不低于90% 的氧气。在减压时被分子筛吸附的氮
气会被释放出来,排放回空气中。在下一次加压时分子筛又可以吸附氮气并获得氧气。
整个过程为周期性的动态循环过程,分子筛并不消耗。其原理如图2-2-10所示。
38 化化 学学
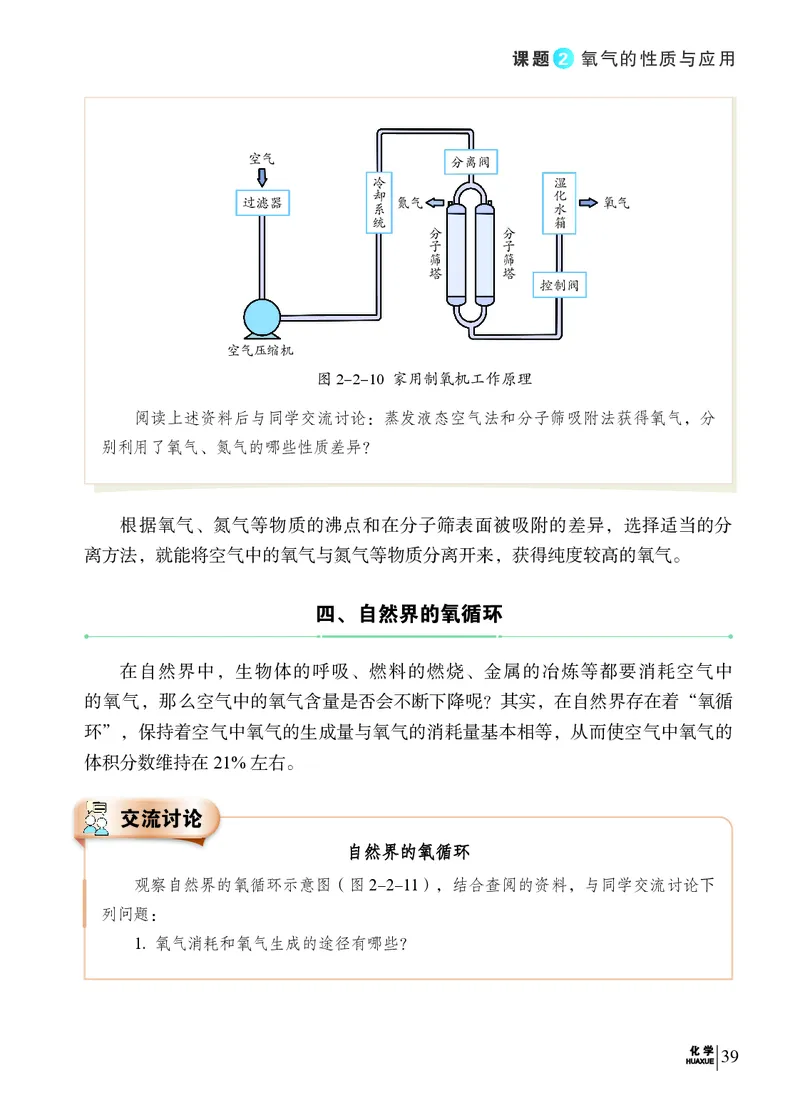
HHUUAAXXUUEE课题 2 氧气的性质与应用
空气 分离阀
冷 湿
却 化
过滤器 系 氮气 水 氧气
统 箱
分 分
子 子
筛 筛
塔 塔
控制阀
空气压缩机
图2-2-10 家用制氧机工作原理
阅读上述资料后与同学交流讨论:蒸发液态空气法和分子筛吸附法获得氧气,分
别利用了氧气、氮气的哪些性质差异?
根据氧气、氮气等物质的沸点和在分子筛表面被吸附的差异,选择适当的分
离方法,就能将空气中的氧气与氮气等物质分离开来,获得纯度较高的氧气。
四、自然界的氧循环
在自然界中,生物体的呼吸、燃料的燃烧、金属的冶炼等都要消耗空气中
的氧气,那么空气中的氧气含量是否会不断下降呢?其实,在自然界存在着“氧循
环”,保持着空气中氧气的生成量与氧气的消耗量基本相等,从而使空气中氧气的
体积分数维持在 21%左右。
交流讨论
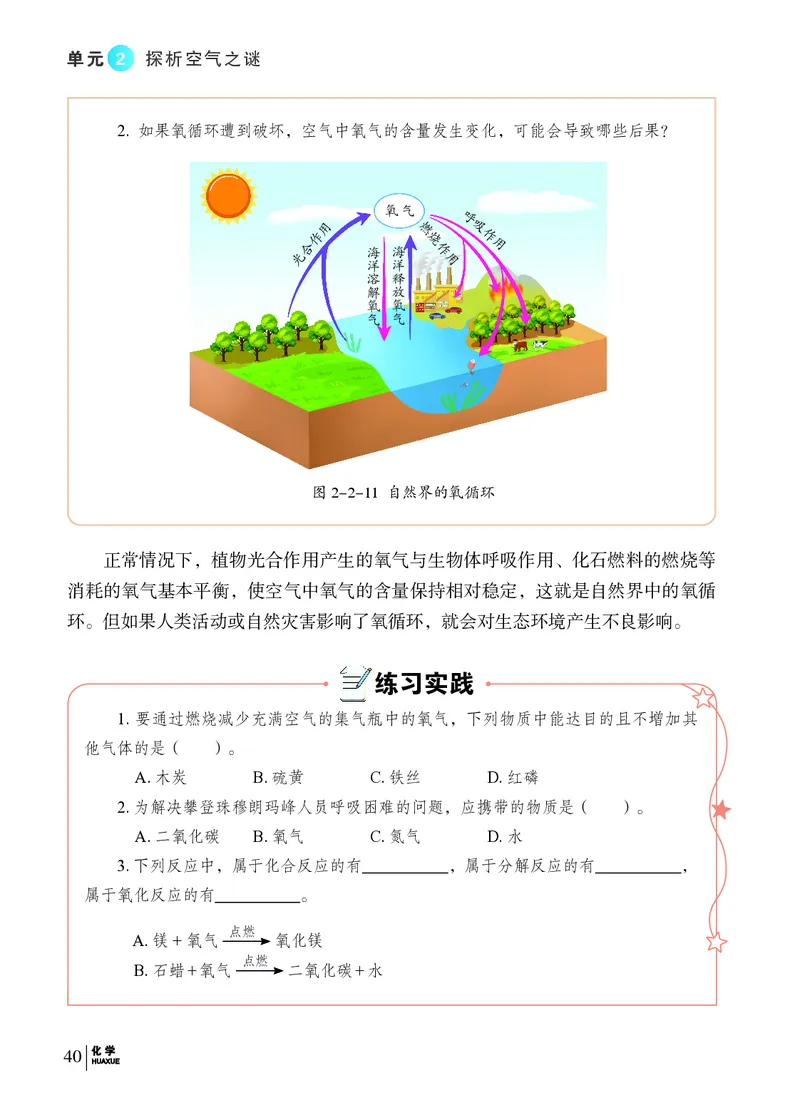
自自然然界界的的氧氧循循环环
观察自然界的氧循环示意图(图2-2-11),结合查阅的资料,与同学交流讨论下
列问题:
1. 氧气消耗和氧气生成的途径有哪些?
化化 学学 39
HHUUAAXXUUEE单元 2 探析空气之谜
2. 如果氧循环遭到破坏,空气中氧气的含量发生变化,可能会导致哪些后果?
氧 气 呼
用 燃 吸
作 烧 作
用
合 海 海 作
光 用
洋 洋
溶 释
解 放
氧 氧
气 气
图2-2-11 自然界的氧循环
正常情况下,植物光合作用产生的氧气与生物体呼吸作用、化石燃料的燃烧等
消耗的氧气基本平衡,使空气中氧气的含量保持相对稳定,这就是自然界中的氧循
环。但如果人类活动或自然灾害影响了氧循环,就会对生态环境产生不良影响。
练习实践
1. 要通过燃烧减少充满空气的集气瓶中的氧气,下列物质中能达目的且不增加其
他气体的是( )。
A.木炭 B.硫黄 C.铁丝 D.红磷
2.为解决攀登珠穆朗玛峰人员呼吸困难的问题,应携带的物质是( )。
A.二氧化碳 B.氧气 C.氮气 D.水
3.下列反应中,属于化合反应的有 ,属于分解反应的有 ,
属于氧化反应的有 。
点燃
A.镁+氧气 氧化镁
点燃
B.石蜡+氧气 二氧化碳+水
40 化化 学学
HHUUAAXXUUEE课题 2 氧气的性质与应用
加热
C. 碱式碳酸铜 氧化铜+二氧化碳+水
高温
D.碳酸钙 氧化钙+二氧化碳
E. 水+二氧化碳 碳酸
4.化学反应在生活中有很多应用,请写出下列应用中化学反应的文字表达式。
(1)白磷常被用作制造烟雾弹的发烟剂,它一遇到空气,就会自行燃烧,产生滚
滚的五氧化二磷浓烟。
(2)烟花的成分中含有硫,硫点燃后会产生二氧化硫气体。
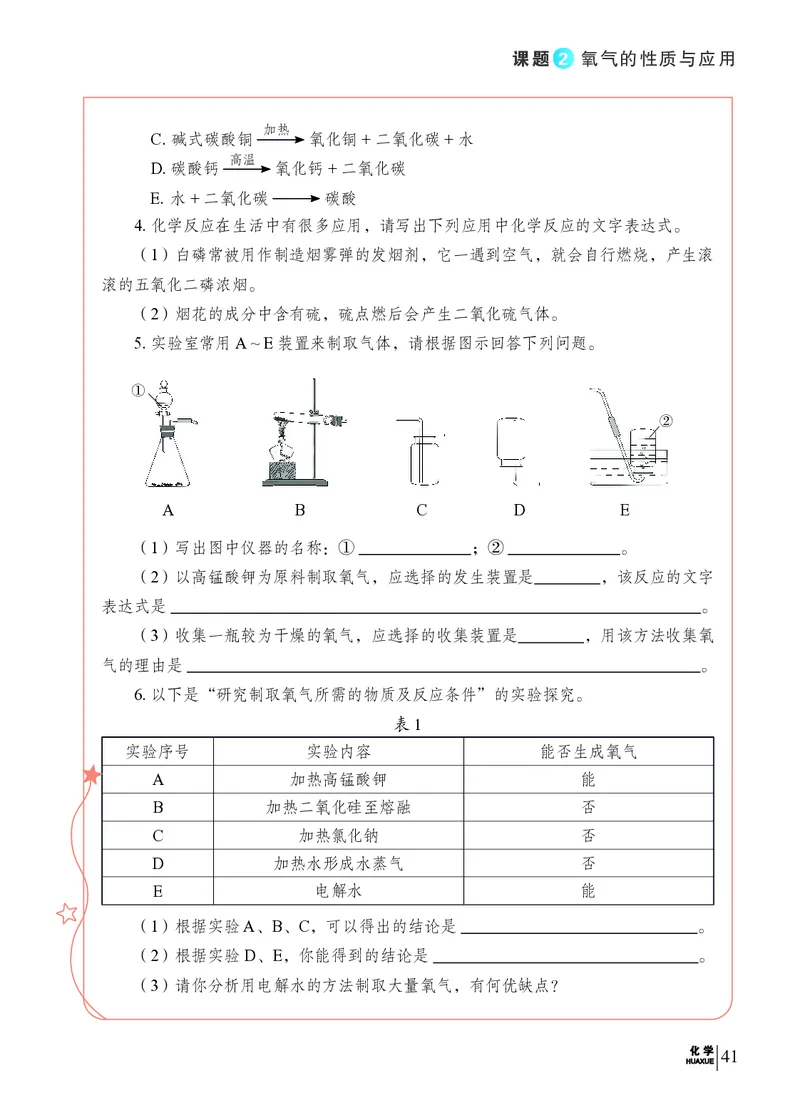
5.实验室常用 A ~ E 装置来制取气体,请根据图示回答下列问题。
①
②
A B C D E
(1)写出图中仪器的名称:① ;② 。
(2)以高锰酸钾为原料制取氧气,应选择的发生装置是 ,该反应的文字
表达式是 。
(3)收集一瓶较为干燥的氧气,应选择的收集装置是 ,用该方法收集氧
气的理由是 。
6.以下是“研究制取氧气所需的物质及反应条件”的实验探究。
表1
实验序号 实验内容 能否生成氧气
A 加热高锰酸钾 能
B 加热二氧化硅至熔融 否
C 加热氯化钠 否
D 加热水形成水蒸气 否
E 电解水 能
(1)根据实验 A、B、C,可以得出的结论是 。
(2)根据实验 D、E,你能得到的结论是 。
(3)请你分析用电解水的方法制取大量氧气,有何优缺点?
化化 学学 41
HHUUAAXXUUEE单元 2 探析空气之谜
课题 3 空气资源的保护
情境问题
空空气气————人人类类宝宝贵贵的的资资源源
空气是一种十分宝贵的资源,人类生存离不开空气。空气中的氮气、氧气、二氧
化碳、稀有气体等,都有重要的应用。空气质量直接影响人类的生活质量,保护空气
资源是我们每一个人的职责。
让我们共同探究下列问题:
1.空气中的各组分有哪些应用?
2.如何评价空气的质量?
3.如何保护空气资源?
一、空气是宝贵的自然资源
空气是最常见的、最重要的物质之一。空气中的各组分都具有广泛的应用。
联系实际
空空气气中中各各组组分分的的用用途途
结合生活实际,与同学交流讨论空气中各组分的用途,并将讨论的结果填入表中。
空气中的组分 用途
氮气
氧气
稀有气体
二氧化碳
水蒸气
42 化化 学学
HHUUAAXXUUEE课题 3 空气资源的保护
空气中含量最高的气体是氮气(N )。以氮气为原料生产的氮肥,为缓解人类
2
面临的粮食危机作出了巨大贡献。通常状况下,氮气很不活泼,在生产中常用作
保护气,如灯泡中填充氮气以延长灯泡的使用寿命,食品包装时填充氮气以保存食
品等。此外,液氮还是一种成本低廉且易于制取的冷冻剂,可以营造低温环境。
储藏粮食 液氮用于医疗冷冻
氮气
生产氮肥 保存食品
图2-3-1 氮气的用途
空气中还含有很少量的氦气(He)、氖气(Ne)、氩气(Ar)、氪气(Kr)、
氙气(Xe)等稀有气体,它们的应用也很广泛。通常情况下,稀有气体很难
与其他物质发生化学反应(人们曾把它们叫做“惰性气体”),因此常用作
焊接金属的保护气;稀有气体在通电时能发出不同颜色的光,因此还可用于
制造航标灯、强照明灯、闪光灯、霓虹灯等多种电光源;氦气、氖气和氩气
等可用于激光技术;氦气还可用来填充升空气球以及用作超导体的冷冻剂;
氙气可用于医疗麻醉等。
图2-3-2 稀有气体用于制作霓虹灯 图2-3-3 我国自主研发的用氦气
作为填充气的浮空艇
化化 学学 43
HHUUAAXXUUEE单元 2 探析空气之谜
二、保护空气,人人有责
通常情况下,空气中各种组分的含量保持相对稳定。随着人类生产和生活活动
范围的增加,空气中有害气体和烟尘不断增加,导致不同程度的空气污染。为了评
价空气质量,依据空气中污染物浓度的高低,我国制定了《环境空气质量标准》。
阅读理解
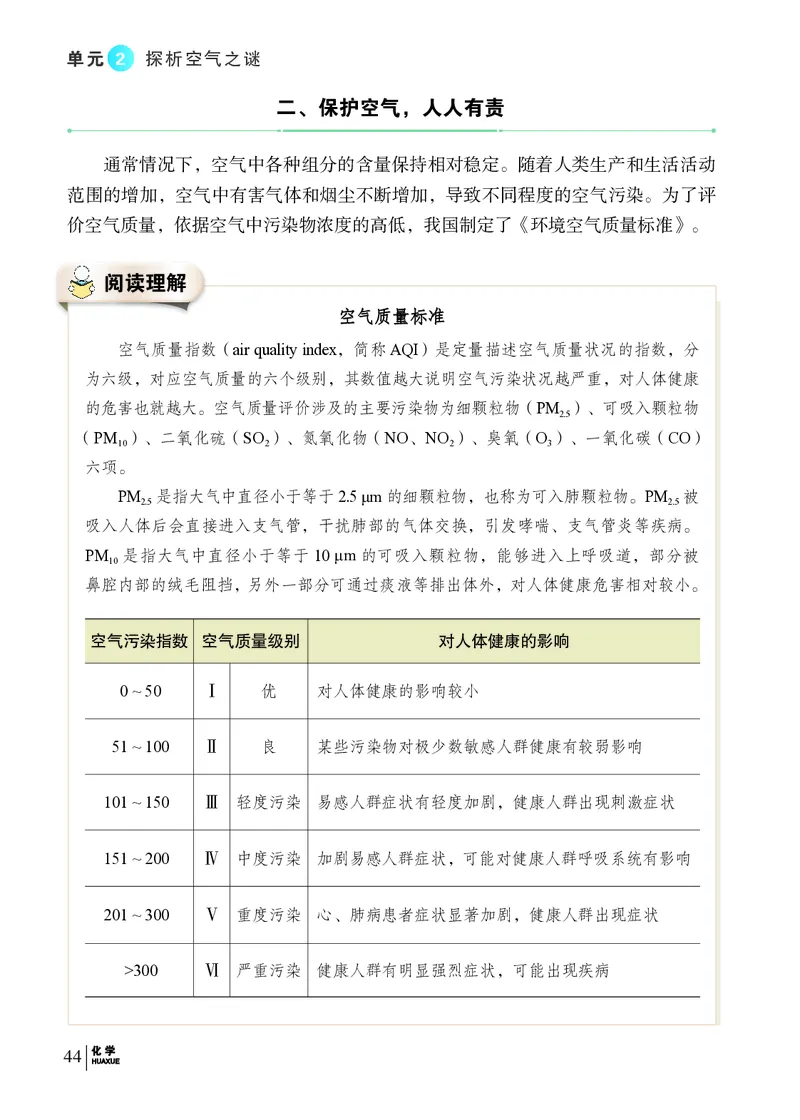
空空气气质质量量标标准准
空气质量指数(air quality index,简称AQI)是定量描述空气质量状况的指数,分
为六级,对应空气质量的六个级别,其数值越大说明空气污染状况越严重,对人体健康
的危害也就越大。空气质量评价涉及的主要污染物为细颗粒物(PM )、可吸入颗粒物
2.5
(PM )、二氧化硫(SO )、氮氧化物(NO、NO )、臭氧(O )、一氧化碳(CO)
10 2 2 3
六项。
PM 是指大气中直径小于等于2.5 μm的细颗粒物,也称为可入肺颗粒物。PM 被
2.5 2.5
吸入人体后会直接进入支气管,干扰肺部的气体交换,引发哮喘、支气管炎等疾病。
PM 是指大气中直径小于等于10 μm的可吸入颗粒物,能够进入上呼吸道,部分被
10
鼻腔内部的绒毛阻挡,另外一部分可通过痰液等排出体外,对人体健康危害相对较小。
空气污染指数 空气质量级别 对人体健康的影响
0 ~ 50 Ⅰ 优 对人体健康的影响较小
51 ~ 100 Ⅱ 良 某些污染物对极少数敏感人群健康有较弱影响
101 ~ 150 Ⅲ 轻度污染 易感人群症状有轻度加剧,健康人群出现刺激症状
151 ~ 200 Ⅳ 中度污染 加剧易感人群症状,可能对健康人群呼吸系统有影响
201 ~ 300 Ⅴ 重度污染 心、肺病患者症状显著加剧,健康人群出现症状
>300 Ⅵ 严重污染 健康人群有明显强烈症状,可能出现疾病
44 化化 学学
HHUUAAXXUUEE课题 3 空气资源的保护
图2-3-4 空气质量日报
阅读以上资料,从你所在地区的环境监测网站了解近期空气质量情况,并依据空
气质量对居民的出行、生活等提出建议。
我国各级环境监测部门均建立了空气质量实时监测、预报系统,并通过新闻
媒体及时、准确地发布空气质量状况,增强人们对环境的关注,提高全民的环保
意识。
空气污染是一个复杂的现象,在特定时间和地点,空气污染物浓度受到许多因
素影响。人为排放污染物是影响空气质量的最主要因素之一,其中包括车辆、
船舶、飞机等交通运输中排放的尾气,工业生产中排放的废气,以及居民生活、取
暖和垃圾焚烧产生的有害物质等。城市的发展密度、地形地貌和气象等也是影响空
气质量的重要因素。被污染的空气不仅对人体健康有害,还影响农作物生长,破坏
生态平衡。全球气候变暖、臭氧层空洞和酸雨等环境问题都与空气污染有关。
为了使天空更蓝,人类正在积极行动,如加强对空气质量的监测,研制和开发
清洁能源,积极植树造林,推进环保科技创新等,通过综合治理有效防治空气污染
以保护空气资源。
化化 学学 45
HHUUAAXXUUEE单元 2 探析空气之谜
练习实践
1. 下列关于空气中几种主要成分的性质及对应用途的说法错误的是( )。
A. 通常状况下,氮气化学性质不活泼,因此可用作保护气
B. 氧气具有助燃性,因此可用作燃料
C. 氦气密度比空气小,且很不活泼,因此可用于填充升空气球
D.稀有气体在通电时能发出不同颜色的光,如通电后氦气会发出橘红色的光,
氖气会发出红色的光,因此可应用于多种电光源
2. 下列措施与改善空气质量无关的是( )。
A. 使用高科技环保的微烟烟花
B. 使用太阳能、氢能等清洁能源
C. 采用风力、光伏发电,代替传统燃煤发电
D. 使用高性能耐蚀钢来建造滑雪赛道
3. 在氧气、二氧化碳、水蒸气、氮气、氖气五种气体中,选择适当的物质填写。
(1)可用于医疗急救的是 。
(2)可用于制造氮肥的是 。
(3)可用于制造霓虹灯等电光源的是 。
(4)能使澄清石灰水变浑浊的是 。
(5)可使空气保持一定湿度的是 。
4. 加强对空气质量的监测是保护环境的一项重要措施。下表是我国北方某城市一
年四季空气质量监测的平均数据。
表1
污染物的空气污染指数
季节 空气质量级别
可吸入颗粒物 氮氧化合物 二氧化硫
春季 88 40 44 II
夏季 67 33 36 II
秋季 90 46 54 II
冬季 105 69 60 III
请根据表中内容回答下列问题。
(1)对该市空气质量影响最大的污染物是什么?
(2)空气质量最差的是哪个季节?你认为造成这种情况的原因有哪些?
(3)你认为可采取哪些有效防治措施优化该市的空气质量?
46 化化 学学
HHUUAAXXUUEE单元小结
单元小结
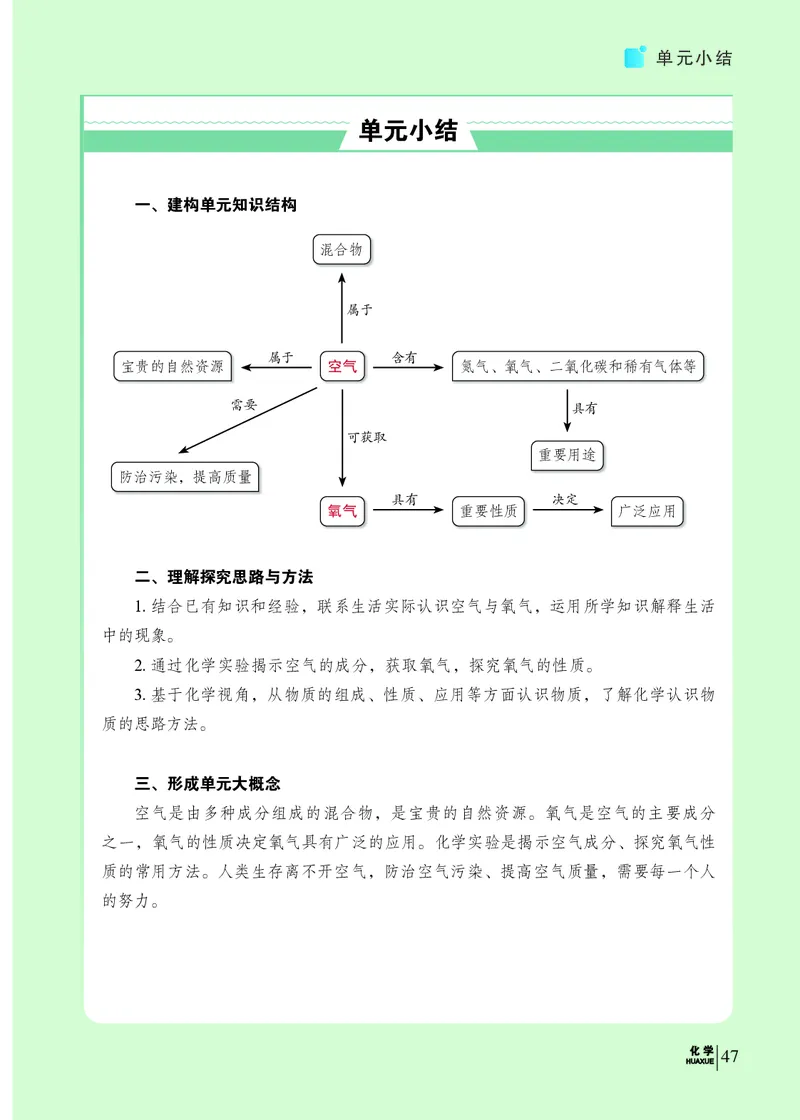
一、建构单元知识结构
混合物
属于
属于 含有
宝贵的自然资源 空气 氮气、氧气、二氧化碳和稀有气体等
需要 具有
可获取
重要用途
防治污染,提高质量
具有 决定
氧气 重要性质 广泛应用
二、理解探究思路与方法
1.结合已有知识和经验,联系生活实际认识空气与氧气,运用所学知识解释生活
中的现象。
2.通过化学实验揭示空气的成分,获取氧气,探究氧气的性质。
3.基于化学视角,从物质的组成、性质、应用等方面认识物质,了解化学认识物
质的思路方法。
三、形成单元大概念
空气是由多种成分组成的混合物,是宝贵的自然资源。氧气是空气的主要成分
之一,氧气的性质决定氧气具有广泛的应用。化学实验是揭示空气成分、探究氧气性
质的常用方法。人类生存离不开空气,防治空气污染、提高空气质量,需要每一个人
的努力。
化化 学学 47
HHUUAAXXUUEE单元作业
单元作业
1. 下列事实不能说明氧气的性质比氮气活泼的是( )。
A. 氧气用于炼钢,氮气常用作保护气
B. 红磷在氧气中可以燃烧,在氮气中不能燃烧
C. 液氧的沸点高,液氮的沸点低
D. 食品包装防腐时充入氮气而不充入氧气
2. 为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是( )。
A. 在同一瓶氧气中,先后进行不同粗细铁丝的燃烧实验
B. 在两瓶不同浓度的氧气中,同时分别进行不同粗细铁丝的燃烧实验
C. 在两瓶不同浓度的氧气中,同时分别进行相同粗细铁丝的燃烧实验
D. 在两瓶相同浓度的氧气中,同时分别进行不同粗细铁丝的燃烧实验
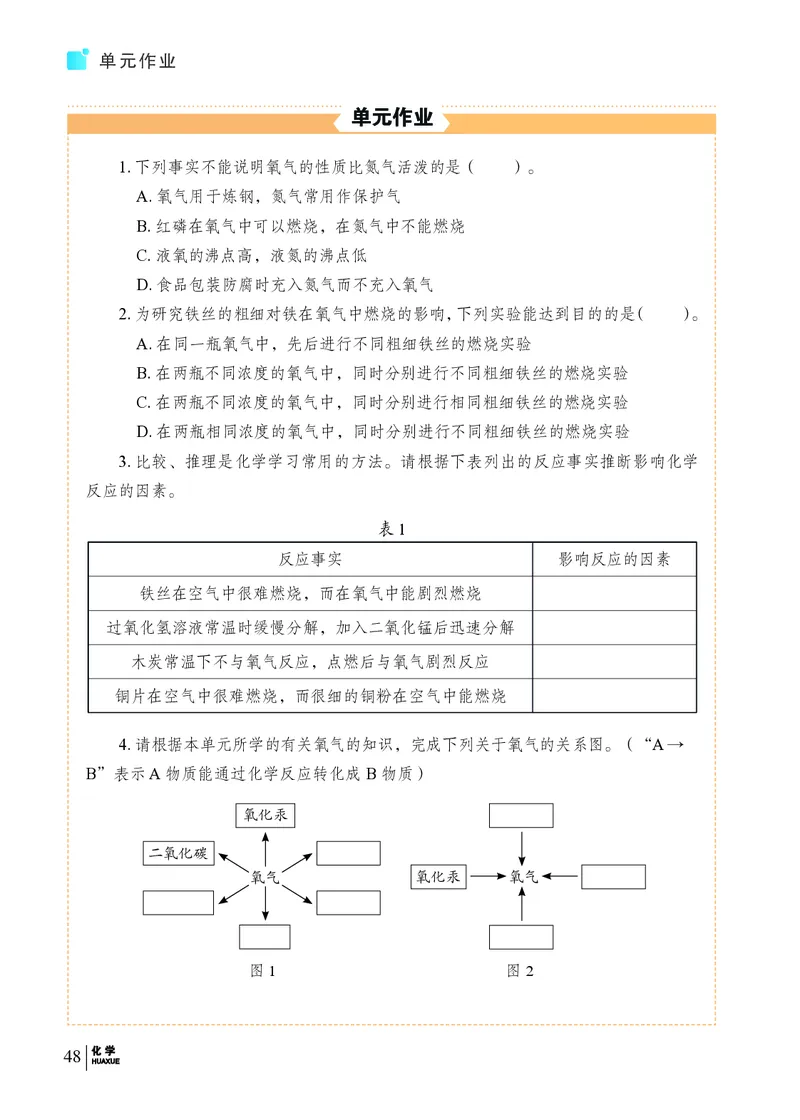
3.比较、推理是化学学习常用的方法。请根据下表列出的反应事实推断影响化学
反应的因素。
表1
反应事实 影响反应的因素
铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧
过氧化氢溶液常温时缓慢分解,加入二氧化锰后迅速分解
木炭常温下不与氧气反应,点燃后与氧气剧烈反应
铜片在空气中很难燃烧,而很细的铜粉在空气中能燃烧
4.请根据本单元所学的有关氧气的知识,完成下列关于氧气的关系图。(“A →
B”表示 A 物质能通过化学反应转化成B物质)
氧化汞
二氧化碳
氧气 氧化汞 氧气
图1 图2
48 化化 学学
HHUUAAXXUUEE单元作业
5.有甲、乙、丙3个集气瓶,分别盛有氧气、氮气、空气,请根据下列实验现象
确定3个集气瓶中分别为何种气体。
燃烧着的
甲 木条在甲瓶中熄灭
木条检验
乙 木条在乙瓶中燃烧更旺
丙 木条在丙瓶中继续燃烧
6.臭氧(O )是大气中自然产生的一种具有特殊臭味的微量气体,绝大部分臭氧
3
存在于距离地面25 km左右处的大气平流层中,它能吸收对人体有害的短波紫外线。
可它为何又是危害环境的污染物呢?
地表空气中的臭氧对人体极为有害。一些易于过敏的人长时间暴露在臭氧含量超
过180 μg ·· m-3的环境中,会产生眼睛刺痛、咳嗽等不良症状。研究表明,空气中每
立方米臭氧含量每增加100 μg,人的呼吸功能就会减弱 3%。
地表臭氧并不是人类活动直接排放出的污染物,而是氮氧化物或挥发性有机污
染物与氧气反应形成的,强烈的阳光照射会加速这些化学反应。氮氧化物主要来自
燃煤、汽车尾气等;挥发性有机污染物来源非常复杂,涂料、燃油及炼油厂、干洗
店等都会产生这种污染物。
依据材料内容,回答下列问题。
(1)下列说法正确的是 。
A. 臭氧是一种无色无味气体
B. 臭氧层具有吸收紫外线的作用
C. 地表空气中臭氧的含量与天气阴晴无关
D. 空气中臭氧浓度不同会对人体造成不同程度的影响
(2)导致地表空气中臭氧含量增加的原因是 。
(3)为了减少臭氧污染,请你向市民提出一条可行建议 。
化化 学学 49
HHUUAAXXUUEE项目学习
项目学习
生生活活中中的的蓝蓝天天保保护护行行动动
项目背景
空气是人类赖以生存的基本环境,也是人类的宝贵资源。随着科学技术的发展,
空气中各成分的应用越来越广泛。我国秉承“像保护眼睛一样保护自然和生态环境,
坚定不移走生产发展、生活富裕、生态良好的文明发展道路,实现中华民族永续发展”
的理念,采取了一系列措施,使生态环境发生了历史性、转折性和全局性变化,祖国
的天更蓝、山更绿、水更清。
实施“生活中的蓝天保护行动”是新时代中国青少年的责任和使命。
项目建议方案
1.查阅资料。查阅资料,了解我国为改善空气质量而制定的法律法规和行动政策。
2. 走访调查。走访调查家庭成员、乡村(社区)邻居或相关部门从业人员,从
禁止秸秆焚烧、改进生活燃料、减少空气扬尘、绿色交通出行、保护树木植被、垃圾
分类回收等角度,了解生活中采取蓝天保护行动取得的成就和需要改进的问题。
3.总结报告。依据国家政策要求,结合走访调查的结果和生活实际,制订一份“保
护蓝天,我在行动”的计划;以小组为单位,制作一份以“我们的蓝天,我们守护”
为题的电子小报或手抄报。
4.成果展示。将你制订的“保护蓝天,我在行动”的计划在小组内交流,并将制
作的“我们的蓝天,我们守护”的电子小报或手抄报在班级展示。
50 化化 学学
HHUUAAXXUUEE单元 3 初探物质构成
课题 1 探秘微观粒子特性
情境问题
运运用用微微观观粒粒子子的的特特性性解解释释生生活活现现象象
在生活中我们经常会观察到如下现象:
1.将少量食盐加入水中,食盐很快消失。
2.在阳光下晒衣服,衣服干得快。
3.在篮球中可以充入空气。
图3-1-1 生活中一些常见的现象
请与同学合作探究下列问题:
1.产生上述现象的原因是什么?如何从构成物质的微观粒子视角进行解释?
2.物质是由哪些微观粒子构成的?构成物质的微观粒子具有哪些特征?
一、微观粒子的特性
为寻求“物质是由什么构成的”这一问题的答案,人类经历了很长时间的
探索。最初人类是从“物质是否可以无限分割”这一问题开始思考的。中国古代
典籍《墨经》中有“非半弗斫,则不动,说在端”的说法,意思是物质无限分
割下去,最终得到“端”,“端”不能再分割。《墨经》中的“端”类似于同时期
的古希腊哲学家德谟克里特所说的“原子”(在希腊语中,原子的意思是“不可
分割”)。《庄子··杂篇··天下》中有“一尺之棰,日取其半,万世不竭”的
说法,意思是物质是可以永远分下去的。如今,人们知道“物质是由微观粒子构
52 化化 学学
HHUUAAXXUUEE课题 1 探秘微观粒子特性
成的”,这一结论已被理论和大量的实验证实,运用这一结论能解释许多宏观
现象。
实验探究
构构成成物物质质的的微微观观粒粒子子的的特特性性
请完成以下实验,观察实验现象,并根据观察到的现象分析推理,形成你对构成
物质的微观粒子特性的认识,将你观察到的现象和得到的结论填写到表格中。
实实验验1 高锰酸钾的溶解
向盛有水的烧杯中加入几小粒高锰酸钾固体,静置,观察加入水中的高锰酸钾颗
粒的变化,用玻璃棒搅拌,观察溶液颜色的变化(图3-1-2)。
图3-1-2 高锰酸钾的溶解
实实验验2 乙醇与水的混合
取 1 支细长的玻璃管,在容积的 1/2 处做标记,向其中加水至标记处,再向玻璃
管中加满乙醇,用拇指堵住管口,上下颠倒玻璃管数次,观察玻璃管中溶液的体积
变化。
实实验验3 氨的挥发
预先准备1个空的矿泉水瓶,在1根棉线上系4个蘸有酚酞
溶液的棉球,将棉线的一端用透明胶带粘在瓶盖内侧,拧紧瓶盖,
在矿泉水瓶底部用一次性注射器压入一滴浓氨水,观察棉球的颜
色变化(图3-1-3)。
图3-1-3 氨的挥发
化化 学学 53
HHUUAAXXUUEE单元 3 初探物质构成
实实验验4 品红在冷水、热水中的溶解
向2个烧杯中分别加入等量的冷水和热水,同时
向烧杯中加入相同质量的几小粒品红固体,观察、比
较2个烧杯中品红的分散现象(图3-1-4)。
图3-1-4 品红在冷水、热水中的溶解
实验 实验现象 实验结论
1
2
3
4
从上述实验中发现,将几小粒高锰酸钾(KMnO )固体加入水中后,高锰酸钾
4
固体“消失”了,而且整杯水都呈紫红色。在这一过程中,高锰酸钾固体在水分子
(构成水的微观粒子)的作用下不断被“分割”成很小、肉眼看不见的微观粒子,
这些粒子通过水分子之间的间隙均匀扩散;水和乙醇能均匀混合,且混合后总体积
比混合前二者的体积之和小,说明构成水和乙醇的微观粒子是不断运动的,水和
乙醇均匀混合后的微观粒子间的间隙比混合前的小;在氨的挥发实验中,浓氨
水中的微观粒子——氨分子扩散到空气中,在空气中运动,接触到蘸有酚酞溶液
的棉球时,氨分子与酚酞溶液作用使酚酞溶液变红;品红在热水中的扩散速率比
在冷水中的快,说明在热水中,水分子的运动速率更快,使品红在热水中扩散速
率更快。
理论和实验均表明,物质是由微观粒子构成的;微观粒子非常小,微观粒子之
间存在间隙,微观粒子是在不断运动的;温度越高,构成物质的微观粒子的运动速
率越快。利用微观粒子的特性可以解释日常生活中的许多现象。
二、构成物质的微观粒子
物质是由微观粒子构成的,原子、分子和离子都是构成物质的微观粒子。
原子是构成物质的一种微观粒子。自然界的许多物质是由原子构成的,如
54 化化 学学
HHUUAAXXUUEE课题 1 探秘微观粒子特性
铁、铜、铝、稀有气体、金刚石、石墨、硅
等。原子的体积很小,1个氧原子的直径约为
1.48×10-10 m,如果将氧原子紧密地排列成
1 cm长的一列,约需7×107 个氧原子。如果
乒乓球
将氧原子与直径为 1 cm 的小球相比较,相
当于将一个乒乓球与地球相比较。 地球
图3-1-5 原子大小示意图
铜由铜原子构成 金刚石由碳原子构成
图3-1-6 由原子构成的物质
分子也是构成物质的一种微观粒子。我们所熟悉的氧气是由氧分子(O )构
2
成的,氮气是由氮分子(N )构成的,水是由水分子(H O)构成的,二氧化碳是
2 2
由二氧化碳分子(CO )构成的,酒精是由乙醇分子(C H O)构成的。
2 2 6
科学研究表明,分子的体积很小,其半径大约在 10-10 m 数量级。分子的质
量也很小,一个水分子的质量约为 3×10-26 kg,10 g 水中约含有 3.33×1023 个水
分子,如果平均分给地球上的 80 亿人,每人可以分到约 4.17×1013 个水分子,这
个数字是地球总人口的 5 200 多倍。
消防员携带的用于呼吸的氧气瓶 海洋中的水由水分子构成 干冰灭火器中的干冰由
中的氧气由氧分子构成 二氧化碳分子构成
图3-1-7 由分子构成的物质
化化 学学 55
HHUUAAXXUUEE单元 3 初探物质构成
拓展视野
分分子子学学说说的的建建立立
19世纪早期,科学家通过实验发现,在同温同压下,相同体积的任何气体均含有
相同数目的微观粒子。但是人们发现1体积的氧气和2体积的氢气经过反应后可以生
成 2 体积的水蒸气。这个实验事实无法用当时的“构成物质的基本微观粒子都是原
子”的理论来解释。后来,在大量的实验和理论研究基础上,人们认识到原子可以构
成比较复杂的微观粒子——分子。氧气、氢气和水都是由分子构成的。分子是由原子
构成的,如1个水分子是由1个氧原子和2个氢原子构成的,1个氧分子是由2个氧
原子构成的(图3-1-8)。
点燃
O H HO
2 2 2
图3-1-8 氢气和氧气反应生成水的分子变化模型
离子是构成物质的另一种微观粒子。自然界的许多物质,如食盐的主要成分氯
化钠(NaCl)和生石灰的主要成分氧化钙(CaO)等,都是由离子构成的。
氯化钠由钠离子和氯离子构成 氧化钙由钙离子和氧离子构成
图3-1-9 由离子构成的物质
原子得到或失去电子转化为带电的原子,我们把带电的原子或原子团叫做
离子。带正电的原子或原子团叫做阳离子,带负电的原子或原子团叫做阴离子。由
离子构成的物质中并不存在分子,如氯化钠中不存在氯化钠分子,它是由钠离子和
氯离子构成的。
56 化化 学学
HHUUAAXXUUEE课题 1 探秘微观粒子特性
表3-1-1 一些常见物质的构成
物质构成 实例
原子 铜(Cu)、金刚石(C)、单晶硅(Si)、稀有气体(He等)
分子 氧气(O )、水(H O)、二氧化碳(CO )、葡萄糖(C H O )
2 2 2 6 12 6
离子 氯化钠(NaCl)、碳酸钙(CaCO )、高锰酸钾(KMnO )
3 4
练习实践
1.下列物质由离子构成的是( )。
Na+
_
Cl
A.氧气 B.水 C.氯化钠 D.金刚石
2.将一定量的氧气置于密闭容器中降温,可以转化为淡蓝色液体。下列关于该过
程的说法正确的是( )。
A.氧分子的体积变小 B.氧分子的质量变小
C.氧分子的数目变少 D.氧分子间的间隙变小
3.请用微观粒子的特性解释下列生活中的常见现象。
(1)“端午到,粽香飘”。
(2)蔗糖放入水中“消失”了。
(3)空气中有水蒸气,但肉眼看不到。
(4)瘪的乒乓球放入热水中,又鼓起来了。
4.将分别盛有冷水和热水的2个烧杯放在桌上,各滴加几滴墨水,请预测可能产
生的现象,并说明预测的理由。
化化 学学 57
HHUUAAXXUUEE单元 3 初探物质构成
课题 2 认识原子结构
情境问题
镁镁条条燃燃烧烧过过程程中中微微观观粒粒子子的的变变化化
镁条在空气中点燃会发生燃烧,放出大量的热,发
出耀眼的白光,并生成白色固体。燃烧过程中,镁(Mg)
与空气中的氧气(O )反应生成氧化镁(MgO)。镁条
2
是由镁原子构成的,氧气是由氧分子构成的,氧化镁是
由镁离子和氧离子构成的。
图3-2-1 镁条的燃烧
请与同学合作探究下列问题:
1. 镁原子、氧原子具有怎样的结构?
2. 镁原子和氧原子是如何转变成镁离子和氧离子的?
一、原子结构的探索
以前,人们一直认为原子是不可分割的、坚硬的、实心的球体。直到1897年,
英国物理学家汤姆生发现电子后,人们才逐渐认识到原子并不是不可分割的,原子
有一定的结构。
阅读理解
人人类类对对原原子子结结构构的的探探索索
人类对原子的认识经历了漫长的时期。
1803年,道尔顿借用“原子”概念提出了原子学说。他认为:原子是不能再分的
粒子,原子是微小的实心球。
1897年,汤姆生等人根据阴极射线实验,发现电子是所有物质的原子中均有的粒
子,并提出新的原子结构模型。他认为电子平均分布在整个原子中,就如同散布在一
个均匀的正电荷的海洋之中,它们的负电荷与那些正电荷相互抵消,所以原子是电中
58 化化 学学
HHUUAAXXUUEE课题 2 认识原子结构
性的。
1909年,卢瑟福和他的研究团队做了著名的α粒子散射实验(α粒子为带2个
单位正电荷的氦原子核):在一个铅盒里放有少量能产生α粒子的放射性元素,它发
出的α射线从铅盒的小孔射出,形成一束很细的射线射到很薄的金箔上;α粒子穿
过金箔后,射到探测屏上产生一个个的闪光点。实验发现:(1)大多数 α粒子能穿
透金箔,而且不改变原来的前进方向;(2)少数α粒子改变了原来的运动路径,发
生偏转;(3)极少数的α粒子好像碰到了不可穿透的坚硬质点而被弹了回来。
金箔
α粒子发生器
狭缝
探测屏
图3-2-2 α粒子轰击金箔实验
1911年,卢瑟福根据α粒子散射实验的结果,类比行星运动,提出了原子结构行
星模型:原子的大部分体积是空的;在原子的中心有一个很小的原子核;原子的全部正
电荷和几乎全部质量都集中在原子核内;带负电的电子在核外空间进行绕核运动。
1913年,丹麦物理学家玻尔在研究氢原子光谱的基础上,大胆地将量子论引入原
子结构,提出了原子结构量子模型:原子的核外电子处在一定的轨道上绕核运行,在
不同轨道上运动的电子能量不同,当电子从一个轨道跃迁到另一个轨道时,会辐射或
吸收能量。
随着科学理论和科学技术的发展,人类对原子结构有了更新的认识。1993年,中
国科学院科研团队利用扫描隧道显微镜通过移动硅原子摆出了“中国”字样,这标
志着我国可自主实现原子操纵。
图3-2-3 能实现原子操纵 图3-2-4 1993年我国科学家通过
的扫描隧道显微镜 移动硅原子得到的汉字“中国”
化化 学学 59
HHUUAAXXUUEE单元 3 初探物质构成
试着回答下列问题,并与同学交流讨论。
1.根据α粒子散射实验的现象,你能得到什么结论?
2.从原子结构模型的演变和发展中,你能得到什么启迪?
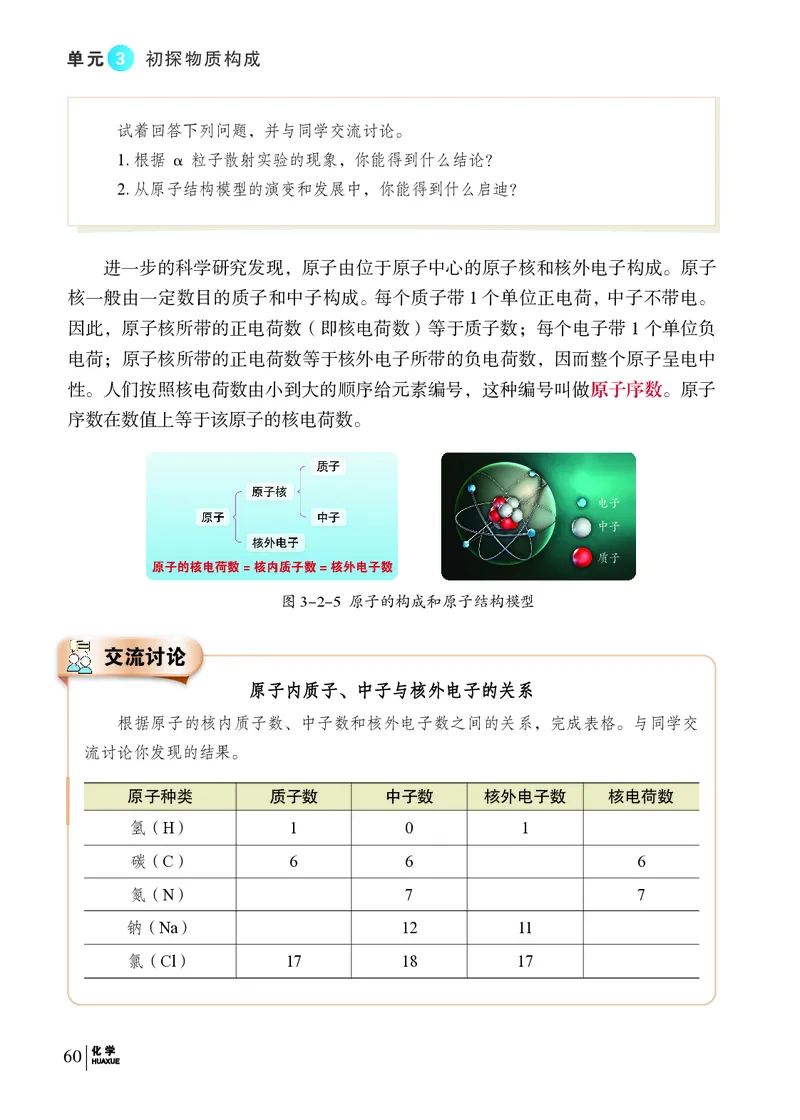
进一步的科学研究发现,原子由位于原子中心的原子核和核外电子构成。原子
核一般由一定数目的质子和中子构成。每个质子带1个单位正电荷,中子不带电。
因此,原子核所带的正电荷数(即核电荷数)等于质子数;每个电子带 1 个单位负
电荷;原子核所带的正电荷数等于核外电子所带的负电荷数,因而整个原子呈电中
性。人们按照核电荷数由小到大的顺序给元素编号,这种编号叫做原子序数。原子
序数在数值上等于该原子的核电荷数。
电子
中子
质子
图3-2-5 原子的构成和原子结构模型
交流讨论
原原子子内内质质子子、、中中子子与与核核外外电电子子的的关关系系
根据原子的核内质子数、中子数和核外电子数之间的关系,完成表格。与同学交
流讨论你发现的结果。
原子种类 质子数 中子数 核外电子数 核电荷数
氢(H) 1 0 1
碳(C) 6 6 6
氮(N) 7 7
钠(Na) 12 11
氯(Cl) 17 18 17
60 化化 学学
HHUUAAXXUUEE课题 2 认识原子结构
化学变化中原子核是不变的,改变的只是核外电子的运动状态或核外电子的
数目。核外电子的运动状态与物质的性质有着密切关系。在化学变化中,原子可
以得到或失去核外电子转变为离子,如镁条在空气中燃烧时,镁原子失去电子转
变为镁离子(Mg2+),氧分子中的氧原子得到电子转变为氧离子(O2-)。在化学
变化中,分子可以分解成原子,原子也能结合成为分子,如硫在氧气中燃烧、过
氧化氢分解制取氧气的反应,存在分子分解为原子、原子结合为分子的过程。
拓展视野
原原子子的的核核外外电电子子排排布布
科学研究表明,在含有多个电子的原子中,核外电子具有不同的能量和运动区
域,电子运动区域离原子核越近,核外电子的能量越低。原子的核外电子是分层排
布的,离核最近的电子层为第一层,次之为第二层,依次类推。
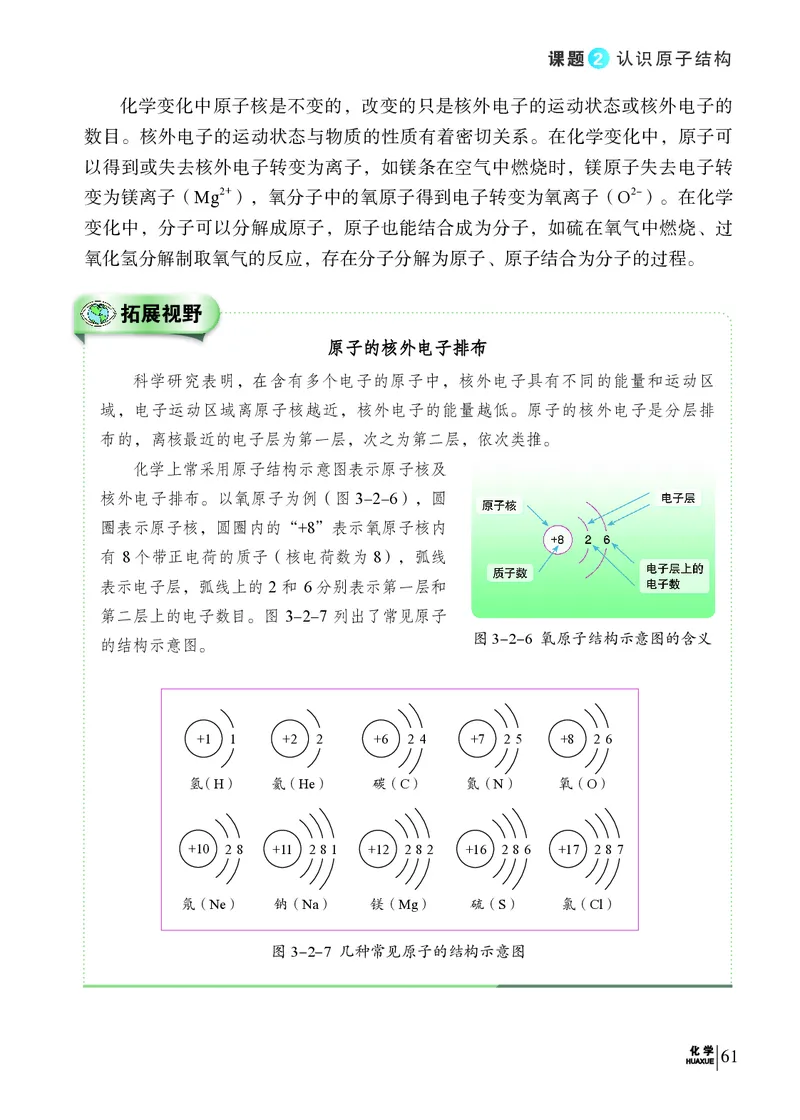
化学上常采用原子结构示意图表示原子核及
核外电子排布。以氧原子为例(图3-2-6),圆
圈表示原子核,圆圈内的“+8”表示氧原子核内
有 8个带正电荷的质子(核电荷数为8),弧线
表示电子层,弧线上的2 和 6分别表示第一层和
第二层上的电子数目。图 3-2-7 列出了常见原子
图3-2-6 氧原子结构示意图的含义
的结构示意图。
+1 1 +2 2 +6 2 4 +7 2 5 +8 2 6
氢(H) 氦(He) 碳(C) 氮(N) 氧(O)
+10 2 8 +11 2 8 1 +12 2 8 2 +16 2 8 6 +17 2 8 7
氖(Ne) 钠(Na) 镁(Mg) 硫(S) 氯(Cl)
图3-2-7 几种常见原子的结构示意图
化化 学学 61
HHUUAAXXUUEE单元 3 初探物质构成
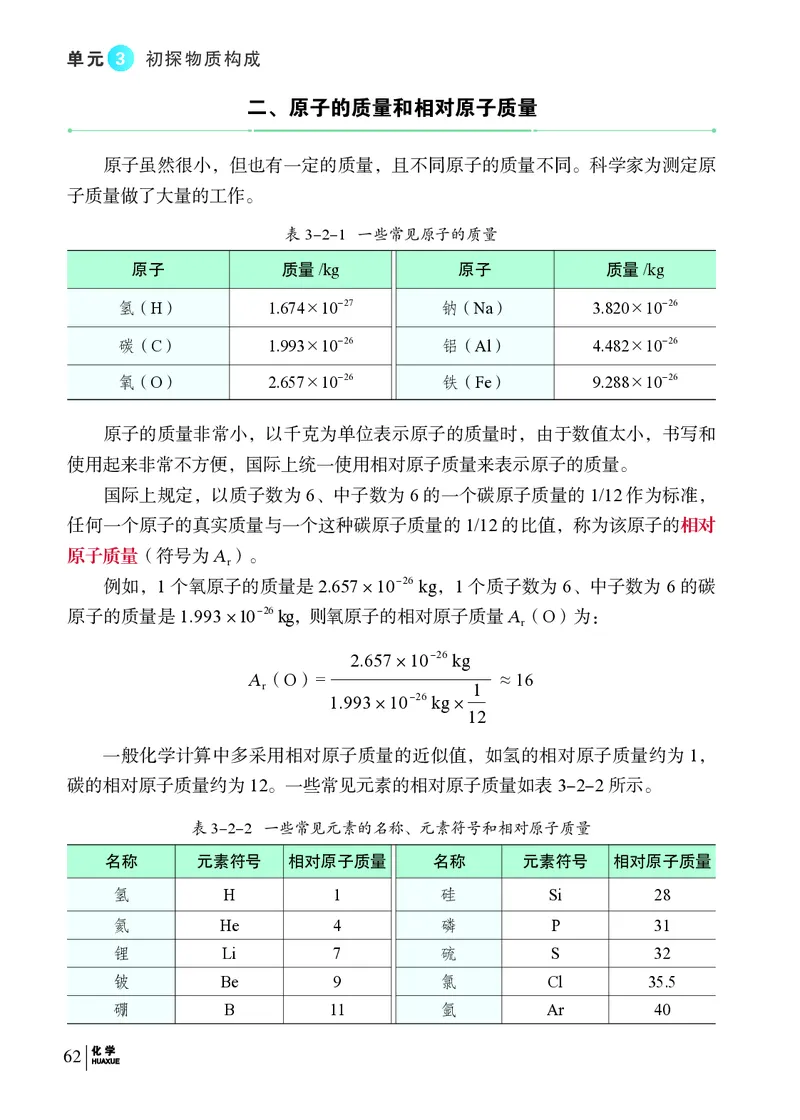
二、原子的质量和相对原子质量
原子虽然很小,但也有一定的质量,且不同原子的质量不同。科学家为测定原
子质量做了大量的工作。
表3-2-1 一些常见原子的质量
原子 质量/kg 原子 质量/kg
氢(H) 1.674×10-27 钠(Na) 3.820×10-26
碳(C) 1.993×10-26 铝(Al) 4.482×10-26
氧(O) 2.657×10-26 铁(Fe) 9.288×10-26
原子的质量非常小,以千克为单位表示原子的质量时,由于数值太小,书写和
使用起来非常不方便,国际上统一使用相对原子质量来表示原子的质量。
国际上规定,以质子数为 6、中子数为 6 的一个碳原子质量的 1/12 作为标准,
任何一个原子的真实质量与一个这种碳原子质量的1/12 的比值,称为该原子的相对
原子质量(符号为A)。
r
例如,1 个氧原子的质量是 2.657×10-26 kg,1 个质子数为 6、中子数为 6 的碳
原子的质量是 1.993×10-26 kg,则氧原子的相对原子质量A(O)为:
r
2.657×10-26 kg
A(O)= ————————— ≈ 16
r 1
1.993×10-26 kg×—
12
一般化学计算中多采用相对原子质量的近似值,如氢的相对原子质量约为 1,
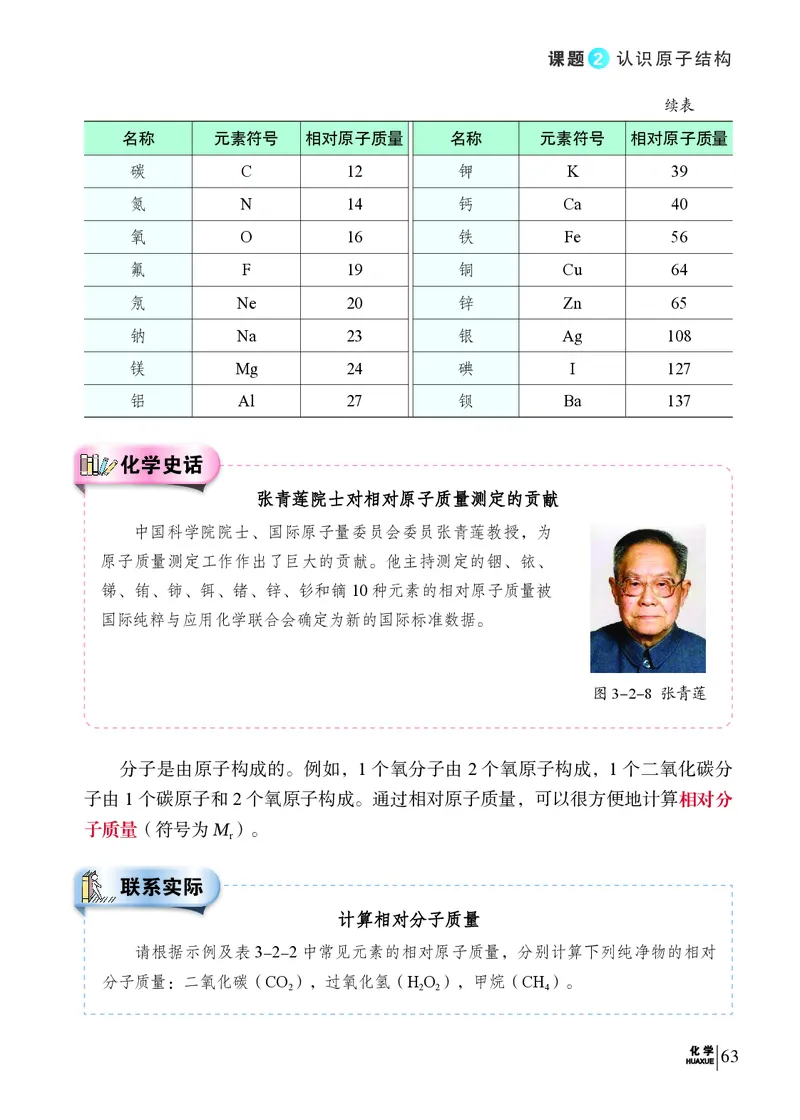
碳的相对原子质量约为12。一些常见元素的相对原子质量如表3-2-2所示。
表3-2-2 一些常见元素的名称、元素符号和相对原子质量
名称 元素符号 相对原子质量 名称 元素符号 相对原子质量
氢 H 1 硅 Si 28
氦 He 4 磷 P 31
锂 Li 7 硫 S 32
铍 Be 9 氯 Cl 35.5
硼 B 11 氩 Ar 40
62 化化 学学
HHUUAAXXUUEE课题 2 认识原子结构
续表
名称 元素符号 相对原子质量 名称 元素符号 相对原子质量
碳 C 12 钾 K 39
氮 N 14 钙 Ca 40
氧 O 16 铁 Fe 56
氟 F 19 铜 Cu 64
氖 Ne 20 锌 Zn 65
钠 Na 23 银 Ag 108
镁 Mg 24 碘 I 127
铝 Al 27 钡 Ba 137
化学史话
张张青青莲莲院院士士对对相相对对原原子子质质量量测测定定的的贡贡献献
中国科学院院士、国际原子量委员会委员张青莲教授,为
原子质量测定工作作出了巨大的贡献。他主持测定的铟、铱、
锑、铕、铈、铒、锗、锌、钐和镝10种元素的相对原子质量被
国际纯粹与应用化学联合会确定为新的国际标准数据。
图3-2-8 张青莲
分子是由原子构成的。例如,1 个氧分子由 2 个氧原子构成,1 个二氧化碳分
子由 1 个碳原子和 2 个氧原子构成。通过相对原子质量,可以很方便地计算相对分
子质量(符号为M)。
r
联系实际
计计算算相相对对分分子子质质量量
请根据示例及表3-2-2中常见元素的相对原子质量,分别计算下列纯净物的相对
分子质量:二氧化碳(CO ),过氧化氢(H O ),甲烷(CH )。
2 2 2 4
化化 学学 63
HHUUAAXXUUEE单元 3 初探物质构成
示例:计算氧化铁(Fe O )的相对分子质量。
2 3
M(Fe O )= 2×A(Fe)+ 3×A(O)
r 2 3 r r
= 2×56 + 3×16
= 160
练习实践
1.氧的相对原子质量为16,表示的意义是( )。
A.氧原子核中有16个质子
B.一个氧原子的质量为16 g
C.一个氧原子的质量是质子数、中子数均为 6的一个碳原子质量的1/12
D.一个氧原子的质量是质子数、中子数均为 6的一个碳原子质量1/12的16倍
2.稀土是一种重要的战略资源。铈就是一种稀土金属,其原子的核电荷数为58。
下列有关铈原子的说法不正确的是( )。
A.铈原子的原子序数是58
B.铈原子的核外电子数是58
C.铈原子的质子数是58
D.铈原子的相对原子质量是58
3.已知一种碳原子可用于测定文物所属年代,该碳原子的原子核内含有6个质子
和8个中子,则该碳原子的核外电子数为 。
4.若1个钠原子的质量为3.820×10-26 kg,1个质子数、中子数均为 6的碳原子
的质量是 1.993×10-26 kg,则钠原子的相对原子质量A(Na)为 。
r
5.计算下列物质的相对分子质量。
(1)臭氧(O )。 (2)二氧化硫(SO )。
3 2
(3)氧化镁(MgO)。 (4)乙醇(C H O)。
2 6
64 化化 学学
HHUUAAXXUUEE课题 3 物质组成的表示
课题 3 物质组成的表示
情境问题
以以元元素素表表示示物物质质组组成成
在生活中,我们经常会遇到有关物质组成的问题。如食盐、矿泉水、食品和药
物等的包装上会用文字或符号的形式列出其主要的配料成分和含量,它们表示何种
含义?如“加碘盐”“钙片”“补铁剂”中的“碘”“钙”“铁”指的是原子还是
其他?
图3-3-1 某品牌加碘盐、矿泉水中的一些成分及含量
请与同学合作探究下列问题:
1.物质(如食盐、水)是由什么组成的?
2.如何表示物质的组成?
一、元素和元素符号
化学上,把一类具有相同核电荷数(即质子数)的原子统称为元素。例如,
二氧化碳分子中的氧原子,以及水分子或氧分子中的氧原子,都有相同的核电荷
数,因此它们属于同一类氧原子,统称为氧元素。生活中常见的“加碘盐”“钙
片”“补铁剂”中,“碘”“钙”“铁”分别指的是碘元素、钙元素和铁元素。
物质都是由元素组成的。如氧气由氧元素组成,金属铜由铜元素组成,水由氢
化化 学学 65
HHUUAAXXUUEE单元 3 初探物质构成
元素和氧元素组成,二氧化碳由碳元素和氧元素组成,碳酸钙由钙元素、碳元素
和氧元素组成。
阅读理解
理理解解元元素素的的概概念念
物质是由原子、原子结合而成的分子、带电的原子(离子)等微观粒子构成的,
因此物质是由元素组成的。无论是原子还是离子,只要它们原子核的核电荷数相
同,它们就是同一种元素。如钠离子和钠原子的核电荷数相等,钠离子和钠原子
均属于钠元素;镁条在氧气中燃烧生成氧化镁,镁条中的镁原子和氧化镁中的镁
离子都属于镁元素;氧分子中的氧原子和氧化镁中的氧离子都属于氧元素。
还有一类原子,其原子核内质子的数目相同,但中子的数目不同,这类原子也属
于同一种元素。如一种碳原子的原子核内有6个质子和6个中子,还有一种碳原子的
原子核内有 6 个质子和 8 个中子,这两种碳原子都属于碳元素;又如氢元素有三种
原子,一种氢原子的原子核内只有1个质子[被称为氕(pie),用符号H表示],一
种氢原子的原子核内有1个质子和1个中子 [被称为氘(dao),用符号D表示],还
有一种氢原子的原子核内有1个质子和2个中子[被称为氚(chuan),用符号T表示]。
自然界的氢元素中以氕原子为主,占氢元素的99.98%。
氕(H) 氘(D) 氚(T)
电子
质子
中子
图3-3-2 氢元素中的三种原子
思考并回答下列问题:
1.作为相对原子质量标准的碳原子与碳元素是什么关系?
2.以一种元素为例,说明同一种元素在自然界有不同的存在形式。
为了研究和交流的方便,国际上统一采用元素的拉丁文名称的第一个大写字母
来表示元素。当几种元素拉丁文名称的第一个字母相同时,可再附加一个小写字母
来区别。例如,用C表示碳元素,用Ca表示钙元素,用S表示硫元素,用Si表示
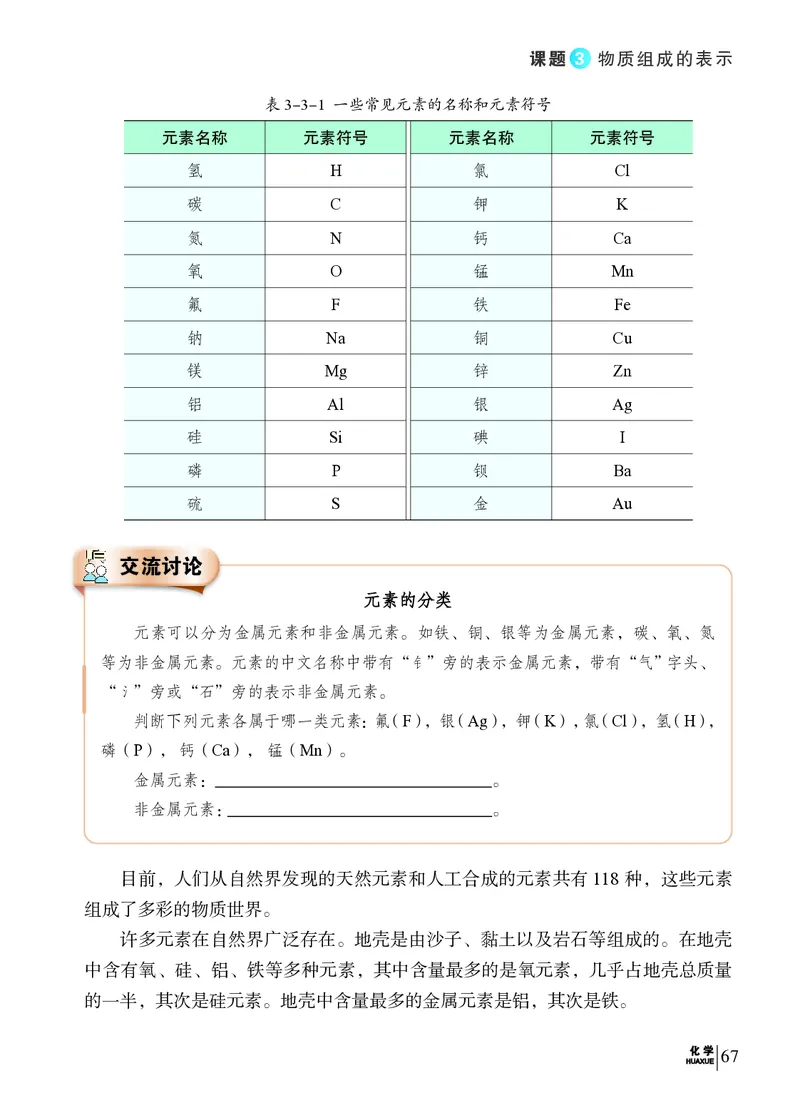
硅元素等。这种符号叫做元素符号。一些常见元素的名称和元素符号见表3-3-1。
66 化化 学学
HHUUAAXXUUEE课题 3 物质组成的表示
表3-3-1 一些常见元素的名称和元素符号
元素名称 元素符号 元素名称 元素符号
氢 H 氯 Cl
碳 C 钾 K
氮 N 钙 Ca
氧 O 锰 Mn
氟 F 铁 Fe
钠 Na 铜 Cu
镁 Mg 锌 Zn
铝 Al 银 Ag
硅 Si 碘 I
磷 P 钡 Ba
硫 S 金 Au
交流讨论
元元素素的的分分类类
元素可以分为金属元素和非金属元素。如铁、铜、银等为金属元素,碳、氧、氮
等为非金属元素。元素的中文名称中带有“钅”旁的表示金属元素,带有“气”字头、
“氵”旁或“石”旁的表示非金属元素。
判断下列元素各属于哪一类元素:氟(F), 银(Ag), 钾(K) ,氯(Cl), 氢(H),
磷(P), 钙(Ca), 锰(Mn)。
金属元素: 。
非金属元素: 。
目前,人们从自然界发现的天然元素和人工合成的元素共有 118 种,这些元素
组成了多彩的物质世界。
许多元素在自然界广泛存在。地壳是由沙子、黏土以及岩石等组成的。在地壳
中含有氧、硅、铝、铁等多种元素,其中含量最多的是氧元素,几乎占地壳总质量
的一半,其次是硅元素。地壳中含量最多的金属元素是铝,其次是铁。
化化 学学 67
HHUUAAXXUUEE单元 3 初探物质构成
海洋的主要成分是水,还含有许多可溶性盐。海水中除了含有大量的氧、氢
元素,还含有氯、钠、镁等 80 多种元素。海水是人类重要的资源宝库,人们可以
通过化学方法从海水中获得许多物质。
人体中含有大量的水,所以含有大量的氧、氢元素。人体中还含有许多有机
化合物,碳、氢、氧、氮是组成这些有机化合物的主要元素。除此之外,人体中
还含有钙、磷、铁、锌等元素,它们在人体的健康中发挥着十分重要的作用。
内核
外核
地幔
地壳
图3-3-3 地壳、海水、人体中主要元素的含量
阅读理解
门门捷捷列列夫夫与与元元素素周周期期表表
门捷列夫是俄国著名的化学家。他在批判地继承前人工作的
基础上,对大量实验事实进行了修正、分析和概括,总结出这样一
条规律:元素的性质随着相对原子质量的递增呈现周期性的变化。
根据这一规律,他将已经发现的63种元素以表的形式排列,编制
了第一个元素周期表。门捷列夫还在表中留下空位,并预测了一
些未知元素的性质,为新元素的探索提供了一个可遵循的规律。
图3-3-4 门捷列夫
在门捷列夫元素周期表的基础上,化学家们又进行了大量
的研究工作,发现元素的性质随着元素原子序数的递增呈现周期性变化(即元素
周期律),并在元素周期律的指导下发现及合成了许多新元素。现代元素周期
表(见附录 4)共有 7 行(称为周期)、18 列(称为族),按元素原子序数递增
的顺序排列了 118 种元素。
阅读上述材料,对照附录4中的元素周期表,与同学讨论下列问题。
1.在元素周期表中找一找常见的元素,说说它们在周期表中的位置。
2.在元素周期表中找出钠(Na)、碳(C)、氧(O)和氯(Cl)等元素,说说周
期表能给出这些元素的哪些信息。
68 化化 学学
HHUUAAXXUUEE课题 3 物质组成的表示
二、纯净物的组成与表示
就像音乐中一套音符可以谱写出无数的乐章那样,一百多种元素以不同的方式
结合,组成了地球上的上亿种物质。如氧元素可以组成氧气(O ),也可以组成臭
2
氧(O );碳、氧两种元素可以组成一氧化碳(CO),也可以组成二氧化碳
3
(CO );氢、氧两种元素可以组成水(H O),也可以组成过氧化氢(H O )。碳、
2 2 2 2
氢、氧等元素可以通过不同的方式组合形成多种多样的有机化合物,如甲烷、乙醇等。
甲烷 乙醇
图3-3-5 甲烷、乙醇分子的结构模型
人们常依据组成纯净物的元素种类,将纯净物分为单质和化合物。由一种元素
组成的纯净物属于单质。由两种或两种以上的元素组成的纯净物属于化合物。如果
化合物仅由两种元素组成,且其中一种是氧元素,则称这类化合物为氧化物。
交流讨论
常常见见物物质质的的分分类类
下列物质是生活中或实验室中常见的纯净物,请对它们进行分类,与同学交流讨
论你分类的结果,并填写在下列表格中。
氧气(O ) 水(H O) 铁(Fe) 二氧化碳(CO )
2 2 2
氮气(N ) 红磷(P) 氯化钠(NaCl) 过氧化氢(H O )
2 2 2
四氧化三铁(Fe O ) 高锰酸钾(KMnO ) 五氧化二磷(P O )
3 4 4 2 5
纯净物的种类 实例
单质
化合物
氧化物
化化 学学 69
HHUUAAXXUUEE单元 3 初探物质构成
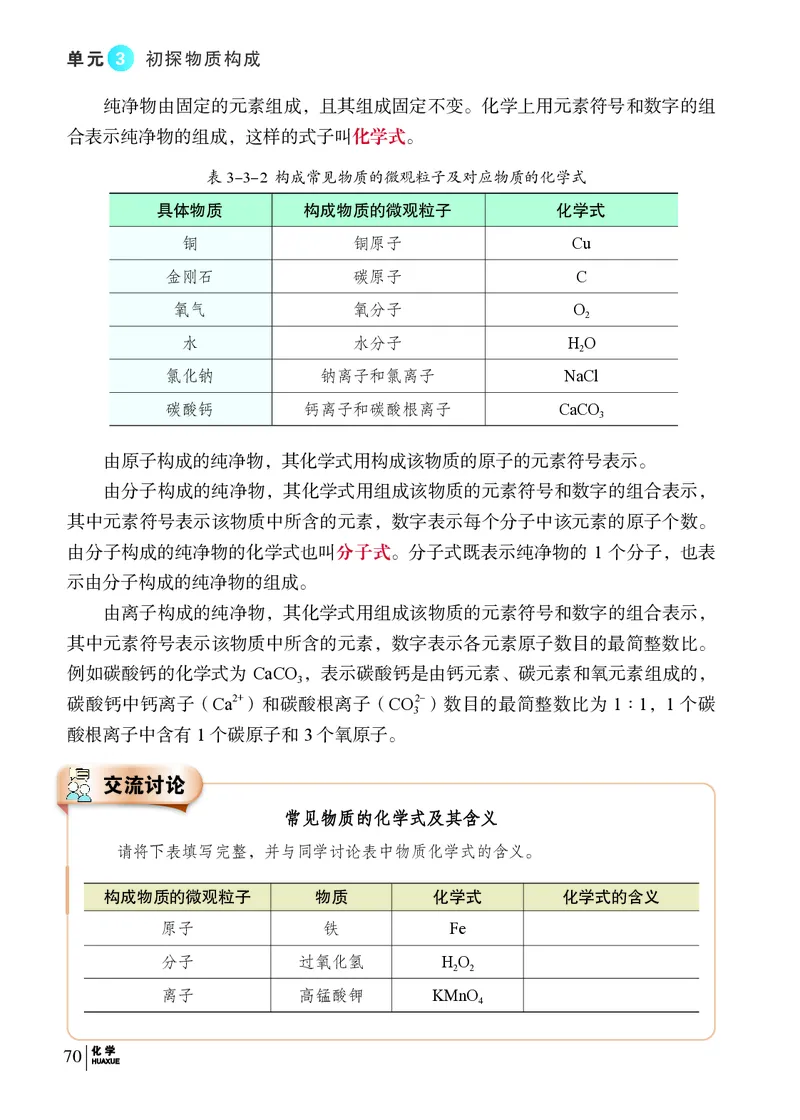
纯净物由固定的元素组成,且其组成固定不变。化学上用元素符号和数字的组
合表示纯净物的组成,这样的式子叫化学式。
表3-3-2 构成常见物质的微观粒子及对应物质的化学式
具体物质 构成物质的微观粒子 化学式
铜 铜原子 Cu
金刚石 碳原子 C
氧气 氧分子 O
2
水 水分子 H O
2
氯化钠 钠离子和氯离子 NaCl
碳酸钙 钙离子和碳酸根离子 CaCO
3
由原子构成的纯净物,其化学式用构成该物质的原子的元素符号表示。
由分子构成的纯净物,其化学式用组成该物质的元素符号和数字的组合表示,
其中元素符号表示该物质中所含的元素,数字表示每个分子中该元素的原子个数。
由分子构成的纯净物的化学式也叫分子式。分子式既表示纯净物的 1 个分子,也表
示由分子构成的纯净物的组成。
由离子构成的纯净物,其化学式用组成该物质的元素符号和数字的组合表示,
其中元素符号表示该物质中所含的元素,数字表示各元素原子数目的最简整数比。
例如碳酸钙的化学式为 CaCO ,表示碳酸钙是由钙元素、碳元素和氧元素组成的,
3
碳酸钙中钙离子(Ca2+)和碳酸根离子(CO2-)数目的最简整数比为 1∶1,1 个碳
3
酸根离子中含有 1 个碳原子和 3 个氧原子。
交流讨论
常常见见物物质质的的化化学学式式及及其其含含义义
请将下表填写完整,并与同学讨论表中物质化学式的含义。
构成物质的微观粒子 物质 化学式 化学式的含义
原子 铁 Fe
分子 过氧化氢 H O
2 2
离子 高锰酸钾 KMnO
4
70 化化 学学
HHUUAAXXUUEE课题 3 物质组成的表示
大量事实表明,化合物都有固定的组成,任一化合物的组成元素都有确定的
原子个数比。
化学上用元素的化合价来体现化合物中不同元素的原子相互化合时具有确定的
原子个数比的性质。化合物中元素的化合价有正、有负,且化合物中元素的正、负
化合价的代数和为0。 在化合物中H 通常为 +1 价,Na 通常为 +1 价,O 通常为-2 价,
Cl 通常为-1 价。
在含有原子团的化合物中,无论是构成化合物还是参与化学反应,原子团都是
作为一个整体出现的,化学上称这些原子团为“根”,如 OH-叫氢氧根、CO2- 叫碳
3
酸根、NH+叫铵根等,“根”也有固定的化合价。
4
元素的化合价是用于描述“化合物”中不同元素的原子相互化合时具有确定的
原子个数比的性质,所以规定单质中元素的化合价为零。常见元素和原子团的主要
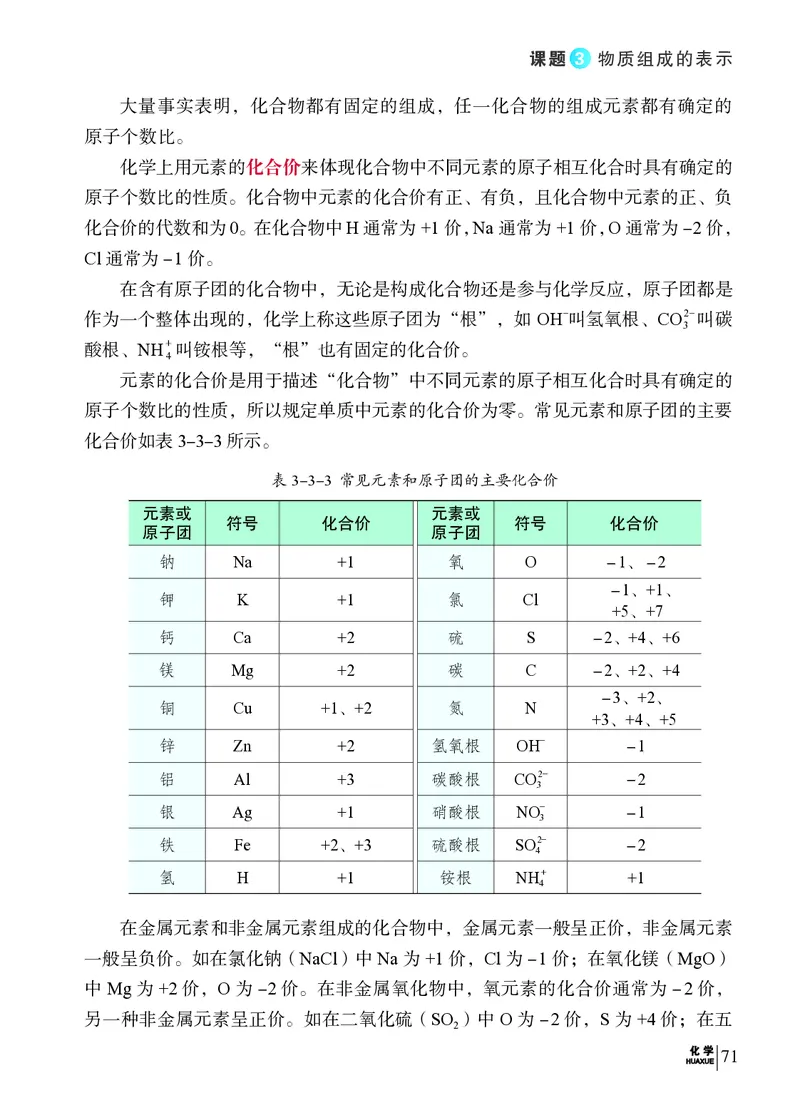
化合价如表 3-3-3所示。
表3-3-3 常见元素和原子团的主要化合价
元素或 元素或
符号 化合价 符号 化合价
原子团 原子团
钠 Na +1 氧 O -1、-2
-1、+1、
钾 K +1 氯 Cl
+5、 +7
钙 Ca +2 硫 S -2、+4、+6
镁 Mg +2 碳 C -2、+2、+4
-3、+2、
铜 Cu +1、+2 氮 N
+3、+4、+5
锌 Zn +2 氢氧根 OH- -1
铝 Al +3 碳酸根 CO2- -2
3
银 Ag +1 硝酸根 NO- -1
3
铁 Fe +2、+3 硫酸根 SO2- -2
4
氢 H +1 铵根 NH+ +1
4
在金属元素和非金属元素组成的化合物中,金属元素一般呈正价,非金属元素
一般呈负价。如在氯化钠(NaCl)中 Na 为 +1 价,Cl 为-1 价;在氧化镁(MgO)
中 Mg 为 +2 价,O 为-2 价。在非金属氧化物中,氧元素的化合价通常为-2 价,
另一种非金属元素呈正价。如在二氧化硫(SO )中 O 为-2 价,S 为 +4 价;在五
2
化化 学学 71
HHUUAAXXUUEE单元 3 初探物质构成
氧化二磷(P O )中O为-2价,P为+5价。
2 5
有些元素在不同的化合物中呈不同的化合价。如在水(H O)中 O 为-2 价,
2
在过氧化氢(H O )中 O 为-1 价;在氧化亚铁(FeO)和硫酸亚铁(FeSO )
2 2 4
中 Fe 为 +2 价,在氧化铁(Fe O )和硫酸铁 [ Fe (SO ) ] 中 Fe 为 +3 价。
2 3 2 4 3
有了元素的化合价,我们可以很方便地写出实际存在的化合物的化学式。根据
元素化合价书写化合物的化学式要遵守如下原则:
1. 一般正价元素(或原子团)的符号写在左边,负价元素(或原子团)的符号
写在右边。原子的数目(或原子个数的最简整数比)用阿拉伯数字写在元素符号的
右下角(原子数目或原子个数比为1时不需要标出数字)。
2. 化合物中各元素正、负化合价的代数和等于零。
交流讨论
化化合合物物中中元元素素化化合合价价的的确确定定和和化化学学式式的的书书写写
1.根据化合物中元素正、负化合价的代数和等于零的原则,写出下列化合物中元
素或原子团的化合价。
H O CO SO HCl HNO MgO Al O Ca(OH) KCl Na CO
2 2 2 3 2 3 2 2 3
2.写出下列物质的化学式,与同学交流讨论你书写化学式的方法。
二氧化氮 氯化铁 氯化亚铁 硫酸铜 硫酸铵 三氧化二铁
方法引导
常见简单化合物的中文命名
1. 对于由两种元素组成的化合物,通常按照化学式从右到左读出元素的名称,中
间用“化”字连接。如 KCl 的中文名称为氯化钾,MgO 的中文名称为氧化镁。
2. 部分由两种元素组成的化合物,除从右到左读出元素的名称,原子的个数也要在
元素的名称之前读出。如 CO 的中文名称为二氧化碳,PO 的中文名称为五氧化二磷。
2 2 5
3. 含有原子团的化合物,从右到左读出原子团或元素的名称,原子团和元素名称之
间用“化”字连接,如Ca(OH) 的中文名称为氢氧化钙,NHCl 的中文名称为氯化铵,
2 4
当原子团为某酸根时,则省略掉“化”字,如 NaCO 的中文名称为碳酸钠。
2 3
72 化化 学学
HHUUAAXXUUEE课题 3 物质组成的表示
三、定量认识物质的组成
纯净物具有固定的组成,因此,化合物中各元素之间有固定的质量比。根据表
示化合物组成的化学式,可以计算出化合物中各元素的质量比,也可以计算出化合
物中某元素的质量在化合物总质量中所占的质量分数。
计算水(H O)中各元素的质量比:
2
氢、氧元素的质量比=(H的相对原子质量×2):(O的相对原子质量×1)
=(1×2):(16×1)
= 1 : 8
计算水(H O)中氢元素的质量分数:
2
H 的相对原子质量×H 的原子个数
水中氢元素的质量分数 = —————————————————×100%
H O的相对分子质量
2
1×2
= — — — ×100%
18
≈ 11%
联系实际
计计算算几几种种氮氮肥肥中中氮氮元元素素的的质质量量分分数数
硫酸铵 [(NH ) SO ]、硝酸铵(NH NO )和碳酸氢铵(NH HCO )都是氮肥,请
4 2 4 4 3 4 3
通过计算说明哪种氮肥的含氮量最高?
化化 学学 73
HHUUAAXXUUEE单元 3 初探物质构成
练习实践
1.甘油(C H O )的保湿作用在生活中具有广泛应用。下列关于甘油的说法不正
3 8 3
确的是( )。
A.甘油由三种元素组成
B.甘油的相对分子质量为(12×3 + 1×8 + 16×3)
C.甘油分子中碳、氢、氧三种原子的个数比为3 ∶ 8∶ 3
12
D.甘油中碳元素的质量分数为 — — — — ×100%
12+1+16
2.甲烷、二氧化硫和臭氧虽然在大气中含量很低,但对空气质量有很大的影响。
(1)写出三种物质的化学式。
(2)说明这三种物质各由哪些元素组成。
(3)分析这三种物质的化学式中包含的信息。
3.使用元素周期表,指出下列元素原子的核电荷数与核外电子数。
(1)氧(O) 。
(2)硫(S) 。
(3)硅(Si) 。
(4)氩(Ar) 。
4.含不同价态的铁的化合物有不同的用途。高铁酸钠(Na FeO )是一种常用的“绿
2 4
色环保高效”消毒剂,其中铁元素的化合价为 ;氯化铁(FeCl )常用作水的
3
净化剂,其中铁元素的化合价为 ;氯化亚铁(FeCl )是补铁类药物的合成原
2
料,其中铁元素的化合价为 。
5.已知尿素的化学式为CO(NH ) ,试计算:
2 2
(1)尿素的相对分子质量 。
(2)尿素中C 、O 、N 、H 的质量比 。
(3)尿素中氮元素的质量分数 。
(4)尿素中各元素化合价的代数和为 。
74 化化 学学
HHUUAAXXUUEE单元小结
单元小结
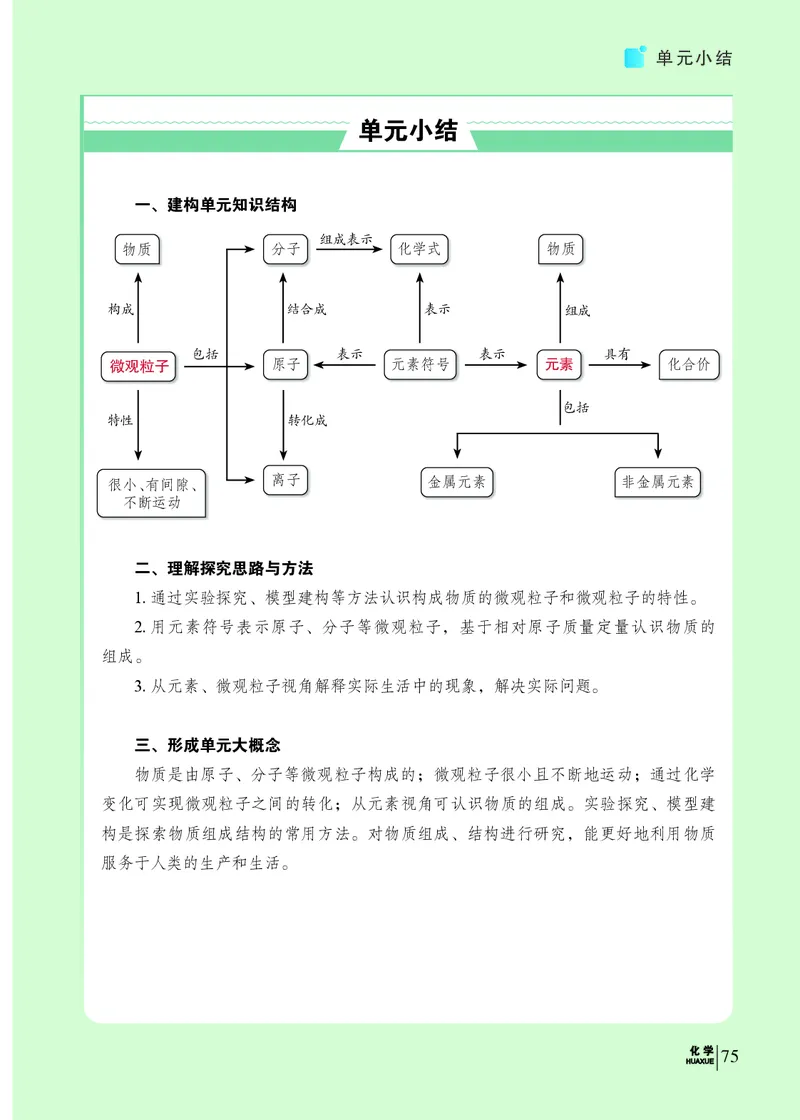
一、建构单元知识结构
组成表示
物质 分子 化学式 物质
构成 结合成 表示 组成
包括 表示 表示 具有
微观粒子 原子 元素符号 元素 化合价
包括
特性 转化成
很小、有间隙、 离子 金属元素 非金属元素
不断运动
二、理解探究思路与方法
1.通过实验探究、模型建构等方法认识构成物质的微观粒子和微观粒子的特性。
2.用元素符号表示原子、分子等微观粒子,基于相对原子质量定量认识物质的
组成。
3.从元素、微观粒子视角解释实际生活中的现象,解决实际问题。
三、形成单元大概念
物质是由原子、分子等微观粒子构成的;微观粒子很小且不断地运动;通过化学
变化可实现微观粒子之间的转化;从元素视角可认识物质的组成。实验探究、模型建
构是探索物质组成结构的常用方法。对物质组成、结构进行研究,能更好地利用物质
服务于人类的生产和生活。
化化 学学 75
HHUUAAXXUUEE单元作业
单元作业
1.构成物质的微观粒子有分子、原子、离子等。下列物质由原子构成的是( )。
K+
OH-
A.氢氧化钾 B.二氧化碳 C.水 D.硅
2.含有“氚”的核废水直接排放会对人类生存环境造成一定的影响。氚原子核内
含有1个质子和2个中子,其原子的核外电子数是( )。
A. 1 B. 2 C. 3 D. 6
3. 2020年6月23日,我国北斗三号全球卫星导航系统星座部署完美收官。该导
航系统应用了星载氢原子钟和铷原子钟。查阅元素周期表,分析下列有关铷的说法错
误的是( )。
A.属于金属元素 B.元素符号是Rb
C.相对原子质量为85.47 D. Rb+核外电子数为37
4.写出下列元素氧化物的化学式或根据化学式标出元素的化合价(提示:元素符
号上方的数字表示该元素在氧化物中的化合价)。
+1 +2 +4
K C S
+5 +1 +2
N Na Fe
一氧化氮(NO) 二氧化氮(NO )
2
一氧化二氮(N O) 三氧化二氮(N O )
2 2 3
5.用合适的符号表示。
(1)硫元素 。
(2)1个硫原子 。
(3)一个分子中含有8个硫原子的硫分子 。
(4)硫原子得到2个电子后形成的硫离子 。
(5)SO 中硫元素的化合价为+4价 。
2
(6)-2价的硫元素和+3价的铁元素形成的化合物的化学式 。
6.花青素(C H O )具有缓解疲劳、保护视力的作用。该物质主要来源于各种蔬
15 11 6
76 化化 学学
HHUUAAXXUUEE单元作业
菜和水果。请回答下列问题。
(1)一个花青素分子中共有 个原子。
(2)花青素分子中碳、氧元素的质量比为 。
(3)花青素的相对分子质量为 。
(4)花青素中氧元素的质量分数为 。
7.大气的对流层中的污染物臭氧(O )有多种产生的途径。其中一种途径是在阳
3
阳光
光照射下,NO 转化为NO和O,即NO NO + O;生成的氧原子再与氧分子结
2 2
合形成臭氧,即O + O → O 。
2 3
(1)晚上对流层中臭氧的浓度较低,解释其原因。
(2)在上述途径的第二步中,出现了三种不同形式的氧,请分析其相同点与差异
之处。
8.观察表1中各物质的密度,回答问题。
表1
物质 密度/(g ·· cm-3)
氮气 1.17×10-3(常温、常压)
氧气 1.33×10-3(常温、常压)
铜 8.92
锌 7.14
(1)从微观粒子的视角出发,解释为何两种固体的密度比两种气体的密度大
得多。
(2)从微观粒子的视角出发,解释为何在描述两种气体的密度时,要指明温度和
压强。
9.钙是人体必需的常量元素,每日必须摄入足够量的钙。目前市场上的补钙药剂
很多。图1是某种品牌的补钙药品的部分说明书。请回答下列问题。
(1)碳酸钙(CaCO )中钙元素的质量分数是
3
XX钙片
多少?
【药品规格】每片含碳酸钙0.625 g
【用量】每次一片,每天两次
(2)如果按此钙片规定用量,每天从钙片中摄
入的钙元素的质量是多少?
图1
化化 学学 77
HHUUAAXXUUEE项目学习
项目学习
情情景景剧剧::一一个个水水分分子子
项目背景
水是人类宝贵的资源,对人类和其他生物的生存、工农业生产具有极其重要的作
用。本项目通过编写“一个水分子”的情景剧剧本,帮助大家进一步从元素、微观粒
子视角认识水的组成和构成,并结合生产和生活实际认识水的性质和用途,形成节约
用水、保护水资源的意识。
项目建议方案
1. 查阅资料。(1)查阅资料了解水的组成元素和微观粒子构成,了解水在自然界
的存在、循环及变化,了解水的性质与应用,了解水的污染及治理、水灾和水荒等;
(2)查阅资料了解情景剧剧本的创作方法。
2. 创作剧本。用拟人的方式,以“一个水分子的旅行”“一个水分子的过去与将
来”“从大海中来的一个水分子”“无处不在的水分子”等为主题,创作“一个水分子”
的情景剧,与小组同学讨论,修改并完善情景剧剧本。
3. 表演实践。与同学合作表演情景剧,在表演过程中继续优化剧本。
4. 成果展示。将“一个水分子”的情景剧剧本和该剧的表演视频在全班进行展示
与交流。
78 化化 学学
HHUUAAXXUUEE单元 4 再探燃烧与燃料
课题 1 燃烧与灭火
情境问题
燃燃烧烧的的利利用用与与控控制制
人类的生产生活离不开燃烧,如食物的烹饪、金属的冶炼、火箭的升空等。但
某些情形下的燃烧也会给人类带来灾难,如森林大火、天然气爆炸等。如何科学地
利用和控制燃烧?
通过对下列问题的探究,我们可以找到答案。
1. 物质燃烧需要哪些条件?
2. 如何控制燃烧的发生和停止?
图4-1-1 生产生活中燃烧的利用与控制
一、物质燃烧的条件
物质燃烧是生产和生活中的一种常见现象,也是一种化学变化。人们常利用燃
烧获取热量,但物质燃烧是有条件的。
实验探究
物物质质燃燃烧烧的的条条件件
【提出问题】通过对生活中燃烧现象的分析,可以提出如下问题:是否所有物质
都能燃烧?隔绝空气的条件下物质能否燃烧?为什么有些物质很容易燃烧,而有些物
质需要在很高的温度下才能燃烧?
80 化化 学学
HHUUAAXXUUEE课题 1 燃烧与灭火
【形成猜想】对 这些问题你的猜想是 。
你提出猜想的依据是 。
【设计方案】请根据你的猜想设计实验方案。
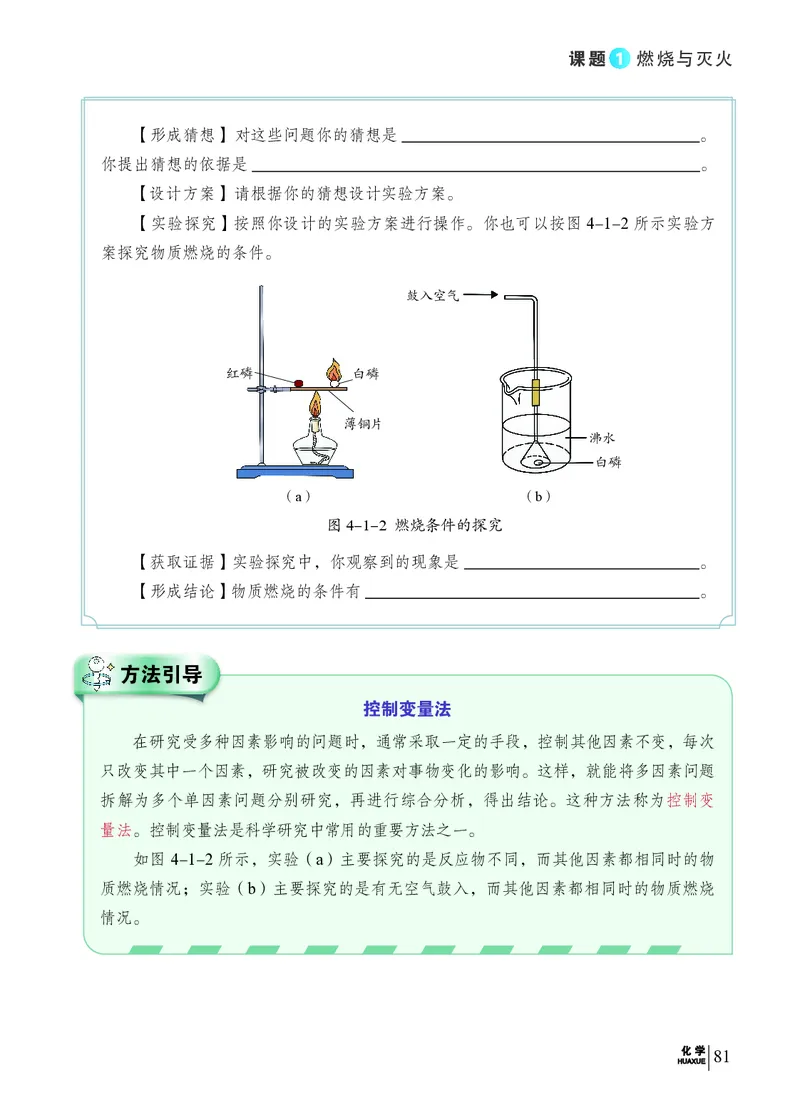
【实验探究】按照你设计的实验方案进行操作。你也可以按图4-1-2所示实验方
案探究物质燃烧的条件。
鼓入空气
红磷 白磷
薄铜片
沸水
白磷
(a) (b)
图4-1-2 燃烧条件的探究
【获取证据】实验探究中,你观察到的现象是 。
【形成结论】物质燃烧的条件有 。
方法引导
控制变量法
在研究受多种因素影响的问题时,通常采取一定的手段,控制其他因素不变,每次
只改变其中一个因素,研究被改变的因素对事物变化的影响。这样,就能将多因素问题
拆解为多个单因素问题分别研究,再进行综合分析,得出结论。这种方法称为控制变
量法。控制变量法是科学研究中常用的重要方法之一。
如图 4-1-2 所示,实验(a)主要探究的是反应物不同,而其他因素都相同时的物
质燃烧情况;实验(b)主要探究的是有无空气鼓入,而其他因素都相同时的物质燃烧
情况。
化化 学学 81
HHUUAAXXUUEE单元 4 再探燃烧与燃料
燃烧是一种发光、放热的剧烈的化学反应。在通常情
温
况下,物质燃烧必须同时满足三个条件(图 4-1-3):一
度
达
氧
是物质具有可燃性;二是可燃物与氧气(或空气)接触; 气 到
着
火
三是温度达到该物质燃烧所需的最低温度(也叫着火点)。 点
可燃物
图4-1-3 燃烧条件示意图
表4-1-1 通常状况下一些常见物质的着火点
可燃物 着火点/℃ 可燃物 着火点/℃ 可燃物 着火点/℃
白磷 40 硫 260 木炭 320 ~ 370
红磷 240 木材 250 ~ 330 无烟煤 700 ~ 750
交流讨论
氧氧气气浓浓度度对对燃燃烧烧程程度度的的影影响响
家用燃气燃烧充分时,会出现蓝色火焰;燃烧不充分时,则会出现黄色火焰,锅
底也会附着黑色物质。
(a) (b)
图4-1-4 氧气充足(a)和不充足(b)时天然气的燃烧情况
结合燃烧的条件以及日常经验,与同学交流讨论:氧气浓度对可燃物燃烧程度有
哪些影响?
一般情况下,氧气的浓度越高,燃烧越剧烈。当氧气充足时,可燃物完全
燃烧,燃烧速率快,放出的热量多;氧气不充足时,可燃物不完全燃烧,燃烧
速率慢,放出的热量少。可燃物完全燃烧和不完全燃烧时的现象不同,反应产物
也可能不同。例如,焦炭、木炭完全燃烧生成二氧化碳,当发生不完全燃烧时有
一氧化碳生成。
82 化化 学学
HHUUAAXXUUEE课题 1 燃烧与灭火
点燃
C + O (不充足) CO
2
含碳、氢元素的燃料完全燃烧时生成二氧化碳和水,不完全燃烧时除生成
二氧化碳和水,还会生成一氧化碳、碳氢化合物等有毒气体和微小的炭黑颗粒
等物质。
燃料不完全燃烧不仅浪费能源,而且产物中的有毒气体会损害人类健康、污染
大气,炭黑颗粒的沉积也会对燃烧装置系统产生不良影响。为使燃料完全燃烧,工
业上常把煤炭粉碎以增大与空气接触的面积,并对锅炉进行鼓风以增加空气的供
给。汽车发动机将汽油、柴油等喷成雾状进行燃烧,也是为了使燃料能够在有限的
空间和时间内完全燃烧。
二、缓慢氧化与爆炸
物质与氧气的反应有的很剧烈,有的很缓慢。如铁生锈、食物腐败等反应很缓
慢,而可燃性气体或粉尘的爆炸等很剧烈。
交流讨论
暖暖足足贴贴为为什什么么会会““发发热热””
暖足贴是一种贴在脚底用于取暖的产品,铁粉是暖足
贴的主要成分。请查阅资料或请教使用过暖足贴产品的
人,然后与同学讨论下列问题:
1.暖足贴产品采用真空包装,这是为什么?
2.使用时撕去外包装贴在脚底,暖足贴便能持续发
热,这又是为什么? 图4-1-5 暖足贴
室温下,铁在空气中与氧气等物质发生的氧化反应速率较慢,不易察觉,像这
种缓慢进行的氧化反应称为缓慢氧化。食物腐败、酒和醋的酿造、农家肥料的腐熟
等都包含缓慢氧化过程。物质缓慢氧化时也会放热,如果热量长时间聚积,最终使
温度达到可燃物的着火点时,可燃物便会自动燃烧。这种由缓慢氧化所引起的自动
燃烧叫做自燃。堆放的稻草、煤炭、粉状金属、棉纱或其他易燃物等,在没有明火
的情况下也可能发生自燃就是这个原因。因此,存放易燃物时,不能堆放过高、
化化 学学 83
HHUUAAXXUUEE单元 4 再探燃烧与燃料
过密,时间也不宜过长,并且要定期进行防火检查。
可燃物如果在有限的空间内急剧燃烧,就会在短时间内聚积大量的热,使气体
的体积迅速膨胀从而引起爆炸。
观察思考
氢氢气气的的燃燃烧烧与与爆爆炸炸
实实验验1 如图4-1-6所示,将从导管中排出的纯净氢气点燃,在火焰上方罩1个
冷而干燥的烧杯,观察现象。
实实验验2 如图4-1-7所示,取1个纸杯,在底部开一小孔,倒置在实验桌上,用
纸团堵住小孔,先收集满氢气,然后把氢气发生装置移开,拿掉堵小孔的纸团,用燃
着的长木条在小孔处点燃氢气,观察现象。
氢气
图4-1-6 氢气的燃烧 图4-1-7 氢气的爆炸
实验 实验现象和结论 化学反应文字表达式
1
2
思考与交流
上述两个实验都是氢气的燃烧反应,为什么现象不同?
实验表明,纯净的氢气在空气中点燃会安静地燃烧并生成水,而混有氧气的氢
气遇到明火可能会发生爆炸。
可燃物(如气体、粉尘等)如果在空气中分散达到一定的浓度,与氧气的接触
面积就会很大,遇明火时与氧气反应就会迅速放出大量的热,使周围的气体迅速猛
烈膨胀而发生爆炸。
84 化化 学学
HHUUAAXXUUEE课题 1 燃烧与灭火
阅读理解
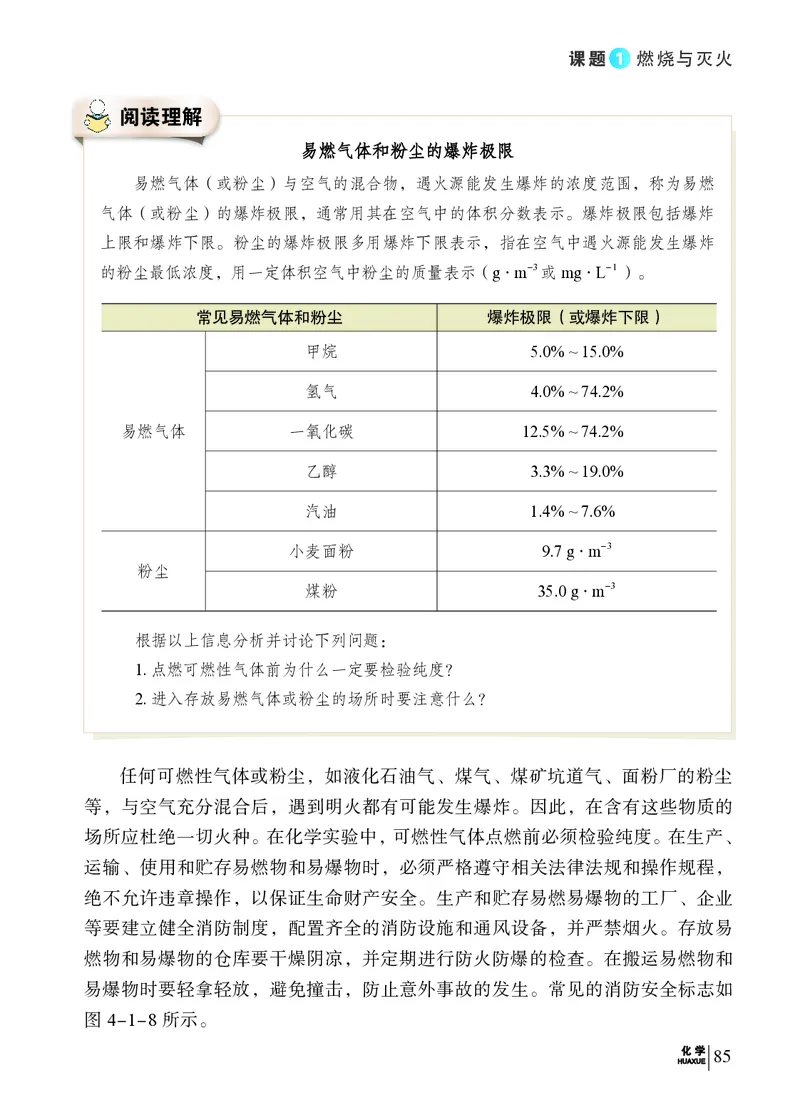
易易燃燃气气体体和和粉粉尘尘的的爆爆炸炸极极限限
易燃气体(或粉尘)与空气的混合物,遇火源能发生爆炸的浓度范围,称为易燃
气体(或粉尘)的爆炸极限,通常用其在空气中的体积分数表示。爆炸极限包括爆炸
上限和爆炸下限。粉尘的爆炸极限多用爆炸下限表示,指在空气中遇火源能发生爆炸
的粉尘最低浓度,用一定体积空气中粉尘的质量表示(g ·· m-3 或mg ·· L- 1 )。
常见易燃气体和粉尘 爆炸极限(或爆炸下限)
甲烷 5.0% ~ 15.0%
氢气 4.0% ~ 74.2%
易燃气体 一氧化碳 12.5% ~ 74.2%
乙醇 3 .3% ~ 19.0%
汽油 1.4% ~ 7.6%
小麦面粉 9.7 g ·· m-3
粉尘
煤粉 35.0 g ·· m-3
根据以上信息分析并讨论下列问题:
1.点燃可燃性气体前为什么一定要检验纯度?
2.进入存放易燃气体或粉尘的场所时要注意什么?
任何可燃性气体或粉尘,如液化石油气、煤气、煤矿坑道气、面粉厂的粉尘
等,与空气充分混合后,遇到明火都有可能发生爆炸。因此,在含有这些物质的
场所应杜绝一切火种。在化学实验中,可燃性气体点燃前必须检验纯度。在生产、
运输、使用和贮存易燃物和易爆物时,必须严格遵守相关法律法规和操作规程,
绝不允许违章操作,以保证生命财产安全。生产和贮存易燃易爆物的工厂、企业
等要建立健全消防制度,配置齐全的消防设施和通风设备,并严禁烟火。存放易
燃物和易爆物的仓库要干燥阴凉,并定期进行防火防爆的检查。在搬运易燃物和
易爆物时要轻拿轻放,避免撞击,防止意外事故的发生。常见的消防安全标志如
图 4-1-8 所示。
化化 学学 85
HHUUAAXXUUEE单元 4 再探燃烧与燃料
禁止烟火 禁止带火种 当心火灾——易燃物质 当心爆炸——爆炸性物质
图4-1-8 常见的消防安全标志
化学史话
黑黑火火药药
黑火药是我国古代“四大发明”之一。黑火药由硝酸钾(KNO )、硫黄粉(S)
3
和木炭粉(C)大致按 15 ∶ 2 ∶ 3 的质量比混合而成。点燃火药包时,首先点燃火药
的引线,当火焰蔓延到火药包内部时,硝酸钾受热分解生成氧气,引发一系列反
应,瞬间产生大量的氮气、二氧化碳等气体,放出大量的热,气体膨胀,产生强烈
的压力,迅猛冲破“外壳”的束缚,发生爆炸,并发出震耳的响声。黑火药爆炸的
主要反应为:
点燃
KNO + C + S K S + CO + N
3 2 2 2
(硝酸钾) (硫化钾)
在日常生产和生活中,人们也会利用爆炸为人类服务。如爆炸产生的巨大能量
可开山炸石、拆除危旧建筑等,重大节日或活动燃放烟花爆竹能烘托欢快的气氛。
建筑爆破 2022年北京冬奥会礼花
图4-1-9 服务于生产生活的爆炸
三、灭火的原理
生活中不需要燃烧继续时,需及时灭火。只要改变物质燃烧的某一个条件,就
能将火熄灭。
86 化化 学学
HHUUAAXXUUEE课题 1 燃烧与灭火
交流讨论
灭灭火火的的方方法法与与原原理理
在日常生活和实验操作中,同学们通常会使用哪些方法灭火?你们还见过哪些灭
火方法?这些方法为什么能灭火?
吹灭蜡烛 熄灭酒精灯火焰 关闭燃气阀门
图4-1-10 常见的灭火情形
1. 将下列灭火实例中的灭火原理填入表格。
灭火实例 灭火原理
吹灭生日蜡烛
用灯帽盖灭酒精灯火焰
关闭燃气阀门以熄灭燃气火焰
用二氧化碳灭火器扑救着火的实验仪器
消防员用高压水枪扑灭大火
消防员把森林大火蔓延路线前的一片树木砍掉,形成隔离带
2. 请通过询问他人、走访消防部门、查阅资料等方式,收集现实生活中不同材料
着火时的灭火方法,并与同学交流讨论你的收获。
灭火的实质就是使燃烧反应不能发生,所以只需破坏燃烧的条件之一即可灭
火,通常有以下方法。
(1)将可燃物撤离燃烧区,与火源隔离。例如,煤气灶起火时,首先要迅速
关闭阀门,以断绝可燃物的来源;扑灭森林火灾时,用设置隔离带的方法将森林中
的树木与燃烧区隔开。
(2)将燃烧着的可燃物与空气隔开。例如,实验时燃着的酒精火焰不慎洒
落在实验台上,可用湿布盖住;厨房油锅起火,盖上锅盖就能灭火;将干沙覆盖
在可燃物表面,也可使可燃物与空气隔绝。
化化 学学 87
HHUUAAXXUUEE单元 4 再探燃烧与燃料
(3)使用大量的冷却剂(如水、干冰等)让可燃物冷却,使温度降低到着火
点以下。
生产和生活中利用燃烧的同时,要注意防范火险,避免火灾带来的破坏和
灾难。在家庭用火时要特别注意及时熄灭火焰;在公共场所要特别注意有无“禁
止烟火”等防火标志,遵守消防规定。
万一遇到火险,不要慌张,要沉着应对。如果火势很小,可根据起火的原因,
采用适当的方法将火扑灭;如果火势较大,或有蔓延的可能,应立即拨打火警电话
“119”;被困在火灾区时,要冷静并采取一定的自救措施,如用湿毛巾或衣物捂
住口鼻,低下身子沿墙壁或贴近地面跑出火灾区,到窗口呼救等。
用科学方法将小火扑灭 拨打火警电话 用湿毛巾捂住口鼻
低身跑出火灾区
图4-1-11 遭遇火灾的自救方法
阅读理解
常常见见火火灾灾类类型型与与灭灭火火器器
火灾场所不同,所用的灭火器也不同。请阅读以下材料并思考:
1.不同灭火器的灭火原理是什么?
2.实验室酒精着火或电器着火引起的火灾分别可选用哪种灭火器?
常见的火灾类型有以下几种:
A类火灾:指固体物质火灾,如木材、纸张、橡胶、塑料等燃烧的火灾。
B类火灾:指液体火灾或可熔化的固体物质火灾,如汽油、柴油、乙醇、乙醚、
沥青、石蜡、油漆等燃烧的火灾。
C类火灾:指气体火灾,如煤气、天然气、氢气等气体燃烧的火灾。
D类火灾:指金属火灾,如钾、钠、镁、铝等活泼金属燃烧的火灾。
E类火灾:指带电火灾,如家电自燃、电源插座起火等引起的火灾。
88 化化 学学
HHUUAAXXUUEE课题 1 燃烧与灭火
F类火灾:烹饪器具内的烹饪物火灾,如动植物油脂燃烧的火灾。
灭火器 灭火原理 适用范围
水基型灭火器经雾化喷嘴,
喷射出细水雾,可快速降低火场 A类、B类和F类
温度,并在可燃物表面形成水膜, 火灾
使可燃物与空气隔离,实现灭火
水基型灭火器
利用二氧化碳或氮气作动力,
将筒内的干粉(主要成分为碳酸
氢钠或磷酸铵盐)喷出,干粉遇
A类、B 类、C 类、
到高温分解,吸收大量的热并放
E类和F类火灾
出水蒸气和二氧化碳,有降温、
隔绝空气及稀释燃烧区空气中氧
干粉灭火器
气的作用
在加压时将液态二氧化碳压
B 类、C 类和E类
缩在小钢瓶中,灭火时将其喷出,
火灾
有降温和隔绝空气的作用
二氧化碳灭火器
主要包括惰性气体灭火剂
(氩气、氮气等)、卤代烃灭火
剂(七氟丙烷、六氟丙烷、三氟 A 类、B 类、C 类、
甲烷)等。在喷射后,这些气体 D 类和E类火灾
能够迅速隔绝氧气,从而达到灭
火的目的
洁净气体灭火器
化化 学学 89
HHUUAAXXUUEE单元 4 再探燃烧与燃料
练习实践
1.用化学知识解释成语 “釜底抽薪”合理的是( )。
A. 隔绝空气 B. 移去可燃物
C. “薪”没有可燃性 D. 使温度降到可燃物着火点以下
2.下列做法存在安全隐患的是( )。
A. 在有明火或热源的区域内不使用含有酒精的消毒剂
B. 在加油站或面粉厂等场所严禁烟火
C. 发现家中燃气泄漏时,先关闭阀门,再开窗通风
D. 炒菜时油锅着火,立即加水灭火
3.解释下列现象。
(1)木柴架空燃烧会更旺。
(2)工厂或企业中原煤堆放场地的地面不宜铺垫空隙较大的物料。
(3)易燃易爆物要轻拿轻放。
(4)棉花易燃烧,而棉花粉尘遇火星易爆炸。
4.中华人民共和国应急管理部批准发布的安全生产行业标准《加油站作业安全规
范》(AQ 3010—2022)规定:作业区人员上岗时应穿防静电工作服、防静电工作鞋,
不应在作业区穿脱及拍打衣服、帽子或类似物;不应在加油站内吸烟;加油作业前,
加油员应确认车辆停稳、熄火。请说说其中的道理。
5.每个人都应懂得防火知识,学会如何逃生。根据所学知识,请和同学交流下列
问题。
(1)如果住房内起火,是否要立即打开所有门窗?为什么?
(2)从火灾中逃生时,常用湿毛巾或衣物捂住口鼻,低下身子沿墙壁或贴近地
面跑出火灾区,这些自救措施所起的作用是什么?
90 化化 学学
HHUUAAXXUUEE课题 2 化学反应中的能量变化
课题 2 化学反应中的能量变化
情境问题
燃燃烧烧中中的的能能量量变变化化
物质燃烧时伴随着发光、放热现象。人们常常利用燃烧中产生的光和热服务于生
产和生活,如金属冶炼、焊接钢轨、制作军用照明弹等。
图4-2-1 化学反应中能量的利用实例
请与同学合作探究下列问题:
1. 是否所有的化学反应都伴随着能量变化?
2. 如何合理利用化学反应中的能量变化?
一、化学反应伴随能量变化
在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化。许多
化学反应中的能量变化主要表现为热量的放出或吸收。
交流讨论
虎虎门门销销烟烟中中的的化化学学
清朝道光年间,为了消除外来鸦片对中国的危害,林则徐下令在虎门海滩当众销
毁收缴的鸦片。据清朝《筹办夷务始末》记载,当时销毁鸦片的方法是:“在海边
挖池,池底铺石,将盐水倒入池中。将烟土倒入池中泡浸半日,后再投入生石灰,水
化化 学学 91
HHUUAAXXUUEE单元 4 再探燃烧与燃料
遇石灰沸腾,烟土溶解。士兵拿木耙不停在池中搅拌,务
求烟土完全溶于水中。退潮时,把池水送入大洋,并用清
水洗刷池底,不留涓滴。”
阅读以上信息,与同学讨论:为什么水遇生石灰(主
要成分为 CaO)便会沸腾?
图4-2-2 林则徐虎门销烟
生石灰与水反应放出大量的热。化学上把有热量放出的反应称为放热反应。放
热反应在生产生活中有着十分广泛的应用。如人利用体内化学反应放出的热量维持
体温,提供机体活动所需要的能量;利用燃料燃烧放出的热量来取暖、煮熟
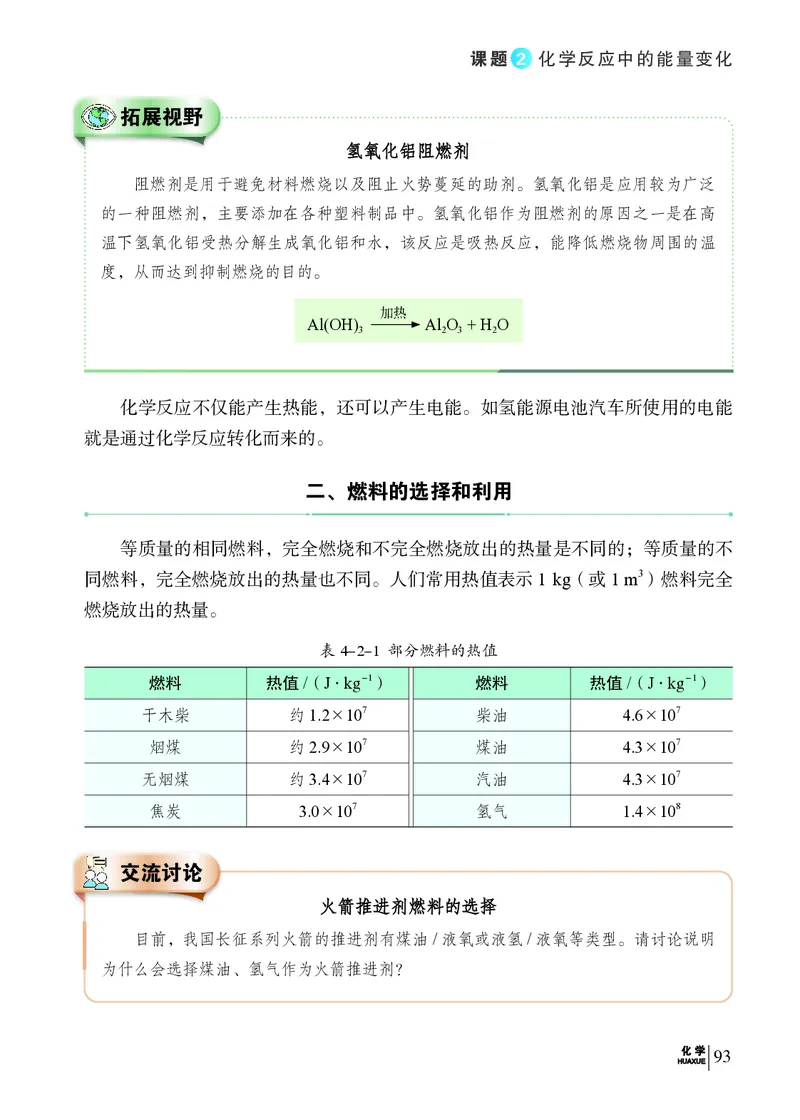
食物、发电、冶炼金属等。火力发电厂通过燃料的燃烧产生热能,再将热能转
化为机械能,机械能再进一步转化为电能,从而实现火力发电。
蒸汽流
涡轮机
发电机 电
沸 冷
热水
腾 凝
器 器
水体
冷水
冷凝水 泵
泵
燃烧器
图4-2-3 火力发电示意图
化学上把吸收热量的反应称为吸热反应。工业中常用水蒸气通过炽热的焦炭生
产水煤气(主要成分是氢气和一氧化碳),这一反应是吸热反应,反应表达式为:
高温
C + H O CO + H
2 2
92 化化 学学
HHUUAAXXUUEE课题 2 化学反应中的能量变化
拓展视野
氢氢氧氧化化铝铝阻阻燃燃剂剂
阻燃剂是用于避免材料燃烧以及阻止火势蔓延的助剂。氢氧化铝是应用较为广泛
的一种阻燃剂,主要添加在各种塑料制品中。氢氧化铝作为阻燃剂的原因之一是在高
温下氢氧化铝受热分解生成氧化铝和水,该反应是吸热反应,能降低燃烧物周围的温
度,从而达到抑制燃烧的目的。
加热
Al(OH) Al O + H O
3 2 3 2
化学反应不仅能产生热能,还可以产生电能。如氢能源电池汽车所使用的电能
就是通过化学反应转化而来的。
二、燃料的选择和利用
等质量的相同燃料,完全燃烧和不完全燃烧放出的热量是不同的;等质量的不
同燃料,完全燃烧放出的热量也不同。人们常用热值表示 1 kg(或 1 m3)燃料完全
燃烧放出的热量。
表4-2-1 部分燃料的热值
燃料 热值/(J ·· kg-1) 燃料 热值/(J ·· kg-1)
干木柴 约1.2×107 柴油 4.6×107
烟煤 约2.9×107 煤油 4.3×107
无烟煤 约3.4×107 汽油 4.3×107
焦炭 3.0×107 氢气 1.4×108
交流讨论
火火箭箭推推进进剂剂燃燃料料的的选选择择
目前,我国长征系列火箭的推进剂有煤油/液氧或液氢/液氧等类型。请讨论说明
为什么会选择煤油、氢气作为火箭推进剂?
化化 学学 93
HHUUAAXXUUEE单元 4 再探燃烧与燃料
选择燃料时不仅需要考虑热值,还需考虑燃料的价格、燃烧产物是否污染环境
等因素。在液体燃料中,煤油不仅热值高,而且密度适宜,燃烧性能好,能
迅速、稳定、连续地完全燃烧,且由于硫含量较低,燃烧产生的污染较少。因此,
煤油是一种优质的液体燃料。氢气的热值是 1.4×108 J ·· kg-1,是目前所有燃料中热
值最高的燃料,且燃烧产物是水,无污染。因此,液氢和液氧的组合是航天飞行的
优良推进剂。但由于氢气沸点很低、分子很小、极易蒸发和逃逸,相应的技术要求
较高,成本也较高。
联系实际
汽汽车车燃燃料料
在加油站,汽车通常可加汽油、柴油等燃料。你知道吗?有些汽车是加天然气的,
2022年北京冬奥会的汽车则是加氢的。请查阅资料,了解不同汽车燃料的优缺点,分
析选择汽车燃料需要考虑的因素,与同学交流你分析的结果。
加油站 加气站 2022年北京冬奥会加氢站
图4-2-4 汽车燃料站
练习实践
1. 关于化学反应中的能量变化,下列说法错误的是( )。
A.化学反应必然伴随着能量变化
B. 化学反应中的能量变化都表现为热量变化
C.一定量的可燃物完全燃烧放出的热量大于不完全燃烧放出的热量
D.化学反应是人类获得所需能量的重要途径
2. 2020 年 5月5日,我国长征五号 B 运载火箭首飞成功,液氢 / 液氧发动机为其
94 化化 学学
HHUUAAXXUUEE课题 2 化学反应中的能量变化
提供部分动力。下列叙述错误的是( )。
A. 液氧用作发动机的燃料 B. 燃料加注时需严禁烟火
C. 液氢与液氧发生的反应是放热反应 D. 液氢和液氧反应的产物无污染
3.判断下列过程是放出热量还是吸收热量。
(1)在室外用木炭进行烧烤。
(2)水从皮肤的表面蒸发。
(3)绿色植物通过光合作用合成葡萄糖。
4.市场上有一种自热火锅,除食材外还配有“发热包”。“发热包”中混合物的
主要成分之一是生石灰(CaO),使用时放入“发热包”并加入凉水即可加热食材。
请说明“发热包”的工作原理。
5.燃油车(燃料通常为汽油)可改装为燃气车(燃料为天然气),改装前后燃料
消耗信息对比见表1。
表1
燃料 单价 每100 km消耗 每日行驶里程
汽油(92 #) 8.3 元 ·· L-1 9 L 300 km
天然气 4.5 元 ·· m-3 8.4 m3 300 km
一辆出租车的改装费大约为6 000元。某出租车司机正在犹豫是否对出租车进行
改装,你对他有何建议?理由是什么?
化化 学学 95
HHUUAAXXUUEE单元 4 再探燃烧与燃料
课题 3 化石燃料的综合利用与新能源开发
情境问题
人人类类对对能能源源的的开开发发利利用用
薪柴是人类使用的第一代能源。当前人类利用的能源以煤、石油、天然气等化石
燃料为主,并正在开发以清洁、低碳、安全、高效为核心的“新能源”体系。
请与同学合作探究下列问题:
1.人类可利用的化石燃料有哪些?化石燃料用作燃料存在哪些问题?
2.化石燃料除了燃烧,还可以怎么利用?
3.人类可以开发和利用哪些新能源?
一、认识化石燃料
早在 2 000 多年前的春秋战国时期,我国就已开始将煤炭作为燃料使用,但由
于当时生产力水平低下,人类对于煤炭的开采获取能力十分有限。第一次工业革
命后,煤炭以热值高、分布广等优点成为全球第一大能源。20 世纪 60 年代,
由于石油、天然气等具有热值更高、更易运输等特点,油气能源时代开启。
煤、石油和天然气是由深埋于地 岩石、泥土
微生物
下的古代动植物遗体,经过漫长的、 煤
高温高压
一系列非常复杂的变化而逐渐形成 岩石
的,它们常被称为化石燃料。化石燃 古代森林植物
料要经过数百万年才能形成,是短期 天然气
微生物 石油
内不可再生能源。人类的大量开采将 水
高温高压
使化石燃料被耗尽,节约使用化石燃 沙泥深埋
枯萎的古代植物、
料是每个公民的义务。
动物尸体
煤,也叫煤炭,是人类历史上最
图4-3-1 化石燃料的形成
早使用的化石燃料之一,是一种复杂的混合物。煤中含量最高的元素是碳,其次
96 化化 学学
HHUUAAXXUUEE课题 3 化石燃料的综合利用与新能源开发
是氢和氧,另外还有少量的硫、磷、氮等元素。煤热值高、分布广、价格相对便
宜,因此被广泛使用。我国是世界上最早认识和使用煤的国家,成书于公元前 5
世纪的《山海经··五藏山经》中就有关于煤的记载,而西方国家关于煤的最早文
字记载始于公元 315 年,比我国晚了近 800 年。
石油是一种组成极为复杂的混合物,成分以碳氢化合物为主。从油井中开采出
来的石油又叫原油,是一种黏稠状液体。
化学史话
我我国国古古代代对对石石油油的的开开发发利利用用
关于石油,我国晋代《博物志》、唐代《酉阳杂俎》等都有相关记载,古人把这
种呈漆黑膏状且能用于照明的液体称为石漆、石脂水、火井油等。北宋杰出的科学家
沈括在其著作《梦溪笔谈》中提到,一种油“生于水际,砂石与泉水相杂,惘惘
而出”,遂将其正式命名为“石油”,并预见“此物后必大行于世”。他还将石油燃
烧产生的烟尘收集起来,按照制墨的流程制墨,从而创造了用石油炭黑代替松木炭黑
来制造烟墨的工艺。
煤和石油作为燃料,主要利用的是其中所含的碳元素发生氧化反应放出的
热量。
煤、石油等化石燃料的燃烧不仅会释放热量,还会产生温室气体二氧化碳
(CO ),并伴随着烟尘、一氧化碳(CO)、二氧化硫(SO )、氮氧化物(NO )
2 2 x
等有害物质的排放,其中二氧化硫、氮氧化物会导致酸雨,对环境造成污染。燃烧
过程中一般只有约 1/3 的能量可以实现有效转化,其他部分则转化为废热排出或损
耗掉,因此,化石燃料利用效率不高。
天然气一般是指在地下自然形成的可燃性气体,主要成分为甲烷(CH )。
4
观察思考
甲甲烷烷的的燃燃烧烧
步骤1 观察甲烷的颜色、状态。
步骤2 点燃从导管中放出的甲烷(点燃前先检验甲烷的纯度),在火焰上方罩
化化 学学 97
HHUUAAXXUUEE单元 4 再探燃烧与燃料
一个冷而干燥的烧杯(图4-3-2),观察现象。
步骤3 将一个内壁涂有澄清石灰水的烧杯罩在火焰上
方,观察现象。
CH
4
图4-3-2 甲烷的燃烧
步骤 实验现象 实验结论
1
2
3
通过以上实验,你能得出甲烷具有哪些主要性质吗?
常温常压下,甲烷是一种无色无味的气体,在点燃的条件下与氧气发生反应,
生成二氧化碳和水,并放出大量的热。
点燃
CH + O CO + H O
4 2 2 2
天然气的燃烧效率、热值都比煤和石油高,且只含碳、氢元素,燃烧产物污染
较小。天然气是一种相对清洁、高效的能源,因此,国家出台了一系列政策推广和
普及天然气的使用。尽管天然气是清洁能源,但其主要成分是一种温室气体,燃烧
产生的二氧化碳也是温室气体。为实现人类与自然的和谐、可持续发展,科学家正
积极研发低碳、绿色、可再生能源。
拓展视野
我我国国化化石石燃燃料料资资源源的的分分布布与与““西西气气东东输输””工工程程
我国化石燃料资源较为丰富,但分布不均衡。煤炭资源主要分布在山西、黑龙
江、辽宁、吉林、内蒙古、河北、山东、江苏以及安徽等地区。石油资源主要分
布在东北、华北、西北以及我国近海地区。天然气资源多半分布在我国的中西部
地区,尤其是新疆和四川地区。
98 化化 学学
HHUUAAXXUUEE课题 3 化石燃料的综合利用与新能源开发
“西气东输”工程是我国西部大开发和能源结构调整的重大项目。该工程将天然
气从新疆输送到江苏、上海等省市,对优化我国能源消费结构、改善大气环境、促进
经济发展以及助力“碳达峰、碳中和”起到了重要作用。
二、化石燃料的综合利用
随着化学工业的发展,化学家发现化石燃料不仅可以提供人类所需的能量,还
可以用于制造化工原料和化工产品以服务人类的生产生活。
煤的综合利用方式多种多样,如煤的干馏、煤的气化、煤的液化等。把煤隔绝
空气加热,便会生成焦炭、煤焦油和焦炉气等,此过程称为煤的干馏。煤的干馏、
气化或液化所获得的产物在医药、农药、化肥、合成材料制造等领域具有重要
作用。
图4-3-3 煤的综合利用
观察思考
不不同同石石油油分分离离产产品品的的燃燃烧烧
实实验验 用滴管分别向4个蒸发皿加入10滴汽油、煤油、柴油和润滑油,点燃,观
察现象。
石油分离产品 沸点范围/℃ 燃烧现象 石油分离产品 沸点范围/℃ 燃烧现象
汽油 30 ~ 160 柴油 220 ~ 350
煤油 160 ~ 220 润滑油 >350
化化 学学 99
HHUUAAXXUUEE单元 4 再探燃烧与燃料
结合表中所给的石油分离产品的沸点范围数据,比较分析实验现象,可得到的结
论是 。
不同燃油,沸点越高,越难充分燃烧,产生的 石油气
黑烟也越多。从油井中开采出来的石油一般不直 汽油
接用作燃料,而是利用其组分的沸点不同,将其
航空煤油
进行分离从而获得不同的燃料或化工原料,此过
煤油
程称为石油的分馏。汽油、柴油等燃料都是石油分
馏的产物。
柴油
化学家把石油分馏的产物在一定的条件下进
润滑油
一步转化成各种化工原料,如乙烯、丙烯等,然后
加工制造成各种产品,如塑料、合成纤维、合成橡
石蜡
胶、医药、农药、化肥、炸药及洗涤剂等,这就是 原油
加热 重油
20 世纪兴起的综合利用石油产品的工业——石油
(沥青等)
化工。
随着化石燃料综合利用技术的不断发展,人 图4-3-4 石油的分馏
们越来越依赖各种化石燃料产品,它们在工业、农业、国防、交通运输、建筑、
医疗卫生等方面以及人们的日常生活中发挥着不可替代的作用。因此,人们称
煤是“工业的粮食”“黑色的金子”,称石油是“工业的血液”。
三、新能源的开发
现代社会发展对能源的需求量越来越大,而地球上的化石燃料储量有限,且短
期内不可再生。煤、石油等化石燃料的燃烧还会带来环境问题。人类解决面临的能
源短缺及环境问题有两个主要路径:一是节约能源,二是进一步开发和利用新
能源。
人类正在开发和利用许多其他能源,如太阳能、风能、地热能、潮汐能、生物
质能和核能等。这些能源的利用,可以解决部分化石燃料将会耗尽的问题,并在一
定程度上减少环境污染。
100 化化 学学
HHUUAAXXUUEE课题 3 化石燃料的综合利用与新能源开发
热能发电 太阳能发电 风能发电
水力发电 地热能发电 核能发电
图4-3-5 人类开发和利用的各种能源
联系实际
氢氢能能助助力力““绿绿色色””冬冬奥奥
往届奥运会大多使用液化天然气或丙烷(C H )等气
3 8
体作为火炬燃料。2022年北京冬奥会首次使用氢气作为火
炬燃料,示范运营了 1 000 多辆氢燃料汽车和 30 多个加
氢站,将“绿色”“环保”理念融入了奥林匹克精神。
你能解释为什么氢气比天然气或丙烷更“绿色”“环
保”吗? 图4-3-6 2022年北京
冬奥会火炬
氢气无毒,完全燃烧放出的热量是同质量甲烷的 2 倍多(液氢完全燃烧
放出的热量约为同质量汽油的 3 倍),且燃烧产物是水,燃烧过程零碳排放,
是最理想的清洁燃料。目前,液氢已在火箭、飞船、导弹和氢燃料电池等方
面得到应用。在地球上,氢元素主要以化合态的形式存在于水和化石燃料中。
所以氢能源的广泛利用需要解决两个主要问题:一是如何以水、天然气等为
原料经济地制取氢气,二是如何储运氢气。科学家正在攻克这些难题。
化化 学学 101
HHUUAAXXUUEE单元 4 再探燃烧与燃料
练习实践
1. 天然气是家庭日常生活的常用燃料。下列说法不正确的是( )。
A.天然气是一种不可再生的化石能源
B.天然气燃烧能放出热量
C.天然气完全燃烧时,会产生大量炭黑颗粒
D.发现家中天然气泄漏,立即关闭阀门,开窗通风
2.以下新能源是通过化学反应获得的是( )。
A.氢能 B. 风能 C. 太阳能 D. 潮汐能
3. 从某种意义上来说,化石燃料是以固态、液态和气态形式储存的古时期的太阳
能。你是如何理解这句话的?为什么说化石燃料是不可再生能源?
4.下图分别为我国2000年、2020年以及世界2020年的能源消费结构图。
天然气 水电、核电等 水电、核电等
7.3% 15.6% 水电、核电等
2.2% 煤
16.9%
天然气 27.2%
8.2% 煤
石油
56.6%
22.0%
石油
煤 19.6% 天然气 石油
24.7% 31.2%
68.5%
中国(2000年) 中国(2020年) 世界(2020年)
图1 图2 图3
(1)通过与世界能源消费结构的比较,分析我国能源消费的特点。
(2)结合化石燃料的元素组成,比较不同化石燃料燃烧对环境的影响。
(3)谈谈你对我国未来能源发展方向及趋势的看法。
5.查阅资料,完成以下问题,并与同学分享交流。
(1)中国航天科技集团有限公司第六研究院团队,在研制2022年北京冬奥会手
持氢气火炬过程中,是如何解决氢气的储存和安全使用问题的?
(2)氢能的广泛使用存在哪些需要解决的问题?
102 化化 学学
HHUUAAXXUUEE单元小结
单元小结
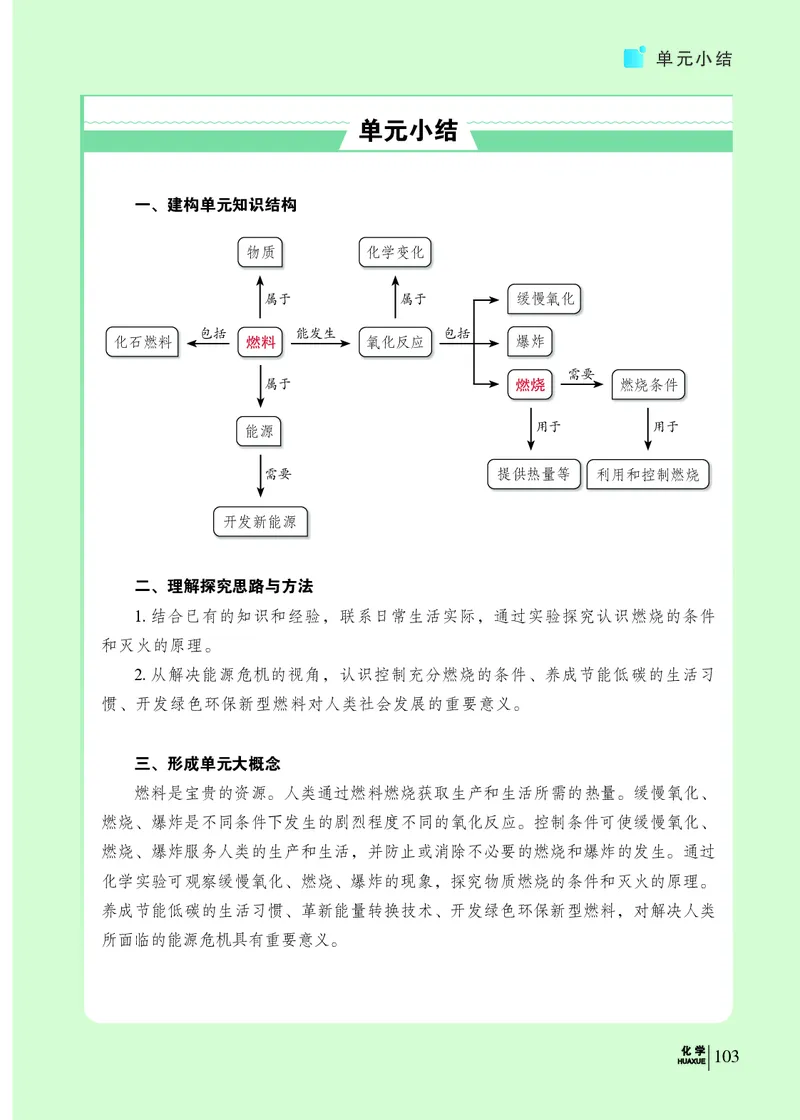
一、建构单元知识结构
物质 化学变化
属于 属于 缓慢氧化
包括 能发生 包括
化石燃料 燃料 氧化反应 爆炸
需要
属于 燃烧 燃烧条件
能源 用于 用于
需要 提供热量等 利用和控制燃烧
开发新能源
二、理解探究思路与方法
1.结合已有的知识和经验,联系日常生活实际,通过实验探究认识燃烧的条件
和灭火的原理。
2.从解决能源危机的视角,认识控制充分燃烧的条件、养成节能低碳的生活习
惯、开发绿色环保新型燃料对人类社会发展的重要意义。
三、形成单元大概念
燃料是宝贵的资源。人类通过燃料燃烧获取生产和生活所需的热量。缓慢氧化、
燃烧、爆炸是不同条件下发生的剧烈程度不同的氧化反应。控制条件可使缓慢氧化、
燃烧、爆炸服务人类的生产和生活,并防止或消除不必要的燃烧和爆炸的发生。通过
化学实验可观察缓慢氧化、燃烧、爆炸的现象,探究物质燃烧的条件和灭火的原理。
养成节能低碳的生活习惯、革新能量转换技术、开发绿色环保新型燃料,对解决人类
所面临的能源危机具有重要意义。
化化 学学 103
HHUUAAXXUUEE单元作业
单元作业
1.酒精运输车须张贴的标志是( )。
A B C D
2.人们曾经将煤加工成如右图所示的形状用于燃烧,原因是
( )。
A.形状美观 B.能降低煤的着火点
C.能增加氧气的浓度 D.能增大煤与氧气的接触面积
3. 森林火灾现场灭火方法之一“砍出隔离带”的原理是 图1
( )。
A. 隔绝氧气 B. 升高着火点
C. 隔离可燃物 D. 降低温度至着火点以下
4.阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气。下
列关于该阻燃剂防火原理的叙述中错误的是( )。
A. 反应吸热,可降低可燃物的着火点
B. 生成的氧化铝覆盖在可燃物表面,可隔绝空气
C. 生成大量水蒸气,可降低可燃物周围氧气的浓度
D. 反应能够降低周围温度,使温度不易达到可燃物的着火点
5.氢气是一种清洁、绿色能源。利用太阳能及
氧气
催化剂的作用可将水分解制得氢气。氢气可用于氢 氢气
能电动车,原理如右图所示。
(1)该条件下水分解的文字表达式是
光催化剂
水
氧气
;氢气用于氢能电动车所
氢气
发生的化学反应的文字表达式是
氢能电动车 氢能储罐
。
图2
(2)上述反应中所发生的能量转化形式分别为 、 。
104 化化 学学
HHUUAAXXUUEE单元作业
(3)与电解水获得氢气相比,该方法的优点是 ;
你认为此方法的技术关键是 。
6. 已知如下实验事实:①氢气可以在氯气中燃烧生成氯化氢;②镁条可以在二氧
化碳中燃烧生成碳和氧化镁。试回答以下问题。
(1)你对燃烧的条件有何新的认识?
(2)运输金属镁的货车发生火灾,消防员用沙土而不用二氧化碳灭火,这是
为什么?
7. 化学兴趣小组同学利用图3所示的装置对燃烧的条件展开探究。
已知白磷的着火点约为40 ℃,图中装在燃
烧匙中的白磷并不燃烧,原因是
。点燃蜡烛后,罩上钟罩。一段时间后,
蜡烛熄灭,原因是 。向上抽动装
有白磷的燃烧匙,白磷露出水面时没有燃烧,原
因是 ;当移开钟罩,白磷露
出水面时立即燃烧,原因是 。
8. 近50年来我国家庭燃料的变迁历程为:木柴或煤 → 液化石油气或管道煤气
→ 天然气。
(1)天然气和煤都是 (填“可再生”或“不可再生”)能源。
(2)充分燃烧天然气和煤各1 kg产生CO 和SO 的质量如下图所示。
2 2
天然气 煤 天然气 煤
燃料 燃料
① 我国正推广“利用天然气代替煤作家庭燃料”的策略,请说明原因。
② 使用液化石油气或天然气的家庭需在恰当的位置安装报警器,并定期检查,这
是为什么?
③ 尝试说明未来的能源变迁方向。
g/)OC(m
2
3 000
2 900
2 800
2 700
2 600
2 500
2 400
2 300
g/)OS(m
2
钟罩
白磷
底部打孔、垫有
80 ℃热水
滤纸的燃烧匙
图3
12
10
8
6
4
2
0
图4 图5
化化 学学 105
HHUUAAXXUUEE项目学习
项目学习
一一次次性性自自发发热热暖暖贴贴的的原原理理和和制制作作
项目背景
一次性自发热产品,如发热暖身贴、发热鞋垫、发热眼罩等,在日常生活中应用
广泛,这是利用“物质化学变化伴随着能量变化”服务人类生活的一个实例。本项目
帮助同学们通过一次性自发热暖贴的制作,深入了解一次性自发热产品的构造和发热
的化学原理,从而学会科学地使用一次性自发热产品。
项目建议方案
1. 查阅资料。查阅相关资料,整理归纳一次性自发热产品的构造、原料、发热
原理、使用方法及注意事项。
2. 走访调查。走访调查家庭成员、社区的邻居以及商店售货员,了解一次性自发
热产品的使用方法和效果。
3. 实验探究。与同学讨论探究“一次性自发热产品中发热物质的成分、发热效果、
发热过程中性质的变化”的实验方案,完成并优化实验方案。小组合作进行实验探究,
形成“一次性自发热产品的探究报告”。
4. 产品制作。依据所查阅的资料和实验探究的结果,设计制作一次性自发热暖贴
的方案,并利用简易的材料制作一次性自发热暖贴,试验所制作的一次性自发热暖贴
的发热效果。
5. 成果展示。将“一次性自发热产品的探究报告”和自制的一次性自发热暖贴在
全班进行展示与交流。
106 化化 学学
HHUUAAXXUUEE单元 5 表征化学反应
课题 1 化学反应是有条件的
情境问题
化化学学反反应应的的条条件件和和控控制制
仔细观察生产、生活和化学实验中的一些化学变化,就会发现许多化学反应的发
生需要外界提供一定的条件,如酒精燃烧需要点燃,煅烧石灰石生产生石灰需要
高温,实验室分解过氧化氢制取少量氧气需要加二氧化锰作催化剂。有些情况下需要
控制条件避免反应发生,如加油站需要严禁烟火,防止燃烧或爆炸。
图5-1-1 点燃酒精灯 图5-1-2 加油站严禁烟火
请与同学合作探究下列问题:
1. 化学反应需要哪些条件?
2. 控制化学反应条件在生产和生活中有哪些应用?
一、化学反应的条件
我们生活的物质世界时刻发生着各种化学变化,仔细观察这些变化会发现,为
了使化学变化快速发生,往往需要外界提供一定的条件。如要使放置在空气中的干
燥柴草在空气中燃烧,就需要“点燃”柴草,或不断摩擦产生热量,使温度达到柴
草的着火点(这就是“钻木取火”的原理)。所以,我们研究化学变化时,要了解
其发生的条件,并通过控制这些条件使化学变化为人类服务。
108 化化 学学
HHUUAAXXUUEE课题 1 化学反应是有条件的
交流讨论
化化学学反反应应条条件件的的表表示示
我们已经接触了很多在一定条件下发生的化学变化。请根据所给示例,用化学反
应表达式表示这些化学反应,并与同学交流讨论反应所需条件。
点燃
【示例】木炭在充足的氧气中燃烧: C + O CO
2 2
1.碱式碳酸铜[Cu (OH) CO ]受热分解为氧化铜(CuO)、水和二氧化碳。
2 2 3
2. 水在通电条件下分解生成氢气和氧气。
3. 二氧化碳与水在光照和叶绿素作用下生成葡萄糖(C H O )和氧气。
6 12 6
大量事实表明,许多化学反应需要一定条件。如物质燃烧常常需要“点燃”;
物质分解常常需要“加热”或提供“高温”;室温下分解水需要“通电”;分解
过氧化氢制取氧气需要“催化剂”;绿色植物发生光合作用需要“光照”和“叶
绿素”的共同作用等。
二、反应条件对化学反应的影响
化学反应的发生是有条件的,我们可以通过化学实验来探究反应所需条件以及
反应条件对化学反应的影响。
实验探究
过过氧氧化化氢氢分分解解生生成成氧氧气气的的反反应应条条件件探探究究
过氧化氢在室温下就能分解产生氧气,但为什么在实验室中通常采用向过氧化氢
中加入二氧化锰的方法来制取少量氧气?请提出你的假设,并通过下列对比实验加
以探究。
实实验验 取 3 支相同的洁净试管,各加入 2 mL 5% 的过氧化氢溶液,将第 1 支试
管置于室温下,将第 2 支试管在酒精灯外焰上加热,在第 3 支试管中加入少量二氧
化锰粉末。将带火星的木条分别伸入 3 支试管(不可接触液面),观察并比较带火
星的木条的复燃情况,分析得出相关结论。
化化 学学 109
HHUUAAXXUUEE单元 5 表征化学反应
反应条件 实验现象 实验结论
室温
加热
加入二氧化锰
在过氧化氢的分解反应中,升高温度会加快反应速率,加入二氧化锰作催化
剂也会加快反应速率。在化工生产中,人们通常通过添加催化剂的方法来改变反应
速率,以满足实际生产的需要,催化剂在化工生产中具有极其广泛的应用。
实验事实表明,化学反应条件不仅影响反应速率,还会影响反应产物和反应
过程中能量的变化。如含有碳元素的燃料,完全燃烧时生成二氧化碳,放出热量
较多,不完全燃烧时生成一氧化碳,放出热量较少;铁丝在空气中与氧气反应主
要生成氧化铁(Fe O ),在氧气中点燃主要生成四氧化三铁(Fe O )。
2 3 3 4
阅读理解
催催化化剂剂及及其其应应用用
催化剂的应用由来已久。古代人们用酵母酿酒、制醋,就是催化剂最古老的应用。
当今,催化技术的突破,往往会引起某一生产领域发生革命性的飞跃。如20世纪初,
铁基催化剂的问世实现了合成氨的工业化,从此化肥工业在世界范围迅速发展;20世
纪50年代末,齐格勒-纳塔(Ziegler-Natta)催化剂推动了合成材料工业的发展;20
世纪70年代,汽车尾气净化催化剂实现了工业化,从而使汽车尾气催化净化技术得到
普遍应用。
催化剂能改变化学反应速率,且在反应前后本身的质量和化学性质不发生改变,
但催化剂是参与化学反应的。如二氧化锰(MnO )催化过氧化氢(H O )分解的
2 2 2
反应,就有研究认为反应过程中二氧化锰经历了“MnO →Mn2+→MnO ”的过程。
2 2
催化剂被誉为现代化学工业的“心脏”,在炼油、化工、制药、环保等行业得到
广泛应用。在化工产品生产中,85% 以上的反应是在催化剂作用下进行的。当前人
类正面临着诸多重大挑战,如资源短缺、环境恶化、能源危机等问题,这些重大问题
的解决与催化剂的开发和应用息息相关。因此,我国在化学工业等领域非常重视新型
催化剂的研制和催化技术的发展,并将催化技术作为创新驱动发展的重点。
110 化化 学学
HHUUAAXXUUEE课题 1 化学反应是有条件的
通过阅读上述资料,结合所学知识,请思考并讨论下列问题:
1.催化剂在化学反应中起到什么作用?反应中有什么变化?
2.催化剂在生产中有什么价值?
三、反应条件调控的应用
人们常常需要对反应条件进行调控,使化学反应加快或减缓发生,甚至避免化
学反应的发生。
交流讨论
化化学学反反应应条条件件的的调调控控
分析下列事例中调控了哪些反应条件?调控反应条件的目的是什么?与同学交流
讨论你的观点。
1.氢气在纯氧中燃烧可获得高温,用于金属的气割、焊接。
2.机动车辆加油站有“禁止烟火”的标志。
3. 将食物放置在冰箱中以延长食物的保鲜时间。
4. 氯酸钾(KClO )加热至400 ℃以上可以缓慢分解放出氧气,但实验室通常采
3
用将氯酸钾与少量二氧化锰混合加热的方式制取氧气。
图5-1-3 氢气在纯氧中燃烧 图5-1-4 将食物储存在冰箱
可获得高温 中可保鲜
在生产、生活和科学研究中,人们总是严格控制反应的条件,如调控反应
温度、反应物浓度、反应物之间的接触面积及加入催化剂等,控制反应进行的速
率、反应生成物的量,使化学反应按人们期望的方向进行,更好地为人类的生产
和生活服务。
化化 学学 111
HHUUAAXXUUEE单元 5 表征化学反应
阅读理解
化化学学反反应应条条件件调调控控的的应应用用
在生产、生活和科学研究中,人们常常通过控制反应条件来控制反应的进行,从
而更好地利用化学反应为人类的生产和生活服务。
调调控控反反应应条条件件,,加加快快反反应应发发生生。如家用的燃气灶需要点火器产生电火花才能点燃
天然气,需要增加空气进气量才能使天然气迅速且完全燃烧;工业上用氢气(H )与
2
氮气(N )反应合成氨气(NH ),需要加入含有铁元素的催化剂,才能使反应迅速
2 3
发生;硫酸工业中将二氧化硫(SO )氧化为三氧化硫(SO ),需要加入含有钒
2 3
元素的催化剂使反应快速进行;工业上分解石灰石(主要成分为 CaCO )生产生
3
石灰(CaO),需要在高温条件下才能实现;在实验室中,人们常常通过加热、搅
拌、增加反应物浓度、使用催化剂等方法,使反应迅速发生。
调调控控反反应应条条件件,,减减缓缓或或防防止止反反应应发发生生。如生活中将食品置于冰箱中保存,是为了
通过降低温度来减缓食品变质相关的化学反应的发生;将盛装食品的袋子抽成真空或
在盛装食品的袋子中放置吸氧剂,是为了减缓食品被空气中氧气氧化的速率;加油
站的“禁止烟火”,以及使用酒精消毒剂或家用燃气灶泄漏时要防止接触明火,都是
为了防止燃烧或爆炸反应的发生;实验室中的硝酸(HNO )、硝酸银(AgNO )
3 3
等试剂要保存在棕色试剂瓶中,并置于阴暗处,是为了防止其见光发生分解反应。
结合已有的生活和学习经验,查阅相关资料,与同学讨论下列问题:
1.生产和生活中调控反应条件的事例有哪些?调控反应条件的意义是什么?
2.为了加快化学反应的进行,人们通常会采取哪些措施?在化学实验探究中,你
采取过哪些加快反应的措施?
总之,化学反应条件的调控在生产和生活中具有重要应用,对有效利用资源、
节能降耗、安全生产和提高人类生活质量等都具有重要意义。
112 化化 学学
HHUUAAXXUUEE课题 1 化学反应是有条件的
练习实践
1.化学反应通常需要在一定条件下才能发生。请根据所学知识和题中信息,在箭
头上方注明该反应的条件。
(1)镁条在空气中点燃后燃烧:
( )
镁(Mg)+氧气(O ) 氧化镁(MgO)
2
(2)碱式碳酸铜受热分解:
( )
碱式碳酸铜[Cu (OH) CO ] 氧化铜(CuO)+水(H O)+二氧化碳(CO )
2 2 3 2 2
(3)葡萄糖在酒化酶的催化作用下生产酒:
( )
葡萄糖(C H O ) 乙醇(C H O)+二氧化碳(CO )
6 12 6 2 6 2
2.分析下列操作是怎样通过改变条件来控制反应速率的。
(1)用30%的硫酸代替10%的硫酸与锌粒反应制取氢气。
(2)将硝酸银(AgNO )存放在棕色瓶中并置于阴暗处。
3
(3)将装有食品的食品袋内的空气抽去并置于低温环境下保存。
3. 在一定的条件下,下列四种物质都能分解产生氧气。
① 水:通电(生成氢气和氧气)。
② 过氧化氢(H O ):加入二氧化锰(MnO )粉末(生成水和氧气)。
2 2 2
③ 高锰酸钾(KMnO )颗粒状固体:加热 [ 生成锰酸钾(K MnO )、二氧化
4 2 4
锰(MnO )和氧气 ]。
2
④ 氯酸钾(KClO ):加入二氧化锰(MnO )粉末混合并加热[生成氯化钾(KCl)
3 2
和氧气] 。
(1)写出上述化学反应的化学反应表达式。
(2)反应②和④中,二氧化锰的作用是什么?
(3)分析说明上述反应的特点。
化化 学学 113
HHUUAAXXUUEE单元 5 表征化学反应
课题 2 质量守恒定律
情境问题
化化学学反反应应前前后后物物质质的的质质量量关关系系
化学变化有新物质生成,并伴随着能量变化。因此,化学变化成为人类获取新
物质和进行能量转换的重要途径。在利用化学变化时,人们首先需要选择合适的化
学反应,其次需要探究化学反应中物质转化的质量关系。如火力发电厂完全燃烧含
有1×105 kg碳的煤能放出多少质量的二氧化碳?植物通过光合作用产生1 kg葡萄糖
(C H O )能吸收多少质量的二氧化碳?
6 12 6
光照
氧气
二氧化碳
糖
水
图5-2-1 火力发电厂 图5-2-2 植物的光合作用
请与同学合作探究下列问题:
1.化学反应中反应物的质量与生成物的质量之间存在怎样的规律?如何探究化学
反应中物质的质量关系?
2.化学反应中物质的质量关系在生产和生活中有哪些应用?
一、化学反应中的元素和原子
化学反应过程中的反应物和生成物,都是由元素组成、由原子等微观粒子构成
的。那么,化学反应前后元素和原子的种类会发生变化吗?
114 化化 学学
HHUUAAXXUUEE课题 2 质量守恒定律
实验探究
酒酒精精燃燃烧烧反反应应中中的的元元素素和和原原子子
酒精是由乙醇分子(C H O)构成的(图5-2-3),能够燃烧。在酒精燃烧反应中,
2 6
元素和原子的种类是否发生了变化?我们将通过下列实验进行探究。
图5-2-3 乙醇分子的构成
实实验验1 点燃酒精灯,观察实验现象。
实实验验2 取1个冷而干燥的烧杯,将烧杯罩在酒精灯火焰的上方,观察实验现象。
实实验验3 向1个洁净的烧杯中加入少量澄清石灰水,使澄清石灰水均匀地润湿烧杯
内壁,将烧杯罩在酒精灯火焰的上方,观察实验现象。
将实验中观察到的现象及由实验现象得出的结论填入表中,并写出该反应的化学
反应表达式,思考该反应前后元素和原子种类是否发生变化。
实验 实验现象 实验结论
1
2
3
酒精在点燃的条件下能与空气中的氧气发生反应,生成二氧化碳和水:
点燃
C H O + O CO + H O
2 6 2 2 2
由上述反应表达式可以看出,反应物酒精由碳、氢、氧三种元素组成,氧气由
氧元素组成,因此反应物包含三种元素。酒精燃烧的产物为二氧化碳和水,也
由碳、氢、氧三种元素组成。反应物的两种分子中包含碳、氢、氧三种原子,产物
中的两种分子也包含这三种原子。
大量实验事实证明,在化学变化前后,组成物质的元素种类没有改变,构成物
质的原子种类也没有发生改变。
化化 学学 115
HHUUAAXXUUEE单元 5 表征化学反应
联系实际
化化学学变变化化中中的的元元素素
分析下列化学反应前后元素的种类,总结出你的结论。
1. 二氧化碳与澄清石灰水的反应:CO + Ca(OH) CaCO + H O
2 2 3 2
点燃
2.在点燃条件下碳与氧气生成二氧化碳的反应:C + O CO
2 2
点燃
3.黑火药爆炸的主要反应:KNO + C + S K S + CO + N
3 2 2 2
加热
4.高锰酸钾加热分解制取氧气的反应:KMnO K MnO + MnO + O
4 2 4 2 2
二、质量守恒定律
很久以前,人们对化学变化前后物质的质量关系并不清楚。18 世纪初,化学家
开始使用天平进行实验研究,天平的使用为定量研究化学变化、揭示化学变化中物
质质量关系打开了大门。
阅读理解
化化学学变变化化前前后后物物质质质质量量关关系系的的探探索索历历史史
海海尔尔蒙蒙特特的的柳柳树树实实验验。17世纪早期,比利时科学家海尔蒙特把一棵2.5 kg的柳树
苗栽种到一个木桶里,桶里盛有事先称量过的土壤。这之后他只用纯净的雨水浇灌树
苗。为了防止灰尘落入,他还专门制作了桶盖。5年过去了,柳树逐渐长大。经过称量,
他大吃一惊:柳树的质量增加了超过 80 kg,而土壤却只减少了不到 100 g。海尔
蒙特推测,柳树增加的质量应该是来源于水和空气。
波波义义耳耳的的金金属属汞汞加加热热实实验验。1673年,英国物理学家罗伯特··波义耳(图5-2-4)
做了汞加热实验,他将金属汞放在密闭的容器里煅烧,煅烧后立刻打开容器盖进行称
量,得出的结论是物质的质量比反应前增加了。
罗罗蒙蒙诺诺索索夫夫的的锡锡煅煅烧烧实实验验。1756年,俄国科学家罗蒙诺索夫(图5-2-5)把锡放
在密闭的容器里煅烧,锡发生变化生成了白色的氧化锡,但容器和容器里物质的总质
量在煅烧前后并没有发生变化。经过反复的实验,都得到同样的结果,于是,他认为
在化学变化中物质的质量是守恒的。
116 化化 学学
HHUUAAXXUUEE课题 2 质量守恒定律
图5-2-4 罗伯特··波义耳 图5-2-5 罗蒙诺索夫
拉拉瓦瓦锡锡密密闭闭容容器器中中的的金金属属煅煅烧烧实实验验。1774年,法国化学家拉瓦锡在密封的玻璃容
器中煅烧锡、铅、汞等金属时发现,加热前后的容器质量毫无变化。拉瓦锡认为,一
切物质是不能凭空创造的,反应前后物质的质量是相等的。
质质量量守守恒恒定定律律的的验验证证实实验验。1908年德国化学家廊道尔特及1912年英国化学家曼
莱做了精确度极高的实验:所用的容器和反应物质量为1 000 g左右,反应前后质量之
差小于 0.0001 g,质量的变化小于 1/10 000 000。他们认为这个差别在实验误差
范围之内,“物质在化学反应前后质量相等”的结论是正确的。
阅读上述资料,思考并与同学讨论下列问题:
1.从科学家探索化学反应中物质质量关系的过程中,你能得到哪些启迪?
2.你认为化学反应前后物质质量具有怎样的关系?
化学变化前后物质质量关系的探索历史告诉我们,实验是进行科学探究的重
要途径,而精确严谨的定量实验,能帮助我们更为准确地收集实验数据,更好地
揭示客观世界的规律。这段历史也让我们认识到,科学是一个不断探索的曲折
过程,研究者注重实证、严谨求实、敢于批判的态度至关重要。
实验探究
化化学学变变化化前前后后物物质质质质量量关关系系的的实实验验探探究究
【提出问题】化学变化前后物质的种类发生了变化,那么反应前物质的总质量与
反应后物质的总质量是否会发生改变?
【形成假设 】请根据已有知识和经验提出假设。
化化 学学 117
HHUUAAXXUUEE单元 5 表征化学反应
【设计方案】请设计实验方案验证你的假设。你也可以从下列方案中选择感兴趣
的实验方案,验证假设。
方方案案1 在1支试管里加入少量胆矾(CuSO ··5H O),用带玻璃导管的橡胶塞
4 2
塞紧试管,取1个气球,挤压出气球内的空气并将气球扎在导管口,放在托盘天平上
称量。取下试管,将试管在酒精灯上加热,观察胆矾颜色的变化。待试管冷却后,将
试管重新放在托盘天平上,观察天平是否平衡(图5-2-6)。
方方案案 2 用胶头滴管吸取少量氢氧化钠(NaOH)溶液,将胶头滴管用橡胶塞固
定在盛有少量硫酸铜溶液的锥形瓶上,将锥形瓶放在托盘天平上称量。挤压胶头滴
管,观察硫酸铜溶液和氢氧化钠溶液发生反应的现象,并观察天平是否保持平衡
(图 5-2-7)。
图5-2-6 胆矾加热反应前后质量的变化 图5-2-7 氢氧化钠溶液与硫酸铜
溶液反应前后质量的变化
方方案案3 取一块木炭放置于陶土网上,将它们放在电子秤上称量,记录数据。用坩
埚钳夹持一块木炭置于酒精灯火焰上加热一段时间,观察现象。将剩余的木炭冷却一
段时间后,放回陶土网上,将它们一起放在电子秤上称量。比较两次读数的差异。
【收集证据】
方案 实验现象
1
2
3
【形成结论】基于你进行的实验探究,讨论以下问题:
1.化学变化前后物质的质量存在怎样的关系?
2.方案3中反应前后电子秤的读数产生差异的原因是什么?如何改进方案3才能
正确反映化学变化前后物质的质量关系?
118 化化 学学
HHUUAAXXUUEE课题 2 质量守恒定律
方法引导
托盘天平的使用
使用托盘天平称量前要调节天平平衡。左盘放物体,右盘
放砝码。增减砝码时要用镊子。称量腐蚀性试剂或易潮解的试
剂时,应将试剂放在玻璃器皿中进行称量。过冷或过热的物质
需要放置至室温后再称量。
图5-2-8 托盘天平
诸多实验证明,参加化学反应的各物质的质量总和等于反应后生成的各物质质
量总和,这个规律叫做质量守恒定律。质量守恒定律是自然界客观存在的规律,它
揭示了化学反应过程中反应物和生成物之间的质量关系。
为什么化学反应前后物质的总质量保持不变呢?下面以氢气和氧气反应生成水
为例(图 5-2-9),从化学反应的微观视角去解释这一规律。
点燃
2H + O 2HO
2 2 2
反应物 生成物
原子种类 氢、氧 氢、氧
原子数目 4个氢原子、2个氧原子 4个氢原子、2个氧原子
相对分子质量总和 1×4+16×2 = 36 (1×2+16)×2 = 36
图5-2-9 氢气与氧气反应的微观示意图
物质是由分子、原子等微观粒子构成的,发生化学反应时,参加反应的各物质
中的原子会重新组合形成新的物质。化学反应中原子核不会发生变化,因而反应中
元素的种类及原子的种类和数目也不变,那么参加化学反应的各物质的质量总和也
不会发生变化,即参加化学反应的各物质的质量总和等于反应后生成的各物质的质
量总和。所有化学反应都遵循质量守恒定律。
化化 学学 119
HHUUAAXXUUEE拓展视野
化化学学反反应应中中的的能能量量守守恒恒
参加化学反应的每一种物质都具有一定的能量。当反应物的总能量低于生成物的
总能量时,反应物需要吸收能量才能转化为生成物;当反应物的总能量高于生成物的
总能量时,反应物转化为生成物就会放出能量(图5-2-10)。其能量关系可表示为:“生
成物具有的能量=反应物具有的能量+化学反应中吸收的能量”或“生成物具有的能
量=反应物具有的能量-化学反应中放出的能量”。化学反应中能量是守恒的。
化学反应中的能量变化主要表现为热的形式,据此化学反应又可分为放热反应和
吸热反应。
反应物
放出能量
生成物
放热反应过程
图5-2-10 化学反应中的能量守恒
量能
联系实际
化化学学反反应应遵遵循循质质量量守守恒恒定定律律
在生活中人们经常发现:
1.木炭燃烧后质量会减少。
2.生石灰放置在空气中质量会增加。
3.铁制品生锈后质量会增加。
你能运用质量守恒定律解释上述化学反应现象吗?
质量守恒定律的发现,推动化学科学由定性研究走向定量研究,使人们能更好
地基于化学反应确定物质的组成与结构,更合理地利用化学反应进行生产和研究。
生成物
吸收能量
反应物
O 吸热反应过程 O
量能
单元 5 表征化学反应
120 化化 学学
HHUUAAXXUUEE课题 2 质量守恒定律
练习实践
1.下列关于化学变化的说法不准确的是 ( )。
A. 化学反应前后元素种类不变 B. 化学反应前后原子种类不变
C. 化学反应前后原子数目不变 D. 化学反应前后分子种类不变
2.某物质燃烧后生成二氧化碳和水。下列有关该物质的叙述中不正确的是( )。
A. 该物质一定含碳、氢元素 B. 该物质可能含氧元素
C. 该物质可能是纯净物 D. 该物质不可能是混合物
3. 用质量守恒定律解释下列现象。
(1)蜡烛燃烧时长度越来越短。
(2)铁丝在氧气中燃烧后,生成物的质量比原铁丝质量增加了。
(3)高锰酸钾受热分解后,剩余固体的质量比原反应物的质量减小了。
4.利用图1所示装置进行如下实验探究。
在锥形瓶中放入一小粒白磷,塞好橡胶塞后玻璃管 气球
玻璃管
下端刚好能与白磷接触,将整套装置放在托盘天平上调
白磷
节至平衡。取下橡胶塞,将玻璃管放在酒精灯火焰上灼
细沙
烧至红热,迅速塞紧橡胶塞,将白磷引燃。
(1)实验时,气球的变化是 。
图1
(2)该实验中发生反应的条件是 ;实验中细沙的作用是 ;
白磷能燃烧,而玻璃管受热不燃烧,原因是 。
(3)实验前,天平保持平衡,实验结束冷却后,松开橡胶塞,则天平指针
(填“向左偏”“向右偏”或“指向中间”)。
5. 请设计实验方案,验证稀盐酸与碳酸钙反应前后物质的总质量保持不变。画出
必要的实验装置图,并写出实验步骤。
化化 学学 121
HHUUAAXXUUEE单元 5 表征化学反应
课题 3 化学方程式及其应用
情境问题
化化学学反反应应的的表表示示及及其其应应用用
2016 年 11 月 3 日,长征五号火箭在我国文昌
航天发射场成功发射。长征五号火箭的一、二级发
动机都采用液氢/液氧燃料系统,氢气(H )与氧
2
气(O )反应生成水(H O),因此长征五号火箭
2 2
是名副其实的“环保箭”。
图5-3-1 我国发射长征五号火箭
请与同学合作探究下列问题:
1.如何用化学符号科学简洁地表示氢气和氧气发生的反应?
2.假如一只火箭推进器携带5×104 kg 氢气,理论上该火箭推进器中的氢气完全燃
烧至少需要消耗多少千克氧气 ?
一、化学方程式
在认识、研究和应用化学反应时,人们通常采用一定的方式来表示化学反应中
的诸多信息。
交流讨论
化化学学反反应应的的表表示示方方法法
甲烷与氧气反应生成二氧化碳和水的过程可用下列方式表示:
(1)甲烷在点燃的条件下与氧气反应,生成二氧化碳和水
点燃
(2)甲烷 + 氧气 二氧化碳 + 水
点燃
(3)CH + O CO + H O
4 2 2 2
点燃
(4)CH + 2O = CO + 2H O
4 2 2 2
在上述表示方式中,哪一种方式既简洁明了又科学准确地表示了该反应的实质?
122 化化 学学
HHUUAAXXUUEE课题 3 化学方程式及其应用
方式(4)对化学反应的表示,不仅用化学式表明了反应物、生成物的组成,
还表示了反应条件、反应物与生成物之间的相对质量关系,体现了化学反应遵循质
量守恒定律。像这样用化学式来表示物质化学反应的式子称为化学方程式。化
学方程式能够简洁明了地表示化学反应。化学方程式中化学式前的数字称为化学
计量数。
反应物 反应条件 生成物
点燃
化学方程式 CH + 2O ==== CO + 2HO
4 2 2 2
化学计量数比 1 : 2 1 : 2
质量比 16 :32×2 44 :18×2
点燃
CH O CO HO
4 2 2 2
图5-3-2 “甲烷与氧气反应”化学方程式的意义
交流讨论
化化学学方方程程式式的的书书写写
按照下列示例,尝试书写长征五号火箭发射时氢气燃烧生成水的化学方程式,并
交流讨论化学方程式的书写方法。
【示例】过氧化氢溶液在二氧化锰催化作用下的分解反应。
1.依据化学事实写出反应物和生成物的化学式。
H O H O + O
2 2 2 2
2.标注反应条件,将反应条件写在横线上方或下方。
MnO
H O 2 H O + O
2 2 2 2
3.依据质量守恒定律,在反应物和生成物的化学式前加上适当的化学计量数,
使化学反应前后各元素的原子个数相等。
2H O
MnO
2 2H O + O
2 2 2 2
化化 学学 123
HHUUAAXXUUEE单元 5 表征化学反应
4.标注生成物状态,有沉淀生成用“↓”符号表示,有气体生成用“↑”符
号表示。
MnO
2H O 2 2H O + O ↑
2 2 2 2
5.将“ ”改写成“ = ”,检验化学方程式书写是否正确。
MnO
2H O =2 2H O + O ↑
2 2 2 2
书写化学反应方程式必须遵守一定的规则:
1.必须以客观事实为依据。不能凭空臆造事实上不存在的物质和化学反应。
2. 必须遵循质量守恒定律。通过在反应物和生成物的化学式前加上适当的化学
计量数,使反应前后各元素的原子数目保持相等。
3.必须注明反应条件。根据反应实际发生的条件,在化学方程式上注明“点燃”
“加热”“高温”“光照”“催化剂”等。反应条件“加热”常用“△”表示。
4. 必须标明某些生成物的状态。生成物是沉淀,用“↓”符号表示;生成物
是气体,用“↑”符号表示。但是,如果反应物和生成物中都有气体,气体生成
物就不需标注“↑” 符号。在溶液反应中,如果反应物和生成物中都有固体,固
体生成物也不需标注“↓”符号。
联系实际
用用化化学学方方程程式式表表示示化化学学反反应应
用化学方程式表示下列反应。
1.植物在光照和叶绿素催化条件下发生光合作用,将水和二氧化碳转化为葡萄糖
(C H O )和氧气。
6 12 6
2.在高温、高压和催化剂条件下,氮气与氢气反应生成氨气(NH )。
3
3.镁条在空气中燃烧生成氧化镁(MgO)。
124 化化 学学
HHUUAAXXUUEE课题 3 化学方程式及其应用
4.氯酸钾(KClO )在二氧化锰催化作用下,加热分解生成氯化钾(KCl)和氧气。
3
二、根据化学方程式进行计算
在化工生产和科学研究中,人们通常需要研究化学变化中各物质之间的质量关
系,以更好地认识、控制和应用化学反应。根据化学方程式所反映出的化学变化中
各物质之间的质量关系,就可以确定一定质量的反应物能转化为多少质量的生成物,
或产生一定质量的生成物需要多少质量的反应物。
交流讨论
化化学学反反应应的的定定量量计计算算
分析以下例题,总结根据化学方程式进行计算的步骤和方法,与同学交流讨论你
的看法。
依依据据化化学学方方程程式式进进行行计计算算
【例题】我国长征五号火箭采用液氢/液氧燃料,假如一只火箭推进器携带
5×104 kg 氢气,理论上该火箭推进器中的氢气完全燃烧至少需要消耗多少千克
氧气?生成多少千克水?
解:设需要消耗的氧气的质量为 x,生成的水的质量为y。
点燃
2H + O = 2H O
2 2 2
2×2 32 2×18
5×104 kg x y
4 5×104 kg 4 5×104 kg
— = ————— — = —————
32 x 36 y
x = 4×105 kg y = 4.5×105 kg
答:燃烧5×104 kg 氢气,至少需要消耗4×105 kg 氧气,生成4.5×105 kg 水。
化化 学学 125
HHUUAAXXUUEE单元 5 表征化学反应
依依据据化化学学反反应应中中元元素素守守恒恒进进行行计计算算
【例题】我国长征五号火箭采用液氢/液氧燃料,假如一只火箭推进器携带
5×104 kg 氢气,理论上该火箭推进器中的氢气完全燃烧至少需要消耗多少千克
氧气?生成多少千克水?
解:设需要消耗的氧气的质量为 x,生成的水的质量为y。
1
H ~ — O ~ H O
2 2 2 2
2 16 18
5×104 kg x y
2 5×104 kg 2 5×104 kg
— = ————— — = —————
16 x 18 y
x = 4×105 kg y = 4.5×105 kg
答:燃烧5×104 kg 氢气,至少需要消耗 4×105 kg 氧气,生成 4.5×105 kg 水。
依据化学方程式进行计算,应遵守下列规则:
1.依据事实正确书写化学方程式。
2.根据问题解决要求假设未知量。
3.根据化学方程式或物质转化关系式,找出已知量与需要计算的未知量之间的
关系,列出关系式。
4.根据关系式进行计算,计算中涉及的物质的质量应是纯净物的质量。
5.完成计算后要进行检查。检查化学方程式是否正确,检查所列出的已知量和
未知量之间的关系是否正确,检查已知量和未知量的单位是否一致,检查解题过程
是否规范、正确等。
6.给出问题解决要求的答案。
126 化化 学学
HHUUAAXXUUEE课题 3 化学方程式及其应用
联系实际
基基于于化化学学方方程程式式进进行行计计算算
根据化学方程式的计算方法,完成下列计算,并与同学讨论你的计算过程和结果。
【问题】工业上用高温煅烧石灰石(主要成分是 CaCO ,假设杂质不参加反应)
3
的方法来生产生石灰。已知碳酸钙分解生成氧化钙(CaO)和二氧化碳,现要生产 2.8 t
生石灰,理论上至少需要多少吨碳酸钙?若石灰石中碳酸钙含量约为 80%,则实际至
少需要煅烧这样的石灰石多少吨?
依据化学反应方程式进行计算是化学定量分析的基础,在化工生产、科学研究
等领域具有广泛的应用。
阅读理解
基基于于化化学学方方程程式式的的计计算算方方法法的的应应用用
在化工生产和科学研究中,依据化学方程式进行计算的方法有如下应用。
11..确确定定反反应应的的投投料料比比。在化工生产和科学实验研究中,往往需要依据化学方程式
确定所需原料(反应物)的投料比。有时实际投料比与理论计算值有所差异,目的是
让某种反应物适当过量,而使另一种反应物能更多地转化为产物,以提高经济效益。
22..测测定定物物质质的的含含量量。化学中,人们通常会通过实验手段来测定混合物中某种物质
的含量或者纯净物的组成,会基于实验中所发生的化学反应方程式进行计算。金属矿
样中金属元素的含量、废水的成分、食盐中氯化钠(NaCl)的含量等,多数都是通过
这种计算得到的。
33..确确定定反反应应放放出出的的热热量量。化学反应过程中质量守恒,能量也守恒,所以基于化学
方程式,也能计算化学反应中放出多少热量。例如,通过计算可知,2 g氢气完全燃烧
需要16 g氧气,生成18 g液态水,同时放出286 kJ热量。
阅读上述资料并查阅其他相关资料,与同学讨论基于化学方程式的计算方法的应
用,并举例说明。
化化 学学 127
HHUUAAXXUUEE单元 5 表征化学反应
练习实践
MnO
1. 根据化学方程式2KClO =22KCl + 3O ↑,无法获取的信息是( )。
3 2
△
A. 反应所需条件 B. 生成物的状态
C. 生成物的化学计量数之比 D. 氧气具有助燃性
2. 偏二甲肼(C H N )和四氧化二氮(N O )是火箭常用推进剂之一,两种物
2 8 2 2 4
质发生反应的化学方程式为 C H N + 2N O =3N + 4X + 2CO ,则 X 的化学式为
2 8 2 2 4 2 2
( )。
A. NH B. H O C. O D. NO
3 2 2 2
3. 我国提出 2060 年前实现碳中和,彰显了负责任大国的作为与担当。捕集、利
用和封存二氧化碳是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁
(MgO)与二氧化碳反应生成碳酸镁(MgCO ),试书写该反应的化学方程式。
3
4. 碳酸氢铵(NH HCO )是一种常用化肥,又叫做碳铵。碳铵受热会分解,生
4 3
成氨气(NH )、水和二氧化碳。
3
(1)写出碳铵分解的化学方程式。
(2)计算碳铵中氮元素的质量分数。
(3)你认为该如何保存碳铵?
5. 工业上用一氧化碳高温还原赤铁矿(主要成分是质量分数为64% 的 Fe O )
2 3
高温
的方法冶炼铁,其化学方程式为 Fe O + 3CO=2Fe + 3CO 。若生产 56 t 铁,理论
2 3 2
上至少需要多少吨赤铁矿?
128 化化 学学
HHUUAAXXUUEE单元小结
单元小结
一、建构单元知识结构
原子重新组合
本质
质量守恒定律
遵循
点燃、加热、 条件
化学变化
添加催化剂等
表示 体现
化学实验 化学方程式
应用
定量研究物质转化
二、理解探究思路与方法
1.通过化学实验探究化学反应条件和质量守恒定律。
2.从微观粒子视角认识化学反应和质量守恒定律的本质。
3.在实际情境中规范表示化学反应。
4.根据化学方程式中各物质间的质量关系计算某一物质的质量。
三、形成单元大概念
物质在一定的条件下能发生化学变化。化学变化的本质是原子的重新组合。化学
变化遵循质量守恒定律,可用化学方程式表示化学变化。通过实验可探究化学反应条
件对化学变化的影响和化学变化中物质的质量关系。化学变化的定量研究在生产和生
活中具有广泛的应用。
化化 学学 129
HHUUAAXXUUEE单元作业
单元作业
1.实验室用过氧化氢制取氧气时,若不加入催化剂二氧化锰,其结果是( )。
A. 不会产生氧气 B. 足够长的时间内,收集到的氧气减少
C. 与加入二氧化锰相比,反应速率减慢D. 与加入二氧化锰相比,反应速率加快
2. 锂电池在生活中的使用越来越普遍。某类型的锂电池内发生的反应可表示为
Li + MnO ==== LiMnO (Li 在化合物中为 +1 价)。下列关于该反应的说法中,正确
2 2
的是( )。
A. 反应中二氧化锰是催化剂 B. 反应前后锰元素的化合价不变
C. 该反应为化合反应 D. 生成物 LiMnO 为氧化物
2
3.农业谚语“雷雨发庄稼”的化学原理是:在雷电和雨水作用下,空气中的氮气
发生一系列化学变化生成微量硝酸。反应过程如图1所示。
NO
单质X 单质X HO
N NO NO 2
2 2
① ② ③
HNO
图1 3
请回答下列问题。
(1)单质X是一种常见气体,其化学式是 。
(2)转化②属于基本反应类型中的 反应。
(3)转化③在常温下即可发生,该反应的化学方程式是 。
4. 图2是某化学反应的微观示意图,据此回答下列问题。
点燃
氢原子 氧原子 碳原子
图2
(1)根据微观示意图,写出该反应的化学方程式 。
(2)参加反应的分子数之比为 。
(3)生成物的质量比为 。
5. 46 g 纯净物 A 在空气中完全燃烧,产生了 88 g二氧化碳和 54 g 水,通过计算
确定A物质的化学式。
130 化化 学学
HHUUAAXXUUEE单元作业
6. 次氯酸钠(NaClO)等含氯消毒剂可有效灭活病毒。
利用图3所示装置,电解饱和氯化钠(NaCl)溶液可制取少
量次氯酸钠(NaClO)消毒液。电解过程中,a 极区生成氯气
(Cl ),b 极区生成气体单质 M 和氢氧化钠(NaOH)。
2
(1)气体 M 具有可燃性,其化学式为 。
(2)氯气与氢氧化钠反应生成次氯酸钠、氯化钠和水,
图3
该反应的化学方程式为 。
7.某补钙剂说明书的部分信息如图4所示。现将由 20 片该
“××”牌钙片
药剂制成的粉末与 40 g 盐酸混合(其他成分不与盐酸反应), 有效成分:碳酸钙
含钙量:0.2 g /片
恰好完全反应后称得剩余物的质量为 55.6 g。(碳酸钙与盐酸反
净含量:100 g
应的化学方程式为:CaCO
3
+ 2HCl=CaCl
2
+ H
2
O + CO
2
↑) 数量:100片/瓶
(1)20 片钙片与盐酸完全反应生成二氧化碳的质量为
图4
多少?
(2)该补钙剂每片含碳酸钙的质量为多少?
(3)通过计算说明该补钙剂的实际含钙量是否与说明书中的标注相符。
8. 碳酸氢钠(NaHCO )是面点膨松剂的主要成分之一,该物质与酸反应能释放出
3
二氧化碳。若其与硫酸反应,化学方程式为:
2NaHCO + H SO =Na SO + 2H O + 2CO ↑
3 2 4 2 4 2 2
某小组同学首先计算了 1.26 g 碳酸氢钠粉末与足量稀硫酸反应释放出的二氧化
碳的理论值,然后通过实验进行了探究:向盛有足量稀硫酸的锥形瓶中加入 1.26 g
碳酸氢钠粉末,完全反应至不再产生气泡,称取反应前后的质量。数据如表1所示。
表1
反应前质量/g 反应后质量/g
碳酸氢钠 锥形瓶+稀硫酸 锥形瓶+反应后溶液
1.26 24.59 25.36
(1)实验发现反应前后质量变化值 (填“大于”“小于”或“等于”)
生成的二氧化碳质量的理论值。
(2)查阅资料得到二氧化碳的物理性质:通常状况下,无色无味,呈气态,密
度约为空气的1.5倍,能溶于水,1 L水中大约能溶解1 L 二氧化碳气体。请分析理
论值与实验值不同的原因是什么。
化化 学学 131
HHUUAAXXUUEE项目学习
项目学习
用用传传感感器器技技术术探探究究反反应应条条件件控控制制
项目背景
数字化传感器是一种方便快捷的测量工具,在生产和生活中具有广泛的应用。人
体体温的测量、生活用水水质的分析等都会用到数字化传感器。数字化化学实验技
术是一种现代化的实验手段,其原理是用特定的传感器检测化学实验过程中物理量的
改变,通过数据采集器采集转换后输入到计算机,进行数据和图形分析、处理,得到
实验现象及结果,从而揭示化学反应现象和规律。
例如,过氧化氢的分解反应,就可以用数字化化学实验技术进行探究。将过氧化
氢置于密闭容器中进行分解反应,用传感器分别测定密闭容器中压强、温度、氧气体
积分数等随时间的变化情况,以探究反应条件对化学反应的影响。
项目建议方案
1. 查阅资料。查阅传感器使用说明,了解常见氧气传感器、压强传感器和温度传
感器的工作原理和使用方法,了解这些传感器的适用范围。
2. 调查研究。调查了解生产和生活中传感器的应用案例及使用效果。
3. 实验探究。(1)以过氧化氢分解为例,选择合适的实验装置及试剂用量,利用
相应的传感器测定该反应中物质及能量的变化;(2)用相应的传感器测量催化剂、溶
液浓度对过氧化氢分解速率的影响,分析实验数据,得到相关结论。
4. 成果展示。以“传感器技术及其应用”“影响过氧化氢分解速率因素的探究”
为题写出探究报告,并在全班进行展示与交流。
132 化化 学学
HHUUAAXXUUEE单元 6 探秘碳的世界
课题 1 神秘的碳家族
情境问题
丰丰富富多多彩彩的的含含碳碳物物质质
你知道吗,我们每时每刻都在接触与利用含有碳元素的物质。
墨汁 燃气 溶洞中的石笋
服装面料 食品 橡胶轮胎
图6-1-1 生活中常见的含有碳元素的物质
请与同学合作探究下列问题:
1.哪些物质含有碳元素?
2.含碳元素的化合物有哪些类型?
3.新型碳材料有怎样的发展和应用?
含有碳元素的物质是一个数目庞大的家族,在生产和生活中,含有碳元素的物
质触手可及,如各种塑料制品、天然和人造的服装面料、米饭和面条、橡胶轮胎等。
碳元素还是构成生命的基本元素之一,生命体中的蛋白质、糖类、脂肪等均含有碳
元素。在自然界中,碳元素既能以金刚石、石墨等单质形式存在,也能以化合物形
式分布于大气、海水、岩石中,如大气中的二氧化碳、地壳中的碳酸钙等。
134 化化 学学
HHUUAAXXUUEE课题 1 神秘的碳家族
交流讨论
认认识识含含碳碳元元素素的的物物质质
在之前的化学学习和日常生活中,你已经接触过一些含碳元素的物质,也知道它
们的一些性质和用途。请将你所知道的填入下表中,并与同学交流讨论。
含碳元素物质的名称 化学式 性质 用途
一、碳的单质
碳的单质有多种,如金刚石、石墨、富勒烯(如 C )、石墨烯等。虽然它
60
们都是由碳元素组成的,但性质和用途却相差很大。
观察思考
金金刚刚石石与与石石墨墨
图6-1-2中透明的晶体是金刚石,又称钻石,非常坚硬,可用于制作切削刀具和
钻头等;图6-1-3中深灰色物质是石墨,常用来制作铅笔芯、干电池的电极等。
金刚石和石墨元素组成相同,性质为何相差很大?请观察图中金刚石和石墨的结
构模型,思考二者的性质存在差异的主要原因。
金刚石晶体 镶金刚石的玻璃刀 金刚石结构模型
图6-1-2 金刚石结构及应用
化化 学学 135
HHUUAAXXUUEE单元 6 探秘碳的世界
石墨晶体 干电池中的石墨电极 石墨结构模型
图6-1-3 石墨结构及应用
金刚石、石墨是两种常见的碳单质。纯净的金刚石是无色透明的晶体,是自然
界中最坚硬的物质,耐磨性好,具有优良的透光性和耐腐蚀性,常用于制作钻探的
钻头,以及切割、切削、磨削的刀具等。石墨是一种深灰色的、有金属光泽而不透
明的细鳞片状固体,质软、能导电、有滑腻感,可用于制作电极、润滑剂等。石墨
与黏土等混合可制作铅笔芯。金刚石和石墨性质、用途的差异是由结构的差异决
定的。
人们还经常用到“炭”,如木炭、焦炭、活性炭、炭黑等,它们的主要成分也
是碳单质,结构与石墨类似,在生产和生活中具有广泛的应用。
实验探究
活活性性炭炭的的吸吸附附性性
通过下列实验(图6-1-4)探究活性炭对染料废水的脱色效果,并与同学交流讨
论所得结论。
步骤1 取1支洁净的U形管,向其中加入一些活性炭,
在U形管的两管口分别放入1个棉花团,用玻璃棒缓慢地
将棉花压至活性炭表面。
步骤2 在U形管左端缓慢加入约20 mL滴有红墨水的
水,观察比较U形管两管中液体的颜色。 图6-1-4 活性炭吸附实验
木炭、活性炭等具有疏松多孔的结构,具有强吸附性,常用作化工生产、食品
加工、水的净化等领域的吸附剂。
136 化化 学学
HHUUAAXXUUEE课题 1 神秘的碳家族
净化水 吸附细菌和有毒气体
图6-1-5 活性炭的用途
阅读理解
文文房房四四宝宝之之““墨墨””
纸、墨、笔、砚被称为“文房四宝”,是我国传统文化
的一种象征,闪耀着独特的艺术光芒。我国明代《天工开物》
中就有制墨的记载:“凡墨,烧烟凝质而为之。取桐油、清
油、猪油烟为者,居十之一,取松烟为者,居十之九”,“凡
松烟造墨,入水久浸,以浮沉分清悫(què)”。
上述记载中简要说明了制墨的原理:将桐油、猪油或松
图6-1-6 文房四宝
木(枝)等进行不完全燃烧,取其黑色粉状物质(烟灰)加
水、加胶制成液体,再浇注在模具中,干燥后即成墨。
我们在家中也可以通过燃烧食用油观察到“烧烟凝质”
的现象:向1个小瓷碗中倒入少量食用油,在油中放置1根
粗棉线(图6-1-7),点燃棉线,将一块洁净干燥的白瓷板
置于火焰的侧上方,就可观察到白瓷板上积累了一层炭黑。
请思考下列问题:
1.桐油、猪油、松枝等燃烧产生的烟灰的主要成分是碳,
说明桐油、猪油、松枝中含有什么元素? 图6-1-7 “烧烟”实验
2.生活中还可以通过什么方法得到少量炭黑?
焦炭是煤在隔绝空气的条件下,加热到 950 ~ 1 050 ℃,经过高温炼焦过程制
得的,主要成分是碳。焦炭是金属冶炼的重要原料。
随着科学技术的不断发展,碳单质的成员不断增多。20 世纪 80 年代,科学家
发现了另一种碳单质 —— C 。这种碳单质由分子构成,每个分子由 60 个碳原子结
60
化化 学学 137
HHUUAAXXUUEE单元 6 探秘碳的世界
合成形似足球的形状。随后科学家又发现了C 、C 等碳单质。20世纪90年代,
70 76
科学家又发现了一种更加奇特的碳单质——碳纳米管。人们把完全由碳组成的形状
呈球型、椭球型、柱型或管状的中空分子统称为富勒烯。21 世纪初,来自英国曼
彻斯特大学的两位科学家,又制得了仅由一层碳原子构成、具有石墨层状结构的石
墨烯。
C 碳纳米管 石墨烯
60
图6-1-8 富勒烯和石墨烯结构模型
交流讨论
碳碳材材料料的的应应用用
碳单质在生产、生活中有着广泛的应用。目前,以富勒烯和石墨烯为代表的碳材
料更是为人类打开了一个全新的碳材料世界的大门。
1.通过查阅资料,了解碳材料已有的应用和可能的应用前景,并与同学分享你了
解的结果。
2.我国科学家在新型碳材料的制备和应用方面作出了巨大贡献。请查找这方面的
事例,并将你的感悟写成小作文在班级中进行交流。
二、有机化合物
化学上通常将含有碳元素的化合物称为有机化合物,而将水(H O)、硫酸
2
(H SO )、氯化钠(NaCl)等不含碳元素的化合物称为无机化合物。一氧化碳
2 4
(CO)、二氧化碳(CO )、碳酸(H CO )、碳酸钙(CaCO )等虽然也含有碳
2 2 3 3
元素,但由于其性质与无机化合物相似,仍被归类为无机化合物。
绝大多数有机化合物除含碳元素外,还含有氢元素,许多还含氧、氮、氯、硫
和磷等元素。目前已知的有机化合物已经超过8 000万种。
138 化化 学学
HHUUAAXXUUEE课题 1 神秘的碳家族
交流讨论
含含碳碳元元素素物物质质的的分分类类
下列物质都含有碳元素:石墨(C)、二氧化碳(CO )、甲烷(CH )、纯碱
2 4
(Na CO )、乙醇(C H O)、醋酸(又称乙酸,CH COOH)、碳酸(H CO )、葡
2 3 2 6 3 2 3
萄糖(C H O )。
6 12 6
请按下列方式对上述物质进行分类。
单质
含有碳元素的物质
无机化合物
化合物
有机化合物
甲烷(CH )是最简单的有机化合物,是天然气的主要成分。甲烷是重要的化
4
工原料和常用燃料。甲烷燃烧能放出大量的热,为人类生产和生活提供热能。
点燃
CH + 2O = CO + 2H O
4 2 2 2
乙醇(俗称酒精,化学式为 C H O)是一种常见
2 6
的有机物,是酒的主要成分之一。我国是世界上最早
掌握酿酒技术的国家,有着悠久的酿酒历史。乙醇在
常温常压下是一种易燃、易挥发的无色透明液体,
可用作燃料。乙醇蒸气能与空气形成具有爆炸性的混
合物,因此,乙醇需要密封保存,并要远离火源。医
疗上常用 75% 的乙醇作消毒剂。乙醇还是一种重要
的原料,被广泛应用于化学工业、医疗卫生、食品工
业、农业生产等领域。
图6-1-9 75%的乙醇用于消毒杀菌
交流讨论
有有机机化化合合物物的的组组成成、、性性质质与与应应用用
联系生活经验,查阅有关资料,将你知道的有机化合物的组成、性质和用途填入
表中,并与同学交流讨论。
化化 学学 139
HHUUAAXXUUEE单元 6 探秘碳的世界
物质名称 化学式 主要性质 主要用途
葡萄糖 C H O 与氧气反应放热 为生命活动提供能量
6 12 6
有机化合物数量众多,自然界的动植物体内含有有机物;化石燃料中含有
大量有机物;人工合成的塑料、橡胶、纤维也是有机物 …… 有机物应用广泛,
人类生产、生活的方方面面都离不开有机物。
图6-1-10 有机物具有广泛的应用
140 化化 学学
HHUUAAXXUUEE课题 1 神秘的碳家族
练习实践
1.下列物质的性质与用途不具有对应关系的是( )。
A.金刚石硬度大,可用于制作钻戒 B.石墨具有导电性,可制作电极
C.活性炭具有吸附性,可用于净水 D.焦炭具有可燃性,可用作燃料
2.我国科学家屠呦呦因发现了抗疟病的药物——青蒿素而获得了诺贝尔奖。青蒿
素属于有机物,青蒿素中一定含有的元素是( )。
A. C B. Ca C. Mg D. Fe
3. C 在众多领域中具有广阔的应用前景。关于C 叙述不正确的是( )。
60 60
A.该物质由C 分子构成 B.该物质由60个碳原子构成
60
C.其相对分子质量为720 D. C 和C 是两种物质
60 70
4.下面是厨房中常用的物质,括号内列出了它们的主要成分,将这些成分按有机
化合物、无机化合物进行分类。
食盐(NaCl) 食用碱(Na CO ) 食用醋(CH COOH)
2 3 3
水(H O) 食用小苏打(NaHCO ) 白砂糖(C H O )
2 3 12 22 11
有机化合物: 。
无机化合物: 。
5. 各种饮用酒和一些消毒剂中都含有乙醇,乙醇属于 (填“有机化
合物”或“无机化合物”);乙醇是由乙醇分子构成的,分子中碳、氢、氧三种元素
的原子个数比是 ;乙醇可由粮食发酵获得,可作为一种生物燃料以减少
化石燃料的使用量,乙醇完全燃烧的产物是 。
6. 判断下列有关金刚石和石墨的说法是否正确。如果不正确,请说出理由。
(1)两者都是由碳元素组成的黑色固体。
(2)构成两者的微粒不同,所以性质上有许多差异。
(3)常温下化学性质都不活泼。
(4)完全燃烧后的产物都是二氧化碳。
化化 学学 141
HHUUAAXXUUEE单元 6 探秘碳的世界
课题 2 二氧化碳的性质与应用
情境问题
身身边边的的二二氧氧化化碳碳
二氧化碳是我们最熟悉的物质之一,空气中含有一定量的二氧化碳,生命体的呼
吸作用会产生二氧化碳,在生产、生活中我们也会使用二氧化碳。
二氧化碳用于灭火 二氧化碳用作气体肥料 干冰(固态二氧化碳)用于人工降雨
图6-2-1 二氧化碳的应用
请与同学合作探究下列问题:
1.二氧化碳有哪些性质和用途?
2.如何在实验室制取少量二氧化碳?
一、二氧化碳的性质和用途
通常状况下,二氧化碳是一种无色、无味的气体,但在加压、降温条件下,二
氧化碳气体可转变为液体或固体。固态二氧化碳外形与冰相似,所以被称为“干
冰”。二氧化碳还有哪些性质?下面我们通过实验进行探究。
实验探究
二二氧氧化化碳碳性性质质的的实实验验探探究究((一一))
【提出问题】许多类型的灭火器主要利用二氧化碳来灭火。为什么二氧化碳能够
灭火?
142 化化 学学
HHUUAAXXUUEE课题 2 二氧化碳的性质与应用
【形成假设】 根据燃烧和灭火的原理,可以推测:可燃物在二氧化碳中不能燃烧,
二氧化碳可以降低可燃物上方氧气的浓度,甚至使可燃物与空气隔离。
【实验探究】 按照下列实验方案验证假设是否正确。
实实验验1 将 CO 气体通入盛有 2 mL 澄清石灰水的试管中(图 6-2-2),观察实
2
验现象;将 CO 充满两个集气瓶。
2
实实验验2 将燃着的木条放在集满CO 的集气瓶口(图 6-2-3),观察实验现象。
2
实实验验3 点燃2支短蜡烛,放在烧杯中一高一低的两个“阶梯”上(图 6-2-4),
沿烧杯内壁缓慢倾倒另一个集气瓶中的CO 气体,仔细观察实验现象。
2
澄清
石灰水
图6-2-2 将CO 通入 图6-2-3 将燃着的木条靠近 图6-2-4 倾倒 CO
2 2
澄清石灰水中 集满CO 的集气瓶口
2
【证据及结论】将上述实验中观察到的现象填入下表中,依据实验现象推理二氧
化碳的性质,并解释二氧化碳能灭火的原因。
实验 实验现象 二氧化碳的性质
1
2
3
由上述实验可知,二氧化碳与澄清石灰水中的氢氧化钙 [Ca(OH) ] 反应生成碳
2
酸钙(CaCO )白色沉淀。人们常用这一方法检验二氧化碳气体。
3
CO + Ca(OH) = CaCO ↓+ H O
2 2 3 2
二氧化碳不能燃烧,一般也不支持燃烧。当用燃着的木条靠近集满二氧化碳的
集气瓶口时,木条上的火焰会熄灭。实验室常用这种方法检验集气瓶中的二氧化碳
是否集满。二氧化碳气体的密度比空气的密度大(约为空气的 1.5 倍),能覆盖
化化 学学 143
HHUUAAXXUUEE单元 6 探秘碳的世界
在可燃物表面,使可燃物与空气隔离,因此,二氧化碳常用于灭火。
实验探究
二二氧氧化化碳碳性性质质的的实实验验探探究究((二二))
【提出问题】加工碳酸饮料时通常要向饮料瓶中充入二氧化碳气体。充入二氧化
碳气体的饮料为何被称为碳酸饮料?
【形成假设】二氧化碳可溶解于水中,并与水反应生成碳酸,因而这种饮料被称
为碳酸饮料。
【设计方案】查阅资料得知,紫色石蕊溶液在碳酸溶液中由紫色转变为红色。为
此可设计如下检验假设的实验方案: 。
【实验探究】按照你设计的实验方案进行实验。你也可以按照下列实验方案进行
探究。
实实验验1 向集满CO 气体的、质地较软的矿泉水瓶中加入约 1/3 体积的水(图 6-2-5),
2
旋紧瓶盖,振荡,观察矿泉水瓶发生的变化。
实实验验2 在试管中加入2 mL蒸馏水,滴加2滴紫色石蕊溶液,向其中通入CO 气
2
体(图 6-2-6),一段时间后,观察试管中溶液颜色的变化。
实实验验3 加热上述试管(图 6-2-7),使试管中的液体沸腾,再观察液体的颜色变化。
水
二氧化碳
图6-2-5 CO 溶于水 图6-2-6 CO 与水的反应 图6-2-7 加热碳酸溶液
2 2
【证据及结论】将上述实验中观察到的现象填入下表中,依据实验现象推理二氧
化碳的性质。
实验 实验现象 二氧化碳的性质
1
2
3
144 化化 学学
HHUUAAXXUUEE课题 2 二氧化碳的性质与应用
二氧化碳能溶于水,通常状况下 1 L 水中大约能溶解 1 L 二氧化碳气体。与氧
气等气体一样,二氧化碳在水中溶解的量也与温度和气体的压强有关。温度越低、
气体压强越大,二氧化碳在水中溶解的量就越多。溶解在水中的二氧化碳少部分能
与水发生化学反应,生成一种酸性物质——碳酸(H CO )。碳酸能使紫色石蕊溶
2 3
液变成红色,但碳酸不稳定,受热容易分解成二氧化碳和水,所以当二氧化碳从溶
液中逸出后,红色石蕊溶液又重新变成紫色。
CO + H O = H CO
2 2 2 3
H CO = CO ↑+ H O
2 3 2 2
干冰易升华(不经过液态而直接转变为
气态),升华时吸收大量的热,因此常用在
食品等的冷藏储存和运输中。遇干旱天气
时,干冰还可用于人工降雨。飞机在云层中
播撒干冰后,干冰升华吸热使空气中的水蒸
气迅速冷凝变成水滴,从而形成降雨。 图6-2-8 干冰用于食品保鲜
二氧化碳还能参与绿色植物的光合作用,所以农业上常将二氧化碳作为气体肥
料使用。
二氧化碳不能供给呼吸,人在二氧化碳含量偏高的环境中,会感觉胸闷、窒息
乃至死亡。因此,在人群密集的地方要注意通风换气。
二、二氧化碳的制取
在工业上,人们常采用高温分解石灰石(主要成分为碳酸钙)的方法来制备纯
度较高的二氧化碳。
高温
CaCO = CaO + CO ↑
3 2
在实验室中,人们常利用稀盐酸与石灰石的反应来制取少量二氧化碳。
CaCO + 2HCl = CaCl + CO ↑+ H O
3 2 2 2
化化 学学 145
HHUUAAXXUUEE单元 6 探秘碳的世界
实验探究
实实验验室室制制取取少少量量二二氧氧化化碳碳
1.设设计计气气体体制制取取装装置置
根据实验室制取二氧化碳的原理,选择制取二氧化碳的试剂和仪器,设计制备和
收集二氧化碳的实验装置,并与老师和同学交流讨论。
2.确确定定制制取取二二氧氧化化碳碳气气体体的的实实验验操操作作步步骤骤
按照与老师和同学讨论过的二氧化碳气体制取装置,确定制取二氧化碳的实验操
作步骤。
3.制制取取二二氧氧化化碳碳气气体体
搭建二氧化碳制备和收集装置,按你确定的实验操作步骤制取一集气瓶二氧化
碳,并检验是否集满。
你也可以按下列方案制取二氧化碳:
(1)按图 6-2-9 所示连接装置,并检验装置气
稀盐酸
密性。
(2)取少量碎块状石灰石放入锥形瓶中,向分液
漏斗中加入适量稀盐酸。从分液漏斗中滴加适量稀盐酸
石灰石
于锥形瓶中,用向上排空气法收集二氧化碳气体。
(3)将燃着的木条置于集气瓶瓶口,检验二氧化 图6-2-9 制取二氧化碳
的实验装置
碳是否集满。
方法引导
实验室制取气体的方法
实验室中通过化学反应制取少量气体时,首先要依据化学反应中元素不变的原
理,思考选择何种原料(反应物)、通过何种反应、控制怎样的条件制取气体,以确
定气体制取的原理,然后根据反应物的状态和反应的条件设计气体制备装置,并根据
气体的性质确定气体收集装置。常见的气体制备和收集装置如图6-2-10和图6-2-11
所示。
146 化化 学学
HHUUAAXXUUEE课题 2 二氧化碳的性质与应用
反应物:固体或“固体+固体” 反应物:“固体+液体”或“液体+液体”
反应条件:加热 反应条件:不需要加热
图6-2-10 常见的气体制备装置
向下排空气法 向上排空气法 排水法
图6-2-11 常见的气体收集装置
制取气体时,通常要经过搭建装置、检验装置气密性、制备气体、净化气体、收
集气体、验满气体等步骤。若制取的气体或者在制取过程中产生的气体对环境有害,
要设计相应的尾气处理装置。
阅读理解
二二氧氧化化碳碳的的获获取取与与应应用用
二氧化碳的获取按其来源可分为两类:一类来源于二氧化碳气田,另一类来源于
工业副产品。
在石油和天然气开采过程中,有时会发现具有开发利用价值的高浓度二氧化碳气
田。工业副产品二氧化碳主要来源于工业制氢过程、石灰生产过程和粮食发酵过程等。
无论是天然二氧化碳气田,还是工业副产品二氧化碳,经过干燥、除尘、提纯
等工艺后,就可以分装使用。
二氧化碳具有广泛的应用。二氧化碳可用作绿色植物光合作用的原料。工业上
化化 学学 147
HHUUAAXXUUEE单元 6 探秘碳的世界
常以二氧化碳为原料生产纯碱、碳酸氢铵、尿素等。食品加工行业用二氧化碳储藏
食物,生产碳酸饮料、啤酒等。固态二氧化碳可用于人工降雨等。在催化剂作用下,
通过化学反应,二氧化碳还可以转化为乙醇、乙酸、葡萄糖等有机化合物。
阅读上述资料,与同学交流讨论下列问题:
1.还有哪些方法可以获取较纯的二氧化碳?
2.大气中二氧化碳含量的增加将会导致环境问题。如何充分利用二氧化碳并减少
二氧化碳向大气中排放?
练习实践
1.下列关于物质的性质和用途的叙述不正确的是( )。
A. 二氧化碳不可燃,一般也不助燃,可用于灭火
B. 氮气化学性质稳定,可用作粮食、瓜果的保护气
C. 生石灰有强烈的吸水性,可用作食品干燥剂
D. 液态氧气具有助燃性,可用作火箭推进燃料
2. 下列说法中正确的是( )。
A. 能使燃着的小木条火焰熄灭的气体一定是二氧化碳
B. 二氧化碳能使紫色石蕊溶液变红
C. 若图书档案室发生火灾,应采用液态二氧化碳灭火器灭火
D. 空气中二氧化碳含量的多少与人类健康无关
3.请根据下列装置图回答问题。
A B C D E
(1)实验室制取少量二氧化碳可选用 (填字母)作为气体制备装置,装
置内发生的化学反应方程式可表示为 。
(2)收集二氧化碳的装置可选用 (填字母),其原因是 ,
148 化化 学学
HHUUAAXXUUEE课题 2 二氧化碳的性质与应用
验满二氧化碳的操作和现象是 。
4. 利用化学知识说明下列行为的道理或产生现象的原因。
(1)在教室中学习时,不能长时间紧闭门窗。
(2)种植大棚蔬菜时,向大棚内通入适量的二氧化碳气体可使蔬菜生长得更
旺盛。
(3)进入久未开启的菜窖前,应先检查二氧化碳浓度是否太高。
(4)盛放石灰水的试剂瓶放置时间过久,在瓶内会形成一层白色物质。
(5)在养鱼的缸里经常放一些水草。
5. 一氧化碳和二氧化碳是两种碳的氧化物,在生产中都具有广泛应用。
(1)指出两种物质中碳元素的化合价,并分别计算一氧化碳、二氧化碳中碳元素
的质量分数。
(2)用化学方程式表示一氧化碳和二氧化碳的相互转化。
(3)举例说明一氧化碳、二氧化碳在生产中的应用。
(4)以煤的燃烧为例,说明减少一氧化碳的释放可采取的措施。
化化 学学 149
HHUUAAXXUUEE单元 6 探秘碳的世界
课题 3 碳循环与碳中和
情境问题
我我国国实实现现碳碳中中和和的的目目标标
中国政府在第75届联合国大会上提出:“中国将提高国家自主贡献力度,采取更
加有力的政策和措施,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前
实现碳中和。”
你一定想知道:
1.何谓碳中和?碳中和与碳循环之间是何种关系?
2. 为何要实现碳达峰、碳中和?
3. 如何实现碳达峰、碳中和?
一、自然界的碳循环
含碳元素的物质在自然界中分布广泛。在岩石圈中,碳元素主要以金刚石、
石墨、石灰石、化石燃料等物质形式存在;在大气圈中,二氧化碳和一氧化碳是
主要的含碳物质;在水圈中,碳元素存在于水生生物合成的有机物里,也存在于
溶解在水中的二氧化碳和碳酸中;在生物圈中,绿色植物通过光合作用生成的有
机物及动物体的有机物是碳元素主要的储存体。
地球上生物圈、岩石圈、水圈及大气圈中含碳元素的物质不断发生着转化,
并随地球的运动循环不止,这一过程称为碳循环(图 6-3-1)。
在生物圈中,光合作用吸收大气中的二氧化碳,呼吸作用向大气中排放二氧化
碳。大气中的二氧化碳可溶解在海水、雨水和地下水中(溶解在水中的二氧化碳部
分形成碳酸),水中的二氧化碳也能进入大气中,大气中二氧化碳的量增多,海洋
吸收的二氧化碳量也随之增多。在长期的物理和化学作用下,地壳中的石灰岩等物
质中含有的碳元素以二氧化碳的形式释放进入大气中,溶解了二氧化碳的水也能把
石灰岩等变为可溶态的碳酸氢盐,碳酸氢盐在江河湖海中通过不同的成岩过程又形
成石灰岩。
150 化化 学学
HHUUAAXXUUEE课题 3 碳循环与碳中和
二氧化碳
释 吸
放 收
光合作用
工厂和
车辆排放
海洋
动植物呼吸
化石燃料
图6-3-1 自然界的碳循环
阅读理解
溶溶洞洞的的形形成成
自然界的溶洞中有千姿百态的石笋、石柱和石钟
乳,有潺潺的地下河流,洞中有洞,洞中有河,使游人
如入仙境,流连忘返。制造这些美丽溶洞的“主角”是
碳酸钙、二氧化碳和水。形成溶洞的地下岩石是石灰
石,石灰石中的碳酸钙遇到溶有二氧化碳的水时,会
生成可溶性的碳酸氢钙。
图6-3-2 自然界的溶洞
CaCO + CO + H O = Ca(HCO )
3 2 2 3 2
如果受热或大气压强变小,溶解在水中的碳酸氢钙又会分解转化成不溶性的碳酸
钙重新沉积下来。
Ca(HCO ) = CaCO ↓ + CO ↑ + H O
3 2 3 2 2
石灰石长年累月进行着上述反应。溶洞中的石笋、石柱和石钟乳就是这样形成的。
化化 学学 151
HHUUAAXXUUEE单元 6 探秘碳的世界
阅读材料内容,思考下列问题:
1.溶洞的形成过程涉及哪些含碳元素的化合物?这些物质分别分布于哪些圈层?
2.在溶洞的形成过程中,哪些过程吸收二氧化碳?哪些过程释放二氧化碳?
由于自然界的碳循环,大气中二氧化碳产生和消耗的量能基本保持平衡,使得
大气中二氧化碳的含量基本恒定。
二、碳达峰与碳中和
二氧化碳产生和消耗的过程涉及大气圈、水圈、岩石圈以及动植物的生长和
人类的各种活动,因而大气中二氧化碳的含量对人类的生存、生活及生态平衡意
义重大。
交流讨论
二二氧氧化化碳碳与与人人类类生生活活
结合已有的知识与经验,与同学交流讨论下列问题:
1. 自然界通过哪些途径向大气中排放二氧化碳?通过哪些途径消耗大气中的二
氧化碳?
2. 人类的哪些活动增加了二氧化碳的排放量?
3.向大气中排放二氧化碳的量增加对环境产生了哪些影响?
在自然界中,除火山喷发、生物的呼吸会释放二氧化碳,有机物在分解、变
质过程(包括动植物遗体腐烂过程)中也会向大气中释放二氧化碳。人类生产和
生活中,化石燃料的燃烧、金属的冶炼和加工也会向大气中释放大量的二氧化碳。
此外,大片森林被人为砍伐,森林吸收二氧化碳的量下降,也是大气中二氧化碳
的量逐渐增加的原因之一。
空气中二氧化碳量的增加是导致温室效应的原因之一。二氧化碳量的增加虽不
影响太阳对地球表面的辐射,但却阻碍由地面反射回高空的红外辐射,阻止地球表
面的热量向外发散,导致地球表面的平均气温上升。温室效应对人类生存环境会产
152 化化 学学
HHUUAAXXUUEE课题 3 碳循环与碳中和
生诸多不良的影响。
冰川融化,海平面上升 土地沙漠化 极端气候事件频发
图6-3-3 温室效应对人类生存环境产生的不良影响
控制二氧化碳的排放量是一个牵涉面极广、非常艰巨且长期的工作。目前,
人类正通过多种手段力争减缓二氧化碳排放量的增长速度。当一个国家年度二氧
化碳排放量达到历史最高值后,将会经历平台期进入持续下降的状态。人们将二
氧化碳排放量由增转降的历史拐点称为碳达峰。我国向世界承诺:二氧化碳排放
力争于 2030 年前达到峰值。
碳中和通常是指一个国家在一定时间内直接或间接产生的二氧化碳或温室气
体排放总量,通过植树造林、节能减排等形式,以抵消自身产生的二氧化碳或温
室气体排放量,实现正负抵消,达到相对“零排放”。我国向世界承诺:努力争
取 2060 年前实现碳中和。
实现碳达峰和碳中和,一方面要减少碳排放,另一方面要增加碳吸收和碳
利用。目前,科学家已经研制出多种捕集和利用二氧化碳的方法。
交流讨论
碳碳捕捕集集和和碳碳利利用用
燃烧化石燃料排放的烟气中含有大量二氧化碳。可对烟气进行除尘、除二氧化
硫和氮氧化合物处理,并用物理、化学等方法将二氧化碳捕集起来,再将烟气排
放到大气中,以减少向大气中排放二氧化碳的量。捕集得到的二氧化碳,既可转
化利用,也可封存到海底和地壳的岩石层间隙中。
化化 学学 153
HHUUAAXXUUEE单元 6 探秘碳的世界
烟气排放
碳利用
含有二氧化碳的烟气 碳捕集 二氧化碳气体
碳封存
图6-3-4 烟气中二氧化碳的捕集及利用
通过查阅相关资料,与同学讨论下列问题:
1.烟气中的二氧化碳可通过哪几种方法进行捕集?捕集烟气中的二氧化碳利用了
二氧化碳的哪些性质?
2.目前科学家研究了多种利用二氧化碳的方法,了解我国科学家在利用二氧化碳
方面所取得的成果。
实验探究
探探究究二二氧氧化化碳碳的的捕捕集集方方法法
根据下列实验选择合适的吸收二氧化碳的试剂。
步骤 1 在 3 个相同容量的软质矿泉水瓶中集满
350 mL塑料瓶
CO ,在瓶身上标记即将要加入的试剂名称。
2
步骤2 分别将 20 mL 水、饱和澄清石灰水、2%的
充满CO
2
氢氧化钠(NaOH)溶液倾倒入3个烧杯中,然后小组成
20 mL吸收剂
员协作,同时将它们倒入相应的矿泉水瓶中,立即盖上
图6-3-5 比较几种试剂吸收
瓶盖,振荡,比较矿泉水瓶变瘪的程度。 CO 程度的实验装置
2
根据观察到的现象,选择你认为合适的吸收二氧化碳的试剂,并说明理由。
实现碳达峰、碳中和是一场广泛而深刻的经济社会系统性变革,需要全民践
行绿色低碳生活;需要世界各国协同构建人类环境保护共同体;需要多领域共同
努力创新低碳技术,开发新能源,进行能源绿色低碳转型;需要研究二氧化碳的
捕集、封存与利用技术 …… 作为一名学生,我们要积极践行低碳生活,努力学习,
发挥自己的才能,保护我们的地球家园。
154 化化 学学
HHUUAAXXUUEE课题 3 碳循环与碳中和
联系实际
低低碳碳生生活活
低碳生活意味着在日常生活中尽可能直接或间接减少化石能源的消耗,从而降低
二氧化碳的排放量。请分析下列行为能减少二氧化碳排放的原因,并思考生活中我们
还可以在哪些方面减少碳排放。
倡导步行和骑自行车 不用或少用一次性筷子 夏天空调温度不低于26 ℃
使用太阳能热水器沐浴 垃圾分类及回收 电器不使用时关闭电源
图6-3-6 生活中的低碳行动
练习实践
1. 使用绿色能源是减少碳排放的主要途径。下列几种燃料中,最理想的绿色燃料
是( )。
A. 优质煤 B. 氢气 C. 汽油 D. 天然气
2.中国政府制定了力争 2030 年前实现碳达峰、2060 年前实现碳中和的行动方
案。下列符合这一要求的举措是( )。
①大力发展绿色公共交通;②开发太阳能、水能、风能等新能源;③减少使用煤、
石油、天然气等化石燃料;④大力植树造林,禁止乱砍滥伐。
A.①②③④ B.②③④ C.①②④ D.①②③
3. 科学家发明了一种利用二氧化碳的新技术,将二氧化碳和氢气以一定比例混
一定条件
合,在一定条件下使其发生如下反应:2CO + 6H = 4H O + X。请推测 X 的化
2 2 2
学式,并说明理由。
4. 一些城市在大型建筑的屋顶种植草类、花卉等以美化环境。请说明“绿色屋
顶”还具有哪些优点。
化化 学学 155
HHUUAAXXUUEE单元 6 探秘碳的世界
5. 阅读下列资料,回答相关问题。
推动绿色发展,促进人与自然和谐共生
大自然是人类赖以生存发展的基本条件。尊重自然、顺应自然、保护自然,是全
面建设社会主义现代化国家的内在要求。必须牢固树立和践行绿水青山就是金山银山
的理念,站在人与自然和谐共生的高度谋划发展。
我们要推进美丽中国建设,坚持山水林田湖草沙一体化保护和系统治理,统筹产
业结构调整、污染治理、生态保护、应对气候变化,协同推进降碳、减污、扩绿、增长,
推进生态优先、节约集约、绿色低碳发展。
(一)加快发展方式绿色转型。推动经济社会发展绿色化、低碳化是实现高质量
发展的关键环节。加快推动产业结构、能源结构、交通运输结构等调整优化。实施全
面节约战略,推进各类资源节约集约利用,加快构建废弃物循环利用体系。完善支持
绿色发展的财税、金融、投资、价格政策和标准体系,发展绿色低碳产业,健全资源
环境要素市场化配置体系,加快节能降碳先进技术研发和推广应用,倡导绿色消费,
推动形成绿色低碳的生产方式和生活方式。
……
(四)积极稳妥推进碳达峰碳中和。实现碳达峰碳中和是一场广泛而深刻的经济
社会系统性变革。立足我国能源资源禀赋,坚持先立后破,有计划分步骤实施碳达峰
行动。完善能源消耗总量和强度调控,重点控制化石能源消费,逐步转向碳排放总量
和强度“双控”制度。推动能源清洁低碳高效利用,推进工业、建筑、交通等领域清
洁低碳转型。深入推进能源革命,加强煤炭清洁高效利用,加大油气资源勘探开发和
增储上产力度,加快规划建设新型能源体系,统筹水电开发和生态保护,积极安全有
序发展核电,加强能源产供储销体系建设,确保能源安全。完善碳排放统计核算制度,
健全碳排放权市场交易制度。提升生态系统碳汇能力。积极参与应对气候变化全球
治理。
(摘自习近平《高举中国特色社会主义伟大旗帜 为全面建设社会主义现代化国家
而团结奋斗——在中国共产党第二十次全国代表大会上的报告》)
(1)判断下列哪些垃圾的主要成分为有机化合物,哪些属于可回收垃圾。
① 铁质衣架;② 碎玻璃;③ 废轮胎;④ 废纸;⑤ 塑料盆。
(2)请结合材料内容,简要概括实现碳达峰和碳中和我们需要做的努力,以
及实现后我们生活的改变。
156 化化 学学
HHUUAAXXUUEE单元小结
单元小结
一、建构单元知识结构
在自然界存在
含有碳元素的物质 碳循环
包括
碳单质 含碳无机化合物 有机化合物
属于 制备方法
光合作用
葡萄糖 二氧化碳 主要性质
排放与吸收平衡 实际应用
碳中和
二、理解探究思路与方法
1.联系日常生活实际,认识含碳元素物质的多样性及其广泛的应用。
2.通过实验探究学习二氧化碳的性质、制取及其应用。
3.基于化学变化中元素不变的视角认识碳循环和碳中和的原理,从辩证的视角认
识空气中二氧化碳的作用。
三、形成单元大概念
丰富多彩的含碳元素的物质,如碳材料、有机化合物等,在生产和生活中具有广
泛的应用。二氧化碳在碳循环和碳中和目标中担任重要角色。通过化学实验可探究二
氧化碳的性质及其应用。空气中的二氧化碳是光合作用的重要原料,但过量的二氧化
碳会导致气候变暖等环境问题。实现碳中和目标需要人们养成节能低碳的生活习惯,
需要化学等科学在二氧化碳的转化利用等方面作出贡献。
化化 学学 157
HHUUAAXXUUEE单元作业
单元作业
1. 下列物质是一些医用品的主要成分,其中属于无机化合物的是( )。
A. 用于制造医用口罩的聚丙烯 B. 消毒液的主要成分过氧化氢
C. 医用酒精中的乙醇 D. 制备乳胶手套的丁腈橡胶
2. C 和 C 是具有广阔应用前景的碳材料。下列对这两种物质的表达中,错误的
60 70
是( )。
A. 它们都是由碳元素组成的单质 B. 它们是两种新型化合物
C. 它们都是由分子构成的 D.它们的相对分子质量差是 120
3.科技人员研制出了一种自动灭火陶瓷砖,砖里压入了一定量的氦气和二氧
化碳。这种砖砌成的房屋发生火灾时,在高温烘烧下,砖会裂开并喷出氦气和二
氧化碳,从而抑制和扑灭火焰。自动灭火陶瓷砖的灭火原理是( )。
A. 清除可燃物 B. 降低燃烧区域的氧气浓度
C. 降低可燃物的着火点 D. 使温度降低到可燃物的着火点以下
4.利用下图所示装置,能完成实验室相关气体制取的是( )。
① ② ③ ④
A.用①④制取氧气 B.用②③制取二氧化碳
C.用②③制取氧气 D.用①③制取二氧化碳
5. 自然界中时刻进行着碳循环和氧循环,两者密切联系,互相交织。请结合氧循
环图和碳循环图,分析有哪些过程在消耗 O 的同时产生 CO ,有哪些过程在消
2 2
耗 CO 的同时产生 O 。试写出它们的化学方程式,并说明这些过程对保持大气中氧
2 2
气、二氧化碳含量相对稳定的重要性。
6. 解释下列现象或行为。
(1)在书写具有保存价值的档案时,一般使用碳素墨水。
(2)抹过石灰浆(熟石灰与水的混合物)的墙壁,一段时间后会变得坚硬。
(3)放置在蜡烛火焰上方的冷白瓷碟子,一段时间后出现少量黑色物质。
158 化化 学学
HHUUAAXXUUEE单元作业
7. 有4瓶无色无味的气体,可能是氧气、空气、氮气和二氧化碳。如何用简单的
实验方法将它们区分开来?
8. 一化学兴趣小组在实验室中进行如下实验探究:
实验 1 取一段铅笔芯放在酒精灯火焰上加热。
实验 2 用小刀削少许铅笔芯粉末于一白纸上,用手指触摸铅笔芯粉末。
实验3 如图1所示,把铅笔芯串联在一个电路中,
观察灯泡是否会发亮。 电池
请依据上述实验方案,预测实验中可能观察到的现
铅笔芯
象,归纳石墨的性质,并根据石墨的性质说一说石墨的
用途。
图1
化化 学学 159
HHUUAAXXUUEE项目学习
项目学习
探探秘秘大大棚棚蔬蔬菜菜种种植植中中的的二二氧氧化化碳碳施施肥肥原原理理
项目背景
二氧化碳是植物进行光合作用的主要原料之一。自20世纪70年代起,人们就开
始在大棚蔬菜种植中应用二氧化碳增施技术。事实证明,适当提高空气中二氧化碳的
浓度,能有效提高蔬菜产量和质量。
通过探秘大棚蔬菜种植中的二氧化碳施肥原理,进一步掌握二氧化碳的性质和制
取二氧化碳的方法,了解化学技术在农业中的应用。
项目建议方案
1.查阅资料。通过网络等渠道,了解大棚蔬菜种植中增施二氧化碳的常用方法及
其原理。
2.走访调查。在老师、家长等的帮助下,实地走访附近大棚蔬菜生产基地,或通
过线上交流、电话采访等方式访谈大棚蔬菜种植的专业人士,了解大棚蔬菜种植中增
施二氧化碳的具体操作方法和注意事项。
3.模拟探究。在农业劳动实践基地内寻找一定面积的两块地,进行大棚蔬菜种植
中增施二氧化碳的模拟实验,其中一个大棚内定期增施二氧化碳,另一个大棚作为对
比。在与同学讨论“二氧化碳的产生方法”“施用二氧化碳的控制方法”“大棚中二
氧化碳的浓度测定”“大棚蔬菜种植中增施二氧化碳的效果评价”等问题后,制订大
棚蔬菜种植中增施二氧化碳的模拟实验方案,与同学合作实施实验,详细记录实验
数据。
4.成果展示。 完成“大棚蔬菜种植中增施二氧化碳的调查与模拟实验研究”
的报告,并在全班进行展示与交流。
160 化化 学学
HHUUAAXXUUEE实验 1 实验基本操作
学生实验
实实验验11 实实验验基基本本操操作作
【实验目的】
1.练习并掌握酒精灯的使用、试剂的取用以及加热等实验操作。
2.初步学会观察、表述、记录实验现象的方法。
3.养成严谨、规范、安全、环保的实验习惯。
【实验用品】
铜绿、稀盐酸、镁条、锌粒、酒精。
酒精灯、坩埚钳、镊子、铁架台(带铁夹)、试管、药匙、陶土网、量筒(10 mL)、
胶头滴管、烧杯。
【安全警示】
1.实验中不要直接用手接触试剂,更要避免试剂进入口中。
2.正确使用酒精灯,以免烫伤或引起火灾。
3.不直接用手去拿加热后的仪器,也不将加热后的仪器直接放在实验桌上。
4.实验过程中,要戴上护目镜。
【实验步骤】
实验1 试剂的取用
步骤1 取用锌粒。取1支干燥洁净的试管,将试管横放,使用镊子(或药匙)
将锌粒放到试管口,然后缓慢竖立试管,使锌粒缓慢滑到试管底部。
步骤2 量取 3 mL 稀盐酸。取 1 只 10 mL 量筒,将试剂瓶中的稀盐酸倒入量筒
中,在接近 3 mL 刻度时,放平量筒,然后用胶头滴管滴加至 3 mL 刻度。读数时视
线要与量筒内液体的凹液面的最低处保持水平。
步骤3 将稀盐酸倒入盛放锌粒的试管内,振荡,观察并记录实验现象。
实验2 酒精灯的使用和镁条的燃烧
步骤1 查看酒精灯中酒精的量,若少于1/3,则须添加酒精(图1),添加后酒
精的总体积不要超过酒精灯容积的2/3。
步骤2 取1根3 ~ 5 cm长的镁条,用砂纸打磨除去表面氧化膜。
步骤3 在实验桌上垫一张陶土网,点燃酒精灯,用坩埚钳夹住镁条,放在酒精
灯火焰上点燃后,使其在陶土网上方燃烧(图 2),观察并记录实验现象。实验结
化化 学学 161
HHUUAAXXUUEE学生实验
束后,将酒精灯灯帽盖上。
实验3 物质的加热
步骤 1 将纸条折叠成纸槽,用药匙从试剂瓶中取半药匙铜绿粉末放到纸槽上,
将纸槽小心地送至干燥洁净的大试管底部,然后将试管直立起来。
步骤2 将铜绿平铺于试管底部,管口略向下倾斜固定于铁架台上,先来回移动酒
精灯预热试管,然后集中对有固体物质的部位加热(图3),观察并记录实验中产生
的现象。
图1 添加酒精 图2 镁条燃烧 图3 加热铜绿
实验报告
实验名称 实验者
实验时间 合作者
【实验现象记录】
实验名称 观察内容 实验现象
锌粒的颜色和状态
实验1 稀盐酸的颜色和状态
锌粒与稀盐酸反应的现象
镁条的颜色、状态和硬度
实验2 镁条燃烧的现象
反应产物的颜色和状态
铜绿的颜色和状态
实验3
铜绿分解的现象
【问题与讨论】
1.使用酒精灯时要注意哪些问题?
2.在点燃镁条前,为什么要在桌上垫一张陶土网?
3.加热铜绿时,大试管口为什么要略向下倾斜?
162 化化 学学
HHUUAAXXUUEE实验 2 氧气的实验室制取与性质
学生实验
实实验验22 氧氧气气的的实实验验室室制制取取与与性性质质
【实验目的】
1.掌握实验室制取氧气的原理和方法。
2.初步学会连接仪器装置和收集氧气的操作。
3.能根据实验现象归纳氧气的化学性质。
4. 经历和体验与同学合作进行实验探究的过程。
【实验用品】
高锰酸钾、木炭、硫粉、细铁丝、澄清石灰水、棉花团等。
铁架台(带铁夹)、试管、烧杯、酒精灯、带玻璃导管的单孔橡胶塞、水槽、集
气瓶、药匙、燃烧匙、坩埚钳、玻璃片。
【安全警示】
1.正确使用酒精灯。
2.用排水法收集完氧气后,应先把导管移出水面再熄灭酒精灯,避免水倒吸而导
致试管炸裂。
3.硫粉在氧气中燃烧后的生成物——二氧化硫有刺激性气味,会污染空气,且对
人体有害,整个操作过程应在通风橱中进行。
4.为防止细铁丝在氧气中燃烧产生的固体物质溅落瓶底而导致集气瓶炸裂,应提
前在集气瓶中加少量水或在集气瓶底铺少量沙子。
【实验步骤】
实验1 氧气的制取
加热分解高锰酸钾制取氧气的原理:
加热
高锰酸钾 锰酸钾 + 二氧化锰+ 氧气
制取氧气的实验操作:
步骤 1 检验装置的气密性。
步骤 2 向试管中装入质量约为 2 g的高锰酸钾固体,并在试管口放一小团棉花,
用带有导管的单孔橡胶塞塞紧试管口,将试管口略向下倾斜并固定在铁架台上。将集
气瓶中盛满水,用玻璃片盖住瓶口,倒立在盛水的水槽内。
化化 学学 163
HHUUAAXXUUEE学生实验
步骤 3 用酒精灯给试管加热,先来回移动酒精灯预热
高锰酸钾
试管,然后集中对有固体物质的部位加热。待气泡连续并均
匀放出时,把导管伸入集气瓶中。当集气瓶中的水排完后,
在水面下用玻璃片盖住瓶口。小心地把集气瓶移出水槽,正
放在桌子上。按此方法至少收集 3 瓶氧气备用。
图1 加热分解高锰酸钾
步骤 4 收集完需要的氧气后,先把导管移出水面,再 制取氧气的装置
熄灭酒精灯。清洗并整理仪器。
实验2 氧气的性质探究
步骤 1 木炭在氧气中的燃烧。用坩埚钳夹取一小块木炭,在酒精灯火焰上加热
至红热,伸进充满氧气的集气瓶里,观察比较木炭分别在空气中和在氧气中燃烧时产
生的现象。燃烧结束后,向集气瓶中加入少量澄清石灰水,轻轻振荡,观察现象。
步骤 2 硫粉在氧气中的燃烧。在燃烧匙里加入少量硫粉,在酒精灯火焰上加热
至燃烧,再将燃烧匙伸进充满氧气的集气瓶里,观察比较硫粉分别在空气中和在氧气
中燃烧时产生的现象。
步骤3 铁丝在氧气中的燃烧。将细铁丝绕成螺旋状,然后在末端系上火柴梗,
用坩埚钳夹住铁丝,在酒精灯上点燃末端的火柴梗。待火柴梗快燃尽时,将它们缓
慢伸入事先装有少量水(或细沙)并充满氧气的集气瓶中,观察比较细铁丝在空气
中加热和在氧气中燃烧的现象。
澄清石灰水
图2 木炭的燃烧
细铁丝
图3 硫的燃烧 图4 铁丝在氧气中燃烧
164 化化 学学
HHUUAAXXUUEE实验 2 氧气的实验室制取与性质
实验报告
实验名称 实验者
实验时间 合作者
【实验现象记录】
1.氧气的制取
实验原理 实验步骤
2.氧气的性质探究
实验步骤 实验现象 反应的表达式
步骤1
步骤2
步骤3
【问题与讨论】
1.如何正确检验装置的气密性?
2.还有哪些方法用于实验室制取少量氧气?
3.碳、硫、铁与氧气反应的共同特点是什么?为什么碳、硫、铁在氧气中反应比
在空气中反应更剧烈?
化化 学学 165
HHUUAAXXUUEE学生实验
学生实验
实实验验33 燃燃烧烧条条件件的的探探究究
【实验目的】
1.能基于实验探究结果总结归纳物质燃烧的条件。
2.能依据物质燃烧的条件,理解防火灭火措施的原理,能说明燃烧条件与灭火原
理的关系。
3.增强消防安全意识。
【实验用品】
白磷(黄豆粒大小)、蜡烛等。
试管、玻璃导管、镊子、酒精灯、玻璃杯等。
【安全警示】
1.白磷有毒且在空气中能自燃,实验中切勿将白磷随意丢弃,要交给老师处理。
2.使用沸水时务必注意安全,避免烫伤。
【实验步骤】
“燃烧条件”探究实验1
步骤1 用镊子分别夹取 1 根小木条和一块小石子,在酒精灯火焰上点燃,观察
比较实验现象。
步骤2 用镊子分别夹取1个蘸有水、1个没蘸水的小棉花团放在酒精灯火焰上点
燃,观察比较实验现象。
步骤3 分别点燃2支小蜡烛,将其中的1支用玻璃杯罩住,观察比较实验现象。
“燃烧条件”探究实验2
取A、B、C 3支试管,向A、C试管中分别注入约10 mL沸水并投入一小块白磷,
向B试管中注入约10 mL冷水并投入一小块白磷,将玻璃导管的一端对准且接触B、
C试管中的白磷,通过导管向B、C试管中通入氧气(图1),观察比较A、B、C试
管中的现象。
166 化化 学学
HHUUAAXXUUEE实验 3 燃烧条件的探究
氧气 氧气
沸水 冷水 沸水
白磷 白磷 白磷
A B C
图1 白磷的燃烧条件
实验报告
实验名称 实验者
实验时间 合作者
【实验现象记录】
“燃烧条件”探究实验1
实验步骤 实验现象 结论与解释
步骤1
步骤2
步骤3
“燃烧条件”探究实验2
实验现象 结论与解释
总结:物质燃烧需要具备的条件是 。
【问题与讨论】
请根据物质燃烧的条件,分析下列灭火措施的原理:
1.炒菜时锅里的油着火,可立即用锅盖盖灭。
2.扑灭森林大火时,常采用设置隔离带的措施来达到灭火的目的。
3.居民住宅着火时,消防队员用高压水枪喷水灭火。
化化 学学 167
HHUUAAXXUUEE学生实验
学生实验
实实验验44 二二氧氧化化碳碳的的实实验验室室制制取取与与性性质质
【实验目的】
1.掌握实验室制取二氧化碳的原理和方法,能在实验室顺利制取少量二氧化碳。
2.能通过实验探究总结归纳二氧化碳的性质。
【实验用品】
石灰石(或大理石)、稀盐酸、澄清石灰水、紫色石蕊溶液、蜡烛、小木条。
集气瓶、玻璃片、试管、烧杯(200 mL)、锥形瓶、弹簧夹、分液漏斗、双孔橡
胶塞、阶梯型铁架、酒精灯、试管夹、导气管、乳胶管。
【安全警示】
盐酸有腐蚀性,要防止它溅到眼睛里或皮肤上。
【实验步骤】
实验1 二氧化碳的制取
步骤1 按图1所示连接好装置,并检验装置的气密性。
步骤2 向锥形瓶中放入一些小碎块状石灰石(或大理石),
然后塞上带分液漏斗和导气管的双孔橡胶塞,用弹簧夹夹住乳
胶管。向分液漏斗中注入一定量的稀盐酸,打开弹簧夹,观察
并记录实验现象。
图1 制取CO
2
步骤3 将导气管伸到集气瓶底部,用向上排空气法收集气体,片刻后,用燃
着的木条在集气瓶口检验二氧化碳是否已集满。用玻璃片盖住已集满二氧化碳的集
气瓶,放在实验台上备用。
实验2 二氧化碳的性质探究
步骤1 如图2所示,取1支试管,加入2 ~ 3 mL蒸馏水,滴入1 ~ 3滴紫色石蕊
溶液。将导气管插入试管中通入二氧化碳,观察并记录实验现象。
步骤2 如图3所示,在酒精灯火焰上加热步骤1所得到的溶液至沸腾,观察并
记录实验现象。
步骤3 取1支试管,向试管中加入少量澄清石灰水,将导气管插入试管中通入
二氧化碳,观察并记录实验现象。
步骤4 点燃2支短蜡烛,放在烧杯中的阶梯型铁架上(图4),沿烧杯内壁缓慢
168 化化 学学
HHUUAAXXUUEE实验 4 二氧化碳的实验室制取与性质
倾倒收集的二氧化碳气体,观察并记录实验现象。
步骤5 拆除实验装置,将废液、废渣倒入指定容器中。清洗仪器,将仪器和试
剂归位。
图2 CO 与H O反应 图3 H CO 分解 图4 倾倒CO
2 2 2 3 2
实验报告
实验名称 实验者
实验时间 合作者
【实验现象记录】
1.二氧化碳的制取
实验现象 反应的表达式
2.二氧化碳的性质探究
实验步骤 实验现象 反应的表达式
步骤1
步骤2
步骤3
步骤4
化化 学学 169
HHUUAAXXUUEE学生实验
【问题与讨论】
1.还可用哪些装置制取少量二氧化碳?
2.总结归纳二氧化碳的物理性质和化学性质。
3.如何鉴别空气、氧气、二氧化碳三种无色气体?
170 化化 学学
HHUUAAXXUUEE跨学科实践活动
跨跨学学科科实实践践活活动动
一一、、简简易易制制氧氧器器的的制制作作
活动目标
1.通过查阅资料和调查研究等方法,了解目前市场上销售的家用供氧机的制氧方
法、工作原理和应用范围,总结归纳氧气的制取方法。
2.通过“设计并制作简易制氧器”的实践活动,提高创新意识、动手能力,以及
综合利用多学科知识合作解决实际问题的能力。
活动方案
活动1:认识家用供氧机原理
通过查阅网上资料,了解目前市场上销售的家用供氧机的制氧方法、工作原理;
通过走访调查使用过家用供氧机的人士,了解家用供氧机的使用方法和使用效果,总
结归纳不同类型供氧机的制氧方法和工作原理,与同学交流讨论调查研究的成果。
活动2:设计制作简易制氧器的方案
基于电解水制氧、双氧水分解制氧等物质转化的知识,借鉴供氧机原理,在老师
或其他专业人士的指导下,小组合作绘制简易制氧器设计图,确定制作流程,选择制
作材料,确定分工合作方案。
活动3:制作简易制氧器
依据方案,小组成员分工合作进行简易制氧器的制作,检验所制作的简易制氧器
的制氧效果,并通过“制氧效果评价—修改设计方案—完善简易制氧器”的过程,不
断完善所制作的简易制氧器。
活动4:成果展示
提交“家用供氧机的应用与简易制氧器的制作”的研究报告;展示所制作的简易
制氧器产品,对产品进行介绍和自我评价;总结在完成跨学科实践活动中的经验,提
炼解决产品制作类问题的思路方法。
活动实施建议
1.该跨学科实践活动一般需要4个课时,主要包括教师对该跨学科实践活动的指
导,家用供氧机调查研究成果的交流讨论,简易制氧器制作方案的讨论,以及简易制
氧器的组装、效果检测、展示和评价等。
2.该跨学科实践活动可采用课堂与课后相结合的方法实施。查阅资料、走访调查、
化化 学学 171
HHUUAAXXUUEE跨学科实践活动
简易制氧器材料的选择和购买等都可以安排在课后作业中完成。
3.教师要在供氧需求的调查、制氧原料的选择、环保和健康材料的选择、制氧量
的计算与控制、制氧器设计图的绘制、制氧机的制作等环节给予充分的指导,帮助学
生解决遇到的困难。
4.从积极参与、学习掌握、探究实践、协同合作、表达交流、反思评价和成果展
示等方面,对学生在活动中的表现和结果进行评价。
二二、、基基于于碳碳中中和和理理念念设设计计低低碳碳行行动动方方案案
活动目标
1.通过查阅资料,了解我国碳中和举措及在碳中和领域中取得的成果,深刻理解
碳中和的意义,强化社会责任感和国家认同感。
2.通过小组合作方式,设计并优化低碳生活方案和绿色低碳行动方案,提升合作
能力和方案设计能力,初步形成节能低碳、节约资源、保护环境的态度。
3.通过“权衡科学技术发展和环境保护需求”的辩论,提高表达及质疑能力,学
会对社会问题进行合理的价值判断。
活动方案
活动1:认识碳中和、低碳行动的意义
查阅资料,了解我国在促进碳中和方面的各项举措和政策。结合2022年北京冬季
奥林匹克运动会,了解我国在促进碳中和方面取得的成就。
活动2:设计低碳生活方案
通过互联网资源检索、社区调查、地区主管部门访谈等方式,综合考虑社会生活
和个人生活实际,设计低碳生活行动方案,并分析和排查所有可能产生二氧化碳的
途径,着重思考中学生在日常生活中应该为减排作出怎样的努力。
活动3:构建绿色低碳行动方案框架
阅读理解国务院印发的《2030年前碳达峰行动方案》,从个人、国家、国际层面
初步构建绿色低碳行动方案框架。小组成员就“权衡科学技术发展和环境保护需求”
为题进行辩论,权衡利弊,以此细化国家、国际层面的行动方案。
活动4:捕捉二氧化碳方法探究
依据二氧化碳的性质和元素守恒的原理,基于碳中和的思想,从化学的视角提出
捕捉二氧化碳的方法设想,并就其中的一些方法进行实验探究,以此提出一些细化捕
172 化化 学学
HHUUAAXXUUEE跨学科实践活动
捉二氧化碳的建议。
活动5:成果展示
以小论文的形式呈现低碳行动方案及设计过程,并在班级中进行交流。将设计的
低碳方案在家庭、学校、社区等进行宣讲或在学校的黑板报、宣传栏等进行展示。
活动实施建议
1.该跨学科实践活动一般需要4个课时,主要包括该跨学科实践活动的动员和指
导,行动方案的讨论和优化,围绕“权衡科学技术发展和环境保护需求”的辩论,捕
捉二氧化碳的方法的实验探究、活动结果的展示和评价等。
2.该跨学科实践活动可采用课堂与课后相结合的方法实施。查阅资料、走访调
查、小论文的撰写等,可安排在课后作业中完成。
3.教师要在低碳生活方案、绿色低碳行动方案框架的设计过程中,引导学生综合
多学科知识和生活经验全面、深入地思考问题;要在进行“权衡科学技术发展和环境
保护需求”辩论前,提供一些相关资料,便于学生获得辩论的证据。
4.从积极参与、学习掌握、探究实践、协同合作、表达交流、反思评价和成果展
示等方面,对学生在活动中的表现和结果进行评价。
化化 学学 173
HHUUAAXXUUEE附 录
附录 1
化化学学实实验验规规则则
化学实验是学习化学、进行科学探究的重要方法。为了在实验过程中体验科学
探究过程,通过实验探究获取化学知识,训练实验技能,养成良好的实验态度和实
验习惯, 在实验过程中请同学们遵循如下的实验规则。
一、实验准备
1.实验前应阅读有关实验说明,了解实验目的,明确实验步骤和实验注意事项。
2.对自行设计的实验方案,要和老师进行讨论,在保证安全、方案可行的基础上
进行操作。
3.实验前要检查实验仪器、试剂是否齐全,试剂规格是否符合要求,实验器皿是
否洁净。
4.做好实验记录的准备。
二、实验实施
1.要按照实验方法或实验方案规定的步骤进行实验。
2.仔细观察实验现象,认真、如实、及时地做好实验记录,同时要边观察、边思考,
养成善于提出问题的习惯。
3.在合作完成的实验中,要互相尊重、合理分工、齐心协力,以共同完成实验任务。
4.实验过程中要注意节约试剂,爱护仪器,注意保持桌面的整洁。
三、实验后处理
1.实验剩余的试剂和实验废弃物要按要求放入指定的容器内,不得乱丢、乱倒。
2.实验完毕后,及时洗净器皿,清理桌面、水池等。
3.清点试剂,尽可能将其放回原位。
4.整理实验记录并按要求分析实验结果,写好实验报告。总结、交流实验的收获。
四、实验安全要求
1.实验过程中须将易燃、易爆试剂远离火源,以防引发事故。
2.不要使用无标签试剂,不要用手直接接触试剂,也不要把鼻孔凑到容器口去闻
试剂气味或用嘴尝试剂味道。实验试剂不要带出实验室。
3.必要时实验过程中要戴上护目镜。
4.实验室须注意通风和保持空气流通。
5.实验过程中如出现意外,不要惊慌,要及时报告老师,并根据具体情况及时处理。
174 化化 学学
HHUUAAXXUUEE附录 2
中中学学化化学学实实验验常常用用仪仪器器
酒精灯 烧杯 集气瓶 表面皿
滴瓶 蒸发皿 研钵 陶土网
试管夹 试管刷 燃烧匙 药匙
胶头滴管 试管 普通漏斗 长颈漏斗
量筒 锥形瓶 水槽 铁架台和铁夹
化化 学学 175
HHUUAAXXUUEE附录 3
相相对对原原子子质质量量表表
(按照原子序数排列)
元素 元素 元素
相对原子质量 相对原子质量 相对原子质量
符号 名称 符号 名称 符号 名称
H 氢 [1.007 84;1.008 11] Nb 铌 92.906 37 Tl 铊 [204.382;204.385]
He 氦 4.002 602 Mo 钼 95.95 Pb 铅 [206.14;207.94]
Li 锂 [6.938;6.997] Tc 锝 [97] Bi 铋 208.980 40
Be 铍 9.012 183 1 Ru 钌 101.07 Po 钋 [209]
B 硼 [10.806;10.821] Rh 铑 102.905 49 At 砹 [210]
C 碳 [12.009 6;12.011 6] Pd 钯 106.42 Rn 氡 [222]
N 氮 [14.006 43;14.007 28] Ag 银 107.868 2 Fr 钫 [223]
O 氧 [15.999 03;15.999 77] Cd 镉 112.414 Ra 镭 [226]
F 氟 18.998 403 162 In 铟 114.818 Ac 锕 [227]
Ne 氖 20.179 7 Sn 锡 118.710 Th 钍 232.037 7
Na 钠 22.989 769 28 Sb 锑 121.760 Pa 镤 231.035 88
Mg 镁 [24.304;24.307] Te 碲 127.60 U 铀 238.028 91
Al 铝 26.981 538 4 I 碘 126.904 47 Np 镎 [237]
Si 硅 [28.084;28.086] Xe 氙 131.293 Pu 钚 [244]
P 磷 30.973 761 998 Cs 铯 132.905 451 96 Am 镅 [243]
S 硫 [32.059;32.076] Ba 钡 137.327 Cm 锔 [247]
Cl 氯 [35.446;35.457] La 镧 138.905 47 Bk 锫 [247]
Ar 氩 [39.792;39.963] Ce 铈 140.116 Cf 锎 [251]
K 钾 39.098 3 Pr 镨 140.907 66 Es 锿 [252]
Ca 钙 40.078 Nd 钕 144.242 Fm 镄 [257]
Sc 钪 44.955 907 Pm 钷 [145] Md 钔 [258]
Ti 钛 47.867 Sm 钐 150.36 No 锘 [259]
V 钒 50.941 5 Eu 铕 151.964 Lr 铹 [262]
Cr 铬 51.996 1 Gd 钆 157.25 Rf 钅卢 [267]
Mn 锰 54.938 043 Tb 铽 158.925 354 Db 钅杜 [268]
Fe 铁 55.845 Dy 镝 162.500 Sg 钅喜 [269]
Co 钴 58.933 194 Ho 钬 164.930 329 Bh 钅波 [270]
Ni 镍 58.693 4 Er 铒 167.259 Hs 钅黑 [269]
Cu 铜 63.546 Tm 铥 168.934 219 Mt 钅麦 [277]
Zn 锌 65.38 Yb 镱 173.045 Ds 钅达 [281]
Ga 镓 69.723 Lu 镥 174.966 8 Rg 钅仑 [282]
Ge 锗 72.630 Hf 铪 178.486 Cn 钅哥 [285]
As 砷 74.921 595 Ta 钽 180.947 88 Nh 钅尔 [286]
Se 硒 78.971 W 钨 183.84 Fl 钅夫 [290]
Br 溴 [79.901;79.907] Re 铼 186.207 Mc 镆 [290]
Kr 氪 83.798 Os 锇 190.23 Lv 钅立 [293]
Rb 铷 85.467 8 Ir 铱 192.217 Ts 石田 [294]
Sr 锶 87.62 Pt 铂 195.084 Og 气 [294]
奥
Y 钇 88.905 838 Au 金 196.966 570
Zr 锆 91.224 Hg 汞 200.592
注: 1.相对原子质量录自国际纯粹与应用化学联合会(IUPAC)公布的“标准相对原子质量2021”。
2.相对原子质量加方括号的为放射性元素半衰期最长的同位素的质量数。
3. [a;b]表示该元素的相对原子质量依据其同位素丰度变化而介于a和b之间。
176 化化 学学
HHUUAAXXUUEE附录 4
表
期
周
素
元
0
A
Ⅰ
期周
81
1
色红(号符素元
eH2
素元属金非
O
8
数序子原
H
1
)素元性射放指
氦
氢
1
AⅦ
AⅥ
A
Ⅴ
AⅣ
AⅢ
氧
称名素元
A
Ⅱ
300.4
素元属金
800.1
71
61
51
41
31
是的*注(
2
eN01
F
9
O
8
N
7
C
6
B
5
量质子原对相
00.61
)素元造人
eB
4
iL
3
素元渡过
氖
氟
氧
氮
碳
硼
该为据数的号括加(
铍
锂
2
81.02
00.91
00.61
10.41
10.21
18.01
最期衰半素元性射放
210.9
49.6
素元体气有稀
)数量质的素位同长
rA81
lC71
S
61
P
51
iS41
lA31
gM21
aN11
氩
氯
硫
磷
硅
铝
镁
钠
3
B
Ⅱ
B
Ⅰ
Ⅷ
BⅦ
BⅥ
B
Ⅴ
BⅣ
BⅢ
59.93
54.53
60.23
79.03
80.82
89.62
03.42
99.22
21
11
01
9
8
7
6
5
4
3
rK63
rB53
eS43
sA33
eG23
aG13
nZ03
uC92
iN82
oC72
eF62
nM52
rC42
V32
iT22
cS12
aC02
K91
氪
溴
硒
砷
锗
镓
锌
铜
镍
钴
铁
锰
铬
钒
钛
钪
钙
钾
4
08.38
09.97
79.87
29.47
36.27
27.96
83.56
55.36
96.85
39.85
48.55
49.45
00.25
49.05
78.74
69.44
80.04
01.93
eX45
I
35
eT25
bS15
nS05
nI94
dC84
gA74
dP64
hR54
uR44
cT34
oM24
bN14
rZ04
Y93
rS83
bR73
氙
碘
碲
锑
锡
铟
镉
银
钯
铑
钌
锝
钼
铌
锆
钇
锶
铷
5
3.131
9.621
6.721
8.121
7.811
8.411
4.211
9.701
4.601
9.201
1.101
]79[
59.59
19.29
22.19
19.88
26.78
74.58
nR68
tA58
oP48
iB38
bP28
lT18
gH08
uA97
tP87
rI77
sO67
eR57
W47
aT37
fH27
17~75
aB65
sC55
氡
砹
钋
铋
铅
铊
汞
金
铂
铱
锇
铼
钨
钽
铪
uL~aL
钡
铯
6
]222[
]012[
]902[
0.902
2.702
4.402
6.002
0.791
1.591
2.291
2.091
2.681
8.381
9.081
5.871
系镧
3.731
9.231
gO811
sT711
vL611cM511
lF411
hN311
nC211
gR111
sD011
tM901
sH801
hB701
gS601
bD501
fR401301~98
aR88
rF78
*
*
* 立
*镆
*
夫
* 尔
*
哥
*
仑
*
达
*
麦
* 黑
* 波
*
喜
**
杜
*
卢
rL~cA
镭
钫
7
]492[
]492[
]392[
]092[
]092[
]682[
]582[
]282[
]182[
]772[
]962[
]072[
]962[
]862[
]762[
系锕
]622[
]322[
uL17
bY07
mT96
rE86
oH76
yD66
bT56
dG46
uE36
mS26
mP16
dN06
rP
95
eC85
aL75
镥
镱
铥
铒
钬
镝
铽
钆
铕
钐
*钷
钕
镨
铈
镧
镧 系
0.571
0.371
9.861
3.761
9.461
5.261
9.851
2.751
0.251
4.051
]541[
2.441
9.041
1.041
9.831
rL301
oN201dM101mF001
sE
99
fC
89
kB79
mC69
mA59
uP
49
pN39
U
29
aP
19
hT09
cA
98
*铹
*锘
*钔
*镄
*锿
*锎
*锫
*锔
*镅
钚
镎
铀
镤
钍
锕
锕 系
]262[
]952[
]852[
]752[
]252[
]152[
]742[
]742[
]342[
]442[
]732[
0.832
0.132
0.232
]722[
化化 学学 177
HHUUAAXXUUEE后后 记记
本套教科书根据教育部最新颁布的《义务教育化学课程标准(2022 年版)》
编修。
此次教科书修订是由化学学科专家、化学教育专家和一线优秀化学教师组成的
教科书修订团队共同进行的。在修订过程中,团队认真研究了教育部制定的《义务
教育化学课程标准(2022 年版)》,分析比较了多种版本的国内外初中化学教
科书,广泛征询了教科书使用地区老师和学生的意见、建议。修订后的教科书具
有基础性、时代性、实践应用性和创新性等特点。
教科书力图让学生轻松愉快地学习多姿多彩、无所不在的化学,力图让学生用
“用中学”“做中学”“创中学”等多种方式学习化学,力图助力学生化学课程核
心素养的发展。
教科书在编写、修改和审校过程中得到了全国许多化学教育专家、教研员和优
秀一线教师的指导和帮助,在此向他们表示诚挚的谢意!
希望老师和同学们在使用本套教科书的过程中与我们保持联系,及时反馈在使
用中发现的问题,提出宝贵的意见和建议,以便我们更好地完善教科书。
电子邮箱:zks_zongbianshi@163.com
联系电话:(010)63581202