文档内容
机密 启用前
高二年
海口市 2024~2025 学年第二学期
级期末考试(化学)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡
上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Fe 56
一、选择题:本题共8小题,每小题2分,共16分。在每小题给出的四个选项中,只有一
项符合题目要求。
1.生活中“无处不化学”,下列常用试剂呈中性的是
A.84 消毒液 B.洁厕灵 C.3%苯酚消毒液 D.75%酒精溶液
2.化学材料的使用对人类生活质量的提高和科技的发展有重要作用,下列说法正确的
A.富勒烯属于传统无机非金属材料 B.纤维素在人体内可水解为葡萄
糖
C.羽绒服的合成纤维面料属于有机高分子化合物
D.废弃的聚乳酸塑料属于白色污染,不可降解
3.下列化学用语或图示正确的是
A.中子数为 19 的钾的核素符号:40 K
19
B.HF 中的 s﹣p σ 键示意图:
C.H O 的电子
2 2
式:
D.甲烷的球棍模 型:
4. CH OH 与 HCl 可发生反应:CH OH + HCl CH Cl + H O,N 代表阿伏加德罗常数
3 3 3 2 A
的值。下列说法正确的是
A.标准状况下,11.2 L CH OH 的分子数为 0.5 N B.常温下,
3 A
pH=1 的盐酸中含有的 H+ 数为 0.1 N
AC.1 mol CH Cl 中含有的共价键数为 4 N
3 A
D.18 g H 18O 中含有的中子数为 10 N
2 A
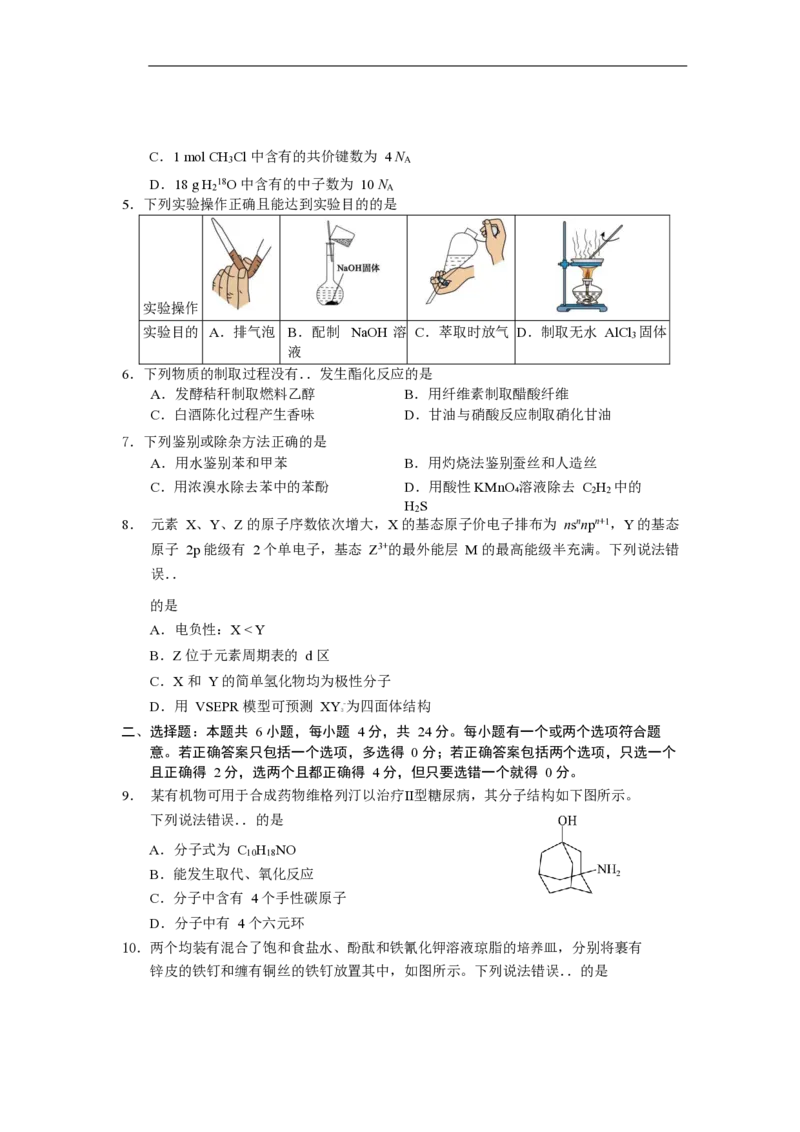
5.下列实验操作正确且能达到实验目的的是
实验操作
实验目的 A.排气泡 B.配制 NaOH 溶 C.萃取时放气 D.制取无水 AlCl 固体
3
液
6.下列物质的制取过程没有..发生酯化反应的是
A.发酵秸秆制取燃料乙醇 B.用纤维素制取醋酸纤维
C.白酒陈化过程产生香味 D.甘油与硝酸反应制取硝化甘油
7.下列鉴别或除杂方法正确的是
A.用水鉴别苯和甲苯 B.用灼烧法鉴别蚕丝和人造丝
C.用浓溴水除去苯中的苯酚 D.用酸性KMnO₄溶液除去 C H 中的
2 2
H S
2
8. 元素 X、Y、Z 的原子序数依次增大,X 的基态原子价电子排布为 nsnnpn+1,Y 的基态
原子 2p 能级有 2 个单电子,基态 Z3+的最外能层 M 的最高能级半充满。下列说法错
误..
的是
A.电负性:X < Y
B.Z 位于元素周期表的 d 区
C.X 和 Y 的简单氢化物均为极性分子
D.用 VSEPR 模型可预测 XY-为四面体结构
3
二、选择题:本题共 6 小题,每小题 4 分,共 24 分。每小题有一个或两个选项符合题
意。若正确答案只包括一个选项,多选得 0 分;若正确答案包括两个选项,只选一个
且正确得 2 分,选两个且都正确得 4 分,但只要选错一个就得 0 分。
9. 某有机物可用于合成药物维格列汀以治疗Ⅱ型糖尿病,其分子结构如下图所示。
下列说法错误..的是
A.分子式为 C H NO
10 18
B.能发生取代、氧化反应
C.分子中含有 4 个手性碳原子
D.分子中有 4 个六元环
10.两个均装有混合了饱和食盐水、酚酞和铁氰化钾溶液琼脂的培养皿,分别将裹有
锌皮的铁钉和缠有铜丝的铁钉放置其中,如图所示。下列说法错误..的是A.离子在琼脂内可定向移动
B.图A 中会出现两处红色
C.图A 中是用外加电流法保护铁钉
D.图B 中出现蓝色的反应:
Fe2++K++[Fe(CN) ]3 =KFe[Fe(CN) ]↓ 11.物质结构决定物质性质,下列性质与结构
6 6
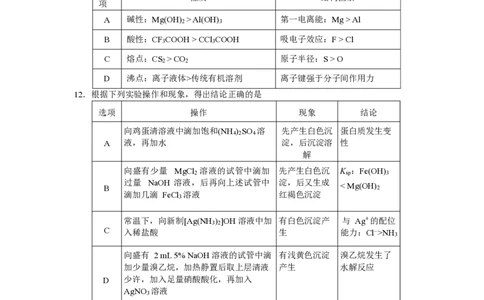
因素匹配正确的是
选
性质 结构因素
项
A 碱性:Mg(OH) > Al(OH) 第一电离能:Mg > Al
2 3
B 酸性:CF COOH > CCl COOH 吸电子效应:F > Cl
3 3
C 熔点:CS > CO 原子半径:S > O
2 2
D 沸点:离子液体>传统有机溶剂 离子键强于分子间作用力
12.根据下列实验操作和现象,得出结论正确的是
选项 操作 现象 结论
向鸡蛋清溶液中滴加饱和(NH ) SO 溶 先产生白色沉 蛋白质发生变
4 2 4
A 液,再加水 淀,后沉淀溶 性
解
向盛有少量 MgCl 溶液的试管中滴加 先产生白色沉 K :Fe(OH)
2 sp 3
B
过量 NaOH 溶液,后再向上述试管中 淀,后又生成
< Mg(OH) 2
滴加几滴 FeCl 溶液 红褐色沉淀
3
常温下,向新制[Ag(NH ) ]OH 溶液中加 有白色沉淀产 与 Ag+ 的配位
3 2
C 入稀盐酸 生 能力:Cl—>NH
3
向盛有 2 mL 5% NaOH 溶液的试管中滴 有浅黄色沉淀 溴乙烷发生了
加少量溴乙烷,加热静置后取上层清液 产生 水解反应
D 少许,加入足量硝酸酸化,再加入
AgNO 溶液
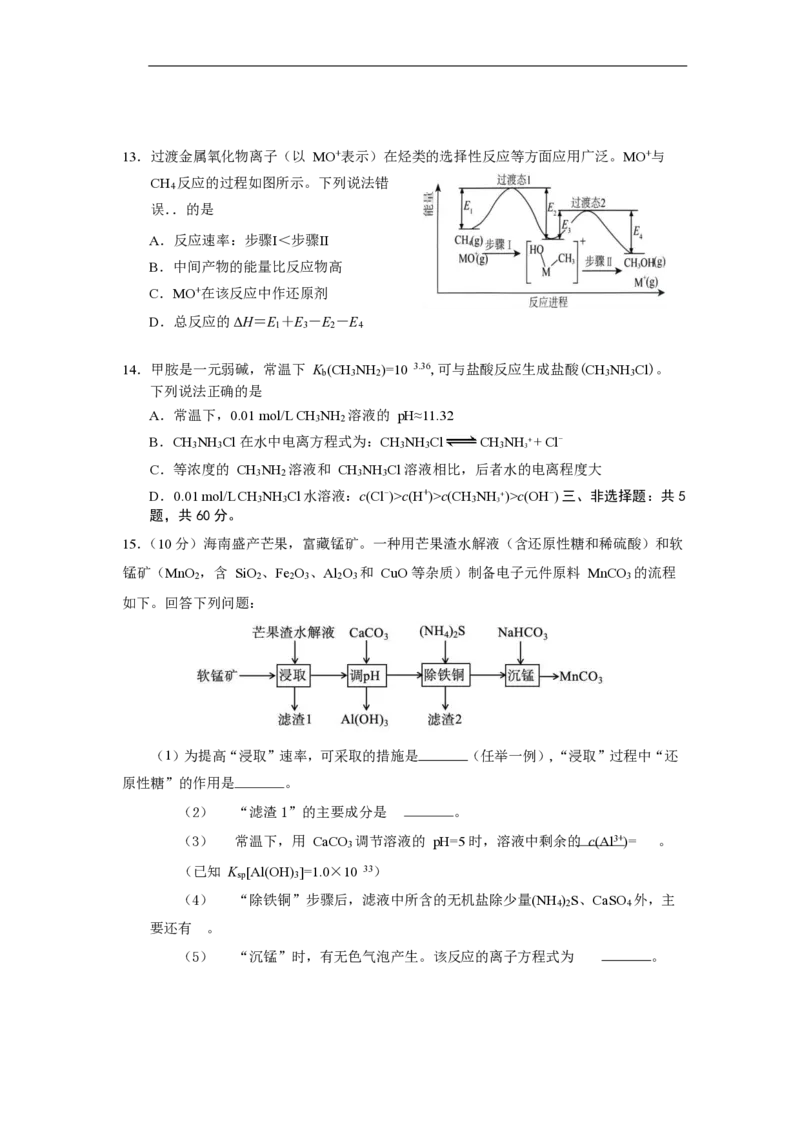
313.过渡金属氧化物离子(以 MO+表示)在烃类的选择性反应等方面应用广泛。MO+与
CH 反应的过程如图所示。下列说法错
4
误..的是
A.反应速率:步骤Ⅰ<步骤Ⅱ
B.中间产物的能量比反应物高
C.MO+在该反应中作还原剂
D.总反应的ΔH=E +E -E -E
1 3 2 4
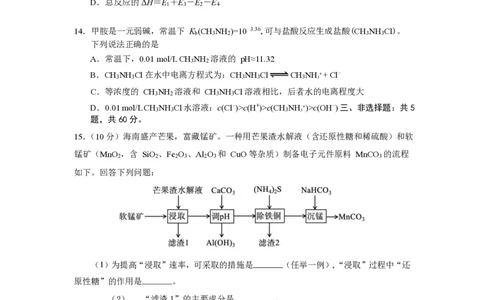
14.甲胺是一元弱碱,常温下 K (CH NH )=10 3.36,可与盐酸反应生成盐酸(CH NH Cl)。
b 3 2 3 3
下列说法正确的是
A.常温下,0.01 mol/L CH NH 溶液的 pH≈11.32
3 2
B.CH 3 NH 3 Cl 在水中电离方程式为:CH 3 NH 3 Cl CH 3 NH 3 + + Cl-
C.等浓度的 CH NH 溶液和 CH NH Cl 溶液相比,后者水的电离程度大
3 2 3 3
D.0.01 mol/L CH 3 NH 3 Cl 水溶液:c(Cl-)>c(H+)>c(CH 3 NH 3 + )>c(OH-) 三、非选择题:共5
题,共60分。
15.(10 分)海南盛产芒果,富藏锰矿。一种用芒果渣水解液(含还原性糖和稀硫酸)和软
锰矿(MnO ,含 SiO 、Fe O 、Al O 和 CuO 等杂质)制备电子元件原料 MnCO 的流程
2 2 2 3 2 3 3
如下。回答下列问题:
(1 )为 提 高“ 浸 取 ”速 率 ,可 采取的措施是 (任 举一例 ), “ 浸 取 ”过 程中“ 还
原性糖” 的作 用是 。
(2) “滤渣1”的主要成分是 。
(3) 常温下,用 CaCO 调节溶液的 pH=5 时,溶液中剩余的 c(Al3+)= 。
3
(已知 K [Al(OH) ]=1.0×10 33)
sp 3
(4) “除铁铜”步骤后,滤液中所含的无机盐除少量(NH ) S、CaSO 外,主
4 2 4
要还有 。
(5) “沉锰”时,有无色气泡产生。该反应的离子方程式为 。16.(10 分)我国提出 2060 年前实现碳中和,其中以 CO 、CH 等温室气体制备燃料及化
2 4
工原料是当前研究热点。回答以下问题:
Ⅰ.CO 在固体催化剂表面加氢合成 CH 过程中发生如下反应:主反应:CO (g)+
2 4 2
4H (g) CH (g)+2H O(g) ΔH <0
2 4 2 1
副反应:CO (g)+H (g) CO(g)+H O(g) ΔH >0
2 2 2 2
(1)主反应自发进行的条件是 。
a.高温 b.低温 c.任意温度
(2)随压强升高,CO 平衡转化率的变化趋势为 ,理由是 。
2
Ⅱ.甲烷干重整反应:CO 2 (g)+CH 4 (g) 2 CO(g) +2 H 2 (g ) ΔH 3
(3)ΔH = (用含ΔH 和ΔH 的代数式表示)。
3 1 2
(4)t ℃时,在 1 L 密闭刚性容器中加入 1 mol CO 与 1 mol CH ,10 min 时达到平衡
2 4
状态,容器内平衡压强比初始压强增加 60%,则 0~10 min 内 v(CH )= mol/(L·min),
4
平衡常数 K= 。
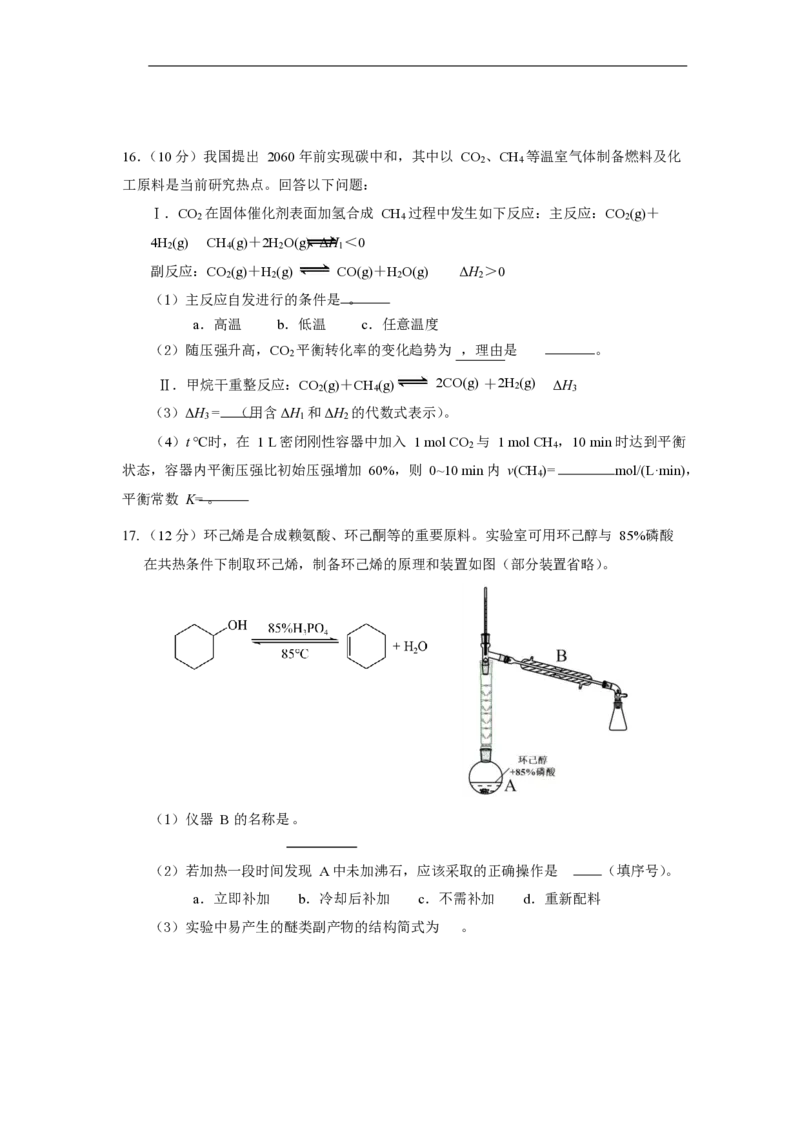
17. (12 分)环己烯是合成赖氨酸、环己酮等的重要原料。实验室可用环己醇与 85%磷酸
在共热条件下制取环己烯,制备环己烯的原理和装置如图(部分装置省略)。
(1)仪器 B 的名称是 。
(2)若加热一段时间发现 A 中未加沸石,应该采取的正确操作是 (填序号)。
a.立即补加 b.冷却后补加 c.不需补加 d.重新配料
(3)实验中易产生的醚类副产物的结构简式为 。(4 )环己烯的提纯流程如下:
①操 作 1、 2 的名称分别是 、 。
②加 10 % 碳酸钠溶液的目的是 。
(5)浓硫酸也可作该反应的催化剂,本实验选择 85%磷酸不用浓硫酸的原因可能
为 。
18. (14 分)物质 G 可做香料,其工业合成路线如下:
回答下列问题:
(1)A→B 的反应类型是 。
(2)C 的核磁共振氢谱有 4 组吸收峰,其结构简式为 。
(3)D 中官能团的名称是 。
(4)E→F 的化学方程式为 。
(5)G 有多种同分异构体,写出符合以下条件的结构简式 (只写顺式结构)。
①具有顺反结构 ②含有酚羟基 ③分子中苯环上的一溴代物有两种
(6)参考上述路线中的信息,请写出以 为原料制备
的合成路线(无机试剂任选)。
19.(14 分)铁、镁、氮等元素在电池材料、储氢合金等高科技领域中发挥重要作用。回答
下列问题:(1) 基态镁原子的价电子轨道表示式为 。
(2) 下列状态的 Fe 中,电离最外层一个电子所需能量最大的是 (填标
号)。
a.[Ar]3d64s2 b.[Ar]3d64s1 c.[Ar]3d64p1
(3) 二甲胺和三甲胺的结构如右图。
①A 分子中 N 的杂化方式为 。
②A 的沸点比 B 的沸点高,其原因是 。
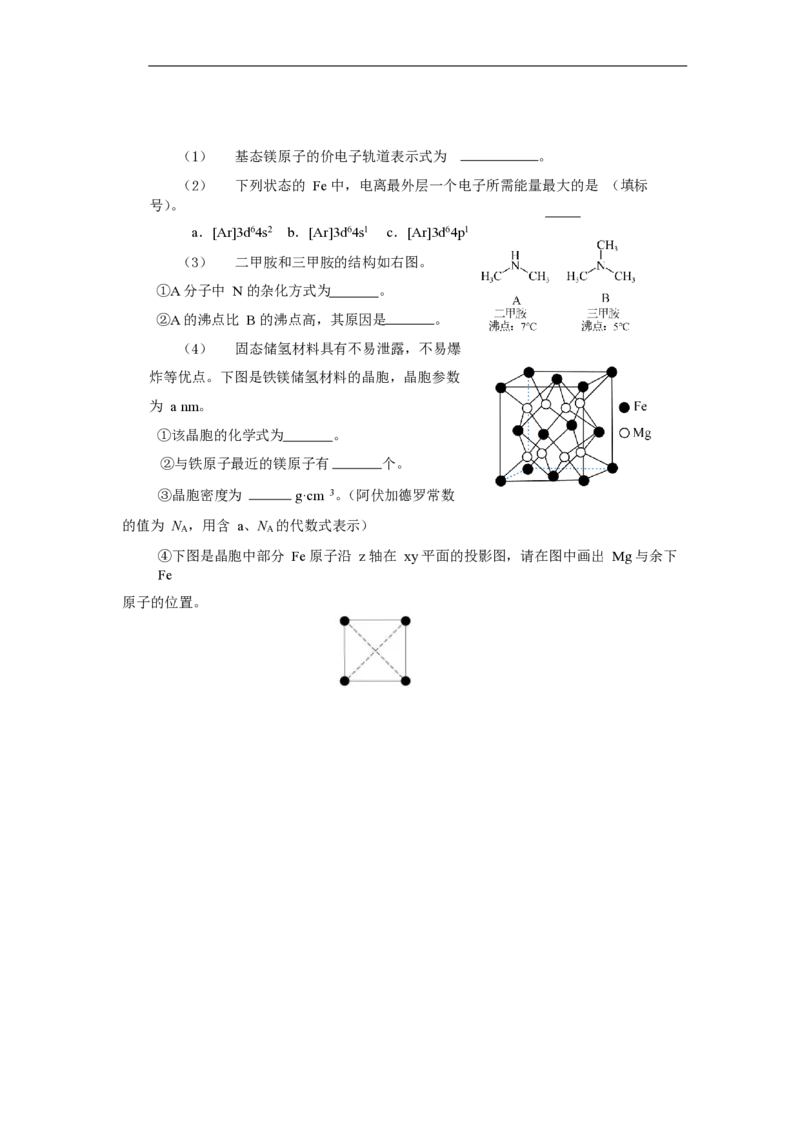
(4) 固态储氢材料具有不易泄露,不易爆
炸等优点。下图是铁镁储氢材料的晶胞,晶胞参数
为 a nm。
①该晶胞的化学式为 。
②与铁原子最近的镁原子有 个。
③晶胞密度为 g·cm 3。(阿伏加德罗常数
的值为 N ,用含 a、N 的代数式表示)
A A
④下图是晶胞中部分 Fe 原子沿 z 轴在 xy 平面的投影图,请在图中画出 Mg 与余下
Fe
原子的位置。