文档内容
2024届高三年级质量监测考试
化学答案与解析
1.【答案】C
【解析】生物质丙烷燃料,由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和
石油提炼的丙烷不同,是一种可再生的清洁燃料,C错误。
2.【答案】B
【解析】雾是由大气中悬浮的水汽凝结形成的,不是由氮的氧化物造成的光化学烟雾,A错
误;布衾的主要成分为纤维素,B正确;氧化铁为红棕色粉末,“红泥”是因含有氧化铁而呈红
色,C错误;酒香中除了乙醇的香味,还有通过酯化反应生成乙酸乙酯的香味,D错误。
3.【答案】A
【解析】NH 的VSEPR模型为四面体形,且有一对孤电子对,A正确;HClO的电子式应为
3
,B错误;HO 中 O为 sp3杂化,其分子不是直线形,C错误;CHCHOHCH 的系统
2 2 3 3
命名为2-丙醇,D错误。
4.【答案】B
【解析】二氧化碳不能与NaCl溶液反应,还需先通入大量氨气,A错误;铁丝网在氯化钠溶液
中发生吸氧腐蚀,使试管中压强减小,导管内红墨水液面上升,B正确;丙装置只能证明石蜡
油裂解得到不饱和烃,但不一定是乙烯,C错误,醋酸具有挥发性,不能证明碳酸的酸性强于
苯酚,D错误。
5.【答案】A
【解析】BBr与PBr的空间结构分别为平面三角形和三角锥形,A错误;HF分子间可以形成
3 3
氢键,因此沸点最高,而相对分子质量HBr大于 HCl,沸点 HBr>HCl,B正确;硼原子最外层
有三个电子,而BP、BN晶体结构与金刚石相似,硼原子形成四个共价键,因此BP与BN中既
有共价键又有配位键,C正确;基态硼原子的电子排布图为 ,D正确。
6.【答案】B
【解析】M存在顺反异构,但M是反式结构,A错误;M的一溴代物有13种,B正确;1molM
最多消耗2molNaOH,C错误;M结构中不存在手性碳原子,D错误。
7.【答案】B
Δ
【解析】TiCl与水混合加热制得TiO·xHO的化学方程式为TiCl+(x+2)HOTiO·xHO↓
4 2 2 4 2 2 2
+4HCl,B错误。
8.【答案】D
【解析】总反应的热化学方程式为2NO(g)N(g)+O(g) ΔH=-1828kJ·mol-1,未标
2 2
物质状态,A错误;能量越低越稳定,因此过渡态的稳定性:TS1>TS2,B错误;反应过程的决
速步骤为a→c,此过程为吸热反应,C错误;反应热只与反应物的始态和终态有关系,与反应
过程无关,因此催化剂能降低反应活化能,但不能改变反应热,D正确。
【 ·高三年级质监考试———化学答案 第1页(共5页)】
{#{QQABAQAEoggAABJAAAhCEwWoCEIQkACACCoGRBAAsAIACRNABAA=}#}
书书书9.【答案】C
【解析】根据所给信息判断 X、Y、Z、M、W五种元素分别为 H、F、N、C、B;第一电离能介于
N和 B之间的同周期元素有 Be、C、O共 3种,A错误;最高价氧化物的水化物的酸性:
HNO >HCO >HBO,B错误;简单氢化物的稳定性:HF>NH,C正确;简单离子半径:
3 2 3 3 3 3
N3->F->H+,D错误。
10.【答案】D
【解析】左侧为电池正极,电池工作时,左侧电势高于右侧,A错误;放电时,电极反应式为
VO++e-+2H+VO2++HO,B错误;放电时H+通过质子交换膜向左侧迁移,C错误;此
2 2
电池的电解液在电池内循环带出部分热量,使电池更安全,D正确。
11.【答案】C
【解析】“酸浸”未发生氧化还原反应,A正确;铁粉作用主要是将 Fe3+还原为 Fe2+,是否完
全反应需检验是否存在 Fe3+,因此选择硫氰化钾溶液,B正确;结晶操作应为降温结晶,
C错误;实验室灼烧固体在坩埚中完成,D正确。
12.【答案】C
【解析】T=25,因此t<t<8,A错误;甲组用 KMnO 的浓度变化表示的平均反应速率为
1 2 1 4
2×002
=5×10-4mol·L-1·s-1,B错误;通过实验乙、丙探究温度对化学反应速率的影响,
10×8
C正确;草酸是弱酸,书写离子方程式时不能拆,D错误。
13.【答案】A
【解析】Fe的离子位于 O2-构成的正四面体空隙或正八面体空隙中,A错误;根据均摊法
计算,立方体中拥有 O2-个数为 4个,Fe的离子个数为 3个,因此化学式为 FeO,B正
3 4
1 1 3
确;根据 b点坐标,确定 a点坐标为( , , ),C正确;立方体中有1个 FeO,体积为
4 4 4 3 4
232
(d×10-7)3cm3,晶体的密度为 g·cm-3,D正确。
N(d×10-7)3
A
14.【答案】B
【解析】根据图像计算,K(HX)=10-31、K(HY)=10-75、K(HZ)=10-92,A正确;B错
a a a
误;直线HX与 y轴交点纵坐标设为 x,则 10x-14×102=10-31,x=89,C正确;常温时,
02mol·L-1HY溶液与等体积01mol·L-1NaOH溶液混合后,得到005mol·L-1HY溶液
和005mol·L-1NaY混合液,且K(HY)=10-75,所以K(Y-)=10-65,NaY水解大于HY
a h
的电离,因此c(HY)>005mol·L-1>c(Y-),D正确。
15.【答案】(15分,除标注分数外,其余每空2分)
(1)ef←ef←b
(2)KMnO(1分,合理即可得分) 还原性和酸性(1分)
4
(3)先向圆底烧瓶中加入乙醇,边振荡边逐滴加入浓硫酸 催化剂和脱水剂(1分)
NaOH溶液和浓硫酸
(4)三颈烧瓶(1分) CHCH+Cl→ClCHCHCl
2 2 2 2 2
(5)蒸馏(1分)
【 ·高三年级质监考试———化学答案 第2页(共5页)】
{#{QQABAQAEoggAABJAAAhCEwWoCEIQkACACCoGRBAAsAIACRNABAA=}#}(6)取少量成品于试管中,加入NaOH溶液并加热,待充分反应后冷却,加入硝酸酸化,再加
入硝酸银溶液,若有白色沉淀产生,则证明有氯原子存在
【解析】(1)装置甲制备氯气,先后用丁装置盛装的饱和食盐水和浓硫酸除去氯气中氯化氢
及水,然后用乙装置制备乙烯气体,先后用氢氧化钠溶液和浓硫酸除去乙烯中的酸性气体
和水,因此装置的连接顺序为a→fe→fe→cd←ef←ef←b。
(2)高锰酸钾与浓盐酸反应不需要加热,且盐酸在反应中表现还原性和酸性。
(3)应将浓硫酸逐滴加入乙醇中,边加边振荡;浓硫酸在制备乙烯时作催化剂和脱水剂。
(4)丙装置的仪器名称为三颈烧瓶,乙烯和氯气发生加成反应。
(5)最后得产品需要蒸馏操作。
(6)检验1,2-二氯乙烷中的氯原子操作为取少量成品于试管中,加入 NaOH溶液并加热,
待充分反应后冷却,加入硝酸酸化,再加入硝酸银溶液,若有白色沉淀产生,则证明有氯原
子存在。
16.【答案】(14分,除标注分数外,其余每空2分)
(1)BiS+6Fe3+3S+6Fe2++2Bi3+ S、PbO、SiO
2 3 2 2
(2)将Fe3+还原为Fe2+,避免调节pH生成BiOCl时Fe3+沉淀析出,影响产品纯度
(3)3≤pH≤47
(4)2BiOCl+2NHHCO (BiO)CO+CO↑+2NHCl+HO
4 3 2 3 2 4 2
(5)629
(6)Pb-2e-Pb2+(1分) 阳极底部(1分)
【解析】(1)利用“溶浸”前后 Bi3+价态未变而进入溶液,因此离子方程式为 BiS+6Fe3+
2 3
3S+6Fe2++2Bi3+,根据信息溶浸后阳离子中不存在铅的离子判断,熔渣不但有 S、SiO,
2
还含有PbO。
2
(2)根据所给信息,“溶浸”后Bi3+与Fe3+完全沉淀的 pH接近,因此需将 Fe3+还原为 Fe2+,
避免“调pH”时Fe3+沉淀析出,影响产品纯度。
(3)“调pH”的目的,使 Bi3+在 pH≥3时完全转化为白色的 BiOCl沉淀,且 Fe2+和 Cu2+不
能沉淀,二者比较 Cu2+更易沉淀,若 Cu2+为 01mol·L-1开始沉淀的 pH应不大于:
10-14
-lg =47,所以3≤pH≤47。
10×10-5×10(67-14)×2
槡
01
高温
(4)因为“煅烧”时(BiO)CO BiO +CO↑,若“转化”时产生相同气体,则2BiOCl+
2 3 2 3 2
2NHHCO (BiO)CO+CO↑+2NHCl+HO。
4 3 2 3 2 4 2
209×2 209×2+48
(5)m(BiO)=10t×7308%× ×(1-5%)× ≈629t。
2 3 209×2+96 209×2
(6)因为金属活泼性铅大于铋,因此阳极电极反应式为Pb-2e-Pb2+,则铋沉积在阳极
底部,为精铋。
【 ·高三年级质监考试———化学答案 第3页(共5页)】
{#{QQABAQAEoggAABJAAAhCEwWoCEIQkACACCoGRBAAsAIACRNABAA=}#}17.【答案】(14分,除标注分数外,其余每空2分)
(1)-51268kJ·mol-1(1分) -34384kJ·mol-1(1分)
(2)①未达到平衡,相同条件下,400℃时用FeO/γAlO 作催化剂时,SO 转化率为045,
x y 2 3 2
若达到平衡状态,使用不同催化剂时,各物质转化率应相同;
低于350℃时,温度升高催化剂活性增大,反应速率加快,SO 转化率增大,当温度高于
2
350℃时,温度升高催化剂活性降低,反应速率减慢,单位时间内SO 转化率减小。
2
②FeO/γAlO 作催化剂,温度为450~500℃
x y 2 3
075 324×075
(3) mol·L-1·min-1 9375%
t 074×042
【解析】(1)标准摩尔生成焓是压力为100kPa,温度298K下最稳定单质生成标准状况下1mol
物质的焓变,由盖斯定律计算ΔH =4×(-39351)+2558-4×(-11053)-2×(-29683)
1
1 1
=-51268kJ·mol-1;ΔH = ×(ΔH +ΔH)= ×(-51268-175)=-34384kJ·mol-1。
3 2 1 2 2
(2)①不同催化剂下,相同条件时,平衡转化率应该相同,因此判断当以CrO/γAlO 作催
x y 2 3
化剂时,400℃时反应未达到平衡状态。低于350℃时,温度升高催化剂活性增大,反应速率
加快,SO 转化率增大,当温度高于350℃时,温度升高催化剂活性降低,反应速率减慢,单
2
位时间内SO 转化率减小。
2
②根据表格数据显示温度为450~500℃,FeO/γAlO 作催化剂,SO的转化率以及生成
x y 2 3 2
硫的选择性数值最大。
(3)根据反应ⅲ为反应ⅰ和反应ⅱ的总反应,利用反应ⅰ和反应ⅲ列出三行式为:
4CO(g)+2SO(g)幑幐 4CO(g)+S(g)
2 2 2
起始物质的量(mol) 8 4 0 0
变化物质的量(mol) 6 4×80%-02 6 15
平衡物质的量(mol) 14 08 64 15
平衡物质的量浓度(mol·L-1) 07 04 32 075
3CO(g)+SO(g)幑幐 2CO(g)+COS(g)
2 2
起始物质的量(mol) 8 4 0 0
变化物质的量(mol) 06 02 04 02
15mol 075
v(S)= = mol·L-1·min-1
2 2L·tmin t
32-02
硫的选择性= ×100%=9375%
32
324×075
K=
074×042
【 ·高三年级质监考试———化学答案 第4页(共5页)】
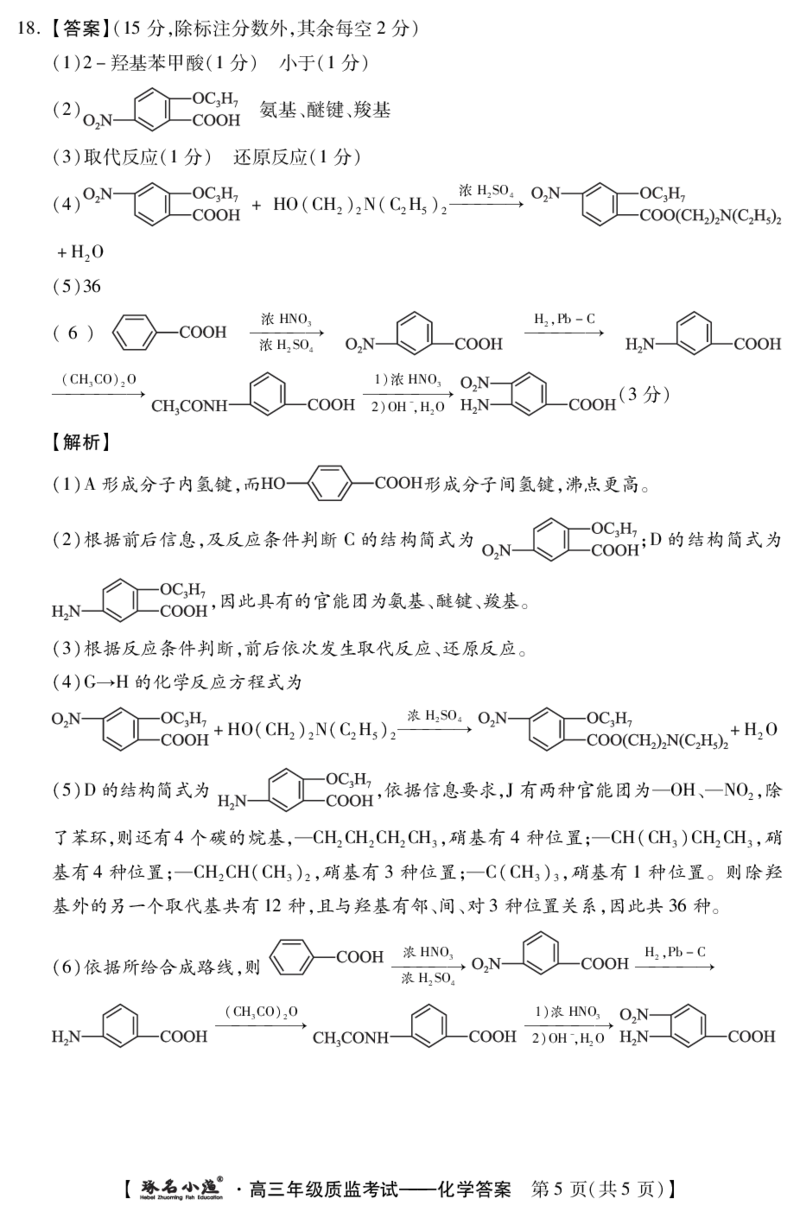
{#{QQABAQAEoggAABJAAAhCEwWoCEIQkACACCoGRBAAsAIACRNABAA=}#}18.【答案】(15分,除标注分数外,其余每空2分)
(1)2-羟基苯甲酸(1分) 小于(1分)
(2) 氨基、醚键、羧基
(3)取代反应(1分) 还原反应(1分)
浓HSO
(4) +HO(CH)N(CH)2 →4
2 2 2 5 2
+HO
2
(5)36
浓HNO H,Pb-C
(6) →3 2→
浓HSO
2 4
(CHCO)O 1)浓HNO
32→ →3 (3分)
2)OH-,HO
2
【解析】
(1)A形成分子内氢键,而 形成分子间氢键,沸点更高。
(2)根据前后信息,及反应条件判断 C的结构简式为 ;D的结构简式为
,因此具有的官能团为氨基、醚键、羧基。
(3)根据反应条件判断,前后依次发生取代反应、还原反应。
(4)G→H的化学反应方程式为
浓HSO
+HO(CH)N(CH)2 →4 +HO
2 2 2 5 2 2
(5)D的结构简式为 ,依据信息要求,J有两种官能团为—OH、—NO,除
2
了苯环,则还有4个碳的烷基,—CHCHCHCH,硝基有4种位置;—CH(CH)CHCH,硝
2 2 2 3 3 2 3
基有4种位置;—CHCH(CH),硝基有3种位置;—C(CH),硝基有1种位置。则除羟
2 3 2 3 3
基外的另一个取代基共有12种,且与羟基有邻、间、对3种位置关系,因此共36种。
浓HNO H,Pb-C
(6)依据所给合成路线,则 →3 2→
浓HSO
2 4
(CHCO)O 1)浓HNO
32→ →3
2)OH-,HO
2
【 ·高三年级质监考试———化学答案 第5页(共5页)】
{#{QQABAQAEoggAABJAAAhCEwWoCEIQkACACCoGRBAAsAIACRNABAA=}#}