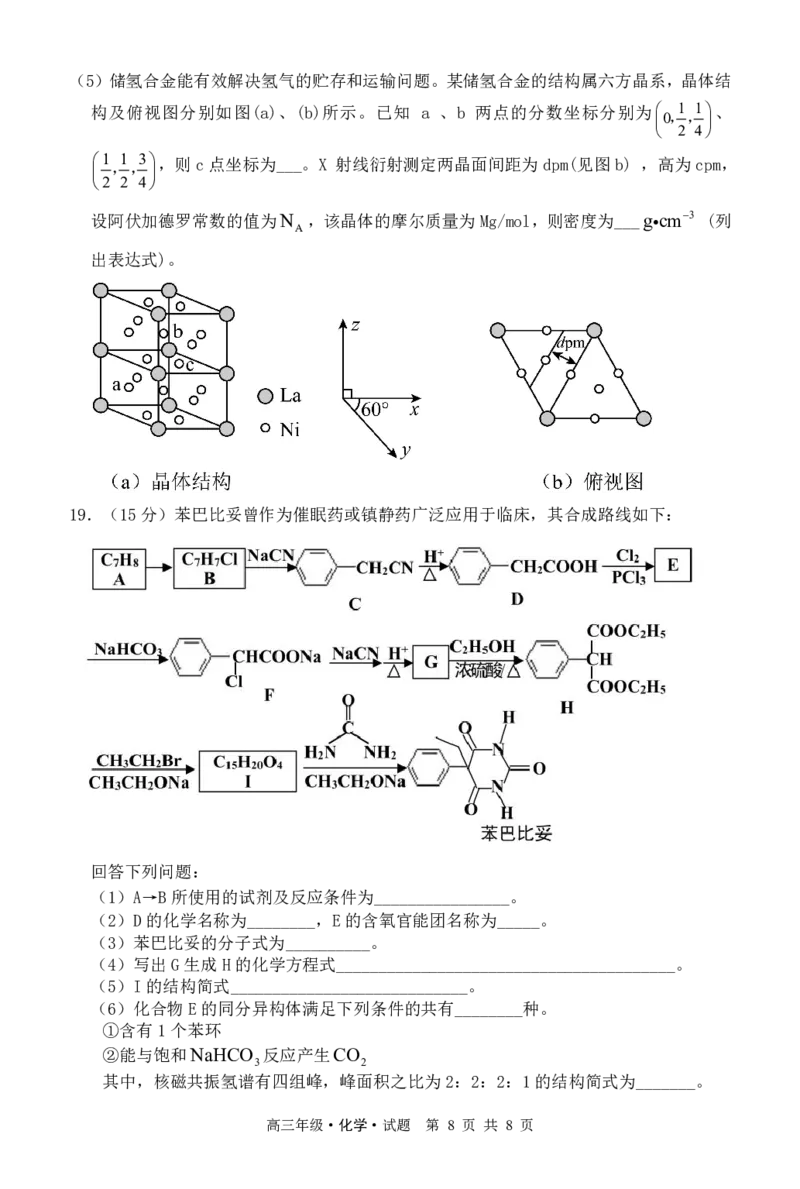
文档内容
牡丹江市第二共同体高三大联考
化学试题
可能用到的相对原子质量:H1C12O16Mn55Co59
第Ⅰ卷(选择题,共 45 分)
本卷共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是最
符合题目要求的。
1.《厉害了,我的国》展示了中国在航空、深海、交通、互联网等方面取得的举世瞩目的
成就,它们与化学有着密切联系。下列说法正确的是( )
A.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
B.港珠澳大桥使用高性能富锌底漆防腐,依据的是外加电流的阴极保护法
C.“鲲龙”水陆两栖飞机实现海上首飞,其所用燃料航空煤油属于纯净物
D.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆主要成分是二氧化硅
2.下列化学用语表达中正确的是( )
A.甲基的电子式:
B.CH CH CH CH COOH系统命名法为:2-甲基丁酸
3 3 2
C.HO的VSEPR模型为
2
D.SO2的空间结构:平面三角形
3
3.N 是阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温常压下,2.24L氨气中共价键的数目为0.3N
A
B.1L 0.1mol/L K Cr O 溶液中,Cr O2的数目为0.1N
2 2 7 2 A
7
C.32 g环状S ( )分子中含有的S—S键数为N
8 A
D.常温下,pH=12的Ba OH 溶液中OH的数目是0.01N
2 A
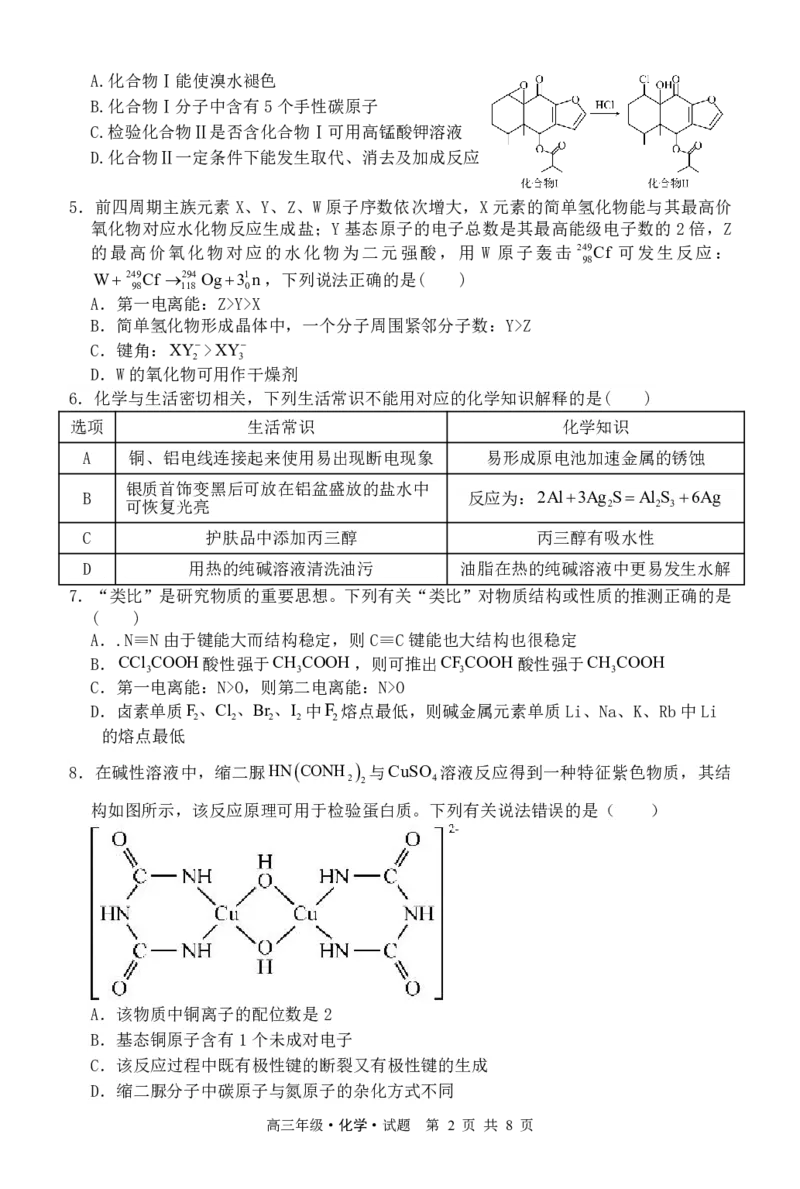
4.我国科研人员以蹄叶橐吾为原料先制得(化合物Ⅰ)再转化为具有抗癌抑菌活性的倍半
萜(化合物Ⅱ),有关转化如图所示,下列有关说法不正确的是( )
高三年级·化学·试题 第 1 页 共 8 页
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}A.化合物Ⅰ能使溴水褪色
B.化合物Ⅰ分子中含有5个手性碳原子
C.检验化合物Ⅱ是否含化合物Ⅰ可用高锰酸钾溶液
D.化合物Ⅱ一定条件下能发生取代、消去及加成反应
5.前四周期主族元素X、Y、Z、W原子序数依次增大,X元素的简单氢化物能与其最高价
氧化物对应水化物反应生成盐;Y基态原子的电子总数是其最高能级电子数的2倍,Z
的最高价氧化物对应的水化物为二元强酸,用 W 原子轰击 249Cf 可发生反应:
98
W249Cf 294 Og31n,下列说法正确的是( )
98 118 0
A.第一电离能:Z>Y>X
B.简单氢化物形成晶体中,一个分子周围紧邻分子数:Y>Z
C.键角:XY>XY
2 3
D.W的氧化物可用作干燥剂
6.化学与生活密切相关,下列生活常识不能用对应的化学知识解释的是( )
选项 生活常识 化学知识
A 铜、铝电线连接起来使用易出现断电现象 易形成原电池加速金属的锈蚀
银质首饰变黑后可放在铝盆盛放的盐水中
B 反应为:2Al3Ag SAl S 6Ag
可恢复光亮 2 2 3
C 护肤品中添加丙三醇 丙三醇有吸水性
D 用热的纯碱溶液清洗油污 油脂在热的纯碱溶液中更易发生水解
7.“类比”是研究物质的重要思想。下列有关“类比”对物质结构或性质的推测正确的是
( )
A..N≡N由于键能大而结构稳定,则C≡C键能也大结构也很稳定
B.CCl COOH酸性强于CH COOH,则可推出CFCOOH酸性强于CH COOH
3 3 3 3
C.第一电离能:N>O,则第二电离能:N>O
D.卤素单质F、Cl、Br、I 中F 熔点最低,则碱金属元素单质Li、Na、K、Rb中Li
2 2 2 2 2
的熔点最低
8.在碱性溶液中,缩二脲HNCONH 与CuSO 溶液反应得到一种特征紫色物质,其结
2 2 4
构如图所示,该反应原理可用于检验蛋白质。下列有关说法错误的是( )
A.该物质中铜离子的配位数是2
B.基态铜原子含有1个未成对电子
C.该反应过程中既有极性键的断裂又有极性键的生成
D.缩二脲分子中碳原子与氮原子的杂化方式不同
高三年级·化学·试题 第 2 页 共 8 页
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}9.硝酸盐本身对人体没有很大伤害,但在人的口腔和肠道细菌会将硝酸盐转化为亚硝酸盐,
可能会使得人体积累亚硝酸盐。下图是电化学降解酸性废水中NO的工作原理示意图。
3
下列有关叙述错误的是( )
..
A.Pt电极上发生的是氧化反应
B.H +由电解池左侧移向右侧
C.当外电路转移2mol电子时,两极一定会收集到 标
况下15.68 L气体
D.阴极反应式为2NO+10e+12H+6H O+N
3 2 2
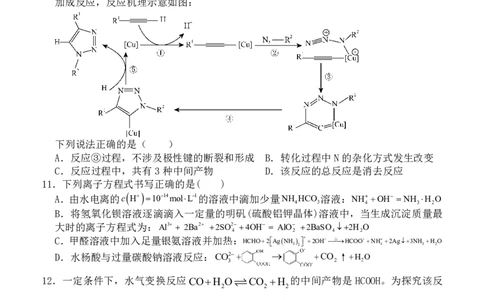
10.在“点击化学和生物正交化学”领域中,点击化学 经
典反应之一是一价铜[Cu]催化的叠氮化物-端炔烃 环
加成反应,反应机理示意如图:
下列说法正确的是( )
A.反应③过程,不涉及极性键的断裂和形成 B.转化过程中N的杂化方式发生改变
C.反应过程中,共有3种中间产物 D.该反应的总反应是消去反应
11.下列离子方程式书写正确的是( )
A.由水电离的c H 1014molL1的溶液中滴加少量NH HCO 溶液:NHOH NH H O
4 3 4 3 2
B.将氢氧化钡溶液逐滴滴入一定量的明矾(硫酸铝钾晶体)溶液中,当生成沉淀质量最
大时的离子方程式为:Al3 2Ba2 2SO24OH AlO 2BaSO 2H O
4 2 4 2
C.甲醛溶液中加入足量银氨溶液并加热: HCHO2 AgNH 3 2 2OH△HCOONH 4 2Ag3NH 3 H 2 O
D.水杨酸与过量碳酸钠溶液反应:CO2+ +CO ↑+H O
3 2 2
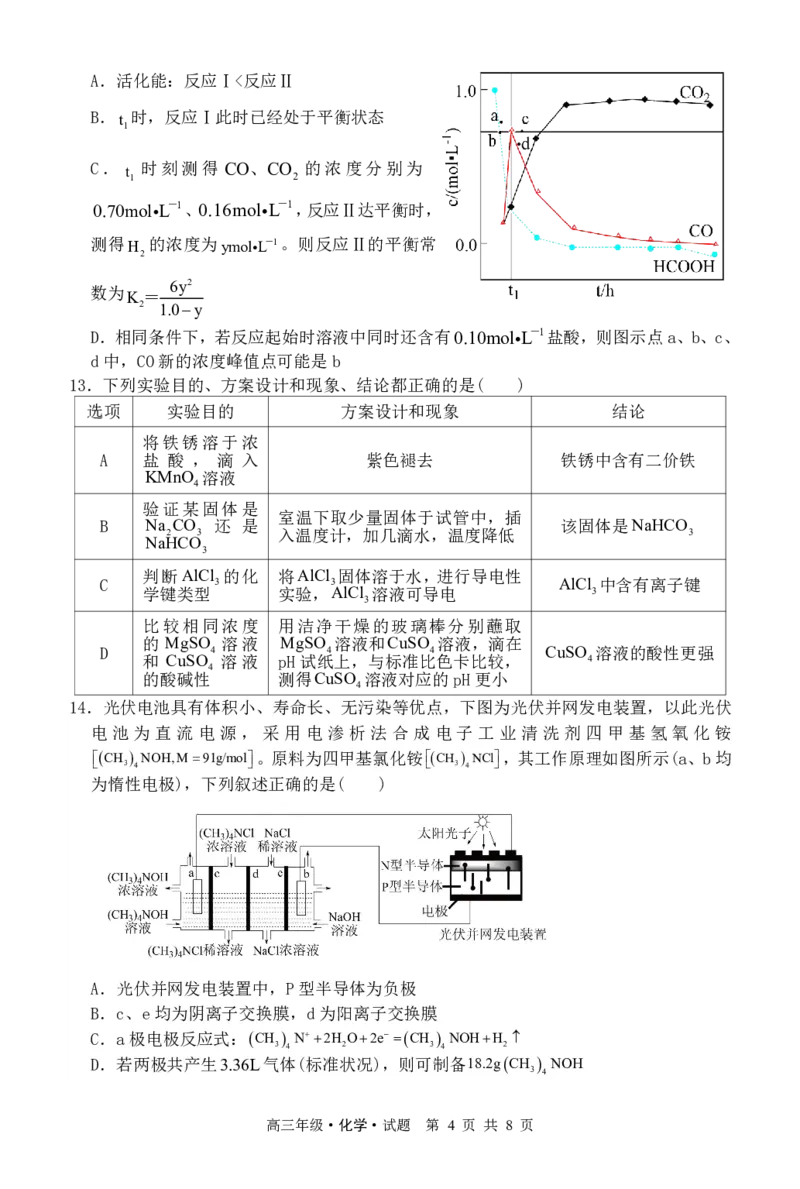
12.一定条件下,水气变换反应 COH OCO H 的中间产物是HCOOH。为探究该反
2 2 2
应过程,研究HCOOH水溶液在密封石英管中的分解反应:
Ⅰ.HCOOHCO+H O(快) Ⅱ. HCOOHCO+H (慢)
2 2 2
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应
Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。
T 温度下,在密封石英管内完全充满1.0 molL -1HCOOH水溶液,使HCOOH分解,分
3
解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其
他存在形式)。下列说法不正确的是( )
高三年级·化学·试题 第 3 页 共 8 页
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}A.活化能:反应Ⅰ<反应Ⅱ
B. 时,反应Ⅰ此时已经处于平衡状态
t
1
C.
t
时刻测得 CO、CO 的浓度分别为
1 2
0.70molL-1、0.16molL-1,反应Ⅱ达平衡时,
测得
H
的浓度为 ymolL-1。则反应Ⅱ的平衡常
2
数为 K=
6y2
2 1.0y
D.相同条件下,若反应起始时溶液中同时还含有0.10molL-1盐酸,则图示点a、b、c、
d中,CO新的浓度峰值点可能是b
13.下列实验目的、方案设计和现象、结论都正确的是( )
选项 实验目的 方案设计和现象 结论
将铁锈溶于浓
A 盐 酸 , 滴 入 紫色褪去 铁锈中含有二价铁
KMnO 溶液
4
验证某固体是
室温下取少量固体于试管中,插
B Na CO 还 是 该固体是NaHCO
2 3 入温度计,加几滴水,温度降低 3
NaHCO
3
判断AlCl 的化 将AlCl 固体溶于水,进行导电性
C 3 3 AlCl 中含有离子键
学键类型 实验,AlCl 溶液可导电 3
3
比较相同浓度 用洁净干燥的玻璃棒分别蘸取
的 MgSO 溶液 MgSO 溶液和CuSO 溶液,滴在
D 4 4 4 CuSO 溶液的酸性更强
和 CuSO 溶液 pH试纸上,与标准比色卡比较, 4
4
的酸碱性 测得CuSO 溶液对应的pH更小
4
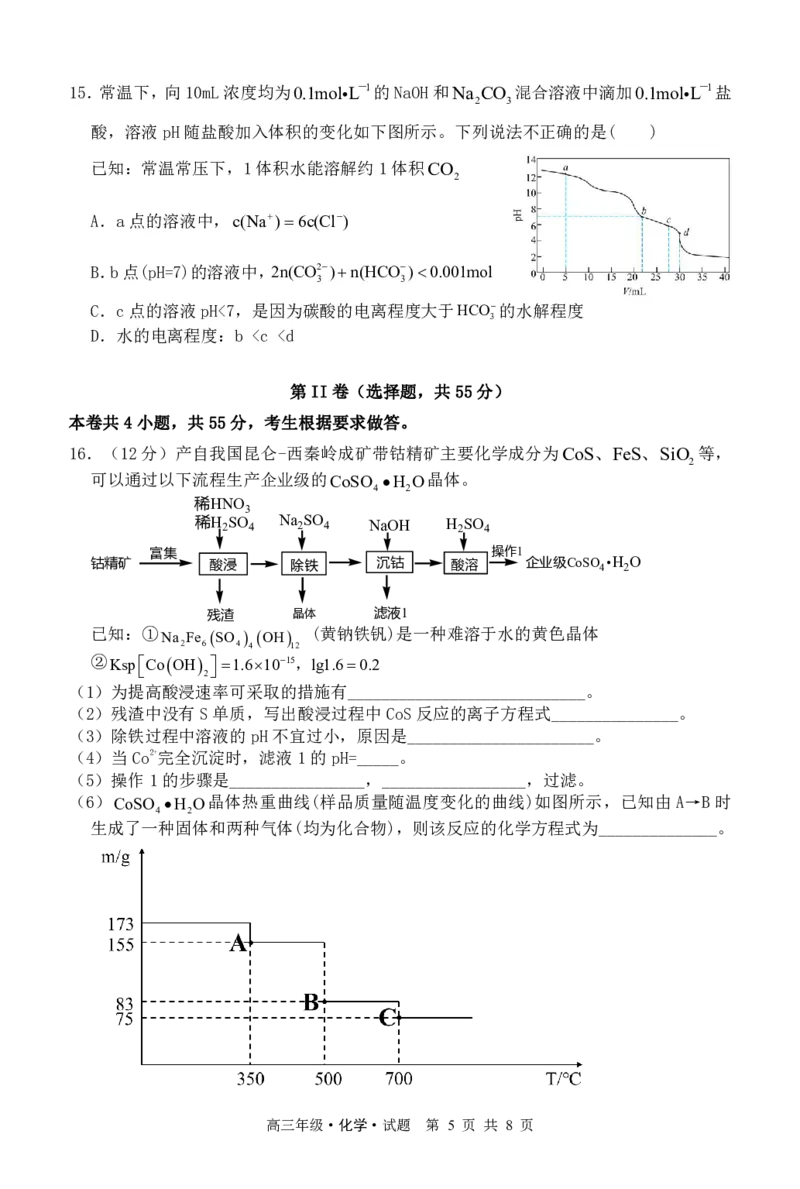
14.光伏电池具有体积小、寿命长、无污染等优点,下图为光伏并网发电装置,以此光伏
电池为直流电源,采用电渗析法合成电子工业清洗剂四甲基氢氧化铵
CH
3
4
NOH,M91g/mol
。原料为四甲基氯化铵
CH
3
4
NCl
,其工作原理如图所示(a、b均
为惰性电极),下列叙述正确的是( )
A.光伏并网发电装置中,P型半导体为负极
B.c、e均为阴离子交换膜,d为阳离子交换膜
C.a极电极反应式:CH N2H O2eCH NOHH
3 4 2 3 4 2
D.若两极共产生3.36L气体(标准状况),则可制备18.2gCH NOH
3 4
高三年级·化学·试题 第 4 页 共 8 页
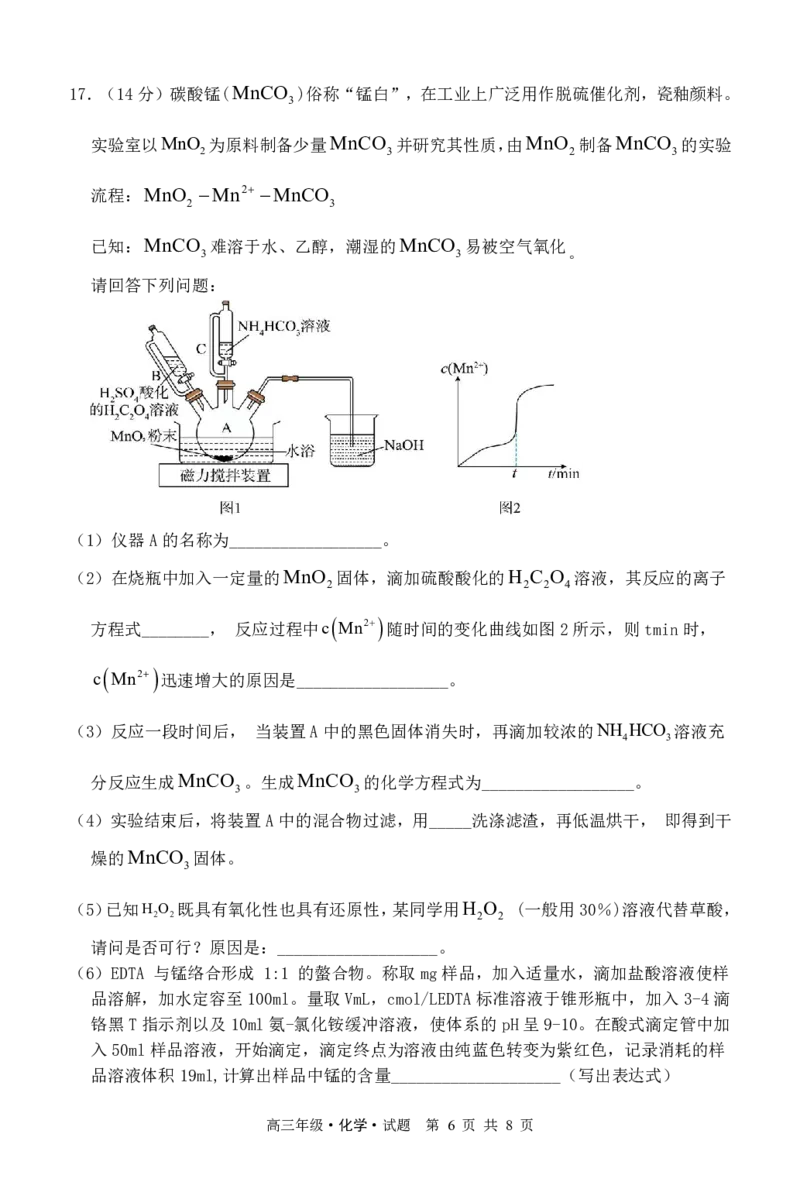
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}15.常温下,向10mL浓度均为0.1molL-1的NaOH和Na CO 混合溶液中滴加0.1molL-1盐
2 3
酸,溶液pH随盐酸加入体积的变化如下图所示。下列说法不正确的是( )
已知:常温常压下,1体积水能溶解约1体积CO
2
A.a点的溶液中,c(Na)6c(Cl)
B.b点(pH=7)的溶液中,2n(CO2)n(HCO)0.001mol
3 3
C.c点的溶液pH<7,是因为碳酸的电离程度大于HCO的水解程度
3
D.水的电离程度:b O>S,A错误;
B.Y、W的简单氢化物分别是 , 形成的晶体中一个水分子周围紧邻的分子数为4个, 形
成的晶体中一个 分子周围紧邻的分子数为12个,B错误;
C. 中N原子价电子对数为 ,无孤电子对; 中N原子价电子对数为 ,有1个孤电子对,
所以键角 > ,故C错误;
D.W的氧化物是CaO,能与水反应,可用作干燥剂,D正确;
6.B
A. 铜、铝水膜容易形成原电池,腐蚀金属而断路
B. 2Al3Ag S6H O2Al(OH) 6Ag+3H S
2 2 3 2
C. 丙三醇有羟基,是亲水基团,能让皮肤保水
D. 热的纯碱能促进酯的水解
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}7.B
A.含有碳碳三键的物质易加成,所以后者不稳定,正确;
CCl COOH CH COOH CFCOOH
B.电负性:F>Cl>H,由 3 酸性强于 3 可推出 3 酸性强于
CH COOH
3 ,C正确;
C.氮价电子排布式2S22P3,氮价电子排布式2S22P4,氮的第二电离能失去的2P3上的电子,
半充满,稳定,要失去所需能量大。
D.碱金属元素单质从Li到Rb,金属键逐渐较弱,熔沸点逐渐降低,所以Li的熔点最高。
8.A
A.该物质中铜离子的配位数是4,A项错误;
B.基态Cu原子的电子排布式为 [Ar]3d104s1,含有1个未成对电子,B项正确;
C.该反应过程中既有极性键氮氢键的断裂又有极性键的生成,C项正确;
D.缩二脲分子中碳为双键碳,采取sp2杂化,氮原子形成的均为单键,采取sp3杂化。D
项正确。
9.C
A.Pt电极上发生失电子的反应,是氧化反应,对
B.阳离子向阴极移动,H+由电解池左侧移向右侧,对
C.当外电路转移2mol电子时,两极共收集15.68L气体,没有说标准状况下,错
D.阴极反应式为2NO +10e-+12H+=6H2O+N2↑,对
10.B
A.由图可知,反应③过程中,涉及碳氮极性键的形成,故A错误;
B.三键氮原子的杂化方式为sp杂化、双键氮原子的杂化方式为sp2杂化,所以转化过程中
氮原子的杂化方式发生改变,故B正确;
C.反应过程中,共有5种中间产物,故C错误;
D.由题意可知,该反应的总反应是一价铜催化的叠氮化物-端炔烃环加成反应,故D错误;
11.B
12.D
反应Ⅰ速率远大于反应Ⅱ,t1时刻CO浓度最大,说明反应Ⅰ此时处于平衡状态,结合碳原
子守恒和题中给出的CO、CO2浓度,可知t1时刻HCOOH的浓度为(1.0-0.70-0.16)mol·L
-1=0.14mol·L-1,则反应I的平衡常数K1=c(CO)c(HCOOH)=0.700.14=5
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}由上述分析及近似认为反应I建立平衡后始终处于平衡状态,知t1时刻之后一氧化碳的浓
度始终是甲酸浓度的5倍,反应Ⅱ平衡时c(CO2)=c(H2)=ymol·L-1,则结合碳原子守恒
知,平衡体系中c(HCOOH)=16×(1.0-y)mol·L-1,c(CO)=56×(1.0-y)mol·L-1,反
应Ⅱ的平衡常数K2=6y21.0-y。加入0.10mol·L-1盐酸后,H+作催化剂,反应Ⅰ的反
应速率加快,达平衡的时间缩短,反应Ⅱ消耗的HCOOH减少,体系中HCOOH浓度增大,
导致CO浓度大于t1时刻的峰值,则CO新的浓度峰值点可能是a点。
13.B
A.盐酸也能使高锰酸钾褪色,故A错误;
NaHCO
B.碳酸钠溶于水放热,碳酸氢钠溶于水吸热,温度降低证明该固体为 3,故B正确;
AlCl AlCl
C. 3为强电解质,其水溶液可以导电,但 3属于共价化合物,不含离子键
,故C错误;
CuSO
D. 4溶液本身呈蓝色,会干扰pH试纸的颜色,故D错误;
14.D
A.由分析可知,P型半导体为正极,A错误;
B.由题中图示信息和分析可知,Na+离子通过e膜,Cl-通过d膜,(CH3)4N+通过c膜,所
以c、e膜为阳离子交换膜,d为阴离子交换膜,B错误;
C.由题中信息可知,a为阴极,发生得电子的还原反应,其电极反应式为 ,C错误;
D.a极电极反应式为 ,b极电极反应式为 ,收集氢气与氧气的体积比为2:1,收集氢气 ,
氧气为 ,转移电子为 ,所以四甲基氢氧化铵为 ,18.2g;D正确。
15.D
A.a点加入5mL的溶液中0.1molL1盐酸,得到溶液中氢氧化钠、氯化钠、碳酸钠物质的
量之比为1:1:2,故溶液中C(Na+)=6C(Cl-),A正确;
B.b点加入盐酸体积大于20mL,则n
Cl-
>0.002mol,根据电荷守恒可知,
n
Na+
+n
H+
=n
OH-
+n
Cl-
+2n
CO2-
+n
HCO-
,pH7,则n
H+
=n
OH-
,故
3 3
n
Na+
=n
Cl-
+2n
CO2-
+n
HCO-
;由钠元素守恒可知,n
Na+
=0.003mol,则溶液中
3 3
2n
CO2-
+n
HCO-
<0.001mol,B正确;
3 3
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}C.c点溶液中含有氯化钠、碳酸氢钠、碳酸,溶液pH7,是因为碳酸的电离程度大于HCO
3
的水解能力,C错误;
D.b点PH=7水的电离无影响,从b-c-d一直加酸,水的电离受抑制一直增大,所以水的电
离程度在减小,D不正确;
故选D。
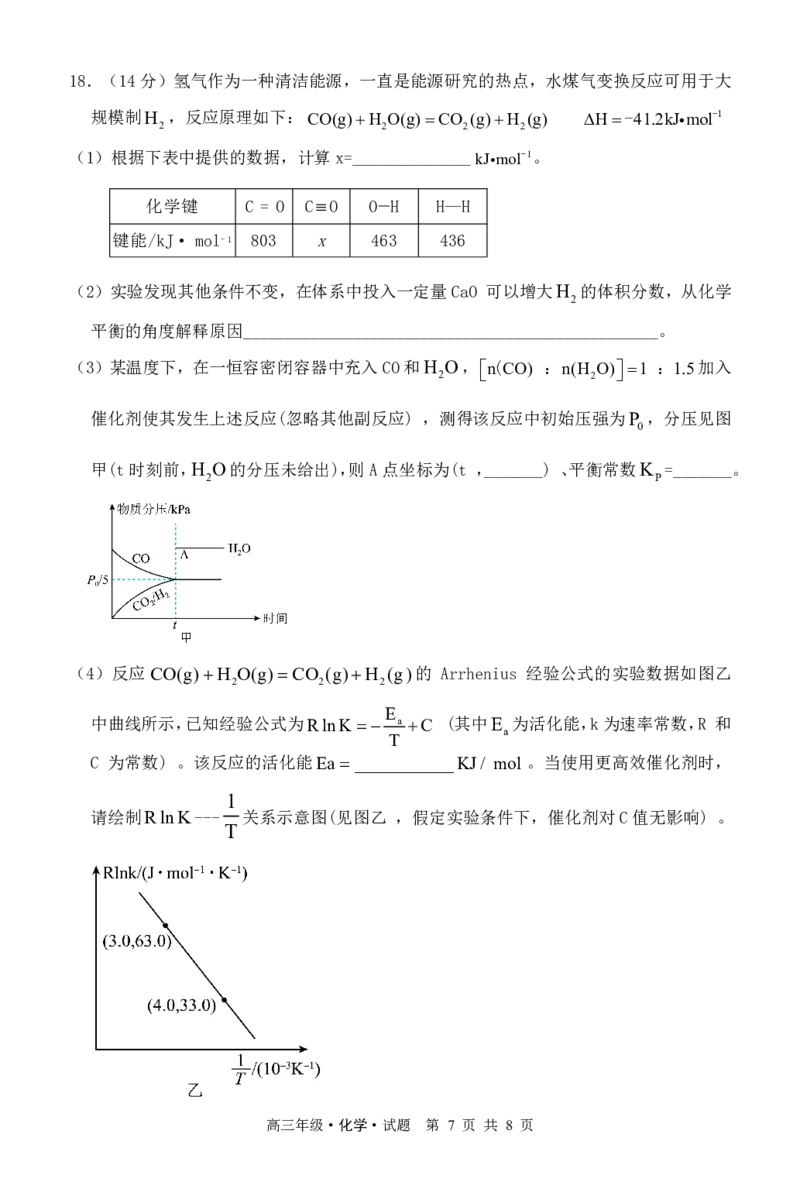
16题答案
(1)粉碎、搅拌、升温、适当提高酸的浓度(合理即可)。(2分)
3CoS8H 8NO 3Co2 3SO 2 8NO4H O
(2) 3 4 2 (2分)
Na Fe SO OH
pH过小,溶液酸性过强,不利于 2 6 4 4 12析出(2分)
(4)9.1(2分)
(5)蒸发浓缩、冷却结晶(2分)
500℃700℃
(6)2CoSO Co O SO SO
4 2 3 2 3
17 答案:(1)三颈烧瓶
(2) ①.MnO +H C O +2H+===2CO ↑+Mn2++2H O
2 2 2 4 2 2
(3) ②. 反应产生的Mn2+对反应具有催化作用
(3) MnSO +2NH HCO ==MnCO ↓+CO ↑+H O+(NH ) SO4
4 4 3 3 2 2 4 2
(4) 乙醇
(5)不行,过量的过氧化氢可能会氧化Mn2+
(6)550CV/19%
18答案 (每空2分)
19题答案
Cl
(1) 2 光照(2分)
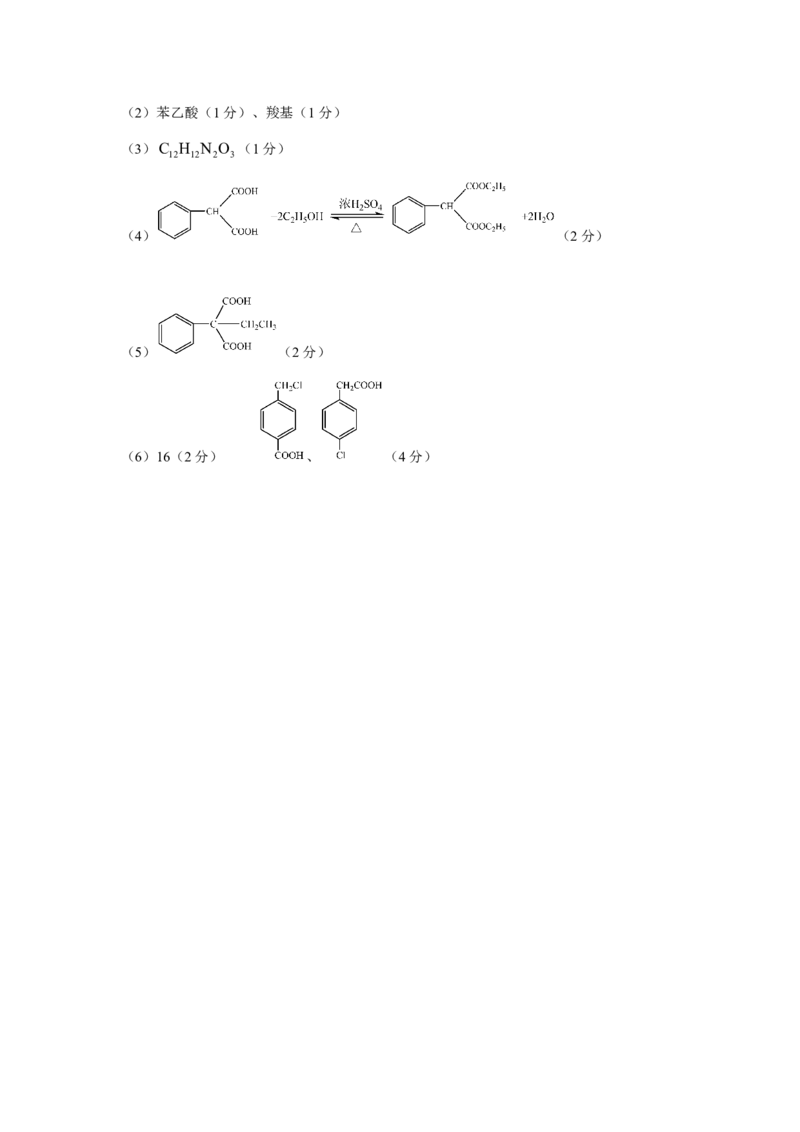
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}(2)苯乙酸(1分)、羧基(1分)
(3)C H N O (1分)
12 12 2 3
(4) (2分)
(5) (2分)
(6)16(2分) 、 (4分)
{#{QQABbYIUggiIAAIAABhCQQGoCkKQkBGCAKoOBEAIMAABwRNABAA=}#}