文档内容
2019年贵州省贵阳市中考化学试卷
一、化学选择题:本题包括6个小题,每小题2分,共12分.每题只有一个选项符合题意.
1.(2分)习近平主席在今年的北京世界园艺博览会上告诉各国来宾:“中国生态文明建设进
入了快车道,天更蓝、山更绿、水更清将不断展现在世人面前”。下列对环境友好的是(
)
A.提倡使用一次性木筷 B.大力增加绿地面积
C.生活垃圾随意丢弃 D.大量使用燃油车代步
2.(2分)生活中处处有化学。下列说法不正确的是( )
A.将肥皂水涂抹在蚊虫叮咬处可减轻痛痒
B.可通过煮沸来降低水的硬度
C.家用电器着火,可用水浇灭
D.铁制品在潮湿的空气中容易生锈
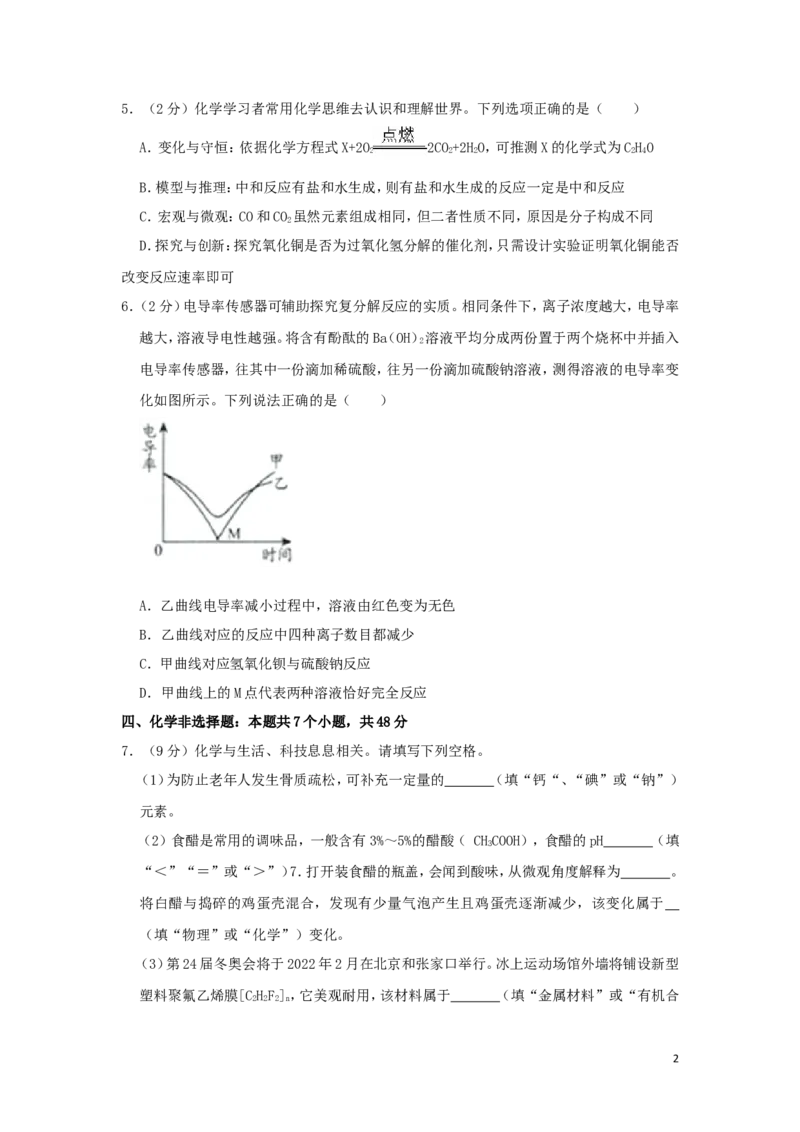
3.(2 分)化学是一门以实验为基础的科学。下列仪器用途不正确的是( )
A.A B.B C.C D.D
4.(2分)归纳、整理是学习化学的有效方法。下列选项正确的是( )
A.认识化学式 B.性质决定用途
“珍惜生命,远离毒品” 石墨具有良好的导电性﹣﹣可作电极
某毒品化学式为C H ON,该物质由四种 氧气具有助燃性﹣﹣可作燃料
12 19 2
元素组成:该物质由33个原子构成
C.理解化学方程式 D.化学与能源
化石燃料属于不可再生能源;
2HO 2H+O↑,反应条件为通电:
2 2 2
太阳能、风能、氢能属于清洁能源
该反应中,水、氢气、氧气的质量比为2:
2:1
A.A B.B C.C D.D
15.(2分)化学学习者常用化学思维去认识和理解世界。下列选项正确的是( )
A.变化与守恒:依据化学方程式X+2O 2CO+2HO,可推测X的化学式为CHO
2 2 2 2 4
B.模型与推理:中和反应有盐和水生成,则有盐和水生成的反应一定是中和反应
C.宏观与微观:CO和CO 虽然元素组成相同,但二者性质不同,原因是分子构成不同
2
D.探究与创新:探究氧化铜是否为过氧化氢分解的催化剂,只需设计实验证明氧化铜能否
改变反应速率即可
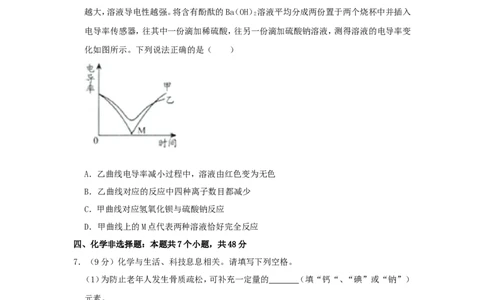
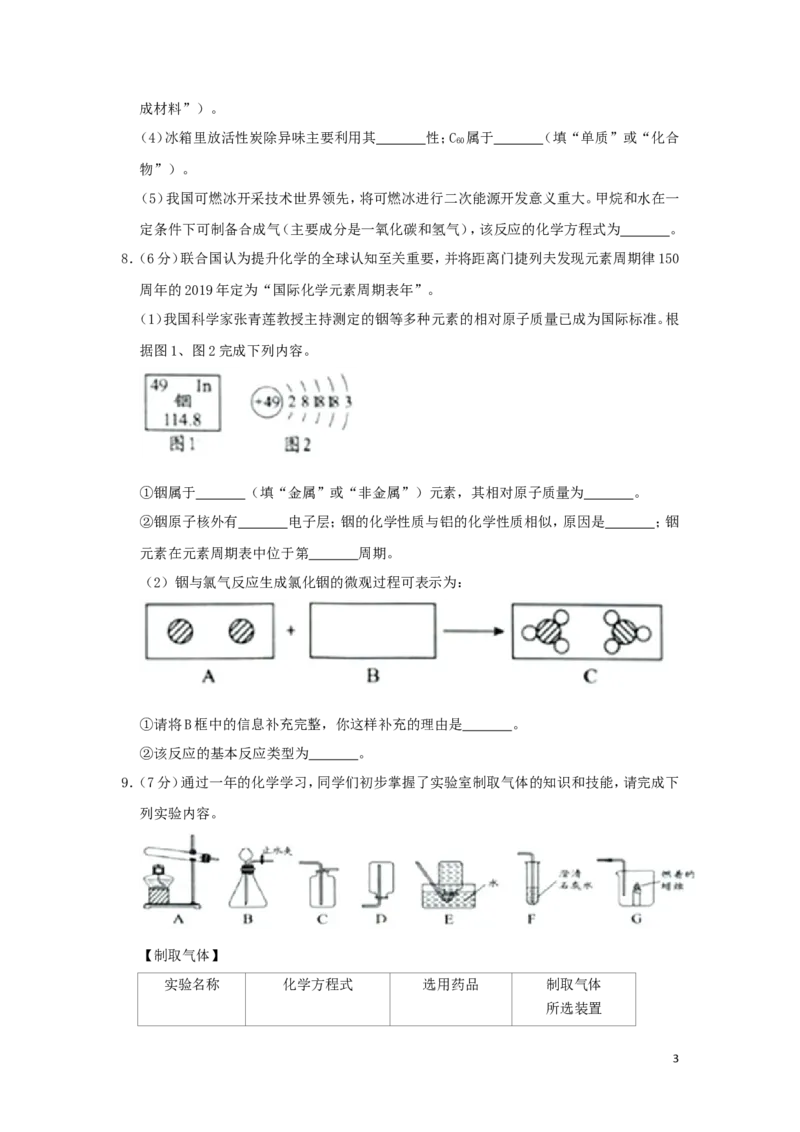
6.(2分)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率
越大,溶液导电性越强。将含有酚酞的Ba(OH)溶液平均分成两份置于两个烧杯中并插入
2
电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,测得溶液的电导率变
化如图所示。下列说法正确的是( )
A.乙曲线电导率减小过程中,溶液由红色变为无色
B.乙曲线对应的反应中四种离子数目都减少
C.甲曲线对应氢氧化钡与硫酸钠反应
D.甲曲线上的M点代表两种溶液恰好完全反应
四、化学非选择题:本题共7个小题,共48分
7.(9分)化学与生活、科技息息相关。请填写下列空格。
(1)为防止老年人发生骨质疏松,可补充一定量的 (填“钙“、“碘”或“钠”)
元素。
(2)食醋是常用的调味品,一般含有3%~5%的醋酸( CHCOOH),食醋的pH (填
3
“<”“=”或“>”)7.打开装食醋的瓶盖,会闻到酸味,从微观角度解释为 。
将白醋与捣碎的鸡蛋壳混合,发现有少量气泡产生且鸡蛋壳逐渐减少,该变化属于
(填“物理”或“化学”)变化。
(3)第24届冬奥会将于2022年2月在北京和张家口举行。冰上运动场馆外墙将铺设新型
塑料聚氟乙烯膜[CHF],它美观耐用,该材料属于 (填“金属材料”或“有机合
2 2 2 n
2成材料”)。
(4)冰箱里放活性炭除异味主要利用其 性;C 属于 (填“单质”或“化合
60
物”)。
(5)我国可燃冰开采技术世界领先,将可燃冰进行二次能源开发意义重大。甲烷和水在一
定条件下可制备合成气(主要成分是一氧化碳和氢气),该反应的化学方程式为 。
8.(6分)联合国认为提升化学的全球认知至关重要,并将距离门捷列夫发现元素周期律150
周年的2019年定为“国际化学元素周期表年”。
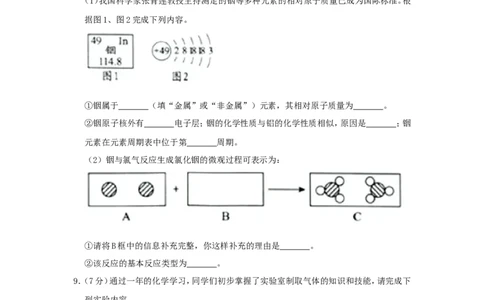
(1)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。根
据图1、图2完成下列内容。
①铟属于 (填“金属”或“非金属”)元素,其相对原子质量为 。
②铟原子核外有 电子层;铟的化学性质与铝的化学性质相似,原因是 ;铟
元素在元素周期表中位于第 周期。
(2)铟与氯气反应生成氯化铟的微观过程可表示为:
①请将B框中的信息补充完整,你这样补充的理由是 。
②该反应的基本反应类型为 。
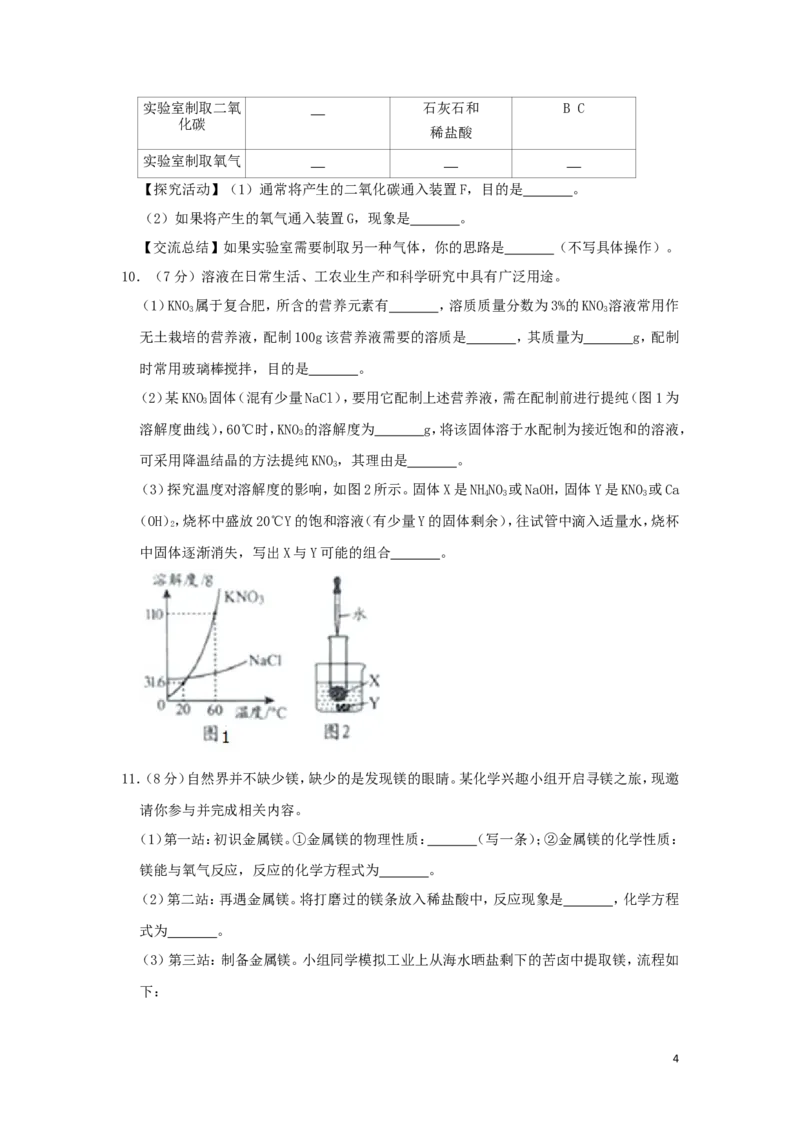
9.(7分)通过一年的化学学习,同学们初步掌握了实验室制取气体的知识和技能,请完成下
列实验内容。
【制取气体】
实验名称 化学方程式 选用药品 制取气体
所选装置
3实验室制取二氧 石灰石和 B C
化碳
稀盐酸
实验室制取氧气
【探究活动】(1)通常将产生的二氧化碳通入装置F,目的是 。
(2)如果将产生的氧气通入装置G,现象是 。
【交流总结】如果实验室需要制取另一种气体,你的思路是 (不写具体操作)。
10.(7分)溶液在日常生活、工农业生产和科学研究中具有广泛用途。
(1)KNO 属于复合肥,所含的营养元素有 ,溶质质量分数为3%的KNO 溶液常用作
3 3
无土栽培的营养液,配制100g该营养液需要的溶质是 ,其质量为 g,配制
时常用玻璃棒搅拌,目的是 。
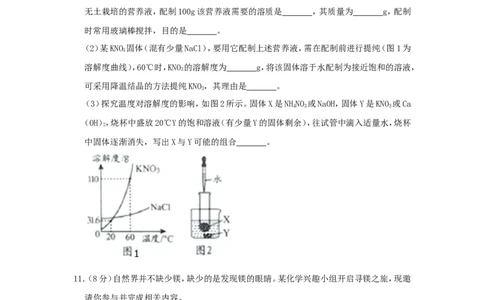
(2)某KNO 固体(混有少量NaCl),要用它配制上述营养液,需在配制前进行提纯(图1为
3
溶解度曲线),60℃时,KNO 的溶解度为 g,将该固体溶于水配制为接近饱和的溶液,
3
可采用降温结晶的方法提纯KNO,其理由是 。
3
(3)探究温度对溶解度的影响,如图2所示。固体X是NHNO 或NaOH,固体Y是KNO 或Ca
4 3 3
(OH),烧杯中盛放20℃Y的饱和溶液(有少量Y的固体剩余),往试管中滴入适量水,烧杯
2
中固体逐渐消失,写出X与Y可能的组合 。
11.(8分)自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀
请你参与并完成相关内容。
(1)第一站:初识金属镁。①金属镁的物理性质: (写一条);②金属镁的化学性质:
镁能与氧气反应,反应的化学方程式为 。
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是 ,化学方程
式为 。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如
下:
4苦卤 Mg(OH) MgCl Mg,流程中X为 。
2 2
(4)第四站:再探金属镁。
【提出问题】镁能否与热水反应?如果反应,产物是什么?
【相关信息】①Mg+2HO=Mg(OH)+H↑;②氢氧化镁在热水中能部分溶解。
2 2 2
实验操作 实验现象 实验结论
镁能与热水反应,生成氢氧化镁和氢气
(5)上述寻镁之旅中你收获到镁的化学性质有 。
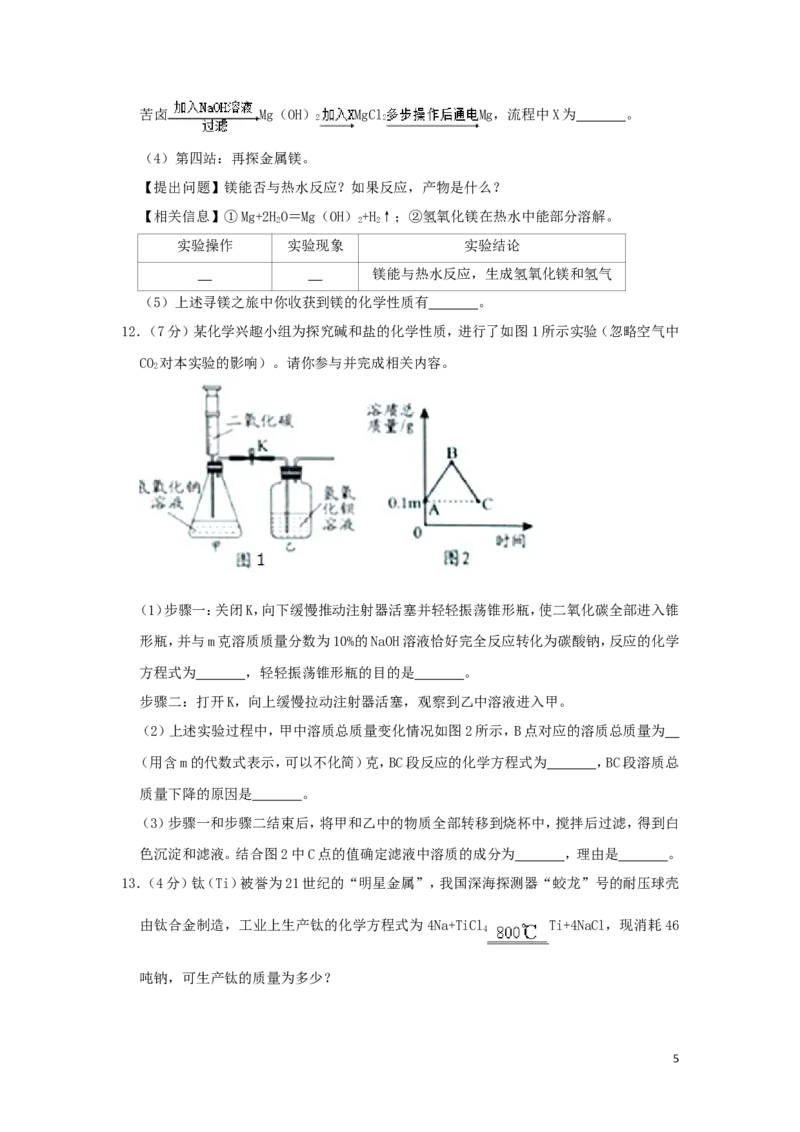
12.(7分)某化学兴趣小组为探究碱和盐的化学性质,进行了如图1所示实验(忽略空气中
CO 对本实验的影响)。请你参与并完成相关内容。
2
(1)步骤一:关闭K,向下缓慢推动注射器活塞并轻轻振荡锥形瓶,使二氧化碳全部进入锥
形瓶,并与m克溶质质量分数为10%的NaOH溶液恰好完全反应转化为碳酸钠,反应的化学
方程式为 ,轻轻振荡锥形瓶的目的是 。
步骤二:打开K,向上缓慢拉动注射器活塞,观察到乙中溶液进入甲。
(2)上述实验过程中,甲中溶质总质量变化情况如图2所示,B点对应的溶质总质量为
(用含m的代数式表示,可以不化简)克,BC段反应的化学方程式为 ,BC段溶质总
质量下降的原因是 。
(3)步骤一和步骤二结束后,将甲和乙中的物质全部转移到烧杯中,搅拌后过滤,得到白
色沉淀和滤液。结合图2中C点的值确定滤液中溶质的成分为 ,理由是 。
13.(4分)钛(Ti)被誉为21世纪的“明星金属”,我国深海探测器“蛟龙”号的耐压球壳
由钛合金制造,工业上生产钛的化学方程式为4Na+TiCl Ti+4NaCl,现消耗46
4
吨钠,可生产钛的质量为多少?
52019年贵州省贵阳市中考化学试卷
参考答案
一、化学选择题:本题包括6个小题,每小题2分,共12分.每题只有一个选项符合题意.
1.B; 2.C; 3.A; 4.D; 5.C; 6.D;
四、化学非选择题:本题共7个小题,共48分
7.钙;<;分子不断的运动;化学;有机合成材料;吸附;单质;CH+HO CO+3H;
4 2 2
8.金属;114.8;5;最外层电子数相同;5;化学反应前后原子的种类、数目不变,一个氯分子
是由两个氯原子构成;化合反应; 9.CaCO +2HCl = CaC l+HO+CO↑;2HO
3 2 2 2 2 2
2HO+O↑;过氧化氢和二氧化锰; B C 或 B E;检验二氧化碳;蜡烛燃烧的更加剧烈; ① 确定反应
2 2
原理,选择药品;
② 根据反应物的状态和反应发生需要的条件确定发生装置;根据气体的密度和水溶性,确定
收集装置;
③ 确定如何验证制取的气体 。; 10. K 、 N;硝酸钾;3;加快溶解速率;110;硝酸钾的溶解度受
温度的影响大,随温度降低其溶解度急剧减小,而氯化钠的溶解度受温度影响较小,故降温
时硝酸钾析出;NHNO 、 C a( O H ) ;或 NaO H 、 KN O; 11.银白色;2Mg+O = 2Mg O;固体逐渐减少,有
4 3 2 3 2
大量气泡产生; Mg+2HC l = MgC l+H↑;盐酸; ① 将打磨好的镁条放入盛有热水的试管中,收集
2 2
气体并将气体点燃;
② 反应后向试管中滴入酚酞沉淀 。; ① 气体被点燃;
② 溶液由无色变成红色。 ; : ① 能与氧气反应; ② 能与酸反应; ③ 能与热水反应 ; 12.
2NaOH+CO = N aCO+HO;增大接触面积使氢氧化钠溶液和二氧化碳充分反应; ;
2 2 3 2
NaCO +B a( O H ) = BaC O ↓ +2NaO H; 加入的氢氧化钡溶液和碳酸钠溶液反应生成沉淀,每 17 1
2 3 2 3
份质量的氢氧化钡,生成 19 7 份质量的碳酸钡沉淀溶质质量减少 2 6 质量,所以 B C 段溶质总
质量下降;氢氧化钡和氢氧化钠; 根据图 2 所提供的信息可知,在 C 点溶质的质量为 0.1 m 克
与 A 点相等,说明步骤一生成的碳酸钠和步骤二中进入的氢氧化钡恰好完全反应,此时溶液
中只有氢氧化钠,将甲和乙混合后氢氧化钡有剩余,因此溶液中的溶质成分为氢氧化钡和氢
氧化钠; 13. ;
67