文档内容
姓名 座位号
(在此卷上答题无效)
绝密 ★ 启用前
2025 届安徽省“江南十校”联考
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号框涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号框。回答非选择题时,将答案写在答题卡上,写
在本试卷上无效。
3.考试结束后,将答题卡交回。
可能用到的相对原子质量:H-1 Li-7 C-12 O-16 S-32 Cl-35.5 Fe-56
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.安徽省文化底蕴深厚,物产丰富。下列说法不正确的是
A.徽墨以松树、胶等为主要原料,经复杂的化学、物理变化而制成
B.宣纸有“纸寿千年”之誉,其主要成分为蛋白质
C.淮南八公山豆腐,制作过程中应用了胶体的性质
D.六安瓜片中含有的茶多酚具有抗氧化作用
2.下列有关晶体的说法正确的是
A.含有阳离子的晶体中,一定含有阴离子
B.氯化钠是由阴、阳离子间通过静电引力结合而成的离子晶体
C.二氧化硅是由共价键结合而成的共价晶体
D.干冰内有共价键,分子间既存在范德华力又存在氢键
3.化学是一门以实验为基础的学科,下列有关说法不正确的是
A.镁条着火时,不可用泡沫灭火器灭火
B.在通风橱中取用液溴时,需戴手套和护目镜
C.KSCN溶液存放于无机盐类试剂柜
D.利用红外光谱仪测定有机物的相对分子质量
4.下列各组离子在给定溶液中一定能大量共存的是
A.C H OH的水溶液中:K+、MnO -、H+、SO 2-
2 5 4 4
B.0.1mol·L-1CH COOH水溶液中:SO 2-、NH +、Br-、H+
3 4 4
C.能使甲基橙变黄的水溶液中:Mg2+、K+、ClO - 、SCN-
4
D.澄清透明的水溶液中:Na+、Al3+、S2-、Cl-
阅读以下材料,回答5-6题:
地壳中铁元素含量较高。工业上用黄铁矿石(主要含FeS )为原料生产硫酸;铁具有还原性,
2
能被卤素单质、H+等氧化,还能与水蒸气在高温下反应;铁及其化合物常用作催化剂。
5.用N 表示阿伏加德罗常数的值,下列说法一定正确的是
A
A.1L1mol·L-1Fe (SO ) 溶液中含有阳离子的数目大于2N
2 4 3 A
B.5.6gFe与0.1L1mol·L-1盐酸充分反应产生气体体积为1.12L
C.0.1molCl 与足量的铁粉充分反应,转移电子数为0.3N
2 A
化学试卷 第 1 页 共 8 页D.1molFe(CO) 中配位原子的质子数为40N
5 A
6.关于铁及其化合物,下列说法正确的是
A.用黄铁矿石制硫酸可经过两步转化实现:FeS O 2SO H2 OH SO
2 高温 3 2 4
B.铁与水蒸气在高温下反应后的剩余固体能被磁铁吸引,证明产物有磁性氧化铁
C.FeCl 与K [Fe(CN) ]溶液反应生成KFe[Fe(CN) ]沉淀
2 3 6 6
D.实验室制溴苯涉及的物质转化:FeBr 2FeBr ,
2
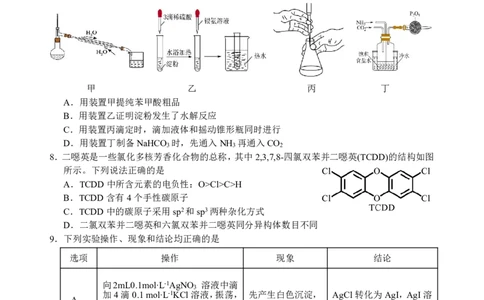
7.下列有关实验装置和操作的说法正确的是
甲 乙 丙 丁
A.用装置甲提纯苯甲酸粗品
B.用装置乙证明淀粉发生了水解反应
C.用装置丙滴定时,滴加液体和摇动锥形瓶同时进行
D.用装置丁制备NaHCO 时,先通入NH 再通入CO
3 3 2
8.二噁英是一些氯化多核芳香化合物的总称,其中2,3,7,8-四氯双苯并二噁英(TCDD)的结构如图
所示。下列说法正确的是
A.TCDD中所含元素的电负性:O>Cl>C>H
B.TCDD含有4个手性碳原子
C.TCDD中的碳原子采用sp2和sp3两种杂化方式
D.二氯双苯并二噁英和六氯双苯并二噁英同分异构体数目不同
9.下列实验操作、现象和结论均正确的是
选项 操作 现象 结论
向2mL0.1mol·L-1AgNO 溶液中滴
3
加4滴0.1mol·L-1KCl溶液,振荡, 先产生白色沉淀, AgCl转化为AgI,AgI溶
A.
观察;再滴加4滴0.1mol·L-1KI溶 后产生黄色沉淀 解度小于AgCl溶解度
液,振荡、观察
光照新制氯水,用pH传感器和Cl- 光照时氯水中HClO发生
B. pH和c(Cl-)均增大
传感器采集数据 了分解
先产生的蓝色沉淀
向CuSO 溶液中逐滴加入过量的 相同条件下,与Cu2+结合
C. 4 逐渐溶解,最终形
氨水 的能力:NH >H O
成深蓝色溶液 3 2
在大试管中加入2.5g苯酚和
苯酚和甲醛发生了加聚
D. 2.5mL40%甲醛溶液,再加入1mL 溶液分层
反应
浓盐酸(催化剂),并加热
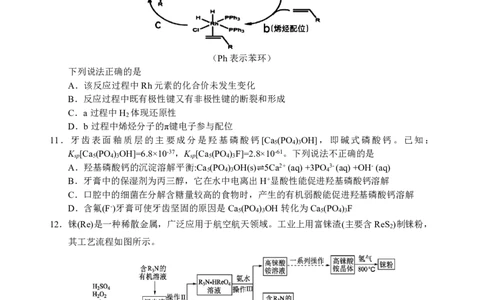
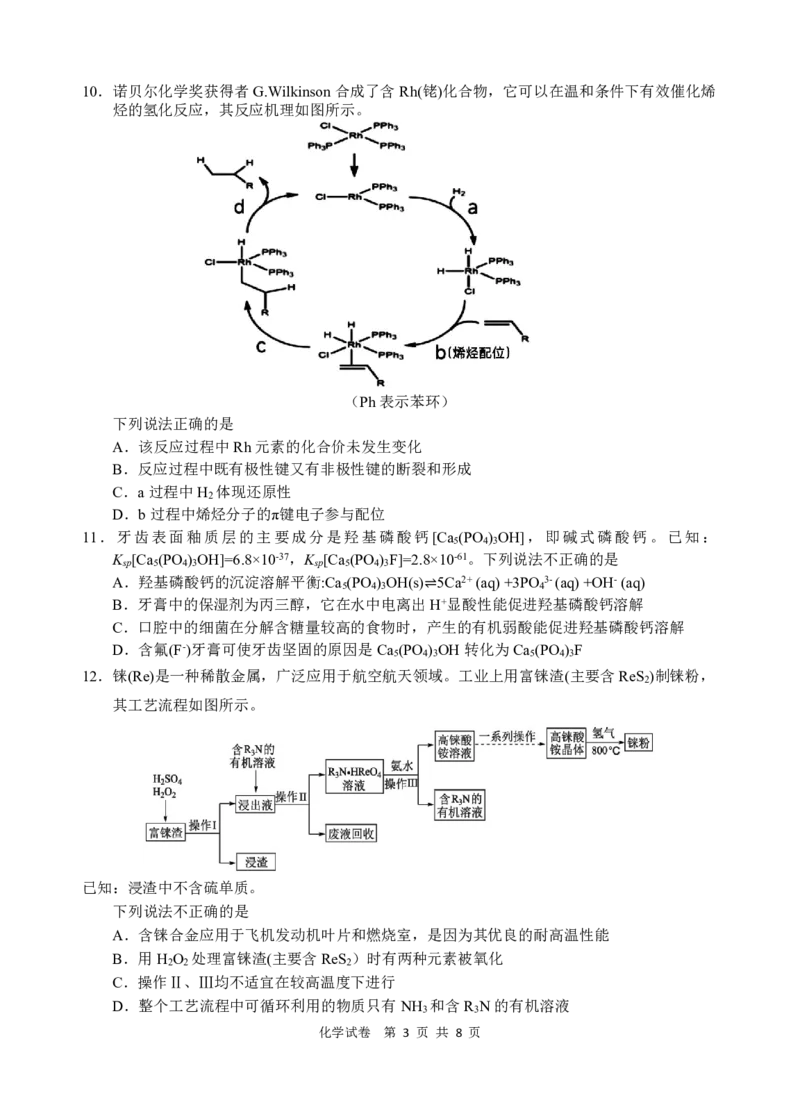
化学试卷 第 2 页 共 8 页10.诺贝尔化学奖获得者G.Wilkinson合成了含Rh(铑)化合物,它可以在温和条件下有效催化烯
烃的氢化反应,其反应机理如图所示。
(Ph表示苯环)
下列说法正确的是
A.该反应过程中Rh元素的化合价未发生变化
B.反应过程中既有极性键又有非极性键的断裂和形成
C.a过程中H 体现还原性
2
D.b过程中烯烃分子的π键电子参与配位
11.牙齿表面釉质层的主要成分是羟基磷酸钙[Ca (PO ) OH],即碱式磷酸钙。已知:
5 4 3
K [Ca (PO ) OH]=6.8×10-37,K [Ca (PO ) F]=2.8×10-61。下列说法不正确的是
sp 5 4 3 sp 5 4 3
A.羟基磷酸钙的沉淀溶解平衡:Ca (PO ) OH(s) 5Ca2+(aq)+3PO 3-(aq)+OH-(aq)
5 4 3 4
B.牙膏中的保湿剂为丙三醇,它在水中电离出H+显酸性能促进羟基磷酸钙溶解
⇌
C.口腔中的细菌在分解含糖量较高的食物时,产生的有机弱酸能促进羟基磷酸钙溶解
D.含氟(F-)牙膏可使牙齿坚固的原因是Ca (PO ) OH转化为Ca (PO ) F
5 4 3 5 4 3
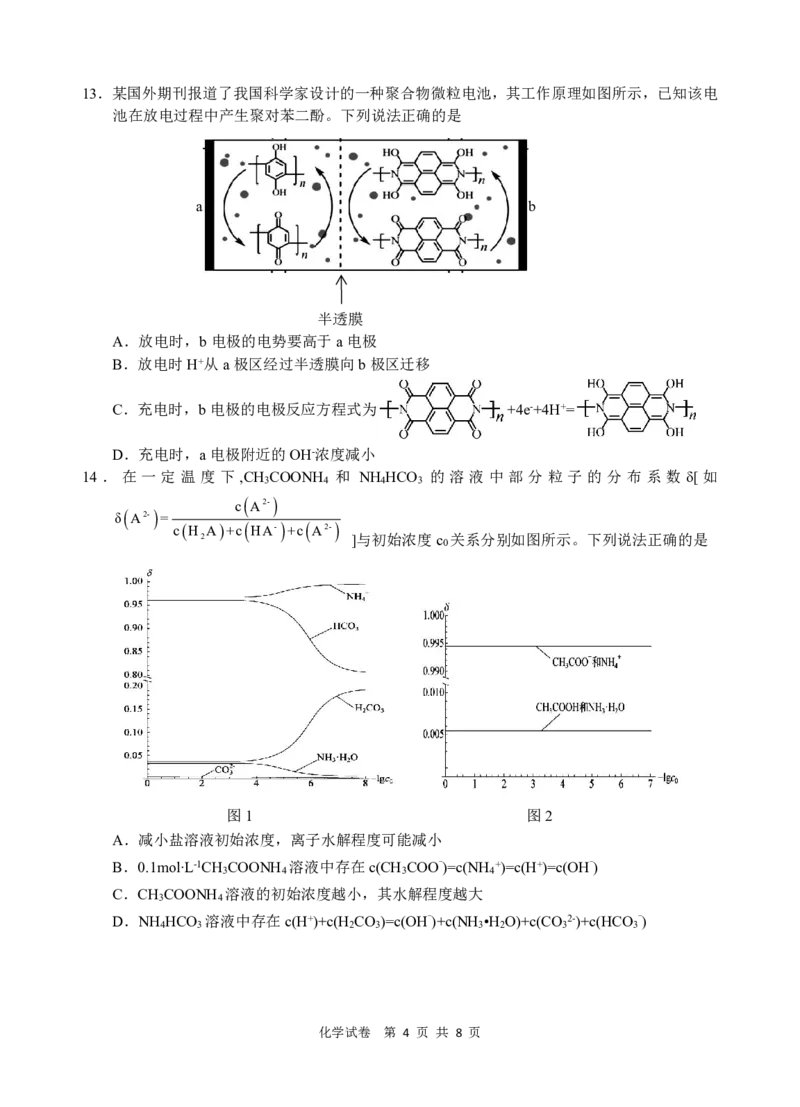
12.铼(Re)是一种稀散金属,广泛应用于航空航天领域。工业上用富铼渣(主要含ReS )制铼粉,
2
其工艺流程如图所示。
已知:浸渣中不含硫单质。
下列说法不正确的是
A.含铼合金应用于飞机发动机叶片和燃烧室,是因为其优良的耐高温性能
B.用H O 处理富铼渣(主要含ReS )时有两种元素被氧化
2 2 2
C.操作Ⅱ、Ⅲ均不适宜在较高温度下进行
D.整个工艺流程中可循环利用的物质只有NH 和含R N的有机溶液
3 3
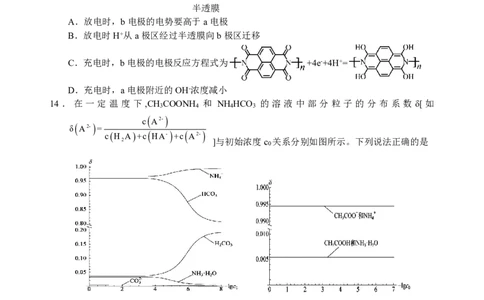
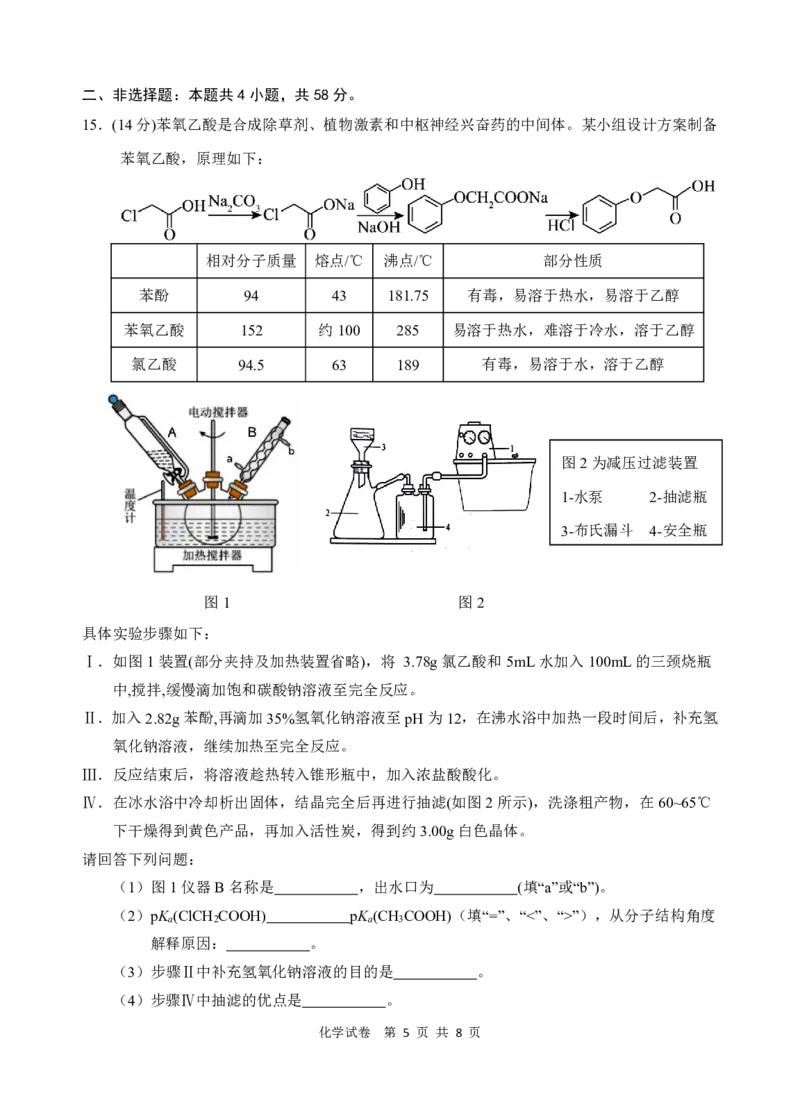
化学试卷 第 3 页 共 8 页13.某国外期刊报道了我国科学家设计的一种聚合物微粒电池,其工作原理如图所示,已知该电
池在放电过程中产生聚对苯二酚。下列说法正确的是
a b
半透膜
A.放电时,b电极的电势要高于a电极
B.放电时H+从a极区经过半透膜向b极区迁移
C.充电时,b电极的电极反应方程式为 +4e-+4H+=
D.充电时,a电极附近的OH-浓度减小
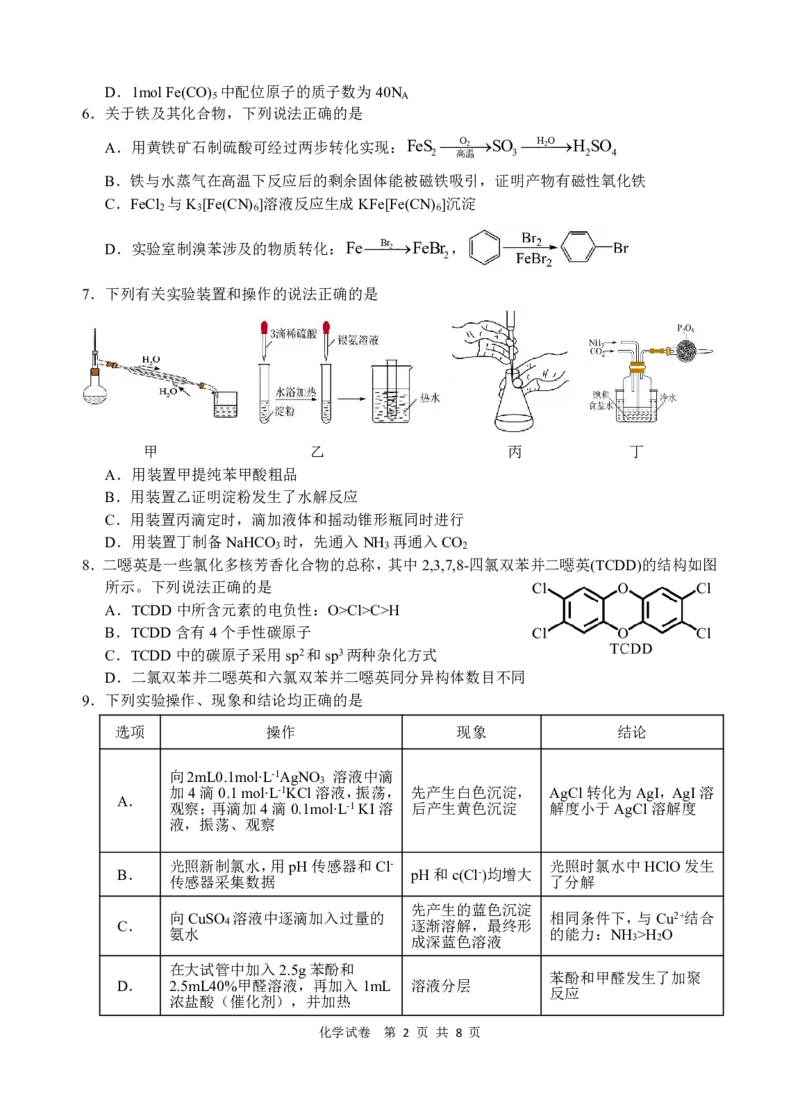
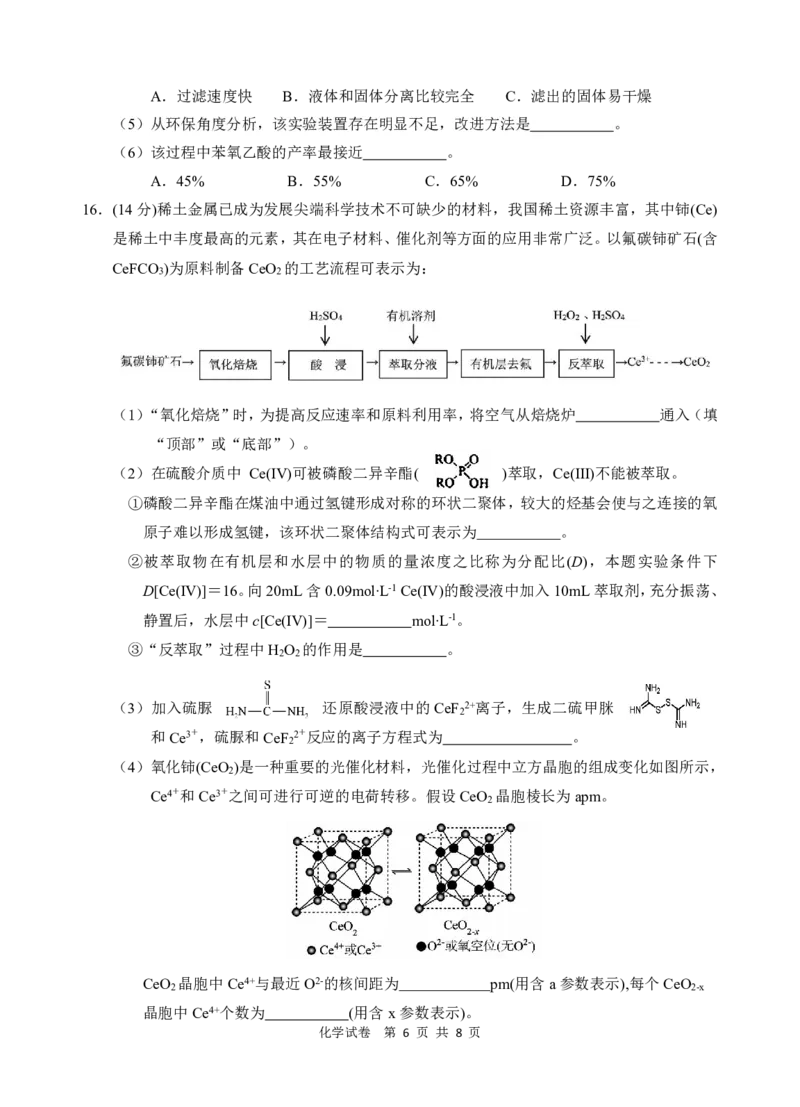
14 . 在 一 定 温 度 下 ,CH COONH 和 NH HCO 的 溶 液 中 部 分 粒 子 的 分 布 系 数 δ[ 如
3 4 4 3
c
A2-
δ
A2-
=
cH A+c HA- +c A2-
2 ]与初始浓度c 关系分别如图所示。下列说法正确的是
0
图1 图2
A.减小盐溶液初始浓度,离子水解程度可能减小
B.0.1mol·L-1CH COONH 溶液中存在c(CH COO-)=c(NH +)=c(H+)=c(OH-)
3 4 3 4
C.CH COONH 溶液的初始浓度越小,其水解程度越大
3 4
D.NH HCO 溶液中存在c(H+)+c(H CO )=c(OH-)+c(NH •H O)+c(CO 2-)+c(HCO -)
4 3 2 3 3 2 3 3
化学试卷 第 4 页 共 8 页二、非选择题:本题共4小题,共58分。
15.(14分)苯氧乙酸是合成除草剂、植物激素和中枢神经兴奋药的中间体。某小组设计方案制备
苯氧乙酸,原理如下:
相对分子质量 熔点/℃ 沸点/℃ 部分性质
苯酚 94 43 181.75 有毒,易溶于热水,易溶于乙醇
苯氧乙酸 152 约100 285 易溶于热水,难溶于冷水,溶于乙醇
氯乙酸 94.5 63 189 有毒,易溶于水,溶于乙醇
图2为减压过滤装置
1-水泵 2-抽滤瓶
3-布氏漏斗 4-安全瓶
图1 图2
具体实验步骤如下:
Ⅰ.如图1装置(部分夹持及加热装置省略),将 3.78g氯乙酸和5mL水加入100mL的三颈烧瓶
中,搅拌,缓慢滴加饱和碳酸钠溶液至完全反应。
Ⅱ.加入2.82g苯酚,再滴加35%氢氧化钠溶液至pH为12,在沸水浴中加热一段时间后,补充氢
氧化钠溶液,继续加热至完全反应。
Ⅲ.反应结束后,将溶液趁热转入锥形瓶中,加入浓盐酸酸化。
Ⅳ.在冰水浴中冷却析出固体,结晶完全后再进行抽滤(如图2所示),洗涤粗产物,在60~65℃
下干燥得到黄色产品,再加入活性炭,得到约3.00g白色晶体。
请回答下列问题:
(1)图1仪器B名称是 ,出水口为 (填“a”或“b”)。
(2)pK (ClCH COOH) pK (CH COOH)(填“=”、“<”、“>”),从分子结构角度
a 2 a 3
解释原因: 。
(3)步骤Ⅱ中补充氢氧化钠溶液的目的是 。
(4)步骤Ⅳ中抽滤的优点是 。
化学试卷 第 5 页 共 8 页A.过滤速度快 B.液体和固体分离比较完全 C.滤出的固体易干燥
(5)从环保角度分析,该实验装置存在明显不足,改进方法是 。
(6)该过程中苯氧乙酸的产率最接近 。
A.45% B.55% C.65% D.75%
16.(14分)稀土金属已成为发展尖端科学技术不可缺少的材料,我国稀土资源丰富,其中铈(Ce)
是稀土中丰度最高的元素,其在电子材料、催化剂等方面的应用非常广泛。以氟碳铈矿石(含
CeFCO )为原料制备CeO 的工艺流程可表示为:
3 2
(1)“氧化焙烧”时,为提高反应速率和原料利用率,将空气从焙烧炉 通入(填
“顶部”或“底部”)。
(2)在硫酸介质中 Ce(IV)可被磷酸二异辛酯( )萃取,Ce(III)不能被萃取。
①磷酸二异辛酯在煤油中通过氢键形成对称的环状二聚体,较大的烃基会使与之连接的氧
原子难以形成氢键,该环状二聚体结构式可表示为 。
②被萃取物在有机层和水层中的物质的量浓度之比称为分配比(D),本题实验条件下
D[Ce(IV)]=16。向20mL含0.09mol·L-1Ce(IV)的酸浸液中加入10mL萃取剂,充分振荡、
静置后,水层中c[Ce(IV)]= mol·L-1。
③“反萃取”过程中H O 的作用是 。
2 2
(3)加入硫脲 还原酸浸液中的CeF 2+离子,生成二硫甲脒
2
和Ce3+,硫脲和CeF 2+反应的离子方程式为 。
2
(4)氧化铈(CeO )是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示,
2
Ce4+和Ce3+之间可进行可逆的电荷转移。假设CeO 晶胞棱长为apm。
2
CeO 晶胞中Ce4+与最近O2-的核间距为 pm(用含a参数表示),每个CeO
2 2-x
晶胞中Ce4+个数为 (用含x参数表示)。
化学试卷 第 6 页 共 8 页17.(15分)2024年10月30日中国航天员搭载神舟十九号载人飞船顺利进入“太空之家”,中国空
间站设有完整的可再生生命保障系统,对二氧化碳进行收集和再生处理,实现了对二氧化
碳的加氢甲烷化,生成甲烷与水,并伴有副反应。
Ⅰ.CO (g)+4H (g) CH (g)+2H O(g) ΔH (主反应)
2 2 4 2 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH (副反应)
2 2 ⇌ 2 2
回答下列问题:
⇌
(1)几种化学键的键能为:E =413kJ• mol-1、E =436kJ •mol-1、E =463kJ •mol-1、
C-H H-H O-H
E =745kJ•mol-1,则ΔH = 。
C=O 1
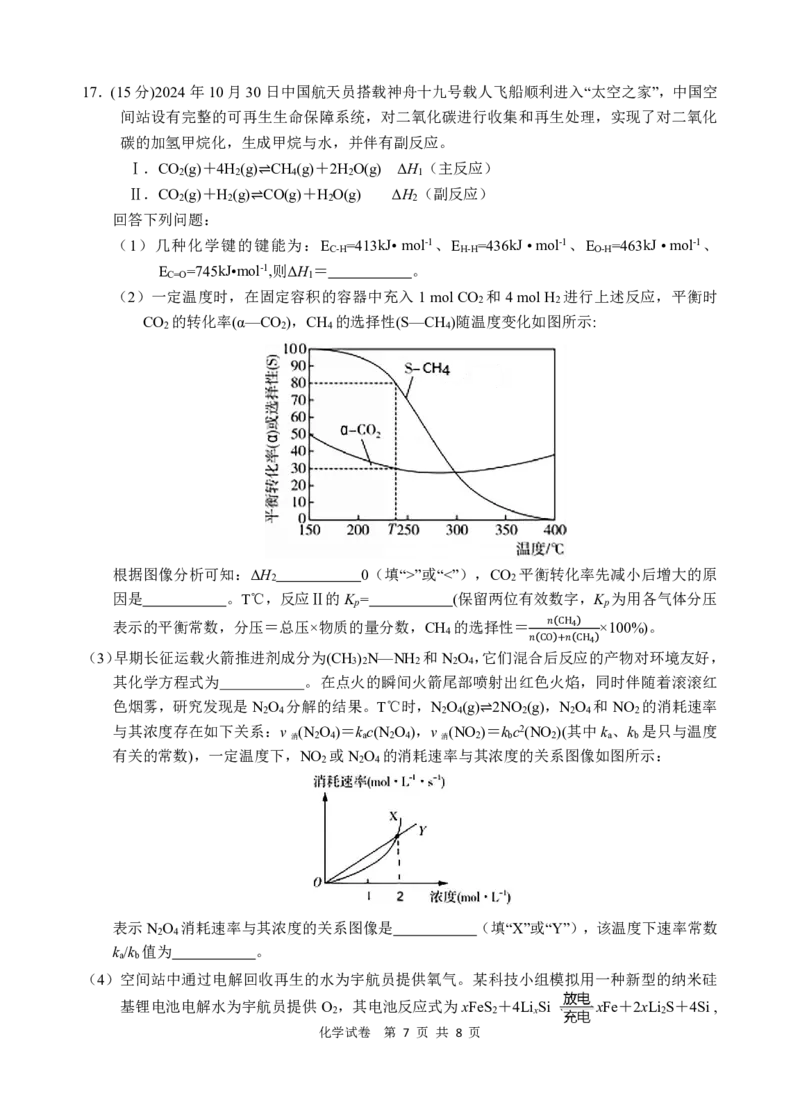
(2)一定温度时,在固定容积的容器中充入1molCO 和4molH 进行上述反应,平衡时
2 2
CO 的转化率(α—CO ),CH 的选择性(S—CH )随温度变化如图所示:
2 2 4 4
根据图像分析可知:ΔH 0(填“>”或“<”),CO 平衡转化率先减小后增大的原
2 2
因是 。T℃,反应Ⅱ的K = (保留两位有效数字,K 为用各气体分压
p p
表示的平衡常数,分压=总压×物质的量分数,CH 的选择性= ×100%)。
4
CH4
(3)早期长征运载火箭推进剂成分为(CH 3 ) 2 N—NH 2 和N 2 O 4 ,它们混合 C 后 O + 反 应 CH 的 4 产物对环境友好,
其化学方程式为 。在点火的瞬间火箭尾部喷射出红色火焰,同时伴随着滚滚红
色烟雾,研究发现是N O 分解的结果。T℃时,N O (g) 2NO (g),N O 和NO 的消耗速率
2 4 2 4 2 2 4 2
与其浓度存在如下关系:v (N O )=k c(N O ),v (NO )=k c2(NO )(其中k 、k 是只与温度
消 2 4 a 2 4 消 2⇌ b 2 a b
有关的常数),一定温度下,NO 或N O 的消耗速率与其浓度的关系图像如图所示:
2 2 4
表示N O 消耗速率与其浓度的关系图像是 (填“X”或“Y”),该温度下速率常数
2 4
k /k 值为 。
a b
(4)空间站中通过电解回收再生的水为宇航员提供氧气。某科技小组模拟用一种新型的纳米硅
基锂电池电解水为宇航员提供O ,其电池反应式为xFeS +4Li Si xFe+2xLi S+4Si,
2 2 x 2
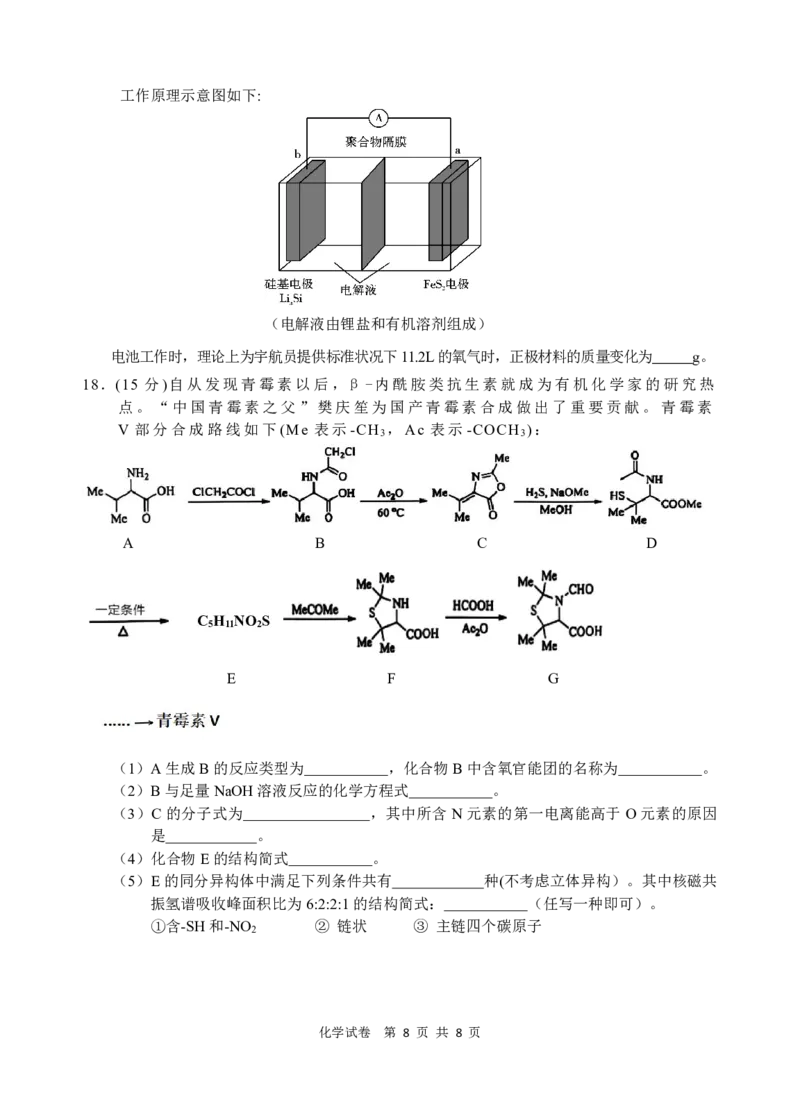
化学试卷 第 7 页 共 8 页工作原理示意图如下:
(电解液由锂盐和有机溶剂组成)
电池工作时,理论上为宇航员提供标准状况下11.2L的氧气时,正极材料的质量变化为 g。
18.(15 分)自从发现青霉素以后,β-内酰胺类抗生素就成为有机化学家的研究热
点。“中国青霉素之父”樊庆笙为国产青霉素合成做出了重要贡献。青霉素
V 部分合成路线如下(Me 表示-CH ,Ac 表示-COCH ):
3 3
A B C D
C H NO S
5 11 2
E F G
(1)A生成B的反应类型为 ,化合物B中含氧官能团的名称为 。
(2)B与足量NaOH溶液反应的化学方程式 。
(3)C的分子式为 ,其中所含N元素的第一电离能高于O元素的原因
是 。
(4)化合物E的结构简式 。
(5)E的同分异构体中满足下列条件共有 种(不考虑立体异构)。其中核磁共
振氢谱吸收峰面积比为6:2:2:1的结构简式: (任写一种即可)。
①含-SH和-NO ② 链状 ③ 主链四个碳原子
2
化学试卷 第 8 页 共 8 页