文档内容
化学参考答案
一、单项选择题(共14小题,每题3分,共42分)
1.【答案】A
【解析】A选项:多酚类化合物和维生素C具有还原性,可抗氧化,怀远石榴汁富含这两种物质,
该说法正确。B选项:碳酸钙是人体骨骼和牙齿的主要成分之一,对人体无毒,蚌埠珍珠主要成分
为碳酸钙,可磨粉冲服,该说法错误。C选项:白莲坡贡米主要成分为淀粉,淀粉水解最终产物为
葡萄糖,而不是氨基酸,该说法错误。D选项:沱湖螃蟹属于动物类食品,主要成分是蛋白质,几
乎不含淀粉,不能作为人体供能的淀粉来源,该说法错误。
2.【答案】D
【解析】A选项:CO 是分子晶体,但SiO 是原子晶体,二者晶体类型不同,类比推理错误。B选
2 2
项:Fe与CuSO 溶液发生置换反应生成FeSO 和Cu,但Na的金属活动性极强,会先与CuSO 溶
4 4 4
液中的水反应生成NaOH和H ,NaOH再与CuSO 反应生成Cu(OH) 沉淀,不能置换出Cu,类比
2 4 2
推理错误。C选项:NaCl与浓H SO 加热可制HCl,是利用难挥发性酸制易挥发性酸;但NaI与
2 4
浓H SO 加热时,I-会被浓H SO 氧化为I,不能制得HI,类比推理错误。D选项:CO 和SO 均
2 4 2 4 2 2 2
为酸性氧化物,与过量的Ba(OH) 反应都生成可溶于水的碳酸氢盐,反应规律相似,类比推理正
2
确。
3.【答案】B
【解析】A选项:铜丝可上下移动,当铜丝插入浓硫酸中时,发生反应生成SO ;当铜丝抽出时,
2
反应停止,有利于达到随制随停的目的,该说法正确。B选项:SO 使品红褪色体现其漂白性,但
2
SO 使蓝色石蕊试纸变红(因为SO 与水反应生成H SO ,显酸性),不会褪色,该说法错误。C
2 2 2 3
选项:SO 具有还原性,能被酸性KMnO 溶液氧化,反应的离子方程式为5SO +2MnO-+2H O
2 4 2 4 2
=5SO2-+2Mn2++4H+,该说法正确。D选项:干燥管容积较大,能容纳倒吸的液体,可防止倒吸,该
4
说法正确。
4.【答案】B
【解析】A选项:氨气极易溶于水,使烧瓶内压强迅速减小,外界大气压将水压入烧瓶形成喷泉,
负压吸入是实验成功的关键,该说法正确。B选项:装置②制备Fe(OH) 时,应先打开止水夹,让
2
生成的氢气排出装置内的空气,防止生成的Fe(OH) 被氧化,待空气排尽后再关闭止水夹,使左边
2
试管中液体压入右边,该说法错误。C选项:减压蒸馏可降低混合组分的沸点,实现低温分离,避
免因温度过高导致混合组分分解,该说法正确。D选项:抽滤装置利用装置内外的压强差,加快液
体通过滤纸的速率,从而加快过滤速率,该说法正确。
5.【答案】D
【解析】A选项:丙烯(CH -CH=CH )与HOCl加成时,由于双键两端的氢原子环境不同,产物
3 2
M有两种结构:CH -CH(OH)-CH Cl和CH -CHCl-CH OH,该说法错误。B选项:从转化关系看,
3 2 3 2
Y→P是通过双键打开相互连接形成高分子化合物,属于加聚反应,而非缩聚反应(缩聚反应会有
小分子生成),该说法错误。C选项:产物Z为主产物,说明反应中a处断键概率比b处高,更容
易形成Z的结构,该说法错误。D选项:Y→P是加聚反应,若Y含碳碳双键(C=C),双键由
1个σ键和1个π键组成,反应时π键会断裂,同时原双键碳的σ键会发生断裂与重组以形成高分子
链,因此该过程既有σ键断裂又有π键断裂,D正确。
6.【答案】A
化学参考答案 第1页(共7页)【解析】A选项:O 分子结构呈V形,分子中正负电中心不重合,属于极性分子,该说法正确。B
3
选项:根据反应2O (g)=3O (g)ΔH=-285kJ⋅mol-1,该反应为放热反应,说明O 的能量高于O ,能量
3 2 3 2
越低越稳定,故氧气比臭氧稳定,该说法错误。 C 选项:臭氧中心原子的价层电子对数为
6-2×2
2+ =3,采用sp2杂化,而非sp3杂化,该说法错误。D选项:臭氧中心原子采用sp2杂化,由
2
于孤电子对的斥力大于成键电子对的斥力,键角∠OOO<120°,该说法错误。
7.【答案】C
【解析】A选项:O 具有强氧化性,能破坏微生物的结构,是一种很好的消毒杀菌剂,该说法正
3
确。B选项:在反应I→IV中,NO先参与反应II生成NO ,NO 再参与反应III生成NO,NO的
2 2
质量和化学性质在反应前后不变,是催化剂,该说法正确。C选项:反应IV的ΔH<0,ΔS>0(气
体物质的量增多),根据ΔG=ΔH-TΔS,在任何温度下ΔG<0,反应均能自发进行,该说法错误。
D选项:O 具有强氧化性,能将KI中的I-氧化为I ,I 遇淀粉变蓝色,可用湿润的淀粉碘化钾试
3 2 2
纸检验O 的存在,该说法正确。
3
8.【答案】C
【解析】A选项:黄色溶液C加KSCN溶液呈血红色,说明溶液中含有Fe3+,但Fe3+可能是X中原
本就含有,也可能是X中的Fe2+被氧化生成,无法确定X中一定含有Fe2+,该说法错误。B选项:
4.66g
白色沉淀B加盐酸不溶解,且质量为4.66g,推测B为BaSO ,物质的量为 =0.02mol,则
4 233g/mol
X中含SO2-为0.02mol;红褐色沉淀E为Fe(OH) ,灼烧生成固体F为Fe O ,若F的质量未知,无
4 3 2 3
法确定Fe3+的物质的量,不能确定X的化学式为Fe(HSO ) ,该说法错误。C选项:D(含
4 3
Fe(SCN) )中加NaOH生成Fe(OH) 沉淀,说明OH-与Fe3+的结合能力强于SCN-,该说法正确。
3 3
D选项:胶粒是多个分子的聚集体,2.49gX(若为Fe(HSO ) ,物质的量为0.01mol)溶于水加热生
4 3
成的胶粒个数小于0.01N ,该说法错误。
A
9.【答案】A
【解析】A选项:钛的原子序数为22,价电子排布式为3d24s2,属于第四周期第IVB族,而非第
1
IVA族,该说法错误。B选项:根据均摊法,A型晶胞中Ca2+的个数为1,Ti4+的个数为8× =1,
8
1 1
O2-的个数为12× =3;另一种晶胞中Ca2+的个数为1,Ti4+的个数为1,O2-的个数为6× =3,两种
4 2
钙钛矿的化学式均为CaTiO ,该说法正确。C选项:由晶胞结构可知,Ca2+周围等距离的O2-有12
3
个,故Ca2+的配位数为12,该说法正确。D选项:若“1”号原子为坐标原点,晶胞边长设为1,“2”
1 1
号原子在x=1、y=1、z= 的位置,坐标可为(1,1, ),该说法正确。
2 2
10.【答案】B
【解析】A选项:题目中只给出了387°C时的平衡常数,未给出其他温度下的平衡常数,无法判断
温度对平衡常数的影响,也就不能确定正反应的ΔH符号,该说法错误。B选项:反应2CH OH(g)
3
⇌CH OCH (g)+H O(g)是气体分子数不变的反应,在恒容密闭容器中,总压始终不变,不能作为平
3 3 2
衡标志;即使是恒压容器,因反应前后分子数不变,总压也不会随反应进程变化。因此,“总压不
变” 无法判断反应是否达到平衡,该说法正确。C选项:设387°C时,1L密闭容器中投入0.2mol
CH OH(g),平衡时转化的CH OH的物质的量为2x,则平衡时c(CH OH)=0.2-2x,c(CH OCH )=x,
3 3 3 3 3
x⋅x 2x
c(H O)=x,平衡常数K= =0.160,解得x≈0.044mol,转化率为 ×100%≈44%≠80%,该说
2 (0.2-2x)2 0.2
化学参考答案 第2页(共7页)c(CH OCH )⋅c(H O) 0.2×0.1
法错误。D选项:387°C时,Q= 3 3 2 = =2>0.160,Q>K,反应将向逆反应
c c2(CH OH) 0.12 c
3
方向进行;若Q 0.160,反应向逆反应方向进行;若投入CH OH 0.2mol、
2 c 0.12 3
0.1×0.1
CH OCH 0.1mol和H O0.1mol时,Q = =0.25>0.160,根据平衡移动规律,反应会向逆反应
3 3 2 c 0.22
方向进行,D选项错误。
11.【答案】B
【解析】原子序数依次增大的短周期元素W、X、Y、Z分别属于前三周期,化合物A、B的反应
及离子化合物M的阴离子为48电子微粒,推测W为H,X为C,Y为Na,Z为Cl,A为NH ,
3
B为CO ,M为(NH ) C O 。A选项:NH 分子间可形成氢键,导致其熔沸点较高,易液化,常做
2 4 2 2 4 3
制冷剂,该说法正确。B选项:CO 是大气成分之一,是导致温室效应的因素之一,但不是罪魁祸
2
首,化石燃料的大量燃烧等人类活动是导致温室效应加剧的主要原因,该说法错误。C选项:Y的
单原子离子为Na+,Z的单原子离子为Cl-,电子层数越多,离子半径越大,故离子半径Na+
4 2 3 4
H CO ,该说法正确。
2 3
12.【答案】C
【解析】A选项:根据电池原理,A极上对氯酚(Cl-C H -OH)发生还原反应,为正极;B极上
6 4
CH COO-发生氧化反应,为负极,电子经外电路由负极(B极)向正极(A极)迁移,该说法正
3
确。B选项:A极为正极,对氯酚得到电子生成苯酚和Cl-,电极反应为Cl-C H -OH+2e-+H+→
6 4
C H OH+Cl-,该说法正确。C选项:微生物在100°C以上的高温下会失活,该电池不能在100°C以
6 5
上的高温下进行,该说法错误。D选项:根据得失电子守恒,CH COO-(C为-3价)氧化为CO
3 2
2 1
(C为+4价),每个CH COO-失去8×2=16e-;对氯酚(Cl-C H -OH中C平均价态为- =- 价)
3 6 4 6 3
2 1
还原为苯酚(C H OH中C平均价态为- =- 价,此处可能题目数据有误,若假设对氯酚中C的
6 5 6 3
氧化态变化为+2价到-2价,每个对氯酚得到4e-),则处理的CH COO-与对氯酚的物质的量之比
3
为4:16=1:4,该说法正确(需根据实际化合价变化调整,此处按题目所给比例)。
13.【答案】C
【解析】A选项:CH COOH的K 小于HCOOH,说明CH -的给电子效应使羧基的电离程度减小,
3 a 3
故-CH 为给电子基,该说法错误。B选项:电负性F>Cl,CH FCOOH的K 大于CH ClCOOH,
3 2 a 2
说明F的吸电子能力强于Cl,电负性更大,该说法错误。C选项:F的吸电子能力强于Cl,
CH FCOOH中-CH F的吸电子效应比CH ClCOOH中-CH Cl强,使羧基更容易电离,故K
2 2 2 2 a1
(CH FCOOH)>1.4×10-3,该说法正确。D选项:酸性越强,其对应酸根离子的水解程度越小,水解
2
常数越小。酸性HCOOH>CH COOH,故水解常数K (HCOO-)K ,水解程度大于电离程度,溶液呈碱性,该说法正确。B选项:
h K 1.0×10-7 h a2
a1
c(H+)⋅c(HS-)
饱和H S溶液浓度为0.1mol/L,酸性主要来自第一步电离,设c(H+)=x,则K = ≈
2 a1 c(H S)
2
x2
=1.0×10-7,解得x=10-4mol/L,pH=4,该说法正确。C选项:根据电荷守恒,H S溶液中c(H+)=
0.1 2
化学参考答案 第3页(共7页)c(OH-)+c(HS-)+2c(S2-),该说法正确。D选项:计算反应R2+(aq)+H S(aq)⇌RS(s)+2H+(aq)的平衡常
2
K ⋅K 1.0×10-7×7.1×10-15
数K:对于Fe2+:K= a1 a2 = ≈1.13<10-5,正向反应基本不能进行,不会产生
K (FeS) 6.3×10-18
sp
1.0×10-7×7.1×10-15
FeS沉淀;对于Cu2+:K= ≈1.13×1014>103,正向反应基本完全,会产生CuS沉淀。
6.3×10-36
因此二者不会均出现黑色沉淀,该说法错误。
二、非选择题(共4道题,共58分)
15.(14分)
(1)恒压滴液漏斗(2分);下进上出(2分)
(2)受热均匀,可实现精准控温(2分)
(3)PCl +SO +Cl
△POCl
+SOCl (2分)
3 2 2 3 2
(4)POCl +3H OH PO +3Cl-+3H+(2分)
3 2 3 4
(5)78.8℃(2分)
(6)阻止尾气吸收装置中的水蒸气进入锥形瓶(2分)
【解析】(1)根据装置图,a为添加液体试剂的仪器,名称为分液漏斗;b为冷凝管,冷水进
出方式为下进上出,可保证冷凝管内充满冷水,提高冷凝效率。
(2)油浴加热相比直接加热,热量通过油传递给反应容器,能使三口烧瓶受热均匀,且油的比
热容较大,温度变化缓慢,便于精确控制反应温度。
(3)由实验目的“探究二氯亚砜(SOCl )和三氯氧磷(POCl )联合生产方法”,结合反应物
2 3
(PCl 、SO 、Cl )和产物(POCl 、SOCl ),根据原子守恒配平化学方程式。
3 2 2 3 2
(4)三氯氧磷(POCl )水解生成磷酸(H PO )和盐酸(HCl),盐酸完全电离,故离子方程
3 3 4
式为POCl +3H OH PO +3Cl-+3H+。
3 2 3 4
(5)根据表格数据,PCl 沸点为76°C,SOCl 沸点为78.8°C,POCl 沸点为105.8°C。控制油浴
3 2 3
温度在78.8°C~105.8°C,可使PCl 先挥发除去,同时收集SOCl ,避免POCl 挥发。
3 2 3
(6)SOCl 和POCl 均易水解,干燥管中PO 为酸性干燥剂,可吸收空气中的水蒸气,防止其
2 3 2 5
进入三口烧瓶或冷凝收集装置,导致产物水解。
16.(15分)
(1)Ag++e−Ag(2分)
(2)减小(1分);阳极参与失电子的金属除了银还有比银活泼的金属,例如Zn,但阴极得电子
的却只有Ag+,因此阴极析出的银多于阳极溶解的银,不足部分由电解质溶液AgNO 提供,所以
3
AgNO 浓度减小(3分)
3
(3)4.0×10−20mol•L−1(2分)
(4)1∶1(2分)
(5)用一支洁净的小试管,取最后清洗液1~2mL,向其中滴加过量的稀硝酸酸化,之后滴加
几滴AgNO 溶液,若出现白色沉淀,说明没有洗干净,反之则洗干净了(3分)
3
(6)(NH )PdCl+2HCOOHPd+2CO ↑+2NH++6Cl−+4H+(2分)
4 2 6 2 4
【解析】(1)精炼银时,纯银棒为阴极,阴极发生还原反应,Ag+得到电子生成Ag,电极反
应方程式为Ag++e-=Ag。
(2)阳极材料为粗银棒,其中含Zn、Cu等活泼杂质,电解时Zn、Cu比Ag更容易失去电子
(还原性:Zn>Cu>Ag),故阳极反应为Zn-2e-=Zn2+、Cu-2e-=Cu2+、Ag-2e-=Ag+;阴极只有Ag+放
电析出Ag。由于阳极溶解的Ag的量小于阴极析出的Ag的量,电解液中AgNO 溶液的浓度将减
3
化学参考答案 第4页(共7页)小。
(3)当c(Ni2+)=2×10-3mol/L时,根据K [Ni(OH) ]=c(Ni2+)⋅c2(OH-)=2.0×10-15,可得c(OH-)
sp 2
=
K
sp
[Ni(OH)
2
]
=
2.0×10-15
=10-6mol/L。
c(Ni2+) 2×10-3
此时溶液中c(Fe3+)=
K
sp
[Fe(OH)
3
]
=
4.0×10-38
=4.0×10-20mol/L。
c3(OH-) (10-6)3
(4)“氧化”过程中,推测Pd的低价态化合物(如PdO或Pd(OH) )被H O 氧化为高价态
2 2 2
(如Pd4+),H O 作为氧化剂,还原产物为H O(O从-1价变为-2价,每个H O 得到2e-);Pd
2 2 2 2 2
元素从+2价变为+4价,每个Pd失去2e-。根据得失电子守恒,氧化剂(H O )与还原剂(含Pd2+
2 2
的物质)的物质的量之比为1:1。
(5)“沉淀”过程中加入NH Cl,滤渣为(NH ) PdCl ,表面可能附着Cl-。检验Cl-即可判断滤渣
4 4 2 6
是否清洗干净,方法为:取最后一次洗涤液,用稀硝酸酸化(排除OH-等干扰),再滴加AgNO
3
溶液,若无白色沉淀(AgCl),则清洗干净。
(6)“还原”步骤中,HCOOH作为还原剂,还原(NH ) PdCl 中的Pd4+为Pd单质(Pd从+4价
4 2 6
变为0价,得到4e-);HCOOH中C从+2价变为CO 中的+4价,失去2e-。根据得失电子守恒、
2
电荷守恒和原子守恒,配平离子反应方程式。
17.(14分)
(1)613.7(2分)
(2)-2058.3(2分)
(3)①反应Ⅰ正向为气相系数和增大的反应,恒压通非反应气体水蒸气相当于增大体积减小反
应物的分压,推动平衡右移,提高反应物的转化率(2分)
②5kPa(2分)
③升温(合理即给分,2分)
(4)60%(2分)
(5)CD(2分)
【解析】(1)反应热ΔH=反应物总键能-生成物总键能。反应I:C H (g)⇌C H (g)+H (g)
3 8 3 6 2
ΔH =+124.3kJ/mol。
1
C H (丙烷)结构为CH -CH -CH ,含2个C-C键和8个C-H键;C H (丙烯)结构为CH -
3 8 3 2 3 3 6 3
CH=CH ,含1个C-C键、1个C=C键和6个C-H键;H 含1个H-H键。
2 2
则ΔH =[2×348+8×413]-[348+a+6×413+436]=+124.3,代入数据计算:
1
[696+3304]-[348+a+2478+436]=124.3
4000-(3262+a)=124.3
解得a=613.7。
(2)燃烧热是1mol纯物质完全燃烧生成稳定氧化物(C→CO 、H→H O(l))放出的热量。
2 2
已知:①C H (g)+5O (g)=3CO (g)+4H O(l)ΔH =-2220kJ/mol
3 8 2 2 2 1
1
②H (g)+ O (g)=H O(l)ΔH =-286kJ/mol
2 2 2 2 2
③C H (g)⇌C H (g)+H (g)ΔH =+124.3kJ/mol
3 8 3 6 2 3
9
根据盖斯定律,①-②-③可得C H (g)+ O (g)=3CO (g)+3H O(l),则ΔH=ΔH -ΔH -ΔH =
3 6 2 2 2 2 1 2 3
-2220-(-286)-124.3=-2058.3kJ/mol。
(3)反应I是气体分子数增多的反应,恒压下通入水蒸气(非反应气体),相当于扩大容器体
化学参考答案 第5页(共7页)积,降低丙烷、丙烯、氢气的浓度,根据勒夏特列原理,平衡向正反应方向移动,从而提高丙烷的
平衡转化率。
n(水) 1
②A点M= =15,n(水)=1mol,则初始n(丙烷)= mol,设丙烷的平衡转化率为0.5,则
n(丙烷) 15
平衡时:
1 1 1 1
n(C H )= ×(1-0.5)= mol,n(C H )=n(H )= ×0.5= mol,n(水)=1mol。
3 8 15 30 3 6 2 15 30
1 1 1 32
总物质的量n = + + +1= mol。
总 30 30 30 30
1
各物质的分压:p(C H )=p(C H )=p(H )= 30 ×115kPa= 115 kPa,p(水)= 1 ×115kPa= 3450 kPa。
3 8 3 6 2 32 32 32 32
30 30
K = p(C 3 H 6 )⋅p(H 2 ) =
1
3
1
2
5×1
3
1
2
5
= 115 ≈3.6kPa(此处需结合题目图表数据修正,若A点转化率为
p p(C H ) 115 32
3 8
32
0.5,计算结果可能为15kPa,需根据实际平衡分压重新核对,核心思路为分压=物质的量分数×总
压,再代入平衡常数表达式)。
③反应I为吸热反应(ΔH >0),升高温度平衡向正反应方向移动;反应I是气体分子数增多的
1
反应,减小压强平衡向正反应方向移动;及时分离出产物(丙烯或氢气),降低产物浓度,平衡也
向正反应方向移动,均可提高丙烷的转化率。
(4)设平衡时反应I中转化的C H 为xmol,反应II中转化的H 为ymol。
3 8 2
反应I:C H (g)⇌C H (g)+H (g),平衡时:n(C H )=1-x,n(C H )=x,n(H )=x-y。
3 8 3 6 2 3 8 3 6 2
反应II:CO (g)+H (g)⇌CO(g)+H O(g),已知n(CO)=0.5mol,则y=0.5mol,平衡时:n(CO )
2 2 2 2
=1-y=0.5mol,n(H O)=0.5mol。
2
c(CO)⋅c(H O) 0.5×0.5
反应II的平衡常数K = 2 = =5,解得x=0.60mol。
2 c(CO )⋅c(H ) 0.5×(x-0.5)
2 2
0.60
丙烷的平衡转化率= ×100%=60%。
1
(5)A选项:CO 在反应中参与反应生成CO,是反应物,不是催化剂(催化剂在反应前后质
2
量和化学性质不变),该说法错误。
B选项:催化过程中,Mo中心原子会参与化学键的形成与断裂,化合价会发生变化,该说法
错误。
C选项:丙烷(CH CH CH )吸附和氧化脱氢时,C-C非极性键、C-H极性键断裂;生成H
3 2 3 2
时,形成H-H非极性键,该说法正确。
D选项:含碳化合物中,CH CH CH (C为sp3杂化)、CH CH=CH (双键C为sp2杂化)、
3 2 3 3 2
CO (C为sp杂化)、CO(C为sp杂化),碳原子的杂化方式有sp、sp2、sp3三种,该说法正确。
2
18.(15分)
(1)酮羰基(2分)
(2) (2分)
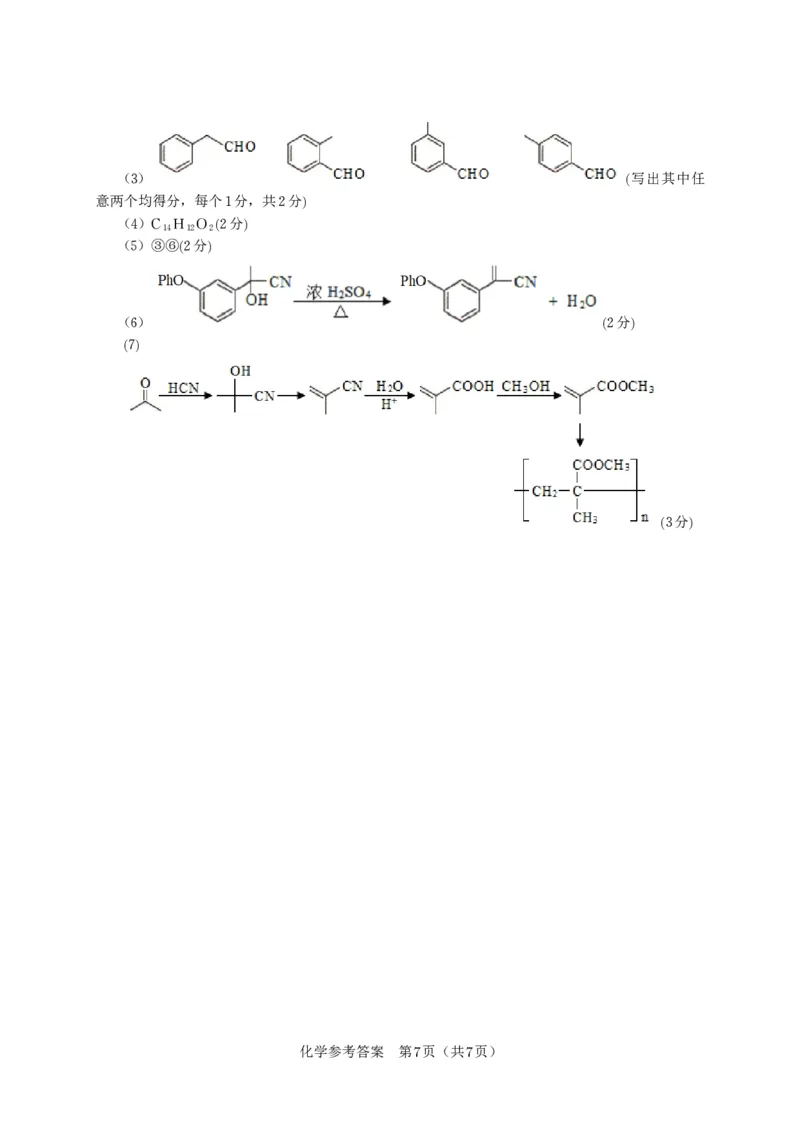
化学参考答案 第6页(共7页)(3) (写出其中任
意两个均得分,每个1分,共2分)
(4)C H O (2分)
14 12 2
(5)③⑥(2分)
(6) (2分)
(7)
(3分)
化学参考答案 第7页(共7页)