文档内容
浙江强基联盟 2025 年 8 月高三联考
化学 试题
浙江强基联盟研究院 命制
考生注意:
1. 本试卷满分 100 分, 考试时间 90 分钟。
2. 考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2 B 铅笔把答题卡上对应
题目的答案标号涂黑;非选择题请用直径 0.5 毫米黑色墨水签字笔在答题卡上各题的答题区域
内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量: H1C12N14O16
一、选择题 (本大题共 16 小题, 每小题 3 分, 共 48 分。每小题列出的四个备选项中只有一个
是 符合题目要求的,不选、多选、错选均不得分)
1. 嫦娥五号返回器带回的月壤中含有 FeTiO ,下列关于 FeTiO 的说法正确的是
3 3
A. 酸 B. 碱 C. 盐 D. 氧化物
2. 下列化学用语表示正确的是
❑
18O
A. 中子数为 10 的氧原子: 10 B. 的名称:2-甲基-3-乙基戊烷
C. BF 的价层电子对互斥 (VSEPR) 模型:
3
Cr
D. 基态 原子的价层电子轨道表示式:
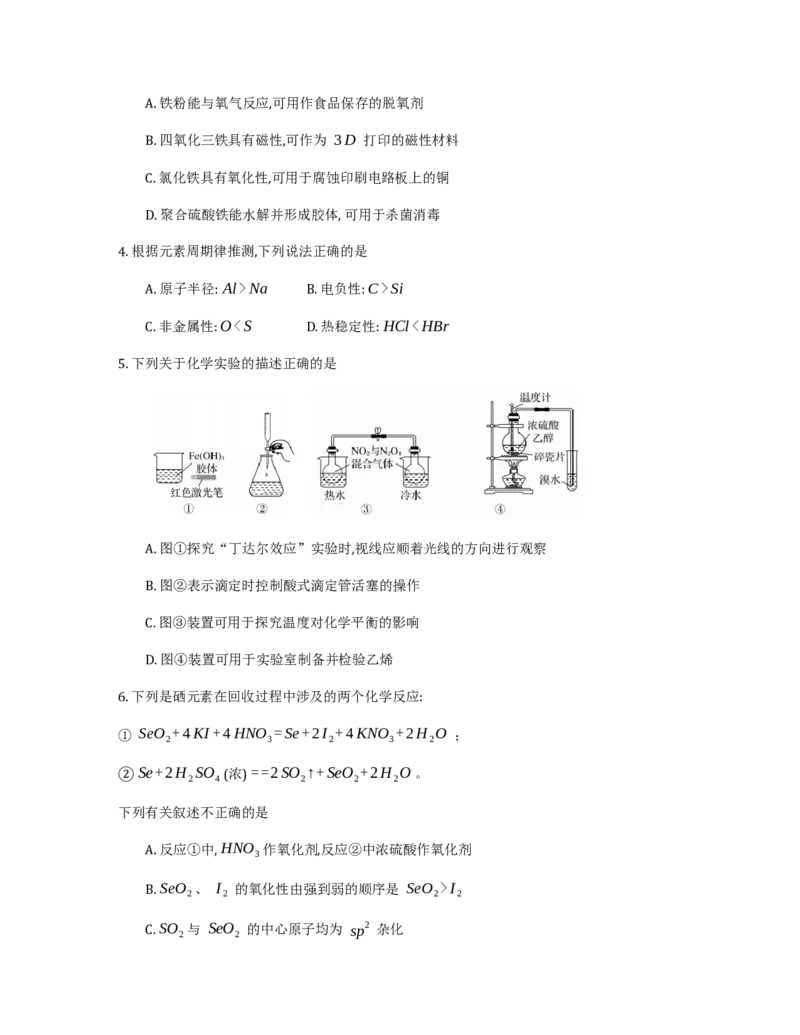
3. 下列有关铁及其化合物的性质与用途不具有对应关系的是A. 铁粉能与氧气反应,可用作食品保存的脱氧剂
B. 四氧化三铁具有磁性,可作为 3D 打印的磁性材料
C. 氯化铁具有氧化性,可用于腐蚀印刷电路板上的铜
D. 聚合硫酸铁能水解并形成胶体, 可用于杀菌消毒
4. 根据元素周期律推测,下列说法正确的是
A. 原子半径: Al>Na B. 电负性: C>Si
C. 非金属性: OI
2 2 2 2
C. SO 与 SeO 的中心原子均为 sp2 杂化
2 2D. 反应①中每生成 0.8molI ,转移电子数为 1.6N
2 A
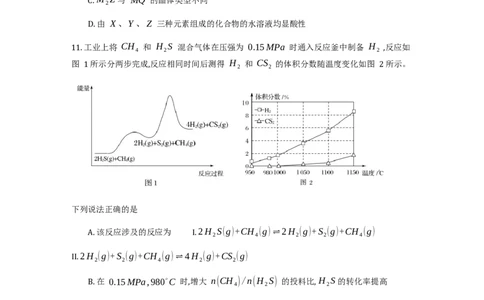
7. 下列有关物质性质的解释不正确的是
性质 解释
A 酸性: CF COOH>CH COOH — CF 是吸电子基团 −CH 是推电子基团
3 3 3 3
B 沸点: 邻羟基苯甲酸 对羟基苯甲 前者在分子内形成了氢键,后者在分子间 形成了氢
酸 键
C 熔点: Fe>Na Fe 的金属键比 Na 强
第一电离能: N>O N 的非金属性强于 O
D
8. 下列离子方程式不正确的是
A. 过氧化钠可用于制备氧气: 2Na O +2H O=4Na++4OH−+O ↑
2 2 2 2
△
B. 尿素溶于热水转化为氨态氮肥: CO(NH ) +2H O=2NH++CO2−
2 2 2 4 3
C. 饱和 Na CO 溶液处理水垢中的硫酸钙:
2 3
CaSO (s)+CO2−(aq)⇌CaCO (s)+SO2−(aq)
4 3 3 4
D. 用 Na S O 溶液清除水中余氯 (Cl ):S O2−+4Cl +5H O=2SO2−+8Cl−+10H+
2 2 3 2 2 3 2 2 4
9. 有机物 X→Y 的异构化反应如图所示,下列说法不正确的是
A. X 、 Y 中存在的官能团不完全相同
B. X 和 Y 中所有碳原子可能共平面
C. X 和 Y 互为对映异构体
D. 类比上述反应, 的异构化产物可能为10.X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。 X 的核外电子数等于其周期数,
YX 分子呈三角锥形, Z 的核外电子数等于 X 、 Y 核外电子数之和。 M 与 X 同主族, Q
3
是同周期中非金属性最强的元素。下列说法正确的是
A. X 与 Z 形成的 10 电子微粒有 2 种
B. Z 与 Q 形成的一种化合物可用于饮用水的消毒
C. M Z 与 MQ 的晶体类型不同
2
D. 由 X、Y、Z 三种元素组成的化合物的水溶液均显酸性
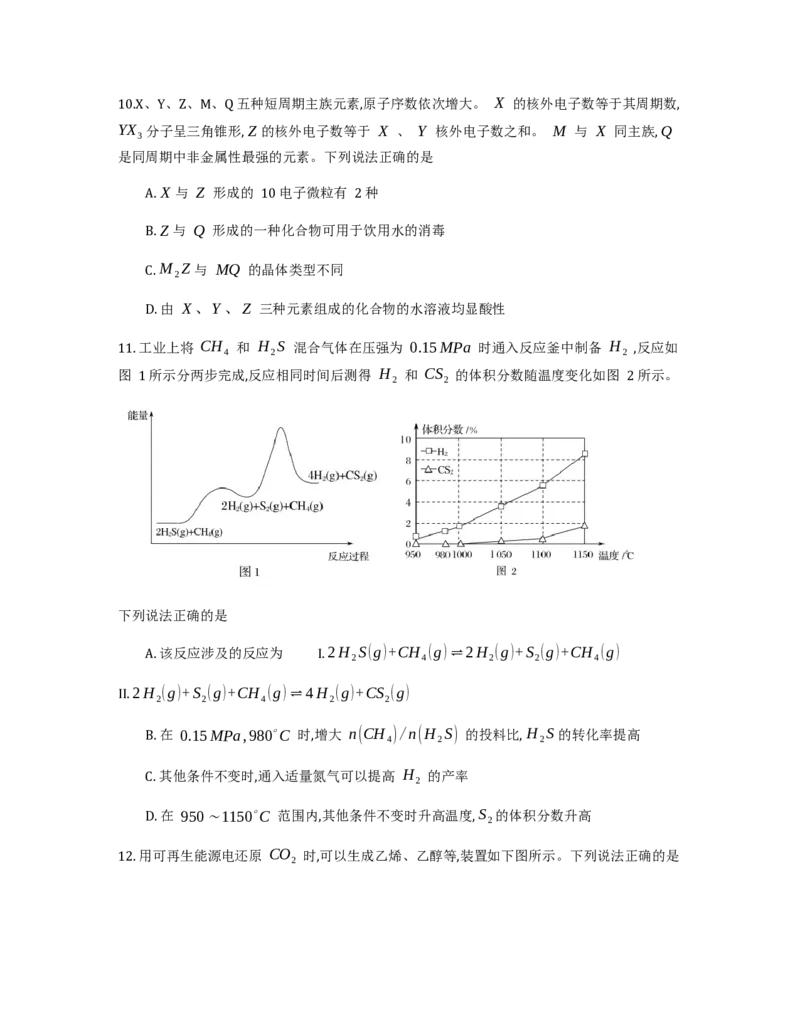
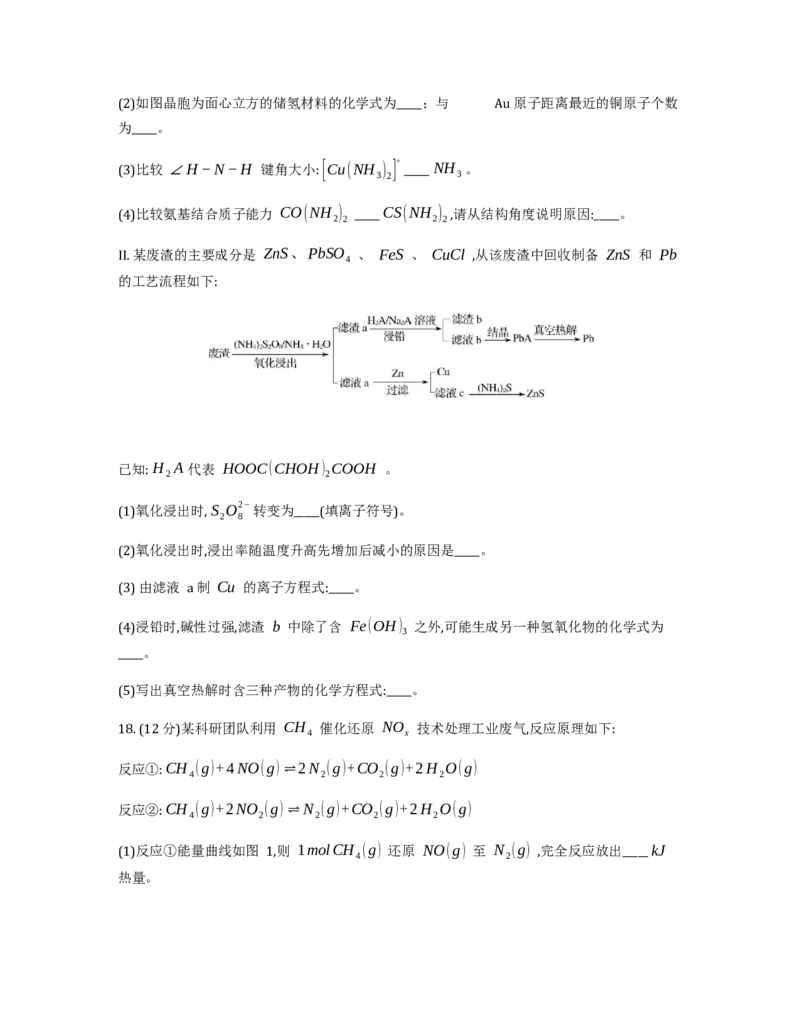
11. 工业上将 CH 和 H S 混合气体在压强为 0.15MPa 时通入反应釜中制备 H ,反应如
4 2 2
图 1 所示分两步完成,反应相同时间后测得 H 和 CS 的体积分数随温度变化如图 2 所示。
2 2
下列说法正确的是
A. 该反应涉及的反应为 I. 2H S(g)+CH (g)⇌2H (g)+S (g)+CH (g)
2 4 2 2 4
II. 2H (g)+S (g)+CH (g)⇌4H (g)+CS (g)
2 2 4 2 2
B. 在 0.15MPa,980∘C 时,增大 n(CH )/n(H S) 的投料比, H S 的转化率提高
4 2 2
C. 其他条件不变时,通入适量氮气可以提高 H 的产率
2
D. 在 950∼1150∘C 范围内,其他条件不变时升高温度, S 的体积分数升高
2
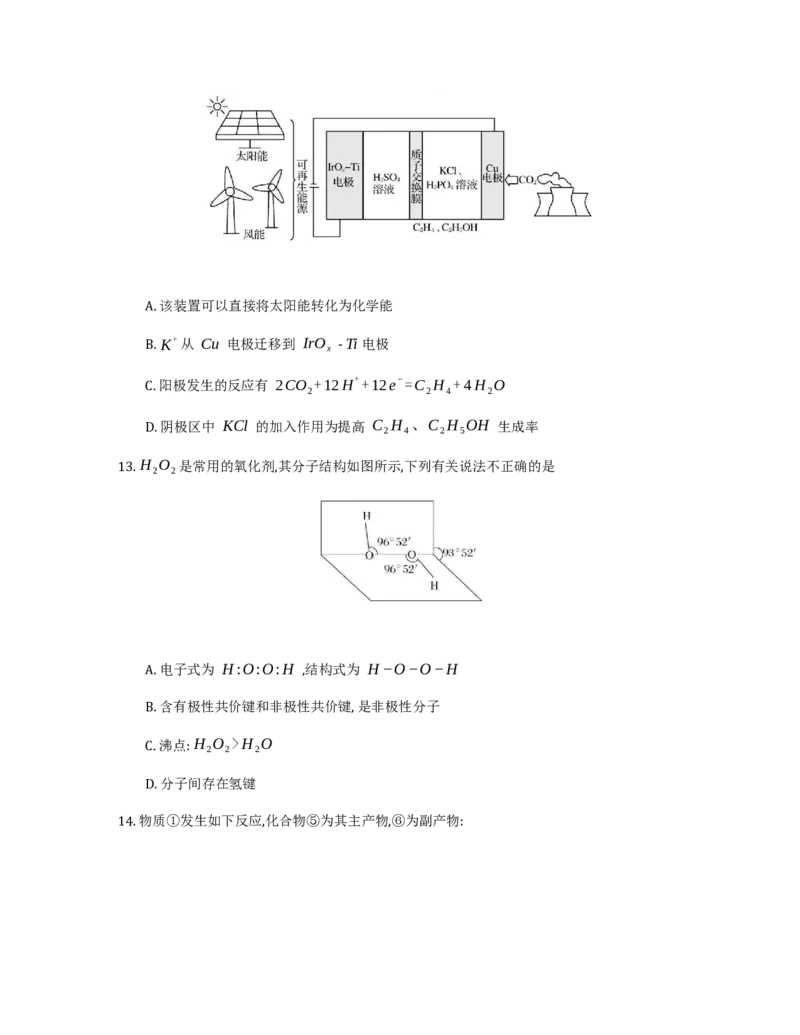
12. 用可再生能源电还原 CO 时,可以生成乙烯、乙醇等,装置如下图所示。下列说法正确的是
2A. 该装置可以直接将太阳能转化为化学能
B. K+ 从 Cu 电极迁移到 IrO - Ti 电极
x
C. 阳极发生的反应有 2CO +12H++12e−=C H +4H O
2 2 4 2
D. 阴极区中 KCl 的加入作用为提高 C H 、C H OH 生成率
2 4 2 5
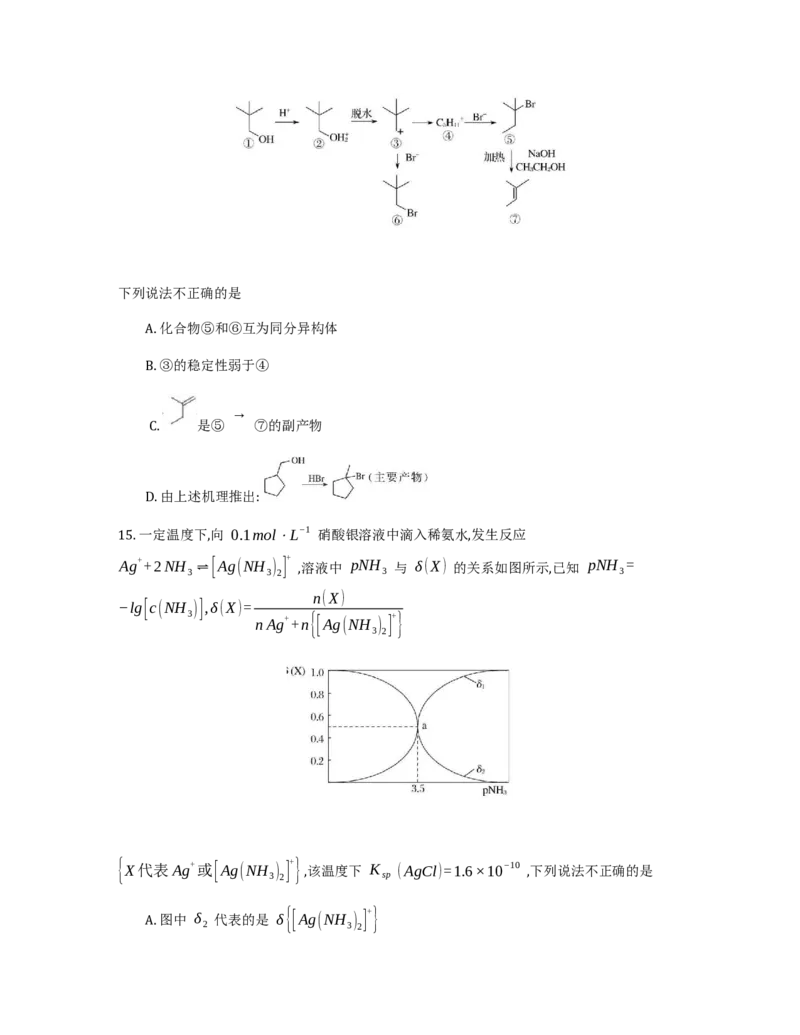
13. H O 是常用的氧化剂,其分子结构如图所示,下列有关说法不正确的是
2 2
A. 电子式为 H:O:O:H ,结构式为 H−O−O−H
B. 含有极性共价键和非极性共价键, 是非极性分子
C. 沸点: H O >H O
2 2 2
D. 分子间存在氢键
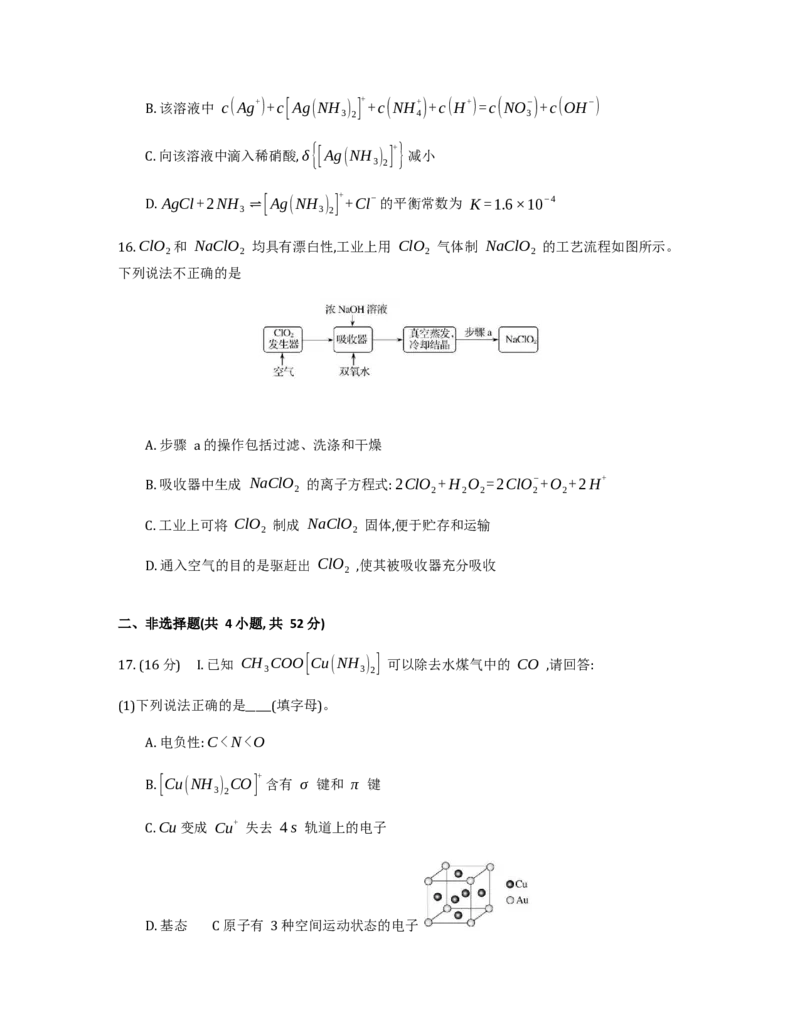
14. 物质①发生如下反应,化合物⑤为其主产物,⑥为副产物:下列说法不正确的是
A. 化合物⑤和⑥互为同分异构体
B. ③的稳定性弱于④
→
C. 是⑤ ⑦的副产物
D. 由上述机理推出:
15. 一定温度下,向 0.1mol⋅L−1 硝酸银溶液中滴入稀氨水,发生反应
Ag++2NH 3 ⇌ [Ag(NH 3 ) 2 ] + ,溶液中 pNH 3 与 δ(X) 的关系如图所示,已知 pNH 3 =
n(X)
−lg[c(NH )],δ(X)=
3 nAg++n{[Ag(NH ) ] +}
3 2
{X代表Ag+或[Ag(NH ) ] +} ,该温度下 K (AgCl)=1.6×10−10 ,下列说法不正确的是
3 2 sp
A. 图中 δ 代表的是 δ{[Ag(NH ) ] +}
2 3 2B. 该溶液中 c(Ag+)+c[Ag(NH ) ] + +c(NH+)+c(H+)=c(NO−)+c(OH−)
3 2 4 3
C. 向该溶液中滴入稀硝酸, δ{[Ag(NH ) ] +} 减小
3 2
D. AgCl+2NH ⇌ [Ag(NH ) ] + +Cl− 的平衡常数为 K=1.6×10−4
3 3 2
16. ClO 和 NaClO 均具有漂白性,工业上用 ClO 气体制 NaClO 的工艺流程如图所示。
2 2 2 2
下列说法不正确的是
A. 步骤 a 的操作包括过滤、洗涤和干燥
B. 吸收器中生成 NaClO 的离子方程式: 2ClO +H O =2ClO−+O +2H+
2 2 2 2 2 2
C. 工业上可将 ClO 制成 NaClO 固体,便于贮存和运输
2 2
D. 通入空气的目的是驱赶出 ClO ,使其被吸收器充分吸收
2
二、非选择题(共 4 小题, 共 52 分)
17. (16 分) I. 已知 CH COO[Cu(NH ) ] 可以除去水煤气中的 CO ,请回答:
3 3 2
(1)下列说法正确的是_____(填字母)。
A. 电负性: C”“<”或“=”), b 点与 c 点相比,_____点
1 2 1 2
(填“b”或“c”) 反应速率更快,理由是_____。
② T 温度下, 10∼20min 内的平均反应速率 v(H O)= _____, CH 的平衡转化率为_____。
1 2 4
(4)利用某分子筛作催化剂, NH 也可脱除废气中的 NO 和 NO ,生成两种无毒物质。其反应
3 2
历程如图 3 所示,上述历程的总反应为_____。
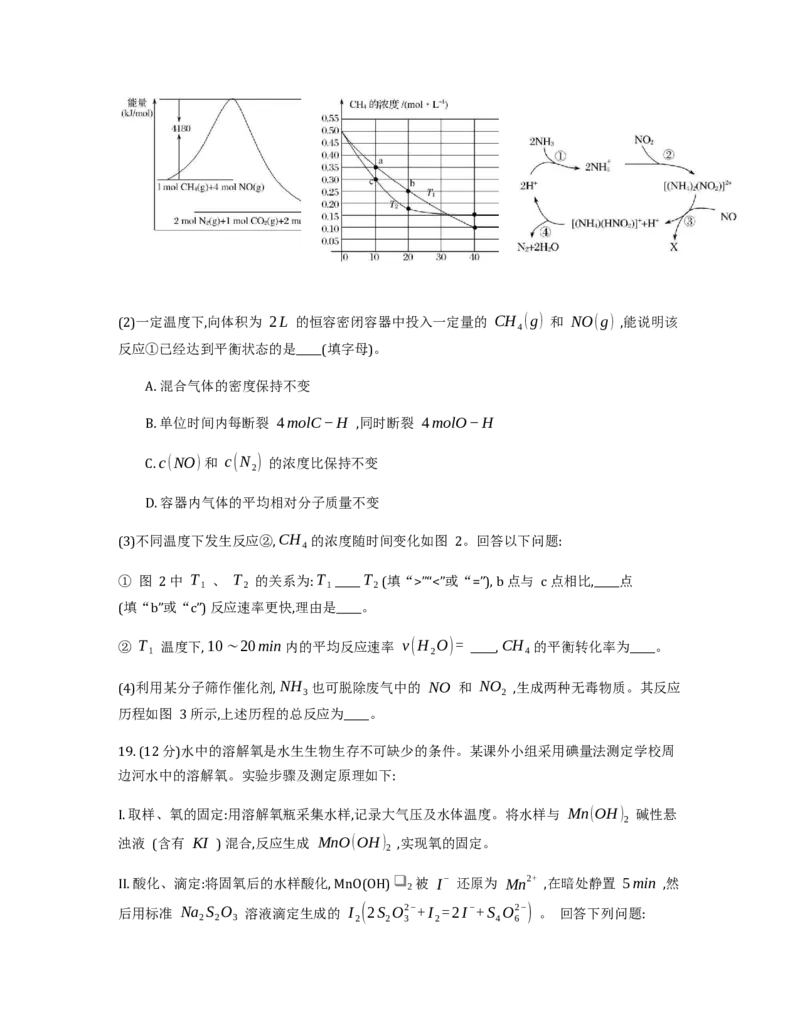
19. (12分)水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周
边河水中的溶解氧。实验步骤及测定原理如下:
I. 取样、氧的固定:用溶解氧瓶采集水样,记录大气压及水体温度。将水样与 Mn(OH) 碱性悬
2
浊液 (含有 KI ) 混合,反应生成 MnO(OH) ,实现氧的固定。
2
II. 酸化、滴定:将固氧后的水样酸化, MnO(OH) ❑ 被 I− 还原为 Mn2+ ,在暗处静置 5min ,然
2
后用标准 Na S O 溶液滴定生成的 I (2S O2−+I =2I−+S O2−) 。 回答下列问题:
2 2 3 2 2 3 2 4 6(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____。
( 2 )“氧的固定”中发生反应的化学方程式为_____。
(3) Na S O 溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试
2 2 3
剂瓶和_____;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除_____及二氧化碳。
(4)取 100.00mL 水样经固氧、酸化后,用 amol⋅L−1Na S O 溶液滴定,以淀粉溶液作指示
2 2 3
剂,终点现象为_____;若消耗 Na S O 溶液的体积为 bmL ,则水样中溶解氧的含量为_____
2 2 3
mg⋅L−1 。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测量结果偏_____。(填“高” 或“低”)
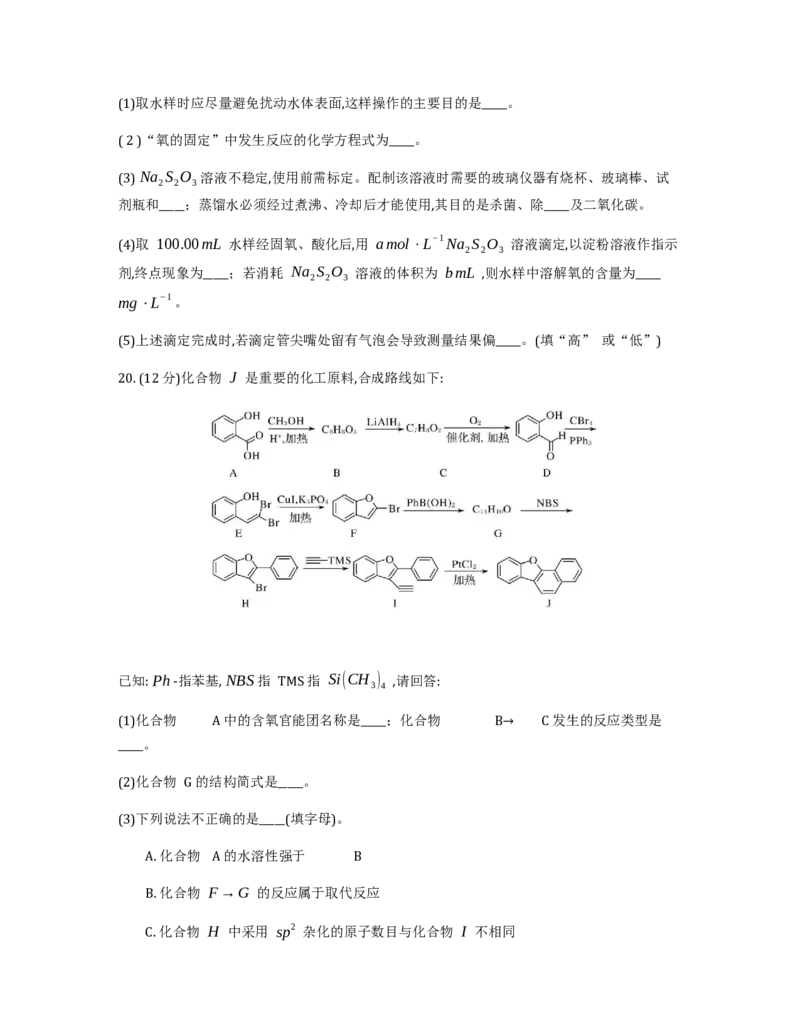
20. (12分)化合物 J 是重要的化工原料,合成路线如下:
已知: Ph -指苯基, NBS 指 TMS 指 Si(CH ) ,请回答:
3 4
(1)化合物 A 中的含氧官能团名称是_____;化合物 B→ C 发生的反应类型是
_____。
(2)化合物 G 的结构简式是_____。
(3)下列说法不正确的是_____(填字母)。
A. 化合物 A 的水溶性强于 B
B. 化合物 F→G 的反应属于取代反应
C. 化合物 H 中采用 sp2 杂化的原子数目与化合物 I 不相同D. 化合物 J 的分子式是 C H O
16 11
(4)化合物 C→D 反应的化学方程式是_____。
(5)I →J 的反应中,若参与成键的苯环及苯环的反应位置不变,则生成与 J 互为同分异构体的副
产物的结构简式为_____。
(6)参考上述路线,以 NBS 、 PhB(OH) 、乙醇、 Bi . Br 为有机原料,设计化合物_____的合
2
成路线_____
_____(用流程图表示,无机试剂任选)