文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修一第一章+第二章第一节(人教版)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23
第Ⅰ卷(选择题 共 45 分)
一、选择题:本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列关于反应热和焓变的理解正确的是
A.任何条件下,化学反应的焓变都等于反应热
B.放热反应的ΔH>0,吸热反应的ΔH<0
C.所有化学反应的反应热都可以通过实验直接测量
D.反应产物的总焓大于反应物的总焓时,ΔH>0
2.某学生用如图所示装置进行化学反应 X+2Y=2Z 能量变化情况的研究。当往试管中滴加试剂 Y 时,看
到试管中甲处液面下降,乙处液面上升。关于该反应的下列叙述正确的是
①该反应为放热反应
②反应产物的总能量比反应物的总能量高
/③该反应过程可以看成是“贮存”于 X、Y 内部的能量转化为热量而释放出来
A.①②③ B.①③
C.①② D.③
3.一定温度下,密闭容器中发生反应 ,A 的初始浓度为 ,10s 后,
A 的浓度降到 。下列说法正确的是
A.
B.
C. 由 继续降到 所需时间大于 10s
D.缩小容器的容积,反应速率减小
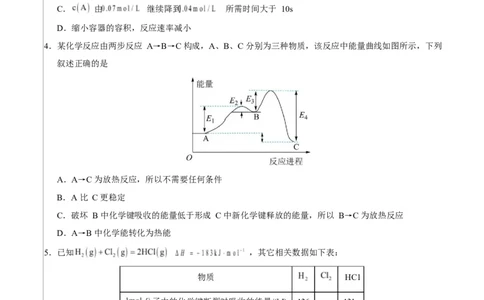
4.某化学反应由两步反应 A→B→C 构成,A、B、C 分别为三种物质,该反应中能量曲线如图所示,下列
叙述正确的是
A.A→C 为放热反应,所以不需要任何条件
B.A 比 C 更稳定
C.破坏 B 中化学键吸收的能量低于形成 C 中新化学键释放的能量,所以 B→C 为放热反应
D.A→B 中化学能转化为热能
5.已知 ,其它相关数据如下表:
物质 HC1
分子中的化学键断裂时吸收的能量/(kJ) 436 a 431
下列说法正确的是
A.
B. 和 的总能量大于 的能量
C. 完全反应放出 热量
D.生成 的能量变化小于
6.关于下列说法,正确的是
/A.恒压容器中发生反应 ,若平衡后在容器中充入 He,则正、逆反应的速
率均不变
B.当一定量的锌粉和过量的 盐酸反应时,为了减慢反应速率,又不影响产生 的总量,可向
反应器中加入一些水、 溶液
C.探究温度对硫代硫酸钠与硫酸反应速率的影响时,应先将两种溶液水浴加热至设定温度,再进行混
合并计时
D.浓度、温度可以改变反应速率,本质原因是可以提高活化分子百分数
7.已知下列反应的热化学方程式:
① 6C(s)+5H(g)+3N(g)+9O(g)=2C H(ONO)(l) H
2 2 2 3 5 2 3 1
② 2H (g)+ O(g)= 2H O(g) H
2 2 2 2
③ C(s)+ O(g)=CO (g) H
2 2 3
则反应 4C H(ONO)(l)=12CO (g)+10HO(g)+O(g)+6N(g)的 H 为
3 5 2 3 2 2 2 2
A.12 H+5 H-2 H B.2 H-5 H-12 H
3 2 1 1 2 3
C.12 H-5 H-2 H D. H-5 H-12 H
3 2 1 1 2 3
8. 和 在催化剂表面合成氨的微观历程示意图如下,已知 属于放热反应。下列说
法不正确的是
A.③→④是吸热过程
B.②→③过程中断裂了非极性共价键
C.合成氨反应中,反应物总能量大于生成物总能量
D.合成氨反应中,反应物断键吸收的能量小于生成物成键释放的能量
9.已知 乙烯与足量氢气发生加成反应放出热量 ,已知键能 、
。 键的键能与 键的键能相差约
A. B. C. D.
10.化学反应中不仅伴随着物质的变化还伴随能量的变化,下列说法正确的是
A.已知 ,则单斜硫比正交硫稳定
B.常温常压下,1mol 完全燃烧比 完全燃烧时的焓变小
C.同温同压下, 在光照和点燃条件下的焓变不同
D.已知: ,则 和 反应:
/11.根据能量变化示意图,下列说法不正确的是
A.相同质量的 NO (g)和 NO(g),前者具有的能量较高
2 2 4
B.ΔH=ΔH +ΔH+ΔH+ΔH
5 1 2 3 4
C.2HO(l)=2H(g)+O(g) ΔH=-ΔH >0
2 2 2 6 5
D.NH(l)+NO (g)= N(g)+2HO(l) ΔH,则ΔH>ΔH
2 4 2 2 2 4
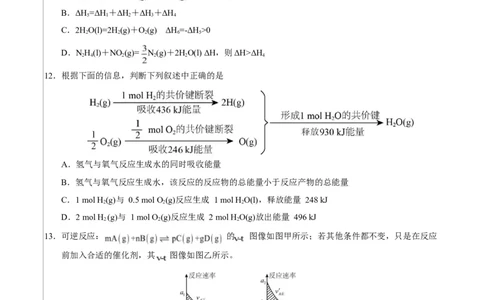
12.根据下面的信息,判断下列叙述中正确的是
A.氢气与氧气反应生成水的同时吸收能量
B.氢气与氧气反应生成水,该反应的反应物的总能量小于反应产物的总能量
C.1 mol H (g)与 0.5 mol O(g)反应生成 1 mol H O(l),释放能量 248 kJ
2 2 2
D.2 mol H (g)与 1 mol O (g)反应生成 2 mol H O(g)放出能量 496 kJ
2 2 2
13.可逆反应: 的 图像如图甲所示;若其他条件都不变,只是在反应
前加入合适的催化剂,其 图像如图乙所示。
① ;② ;③ ;④ ;⑤ ;⑥ ;⑦图甲与图乙中阴影部分的面积相等;⑧
图乙中阴影部分面积更大。
以上所述正确的组合为
A.②④⑤⑦ B.②④⑥⑧ C.②③⑤⑦ D.①④⑤⑧
/14.基于非金属原子嵌入石墨烯三嗪基 C N 中,用于催化一氧化碳加氢生成甲醇的反应历程如图,其中
3 4
吸附在催化剂表面上的物种用“*”标注,下列说法中错误的是
A.过渡态相对能量:TS55>TS44>TS77
B.整个反应历程中有极性键的断裂和生成
C.反应决速步的活化能为 0.95eV
D.物种吸附在催化剂表面的过程为吸热过程
15.用纯净的 CaCO 固体与 100mL 稀盐酸反应制取 CO,反应过程中溶液体积变化忽略不计,实验过程
3 2
中 CO 的体积变化如图所示(CO 的体积已折算为标准状况下的体积)。下列分析正确的是
2 2
A.0E 段表示的平均反应速率最大
B.EF 段,用 HCl 表示该反应的平均反应速率为 0.04mol·L-1·min-1
C.0E、EF、FG 三段中,该反应用 CO 表示的平均反应速率之比为
2
D.0~3min 内,该反应的平均反应速率为 v(HCl)=0.23mol·L-1·min-1
第 II 卷(非选择题 共 55 分)
二、填空题(共 4 小题,共 55 分)
16.(13 分)结合题干信息,利用已有的热化学知识完成下列问题。
Ⅰ.氧化亚铜常用于制船底防污漆。用 与 高温烧结可制取 。
/已知一定温度下:
①
②
③
(1)在该温度下反应①属于 反应(填“吸热”或“放热”)。
(2)在该温度下反应③的 。
Ⅱ.已知 、 时,部分物质的摩尔燃烧焓为:
化学式
-283.0 -285.8 -726.51 -890.31
(3)根据盖斯定律完成下列反应的热化学方程式: 。
(4)现有 和 的混合气体 (标准状况),使其完全燃烧生成 和 ,共放出热量
,则原混合气体中 和 的物质的量之比是_____(填标号)。
A. B. C. D.
Ⅲ.室温下,用 盐酸与 溶液在如图所示装置中进行中和反应。
(5)仪器 a 的名称为 ;实验中,所用 NaOH 稍过量的原因是 。
(6)该实验小组做了三次实验,每次取盐酸和 溶液各 ,实验数据如表所示:
起始温度
实验序 终止温度
溶
号
盐酸
平均值
液
1 25.1 24.9 25.0 28.3
2 25.1 28.1 25.1 30.5
/3 25.1 25.1 25.1 28.6
已知盐酸、 溶液密度均近似为 ,中和后混合液的比热容 ),则该
反应的中和热 (保留到小数点后 1 位)。
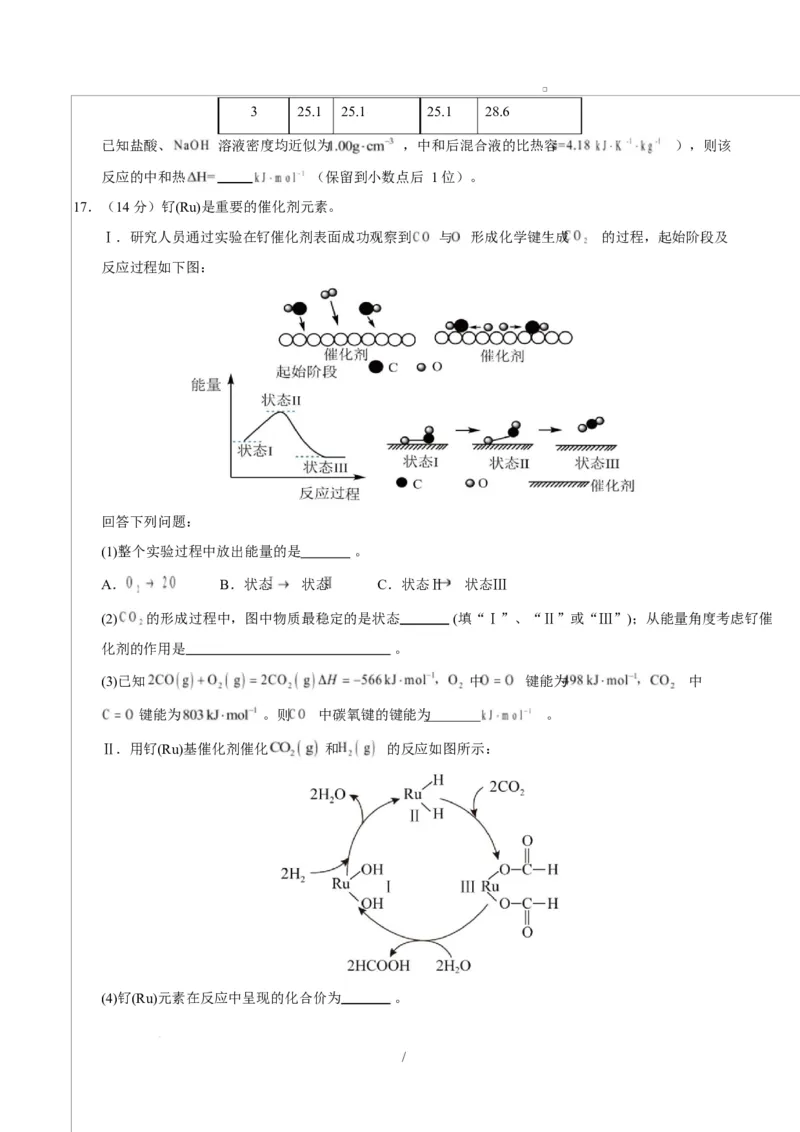
17.(14 分)钌(Ru)是重要的催化剂元素。
Ⅰ.研究人员通过实验在钌催化剂表面成功观察到 与 形成化学键生成 的过程,起始阶段及
反应过程如下图:
回答下列问题:
(1)整个实验过程中放出能量的是 。
A. B.状态 状态 C.状态Ⅱ 状态Ⅲ
(2) 的形成过程中,图中物质最稳定的是状态 (填“Ⅰ”、“Ⅱ”或“Ⅲ”);从能量角度考虑钌催
化剂的作用是 。
(3)已知 中 键能为 中
键能为 。则 中碳氧键的键能为 。
Ⅱ.用钌(Ru)基催化剂催化 和 的反应如图所示:
(4)钌(Ru)元素在反应中呈现的化合价为 。
/(5)图示中物质 (填化学式或结构简式)为该反应的中间产物。
(6)反应生成 液态 时放出 的热量,此时转移 电子,该反应的热化学方
程式为 。
18.(14 分)某研究小组利用 溶液和酸性 溶液的反应来探究外界条件改变对化学反应速率
的影响,实验如下:
参加反应的物质
溶液颜色褪至无
实验序 实验温
溶液(含硫酸) 溶液
号 度/K 色时所需时间/
s
V/mL V/mL V/mL
① 290 2 0.02 4 0.1 0 6
② 2 0.02 3 0.1 8
③ 315 2 0.02 0.1 1
回答下列问题:
(1)通过实验①②,可探究 的改变对反应速率的影响,其中 。
(2)通过实验 (填实验序号)可探究温度变化对反应速率的影响,由实验②中数据可知
(结果保留两位小数)。
(3)实验过程中发现,反应开始一段时间溶液褪色不明显,不久后迅速褪色。甲同学认为是反应放热导
致溶液温度升高所致,重做实验②,测得反应过程中不同时间的温度如下:
时间/s 0 2 4 6 8 10
温度/K 290 291 291 291.5 292 292
①结合实验目的与表中数据,得出的结论是 。
②猜想可能是 的影响。若证明猜想正确,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的
最佳试剂是 (填字母)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
19.(14 分)氮元素是一种重要元素,其单质及化合物在化工、生产等领域应用非常广泛。请回答下列问
题:
(1)氮元素的常见单质有 、 、 ,三种分子中的每个氮原子均为 8 电子稳定结构,则 的结构
简式为 。
/(2)碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
第一步: (快反应)
第二步: (慢反应)
第三步: (快反应)
实验表明:含碘时 分解速率方程 (k 为速率常数)。下列表述正确的是
___________。
A.升高温度,第一步反应向右进行的程度变大
B.第二步反应的活化能比第三步反应的小
C.IO 为反应的催化剂
D. 分解反应的速率与是否含碘蒸气有关
(3)为探究温度及不同催化剂对反应 的影响,
分别在不同温度、不同催化剂下,保持其他初始条件不变重复实验,在相同时间内测得 NO 转化率与
温度的关系如图所示。在催化剂乙作用下,图中 M 点对应的速率(对应温度 400℃)v(正) v(
逆)(填“>”“<”或“=”),温度升高后,两种催化剂条件下 NO 转化率均明显降低,原因可能
是 。
(4) 催化还原 NO 是重要的烟气脱硝技术。
某研究小组将 、 和一定量的 充入 2L 密闭容器中,在 催化剂表面发生反应
,NO 的转化率随温度变化的情况如图所示。
/在 15min 内将温度从 420℃升高到 580℃,此时间段内 NO 的平均反应速率为
。
(5)已知 的反应历程分两步:
第一步: (快速平衡)
第二步: (慢反应)
①用 表示的速率方程为 ;用 表示的速率方程为
, 与 分别表示速率常数,则 。
②下列关于反应 的说法正确的是 (填字母)。
A.增大压强,反应速率常数一定增大
B.第一步反应的活化能小于第二步反应的活化能
C.反应的总活化能等于第一步和第二步反应的活化能之和
/