文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【广西版】
可能用到的相对原子质量:H—1、C—12、N—14、O—16、Na—23、S—32、Ti—48、
Fe—56、Ni—59、Cu—64
一、单项选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.下列物品中含有大量纤维素的是( )
物品
A .狼毫(黄
选项 B .涤纶布料 C .纸张 D .碳纤维管
鼠狼毛制成)
2.向CuSO 溶液中通入H S,会生成CuS沉淀,反应为CuSO H S CuSH SO 。下
4 2 4 2 2 4
列有关说法正确的是( )
A.SO2的空间构型为三角锥形 B.H S属于电解质
4 2
C.Cu在周期表中位于 d区 D.S2的结构示意图为
3.下列关于物质的结构或性质及解释均正确的是( )
选
物质的结构或性质 解释
项
A 键角:H O NH 水分子中O上孤电子对数比氨分子中 N上的多
2 3
B 稳定性:HFHCl HF分子间氢键强于HCl分子间作用力
C 熔点:碳化硅>金刚石 CSi的键能大于CC的键能
酸性: CF的极性大于CCl的极性,导致CFCOOH的羧基中
3
D
CFCOOHCCl COOH 的羟基极性更大,氢更易电离
3 3
4.具备基本的化学实验技能是进行科学探究的基础和保证。下列有关实验操作正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A. B.
C. D.
5.短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W
简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:ZQ
C.第一电离能:YZ D.电负性:WZ
6.茯苓新酸DM是从茯苓中提取的一种天然产物,具有一定的生理活性,其结构简式如图。
关于该化合物,下列说法错误的是( )
A.可使酸性KMnO 溶液褪色 B.可发生取代反应和加成反应
4
C.可与金属钠反应放出H D.分子中含有3种官能团
2
7.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3N
A
B.电解熔融CuCl ,阴极增重 6.4g,外电路中通过电子的数目为0.20N
2 A
C.12gNaHSO 晶体中含有 0.2N 个阳离子
4 A
D.1LpH=1的稀H SO 溶液中含有H的数目为0.2N
2 4 A
8.下图是物质间发生化学反应的颜色变化,下表选项物质对应正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
选项 M N P Q
A NH H O BaOH Zn KSCN
3 2 2
B Na BaCl FeO KSCN
2
C NaOH
BaNO
Fe KSCN
3 2
D Na O MgCl Fe KSCN
2 2 2
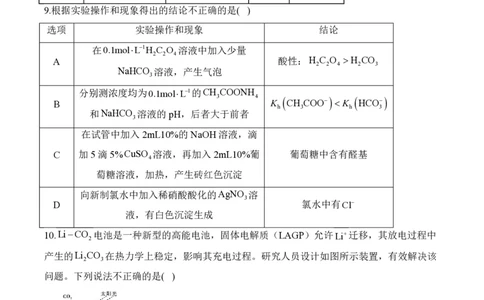
9.根据实验操作和现象得出的结论不正确的是( )
选项 实验操作和现象 结论
在0.1molL1H C O 溶液中加入少量
2 2 4
A 酸性:H C O H CO
2 2 4 2 3
NaHCO 溶液,产生气泡
3
分别测浓度均为0.1molL1的CH COONH
B
3 4
K
CH
COO
K
HCO
h 3 h 3
和NaHCO 溶液的pH,后者大于前者
3
在试管中加入2mL10%的NaOH溶液,滴
C 加5滴 5%CuSO 溶液,再加入 2mL10%葡 葡萄糖中含有醛基
4
萄糖溶液,加热,产生砖红色沉淀
向新制氯水中加入稀硝酸酸化的AgNO 溶
3
D 氯水中有Cl
液,有白色沉淀生成
10.LiCO 电池是一种新型的高能电池,固体电解质(LAGP)允许Li迁移,其放电过程中
2
产生的Li CO 在热力学上稳定,影响其充电过程。研究人员设计如图所示装置,有效解决该
2 3
问题。下列说法不正确的是( )
A.放电时,b作负极
B.放电时,Li由b向a迁移
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
C.充电时,a极的电极反应式:4Li 3CO 4e 2Li CO C
2 2 3
D.充电时,太阳光有利于Li CO 的分解,降低充电电压
2 3
11.能正确表示下列反应的离子方程式的是( )
A.测定空气中SO 的含量可用酸性高锰酸钾溶液:
2
5SO 2MnO 4H 5SO2 2Mn2 2H O
2 4 4 2
B.向含有漂白粉的溶液中通入足量的SO ,效果会更好:
2
SO H O2ClO 2HClOSO2
2 2 3
C.泡沫灭火器的原理:3CO2 2Al3 3H O 3CO 2Al(OH)
3 2 2 3
D.工业上用FeCl 溶液制作印刷电路板的原理:2Fe3 Cu Cu2 2Fe2
3
12.镍钛记忆合金被广泛应用于人造卫星和宇宙飞船的天线。一种镍钛合金的晶胞结构如图所
示,已知合金的密度为gcm3,gcm3代表阿伏加德罗常数的值,下列说法错误的是( )
A.记忆合金的两种金属都属于过渡金属元素,Ti在元素周期表中位于第四周期ⅣB族
B.晶体中 Ni原子位于由Ti原子形成的正八面体的空隙中
C.该合金的熔点低于金属钛的熔点
2 1074
D.晶胞中两个钛原子间的最近距离是
3
pm
2 N
A
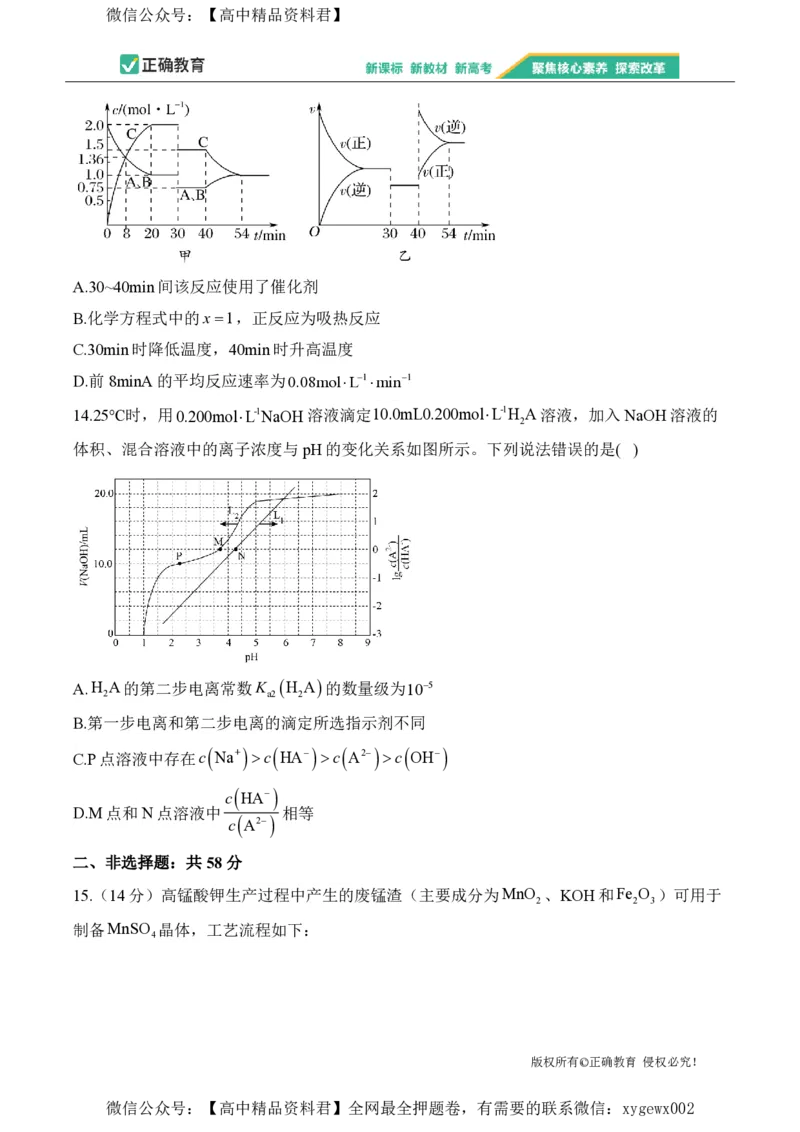
13.某密闭容器中充入等物质的量的A和B,一定温度下发生反应AgxBg 2Cg,
达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时
间的变化如图乙所示,下列说法中正确的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.30~40min间该反应使用了催化剂
B.化学方程式中的x1,正反应为吸热反应
C.30min时降低温度,40min时升高温度
D.前8minA的平均反应速率为0.08molL1min1
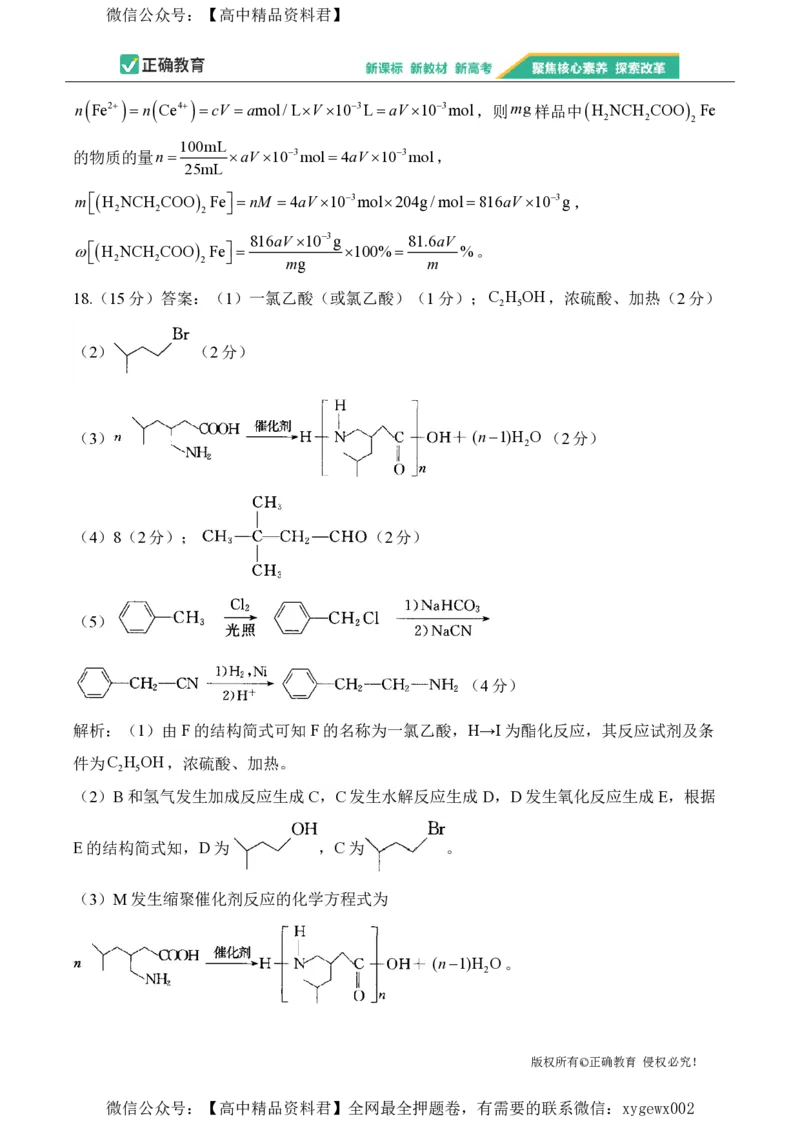
14.25℃时,用0.200molL-1NaOH溶液滴定10.0mL0.200molL-1H A溶液,加入NaOH溶液的
2
体积、混合溶液中的离子浓度与pH的变化关系如图所示。下列说法错误的是( )
A.H A的第二步电离常数K H A的数量级为105
2 a2 2
B.第一步电离和第二步电离的滴定所选指示剂不同
C.P点溶液中存在c
Na+
c
HA
c
A2
c
OH
c
HA
D.M点和 N点溶液中 相等
c
A2
二、非选择题:共 58 分
15.(14分)高锰酸钾生产过程中产生的废锰渣(主要成分为MnO 、KOH和Fe O )可用于
2 2 3
制备MnSO 晶体,工艺流程如下:
4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:硫铁矿的主要成分为二硫化亚铁(FeS ,杂质不参与反应)。
2
回答下列问题:
(1)二硫化亚铁中S元素的化合价为___________。
(2)滤渣A的主要成分是___________(填化学式);“反应Ⅱ”生成FeSO 、MnSO 等物质
4 4
的离子方程式为___________。
(3)“反应Ⅲ”中还原剂和氧化剂物质的量之比为___________;加入MnO 作为氧化剂的优点
2
是___________。
(4)“调pH”时,验证Fe3已经沉淀完全的实验操作和现象为____________________。
(5)“蒸发结晶”时,应在___________时停止加热。
16.(14分)将CO 转化为CO、CH 、CH OH等燃料,不仅能缓解碳排放带来的环境问题,
2 4 3
还将成为理想的能源补充形式。
(1)一种特定条件下,由CO 和H 合成CH OH的反应过程如下:
2 2 3
Ⅰ.CO (g)H (g)CO(g)H O(g) H 40.9kJmol1
2 2 2 1
Ⅱ.CO(g)2H (g)CH OH(g) H 90.4kJmol1
2 3 2
写出由CO 和H 合成CH OH的热化学方程式:______。
2 2 3
(2)在催化剂Cu/ZnO作用下,利用CO 和H 合成甲醇,可发生如下两个反应。
2 2
反应Ⅲ:CO (g)3H (g)CH OH(g)H O(g)
2 2 3 2
反应Ⅳ:CO (g)H (g)CO(g)H O(g)
2 2 2
相同时间内,温度对CO 转化率及甲醇和CO产率的影响如图所示。
2
①由图乙判断合成CH OH最适宜的温度是_______。
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
②由图乙可知,温度升高,CH OH产率先升高后降低,降低的可能原因是_______(任写两
3
条)。
③下列措施有利于提高CO 转化为CH OH的平(衡转化率的有_______填序号)。
2 3
A.增大体系压强
B.提高CO 和H 的投料比
2 2
C.容器容积和投料比不变,提高反应物浓度
④保持温度 T 不变,在一刚性密闭容器中,充入一定量的CO 及H ,起始及达到平衡时,
2 2
容器内各气体物质的量如表所示。
CO H CH OH CO H O(g) 总压/kPa
2 2 3 2
起始量/mol 5.0 7.0 0 0 0 p
0
平衡量/mol n n p
1 2
达到平衡时, p 1.2p,则表中n _____;若此时n 3,则反应Ⅲ的平衡常数K =_____
0 1 2 p
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。用含 p 的代数式表示)。
17.(15分)甘氨酸亚铁[ H NCH COO Fe]可有效改善缺铁性贫血,实验室可利用FeCO 与
2 2 2 3
甘氨酸(H NCH COOH)反应制备,原理为
2 2
FeCO 2H NCH COOH H NCH COO FeCO H O。某学习小组利用如图实验装
3 2 2 2 2 2 2 2
置制备甘氨酸亚铁(夹持和加热、搅拌仪器已省略)。
已知:
甘氨酸
柠檬酸 甘氨酸亚铁
(H NCH COOH)
2 2
易溶于水,微溶于乙 易溶于水和乙醇,有强
易溶于水,难溶于乙醇
醇,两性化合物 酸性和还原性
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
实验过程:
Ⅰ.制备FeCO :
3
(1)实验操作如下:关闭活塞K ,打开K ,打开活塞K 加入适量稀硫酸,有气体生成,该
2 3 1
气体的作用是_______;反应一段时间后,关闭活塞K 和K ,打开活塞K ,有溶液流入B,
1 3 2
其原因是_______。
(2)B中生成FeCO 沉淀的离子方程式为_____。
3
Ⅱ.制备H NCH COO Fe:
2 2 2
将甘氨酸和少量柠檬酸的混合溶液加入B中,调节溶液pH至5.5左右,加热使反应物充分反
应。反应结束后过滤,滤液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到甘氨酸亚铁产
品。
(3)仪器b的名称为_____;该仪器的优点是_____。
(4)需要控制B中反应溶液的pH在5.5左右,其原因为_____。
(5)装置C的作用为_____;洗涤操作中,选用的最佳洗涤试剂是_____(填字母)。
A.热水
B.乙醇
C.柠檬酸
(6)测定产品的含量:
实验室用CeSO 溶液对甘氨酸亚铁中的Fe2进行测定[假设样品中其他成分不与CeSO
4 2 4 2
反应]。称取mg样品溶于稀H SO 中,配制成100.0mL溶液。用移液管取出25.00mL溶液于
2 4
锥形瓶中,用amol/LCeSO 标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴
4 2
定反应为Ce4 Fe2 Ce3 Fe3)。产品中甘氨酸亚铁的质量分数为__________%。
18.(15分)普瑞巴林是一种在临床上广泛使用的抗癫痫药物,其合成路线如图所示。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
回答下列问题:
(1)F的名称为________,实现H→I的反应试剂及条件为________。
(2)C的结构简式为_______。
(3)M发生缩聚反应的化学方程式为_______。
(4)化合物N是E的同系物,N比E多一个碳原子,则化合物N的结构有_______种,其中
核磁共振氢谱峰面积之比为9:2:1的结构简式为_______。
(5)参考以上合成路线及反应条件,请写出以甲苯( )和必要的无机试剂为
原料,合成苯乙胺( )的路线流程图:_______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:C
解析:黄鼠狼毛的主要成分是蛋白质,A项错误;涤纶是对苯二甲酸和乙二醇经缩聚反应而
制得的聚酯纤维,B项错误;纸张的主要成分是纤维素,C项正确;碳纤维管的主要成分为
碳纤维复合材料,D项错误。
2.答案:B
6224
解析:SO2的中心原子S的价层电子对数为4 4,为sp杂化,无孤电子对,
4 2
SO2为正四面体形,A项错误;H S为弱酸,属于电解质,B项正确;Cu位于第四周期第ⅠB
4 2
族,在周期表中位于ds区,C项错误;S2核外有 18个电子,结构示意图为
,D项错误。
3.答案:D
解析:A.随着孤电子对数增多,成键电子对与成键电子对之间的斥力减小,键角也减小,
H O和NH 的键角大小为H O碳化硅,选项 C错误;D.CF的极性大于CCl的极性,导致CFCOOH的羧基
3
中的羟基极性更大,更容易电离出氢离子,CFCOOH酸性大于CCl COOH,选项D正确;
3 3
答案选D。
4.答案:C
解析:A中酒精灯不能用另一盏燃烧的酒精灯来点;B中托盘天平的精度为0.1g;D中选用
量器要“大而近”的原则,所以量取9.5mL液体要选用 10mL量筒。
5.答案:B
解析:C能与H、O、N、S、Cl等元素形成共价键,A项正确;
O的简单氢化物为H O,S的简单氢化物为H S,H O分子间存在氢键,故沸点
2 2 2
H OH S,B项错误;
2 2
N、O为同周期相邻元素,N原子的2p轨道为半满稳定结构,其第一电离能大于 O,C项正
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
确;
电负性OAl,D项正确。
6.答案:D
解析:该分子中含有碳碳双键、羟基,能被酸性高锰酸钾溶液氧化而使溶液褪色,A项正
确;分子中含有羧基、羟基,能发生酯化反应(属于取代反应),含有酯基,能发生水解反
应(属于取代反应),含有碳碳双键,能发生加成反应,B项正确;分子中含有羟基、羧
基,能和金属钠发生反应放出H ,C项正确;分子中含有酯基、羟基、羧基、碳碳双键4种
2
官能团,D项错误。
7.答案:B
解析:没有给出混合气体所处的状态,不能计算碳氢键数,A项错误;电解熔融CuCl ,阴
2
极反应为Cu2 2e Cu,增重6.4g即生成0.1 molCu,外电路中通过电子的数目为
0.2N ,B项正确;NaHSO 晶体含有的离子为Na和HSO,12gNaHSO 晶体的物质的量为
A 4 4 4
0.1mol,含有0.1N 个阳离子,C项错误;1LpH=1的稀H SO 溶液中含有H的数目为0.1
A 2 4
N ,D项错误;
A
故选B。
8.答案:C
解析:A.N不能是氢氧化钡,因为它与硫酸铁反应除了生成硫酸钡,还会生成氢氧化铁,为
红褐色沉淀,故A错误;
B.P不能为氧化亚铁,它不能与硫酸铁反应生成亚铁离子,故 B错误;
D.N不能为氯化镁,它不能与硫酸铁反应生成白色沉淀,故D错误。
故选:C。
9.答案:B
解析:在0.1molL1H C O 溶液中加入少量NaHCO 溶液,产生气泡,说明二者发生反应生
2 2 4 3
成CO ,由较强酚可制较弱酸可知,酸性:H C O H CO ,A项正确;CH COONH 溶液
2 2 2 4 2 3 3 4
中CH COO和NH都发生水解,CH COO水解使溶液呈碱性,NH水解使溶液呈酸性,
3 4 3 4
NaHCO 溶液中只有HCO水解使溶液呈碱性,因此不能根据题述现象判断K
CH
COO
和
3 3 h 3
K
HCO
的大小,B项错误;氢氧化钠量多,硫酸铜量少,硫酸铜全部反应生成氢氧化
h 3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
铜,加入葡萄糖溶液,加热产生砖红色沉淀,说明葡萄糖中含有醛基,C项正确;向新制氯
水中加入稀硝酸酸化的AgNO 溶液,有白色沉淀生成,说明氯水中含有Cl,D项正确。
3
10.答案:C
解析:电池放电时活泼金属作负极,故A正确;在原电池中,阳离子移向正极,阴离子移向
负极,故B正确;充电时,a极为阳极,发生氧化反应,故 C错误;根据题意可知,充电
时,太阳光有利于的分解,降低充电电压,D正确。
11.答案:D
解析:测定空气中SO 的含量可用酸性高锰酸钾溶液:
2
5SO 2MnO 2H O 5SO2 2Mn2 4H,A错误;向含有漂白粉的溶液中通入足量的
2 4 2 4
SO ,会发生氧化还原反应:SO H OClO 2H Cl SO2,使漂白粉失效,B错
2 2 2 4
误;泡沫灭火器的原理:3HCO Al3 3CO Al(OH) ,C错误;工业上用FeCl 溶
3 2 3 3
液制作印刷电路板的原理:2Fe3 Cu Cu2 2Fe2,D正确。
12.答案:D
解析:记忆合金的两种金属(Ni、Ti)都属于过渡金属元素,位于元素周期表的d区,其中
Ti在元素周期表中位于第四周期ⅣB族,A选项正确;晶胞中位于面心的六个Ti原子构成了
正八面体结构,Ni原子位于其中心,B选项正确;合金的熔点低于其组分金属的熔点,C选
项正确;利用均摊法,每个晶胞中含有4个Ti原子和4个Ni原子,合金的密度为g/cm3,
m 1074
N 代表阿伏加德罗常数的值,则晶胞体积为V cm3,两个钛原子间的最近距离
A N
A
2 1074 2 1074
为
3
cm
3
1010pm,D选项错误。
2 N 2 N
A A
13.答案:D
解析:A.若使用催化剂,则化学反应速率加快,A项错误;
B.由甲图象可知,A、B的浓度变化相同,故A、B的化学计量数相同,都为1;由乙图象可
知,30min时改变的条件为减小压强,40min时改变的条件为升高温度,且升高温度平衡向逆
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
反应方向移动,则正反应为放热反应,B项错误;
C.30min时改变的条件为减小压强,40min时改变的条件为升高温度,C项错误;
(2.001.36)mol/L
D.前8minA的平均反应速率为 0.08molL1min1,D项正确;
8min
故选D。
14.答案:D
c
H
c
A2
解析:A.K H A ,由N点可知K H A104.3,数量级为105,故A正
a2 2
c
HA a2 2
确;B.由电离常数和水解常数知,NaHA溶液显酸性、Na A溶液显碱性,第一步滴定选择甲
2
基橙作指示剂、第二步滴定选择酚酞作指示剂,故B正确;C.P点为NaHA溶液,HA电离
程度大于水解,溶液中c
Na
c
HA
c
A2
c
OH
,故C正确;D.M点和N点溶液
c
HA
的pH不同,溶液中 不相等,故D错误;故选 D。
c
A2
15.(14分)答案:(1)-1(2分)
(2)MnO (2分);4H FeS MnO Fe2 2SMn2 2H O(2分)
2 2 2 2
(3)2:1(2分);MnO 会转化为MnSO ,氧化Fe2同时可以提高MnSO 的产量(2分)
2 4 4
(4)取上层清液于试管中,滴入几滴KSCN溶液,溶液未变为血红色(2分)
(5)有大量晶体析出(2分)
解析:(1)二硫化亚铁中亚铁显+2价,故S元素化合价为-1价;
(2)根据分析知滤渣A的主要成分是MnO 。反应Ⅱ中,MnO 作氧化剂,Mn元素被还原生
2 2
成Mn2,FeS 作还原剂,S元素被氧化生成S单质,反应的离子方程式为:
2
4H FeS MnO Fe2 2SMn2 2H O;
2 2 2
(3)反应Ⅲ中,Fe2作还原剂被氧化生成Fe3,MnO 作氧化剂被还原生成Mn2,根据氧
2
化还原反应中得失电子总数相同,还原剂和氧化剂物质的量之比为2:1。用MnO 作氧化剂的
2
好处是:MnO 会转化为MnSO ,在氧化Fe2同时可以提高MnSO 的产量;
2 4 4
(4)验证Fe3已经完全沉淀的实验操作和现象为:取上层清液于试管中,滴入几滴KSCN
溶液,溶液未变为血红色;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(5)根据蒸发的实验要求,应在有大量晶体析出时停止加热。
16.(14分)答案:(1)CO (g)3H (g)CH OH(g)H O(g) H 49.5kJmol1(2
2 2 3 2
分)
(2)①250℃(2分);②反应Ⅲ的正反应为放热反应,升高温度平衡逆向移动,CH OH产
3
率降低(2分);温度升高,催化剂的活性下降,CH OH产率降低(合理即可)(2分);
3
75
③AC(2分);④1(2分); (2分)
4p2
解析:(1)由盖斯定律可知,反应Ⅰ+反应Ⅱ可得二氧化碳和氢气合成甲醇的热化学方程式:
CO (g)3H (g)CH OH(g)H O(g),则
2 2 3 2
H 40.9kJmol1 90.4kJmol1 49.5kJmol1。
(2)①由图乙可知,250℃时CH OH的产率最高,所以合成CHgOH最适宜的温度是
3
250℃。②由图乙可知,温度升高CH OH产率先升高后降低,250℃之前,反应还未达到平
3
衡,温度升高,反应速率加快,甲醇产率升高,由(1)可知,反应Ⅲ正向放热,250℃之
后,升高温度平衡逆向移动,也可能是温度升高,催化剂的活性下降,从而导致CH OH产率
3
降低。③反应Ⅲ正向是气体分子数减小的反应,所以增大体系压强,平衡正向移动,反应Ⅳ
是气体分子数不变的反应,增大体系压强对反应Ⅳ平衡无影响,所以增大压强有利于提高
CO 转化为CH OH的平衡转化率,A正确;提高CO 和H 的投料比,虽然平衡正向移动,
2 3 2 2
但CO 的平衡转化率降低,B错误;容器容积和投料比不变,提高反应物浓度,相当于增大
2
压强,根据A项分析可知,能使CO 转化为CH OH的平衡转化率增大,C正确。④恒温恒
2 3
容条件下,气体物质的量之比等于压强之比,起始时气体总物质的量为12mol,达到平衡
时,存在 p 1.2p,则平衡时气体总物质的量为10mol,气体总物质的量减小12mol-
0
10mol=2mol,由于反应Ⅳ是气体分子数不变的反应,则减少的2 mol由反应Ⅲ造成,平衡时
CH OH的物质的量为n mol,则有
3 1
CO (g)3H (g)CH OH(g)H O(g) x
2 2 3 2
1 3 1 1 2
变化量/mol n 2
1
则n 1;若此时n 3,即平衡时H O(g)的物质的量为3mol,则反应Ⅳ生成2molH O(g),
1 2 2 2
平衡时CO 、H 、CH OH、H O(g)、CO的物质的量分别为2mol、2mol、1mol、3mol、
2 2 3 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
1 1 1 3
2mol,CO 、H 、CH OH、H O(g)的物质的量分数分别为 、、 、 ,反应Ⅲ的平衡常数
2 2 3 2 5 5 10 10
3 1
p p
10 10 75
K 。
p
1 1
3 4p2
p p
5 5
17.(15分)答案:(1)排出装置中的空气(1分);产生的氢气使装置A中压强大于大气
压(1分)
(2)Fe2 2HCO FeCO H OCO (2分)
3 3 2 2
(3)恒压滴液漏斗(1分);可以平衡压强,使液体顺利滴下(1分)
(4)pH过低,c H 较大,H和H NCH COOH反应,不利于H NCH COO Fe的生成,
2 2 2 2 2
pH过高,易生成Fe(OH) 沉淀(3分)
2
(5)液封,防止空气进入装置B而将Fe2氧化(2分);B(2分)
81.6aV
(6) (2分)
m
解析:(1)亚铁离子易被氧化,故实验前需先排出装置内的空气,防止亚铁离子被氧化;打
开活塞K ,有溶液流入装置B,其原因是装置A中产生的H 使装置A中的压强大于大气
2 2
压,故有溶液流入装置B。
(2)Fe2结合HCO电离出的CO2,使HCO的电离平衡正向移动,产生的H又与HCO
3 3 3 3
反应生成CO ,故反应的离子方程式为Fe2 2HCO FeCO H OCO 。
2 3 3 2 2
(4)H NCH COOH中含有NH ,NH 显碱性,pH过低,c
H
较大,H和
2 2 2 2
H NCH COOH中的氨基反应,不利于H NCH COO Fe的生成,pH过高,碱性较强,易
2 2 2 2 2
生成Fe(OH) 沉淀。
2
(5)亚铁离子易被氧化,所以装置B中应保持无氧状态,装置C的作用为液封,防止空气
进入装置B而将Fe2氧化;甘氨酸亚铁难溶于乙醇,可减少产品溶解损耗,且乙醇易挥发,
可尽快干燥,防止亚铁离子被氧化。
(6)由Ce4 Fe2 Fe3 Ce3可知:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
n Fe2 n Ce4 cV amol/LV103LaV103mol,则mg样品中H NCH COO Fe
2 2 2
100mL
的物质的量n aV103mol4aV103mol,
25mL
mH NCH COO Fe nM 4aV103mol204g/mol816aV103g,
2 2 2
816aV103g 81.6aV
H NCH COO Fe 100% %。
2 2 2 mg m
18.(15分)答案:(1)一氯乙酸(或氯乙酸)(1分);C H OH,浓硫酸、加热(2分)
2 5
(2) (2分)
(3) (n1)H O(2分)
2
(4)8(2分); (2分)
(5)
(4分)
解析:(1)由F的结构简式可知F的名称为一氯乙酸,H→I为酯化反应,其反应试剂及条
件为C H OH,浓硫酸、加热。
2 5
(2)B和氢气发生加成反应生成C,C发生水解反应生成D,D发生氧化反应生成E,根据
E的结构简式知,D为 ,C为 。
(3)M发生缩聚催化剂反应的化学方程式为
(n1)H O。
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(4)化合物N是E的同系物,比E多一个碳原子,说明N中含有醛基,其
结构可表示为C H CHO,戊基的同分异构体有8种,所以N的结构有8种。其中核磁共振
5 11
氢谱峰面积之比为9:2:1的结构简式为 。
(5)根据题给信息,甲苯先引入氯原子,再进行合成,具体路线如下:
。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002