文档内容
2025 年高三 5 月壮行考试
化学答案
1 2 3 4 5 6 7 8
A D A B B C D A
9 10 11 12 13 14 15
D A B D D C D
1.【解析】化学品可分为大宗化学品和精细化学品两大类。乙烯、硫酸、纯碱和化肥属于大宗化学品,医
药、农药、日用化学品、食品添加剂等属于精细化学品。故答案选A。
2.【解析】钡元素的焰色为黄绿色,铜的焰色为绿色,A项正确;Ba为+2价,Si为+4价,O为-2价,以
化合价代数和为零计算,Cu为+2价,B项正确;该物质属于硅酸盐材料,C项正确;在硅酸盐中,Si和
O构成硅氧四面体结构,每个Si周围连接4个O,D项错误。故答案选D。
3.【解析】“OTC”标识代表非处方药,A项错误;MgCl 为电解质,可使豆浆中的蛋白质聚沉,故可作豆
2
腐凝固剂,B项正确;加入适量石膏可调节水泥硬化速率,C项正确;硬铝具有密度小、强度高、耐腐蚀
的特性,是制造飞机和宇宙飞船的理想材料,D项正确。故答案选A。
4.【解析】蛋白质两端存在氨基和羧基,侧链中也往往存在酸性或碱性基团,和氨基酸类似,具有两性,
A项正确;肽链中的氧原子和氢原子之间存在氢键,会使肽链盘绕或折叠为特定的空间结构,形成蛋白质
的二级结构,B项错误;含有苯环的蛋白质遇浓硝酸会有白色沉淀产生,加热后沉淀变黄色,C项正确;
从动物皮、骨中提取的明胶蛋白可用作食品增稠剂,D项正确。故答案选B。
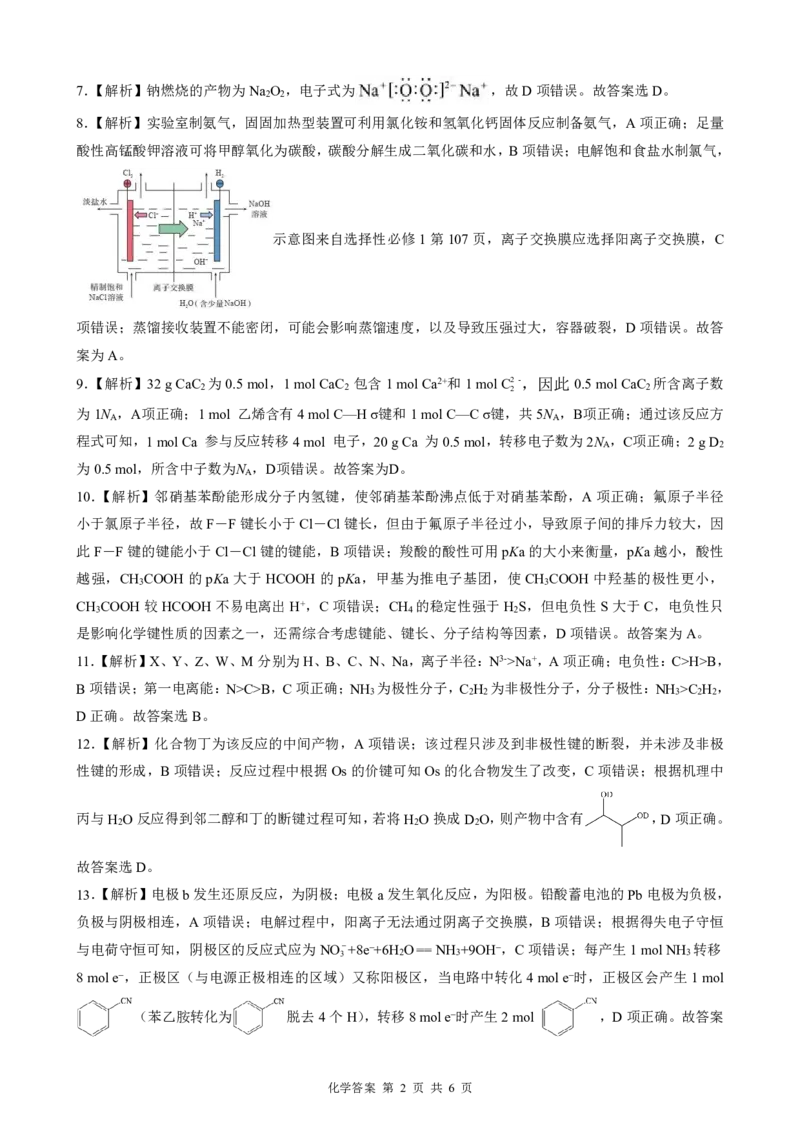
5.【解析】 由图可知,分子中含有10个手性碳原子,A项正确;该分子中含
有碳碳双键和羟基,因此可使酸性K Cr O 溶液从橙色变为绿色,B项错误;该分子的不饱和度为6,芳
2 2 7
香族化合物不饱和度大于等于4,因此同分异构体中可能有芳香族化合物,C项正确;红外光谱可获得分
子中所含官能团的信息,该分子有碳碳双键和羟基两种官能团,因此红外光谱中至少含有2组峰,D项正
确。故答案选B。
6.【解析】必修第一册第9页“提示”中有与实验有关的图标及说明, 表示实验结束后,离开实
验室前需用肥皂等清洗双手,A项正确;必修第一册第124页附录II中, 表示暴露在空气容
易自燃的物质,B项正确;必修第一册第123页附录I中,关于常见废弃物的处理方法中写道:不需要回
收利用的,可用焚烧法处理,但含卤素的有机废液焚烧后的尾气处理具有特殊性,应单独处理,C项错误;
如果不慎将碱液沾到皮肤上,应用大量水冲洗,然后涂上1%的硼酸,D项正确。故答案选C。
化学答案 第 1 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}7.【解析】钠燃烧的产物为Na O ,电子式为 ,故D项错误。故答案选D。
2 2
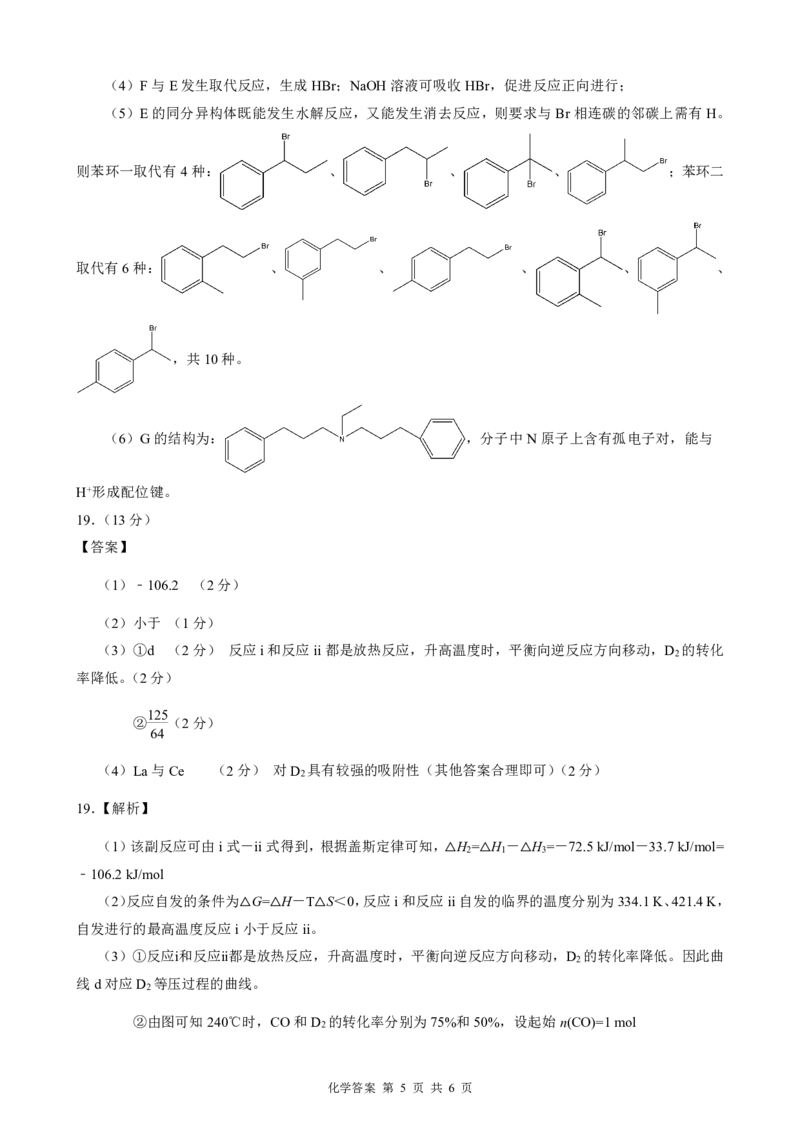
8.【解析】实验室制氨气,固固加热型装置可利用氯化铵和氢氧化钙固体反应制备氨气,A项正确;足量
酸性高锰酸钾溶液可将甲醇氧化为碳酸,碳酸分解生成二氧化碳和水,B项错误;电解饱和食盐水制氯气,
示意图来自选择性必修1第107页,离子交换膜应选择阳离子交换膜,C
项错误;蒸馏接收装置不能密闭,可能会影响蒸馏速度,以及导致压强过大,容器破裂,D项错误。故答
案为A。
9.【解析】32gCaC 为0.5mol,1molCaC 包含1molCa2+和1molC2-,因此 0.5molCaC 所含离子数
2 2 2 2
为1N ,A项正确;1mol 乙烯含有4molC—Hσ键和1molC—Cσ键,共5N ,B项正确;通过该反应方
A A
程式可知,1molCa 参与反应转移4mol 电子,20gCa 为0.5mol,转移电子数为2N ,C项正确;2gD
A 2
为0.5mol,所含中子数为N ,D项错误。故答案为D。
A
10.【解析】邻硝基苯酚能形成分子内氢键,使邻硝基苯酚沸点低于对硝基苯酚,A项正确;氟原子半径
小于氯原子半径,故F―F键长小于Cl―Cl键长,但由于氟原子半径过小,导致原子间的排斥力较大,因
此F―F键的键能小于Cl―Cl键的键能,B项错误;羧酸的酸性可用pKa的大小来衡量,pKa越小,酸性
越强,CH COOH 的pKa 大于 HCOOH 的 pKa,甲基为推电子基团,使CH COOH 中羟基的极性更小,
3 3
CH COOH较HCOOH不易电离出H+,C项错误;CH 的稳定性强于H S,但电负性S大于C,电负性只
3 4 2
是影响化学键性质的因素之一,还需综合考虑键能、键长、分子结构等因素,D项错误。故答案为A。
11.【解析】X、Y、Z、W、M分别为H、B、C、N、Na,离子半径:N3->Na+,A项正确;电负性:C>H>B,
B项错误;第一电离能:N>C>B,C项正确;NH 为极性分子,C H 为非极性分子,分子极性:NH >C H ,
3 2 2 3 2 2
D正确。故答案选B。
12.【解析】化合物丁为该反应的中间产物,A项错误;该过程只涉及到非极性键的断裂,并未涉及非极
性键的形成,B项错误;反应过程中根据Os的价键可知Os的化合物发生了改变,C项错误;根据机理中
丙与H O反应得到邻二醇和丁的断键过程可知,若将H O换成D O,则产物中含有 ,D项正确。
2 2 2
故答案选D。
13.【解析】电极b发生还原反应,为阴极;电极a发生氧化反应,为阳极。铅酸蓄电池的Pb电极为负极,
负极与阴极相连,A项错误;电解过程中,阳离子无法通过阴离子交换膜,B项错误;根据得失电子守恒
与电荷守恒可知,阴极区的反应式应为NO‒+8e‒+6H O==NH +9OH‒,C项错误;每产生1molNH 转移
3 2 3 3
8mole‒,正极区(与电源正极相连的区域)又称阳极区,当电路中转化4mole‒时,正极区会产生1mol
(苯乙胺转化为 脱去4个H),转移8mole‒时产生2mol ,D项正确。故答案
化学答案 第 2 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}选D。
14.【解析】La位于元素周期表的f区,A项错误;原子半径:La>Cu>O,故该俯视图错误,B项错误;
Cu 位于 O 构成的八面体的体心,C 项正确;该晶胞中,Cu 原子数为 2,La 原子数为 4,O 原子数为
1 1
16 428,该晶胞的化学式为La CuO ,不能称之为分子式,D项错误。故答案选C。
2 4
4 2
15.【解析】由K (AgIO )=c(Ag+)·c(IO -)和K [Pb(IO ) ]=c(Pb2+)·c2(IO -) ;对上述等式两边同时取负对数,
sp 3 3 sp 3 2 3
斜率为-1的曲线①对应的是Ag+与-lg[c(IO -)]的关系;曲线②的斜率为-2,代表的是Pb2+与-lg[c(IO -)]的关
3 3
系,A选项错误;若向a点饱和溶液中加入适量NaIO 固体,c(IO -)增大,-lg[c(IO -)]会减小,不会由a
3 3 3
点变成b点,B错误;且由b点坐标值可知:K (AgIO )=105.09102.21=107.30和
sp 3
K sp PbIO 3 2 =105.09105.09102.21=1012.39,常温AgIO 3 在水中的溶解度约为10-3.65mol/L ,C选项错误;
K (AgIO )
sp 3 比值为105.09,其数量级为105,D选项正确。故答案选D。
K [Pb(IO ) ]
sp 3 2
16.(14分)
【答案】
(1)5s25p3 (1分)
(2)SiO (1分);提高锑的回收率 (2分)
2
(3)Fe3+、Cu2+和Sb5+ (2分,写2个得1分,写3个得2分,写1个不得分)
(4)促进Sb3+的水解,形成稳定的晶型,便于过滤分离(2分)
(5)K [Fe(CN) ]溶液(2分)
3 6
(6)2SbOCl+(NH ) CO ==Sb O +2NH Cl+CO ↑(2分)
4 2 3 2 3 4 2
(7)X射线衍射仪 (2分)
16.【解析】
(1)Sb位于第五周期第VA族,价电子排布式为5s25p3;
(2)SiO 不与盐酸反应,因此滤渣1的主要成分为SiO ;再次返回溶解,进行二次酸浸,可以提高
2 2
锑的回收率;
(3)酸浸溶解后,溶液中的阳离子为Fe3+、Cu2+、Sb3+和Sb5+,铁粉作为还原剂可将Fe3+、Cu2+和Sb5+
还原;
(4)Sb3++Cl-+H O==SbOCl(胶体)+2H+,不断搅拌的原因是避免形成胶体,加入NaCl是为了促
2
进Sb3+的水解,因此原因为:促进Sb3+的水解形成稳定的晶型,便于过滤分离;
(5)沉淀上可能附着Fe2+,可用铁氰化钾溶液进行检验;
(6)“中和”过程中(NH ) CO 与前面生成的SbOCl反应,生成Sb O ,因此方程式为:2SbOCl+
4 2 3 2 3
(NH ) CO ==Sb O +2NH Cl+CO ↑
4 2 3 2 3 4 2
化学答案 第 3 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}(7)X射线衍射仪可用于晶体结构的测定,可获得键长、键角等信息,是物质结构测定的一种重要
技术。
17.(14分,每空2分)
【答案】
(1)球形冷凝管 (2分)
(2)使样品转移完全 (2分) 盖上瓶塞,反复上下颠倒摇匀 (2分)
(3)4NaBH +2Se+7H O=2NaHSe+Na B O +14H ↑ (2分)
4 2 2 4 7 2
(4)排尽装置内空气,防止NaHSe被氧化 (2分)
(5)丁达尔效应(用一束光照射产生光亮的通路)(2分)
(6)C(2分)
17.【解析】
(1)该仪器为球形冷凝管
(2)配制一定物质的量浓度溶液的过程中,洗涤烧杯和玻璃棒2~3次,是为了将样品转移完全至容
量瓶中;定容后,应盖上瓶塞,反复上下颠倒摇匀;
(3)由所给信息可知,Se被NaBH 还原,推断出产物中应有H ,因此该反应方程式为:4NaBH +2Se
4 2 4
+7H O=2NaHSe+Na B O +14H ↑;
2 2 4 7 2
(4)NaHSe具有还原性,实验过程中通入N 的目的是,排尽装置内空气,防止NaHSe被氧化;
2
(5)由题干可知,CdSe粒子直径介于1~100nm,因此该量子点产物为胶体,可用丁达尔效应检验;
(6)HSCH COOH中S上有孤电子对,因此与Cd2+配位的原子为S。
2
18.(14分,每空2分)
【答案】
(1)乙胺
(2)酸性KMnO 溶液会将甲苯氧化为苯甲酸
4
(3)
(4)取代反应 ;吸收HBr,促进反应正向进行
(5)10
(6)G分子中N原子上含有孤电子对,能与H+形成配位键。
18.【解析】
(1)A为乙胺;
(2)B为苯甲醛,若用酸性KMnO 溶液氧化性过强,会将甲苯氧化为苯甲酸;
4
(3)苯甲醛与乙醛发生羟醛缩合生成 ;
化学答案 第 4 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}(4)F与E发生取代反应,生成HBr;NaOH溶液可吸收HBr,促进反应正向进行;
(5)E的同分异构体既能发生水解反应,又能发生消去反应,则要求与Br相连碳的邻碳上需有H。
则苯环一取代有4种: 、 、 、 ;苯环二
取代有6种: 、 、 、 、 、
,共10种。
(6)G的结构为: ,分子中N原子上含有孤电子对,能与
H+形成配位键。
19.(13分)
【答案】
(1)﹣106.2 (2分)
(2)小于 (1分)
(3)①d (2分) 反应i和反应ii都是放热反应,升高温度时,平衡向逆反应方向移动,D 的转化
2
率降低。(2分)
125
② (2分)
64
(4)La与Ce (2分) 对D 具有较强的吸附性(其他答案合理即可)(2分)
2
19.【解析】
(1)该副反应可由i式-ii式得到,根据盖斯定律可知, H = H - H =-72.5kJ/mol-33.7kJ/mol=
2 1 3
﹣106.2kJ/mol
△ △ △
(2)反应自发的条件为 G= H-T S<0,反应i和反应ii自发的临界的温度分别为334.1K、421.4K,
自发进行的最高温度反应i△ 小于
△
反应ii。
△
(3)①反应ⅰ和反应ⅱ都是放热反应,升高温度时,平衡向逆反应方向移动,D 的转化率降低。因此曲
2
线d对应D 等压过程的曲线。
2
②由图可知240℃时,CO和D 的转化率分别为75%和50%,设起始n(CO)=1mol
2
化学答案 第 5 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}CO(g)+2D (g) CD OD(g)
2 3
起始 1
转化 0.75 1.5 0.75
平衡 0.25
反应ⅰ转化的D 为6×50%-1.5=1.5
2
CO (g)+3D (g) CD OD(g)+D O(g)
2 2 3 2
起始 1
转化 0.5 1.5 0.5 0.5
平衡 0.5
综上平衡时n(CO)=0.25mol,n(CO )=0.5mol,n(D )=3mol,n(CD OD)=0.75+0.5=1.25mol,n(D O)=0.5
2 2 3 2
mol,n(N )=2mol,平衡时气体总物质的量n =7.5mol
2 总
1.25
4MPa
则反应ⅱK = p(CD 3 OD) = 7.5 = 125 (MPa)-2
p p(CO)p2(D 2 ) ( 0.25 4MPa)( 3 4MPa)2 64
7.5 7.5
(4)加入稀土元素La和Ce的催化剂相较于不加入的,D 转化率和CD OD产率更高,因此有利于提
2 3
高该催化剂催化活性的稀土元素是La和Ce。由于La和Ce是较好的储氢材料,因此推测La和Ce可以提
高该催化剂活性的原因可能为其对D 具有较强的吸附性。
2
化学答案 第 6 页 共 6 页
{#{QQABTYCpwgi4gAaACL4rQQHoCksQkJMgJUoExUAQqAQCgJNABAA=}#}