文档内容
2019年黑龙江省绥化市中考化学试卷
一、选择题(每题2分,共30分;1-12题只有一个正确答案;13-15题为多项选择)
1.下列变化属于化学变化的是( )
A.电灯通电发光 B.水力发电
C.液化石油气燃烧 D.干冰升华
2.“推动绿色发展、建设美丽中国”是当前工作重点。下列做法不符合这一要求的是( )
A.农业上合理使用农药化肥 B.焚烧方法处理塑料垃圾
C.不任意排放工业废水 D.推广使用清洁能源
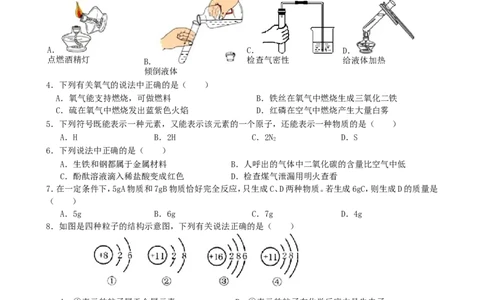
3.下列实验基本操作正确的是( )
A. C. D.
点燃酒精灯 B. 检查气密性 给液体加热
倾倒液体
4.下列有关氧气的说法中正确的是( )
A.氧气能支持燃烧,可做燃料 B.铁丝在氧气中燃烧生成三氧化二铁
C.硫在氧气中燃烧发出蓝紫色火焰 D.红磷在空气中燃烧产生大量白雾
5.下列符号既能表示一种元素,又能表示该元素的一个原子,还能表示一种物质的是( )
A.H B.2H C.2N D.S
2
6.下列说法中正确的是( )
A.生铁和钢都属于金属材料 B.人呼出的气体中二氧化碳的含量比空气中低
C.酚酞溶液滴入稀盐酸变成红色 D.检查煤气泄漏用明火查看
7.在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是
( )
A.5g B.6g C.7g D.4g
8.如图是四种粒子的结构示意图,下列有关说法正确的是( )
A.④表示的粒子属于金属元素 B.①表示的粒子在化学反应中易失电子
C.①②③④表示四种不同元素 D.②④所表示的粒子化学性质相似
9.下列物质的名称、俗称、化学式和分类对应完全正确的一组是( )
A.氧化钙、熟石灰、CaO、氧化物 B.氯化氢、盐酸、HCl、酸
C.氢氧化钠、火碱、NaOH、碱 D.碳酸氢钠、苏打、NaHCO、盐
3
10.下列食物中富含蛋白质的是( )
A.鸡蛋 B.小米粥 C.黄瓜 D.馒头
11.农作物出现倒伏现象,应该施用下列化肥中的( )
A.尿素 B.硝酸铵 C.碳酸钾 D.磷酸二氢铵
12.下表是对部分知识的归纳,其中完全正确的一组是( )
1A B
用燃烧的方法区分羊毛和涤纶 闻到花香是因为分子不断运动
用品尝的方法区分糖水和石灰水 催化剂只能加快化学反应速率
用肥皂水区分软水和硬水 洗涤剂能洗涤油污是因为它有乳化功能
C D
用工业酒精勾兑白酒 煤、石油、天然气是三大化石燃料
用小苏打做糕点膨松剂 塑料、合成纤维、合成橡胶是三大合成材料
用硫酸铜做游泳池消毒剂 分子、原子、离子是构成物质的三种基本粒子
13.对化学反应A + B = C + D的下列说法中正确的是( )
A.若A是稀硫酸,则生成物质中一定有水
B.若C、D是盐和水,则A、B不一定是酸和碱
C.若A是可溶性碱,B是可溶性盐,则C、D不可能是两种沉淀
D.若A、B、C、D都是化合物,则该反应不一定是复分解反应
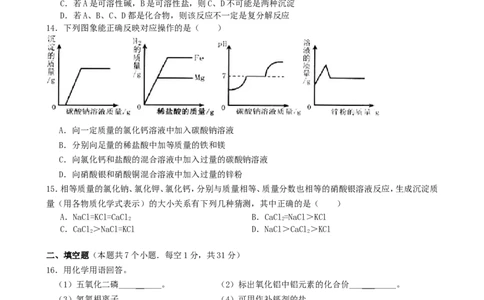
14.下列图象能正确反映对应操作的是( )
A.向一定质量的氯化钙溶液中加入碳酸钠溶液
B.分别向足量的稀盐酸中加等质量的铁和镁
C.向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液
D.向硝酸银和硝酸铜混合溶液中加入过量的锌粉
15.相等质量的氯化钠、氯化钾、氯化钙,分别与质量相等、质量分数也相等的硝酸银溶液反应,生成沉淀质
量(用各物质化学式表示)的大小关系有下列几种猜测,其中正确的是( )
A.NaCl=KCl=CaCl B.CaCl=NaCl>KCl
2 2
C.CaCl>NaCl=KCl D.NaCl>CaCl>KCl
2 2
二、填空题(本题共7个小题.每空1分,共31分)
16.用化学用语回答。
(1)五氧化二磷____ ____。 (2)标出氧化铝中铝元素的化合价___ _____。
(3)氢氧根离子___ _____。 (4)可用作补钙剂的盐___ _____。
17.化学与人类生产、生活息息相关,请回答下列问题。
(1)烧水用的水壶其手柄所用的塑料应具有____ ____。(填“热固性”或“热塑性”)
(2)体温计中的金属是________。
(3)森林着火,设置防火隔离带,其灭火原理是____ ____。
(4)爱护水资源,一方面要防治水体污染,另一方面要____ ____。
(5)生活中常用来降低水硬度的方法是_____ ___。
18.金属在生产、生活中有广泛应用。
(1)我国深水钻井平台“981”用钢量达3万吨,露出平台的钢、铁很容易生锈,钢铁生锈的条件
是_____ _ __,写出一种防止钢铁生锈的方法_____ ___。
2(2)写出用盐酸除去铁制品表面铁锈的化学方程式___ _____。
(3)硫酸铜、硫酸亚铁的混合溶液中加入一定量镁粉,充分反应后过滤,得到滤渣和滤液。若滤液呈
无色,则滤渣中一定含有的金属是____ ____。
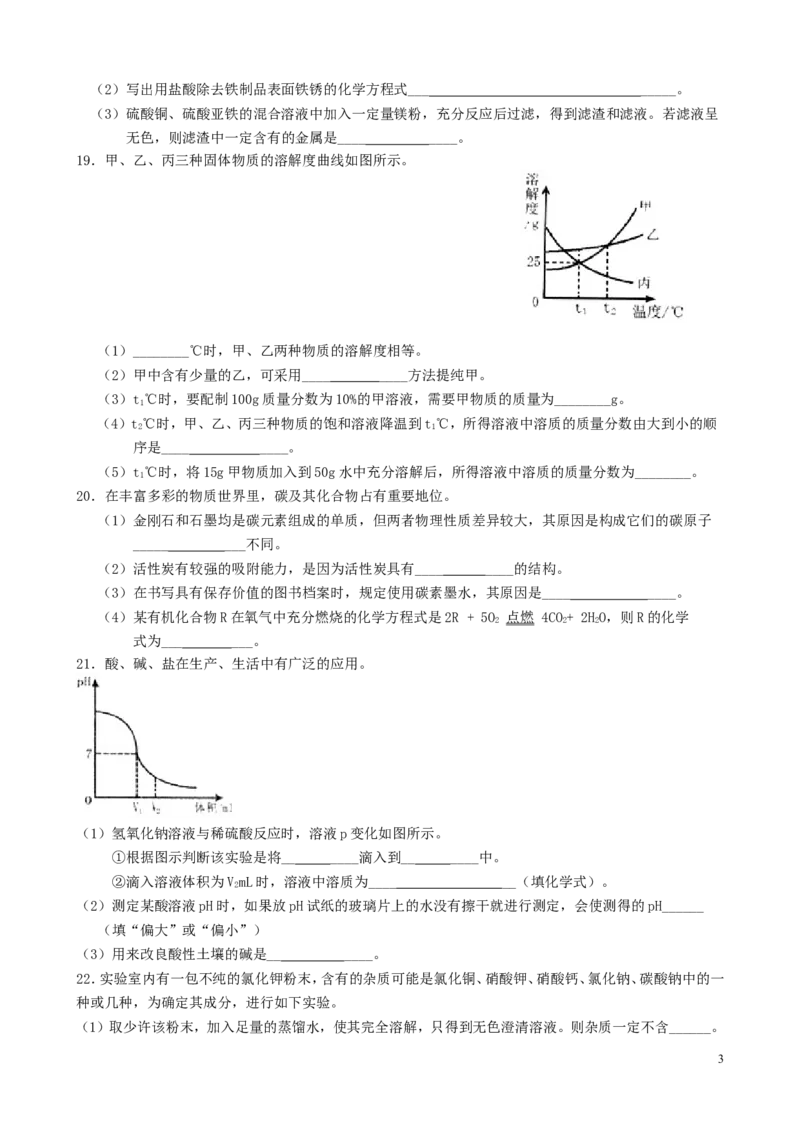
19.甲、乙、丙三种固体物质的溶解度曲线如图所示。
(1)________℃时,甲、乙两种物质的溶解度相等。
(2)甲中含有少量的乙,可采用____ ____方法提纯甲。
(3)t℃时,要配制100g质量分数为10%的甲溶液,需要甲物质的质量为________g。
1
(4)t℃时,甲、乙、丙三种物质的饱和溶液降温到t℃,所得溶液中溶质的质量分数由大到小的顺
2 1
序是____ ____。
(5)t℃时,将15g甲物质加入到50g水中充分溶解后,所得溶液中溶质的质量分数为________。
1
20.在丰富多彩的物质世界里,碳及其化合物占有重要地位。
(1)金刚石和石墨均是碳元素组成的单质,但两者物理性质差异较大,其原因是构成它们的碳原子
_____ ___不同。
(2)活性炭有较强的吸附能力,是因为活性炭具有____ ____的结构。
(3)在书写具有保存价值的图书档案时,规定使用碳素墨水,其原因是____ ____。
(4)某有机化合物R在氧气中充分燃烧的化学方程式是2R + 5O 点燃 4CO+ 2HO,则R的化学
2 2 2
式为___ ___。
21.酸、碱、盐在生产、生活中有广泛的应用。
(1)氢氧化钠溶液与稀硫酸反应时,溶液p变化如图所示。
①根据图示判断该实验是将__ ____滴入到__ ____中。
②滴入溶液体积为VmL时,溶液中溶质为____ __(填化学式)。
2
(2)测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH______
(填“偏大”或“偏小”)
(3)用来改良酸性土壤的碱是__ ____。
22.实验室内有一包不纯的氯化钾粉末,含有的杂质可能是氯化铜、硝酸钾、硝酸钙、氯化钠、碳酸钠中的一
种或几种,为确定其成分,进行如下实验。
(1)取少许该粉末,加入足量的蒸馏水,使其完全溶解,只得到无色澄清溶液。则杂质一定不含______。
3(2)取(1)中无色溶液加入BaCl2溶液,产生白色沉淀,则杂质一定含有___ ___。
(3)另称取14.9g该粉末于烧杯中,加入蒸馏水使其完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分
反应后生成28.7g白色沉淀,则杂质还一定含有___ ___。通过以上三个实验还不能确定含有
的杂质是___ ___。
三、实验与探究(本题共4个小题.每空1分,共28分)
23.如图是实验室制取气体的相关装置,请回答下列问题。
(1)①仪器的名称是___ ___。
(2)实验室用高锰酸钾制取氧气。若要收集一瓶较纯净的氧气,应选择的发生装置和收集装置是______
(填装置对应的字母,下同)该反应的化学方程式是___ ___,
反应的基本类型是__ ____。
(3)实验室制取二氧化碳,应选择的发生装置是__ ____。若用C装置收集二氧化碳气体,验满
方法是__ ____。
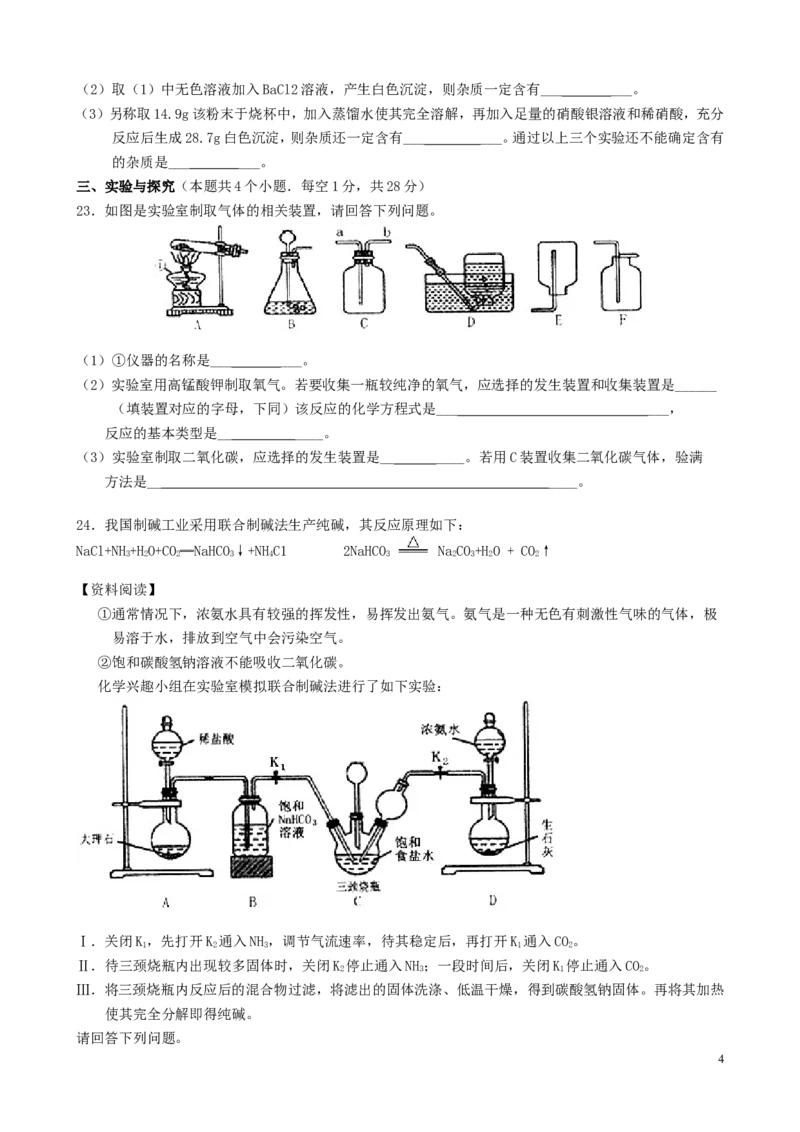
24.我国制碱工业采用联合制碱法生产纯碱,其反应原理如下:
NaCl+NH+HO+CO═NaHCO↓+NHC1 2NaHCO NaCO+HO + CO↑
3 2 2 3 4 3 2 3 2 2
【资料阅读】
①通常情况下,浓氨水具有较强的挥发性,易挥发出氨气。氨气是一种无色有刺激性气味的气体,极
易溶于水,排放到空气中会污染空气。
②饱和碳酸氢钠溶液不能吸收二氧化碳。
化学兴趣小组在实验室模拟联合制碱法进行了如下实验:
Ⅰ.关闭K,先打开K 通入NH,调节气流速率,待其稳定后,再打开K 通入CO。
1 2 3 1 2
Ⅱ.待三颈烧瓶内出现较多固体时,关闭K 停止通入NH;一段时间后,关闭K 停止通入CO。
2 3 1 2
Ⅲ.将三颈烧瓶内反应后的混合物过滤,将滤出的固体洗涤、低温干燥,得到碳酸氢钠固体。再将其加热
使其完全分解即得纯碱。
请回答下列问题。
4(1)写出A装置中反应的化学方程式____ __。
(2)B装置中饱和碳酸氢钠溶液的作用是___ ___。
(3)D装置中生石灰的作用是___ ___。
(4)C装置中长颈漏斗的作用除了随时添加饱和食盐水,还有___ ___作用。
有同学认为应该在长颈漏斗内放置浸有稀硫酸的棉花团,其目的是__ ____。
(5)关闭K 停止通入NH,还要继续通入一段时间CO,其目的是___ ___。
2 3 2
(6)写出副产品氯化铵和熟石灰反应的化学方程式___ ___。
25.实验室有失去标签的两瓶无色溶液,分别是氢氧化钡溶液和稀硫酸。为了鉴别它们设计如下鉴别方法:
先把两瓶溶液分别贴上标签A、B,然后进行实验。
加入的试剂 实验现象 实验结论
A中无明显现象
方法1 锌粒
B中产生气泡
A是_ _ ____溶液;
B是___ ___溶液
A中___ ___;
方法2 碳酸钠溶液
B中___ ___。
化学小组同学对方法2进一步探究,设计了如下实验方案
溶液C和溶液D混合,可能有以下三种情况:
(1)若有气泡产生,写出反应的化学方程式___ ___;
(2)若有沉淀产生,通过现象可推出溶液C中的溶质是___ ___;
(3)若无明显现象,混合物E中所含溶质种类最多时,写出所有溶质的化学式___ ___。
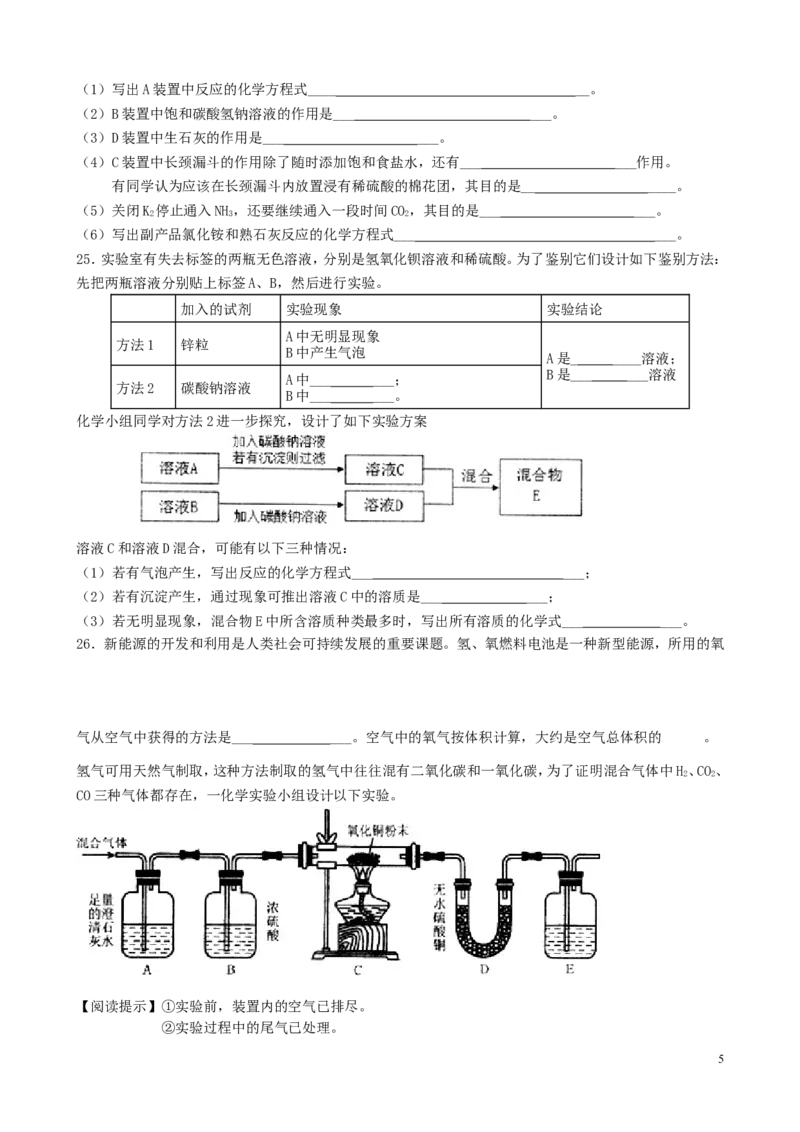
26.新能源的开发和利用是人类社会可持续发展的重要课题。氢、氧燃料电池是一种新型能源,所用的氧
气从空气中获得的方法是___ ___。空气中的氧气按体积计算,大约是空气总体积的 。
氢气可用天然气制取,这种方法制取的氢气中往往混有二氧化碳和一氧化碳,为了证明混合气体中H、CO、
2 2
CO三种气体都存在,一化学实验小组设计以下实验。
【阅读提示】①实验前,装置内的空气已排尽。
②实验过程中的尾气已处理。
5③无水硫酸铜是白色粉末,吸水后变蓝。
请回答下列问题。
(1)A装置的作用是__ ____。
(2)C装置中的实验现象是__ ____。
(3)E装置中盛放的试剂应该是__ ,该装置中发生反应的化学方程式为___ ___。
(4)证明氢气存在的实验现象是___ ___。
(5)另一小组同学利用上述实验装置(把其中的E装置换成装有碱石灰的干燥管),仿照上述实验过程,通
过定量的方法确定一氧化碳存在,记录实验数据如下:
(注:反应生成的水蒸气被D装置完全吸收,不考虑其他水蒸气对实验结果的影响)
实验前C装置玻璃管内固体总质量/g m
1
实验后C装置玻璃管内固体总质量/g m
2
实验前D装置总质量/g n
1
实验后D装置总质量/g n
2
利用如表数据,计算出能证明CO存在的质量关系是___ ___。(用m、m、n、n 表示)
1 2 1 2
四、计算题(本题共2个小题.27题4分,28题7分,共11分)
27.蛋白质是由丙氨酸(CHNO)等多种氨基酸构成的。根据丙氨酸的化学式计算:
3 7 2
(1)CHNO 的相对分子质量是___ ___。
3 7 2
(2)丙氨酸中各元素的质量比C:H:N:O=___ ___。
(3)丙氨酸中氮元素的质量分数为__ ____(结果保留0.1%)
(4)8.9g CHNO 中含有氢元素的质量是____ __g。
3 7 2
28.为测定硫酸钠和硫酸镁固体混合物中硫酸镁的质量分数。某同学取固体混合物26.2g,向其中加入
219.6g水,使其完全溶解配制成混合溶液。将200g一定溶质质量分数的氢氧化钠溶液平均分成5等份,依
次加入到上述混合溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下表:
次数 第一次 第二次 第三次 第四次 第五次
氢氧化钠溶液质量/g 40 40 40 40 40
产生沉淀质量/g 1.45 2.9 m 5.8 5.8
试分析计算。
(1)m的值为 __ ____。
(2)固体混合物中硫酸镁的质量分数。(结果保留0.1%)
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数。
2019年黑龙江省绥化市中考化学试卷答案
1、C。2、B。3. C。4. C。5. D。6. A。7. B。8. A。9. C。10. A。
11. C。12. D。13. BD。14. C。15. AB。
16.(1)PO; (2) ; (3)OH-; (4)CaCO。
2 5 3
17.(1)热固性; (2)汞; (3)移除可燃物; (4)节约用水; (5)煮沸。
18.(1)潮湿的空气;在钢铁表面涂油、刷漆等涂上保护层;保持钢铁干燥等; (2)
; (3)铜和铁。
19.(1)t2; (2)降温结晶; (3)10; (4)乙>甲>丙; (5)20%。
620. (1)排列方式; (2)疏松多孔; (3)碳在常温下化学性质不活泼; (4)CH。
2 2
21.(1)①稀硫酸;氢氧化钠溶液;②HSO、NaSO; (2)偏大; (3)氢氧化钙。
2 4 2 4
22.氯化铜、硝酸钙,碳酸钠,氯化钠,硝酸钾。
三、(1)酒精灯; (2)AF或AD; ;是分解反应; (3)B;把燃着的木
条放在集气瓶口,若木条熄灭,则集满。
24.(1)CaCO+2HCl=CaCl+HO+CO↑; (2)除去二氧化碳中的氯化氢气体; (3)氧化钙和水反应产生热量使
3 2 2 2
氨气的挥发加快; (4)平衡气压的作用;吸收氨气,防止其污染空气; (5)尽可能多的吸收二氧化碳增大碳
酸氢钠的产率; (6)NHCl+Ca(OH)=CaCl+2HO+2NH↑。
4 2 2 2 3
25.
(1) ; (2)氢氧化钠、氢氧化钡 ;
(3)
26.分离液态空气法; 1/ 5 ; (1)验证二氧化碳并除去; (2)黑色粉末变成红色; (3)澄清石灰水;
; (4)无水硫酸铜变蓝色; (5) 。
27.(1)89; (2)36:7:32:14; (3)15.7%;(4)0.7。
28.【解答】解:根据前四次,每次对应的沉淀的质量为1.45g,所以第三次的m=1.45×4=4.35,且第四次为
恰好完全反应。 设硫酸镁的质量为x,生成的硫酸钠的质量为y
7恰好完全反应时,所得不饱和溶液中溶质的质量分数为
故答案为: (1)4.35; (2)45.8%; (3)7.1%。
8