文档内容
机密★启用前 试卷类型A
山东名校考试联盟
2025-2026学年高三年级开学摸底考试
化 学 试 题
2025.9
注意事项:
1.答题前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号;回答非选择题时,将答案写在答题卡上,写在本
试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C 12 N 14 O16 Ce 140
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.“国之重器”是我国科技综合实力的结晶。下述材料不属于有机高分子材料的是
A.“望宇”登月服用的聚酰亚胺隔热层 B.“雪龙2”号破冰船制淡水用的反渗透膜
C.“815A”型电子侦察船用的氮化镓雷达 D.“东福一号”制氢平台用的聚四氟乙烯材料
2.下列有关物质用途的说法错误的是
A.生石灰可用作脱氧剂 B.碳酸氢铵可用作食品膨松剂
C.硫酸铝可用作净水剂 D.乙二醇溶液可用作汽车防冻液
3.下列实验事故的处理方法不合理的是
实验事故 处理方法
A 金属K 着火 用灭火毯盖灭
B 温度计中水银洒落地面 用硫粉覆盖
C 苯酚不慎沾到手上 先用乙醇冲洗,再用水冲洗
D 稀释浓硫酸时,酸溅到皮肤上 用3%-5%的 NaHCO₃ 溶液冲洗
4.实验室将粗盐提纯并配制 0.1000 mol·L⁻¹ 的 NaCl溶液。下列仪器中不需要使用的
A.分液漏斗 B.烧杯 C.酒精灯 D.蒸发皿
化学试题 第1页 (共8页)
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}5.下列实验涉及反应的离子方程式书写正确的是
A.用稀硫酸溶解少量 Fe粉:
B.用稀硝酸溶解少量 Cu粉:
C.向 悬浊液中加入 NaOH溶液:
D.用 NaOH 浓溶液检验 溶液中的
6.科学家通过核反应 发现氚(H)。下列说法正确的是
A. n表示一个质子
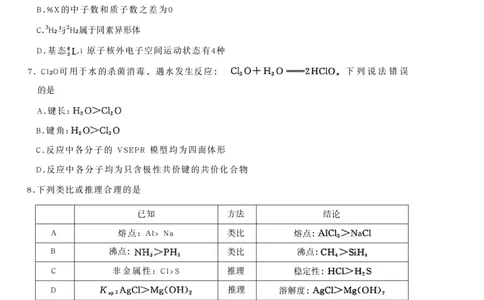
B.%X的中子数和质子数之差为0
C.³H₂与²H₂属于同素异形体
D.基态 Li 原子核外电子空间运动状态有4种
7. Cl₂O可用于水的杀菌消毒,遇水发生反应: 下 列 说 法 错 误
的是
A.键长:
B.键角:
C.反应中各分子的 VSEPR 模型均为四面体形
D.反应中各分子均为只含极性共价键的共价化合物
8.下列类比或推理合理的是
已知 方法 结论
A 熔点: Al> Na 类比 熔点:
B 沸点: 类比 沸点:
C 非金属性: Cl>S 推理 稳定性:
D 推理 溶解度:
9.科学家发现某些生物酶体系可以促进H⁺和e⁻ 的转移(如a、b和c),能将海洋中的NO₂ 转
化为N₂进入大气层,反应过程如图所示。下列说法错误的是
A.过程I中 NO是还原反应的产物
B.过程Ⅱ中溶液的pH减小
C.过程Ⅲ中 N₂H₄是还原剂
D.过程I→Ⅲ的总反应为
化学试题 第2页 (共8页)
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}10. SCl₂和O₂ 制备SOCl₂ 的相关反应如下,T℃时,反应在密闭体系中达平衡时各组分摩尔
分数随 的变化关系如图所示。
已知:
下列说法错误的是
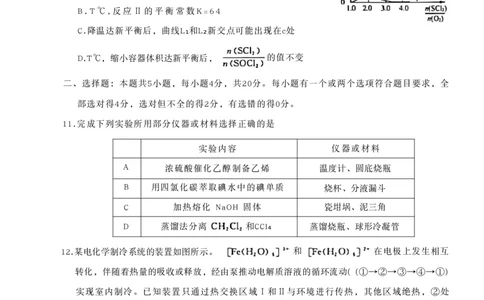
A.曲线L₁表示 SCl₂摩尔分数随 的变化
B.T℃,反应Ⅱ的平衡常数K=64
C.降温达新平衡后,曲线L₁和L₂新交点可能出现在c处
D.T℃,缩小容器体积达新平衡后, 的值不变
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全
部选对得4分,选对但不全的得2分,有选错的得0分。
11.完成下列实验所用部分仪器或材料选择正确的是
实验内容 仪器或材料
A 浓硫酸催化乙醇制备乙烯 温度计、圆底烧瓶
B 用四氯化碳萃取碘水中的碘单质 烧杯、分液漏斗
C 加热熔化 NaOH 固体 瓷坩埚、泥三角
D 蒸馏法分离 和CCl₄ 蒸馏烧瓶、球形冷凝管
12.某电化学制冷系统的装置如图所示。 和 在电极上发生相互
转化,伴随着热量的吸收或释放,经由泵推动电解质溶液的循环流动( (①→②→③→④→①)
实现室内制冷。已知装置只通过热交换区域Ⅰ和Ⅱ与环境进行传热,其他区域绝热,②处
的电解液温度比①处的低。下列说法错误的是
A. a为电源正极
B.多孔隔膜为阴离子交换膜
C.热交换区域Ⅱ应置于室内
D.阳极反应为
化学试题 第3页 ( 共 8 页 )
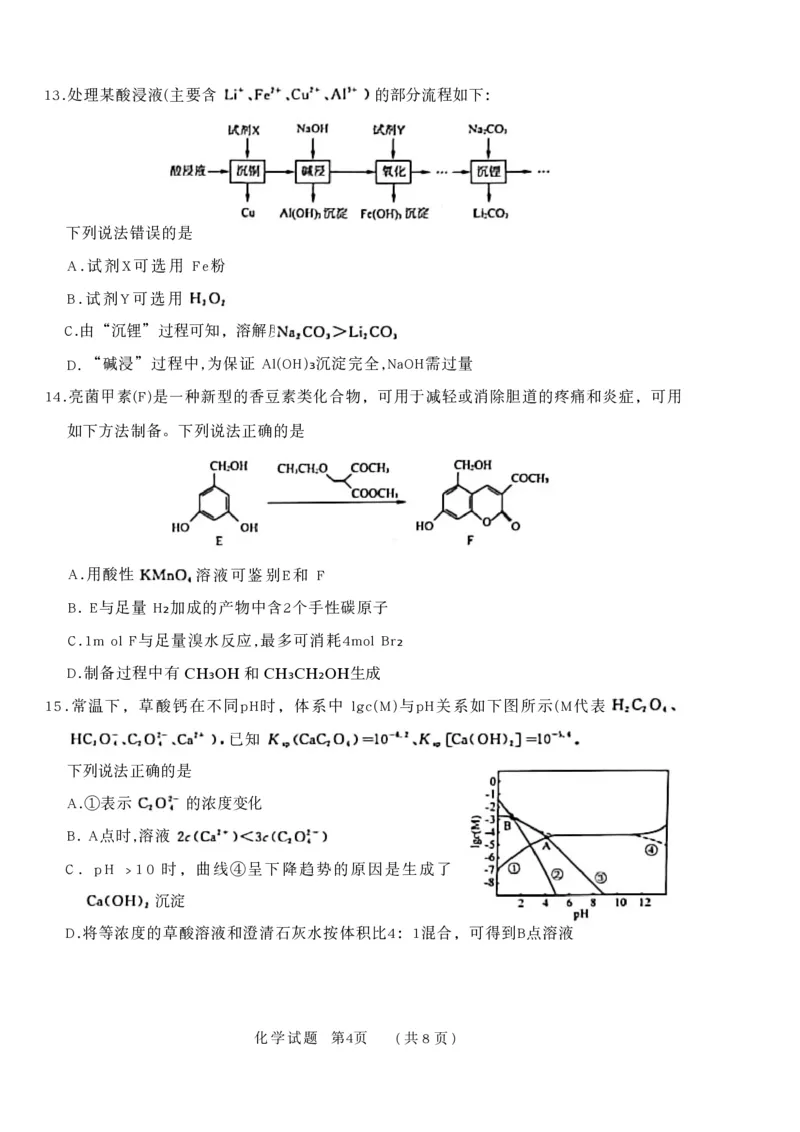
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}13.处理某酸浸液(主要含 的部分流程如下:
下列说法错误的是
A.试剂X可选用 Fe粉
B.试剂Y可选用
C.由“沉锂”过程可知,溶解度:
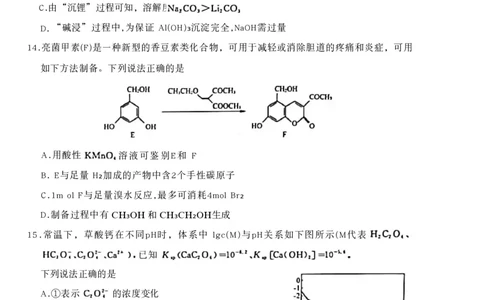
D. “碱浸”过程中,为保证 Al(OH)₃沉淀完全,NaOH需过量
14.亮菌甲素(F)是一种新型的香豆素类化合物,可用于减轻或消除胆道的疼痛和炎症,可用
如下方法制备。下列说法正确的是
A.用酸性 溶液可鉴别E和 F
B. E与足量 H₂加成的产物中含2个手性碳原子
C.1m ol F与足量溴水反应,最多可消耗4mol Br₂
D.制备过程中有 CH₃OH 和 CH₃CH₂OH生成
15.常温下,草酸钙在不同pH时,体系中 lgc(M)与pH关系如下图所示(M代表
已知
下列说法正确的是
A.①表示 的浓度变化
B. A点时,溶液
C. pH >10 时,曲线④呈下降趋势的原因是生成了
沉淀
D.将等浓度的草酸溶液和澄清石灰水按体积比4:1混合,可得到B点溶液
化学试题 第4页 ( 共 8 页 )
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}三、非选择题:本题共5小题,共60分。
16.(12分)全固态锂电池凭借其本质安全性和理论高能量密度,已成为下一代储能体系的核
心发展方向,而无机固态电解质在其中扮演着关键角色。
回答下列问题:
(1)在阴极侧,自愈合涂层 显著缓解高镍正极与硫化物的副反应。Nb原子序号
为41,在元素周期表中的位置为 ,基态 价层电子排布式为 。
(2) Ni可形成 Ni(CO)₄、 等多种配合物。
①Ni(CO)₄中含有σ键与π键的数目之比为 , Ni(CO)₄中CO 的三键键长
(填“>”“<”或“=”)游离态CO的三键键长,可能的原因为 ;
组成元素中,第一电离能最大的是 (填元素符号),
的空间构型为 。
四方晶胞结构如图所示,晶胞参数分别为a、a、
c pm,晶体密度为 设 为阿伏加德罗常数的值。
①则 的摩尔质量为 (用含ρ、a、c
和 代数式表示);
②晶胞中 Li和 Nb的配位数之比为 。
17.(12分)二氧化铈可用在化妆品中起到抗紫外线作用,某工业以炼铈废渣 含
等杂质)为原料制备 二氧化铈,同时提炼 Co和Zn,其工艺流程
如图所示:
已知:①“氧化焙烧”时得固态氧化物有 ZnO和 不溶于硫酸,也
不溶于NaOH 溶液;
( ;当
离子浓度 可认为沉淀完全。
回答下列问题:
发生“氧化焙烧”时化学方程式为 ,此时气体与矿料逆流而行进行投
料,目的是 。
化学试题 第5页 ( 共 8 页 )
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}(2)“二次焙烧”过程中,理论上氧化剂与还原剂的物质的量之比为 。“滤渣Ⅰ”中
加入浓盐酸溶解的缺点是 。
(3)“溶液Ⅱ”中 (图a)与铈的沉淀率关系如图所示:
根据图分析:沉铈时应选择最佳条件为 。
经充分“焙烧”质量减少2.9t,则获得 的质
量为 t。
(4)“调pH”操作中加入物质X的最佳试剂为
(填标号),调pH约为5,再加入 氧化,则 发生
反应的离子方程式为 ,随着反应的进行,还要分批加入少量物质X。
A.氨水
18.(12分)苯胺乙酰化常用来保护苯环上的氨基使其不易被氧化,且使苯环上取代反应由多
元取代变为有用的一元取代,同时使对位的反应活性较邻位高。实验室制备乙酰苯胺原
理:
步骤如下:
Ⅰ.制备:装置如图(部分加热、夹持装置已略去)。在蒸馏瓶中依次放入
5mL新蒸馏过的苯胺、7.4mL冰醋酸和0.1g 锌粉,小火加热,使分馏柱顶温
度计示数保持在 左右。当温度计读数发生上下波动或自行下降时停止
加热;
Ⅱ.分离:在不断搅拌下,把反应混合物趁热倒入盛有100mL水的烧杯中,
搅拌并冷却,使粗乙酰苯胺析出。抽滤析出的固体并冷水洗涤;
Ⅲ.提纯:把粗乙酰苯胺加入150mL热水中加热至沸腾。稍冷后加入0.5g活性炭,煮沸
1~2分钟。趁热减压过滤,冷却滤液。乙酰苯胺呈无色片状晶体析出。产物晾干后称重并测
熔点。
已知:
名称 性状 熔点 沸点
苯胺 无色油状有强烈气味液体、有毒 - 6 . 2 118.13
冰醋酸 无色刺激性液体 16.7 118
乙酰苯胺 白色晶体 114~116 305
化 学 试 题第6页 ( 共 8 页 )
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}回答下列问题:
(1)加入锌粉的作用是 。.
(2)写出乙酰苯胺与溴发生取代反应的主要反应方程式 。
(3)刺形分馏柱的作用为 ,锥形瓶中收集的主要物质为 。
(4)分离步骤中把反应混合物趁热倒入烧杯中的原因 。
(5)设定如下操作测定乙酰苯胺样品纯度:
取m g乙酰苯胺样品,溶于 溶液并加热,充分反应后,经分
液处理,配成500mL溶液,取25.00mL于锥形瓶中,加入指示剂X,并用 盐
酸滴定剩余的 NaOH,重复滴定3次,平均每次消耗标准液20.00 mL。
①指示剂X为 (填“甲基橙”或“酚酞”);
②样品中乙酰苯胺的质量分数为 (含m 计算式表示),下列情况会导致乙酰苯胺
的质量分数偏大的是 (填标号)。
A.配成500 mL溶液时忘记冷却
B.用碱式滴定管移取25.00 mL溶液读数时,先俯视后仰视
C.没有用盐酸标准液润洗滴定管
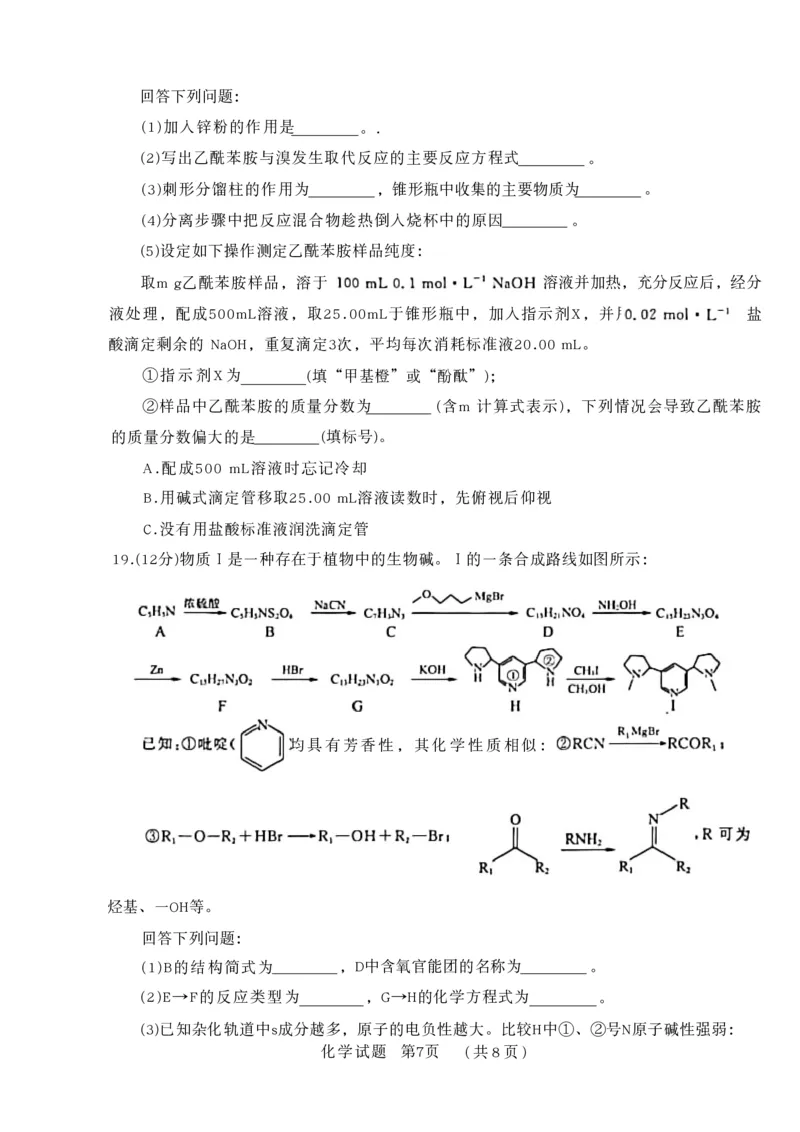
19.(12分)物质Ⅰ是一种存在于植物中的生物碱。Ⅰ的一条合成路线如图所示:
◯)与苯均具有芳香性,其化学性质相似:
烃基、一OH等。
回答下列问题:
(1)B的结构简式为 ,D中含氧官能团的名称为 。
(2)E→F的反应类型为 ,G→H的化学方程式为 。
(3)已知杂化轨道中s成分越多,原子的电负性越大。比较H中①、②号N原子碱性强弱:
化学试题 第7页 (共8页)
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}① ②(填“>”“<”或“=”)。H→I的反应过程中,需要加入少量KOH,其原因是 。
(4)物质M(C₇H₃N)是A的同系物,则M具有芳香性的同分异构体有 种(包含
M本身)。
( 5 ) 以 和 为原料,设计合成 的路
线(无机试剂任选)。
20.(12分)新型碳还原白云石(MgO·CaO)炼镁工艺分为“炼镁”和部分碳化钙“再生”两阶
段,对应的主要反应如下:
反应①:
反应②:
反应③:
回答下列问题:
(1)反应②的
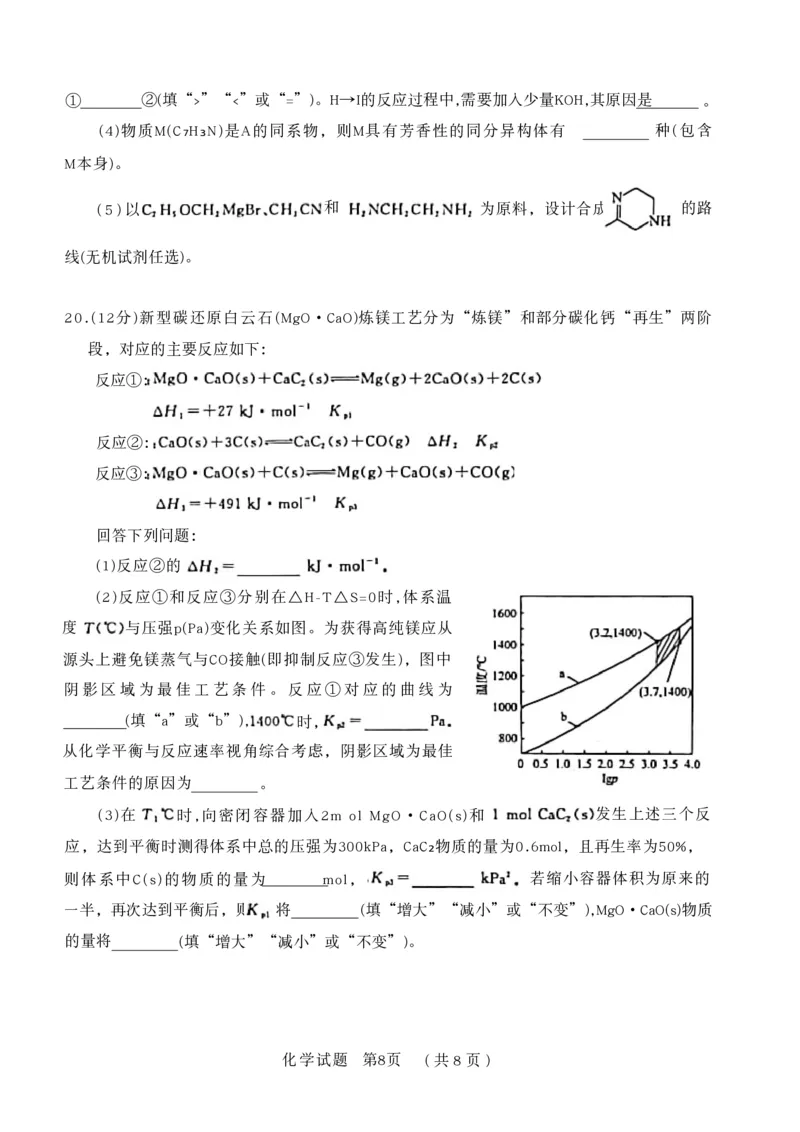
(2)反应①和反应③分别在△H-T△S=0时,体系温
度 与压强p(Pa)变化关系如图。为获得高纯镁应从
源头上避免镁蒸气与CO接触(即抑制反应③发生),图中
阴 影 区 域 为 最 佳 工 艺 条 件 。 反 应 ① 对 应 的 曲 线 为
(填“a”或“b”),在 时,
从化学平衡与反应速率视角综合考虑,阴影区域为最佳
工艺条件的原因为 。
(3)在 时,向密闭容器加入2m ol MgO·CaO(s)和 发生上述三个反
应,达到平衡时测得体系中总的压强为300kPa,CaC₂物质的量为0.6mol,且再生率为50%,
则体系中C(s)的物质的量为 mol, 若缩小容器体积为原来的
一半,再次达到平衡后,则 将 (填“增大”“减小”或“不变”),MgO·CaO(s)物质
的量将 (填“增大”“减小”或“不变”)。
化学试题 第8页 ( 共 8 页 )
{#{QQABCQE1wgiQkBbACD5qQ02YCUqQkICjLYoERUCauA4LyBFAFIA=}#}