文档内容
高途高中·化学
点睛卷
2024
重庆市-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024 年重庆市普通高中学业水平选择性考试模拟测试卷
化 学
本试卷共9页,18小题,满分100分,考试用时75分钟
可能用到的相对原子质量:
H-1 C-12 B-11 N-14 O-16 Na-23 Mg-24 Cl-35.5 K-39 Fe-56 Sn-119
一、选择题:本题共 14小题,每小题 3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.预计于2023年发射的中国空间站望远镜运行后将成为太空中最大的望远镜。下列有关叙述错误的是
A.主镜材料为密度小,性能好的金属铍,铍元素在元素周期表中位于第二周期ⅡA族
B.望远镜需要避免太阳辐射,制作遮阳帆的聚酰亚胺薄膜属于有机高分子材料
C.望远镜需要超低温环境,主动冷却器用氦制冷,氦的分子间作用力很弱,沸点极低
D.望远镜工作的推进剂为N H 和N O ,N O 本身的颜色会随温度升高变为红棕色
2 4 2 4 2 4
2.高铁酸钠(Na FeO )是一种新型净水剂,可用于饮用水处理。湿法制高铁酸钠的反应原理为
2 4
2Fe(OH) +3NaClO+4NaOH=2Na FeO +3NaCl+5H O。下列有关说法不正确的是
3 2 4 2
A.H O的球棍模型为 B.基态Fe3+的简化电子排布式为[Ar]3d34s2
2
C.NaClO的电子式为 D.37Cl原子结构示意图为
3.宏观辨识与微观探析是化学学科核心素养之一,下列化学变化对应的离子方程式正确的是
A.用FeCl3 溶液腐蚀覆铜板的反应:2Fe3++3Cu=3Cu2++2Fe
B.丙醛与银氨溶液反应:C2H5CHO+2[Ag(NH3)2]++2OH ﹣ C2H5COO ﹣ +NH
4
++2Ag↓+3NH3+H2O
C.用氢氟酸生产磨砂玻璃的反应:SiO2+4H++4F ﹣=SiF4 ↑+2H2O
D.向NaHSO4 溶液加入适量Ba(OH)2 溶液至SO
4
2-恰好完全沉淀:2H++2OH ﹣ +SO
4
2-+Ba2+=BaSO4 ↓+2H2O
4.N 是阿伏加德罗常数的值。利用反应2NH NaClON H NaClH O可制火箭推进器的燃料N H 。
A 3 2 4 2 2 4
下列说法正确的是
A.常温下,22.4LNH 含有的中子数为7N
3 A
B.室温下,pH=10的NaClO溶液中由水电离出的OH数目为104N
A
C.3.2gN H 中极性共价键的数目为0.2N
2 4 A
D.每生成3.6gH O时,该反应转移电子数为0.4N
2 A
试卷第2页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
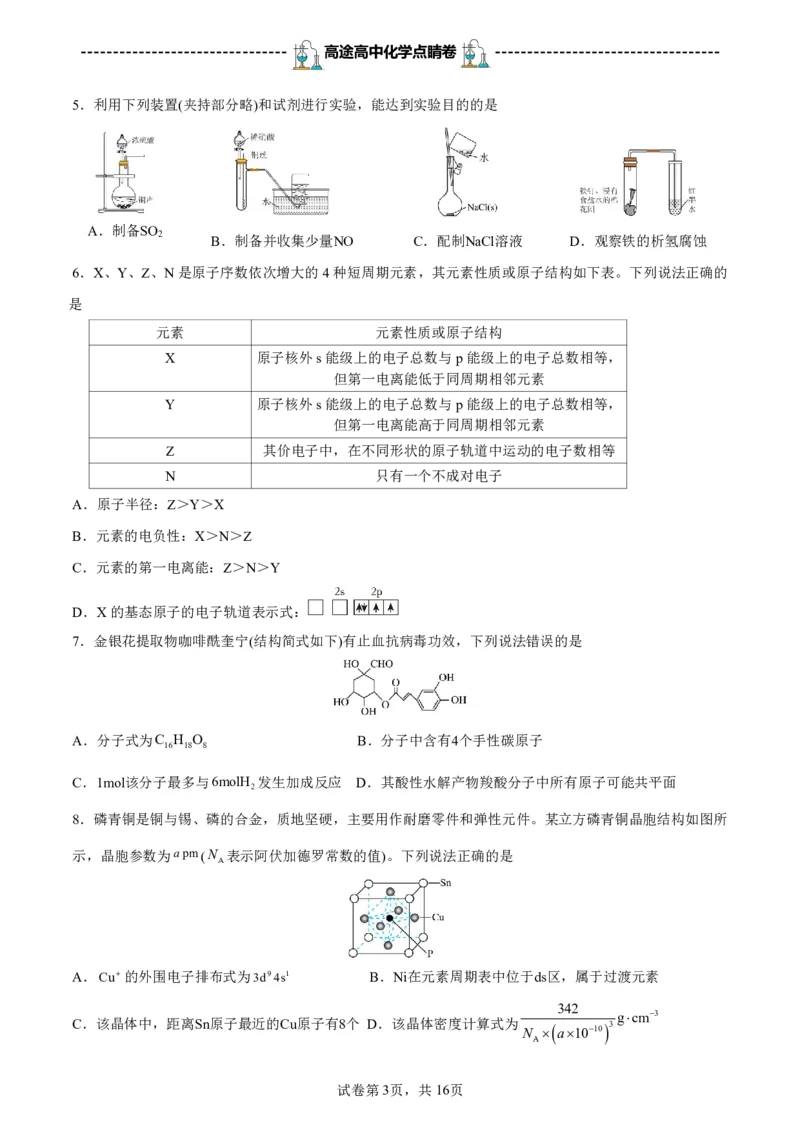
5.利用下列装置(夹持部分略)和试剂进行实验,能达到实验目的的是
A.制备SO
2 B.制备并收集少量NO C.配制NaCl溶液 D.观察铁的析氢腐蚀
6.X、Y、Z、N是原子序数依次增大的4种短周期元素,其元素性质或原子结构如下表。下列说法正确的
是
元素 元素性质或原子结构
X 原子核外s能级上的电子总数与p能级上的电子总数相等,
但第一电离能低于同周期相邻元素
Y 原子核外s能级上的电子总数与p能级上的电子总数相等,
但第一电离能高于同周期相邻元素
Z 其价电子中,在不同形状的原子轨道中运动的电子数相等
N 只有一个不成对电子
A.原子半径:Z>Y>X
B.元素的电负性:X>N>Z
C.元素的第一电离能:Z>N>Y
D.X的基态原子的电子轨道表示式:
7.金银花提取物咖啡酰奎宁(结构简式如下)有止血抗病毒功效,下列说法错误的是
A.分子式为C H O B.分子中含有4个手性碳原子
16 18 8
C.1mol该分子最多与6molH 发生加成反应 D.其酸性水解产物羧酸分子中所有原子可能共平面
2
8.磷青铜是铜与锡、磷的合金,质地坚硬,主要用作耐磨零件和弹性元件。某立方磷青铜晶胞结构如图所
示,晶胞参数为apm(N 表示阿伏加德罗常数的值)。下列说法正确的是
A
A.Cu的外围电子排布式为3d94s1 B.Ni在元素周期表中位于ds区,属于过渡元素
342
C.该晶体中,距离Sn原子最近的Cu原子有8个 D.该晶体密度计算式为
N
a10103
gcm3
A
试卷第3页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
9.下列实验中,实验现象与结论相匹配的是
实验操作 实验现象 结论
向NaBr溶液中滴加过量氯水,再加入淀粉
A 溶液先变橙色,后变蓝色 氧化性:Cl Br I
KI溶液 2 2 2
在Na SO 饱和溶液中滴加稀硫酸,将产生 该气体产物具有还原
B 2 3 KMnO 溶液褪色
的气体通入KMnO 溶液中 4 性
4
向蔗糖溶液中滴加稀硫酸,加热,再加入 蔗糖在酸性条件下未
C 无银镜现象
银氨溶液并水浴加热 发生水解反应
常温下,用酚酞测定等物质的量浓度的 NaClO溶液变红,NaCl
D 酸性:HClOHCl
NaCl和NaClO溶液的碱性 溶液不变色
10.X YZ 常用作还原剂,X、Y和Z均为短周期元素,X的单质在空气中燃烧得到淡黄色固体,Y和Z为同
2 2 4
族元素,1molX Y Z 含86mol电子。下列叙述正确的是
2 2 4
A.X和Z形成的化合物中只含离子键 B.X和Y形成的化合物的水溶液呈碱性
C.Y和Z的原子半径较大的是Z D.Y的氧化物的水化物是强酸
11.25℃时,用0.1000mol/L的NaOH溶液滴定20.00mL0.1000mol/L的一元强酸甲和一元弱酸乙,滴定曲
线如图所示。下列有关判断正确的是
A.曲线Ⅰ代表的滴定最好选用甲基橙作指示剂 B.曲线Ⅱ为NaOH溶液滴定一元弱酸乙
C.电离常数Ka (乙)=1.01×10 ﹣5 D.图象中的x>20.00
12.科学工作者提出了一种在室温条件下以CO
2
和甲醇为原料合成碳酸二甲酯
CH
3
O
2
CO
的电化学方案
,其原理如图所示。下列说法中错误的是
A.催化电极b连接电源的正极
B.Br-数目在反应过程中减少了
C.阴极的电极反应为CO 2CH OH2e- CO2CH O-H O
2 3 3 2
D.电路中转移2mole-时,理论上会产生90g碳酸二甲酯
试卷第4页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
13.在恒容密闭容器中,分别在T、T 温度下T后者
4
B.用相同浓度的NaOH溶液分别滴定等体积、pH均为3的HCOOH和CH COOH溶液至终点,消耗NaOH溶
3
液的体积:前者<后者
C.0.2mol/L CH COONa与0.1mol/L盐酸等体积混合后,溶液中微粒浓度:
3
c Na c CH COO c Cl c CH COOH c H c O H
3 3
D.0.2mol/LHCOONa溶液与0.1mol/LNaOH溶液等体积混合后的溶液中:
c HCOO c OH cHCOOHc H
二、非选择题:共 4题,共 58分。
15.(14分)铬盐是重要的无机化工产品。我国某科研团队研究了一种铬铁矿(主要成分为CrO ,含少量Fe O 、
2 3 2 3
MgO和少量硬度比金刚石大的BN)液相氧化浸出制备CrOH 的工艺,流程如下:
3
回答下列问题:
试卷第5页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(1)“碱浸”步骤提高浸出率的方法有_______(任写出一条),滤渣的成分为_______,该步骤CrO 发生反应的
2 3
化学方程式是_______。
(2)已知K BaCrO 1.21010,在“转化”步骤将铬元素完全沉淀时(离子浓度不大于1.0105molL1),需
sp 4
保持转化液中c
Ba2
至少为_______molL1。
(3)“还原”步骤的尾气为无色无味气体,则其反应离子方程式为_______。
(4)该团队在实验室模拟流程中用到的主要分离方法,所需玻璃仪器有_______。
(5)立方氮化硼(BN)晶体是一种硬度比金刚石大的特殊耐磨和削切材料,其晶胞结构如图所示:
该晶体中B的配位数为_______,其晶胞参数为anm,则立方氮化硼晶体的密度为_______gcm3。
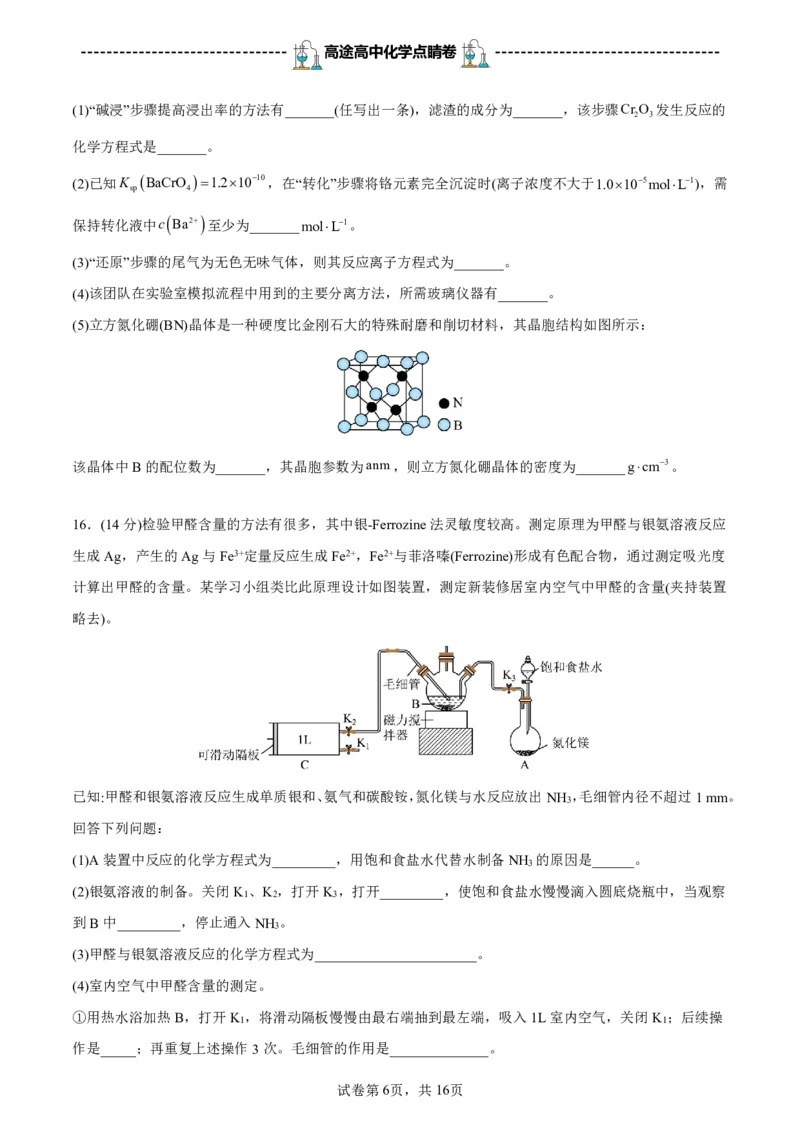
16.(14分)检验甲醛含量的方法有很多,其中银-Ferrozine法灵敏度较高。测定原理为甲醛与银氨溶液反应
生成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度
计算出甲醛的含量。某学习小组类比此原理设计如图装置,测定新装修居室内空气中甲醛的含量(夹持装置
略去)。
已知:甲醛和银氨溶液反应生成单质银和、氨气和碳酸铵,氮化镁与水反应放出NH ,毛细管内径不超过1mm。
3
回答下列问题:
(1)A装置中反应的化学方程式为_________,用饱和食盐水代替水制备NH 的原因是______。
3
(2)银氨溶液的制备。关闭K 、K ,打开K ,打开_________,使饱和食盐水慢慢滴入圆底烧瓶中,当观察
1 2 3
到B中_________,停止通入NH 。
3
(3)甲醛与银氨溶液反应的化学方程式为_______________________。
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K ,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K ;后续操
1 1
作是_____;再重复上述操作3次。毛细管的作用是______________。
试卷第6页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=l,再加入足量Fe (SO ) 溶液,充分反应后立
2 4 3
即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成1.12mgFe2+,空气中甲醛
的含量为_________mg·L-1。
17.(15分)磷石膏是湿法生产磷酸的固体废弃物,用磷石膏生产硫酸或硫,既可减少对环境的污染又可使资
源循环利用。回答下列问题:
(1)用焦炭、硫磺等均可还原磷石膏。已知下列反应:
I.CaSO (s)+2C(s)=CaS(s)+2CO (g) H =+226kJ∙mol−1
4 2 1
II.3CaSO (s)+CaS(s)=4CaO(s)+4SO△(g) H =akJ∙mol−1
4 2 2
III.3CaS(s)+CaSO (s)=4CaO(s)+4S(s) △H =bkJ∙mol−1
4 3
①反应(I)能在___________(填“低温”“高△温”或“任何温度”)下自发进行。
②用硫磺还原CaSO 反应为2CaSO (s)+S(s)=2CaO(s)+3SO (g),其 H=___________kJ·mol-1(用含a、b的代
4 4 2
数式表示)。 △
(2)磷石膏转氨法制硫酸的主要反应为CaSO
4
(s)+(NH
4
)
2
CO 3CaCO
3
(s)+(NH
4
)
2
SO
4
,该反应的平衡常数
K=___________[已知:K (CaCO )=2.5×10−9,K (CaSO )=3.2×10−7]。
sp 3 sp 4
(3)一氧化碳还原CaSO 可发生下列反应,其lgK 与温度(T)的关系如图所示(K 为以分压表示的平衡常数)。
4 p p
I.SO2(g)+3CO(g)=2CO2(g)+COS(g)
II.CaSO4(s)+CO(g)=CaO(s)+CO2(g)+SO2(g)
①△H>0的反应是___________(填“I”或“II”)。
②在交点A处,气体分压间满足的关系是:p(COS)=___________。
③在恒温恒容密闭容器中进行反应(I),能说明已达到平衡状态的是___________(填字母)。
a.2v(CO) =3v(CO ) b.气体的密度不再随时间变化
正 2 正
c2CO cCOS
c.气体的压强不再随时间变化 d. 2 的值不再随时间而变化
c3CO
④若在1.0L的恒容密闭容器中加入1molCaSO ,并充入1molCO,只发生反应II,在B点时气体总压强
4
为1MPa,则此时CaSO
4
转化率为___________(已知 2≈1.41)。
试卷第7页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
18.(15分)有机物A(C H N )用于合成药物、塑料等物质。
6 8 2
I.由A合成佐匹克隆(J)的路线如图。
已知:i:RNH R'CHORN=CHR′ ii: RNH2
2
(1)A属于芳香族化合物,核磁共振氢谱有3组峰,峰面积比为2:1:1,A→B的化学方程式为
_________________。
(2)OHC-CHO中官能团的检验方法:向_________(填试剂)中加入待测液,加热至沸腾,产生砖红色沉淀。
(3)C中含氧官能团名称为_________。
(4)物质a的结构简式为_____________。
(5)G→J的反应类型为_____________。
II.以A为原料合成PAI塑料的路线如图。
(6)参照I中流程的信息分析,K、M的结构简式分别为_________、_________。
试卷第8页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2024 年重庆市普通高中学业水平选择性考试模拟测试卷
化学参考答案
1.【答案】D
【详解】A.Be为4号元素最外层2个电子,它位于第二周期ⅡA族,同时密度小,性能好的金属铍可作为主
镜材料,A项正确;
B.聚酰亚胺为人工合成的高分子化合物,B项正确;
C.He相对分子质量小,分子间范德华力弱,所以氦的分子间作用力很弱,沸点极低,C项正确;
D.N O 本身为无色,D项错误;
2 4
故选D。
2.【答案】B
【详解】A.H O是角形分子,球棍模型为 ,A正确;
2
B.铁原子失去3个电子形成铁离子,基态Fe3+的简化电子排布式为[Ar]3d5,B错误;
C.NaClO是由次氯酸根离子和钠离子构成的离子化合物,电子式为 ,C正确;
D.氯为17号元素,原子结构示意图为 ,D正确;故选B。
3.【答案】B
【详解】A.铁离子和铜生成亚铁离子和铜离子,离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故A错误;
B.丙醛含有醛基,具有还原性,与银氨溶液反应生成铵盐和银单质,离子方程式为:
+H2O,故B正确;
C.氢氟酸生产磨砂玻璃中二氧化硅反应生成四氟化硅和水,离子方程式为:SiO2+4HF=SiF4 ↑+2H2O,故
C错误;
D.向NaHSO4 溶液加入适量Ba(OH)
2
溶液至SO
4
2-恰好完全沉淀,则氢离子也完全反应生成水,离子方
程式为: ,故D错误;
故选:B。
4.【答案】D
【详解】A.常温下,不能使用标况下的V
m
=22.4Lmol1来计算NH
3
的物质的量,故不能计算22.4LNH
3
所
含有的中子数,选项A错误;
B.溶液体积未知,则不能计算OH数目,选项B错误;
试卷第9页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
3.2g4N mol1
C.N
2
H
4
分子中含有4个氮氢极性键,则3.2gN
2
H
4
中极性共价键的数目为
32gmo
A
l1
0.4N
A
,选项C
错误;
D.每生成1molH O时转移2mol电子,故每生成3.6g0.2molH O,转移0.4mol电子,选项D正确;
2 2
答案选D。
5.【答案】B
【详解】A.铜和浓硫酸在加热条件下才能反应生成二氧化硫气体,故不选A;
B.铜和稀硝酸反应生成硝酸铜、一氧化氮、水,NO难溶于水,用排水法收集NO,能达到实验目的,故选
B;
C.配制NaCl溶液,不能直接在容量瓶中溶解氯化钠固体,故不选C;
D.铁钉在氯化钠溶液中发生吸氧腐蚀,不能达到实验目的,故不选D;
选B。
6.【答案】B
【详解】A.X为O,Y为Mg,Z为Si,原子半径大小为Mg>Si>O,故A错误;
B.X为O,Z为Si,N为Cl,电负性大小为O>Cl>Si,故B正确;
C.Y为Mg,Z为Si,N为Cl,元素的第一电离能Cl>Si>Mg,故C错误;
D.X为O,O的基态原子的电子轨道表示式 ,故D错误;
故选:B。
7.【答案】C
【详解】A.由结构简式是可知有16个C,8个O,8个不饱和度,则有18个H,分子式为C H O ,A项正确;
16 18 8
B.连接4个不同原子或原子团的碳原子为手性碳,方便观察将手性碳原子标号, 手性
碳一共有4个,B项正确;
C.该物质中含有苯环,碳碳双键,可与氢气加成,酯基上的双键不能和氢气加成,所以1mol该分子最多可
与5molH 发生加成反应,C项错误;
2
D.酸性水解产物羧酸分子中,苯环,碳碳双键,碳氧双键都为平面结构,经过旋转单键,可以在同一平面
,D项正确;答案选C。
8.【答案】D
【详解】A.基态铜原子的外围电子排布式为3d104s1,因此Cu的外围电子排布式为3d10,A错误;
试卷第10页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
B.Ni位于第四周期Ⅷ族,属于过渡元素,位于d区,B错误;
C.以任一顶点处的Sn为例,距离Sn最近的Cu位于相邻面的面心,一个晶胞中有3个,每个Cu被两个面共用
,该Sn被8个晶胞共用,因此距离Sn最近的Cu有3×8÷2=12个,C错误;
D.由均摊法可知,每个晶胞中含有1个Sn、3个Cu、1个P,摩尔质量为342g/mol,因此晶体密度为
342
gcm3
N
a10103
,D正确;
A
故选D。
9.【答案】B
【详解】A.向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液,氯水过量,也会将碘离子氧化为碘单质,
不能说明氧化性Br I ,A错误;
2 2
B.在Na SO 饱和溶液中滴加稀硫酸,发生复分解反应产生SO 气体,将产生的气体通入KMnO 溶液中,二
2 3 2 4
者发生氧化还原反应使KMnO 反应变为无色Mn2+,因此看到溶液褪色,证明了SO 具有还原性,B正确;
4 2
C.要证明蔗糖在酸性条件下是否发生水解,应该向蔗糖溶液中滴加稀硫酸,加热,加入氢氧化钠溶液使溶
液呈碱性,再加入银氨溶液并水浴加热,C错误;
D.次氯酸钠溶液具有强氧化性,会使有机色质漂白褪色,则用酚酞试液不能判断次氯酸钠溶液是否呈碱性
,故D错误;
10.【答案】B
【分析】X的单质在空气中燃烧得到淡黄色固体,X为Na,设Y的核电荷数为x,Y和Z为同族元素,则Z的核
32
电荷数为x-8或x+8,1molX Y Z 含86mol电子,故22+2x+4x-32=86或22+2x+4x+32=86,解得x=16或x= (
2 2 4
6
舍去),故Y为S,Z为O。
【详解】A.X和Z形成的化合物为Na O和Na O ,Na O 中即含离子键又含共价键,A错误;
2 2 2 2 2
B.X和Y形成的化合物为Na S,水溶液因硫离子水解而呈碱性,B正确;
2
C.Y和Z分别为S和O,同主族元素从上往下原子半径增大,原子半径较大的是S,C错误;
D.Y的最高价氧化物的水化物H SO 是强酸,但不是最高价的可能为弱酸,如H SO ,D错误;
2 4 2 3
故选B。
11.【答案】C
【详解】解:0.1000mol/L的强酸甲溶液的pH为1,0.1000mol/L弱酸乙溶液的pH>1,根据图知,曲线Ⅰ
表示弱酸乙和NaOH溶液的滴定曲线,曲线Ⅱ表示强酸甲和NaOH溶液的滴定曲线;
A.乙的钠盐溶液呈碱性,应该选取酚酞作指示剂,故A错误;
B.曲线Ⅱ为NaOH溶液滴定一元强酸甲,故B错误;
试卷第11页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
C.0.1000mol/L弱酸乙溶液的pH=3,该溶液中c(乙酸根离子)≈c(H+)=10 ﹣3mol/L,c(乙)=(0.1
000﹣10 ﹣3)mol/L,电离平衡常数K(乙)= ≈ =1.01×10 ﹣5,故C
a
正确;
D.甲为强酸,甲的钠盐溶液呈中性,酸碱都是一元的且酸碱的物质的量浓度相等,要使酸碱恰好完全反应,
则酸碱溶液的体积相等,所以x=20.00,故D错误;
故选:C。
12.【答案】B
【详解】A.根据催化电极b处Br转化为Br ,发生氧化反应,可知催化电极b为阳极,催化电极b连接电源
2
的正极,故A正确;
B.CO
2
和甲醇为原料生成碳酸二甲酯
CH
3
O
2
CO
和水,溴离子的数目在反应过程中不发生变化,故B错
误:
C.根据图示,阴极(催化电极a)的电极反应为CO +2CH OH+2e-=CO+2CH O+H O,故C正确;
2 3 3 2
D.根据CO +2CH OH+2e-=CO+2CH O+H O,电路中转移2moleˉ时,理论上会产生1mol碳酸二甲酯,其质
2 3 3 2
量为90g,故D正确。选B。
13.【答案】C
【分析】曲线a、b都在下降,说明a、b都是A物质的浓度变化情况,且b先达到平衡,反应速率更快,故b对
应的是T 温度。根据物质的量浓度的变化量,结合反应比例可知曲线c为T 温度下的B的浓度随时间的变化
2 1
曲线。
【详解】A.恒容条件下充入He,各物质的分压没有发生改变,平衡不移动,A错误;
2mol/L-1mol/L
B.a曲线条件下,10~30min内vA= =0.05mol L-1min -1,反应速率比等于化学计量数之比
20min
2 2
,则vB vA 0.05molL1 min1,B错误;
3 3
C.结合分析可知,a、b都是A物质的浓度变化情况,b对应的是T 温度,C正确;
2
D.降低温度,平衡正向移动,反应物的转化率提升,但温度过低会导致反应速率过慢,不利于提高生产效
率,D错误;答案选C。
14.【答案】D
【详解】A.由电荷守恒可知c HCOO c OH c Na c H 、c Cl c OH c NH c H ,
4
由甲酸和一水合氨的电离常数可知,甲酸根的水解程度小于铵根的水解程度,即甲酸钠中氢氧根的浓度小
试卷第12页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
于氯化铵中氢离子的浓度,因此甲酸钠中氢离子的浓度大于氯化铵中氢氧根的浓度,钠离子与氯离子浓度
相同,因此甲酸钠中阳离子浓度大于氯化铵中阳离子浓度,A正确;
B.由电离平衡常数可知,甲酸的酸性比乙酸强,pH相同时乙酸的物质的量浓度更高,用相同浓度的氢氧化
钠滴定时,消耗氢氧化钠溶液的体积更多,B正确;
C.醋酸钠与盐酸反应,生成醋酸和氯化钠,因此混合溶液中醋酸钠、醋酸、氯化钠的物质的量浓度相同,
均为0.05mol/L(忽略体积变化),由醋酸的电离常数可知,相同浓度的醋酸电离程度大于醋酸根的水解程度,
溶液呈酸性,因此离子浓度为c Na c CH COO c Cl c CH COOH c H c O H ,C正确;
3 3
D.由电荷守恒可得c
HCOO
c
OH
c
Na
c
H
,由物料守恒可得
c Na+ 1.5cHCOOH1.5c HCOO ,由此可得c OH 1.5cHCOOH0.5c HCOO c H ,D错
误;故选D。
二、非选择题:共 4题,共 58分。
15.(14分)【答案】(1)粉碎或适当升高温度或增大NaOH浓度 Fe O 、MgO、BN
2 3
2Cr O +3O +8NaOH=4Na CrO +4H O
2 3 2 2 4 2
(2)1.2×10-5
(3)4BaCrO +C H OH+20H+=4Ba2++4Cr3++2CO ↑+13H O
4 2 5 2 2
(4)漏斗、烧杯、玻璃棒
1023
(5)4
a3N
A
【分析】由题给流程可知,铬铁矿在氢氧化钠溶液和氧气碱浸时,三氧化二铬与氢氧化钠溶液、氧气反应
生成铬酸钠和水,氧化铁、氧化镁、氮化硼与氢氧化钠溶液不反应,过滤得到含有氧化铁、氧化镁、氮化
硼的滤渣和含有铬酸钠的高铬液;向高铬液中加入氢氧化钡溶液,将铬酸钠转化为铬酸钡沉淀,过滤得到
铬酸钡;向铬酸钡中加入乙醇和盐酸的混合溶液,铬酸钡被乙醇还原为铬离子,向反应后的溶液中加入氢
氧化钡溶液调节溶液pH,将铬离子转化为氢氧化铬沉淀,
【详解】(1)粉碎、适当升高温度、增大NaOH浓度能提高“碱浸”步骤的浸出率;由分析可知,滤渣的成分
为氧化铁、氧化镁、氮化硼;三氧化二铬发生的反应为三氧化二铬与氢氧化钠溶液、氧气反应生成铬酸钠
和水,反应的化学方程式为2Cr O +3O +8NaOH=4Na CrO +4H O,故答案为:粉碎或适当升高温度或增大
2 3 2 2 4 2
NaOH浓度;Fe O 、MgO、BN;2Cr O +3O +8NaOH=4Na CrO +4H O;
2 3 2 3 2 2 4 2
1.21010
(2)由铬酸钡溶度积可知,铬离子完全沉淀时,溶液中钡离子的浓度为 =1.2×10—5mol/L,故答
1.0105mol/L
案为:1.2×10-5;
(3)由分析可知,“还原”步骤发生的反应为铬酸钡与乙醇和盐酸的混合溶液反应生成氯化钡、氯化铬、二氧
试卷第13页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
化碳和水,反应的离子方程式为4BaCrO +C H OH+20H+=4Ba2++4Cr3++2CO ↑+13H O,故答案为:
4 2 5 2 2
4BaCrO +C H OH+20H+=4Ba2++4Cr3++2CO ↑+13H O;
4 2 5 2 2
(4)由题给流程可知,在实验室中该流程中用到的主要分离方法为过滤,过滤用到的仪器为漏斗、烧杯、玻
璃棒,故答案为:漏斗、烧杯、玻璃棒;
1 1
(5)由晶胞结构可知,晶胞中位于顶点和面心的氮原子个数为8× +6× =4,位于体内的硼原子个数为4,体
8 2
内每个硼原子与4个氮原子距离最近,则该晶体中B的配位数为4,设晶体的密度为dg/cm3,由晶胞的质
425 1023 1023
量公式可得: =10-21a3d,解得d= ,故答案为: 。
N a3N a3N
A A A
16.(14分)【答案】(1)Mg N +6H O=3Mg(OH) ↓+2NH ↑ 饱和食盐水可减缓生成氨的速率
3 2 2 2 3
(2)分液漏斗的塞子与旋塞 沉淀恰好完全溶解时
(3)HCHO+4Ag(NH ) OH水浴加热(NH ) CO +6NH +4Ag↓+2H O
3 2 4 2 3 3 2
(4)打开K ,缓慢推动滑动隔板,将气体全部推出,再关闭K 减小气体的流动速率,使空气中的甲醛
2 2
气体被完全吸收 0.0375
【分析】在仪器A中Mg N 与H O反应产生Mg(OH) 和NH ,NH 通入到AgNO 溶液中首先反应产生AgOH
3 2 2 2 3 3 3
白色沉淀,后当氨气过量时,反应产生Ag(NH ) OH,然后向溶液中通入甲醛,水浴加热,发生银镜反应产
3 2
生单质Ag和CO 气体,产生的Ag与加入的Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪形成有色物质,在562nm
2
处测定吸光度,测得生成Fe2+1.12mg,据此结合反应过程中电子守恒,可计算室内空气中甲醛含量。
【详解】(1)Mg N 与水发生盐的双水解反应产生Mg(OH) 和NH ,反应方程式为:
3 2 2 3
Mg N +6H O=3Mg(OH) ↓+2NH ↑;用饱和食盐水代替水,单位体积溶液中水的含量降低,可减缓生成氨气
3 2 2 2 3
的速率;
(2)银氨溶液的制备:关闭K 、K ,打开K ,打开分液漏斗的活塞与旋塞,使饱和食盐水慢慢滴入圆底烧瓶
1 2 3
中,首先发生反应:Ag++NH +H O=AgOH↓+NH+,后又发生反应:AgOH+2NH ·H O=[Ag(NH ) ]++OH-+2H O,
3 2 4 3 2 3 2 2
当观察到B中白色沉淀恰好完全溶解时,就得到了银氨溶液,此时关闭K 和分液漏斗旋塞;
3
(3)装置C中可滑动滑板将空气毛细管进入到装置B中,毛细管的内径不超过1mm可充分与银氨溶液反应,
目的为减小气体的通入速率,使空气中的甲醛气体被完全吸收;
甲醛的结构简式为 ,则B中甲醛和银氨溶液反应方程式为:
HCHO+4AgNH OH水浴NH CO +4Ag+6NH +2H O;
3 2 4 2 3 3 2
(4)①用热水浴加热B,打开K ,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K ;后续
1 1
操作是打开K ,缓慢推动滑动隔板,将气体全部推出,再关闭K ;再重复上述操作3次。毛细管的作用是
2 2
减小气体的通入速率,使空气中的甲醛气体被完全吸收;
试卷第14页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
②甲醛和银氨溶液加热反应生成银,银具有还原性,被Fe3+氧化,结合甲醛被氧化为CO ,氢氧化二氨合银
2
被还原为银,甲醛中碳元素化合价0价变化为+4价,银+1价变化为0价,生成的银又被铁离子氧化,铁离
m 1.1210-3g
子被还原为亚铁离子,生成亚铁离子1.12mg,物质的量n(Fe)= = ==2×10-5mol,根据氧化还
M 56g/mol
原反应电子守恒计算,设消耗甲醛物质的量为xmol,则4x=2×10-5mol×1,x=5×10-6mol,因此实验进行了
4次操作,所以测得1L空气中甲醛的含量为1.25×10-6mol,空气中甲醛的含量为1.25×10-6mol/L×30g/mol
=0.0375×10-3g/L=0.0375mg/L。
3ab p2(SO )p2(CO)
17.(15分【) 答案】(1)①高温 ② (2)1.28102 (3)①II ② 2 ③cd ④70.5%
4 p(CO )
2
【详解】(1)①反应(I)是吸热反应( H>0),熵增的反应( S>0),根据 G= H-T S<0,得出该反应在高
温下自发进行;故答案为:高温。△ △ △ △ △
②将第II个方程式3倍减去第III个方程式,再整体除以4得到硫磺还原CaSO 反应为
4
3ab 3ab
2CaSO (s)+S(s)=2CaO(s)+3SO (g),其 H= kJ·mol−1;故答案为: 。
4 2
4 4
△
(2)磷石膏转氨法制硫酸的主要反应为CaSO
4
(s)+(NH
4
)
2
CO 3CaCO
3
(s)+(NH
4
)
2
SO
4
,其离子方程式为
CaSO
4
(s)+CO
3
2(aq)CaCO
3
(s)+ SO2
4
(aq),该反应的平衡常数
c(SO2) c(Ca2)c(SO2) K CaSO 3.2107
K 4 4 sp 4 1.28102;故答案为:1.28102。
c(CO2) c(Ca2)c(CO2) K CaCO 2.5109
3 3 sp 3
(3)①升高温度,反应I的lgK 逐渐减小,K 减小,即逆向移动,说明逆向是吸热反应,正向是放热反应,
p p
升高温度,反应II的lgK 逐渐增大,K 增大,即正向移动,说明正向是吸热反应,则 H>0的反应是II;
p p
故答案为II。 △
p(COS)p2(CO ) p(SO )p(CO )
②在交点A处,根据两个方程式的压强平衡常数得出:K 2 2 2 ,因此气体
p p(SO )p3(CO) p(CO)
2
p2(SO )p2(CO) p2(SO )p2(CO)
分压间满足的关系是:p(COS) 2 ;故答案为: 2 。
p(CO ) p(CO )
2 2
③a.2υ(CO) =3υ(CO ) ,都为正反应,不满足两个不同的方向,不能作为判断平衡标志,故a不符合题意;
正 2 正
b.气体密度等于气体质量除以容器体积,气体质量不变,容器体积不变,密度始终不变,当气体的密度不
再随时间变化,不能作为判断平衡标志,故b不符合题意;c.该反应正向反应是体积减小的反应,压强不
断减小,当气体的压强不再随时间变化,可以作为判断平衡标志,故c符合题意;d.正向反应,生成物浓
c2CO cCOS
度增大,反应物物浓度减小, 2 在一直增大,当比值不再随时间而变化,说明达到化学平衡,
c3CO
试卷第15页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
故d符合题意;综上所述,答案为cd。
④若在1.0L的恒容密闭容器中加入1molCaSO ,并充入1molCO,只发生反应II,建立三段式得到
4
CaSO (s)+ CO(g) CaO(s)+SO (g)+CO (g)
4 2 2
开始 1mol 1mol 0 0 0
,在B点时气体总压强为1MPa,lgK =0即K =1,
转化 bmol bmol bmol bmol bmol p p
平衡(1b)mol (1b)mol bmol bmol bmol
b b
1 1 2
K
p
= p(SO
p
2
(
)
C
p
O
(
)
CO 2 ) = 1
1
+
b
1b
1+b =1,解得b=
2
2 ,则此时CaSO
4
转化率为
α= 2
mol
100%70.5%
;故答
1mol
1+b
案为:70.5%。
18.(15分)【答案】(1) +OHC-CHO→ +2H O(2)新制Cu(OH) (3)羧基(4)
2 2
(5)取代反应(6) 或
【分析】由有机物的转化关系可知, 与乙二醛发生信息反应生成 ,则A为 、B为
; 发生氧化反应生成 ,则C为 ; 发生脱水反应生成
, 与 发生信息反应生成 ,则E为 、
a为 ; 发生脱水反应生成 ,则F为 ;
与硼氢化钾发生还原反应生成 ,则G为 ;
与 发生取代反应生成 ; 与SOCl 发生反应
2
生成 或 ,则K为 、L为 ;一定条件
试卷第16页,共16页-------------------------------- 高途高中化学点睛卷 -----------------------------------
与 发生缩聚反应生成 或 ,则M为 或
; 或 发生分子内脱水反应生成
。
【详解】(1)由分析可知,A→B的反应为 与乙二醛发生信息反应生成 和水,反应的化学方
程式为: +OHC-CHO→ +2H O;
2
(2)检验乙二醛中含有醛基的方法为向新制的氢氧化铜中加入待测液,加热至沸腾,产生砖红色沉淀说明乙
二醛中含有醛基,故答案为:新制Cu(OH) ;
2
(3)由分析可知,C的结构简式为 ,含氧官能团为羧基;
(4)由分析可知,a的结构简式为 ;
(5)由分析可知,G→J的反应为 与 发生取代反应生成
和氯化氢,故答案为:取代反应;
(6)由分析可知,K、M的结构简式分别为 、 或
。
试卷第17页,共16页