文档内容
学年度上学期 级
2025—2026 2023
⽉⽉考化学试卷
8
命题⼈:尚邦全 审题⼈:蔡艳
时间:90分钟 分数:100分
考试时间:2025年8⽉15⽇
可能⽤到的相对原⼦质量:H1 Li7 C12 N14 O16 Na23 P31 S32 Cl35.5 Fe56
第Ⅰ卷(选择题 共 分)
45
⼀、选择题(本题包括15⼩题,每⼩题3分,共45分,每⼩题只有⼀个选项符合题意)
1.材料是⼈类赖以⽣存和发展的物质基础。下列材料类别与其他三项不同的是
A.⾼强韧⽆磁不锈钢——聚变能实验装置中的低温结构部件
B.⾦刚⽯薄膜——“梦想”号⼤洋钻探船使⽤的钻头表⾯涂层
C.超细⽞武岩纤维——嫦娥六号携带的⽉⾯国旗的纺织材料
D.超细玻璃纤维——国产⼤⻜机中隔⾳隔热的“⻜机棉”
2.化学与我们的⽣活、饮⻝、健康密不可分,下列说法不正确的是
A.还原铁粉、抗坏⾎酸(即维⽣素C))都可做⻝品抗氧化剂
B. 可⽤于杀菌消毒,还是⼀种⻝品添加剂
C.⻝盐中加少量的单质碘,可预防甲状腺肿⼤
D.碳酸氢铵、碳酸氢钠可⽤作⻝品膨松剂
3.下列化学⽤语或图示表达正确的是
A. 的名称:1,3,5-三硝基甲苯
B. 的名称:2-甲基-2-⼄基丁烷
C.邻羟基苯甲醛分⼦内氢键示意图:
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司D.基态Ga原⼦的简化电⼦排布式:
4.下列实验⽅法或试剂使⽤不合理的是
选项 实验⽬的 实验⽅法或试剂
A 检验溶液中SO 2- HCl酸化的BaCl 溶液
4 2
B 除去苯甲酸混有的NaCl 重结晶
C 测定废⽔中苯酚含量 浓溴⽔
D 分离提纯蛋⽩质 加⼊饱和 溶液,过滤
A.A B.B C.C D.D
5.下列离⼦⽅程式书写正确的是
A.溴化亚铁溶液中通⼊等物质的量的氯⽓;2C1 +2Fe2++2Br⼀=4C1-+2Fe3++Br
2 2
B.CuSO 溶液中加⼊⾜量的氨⽔:Cu2++2NH ‧H O=Cu(OH) +2NH +
4 3 2 2 4
C.Cl 与⽔的反应:Cl +H O=2H++Cl-+ClO-
2 2 2
D.碳酸氢镁溶液中加⼊过量澄清⽯灰⽔:
Mg2++2HCO -+Ca2++2OH-=CaCO ↓+2H O+MgCO ↓
3 3 2 3
6.电导率(I)是衡量溶液的导电能⼒强弱的⼀个物理量,⼀般来说溶液中离⼦浓度越⼤,电导
率越⼤,下列⼏种溶液电导率变化图像对应关系错误的是
A.图 A代表向饱和澄清⽯灰⽔中不断通⼊ CO ⽓体
2
B.图 B代表向 NaOH溶液中滴加相同浓度的 CH COOH溶液
3
C.图 C代表向 NaOH溶液中通⼊ Cl ⾄恰好完全反应
2
D.图 D代表向 H SO 溶液中加⼊等体积、等物质的量浓度的 Ba 溶液
2 4
7.在给定条件下,下列制备过程涉及的物质转化均能实现的是
A. B.
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司C. D.NaCl溶液
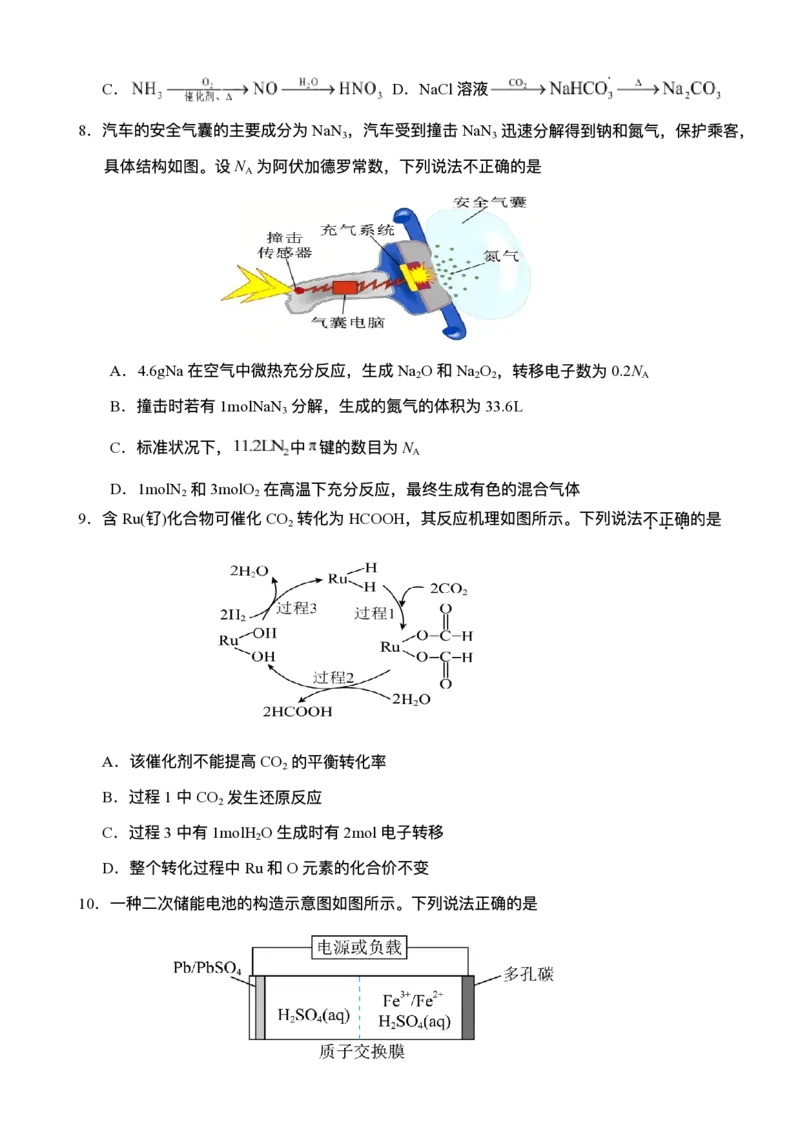
8.汽⻋的安全⽓囊的主要成分为NaN ,汽⻋受到撞击NaN 迅速分解得到钠和氮⽓,保护乘客,
3 3
具体结构如图。设N 为阿伏加德罗常数,下列说法不正确的是
A
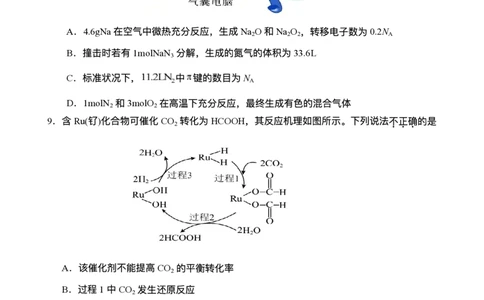
A.4.6gNa在空⽓中微热充分反应,⽣成Na O和Na O ,转移电⼦数为0.2N
2 2 2 A
B.撞击时若有1molNaN 分解,⽣成的氮⽓的体积为33.6L
3
C.标准状况下, 中 键的数⽬为N
A
D.1molN 和3molO 在⾼温下充分反应,最终⽣成有⾊的混合⽓体
2 2
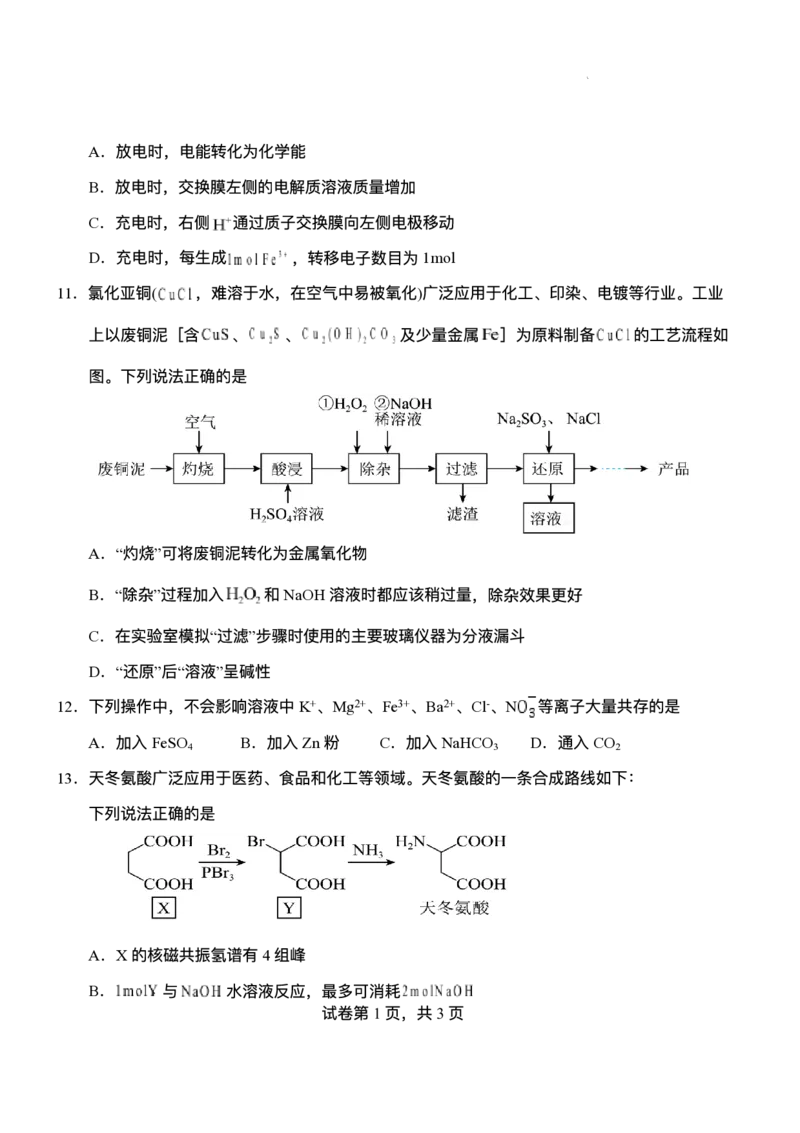
9.含Ru(钌)化合物可催化CO 转化为HCOOH,其反应机理如图所示。下列说法不正确的是
2
A.该催化剂不能提⾼CO 的平衡转化率
2
B.过程1中CO 发⽣还原反应
2
C.过程3中有1molH O⽣成时有2mol电⼦转移
2
D.整个转化过程中Ru和O元素的化合价不变
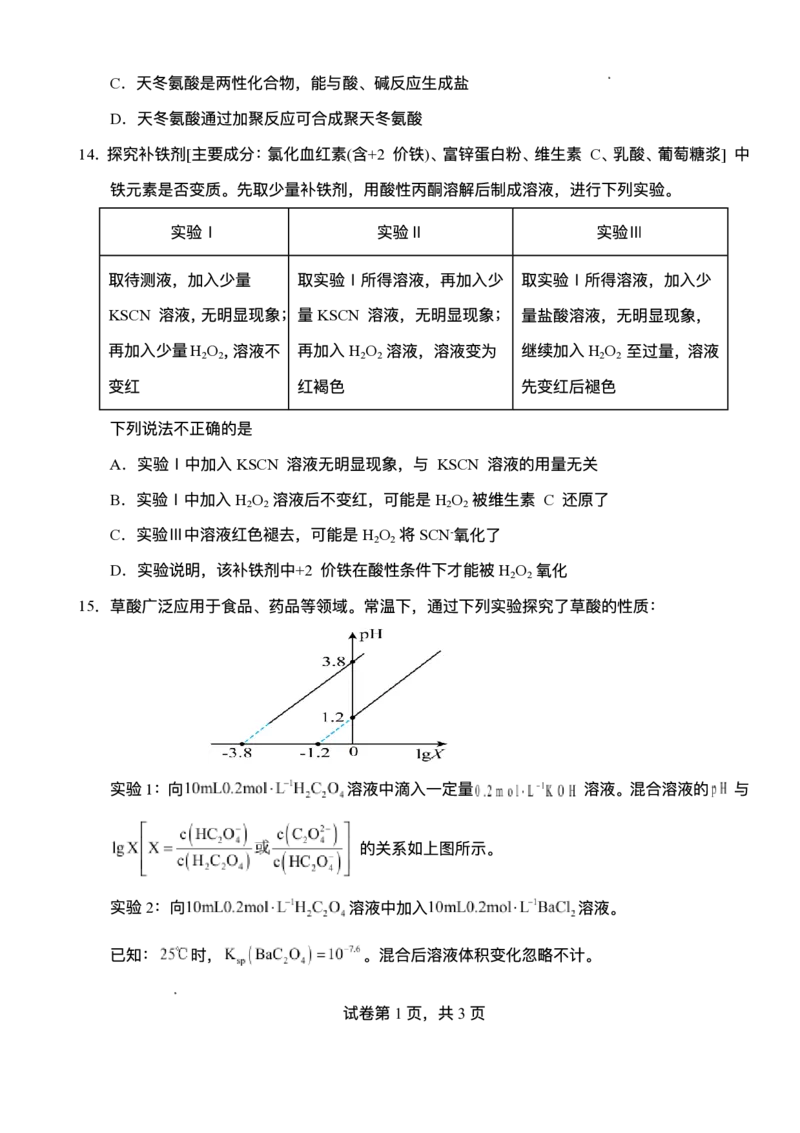
10.⼀种⼆次储能电池的构造示意图如图所示。下列说法正确的是
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司A.放电时,电能转化为化学能
B.放电时,交换膜左侧的电解质溶液质量增加
C.充电时,右侧 通过质⼦交换膜向左侧电极移动
D.充电时,每⽣成 ,转移电⼦数⽬为1mol
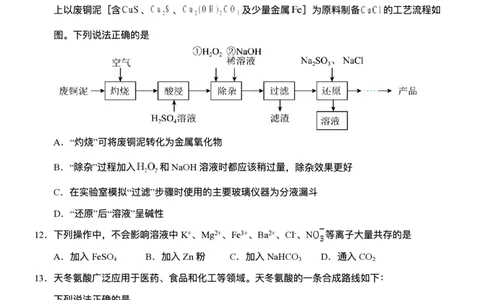
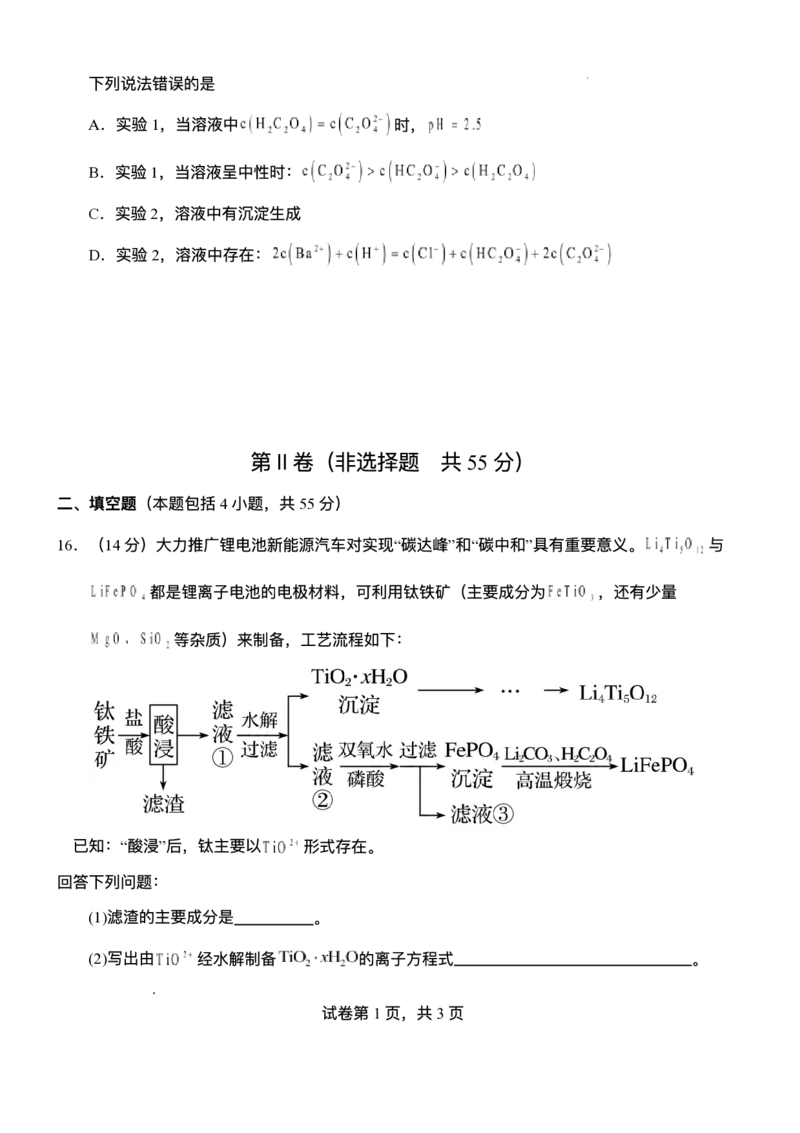
11.氯化亚铜( ,难溶于⽔,在空⽓中易被氧化)⼴泛应⽤于化⼯、印染、电镀等⾏业。⼯业
上以废铜泥[含 、 、 及少量⾦属 ]为原料制备 的⼯艺流程如
图。下列说法正确的是
A.“灼烧”可将废铜泥转化为⾦属氧化物
B.“除杂”过程加⼊ 和NaOH溶液时都应该稍过量,除杂效果更好
C.在实验室模拟“过滤”步骤时使⽤的主要玻璃仪器为分液漏⽃
D.“还原”后“溶液”呈碱性
12.下列操作中,不会影响溶液中K+、Mg2+、Fe3+、Ba2+、Cl-、N 等离⼦⼤量共存的是
A.加⼊FeSO B.加⼊Zn粉 C.加⼊NaHCO D.通⼊CO
4 3 2
13.天冬氨酸⼴泛应⽤于医药、⻝品和化⼯等领域。天冬氨酸的⼀条合成路线如下:
下列说法正确的是
A.X的核磁共振氢谱有4组峰
B. 与 ⽔溶液反应,最多可消耗
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司C.天冬氨酸是两性化合物,能与酸、碱反应⽣成盐
D.天冬氨酸通过加聚反应可合成聚天冬氨酸
14.探究补铁剂[主要成分:氯化⾎红素(含+2 价铁)、富锌蛋⽩粉、维⽣素 C、乳酸、葡萄糖浆] 中
铁元素是否变质。先取少量补铁剂,⽤酸性丙酮溶解后制成溶液,进⾏下列实验。
实验Ⅰ 实验Ⅱ 实验Ⅲ
取待测液,加⼊少量 取实验Ⅰ所得溶液,再加⼊少 取实验Ⅰ所得溶液,加⼊少
KSCN 溶液,⽆明显现象;量KSCN 溶液,⽆明显现象; 量盐酸溶液,⽆明显现象,
再加⼊少量H O ,溶液不 再加⼊H O 溶液,溶液变为 继续加⼊H O ⾄过量,溶液
2 2 2 2 2 2
变红 红褐⾊ 先变红后褪⾊
下列说法不正确的是
A.实验Ⅰ中加⼊KSCN 溶液⽆明显现象,与 KSCN 溶液的⽤量⽆关
B.实验Ⅰ中加⼊H O 溶液后不变红,可能是H O 被维⽣素 C 还原了
2 2 2 2
C.实验Ⅲ中溶液红⾊褪去,可能是H O 将SCN-氧化了
2 2
D.实验说明,该补铁剂中+2 价铁在酸性条件下才能被H O 氧化
2 2
15.草酸⼴泛应⽤于⻝品、药品等领域。常温下,通过下列实验探究了草酸的性质:
实验1:向 溶液中滴⼊⼀定量 溶液。混合溶液的 与
的关系如上图所示。
实验2:向 溶液中加⼊ 溶液。
已知: 时, 。混合后溶液体积变化忽略不计。
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司下列说法错误的是
A.实验1,当溶液中 时,
B.实验1,当溶液呈中性时:
C.实验2,溶液中有沉淀⽣成
D.实验2,溶液中存在:
第Ⅱ卷(⾮选择题 共 分)
55
⼆、填空题(本题包括4⼩题,共55分)
16.(14分)⼤⼒推⼴锂电池新能源汽⻋对实现“碳达峰”和“碳中和”具有重要意义。 与
都是锂离⼦电池的电极材料,可利⽤钛铁矿(主要成分为 ,还有少量
等杂质)来制备,⼯艺流程如下:
已知:“酸浸”后,钛主要以 形式存在。
回答下列问题:
(1)滤渣的主要成分是 。
(2)写出由 经⽔解制备 的离⼦⽅程式 。
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司(3)在制备 的过程中会⽣成 ( 为+4价),则每个 结构单元中含
有过氧键的数⽬为 。
(4)滤液②加双氧⽔的⽬的是 。
(5)写出制备 的化学⽅程式 。
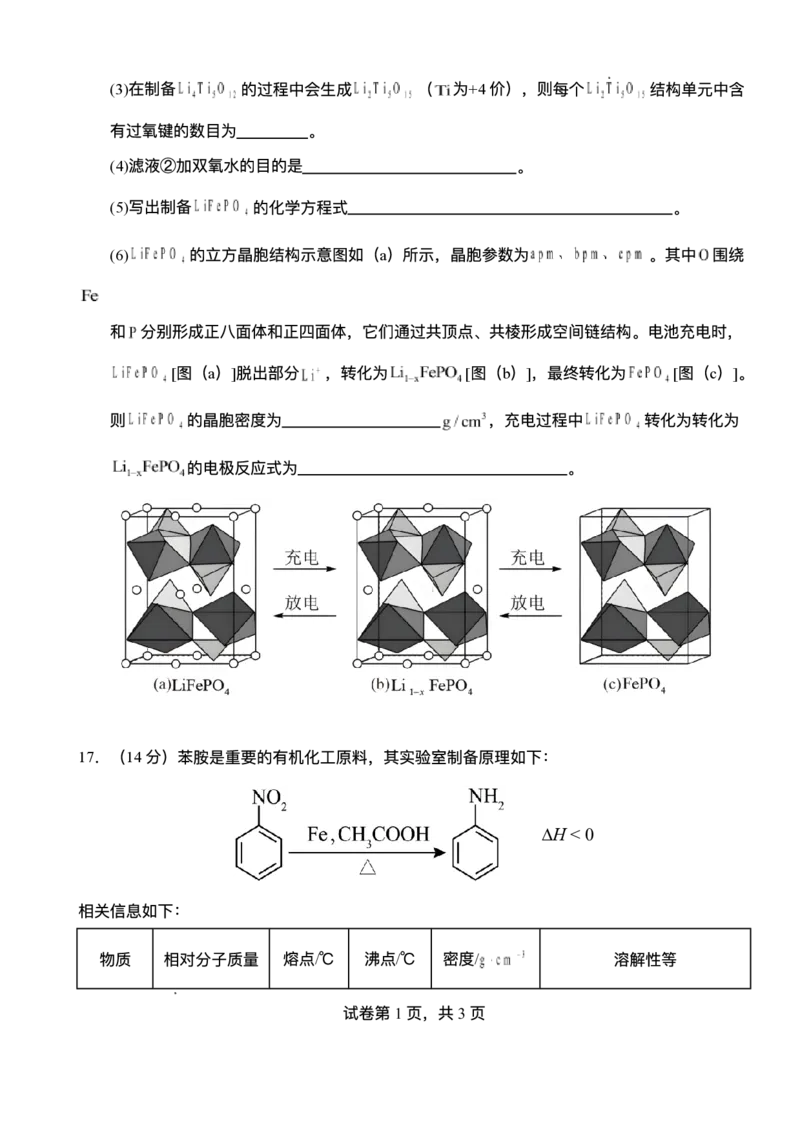
(6) 的⽴⽅晶胞结构示意图如(a)所示,晶胞参数为 。其中 围绕
和 分别形成正⼋⾯体和正四⾯体,它们通过共顶点、共棱形成空间链结构。电池充电时,
[图(a)]脱出部分 ,转化为 [图(b)],最终转化为 [图(c)]。
则 的晶胞密度为 ,充电过程中 转化为转化为
的电极反应式为 。
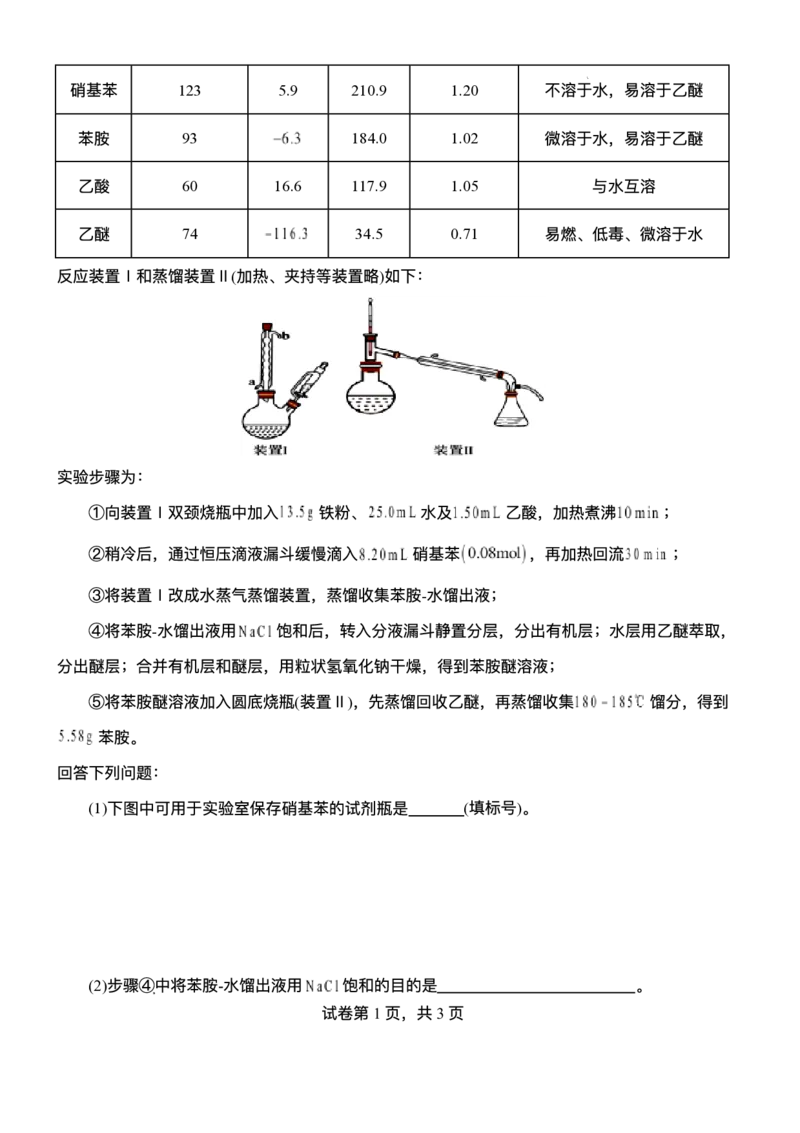
17.(14分)苯胺是重要的有机化⼯原料,其实验室制备原理如下:
∆H < 0
相关信息如下:
物质 相对分⼦质量 熔点/℃ 沸点/℃ 密度/ 溶解性等
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司硝基苯 123 5.9 210.9 1.20 不溶于⽔,易溶于⼄醚
苯胺 93 184.0 1.02 微溶于⽔,易溶于⼄醚
⼄酸 60 16.6 117.9 1.05 与⽔互溶
⼄醚 74 34.5 0.71 易燃、低毒、微溶于⽔
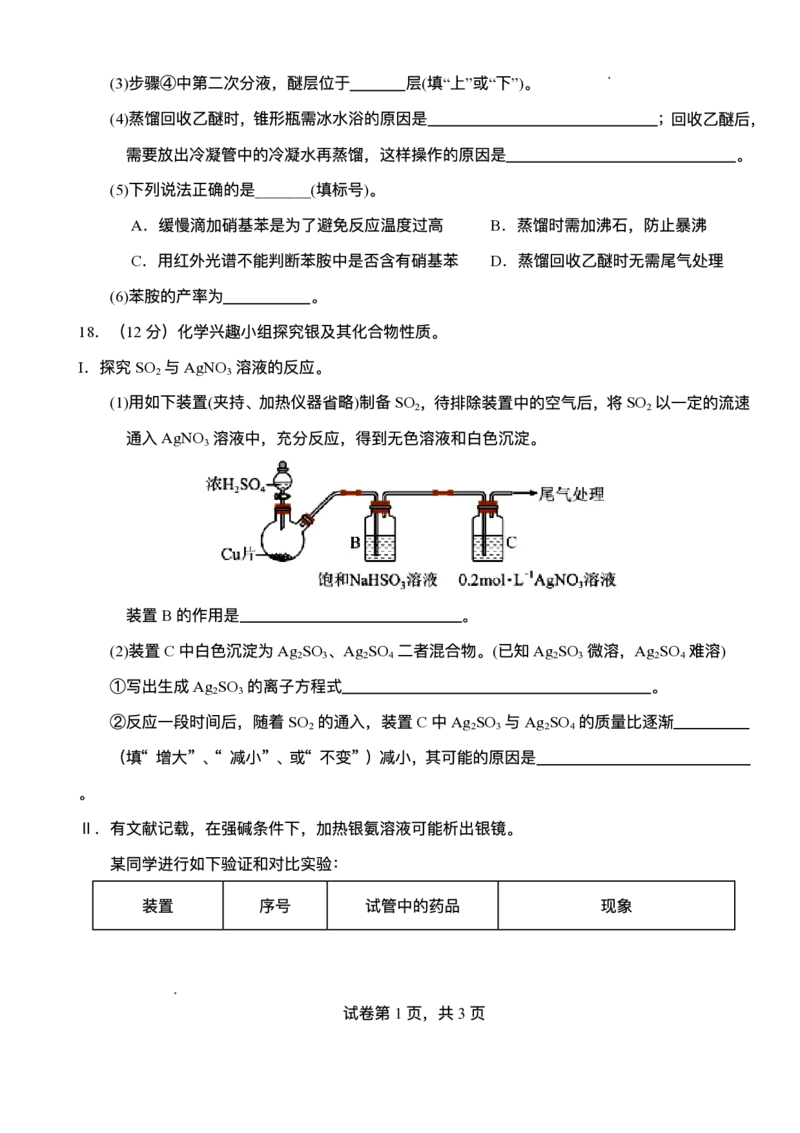
反应装置Ⅰ和蒸馏装置Ⅱ(加热、夹持等装置略)如下:
实验步骤为:
①向装置Ⅰ双颈烧瓶中加⼊ 铁粉、 ⽔及 ⼄酸,加热煮沸 ;
②稍冷后,通过恒压滴液漏⽃缓慢滴⼊ 硝基苯 ,再加热回流 ;
③将装置Ⅰ改成⽔蒸⽓蒸馏装置,蒸馏收集苯胺-⽔馏出液;
④将苯胺-⽔馏出液⽤ 饱和后,转⼊分液漏⽃静置分层,分出有机层;⽔层⽤⼄醚萃取,
分出醚层;合并有机层和醚层,⽤粒状氢氧化钠⼲燥,得到苯胺醚溶液;
⑤将苯胺醚溶液加⼊圆底烧瓶(装置Ⅱ),先蒸馏回收⼄醚,再蒸馏收集 馏分,得到
苯胺。
回答下列问题:
(1)下图中可⽤于实验室保存硝基苯的试剂瓶是 (填标号)。
(2)步骤④中将苯胺-⽔馏出液⽤ 饱和的⽬的是 。
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司(3)步骤④中第⼆次分液,醚层位于 层(填“上”或“下”)。
(4)蒸馏回收⼄醚时,锥形瓶需冰⽔浴的原因是 ;回收⼄醚后,
需要放出冷凝管中的冷凝⽔再蒸馏,这样操作的原因是 。
(5)下列说法正确的是_______(填标号)。
A.缓慢滴加硝基苯是为了避免反应温度过⾼ B.蒸馏时需加沸⽯,防⽌暴沸
C.⽤红外光谱不能判断苯胺中是否含有硝基苯 D.蒸馏回收⼄醚时⽆需尾⽓处理
(6)苯胺的产率为 。
18.(12分)化学兴趣⼩组探究银及其化合物性质。
I.探究SO 与AgNO 溶液的反应。
2 3
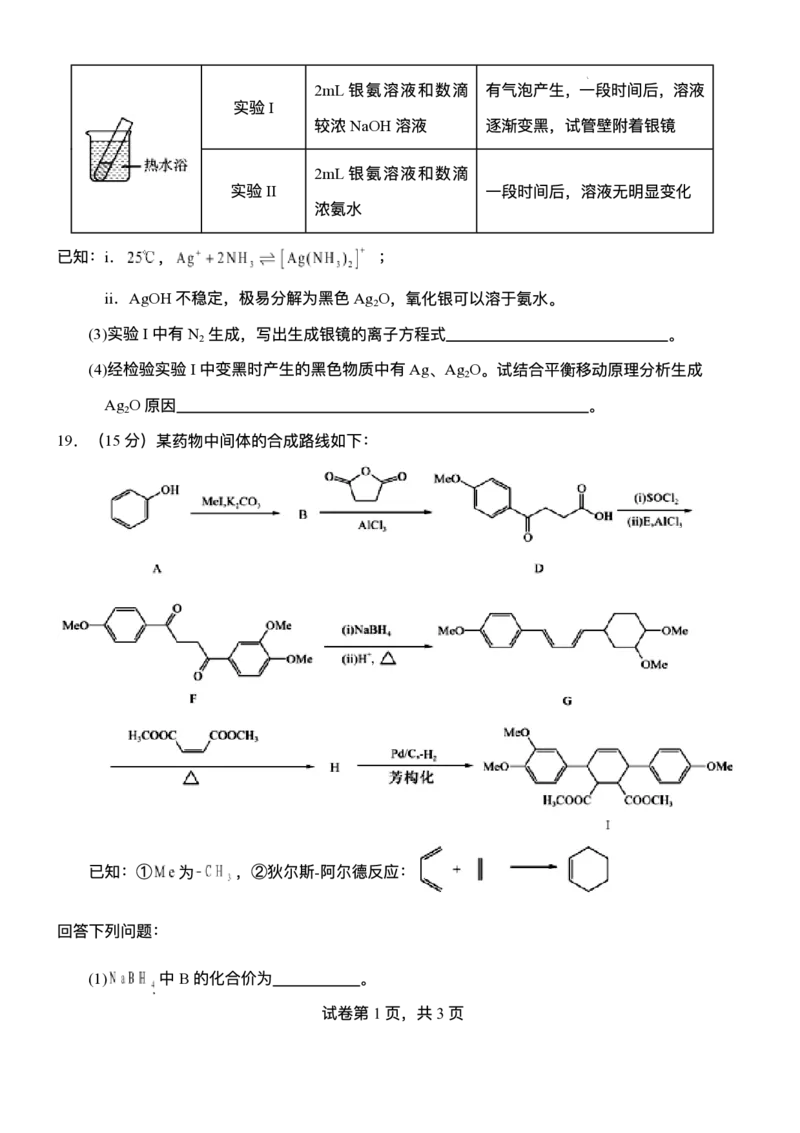
(1)⽤如下装置(夹持、加热仪器省略)制备SO ,待排除装置中的空⽓后,将SO 以⼀定的流速
2 2
通⼊AgNO 溶液中,充分反应,得到⽆⾊溶液和⽩⾊沉淀。
3
装置B的作⽤是 。
(2)装置C中⽩⾊沉淀为Ag SO 、Ag SO ⼆者混合物。(已知Ag SO 微溶,Ag SO 难溶)
2 3 2 4 2 3 2 4
①写出⽣成Ag SO 的离⼦⽅程式 。
2 3
②反应⼀段时间后,随着SO 的通⼊,装置C中Ag SO 与Ag SO 的质量⽐逐渐
2 2 3 2 4
(填“ 增⼤” 、“ 减⼩” 、或“ 不变” )减⼩,其可能的原因是
。
Ⅱ.有⽂献记载,在强碱条件下,加热银氨溶液可能析出银镜。
某同学进⾏如下验证和对⽐实验:
装置 序号 试管中的药品 现象
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司2mL银氨溶液和数滴 有⽓泡产⽣,⼀段时间后,溶液
实验I
较浓NaOH溶液 逐渐变⿊,试管壁附着银镜
2mL银氨溶液和数滴
实验II ⼀段时间后,溶液⽆明显变化
浓氨⽔
已知:i. , ;
ii.AgOH不稳定,极易分解为⿊⾊Ag O,氧化银可以溶于氨⽔。
2
(3)实验I中有N ⽣成,写出⽣成银镜的离⼦⽅程式 。
2
(4)经检验实验I中变⿊时产⽣的⿊⾊物质中有Ag、Ag O。试结合平衡移动原理分析⽣成
2
Ag O原因 。
2
19.(15分)某药物中间体的合成路线如下:
已知:① 为 ,②狄尔斯-阿尔德反应:
回答下列问题:
(1) 中B的化合价为 。
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司(2)有机物B的化学名称为: 。
(3)有机物D中的官能团名称分别为:醚键、 、 。
(4)F→G转化分为两步,第⼀步的反应类型为 ;第⼆步的反应类型为
。
(5)G→H的化学⽅程式为 。
(6)若X是D的同系物,且X的相对分⼦质量⽐D少14,则和X具有相同分⼦式且符合下列
条件的X的同分异构体有 种。
①含有苯环;②苯环上有三个⽀链,其中两个⽀链各含有1个酯基。
其中,核磁共振氢谱显示有5组峰,且峰⾯积之⽐为 的同分异构体的结构简式
为 。(写出1种即可)
试卷第1⻚,共3⻚
学科⽹(北京)股份有限公司⽉⽉考化学试卷答案
8
题⽬ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A C D A A B A B C C A D C D D
1.【详解】A.不锈钢是铁基合⾦,属于⾦属材料;
B.⾦刚⽯是碳的⾮⾦属形态,属于⽆机⾮⾦属材料;
C.⽞武岩纤维是由⽕⼭岩(主要成分为硅酸盐矿物)熔融制成,类似于玻璃纤维,属于⽆机⾮⾦
属材料;
D.玻璃纤维的主要成分是⼆氧化硅等⾮⾦属氧化物,属于⽆机⾮⾦属材料;
2.【详解】A.还原铁粉和维⽣素C都具有还原性,能与氧⽓反应,从⽽防⽌⻝品被氧化,可做
⻝品抗氧化剂,A正确;
B. 虽然有毒,但在⼀定范围内可⽤于⻝品添加剂,如葡萄酒中添加适量 ,可起到杀菌、
抗氧化等作⽤,B错误;
C.碘是合成甲状腺激素的重要元素,⻝盐中加碘酸钾,⽽不是单质碘,C错误;
D.碳酸氢铵、碳酸氢钠可中和酸并受热分解,产⽣⼤量⽓体,使⾯团松软、多孔,可⽤作⻝品膨
松剂,D正确;
3.【详解】A. 按照系统命名法应该为:2,4,6-三硝基甲苯,A错误;
B. 主链上含有5个碳原⼦,两个甲基在3号碳原⼦上,名称为3,3-⼆甲基戊烷,B错误;
C.邻羟基苯甲醛中的氢键,应表示为 ,C错误;
D.Ga为31号元素,基态Ga原⼦的简化电⼦排布式 ,D正确;故选D。
4.【详解】A.检验 时,应先向待测液中加⼊稀盐酸酸化,排除 等的影响,再加⼊BaCl
2
溶液,若出现⽩⾊沉淀,说明待测液中含有 。若加⼊HCl酸化的BaCl 溶液,待测液中含有
2
时会⽣成AgCl⽩⾊沉淀,影响 的检验,A错误;
B.苯甲酸在热⽔中的溶解度较⼤,在冷⽔中较⼩,⽽NaCl在⽔中的溶解度随温度变化不⼤。通
过重结晶,苯甲酸可结晶析出,NaCl留在⺟液中,从⽽实现分离,B正确;
C.苯酚与溴⽔反应⽣成三溴苯酚⽩⾊沉淀,常⽤于定性、定量检测苯酚的存在,C正确;
D.饱和硫酸铵溶液可使蛋⽩质发⽣盐析,过滤后得到的沉淀为蛋⽩质,是分离提纯蛋⽩质的常⽤
⽅法,D正确;故选A。
5.【详解】A.氯⽓先与亚铁离⼦反应,再与溴离⼦反应,另有溴离⼦过量,反应的离⼦⽅程为:
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司2Cl +2Fe2++2Br-=4Cl-+2Fe3++Br ,故A正确;
2 2
B.CuSO 溶液中加⼊⾜量的氨⽔所得产物为[Cu(NH ) ]2+,故B错误;
4 3 4
C.HClO是弱酸,且该反应可逆反应,即为Cl +H O H++Cl-+HClO-,故C错误;
2 2
D.氢氧化钙过量,反应⽣成碳酸钙沉淀和氢氧化镁沉淀(碳酸镁微溶,氢氧化镁难溶),正确的
离⼦⽅程式为:Mg2++2HCO -+2Ca2++4OH-=2CaCO ↓+2H O+Mg(OH) ↓,故D错误;
3 3 2 2
6.【详解】A.向饱和澄清⽯灰⽔中不断通⼊ CO ⽓体,先⽣成碳酸钙沉淀和⽔,恰好完全反应
2
时电导率⼏乎为0,继续通⼊⼆氧化碳,反应⽣成碳酸氢钙,电导率增⼤,故A正确;
B.向 NaOH溶液中滴加相同浓度的 CHCOOH溶液,反应⽣成醋酸钠和⽔,离⼦数⽬⼏乎不变,但
3
溶液体积增⼤,电导率会下降,故B错误;
C.向NaOH溶液中通⼊Cl ⾄恰好完全反应:Cl +2NaOH===NaCl +NaCl O+HO,离⼦数⽬不变,溶液
2 2 2
体积不变,电导率不变,故C正确;
D.向HSO 溶液中加⼊等体积、等物质的量浓度的 溶液,两者反应⽣成硫酸钡沉淀和
2 4
⽔,则完全反应时电导率⼏乎为0,故D正确。
7.【详解】A.浓硫酸与碳加热⽣成SO ,SO 与H S反应⽣成S,两步均正确,A正确;
2 2 2
B.铝热反应⽣成Fe正确,但Fe与Cl₂加热⽣成FeCl 错误(应⽣成FeCl ),B错误;
2 3
C.NH 催化氧化⽣成NO正确,但NO不能直接与⽔反应⽣成HNO (需O₂参与),C错误;
3 3
D.NaCl溶液直接通CO ⽆法⽣成NaHCO (需先通NH ),D错误;故选A。
2 3 3
8.【详解】A.钠⽣成 和 ,都是由0价变为 价,即4.6g钠参与反应,转移电⼦数
为 ,A正确;
B.撞击时发⽣反应的⽅程式为 ,根据⽅程式,1mol 分解,⽣成1mol
氮⽓,在标况下的体积为33.6L,但选项未提供标况条件,B错误;
C.标准状况下, 的物质的量为0.5mol, 键的数⽬为 ,C正确;
D. 和 在⾼温下充分反应⽣成NO,氧⽓过量,NO与氧⽓⽣成 , 部分转化成 ,
发⽣的反应为 、 、 ,同时剩余 ,即最终
⽓体为有⾊的混合⽓体。D正确;
9.【详解】A.催化剂只能改变反应速率,不能使平衡发⽣移动,不能提⾼平衡转化率,A正确;
B.Ru的化合物与⼆氧化碳反应,增加了氧原⼦,发⽣了氧化反应,⼆氧化碳被还原,B正确;
C.由图可知,反应⽅程式为 ,反应中钌元素的化合价没有变化,
氢元素的化合价既升⾼被氧化,⼜降低被还原,氢⽓既是反应的氧化剂也是反应的还原剂,所以
当 转化为 时,氢⽓得到2mol电⼦, 并没有电⼦得失,所以当
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司⽣成时有 电⼦转移,C错误;
D.由图知, 元素在化合物中的化学式分别为 ;氧均形成含氧
化合物,没有形成过氧化物,由化合价代数和为 可知, 元素的化合价不变,D正确;
10.【详解】A.放电时该装置是原电池,是化学能转化成电能,故A错误;
B.放电时 作负极,电极反应式为 , 为难溶物,氢离⼦向右侧移
动,故交换膜左侧的电解质溶液质量减少,,故B错误;
C.充电时该装置是电解池, 作阴极,溶液中的阳离⼦移向阴极,故 通过质⼦交换膜
向左侧电极移动,故C正确;
D.充电时,右侧阳极的电极反应式为 ,每⽣成 ,转移电⼦的物质的量为
1mol,其数⽬为 ,或 ,故D错误;
11.【详解】A.“灼烧”过程中,废铜泥中的⾦属元素转化为⾦属氧化物,硫元素转化为⽓体逸出,
所以“灼烧”可将废铜泥转化为⾦属氧化物,A正确;
B.H O 因为⽣成Fe3+的催化分解⽽应稍过量;加⼊NaOH是为了调节溶液的pH沉淀Fe3+,NaOH
2 2
溶液过量会使Cu2+同时沉淀,减弱除杂效果,B错误;
C.在实验室模拟“过滤”步骤时使⽤的主要玻璃仪器为漏⽃、玻璃棒、烧杯,C错误;
D.“还原”时溶液中反应的离⼦⽅程式为 ,所以
“还原”后“溶液”呈酸性,D错误;
12.【详解】A.加⼊硫酸亚铁,硫酸根离⼦会与溶液中的钡离⼦反应⽣成BaSO 沉淀,故A错误
4
B.向溶液中加⼊Zn粉,铁离⼦会被还原,锌过量时会被置换,故B不符合题意;
C.向溶液中加⼊NaHCO,铁离⼦会与碳酸氢根离⼦发⽣双⽔解反应⽣成氢氧化铁、⼆氧化碳⽓体
3
,故C不符合题意;
D.向溶液中通⼊⼆氧化碳,⼆氧化碳与溶液中离⼦均不发⽣反应,故D符合题意。
13.【详解】A.X是对称结构,核磁共振氢谱有2组峰,A错误;
B. 含有2mol羧基、1mol碳溴键,2mol羧基能消耗2mol 、1mol碳溴键能消耗1mol
,1molY最多可消耗 ,B错误;
C.天冬氨酸含有羧基,能和碱反应,含有氨基能和酸反应⽣成盐,属于两性化合物,C正确;
D.天冬氨酸含有羧基和氨基,可通过缩聚反应可合成聚天冬氨酸,D错误;
14.【详解】A.实验Ⅰ中加⼊KSCN 溶液⽆明显现象,实验Ⅱ中再加⼊少量KSCN 溶液,仍⽆
明显现象,从⽽表明溶液中的现象与 KSCN 溶液的⽤量⽆关,A正确;
B.补铁剂中含有铁元素,实验Ⅰ中加⼊能将Fe2+氧化为Fe3+的H O 溶液后,溶液仍不变红,则
2 2
表明H O 被其它还原剂还原,所以可能是H O 被维⽣素 C 还原了,B正确;
2 2 2 2
C.实验Ⅲ中溶液变红,表明⽣成了Fe(SCN) ,但当H O 加⼊过量后,溶液的红⾊⼜褪去,则表
3 2 2
明Fe(SCN) 的结构被破坏,因为H O 不能氧化Fe3+,所以可能是 H O 将SCN-氧化了,C正确;
3 2 2 2 2
D.实验Ⅲ中加⼊盐酸,Fe2+被H O 氧化为Fe3+,在实验Ⅱ中未加盐酸,Fe2+也被H O 氧化为Fe3
2 2 2 2
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司+[溶液变为红褐⾊,表明反应⽣成了+3价的Fe,所以该补铁剂中+2 价铁被H O 氧化并不⼀定需
2 2
要酸性条件,D不正确;
15.【分析】 、 ,根据 可知,当 时,
对应的 ⼤,pH数值⼩,因此 ,
,以此解题。
【详解】A. ,当溶液中
时, ,pH=2.5,A正确;
B.当溶液呈中性时, ,由两步电离平衡常数可知, ,
,同理: , ,B正确;
C.实验2的离⼦⽅程式: ,平衡常数:
,
平衡常数较⼤,该反应进⾏的程度较⼤,判断可产⽣沉淀;或进⾏定量计算,两步电离平衡反应
式相加,得到 ,⼆者等体积混合, ,列三
段式: ,则 ,估算x的数量级为 ,故
,故有沉淀⽣成,C正确;
D.电荷守恒中右侧缺少了 的浓度项,D错误;故选D。
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司16.【答案】(每空2分,共14分)
(1) (2) (3)4
(4)将 氧化为 (便于沉淀得 )(5)
(6)
【详解】(1) 、 加⼊硫酸, 与盐酸反应⽣成 、Fe2+, 与盐
酸反应⽣成Mg2+, 和硫酸不反应,滤渣是 ;
(3) ( 为+4价),设 中过氧键的数⽬为x,即
,解得x=4;
(6)每个晶胞中有4个 单元,晶胞的体积为:
,即其密度为
;充电过程 脱出部分 ,转化为 ,电极反应式为:
。
17.【答案】(每空2分,共14分)
(1)C
(2)盐析(降低苯胺的溶解度,使其析出,提升产率)
(3)上
(4) 防⽌其挥发损失并提⾼冷凝效率
防⽌⾼温蒸馏时冷凝管因温差过⼤⽽破裂
(5)AB (6)75%
【分析】由硝基苯制苯胺过程中,由于反应⽐较剧烈,故硝基苯需从上⽅缓慢加⼊;反应完成后,
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司改⽤蒸馏装置,将苯胺-⽔蒸馏出,苯胺在⽔中有⼀定的溶解度,加⼊NaCl固体,可使溶解在⽔
中的⼤部分苯胺就以油状物晶体析出,分液分离出有机层,⽔层⽤⼄醚萃取,分出醚层;合并有
机层和醚层,加⼊粒状氢氧化钠⼲燥,得到苯胺醚溶液,再次蒸馏得到苯胺,据此解答。
【详解】(1)硝基苯在常温下是液态有机物,对光的稳定性较强,可保存在带磨砂玻璃塞的细⼝
瓶中,故选C;(若使⽤橡胶塞,硝基苯作为有机溶剂可能会溶解橡胶中的有机成分)
(2)由于苯胺在⽔中有⼀定溶解度,利⽤盐析效应,加⼊NaCl固体,溶液中离⼦浓度增加,会
争夺⽔分⼦,导致苯胺的溶解度降低,溶解在⽔中的⼤部分苯胺就会以油状物晶体析出,提升实
验产率;
(3)⼄醚密度⼩于⽔,故醚层位于上层;
(4)⼄醚沸点低(34.5℃),冰⽔浴可防⽌其挥发损失并提⾼冷凝效率;
放空冷凝管中的冷凝⽔再蒸馏是为了收集苯胺,其沸点较⾼(当馏分沸点>140℃,⼀般利
⽤空⽓冷凝),这样操作的原因是:防⽌⾼温下冷凝管因温差过⼤破裂
(5)A.缓慢滴加是为了控制反应温度,因为该反应为放热反应,若温度过⾼,反应会太剧烈,
同时产物苯胺会与⼄酸也可能发⽣取代反应,导致产率下降,故A正确;
B.蒸馏时加沸⽯防暴沸是正确的操作,B正确;
C.红外光谱可区分硝基苯(含硝基特征峰)和苯胺(含氨基特征峰),C错误;
D.⼄醚是⼀种有毒物质,具有挥发性,尾⽓需要处理,D错误;故选AB;
(6)根据反应原理可知,0.08mol硝基苯,理论上制备0.08mol苯胺,理论产量:0.08mol×93g/mol
=7.44g,实际产量:5.58g,产率: 75% 。
18.【答案】(每空2分,共12分)
(1)观察 ⽓体流速,同时吸收硫酸酸雾(答出⼀条即可)
(2)2Ag++SO +H O=Ag SO ↓+2H+
2 2 2 3
减⼩ 随着反应的进⾏,溶液酸性增强, 氧化性增强,更多的 被氧化为
(或⽤离⼦⽅程式解释 )
(3)
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司(4)在 存在下,加热促进 分解⽽逸出 ,促使 平衡
正向移动, 浓度增⼤并与 反应,⽴即转化为 ( )。
[或总反应为 加热时,NH 逸出,平衡右移,所以
3
能⽣成 ]
19.【答案】(除标注外,每空2分,共15分)
(1) +3(1分)
(2)苯甲醚(或甲苯醚) (2分)
(3)酮羰基、羧基 (2分)
(4)还原反应 消去反应
(5)
(6) 36 或
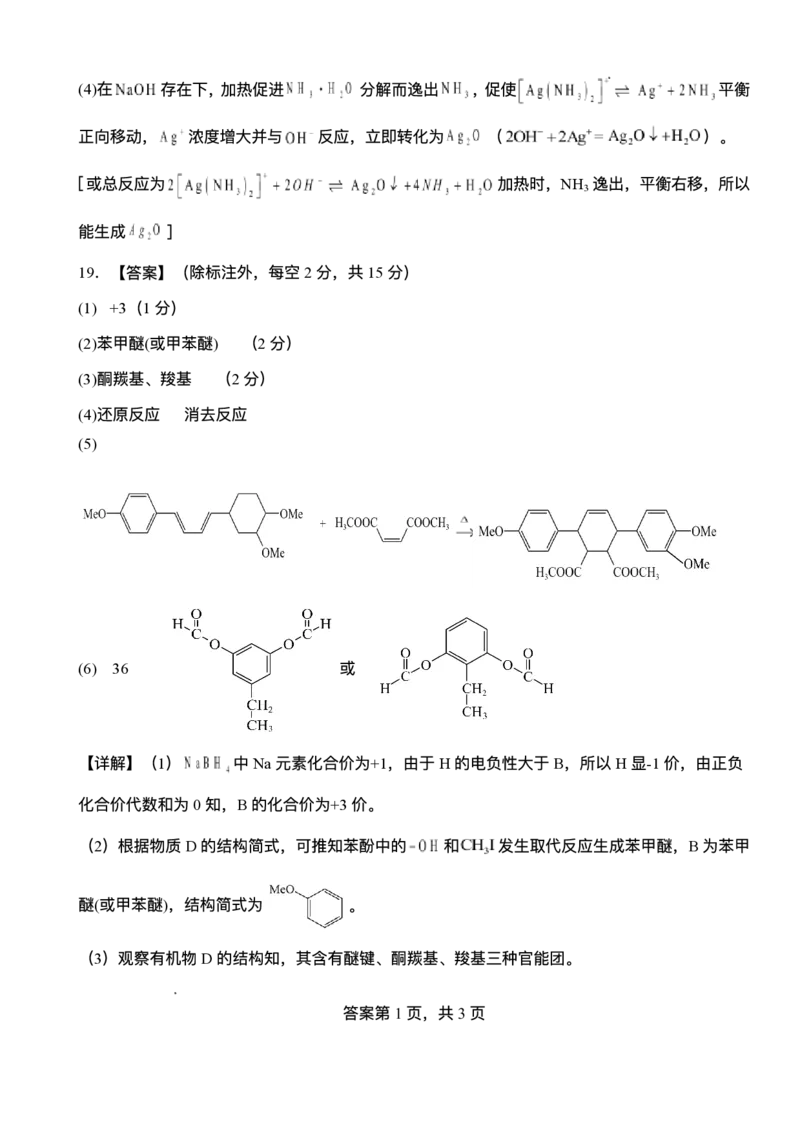
【详解】(1) 中Na元素化合价为+1,由于H的电负性⼤于B,所以H显-1价,由正负
化合价代数和为0知,B的化合价为+3价。
(2)根据物质D的结构简式,可推知苯酚中的 和 发⽣取代反应⽣成苯甲醚,B为苯甲
醚(或甲苯醚),结构简式为 。
(3)观察有机物D的结构知,其含有醚键、酮羰基、羧基三种官能团。
答案第1⻚,共3⻚
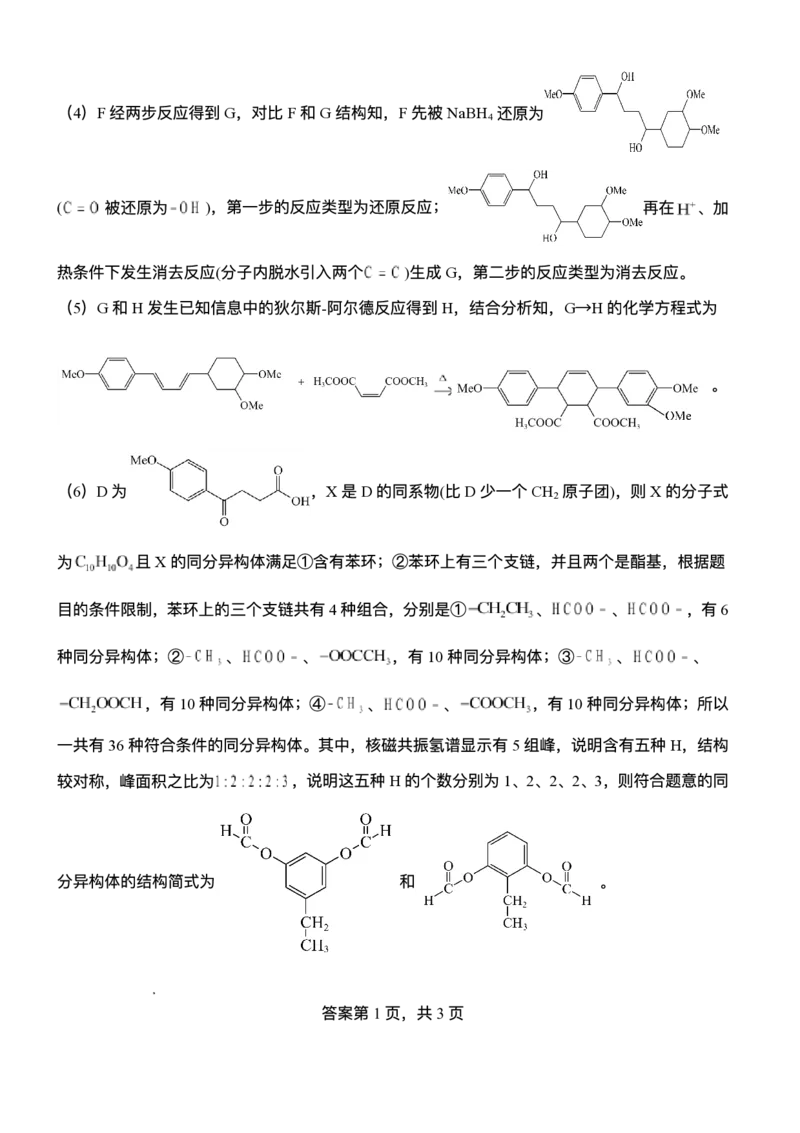
学科⽹(北京)股份有限公司(4)F经两步反应得到G,对⽐F和G结构知,F先被NaBH 还原为
4
( 被还原为 ),第⼀步的反应类型为还原反应; 再在 、加
热条件下发⽣消去反应(分⼦内脱⽔引⼊两个 )⽣成G,第⼆步的反应类型为消去反应。
(5)G和H发⽣已知信息中的狄尔斯-阿尔德反应得到H,结合分析知,G→H的化学⽅程式为
。
(6)D为 ,X是D的同系物(⽐D少⼀个CH 原⼦团),则X的分⼦式
2
为 且X的同分异构体满⾜①含有苯环;②苯环上有三个⽀链,并且两个是酯基,根据题
⽬的条件限制,苯环上的三个⽀链共有4种组合,分别是① 、 、 ,有6
种同分异构体;② 、 、 ,有10种同分异构体;③ 、 、
,有10种同分异构体;④ 、 、 ,有10种同分异构体;所以
⼀共有36种符合条件的同分异构体。其中,核磁共振氢谱显示有5组峰,说明含有五种H,结构
较对称,峰⾯积之⽐为 ,说明这五种H的个数分别为1、2、2、2、3,则符合题意的同
分异构体的结构简式为 和 。
答案第1⻚,共3⻚
学科⽹(北京)股份有限公司