文档内容
专题48 化学电源——燃料电池
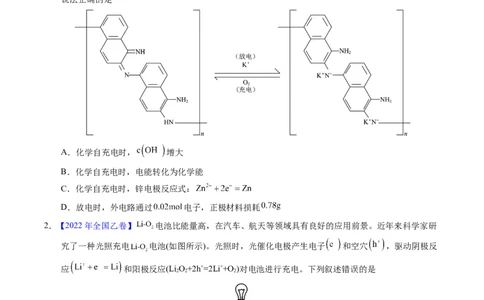
1.【2022年福建卷】一种化学“自充电”的锌-有机物电池,电解质为 和 水溶液。将
电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列
说法正确的是
A.化学自充电时, 增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过 电子,正极材料损耗
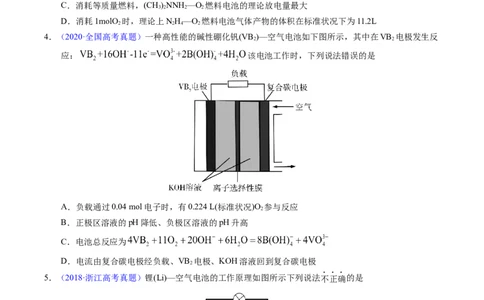
2.【2022年全国乙卷】 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研
究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极反
应 和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
3.(2021·山东真题)以KOH溶液为离子导体,分别组成CHOH—O、NH—O、(CH)NNH—O 清洁
3 2 2 4 2 3 2 2 2
燃料电池,下列说法正确的是
A.放电过程中,K+均向负极移动
B.放电过程中,KOH物质的量均减小
C.消耗等质量燃料,(CH)NNH—O 燃料电池的理论放电量最大
3 2 2 2
D.消耗1molO 时,理论上NH—O 燃料电池气体产物的体积在标准状况下为11.2L
2 2 4 2
4.(2020·全国高考真题)一种高性能的碱性硼化钒(VB )—空气电池如下图所示,其中在VB 电极发生反
2 2
应: 该电池工作时,下列说法错误的是
A.负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B.正极区溶液的pH降低、负极区溶液的pH升高
C.电池总反应为
D.电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
5.(2018·浙江高考真题)锂(Li)—空气电池的工作原理如图所示下列说法不正确的是
A.金属锂作负极,发生氧化反应
B.Li+通过有机电解质向水溶液处移动
C.正极的电极反应:O+4e—==2O2—
2D.电池总反应:4Li+O+2H O==4LiOH
2 2
6.(2019·全国高考真题)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与
酶之间传递电子,示意图如下所示。下列说法错误的是
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应H+2MV2+ 2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
7.(2017·浙江高考真题)金属(M)-空气电池的工作原理如图所示。下列说法不正确的是
A.金属M作电池负极
B.电解质是熔融的MO
C.正极的电极反应
D.电池反应
8.(2016·浙江高考真题)MgHO 电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意
2 2
图如图。下列说法不正确的是( )
A.石墨电极是该电池的正极
B.石墨电极上发生还原反应
C.Mg电极的电极反应式:Mg-2e-=Mg2+
D.电池工作时,电子从Mg电极经导线流向石墨电极,再由石墨电极经电解质溶液流向Mg电极
9.(2012·北京高考真题)人工光合作用能够借助太阳能,用CO 和HO制备化学原料。下图是通过人工
2 2
光合作用制备HCOOH的原理示意图,下列说法不正确的是A.该过程是将太阳能转化为化学能的过程
B.催化剂a表面发生氧化反应,有O 产生
2
C.催化剂a附近酸性减弱,催化剂b附近酸性增强
D.催化剂b表面的反应是CO+2H++2e一=HCOOH
2
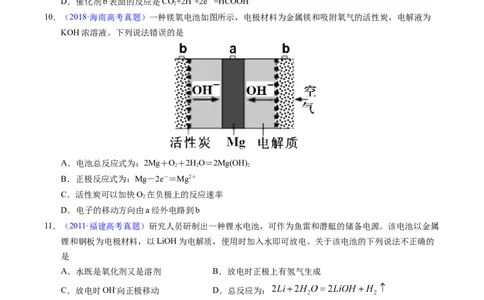
10.(2018·海南高考真题)一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为
KOH浓溶液。下列说法错误的是
A.电池总反应式为:2Mg+O+2HO=2Mg(OH)
2 2 2
B.正极反应式为:Mg-2e-=Mg2+
C.活性炭可以加快O 在负极上的反应速率
2
D.电子的移动方向由a经外电路到b
11.(2011·福建高考真题)研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属
锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的
是
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成
C.放电时OH-向正极移动 D.总反应为:
12.(2008·北京高考真题)据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动
员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A.正极反应式为:O+2H O+4e-====4OH-
2 2
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H+O ====2H O
2 2 2
D.用该电池电解CuCl 溶液,产生2.24 L Cl (标准状况)时,有0.1 mol电子转移
2 2
13.(2008·宁夏高考真题)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧
化碳。该电池负极发生的反应是A.CHOH(g)+O (g)=HO(1)+CO (g)+2H+(aq)+2e-
3 2 2 2
B.O(g)+4H+(aq)+4e-=2H O(1)
2 2
C.CHOH(g)+H O(1)=CO (g)+6H+(aq)+6e–
3 2 2
D.O(g)+2HO(1)+4e–=4OH-
2 2
14.(2017·上海高考真题)能量转化率大;氧化剂和还原剂可以不断从外部输入;电极产物可以不断输出;
且能代替汽油作为汽车的动力,能持续使用的新型电池为
A.锂电池 B.燃料电池
C.干电池 D.铅蓄电池
15.(2016·全国高考真题)锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,
反应为2Zn+O +4OH–+2H O===2Zn(OH) 2-。下列说法正确的是( )
2 2 4
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-) 逐渐减小
C.放电时,负极反应为:Zn+4OH–-2e–= Zn(OH) 2-
4
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
16.(2015·全国高考真题)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如
图所示。下列有关微生物电池的说法错误的是
A.正极反应中有CO 生成
2
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C H O+6O =6CO +6H O
6 12 6 2 2 2
17.(2013·安徽高考真题)热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所
示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:
PbSO +2LiCl+Ca = CaCl +Li SO +Pb。下列有关说法正确的是
4 2 2 4
A.正极反应式:Ca + 2Cl--2e- = CaCl
2
B.放电过程中,Li+向负极移动
C.每转移0.1mol电子,理论上生成20.7 g PbD.常温时,在正负极间接上电流表或检流计,指针不偏转
18.(2012·四川高考真题)一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CHCHOH
3 2
– 4e-+ H O = CH COOH + 4H+。下列有关说法正确的是
2 3
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为:CHCHOH + O = CHCOOH + H O
3 2 2 3 2
D.正极上发生的反应为:O+ 4e-+ 2H O = 4OH-
2 2
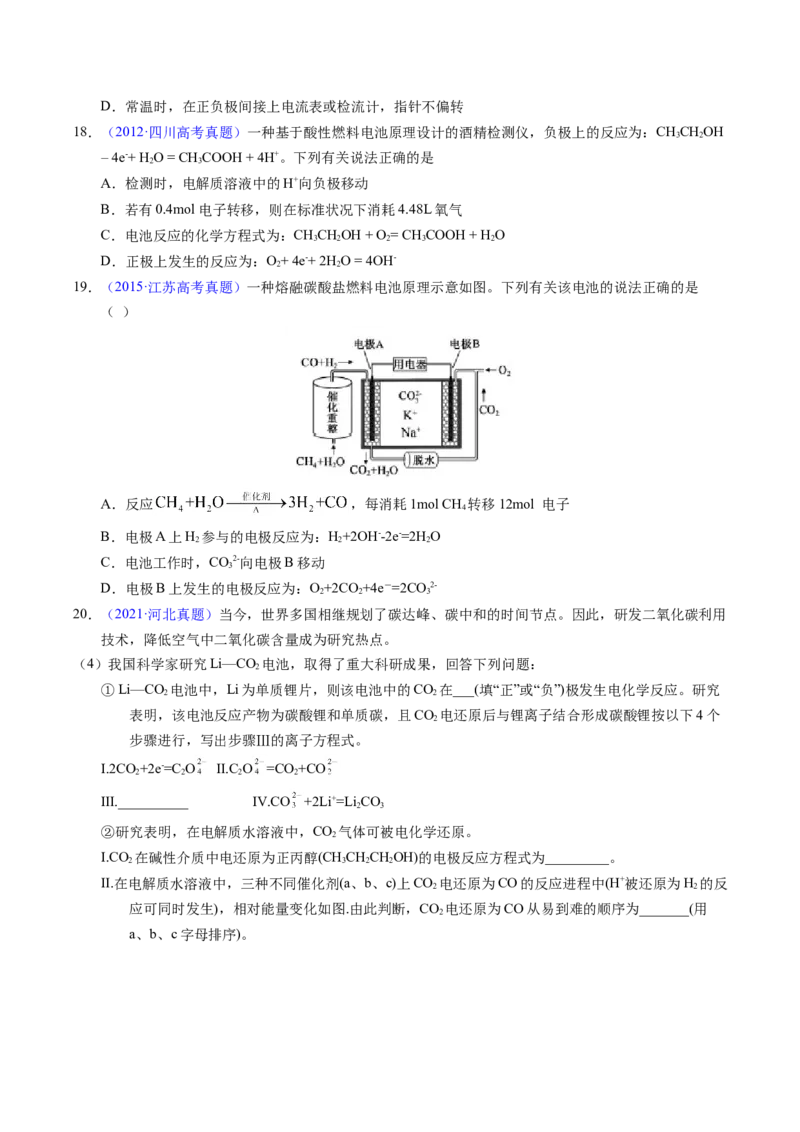
19.(2015·江苏高考真题)一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
( )
A.反应 ,每消耗1mol CH 转移12mol 电子
4
B.电极A上H 参与的电极反应为:H+2OH--2e-=2H O
2 2 2
C.电池工作时,CO2-向电极B移动
3
D.电极B上发生的电极反应为:O+2CO +4e-=2CO 2-
2 2 3
20.(2021·河北真题)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用
技术,降低空气中二氧化碳含量成为研究热点。
(4)我国科学家研究Li—CO 电池,取得了重大科研成果,回答下列问题:
2
①Li—CO 电池中,Li为单质锂片,则该电池中的CO 在___(填“正”或“负”)极发生电化学反应。研究
2 2
表明,该电池反应产物为碳酸锂和单质碳,且CO 电还原后与锂离子结合形成碳酸锂按以下4个
2
步骤进行,写出步骤Ⅲ的离子方程式。
Ⅰ.2CO +2e-=C O Ⅱ.C O =CO +CO
2 2 2 2
Ⅲ.__________ Ⅳ.CO +2Li+=Li CO
2 3
②研究表明,在电解质水溶液中,CO 气体可被电化学还原。
2
Ⅰ.CO 在碱性介质中电还原为正丙醇(CHCHCHOH)的电极反应方程式为_________。
2 3 2 2
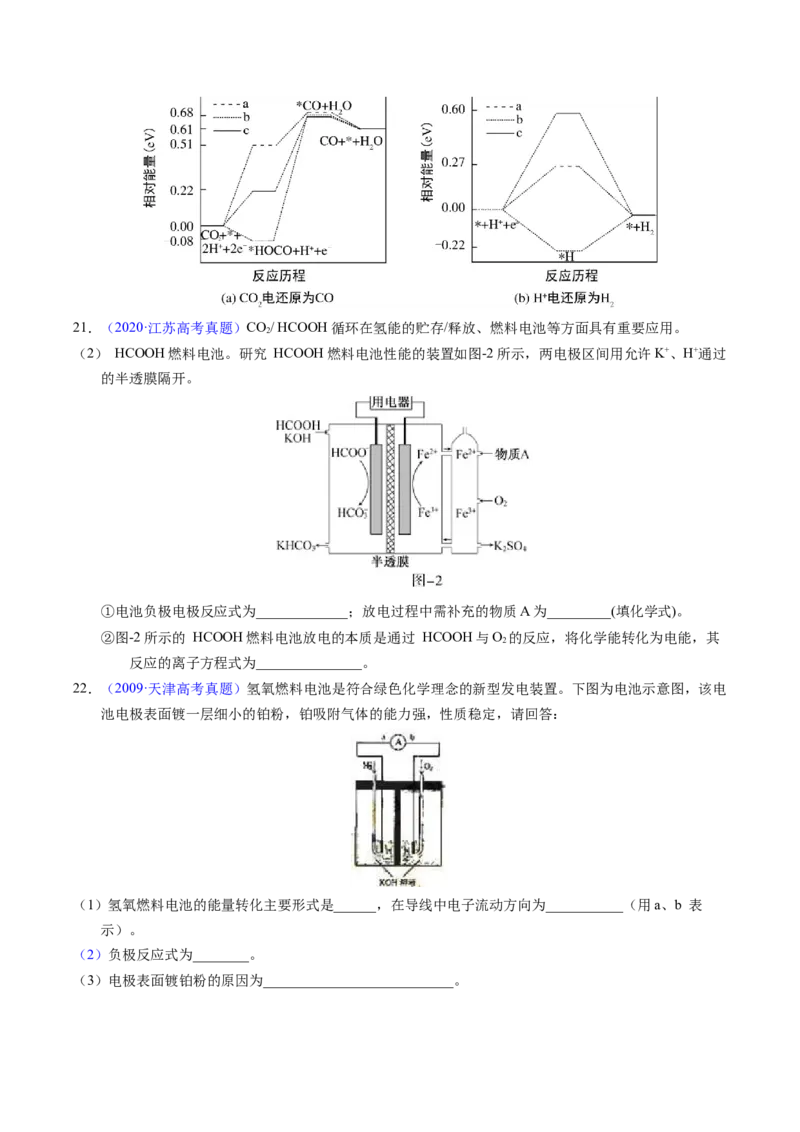
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO 电还原为CO的反应进程中(H+被还原为H 的反
2 2
应可同时发生),相对能量变化如图.由此判断,CO 电还原为CO从易到难的顺序为_______(用
2
a、b、c字母排序)。21.(2020·江苏高考真题)CO/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
2
(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过
的半透膜隔开。
①电池负极电极反应式为_____________;放电过程中需补充的物质A为_________(填化学式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O 的反应,将化学能转化为电能,其
2
反应的离子方程式为_______________。
22.(2009·天津高考真题)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电
池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是______,在导线中电子流动方向为___________(用a、b 表
示)。
(2)负极反应式为________。
(3)电极表面镀铂粉的原因为___________________________。