文档内容
秘密★启用前
2025年9月
绵阳南山中学高 2023 级高三第二次教学质量检测
化学试题
命题人:仲竞之 罗珍 审题人:张明盛
本试卷分为试题卷和答题卡两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)
组成,共7页;答题卡共2页。满分100分,考试时间75分钟。
可能用到的相对原子质量:H1 B11 O16 N14 Na23 P31 Fe56
一、单选题(共15小题,每小题3分,共45分。每小题仅一个选项最符合题意)
1.下列关于九三阅兵中涉及到的材料不属于有机化合物的是
A.绚丽彩烟是飞机喷射高沸点的汽油、煤油等油液而形成的
B.坦克涂有耐化学腐蚀的脂肪族聚氨酯伪装涂料
C.隐形飞机发动机外部涂有超高密度的碳质吸波材料
D.迷彩服面料一般都采用化学合成纤维制成
2.下列化学用语表示正确的是
A.基态氧原子的轨道表示式:
B.用电子式表示HCl的形成过程为
C.NaCl溶液中的水合离子为
D.中子数为21的钾核素:21K
19
3.钠及其化合物的部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是
A
① ② ③ ④
NaCl Na Na O NaOH NaClO
电解 O 2 2 HO Cl
2 2 2
A.反应①采用电解饱和食盐水冶炼Na
B.反应②中Na O 只含有离子键
2 2
C.反应③中1molNa O 与足量H O反应转移电子的数目为N
2 2 2 A
D.向反应④的产物NaClO溶液中通入少量的CO ,生成纯碱和HClO
2
4.关于实验安全和化学试剂的保存与处理,下列叙述正确的是
A.检验完SO2-后的废液,先倒入水槽,再用水冲入下水道
4
B.中学实验室中,未用完的钾、白磷可放回原试剂瓶
C.盛有液溴的棕色广口瓶中加水液封,并盖好橡胶塞
D.金属汞一旦洒落在实验室地面或桌面时,须尽可能收集、深埋处理
5.下列离子方程式正确的是
A.向AlCl 溶液中加入过量的氨水:Al3++4NH ·H O=[Al(OH) ]—+4NH+
3 3 2 4 4
B.NaHCO 溶液中通入少量Cl : Cl +HCO-==Cl-+HClO+CO
3 2 2 3 2
C.食醋去除水垢中的CaCO :CaCO +2H+==Ca2++H O+CO ↑
3 3 2 2
D.侯氏制碱法: 2Na++2NH +CO +H O==Na CO ↓+2NH+
3 2 2 2 3 4
6.只用一种试剂将Na SO 、(NH ) CO 、AlCl 、KNO 四种物质溶液区分开,该试剂是
2 4 4 2 3 3 3
A.NaOH溶液 B.Ba(OH) 溶液 C.H SO 溶液 D.AgNO 溶液
2 2 4 3
试卷第1页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}7.中医药学是中国传统文化的瑰宝。a-山道年是一种蒿类植物提取物,有驱虫功能,其结
构如图所示。下列关于该分子的说法错误的是
A.最多能与3molH 发生加成反应 B.手性碳原子数目为4
2
C.该分子中sp2杂化的碳原子数目为6 D.能与2molNaOH发生反应
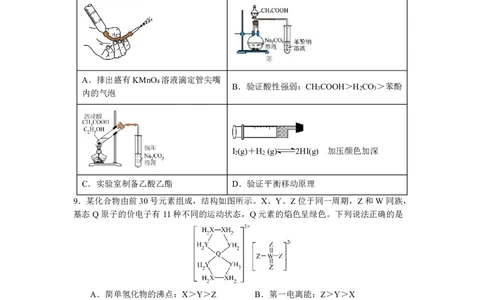
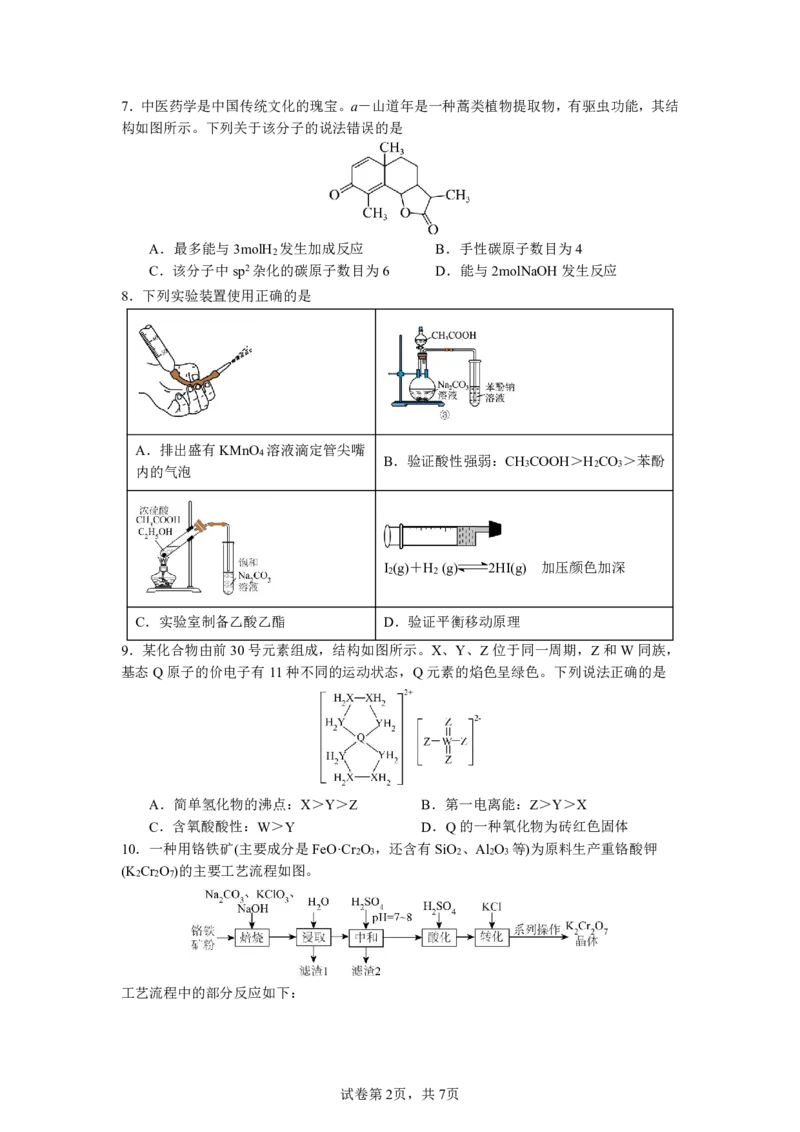
8.下列实验装置使用正确的是
A.排出盛有KMnO 溶液滴定管尖嘴
4
B.验证酸性强弱:CH COOH>H CO >苯酚
3 2 3
内的气泡
I (g)+H (g) 2HI(g) 加压颜色加深
2 2
C.实验室制备乙酸乙酯 D.验证平衡移动原理
9.某化合物由前30号元素组成,结构如图所示。X、Y、Z位于同一周期,Z和W同族,
基态Q原子的价电子有11种不同的运动状态,Q元素的焰色呈绿色。下列说法正确的是
A.简单氢化物的沸点:X>Y>Z B.第一电离能:Z>Y>X
C.含氧酸酸性:W>Y D.Q的一种氧化物为砖红色固体
10.一种用铬铁矿(主要成分是FeO·Cr O ,还含有SiO 、Al O 等)为原料生产重铬酸钾
2 3 2 2 3
(K Cr O )的主要工艺流程如图。
2 2 7
工艺流程中的部分反应如下:
试卷第2页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}高温
①焙烧:6FeO·Cr O +12Na CO +7KClO ====12Na CrO +7KCl+12CO ↑+3Fe O
2 3 2 3 3 2 4 2 2 3
②酸化: 2CrO2-+2H+ Cr O2- +H O
4 2 7 2
下列有关叙述正确的是
A.滤渣1的主要成分为SiO
2
B.中和的目的是除铁和铝
C.酸化的现象为溶液颜色由橙色变为黄色
D.系列操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
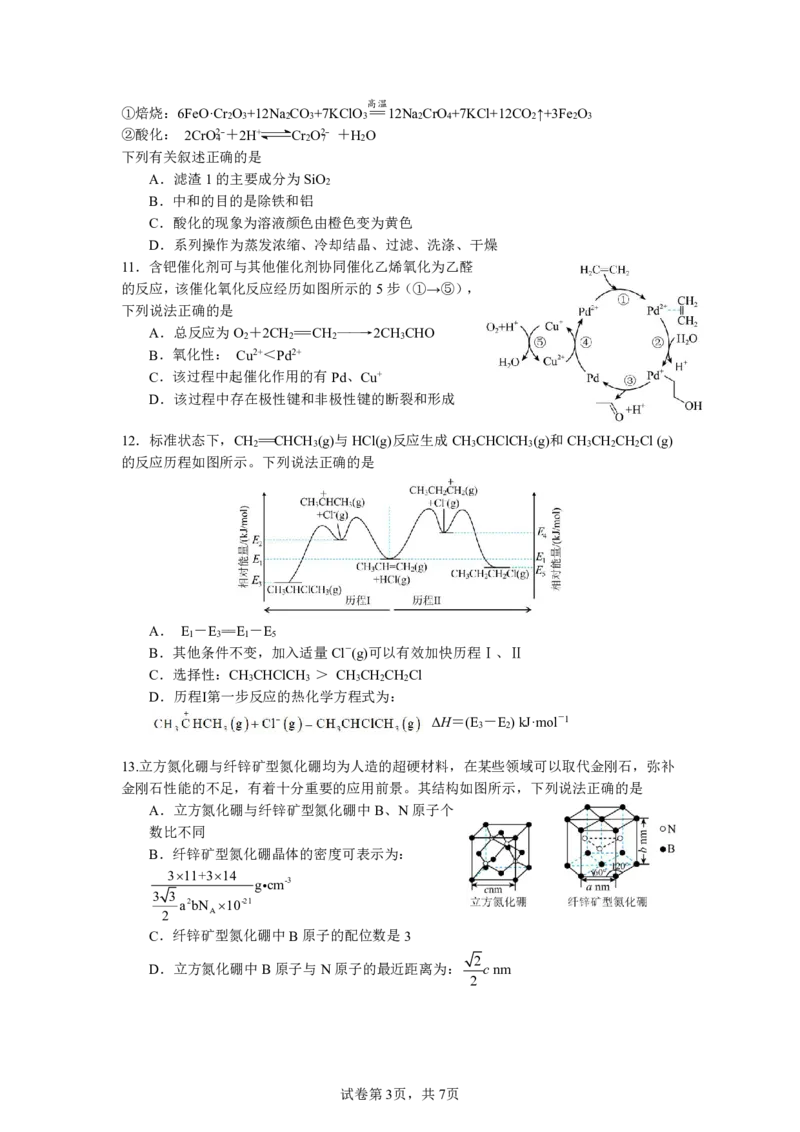
11.含钯催化剂可与其他催化剂协同催化乙烯氧化为乙醛
的反应,该催化氧化反应经历如图所示的5步(①→⑤),
下列说法正确的是
A.总反应为O +2CH ==CH ——→2CH CHO
2 2 2 3
B.氧化性: Cu2+<Pd2+
C.该过程中起催化作用的有Pd、Cu+
D.该过程中存在极性键和非极性键的断裂和形成
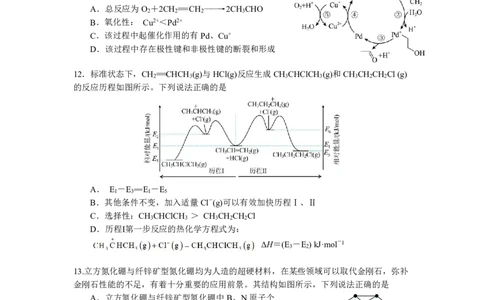
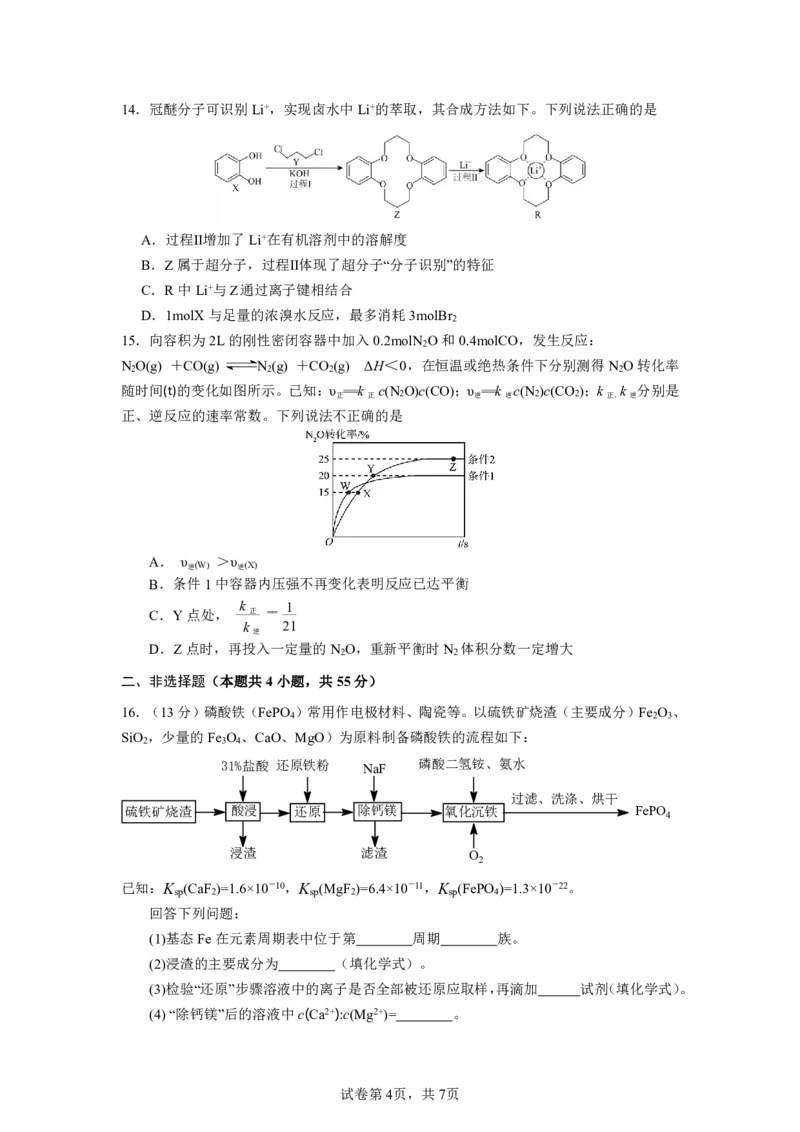
12.标准状态下,CH ==CHCH (g)与HCl(g)反应生成CH CHClCH (g)和CH CH CH Cl(g)
2 3 3 3 3 2 2
的反应历程如图所示。下列说法正确的是
A. E -E ==E -E
1 3 1 5
B.其他条件不变,加入适量Cl-(g)可以有效加快历程Ⅰ、Ⅱ
C.选择性:CH CHClCH > CH CH CH Cl
3 3 3 2 2
D.历程Ⅰ第一步反应的热化学方程式为:
ΔH=(E -E )kJ·mol-1
3 2
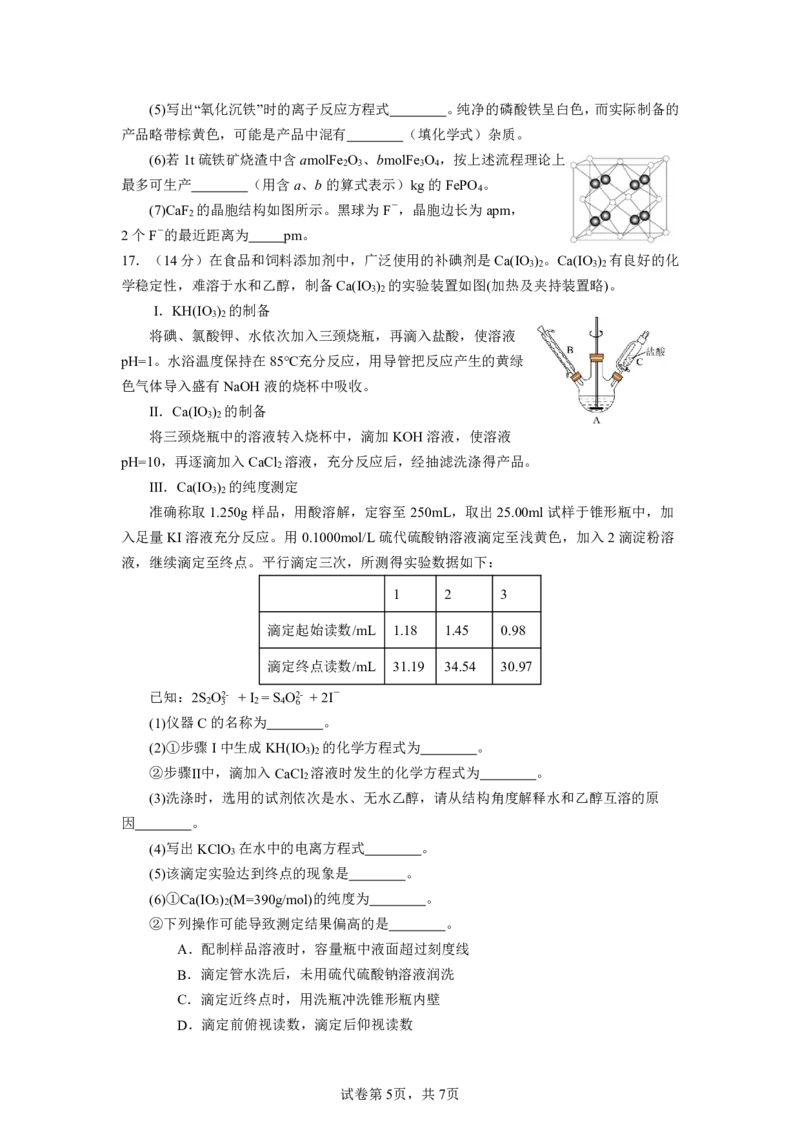
13.立方氮化硼与纤锌矿型氮化硼均为人造的超硬材料,在某些领域可以取代金刚石,弥补
金刚石性能的不足,有着十分重要的应用前景。其结构如图所示,下列说法正确的是
A.立方氮化硼与纤锌矿型氮化硼中B、N原子个
数比不同
B.纤锌矿型氮化硼晶体的密度可表示为:
311+314
gcm-3
3 3
a2bN 10-21
2 A
C.纤锌矿型氮化硼中B原子的配位数是3
2
D.立方氮化硼中B原子与N原子的最近距离为: ccnnmm
2
试卷第3页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}14.冠醚分子可识别Li+,实现卤水中Li+的萃取,其合成方法如下。下列说法正确的是
A.过程Ⅱ增加了Li+在有机溶剂中的溶解度
B.Z属于超分子,过程Ⅱ体现了超分子“分子识别”的特征
C.R中Li+与Z通过离子键相结合
D.1molX与足量的浓溴水反应,最多消耗3molBr
2
15.向容积为2L的刚性密闭容器中加入0.2molN O和0.4molCO,发生反应:
2
N O(g) +CO(g) N (g) +CO (g) ΔH<0,在恒温或绝热条件下分别测得N O转化率
2 2 2 2
随时间(t)的变化如图所示。已知:υ ==k c(N O)c(CO);υ ==k c(N )c(CO );k k 分别是
正 正 2 逆 逆 2 2 正、 逆
正、逆反应的速率常数。下列说法不正确的是
A. υ >υ
逆(W) 逆(X)
B.条件1中容器内压强不再变化表明反应已达平衡
k 1
C.Y点处, 正 ==
k 21
逆
D.Z点时,再投入一定量的N O,重新平衡时N 体积分数一定增大
2 2
二、非选择题(本题共4小题,共55分)
16.(13分)磷酸铁(FePO )常用作电极材料、陶瓷等。以硫铁矿烧渣(主要成分)Fe O 、
4 2 3
SiO ,少量的Fe O 、CaO、MgO)为原料制备磷酸铁的流程如下:
2 3 4
31%盐酸 还原铁粉 磷酸二氢铵、氨水
NaF
过滤、洗涤、烘干
硫铁矿烧渣 酸浸 还原 除钙镁 氧化沉铁 FePO
4
浸渣 滤渣
O
2
已知:K (CaF )=1.6×10-10,K (MgF )=6.4×10-11,K (FePO )=1.3×10-22。
sp 2 sp 2 sp 4
回答下列问题:
(1)基态Fe在元素周期表中位于第 周期 族。
(2)浸渣的主要成分为 (填化学式)。
(3)检验“还原”步骤溶液中的离子是否全部被还原应取样,再滴加 试剂(填化学式)。
(4)“除钙镁”后的溶液中c(Ca2+):c(Mg2+)= 。
试卷第4页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}(5)写出“氧化沉铁”时的离子反应方程式 。纯净的磷酸铁呈白色,而实际制备的
产品略带棕黄色,可能是产品中混有 (填化学式)杂质。
(6)若1t硫铁矿烧渣中含amolFe O 、bmolFe O ,按上述流程理论上
2 3 3 4
最多可生产 (用含a、b的算式表示)kg的FePO 。
4
(7)CaF 的晶胞结构如图所示。黑球为F-,晶胞边长为apm,
2
2个F-的最近距离为 pm。
17.(14分)在食品和饲料添加剂中,广泛使用的补碘剂是Ca(IO ) 。Ca(IO ) 有良好的化
3 2 3 2
学稳定性,难溶于水和乙醇,制备Ca(IO ) 的实验装置如图(加热及夹持装置略)。
3 2
Ⅰ.KH(IO ) 的制备
3 2
将碘、氯酸钾、水依次加入三颈烧瓶,再滴入盐酸,使溶液
pH=1。水浴温度保持在85℃充分反应,用导管把反应产生的黄绿
色气体导入盛有NaOH液的烧杯中吸收。
Ⅱ.Ca(IO ) 的制备
3 2
将三颈烧瓶中的溶液转入烧杯中,滴加KOH溶液,使溶液
pH=10,再逐滴加入CaCl 溶液,充分反应后,经抽滤洗涤得产品。
2
Ⅲ.Ca(IO ) 的纯度测定
3 2
准确称取1.250g样品,用酸溶解,定容至250mL,取出25.00ml试样于锥形瓶中,加
入足量KI溶液充分反应。用0.1000mol/L硫代硫酸钠溶液滴定至浅黄色,加入2滴淀粉溶
液,继续滴定至终点。平行滴定三次,所测得实验数据如下:
1 2 3
滴定起始读数/mL 1.18 1.45 0.98
滴定终点读数/mL 31.19 34.54 30.97
已知:2S O2- +I =S O2- +2I-
2 3 2 4 6
(1)仪器C的名称为 。
(2)①步骤I中生成KH(IO ) 的化学方程式为 。
3 2
②步骤Ⅱ中,滴加入CaCl 溶液时发生的化学方程式为 。
2
(3)洗涤时,选用的试剂依次是水、无水乙醇,请从结构角度解释水和乙醇互溶的原
因 。
(4)写出KClO 在水中的电离方程式 。
3
(5)该滴定实验达到终点的现象是 。
(6)①Ca(IO ) (M=390g/mol)的纯度为 。
3 2
②下列操作可能导致测定结果偏高的是 。
A.配制样品溶液时,容量瓶中液面超过刻度线
B.滴定管水洗后,未用硫代硫酸钠溶液润洗
C.滴定近终点时,用洗瓶冲洗锥形瓶内壁
D.滴定前俯视读数,滴定后仰视读数
试卷第5页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}18.(13分)乙烯是重要的基础化工原料,工业上利用乙烷脱氢制乙烯的相关反应如下:
反应Ⅰ: C H (g) C H (g)+H (g) ΔH =+137kJ·mol-1
2 6 2 4 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH =+41kJ·mol-1
2 2 2 2
(1)反应C H (g)+CO (g) C H (g)+CO(g)+H O(g) 的ΔH = kJ·mol-1。
2 6 2 2 4 2 3
(2)以C H 和N 的混合气体为起始投料(N 不参与反应),保持混合气体总物质的量不变,
2 6 2 2
在恒容的容器中对反应Ⅰ进行研究。下列说法正确的是 。
A.升高温度,正、逆反应速率同时增大
B.C H 、C H 和H 的物质的量相等时,反应达到平衡状态
2 6 2 4 2
C.增加起始投料时C H 的体积分数,单位体积的活化分子数增加
2 6
D.增加起始投料时C H 的体积分数,C H 平衡转化率增大
2 6 2 6
(3)科研人员研究催化剂对乙烷无氧脱氢的影响
①在一定条件下,Zn/ZSM-5催化乙烷脱氢转化为乙烯的反应历程如图所示,该历程
的各步反应中,生成下列物质速率最慢的是 。
A.C H B.ZnC H C.C H D.H
2 6 2 5 2 4 2
②用Co基催化剂研究C H 催化脱氢,该催化剂对CH键和CC键的断裂均有高活
2 6
性,易形成碳单质。一定温度下,Co基催化剂在短时间内会失活,其失活的原因是 。
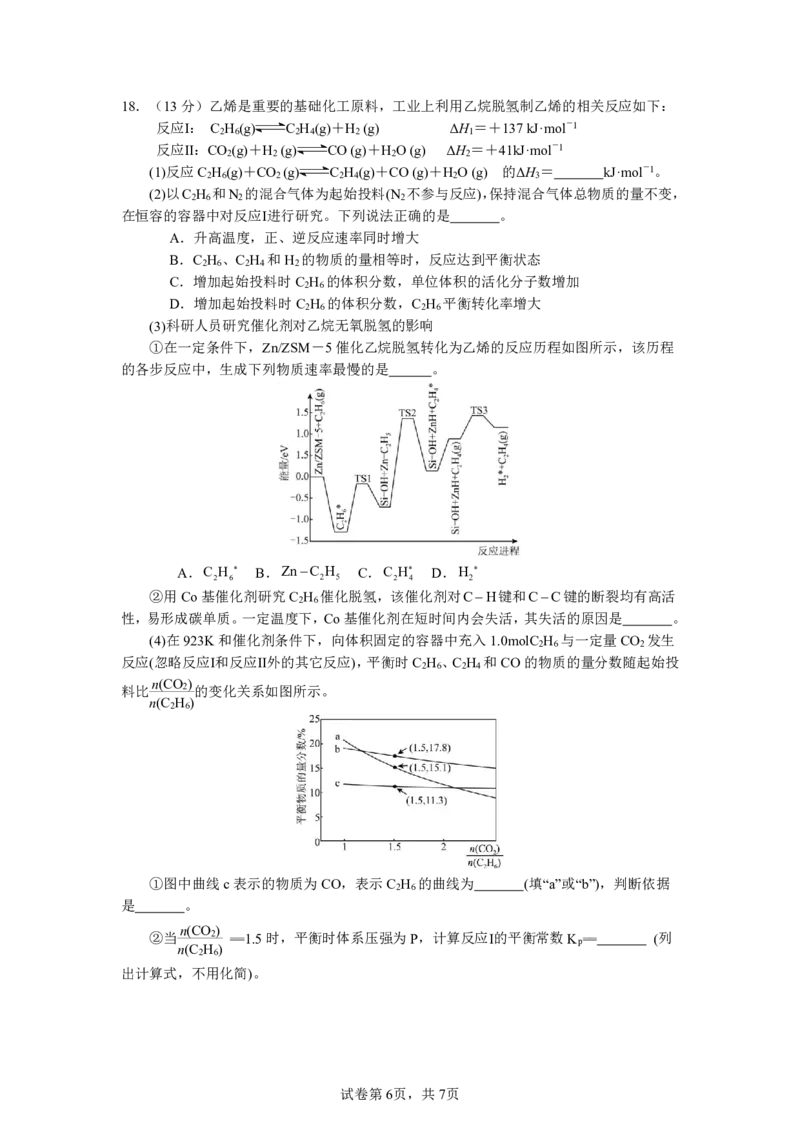
(4)在923K和催化剂条件下,向体积固定的容器中充入1.0molC H 与一定量CO 发生
2 6 2
反应(忽略反应Ⅰ和反应Ⅱ外的其它反应),平衡时C H 、C H 和CO的物质的量分数随起始投
2 6 2 4
n(CO )
料比 2 的变化关系如图所示。
n(C H )
2 6
①图中曲线c表示的物质为CO,表示C H 的曲线为 (填“a”或“b”),判断依据
2 6
是 。
n(CO )
②当 2 ==1.5时,平衡时体系压强为P,计算反应Ⅰ的平衡常数K == (列
p
n(C H )
2 6
出计算式,不用化简)。
试卷第6页,共7页
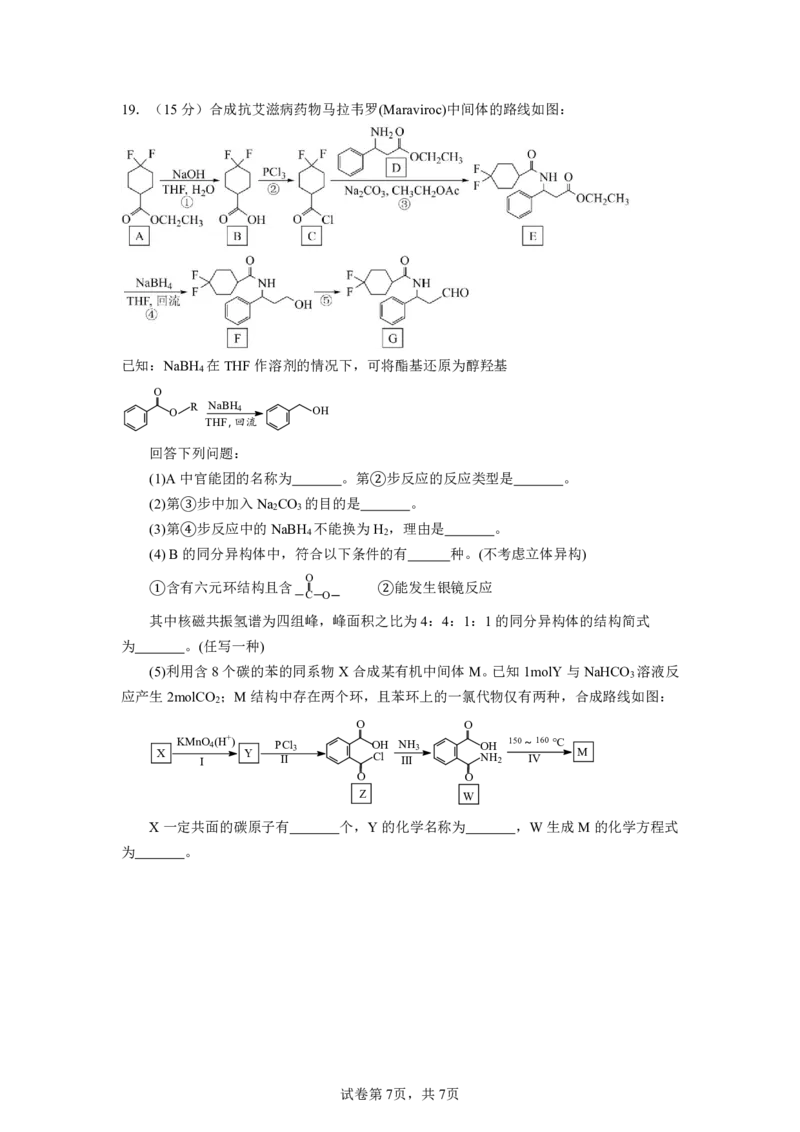
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}19.(15分)合成抗艾滋病药物马拉韦罗(Maraviroc)中间体的路线如图:
已知:NaBH 在THF作溶剂的情况下,可将酯基还原为醇羟基
4
O
O R NaBH 4 OH
THF,回流
回答下列问题:
(1)A中官能团的名称为 。第 步反应的反应类型是 。
(2)第 步中加入Na CO 的目的是 。
2 3 ②
(3)第 步反应中的NaBH 不能换为H ,理由是 。
③ 4 2
(4)B的同分异构体中,符合以下条件的有 种。(不考虑立体异构)
④
O
含有六元环结构且含 能发生银镜反应
C O
①其中核磁共振氢谱为四组峰,峰面积之②比为4:4:1:1的同分异构体的结构简式
为 。(任写一种)
(5)利用含8个碳的苯的同系物X合成某有机中间体M。已知1molY与NaHCO 溶液反
3
应产生2molCO ;M结构中存在两个环,且苯环上的一氯代物仅有两种,合成路线如图:
2
O O
X KMn I O 4 (H+) Y P Ⅱ Cl 3 O C H l N Ⅲ H 3 O N H H 2 150~ Ⅳ 160℃ M
O O
Z W
X一定共面的碳原子有 个,Y的化学名称为 ,W生成M的化学方程式
为 。
试卷第7页,共7页
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}绵阳南山中学高 2023 级高三第二次教学质量检测
化学参考答案和评分标准
说明:1.方程式缺少条件、↑或↓符号,扣1分。2.错别字无分。
一、单选题(每小题3分,共45分)
1-5CACBB 6-10 BDCDD 11-15ACBAD
二、非选择题(本题共4小题,共55分)
16.(13分)(1)四 (1分)Ⅷ (1分) (2)SiO (1分) (3)KSCN(1分) (4)5:2(2分)
2
(5)4Fe2++O +4H PO-+4NH ·H O=4FePO ↓+6H O+4NH + (2分) Fe(OH) /Fe O (1分)
2 2 4 3 2 4 2 4 3 2 3
a
(6)0.151(3a+4b)(2分)(7) (2分)
2
17.(14分)(1)恒压滴液漏斗(1分)
85℃
(2)I +2KClO +HCl ==== KH(IO ) +KCl+Cl ↑ (2分)
2 3 3 2 2
KIO +CaCl =Ca(IO ) ↓+2KCl (2分)
3 2 3 2
(3)乙醇结构中的-OH与水分子中的-OH相近,满足“相似相溶”规律;乙醇与水分子之间可
以形成氢键,会增大溶解性,因而乙醇与水互溶(写一个即可)(2分)
(4)KClO =K++ClO-(1分)
3 3
(5)加入最后半滴标准液,溶液由蓝色变为无色,且30s不复原(2分)
(6)78.00% (2分) BD(2分)
18.(13分)(1)+178(2分)
(2)AC(2分)
(3)①C(2分) ②积碳在其表面快速沉积使其活性降低(2分)
n(CO )
(4) ①a(1分) 2 比值增大,乙烷转化率增大,物质的量分数变化比CO和C H
2 4
n(C H )
2 6
P(H )P(C H ) 6.5%P17.8%P
要大(2分)② K 2 2 4 0.077P(2分)
p P(C H ) 15.1%P
2 6
19.(15分)(1)碳氟键、酯基(2分) 取代反应(1分)
(2)与生成的HCl反应,促使反应正向进行(2分)
(3)氢气无法选择性还原酯基(或氢气会还原苯环) (2分)
(4)12 (2分) 或 (2分)
(5) 8(1分) 邻苯二甲酸 (1分)
O O
OH
150~160℃
NH H O
NH 2
2
O O (2分)
{#{QQABBYKAogggApBAARhCQQVQCgCQkBEACYoOwAAQoAIAyRFABAA=}#}