文档内容
2023 年高考考前押题密卷(全国甲卷)
化学·全解全析
(考试时间:50分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Fe 56 Zn 65
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
7.化学在人类进步中起着关键作用,下列叙述不正确的是
A.“奋斗者号”潜水器含钛合金,其强度、韧性高于纯钛金属
B.绿色零碳氢能是未来能源发展的重要方向
C.《本草纲目》记载“凡酸坏之酒,皆可蒸烧”,所用的分离方法是蒸馏
D.载人飞船中的太阳能电池和储能电池均可将化学能转化为电能
【答案】D
【解析】A.钛合金为合金材料,硬度大,其强度、韧性高于纯钛金属,故A正确;B.氢能源燃烧放出
大量的热,且燃烧产物为水,无污染,是重要的新型能源,故B正确;C.“凡酸坏之酒,皆可蒸烧”,
其中的蒸烧指的是蒸馏,故C正确;D.太阳能电池是将太阳能转化为电能,故D错误;答案选D。
8.化合物M是一种治疗慢性结肠炎药物柳氨磺吡啶的主要原料,结构如下图所示。下列有关 M说法正确
的是
A.M的分子式为C HON
7 6 3
B.M能使FeCl 溶液显紫色
3
C.M分子中的3个氧原子一定在同一平面
D.M含有四种官能团——氨基、羟基、碳碳双键、羧基
【答案】B
【解析】A.由M结构简式可知,其分子式为C HON,A错误;B.由M的结构简式可知,分子中含有
7 7 3
酚羟基,能使FeCl 溶液显紫色,B正确;C.M分子中羧基平面与苯环平面是以单键相连,这两个平面可
3
能共面,也可能不共面,因此分子中的3个氧原子不一定在同一平面上,C错误;D.M分子中不含碳碳
双键,D错误;答案选B。
1
学科网(北京)股份有限公司9.下列解释生活事实的离子方程式正确的是
A.漂白粉溶液在空气中失效:
B.泡沫灭火器的反应原理:
C.用白醋除铁锈:Fe O·xHO+6CHCOOH=2Fe3++(3+x)H O+6CHCOO−
2 3 2 3 2 3
D.氢氟酸雕刻玻璃:
【答案】C
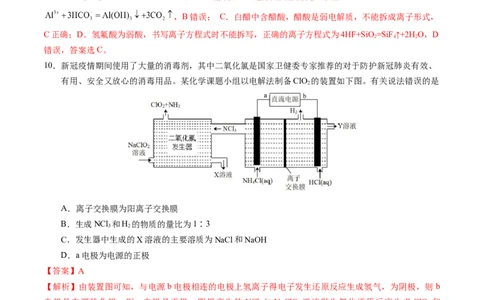
【解析】A.漂白粉溶液在空气中与二氧化碳反应生成次氯酸和碳酸钙:
,A错误;B.泡沫灭火器的反应原理:
,B错误; C.白醋中含醋酸,醋酸是弱电解质,不能拆成离子形式,
C正确;D.氢氟酸为弱酸,书写离子方程式时不能拆写,正确的离子方程式为4HF+SiO =SiF ↑+2H O,D
2 4 2
错误,答案选C。
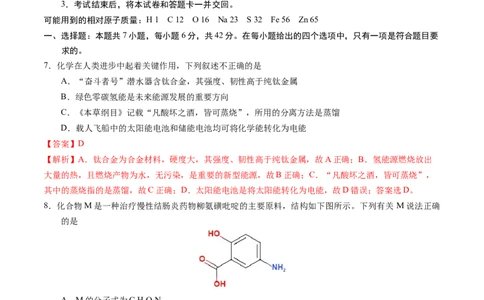
10.新冠疫情期间使用了大量的消毒剂,其中二氧化氯是国家卫健委专家推荐的对于防护新冠肺炎有效、
有用、安全又放心的消毒用品。某化学课题小组以电解法制备ClO 的装置如下图。有关说法错误的是
2
A.离子交换膜为阳离子交换膜
B.生成NCl 和H 的物质的量比为1∶3
3 2
C.发生器中生成的X溶液的主要溶质为NaCl和NaOH
D.a电极为电源的正极
【答案】A
【解析】由装置图可知,与电源b电极相连的电极上氢离子得电子发生还原反应生成氢气,为阴极,则 b
电极是电源的负极,则 a电极是正极;阳极产生的 NCl 与NaClO 溶液发生氧化还原反应生成 ClO 和
3 2 2
NH ,依据得失电子守恒和原子守恒可知,反应的化学方程式为:NCl +6NaClO +3H O=3NaCl+3NaOH+
3 3 2 2
6ClO ↑+NH↑。由以上分析可知,A.由题意知,左室中原料为NH Cl,产物为NCl ,根据原子守恒可知,
2 3 4 3
左室要增加Cl−,因此通过离子交换膜过左室的离子为 Cl−,故离子交换膜为阴离子交换膜,故 A错误;
B.NCl 中N为−3价,Cl为+1价,生成1molNCl 要失去6mol电子,生成1molH 要得到2mol电子,根据
3 3 2
电子得失守恒,则生成的NCl 和H 的物质的量比为1∶3,B正确;C.由分析可知,发生器中发生的反应
3 2
为NCl +6NaClO +3H O=3NaCl+3NaOH+6ClO ↑+NH↑,故生成的X溶液的主要溶质为NaCl和NaOH,C
3 2 2 2 3
正确;D.a电极为电源的正极,D正确,答案选A。
11.已知N 是阿伏加德罗常数的值,下列说法错误的是( )
A
2
学科网(北京)股份有限公司A.1 L 0.1 mol·L−1KNO 溶液中离子总数大于0.2N
3 A
B.D18O和TO的混合物1.1 g, 含有的质子数为0. 5N
2 2 A
C.5.6 g Fe与足量的S反应转移的电子数为0.3N
A
D.0.1 mol H 和0.2 mol I 充分反应后分子总数等于0.3N
2 2 A
【答案】C
【解析】A.1L0.1mol·L−1KNO 溶液中,K+和NO −总物质的量为0.2mol,但溶液中还会电离出H+和OH−,
3 3
则溶液中离子总数大于0.2N ,故A正确;B.D18O和TO的摩尔质量均为22g/mol,所以1.1 g混合物的
A 2 2
物质的量为0.05mol,一个D18O分子和一个TO分子均含有10个质子,所以混合物含有的质子数为
2 2
0.5N ,B正确;C.5.6g Fe的物质的量为0.1mol,与足量的S反应生成FeS,转移电子数为0.2N ,C错误;
A A
D.H 和I 反应方程式为H+I 2HI,反应前后分子数不变,所以0.1 mol H 和0.2 mol I 充分反应后分子
2 2 2 2 2 2
总数为0.3N ,故D正确;综上所述答案为C。
A
12.某化合物是有机合成重要试剂,由W、X、Y、Z四种原子序数增大的短周期元素组成,其结构可表示
为 ,其中W为周期表中原子半径最小的元素,X的最外层电子数是次外层电子数
的两倍,Y为金属元素,Z的最外层电子数等于W、X原子序数之和,下列有关说法中正确的是
A.W、X、Y、Z原子半径依次增大
B.元素W与元素X形成的化合物可能与Z元素形成的单质发生加成反应
C.0.1molZ元素形成的单质与足量的W的简单氧化物反应转移的电子数为0.1N
A
D.工业上通过电解元素Y的最高价氧化物来制备Y单质
【答案】B
【解析】W为周期表中原子半径最小的元素,则W为H元素,X的最外层电子数是次外层电子数的两倍,
则X为C元素,从结构上可知,Y为二价金属,且原子序数比C元素大,又是短周期元素,则Y为Mg元
素,Z的最外层电子数等于W、X原子序数之和,则Z的最外层电子数为7,且原子序数比Mg元素大又是
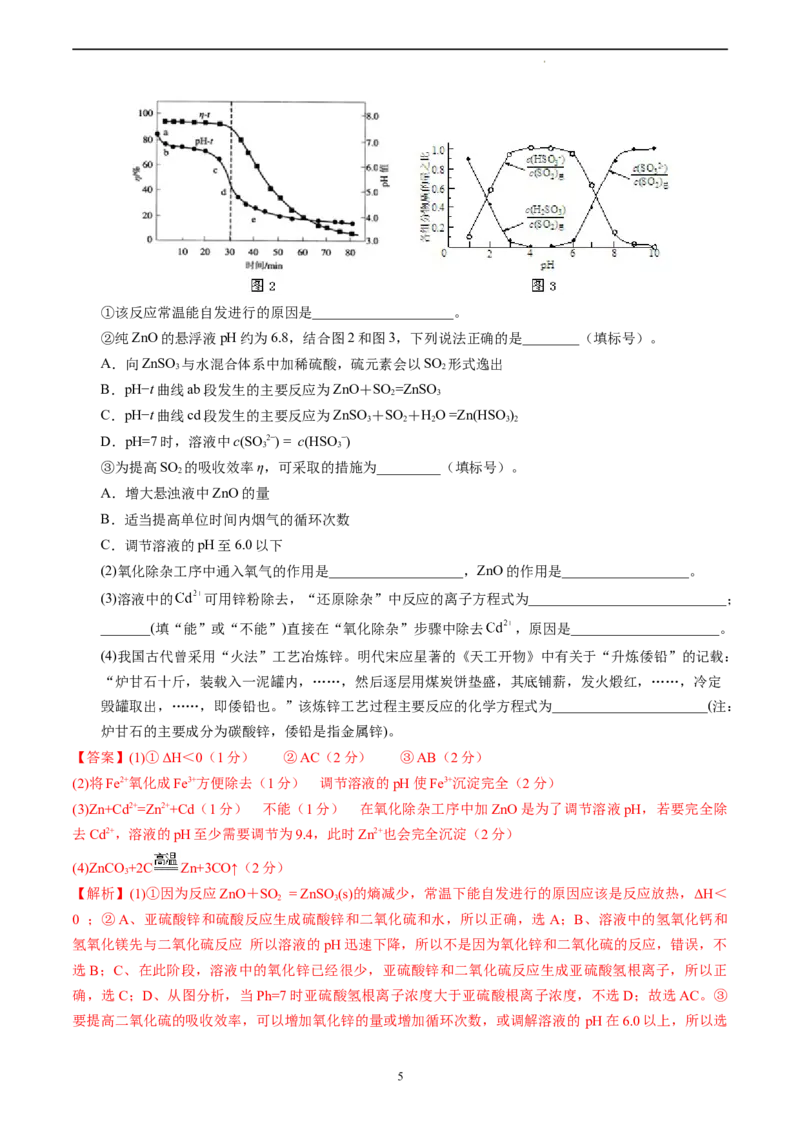
短周期元素,故Z为Cl元素。A.W、X、Y、Z分别为H、C、Mg、Cl,原子半径大小为H0。
2 4 2 2 2 2
回答下列问题:
(1)已知:2C H(g)+7O(g)=4CO (g)+6HO(g) ∆H
2 6 2 2 2 3
C H(g)+3O(g)=2CO (g)+2HO(g) ∆H
2 4 2 2 2 4
则∆H=______________(用∆H、∆H 表示)。
1 3 4
(2)有利于提高平衡体系中乙烯体积分数的措施有_______(填标号)。
A.适当升温 B.适当降温 C.适当加压 D.适当减压
(3)主反应在管式反应器中进行,实际投料往往在n(C H)∶n(O )的基础上适当增大O 用量,其目的是
2 6 2 2
__________________________________________。
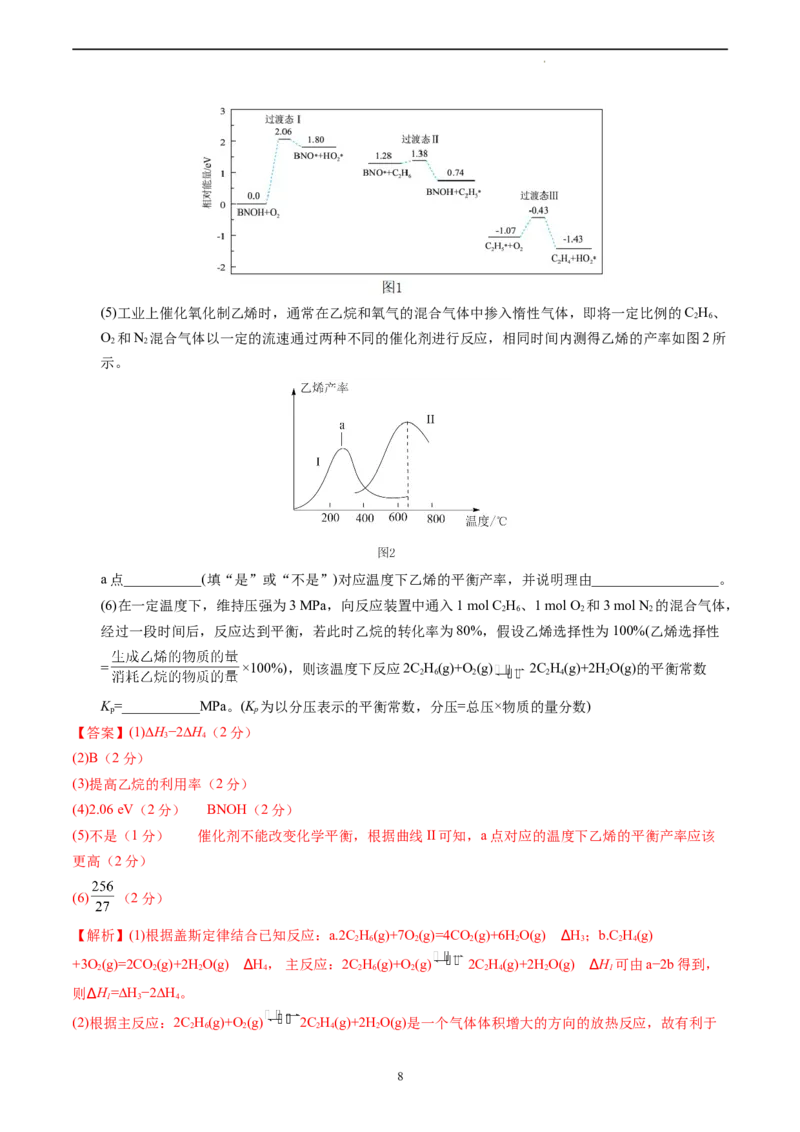
(4)主反应分多步进行,其中的部分反应历程如图1所示,该历程的催化剂是______________,这一部
分反应中慢反应的活化能E =__________________。
正
7
学科网(北京)股份有限公司(5)工业上催化氧化制乙烯时,通常在乙烷和氧气的混合气体中掺入惰性气体,即将一定比例的C H、
2 6
O 和N 混合气体以一定的流速通过两种不同的催化剂进行反应,相同时间内测得乙烯的产率如图2所
2 2
示。
a点___________(填“是”或“不是”)对应温度下乙烯的平衡产率,并说明理由__________________。
(6)在一定温度下,维持压强为3 MPa,向反应装置中通入1 mol C H、1 mol O 和3 mol N 的混合气体,
2 6 2 2
经过一段时间后,反应达到平衡,若此时乙烷的转化率为80%,假设乙烯选择性为100%(乙烯选择性
= ×100%),则该温度下反应2C H(g)+O(g) 2C H(g)+2HO(g)的平衡常数
2 6 2 2 4 2
K =___________MPa。(K 为以分压表示的平衡常数,分压=总压×物质的量分数)
p p
【答案】(1)∆H−2∆H(2分)
3 4
(2)B(2分)
(3)提高乙烷的利用率(2分)
(4)2.06 eV(2分) BNOH(2分)
(5)不是(1分) 催化剂不能改变化学平衡,根据曲线II可知,a点对应的温度下乙烯的平衡产率应该
更高(2分)
(6) (2分)
【解析】(1)根据盖斯定律结合已知反应:a.2C H(g)+7O(g)=4CO (g)+6HO(g) ∆H;b.C H(g)
2 6 2 2 2 3 2 4
+3O (g)=2CO (g)+2HO(g) ∆H,主反应:2C H(g)+O(g) 2C H(g)+2HO(g) ∆H 可由a−2b得到,
2 2 2 4 2 6 2 2 4 2 1
则∆H=∆H −2∆H 。
1 3 4
(2)根据主反应:2C H(g)+O(g) 2C H(g)+2HO(g)是一个气体体积增大的方向的放热反应,故有利于
2 6 2 2 4 2
8
学科网(北京)股份有限公司提高平衡体系中乙烯体积分数即使平衡向正方向移动,根据勒夏特列原理,可采用适当降低温度和实当减
压有利平衡正向移动,而副反应C H(g)=C H(g)+H(g)是一个气体体积增大的方向的吸热反应,降温和加
2 4 2 2 2
压都将使副反应平衡逆向移动,故答案为:B。
(3)主反应在管式反应器中进行,实际投料往往在n(C H):n(O)的基础上适当增大O 用量,增大O 的浓度
2 6 2 2 2
将使平衡正向移动,从而提高乙烷的转化率即利用率,故适当增大O 用量的目的是提高乙烷的利用率;
2
(4)慢反应的活化能最大,根据图示可知活化能最大值是2.06 eV,故这一部分反应中慢反应的活化能E
正
=2.06 eV;该历程中BNOH参与反应,最后又生成BNOH,因此该历程的催化剂是BNOH。
(5)催化剂只能改变反应途径,而不能使化学平衡发生移动,根据曲线II可知,a点对应的温度下乙烯的平
衡产率应该更高,a点不是对应温度下乙烯的平衡产率;
(6)在反应开始时,在一定温度下,维持压强为3 MPa,向反应装置中通入1 mol C H、1 mol O 和3 mol N
2 6 2 2
的混合气体,发生反应:2C H(g)+O(g) 2C H(g)+2HO(g)经过一段时间后,反应达到平衡,若此时
2 6 2 2 4 2
乙烷的转化率为80%,假设乙烯选择性为100%,则反应产生C H(g)、HO(g)的物质的量是0.8 mol,平衡
2 4 2
时n(C H)=1 mol−0.8 mol=0.2 mol,n(O )=1 mol−0.4 mol=0.6 mol,此时混合气体总物质的量为
2 6 2
n(总)=n(N )+n(C H)+n(O )+n(C H)+n(H O)=3 mol+0.2 mol+0.6 mol+0.8 mol+0.8 mol=5.4 mol,故该反应的化
2 2 6 2 2 4 2
学平衡常数K = 。
p
(二)选考题:共15分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。
35.[化学——选修3:物质结构与性质](15分)微信搜索“高中试卷君”公众号 领取押题卷联考卷
锌、镓等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)葡萄糖酸锌为有机锌补剂,对胃黏膜刺激小,在人体中吸收率高。如图是葡萄糖酸锌的结构简式。
①基态Zn原子的核外电子排布式[Ar] ______________;
②1个葡萄糖酸锌分子中有______________个手性碳原子;
③葡萄糖酸的熔点______________(填“大于”、“等于”或“小于”)葡萄糖酸锌的熔点,原因是
___________________________________。
(2)氨基酸锌是研究最早和使使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图是氨
基酸锌的结构简式。
9
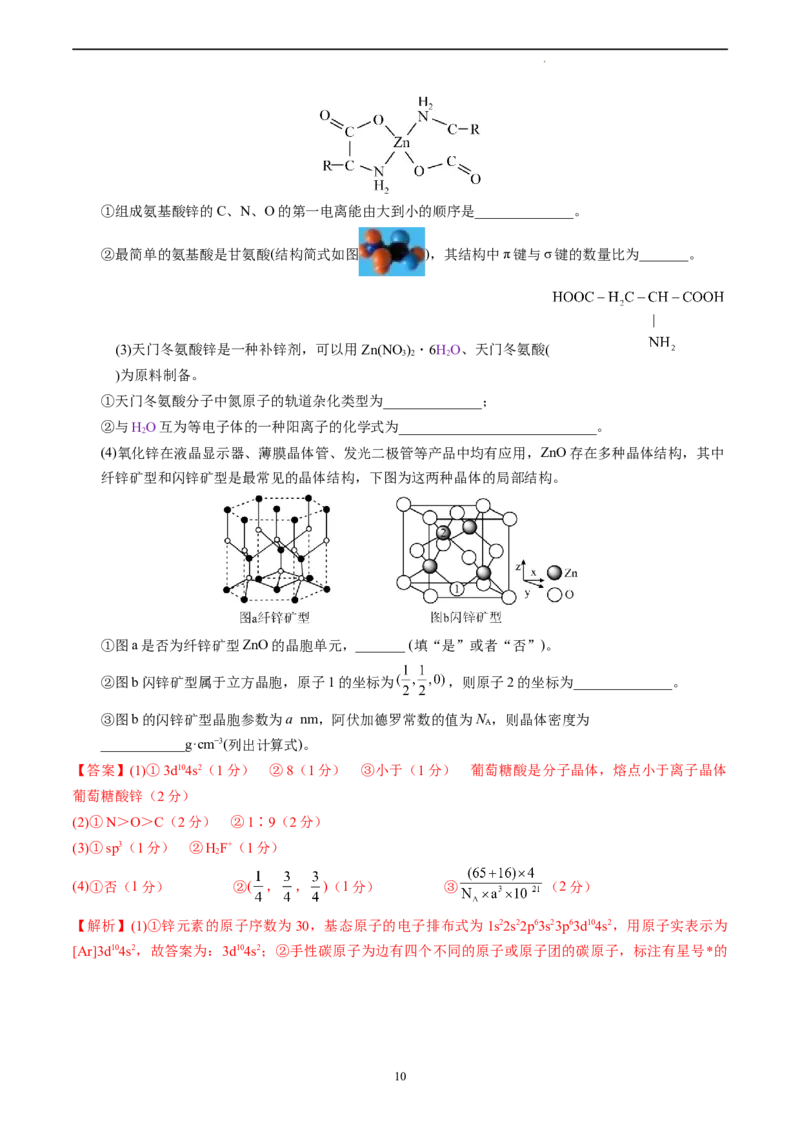
学科网(北京)股份有限公司①组成氨基酸锌的C、N、O的第一电离能由大到小的顺序是______________。
②最简单的氨基酸是甘氨酸(结构简式如图 ),其结构中π键与σ键的数量比为_______。
(3)天门冬氨酸锌是一种补锌剂,可以用Zn(NO )・6HO、天门冬氨酸(
3 2 2
)为原料制备。
①天门冬氨酸分子中氮原子的轨道杂化类型为______________;
②与HO互为等电子体的一种阳离子的化学式为____________________________。
2
(4)氧化锌在液晶显示器、薄膜晶体管、发光二极管等产品中均有应用,ZnO存在多种晶体结构,其中
纤锌矿型和闪锌矿型是最常见的晶体结构,下图为这两种晶体的局部结构。
①图a是否为纤锌矿型ZnO的晶胞单元,_______ (填“是”或者“否”)。
②图b闪锌矿型属于立方晶胞,原子1的坐标为 ,则原子2的坐标为______________。
③图b的闪锌矿型晶胞参数为a nm,阿伏加德罗常数的值为N ,则晶体密度为
A
____________g·cm−3(列出计算式)。
【答案】(1)①3d104s2(1分) ②8(1分) ③小于(1分) 葡萄糖酸是分子晶体,熔点小于离子晶体
葡萄糖酸锌(2分)
(2)①N>O>C(2分) ②1∶9(2分)
(3)①sp3(1分) ②HF+(1分)
2
(4)①否(1分) ②( , , )(1分) ③ (2分)
【解析】(1)①锌元素的原子序数为30,基态原子的电子排布式为1s22s22p63s23p63d104s2,用原子实表示为
[Ar]3d104s2,故答案为:3d104s2;②手性碳原子为边有四个不同的原子或原子团的碳原子,标注有星号*的
10
学科网(北京)股份有限公司为手性碳(即 ),共有8个,故答案为:8;③离子晶体的熔点高于分子晶体,
葡萄糖酸锌是离子晶体,葡萄糖酸是分子晶体,所以熔点小于离子晶体葡萄糖酸锌。
(2)①同一周期主族元素从左向右第一电离能呈增大趋势,但第IIA族和第VA族处于全满和半满结构,第
一电离能比同周期相邻元素第一电离能大,因此C、N、O的第一电离能由大到小的顺序是:N>O>C。
②由甘氨酸的填充模型可知,甘氨酸的结构式为 ,其结构中含σ键9个、含π键1个,因
此π键与σ键的数量比为1:9。
(3)①N原子相连的δ键数为3,其价层电子对数为 =4,其轨道杂化类型为sp3;
②HO中价层电子总数为8+2=10,原子数为3,因此与HO互为等电子体的一种阳离子为:HF+;
2 2 2
(4)①晶胞单元是晶体的最小重复结构单元,图示结构中包含了三个更小的重复结构单元,所以不是ZnO的
晶胞单元;
②根据原子1的坐标可知底面左上角O原子为原点,晶胞棱长为单位1,原子2位于体对角线上,坐标为(
, , );
③根据晶胞结构可知一个晶胞中有4个Zn原子,化学式为ZnO,所以一个晶胞O原子的个数也为4,则晶
胞的质量为 g,晶胞参数为a nm,则体积为a3 nm3=a3×10﹣21 cm3,所以密度为
g/cm3。
36.[化学——选修5:有机化学基础](15分)
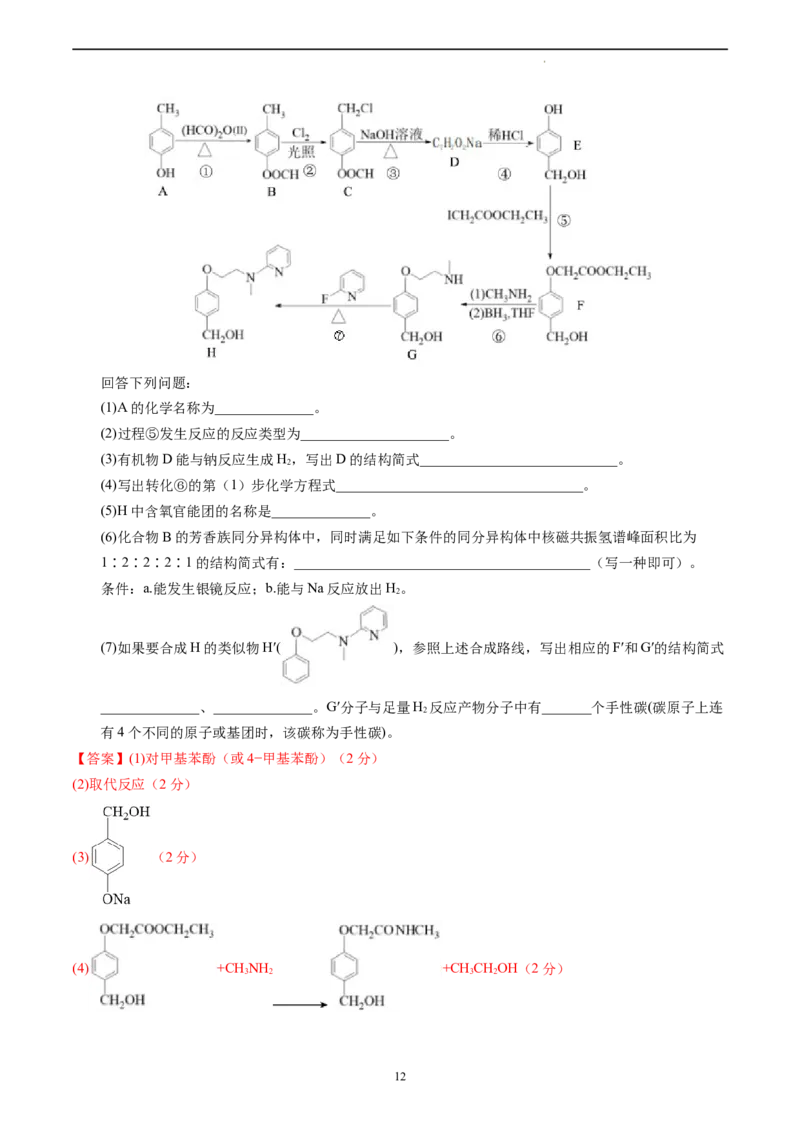
化合物H是合成药物的一种中间体,其合成路线如下:
11
学科网(北京)股份有限公司回答下列问题:
(1)A的化学名称为______________。
(2)过程⑤发生反应的反应类型为_____________________。
(3)有机物D能与钠反应生成H,写出D的结构简式____________________________。
2
(4)写出转化⑥的第(1)步化学方程式___________________________________。
(5)H中含氧官能团的名称是______________。
(6)化合物B的芳香族同分异构体中,同时满足如下条件的同分异构体中核磁共振氢谱峰面积比为
1∶2∶2∶2∶1的结构简式有:__________________________________________(写一种即可)。
条件:a.能发生银镜反应;b.能与Na反应放出H。
2
(7)如果要合成H的类似物H′( ),参照上述合成路线,写出相应的F′和G′的结构简式
______________、______________。G′分子与足量H 反应产物分子中有_______个手性碳(碳原子上连
2
有4个不同的原子或基团时,该碳称为手性碳)。
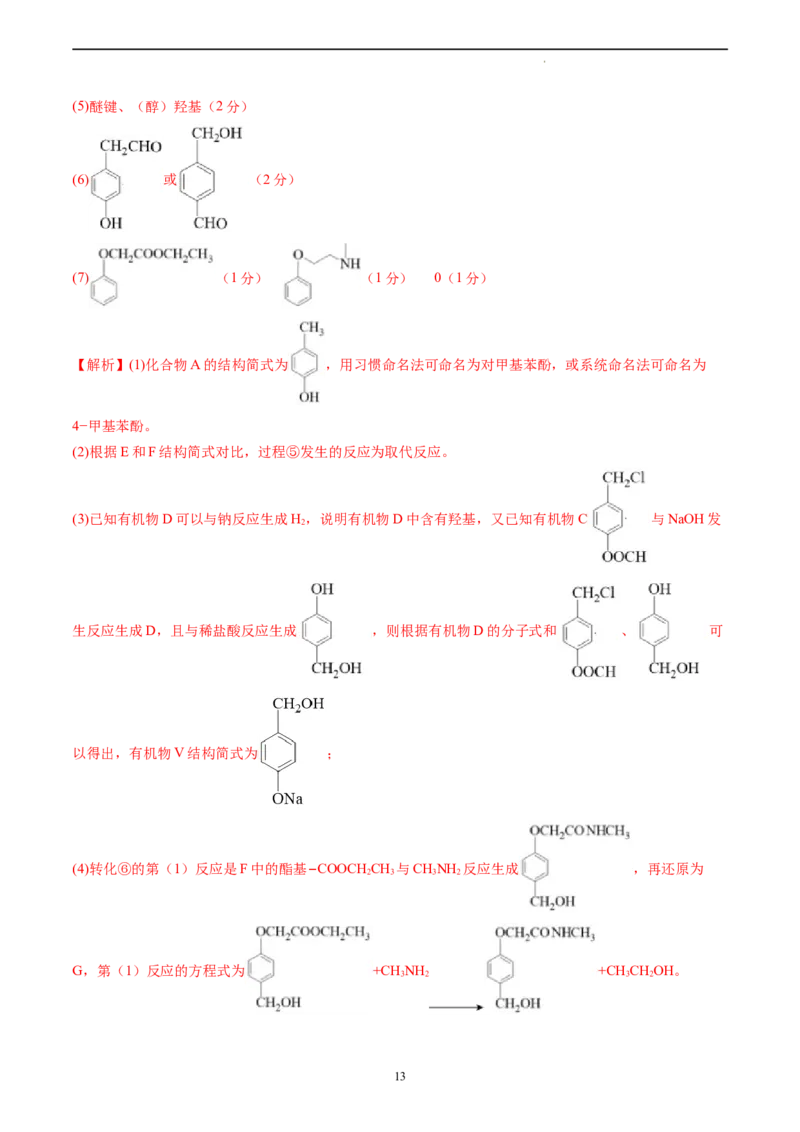
【答案】(1)对甲基苯酚(或4−甲基苯酚)(2分)
(2)取代反应(2分)
(3) (2分)
(4) +CH NH +CH CHOH(2分)
3 2 3 2
12
学科网(北京)股份有限公司(5)醚键、(醇)羟基(2分)
(6) 或 (2分)
(7) (1分) (1分) 0(1分)
【解析】(1)化合物A的结构简式为 ,用习惯命名法可命名为对甲基苯酚,或系统命名法可命名为
4−甲基苯酚。
(2)根据E和F结构简式对比,过程⑤发生的反应为取代反应。
(3)已知有机物D可以与钠反应生成H,说明有机物D中含有羟基,又已知有机物C 与NaOH发
2
生反应生成D,且与稀盐酸反应生成 ,则根据有机物D的分子式和 、 可
以得出,有机物V结构简式为 ;
(4)转化⑥的第(1)反应是F中的酯基−COOCH CH 与CHNH 反应生成 ,再还原为
2 3 3 2
G,第(1)反应的方程式为 +CH NH +CH CHOH。
3 2 3 2
13
学科网(北京)股份有限公司(5)H的分子式为 ,其中的含氧官能团有醚键和醇羟基,故答案为:醚键、(醇)羟基;
(6)化合物B的分子式为C HO,能发生银镜反应为醛基(−CHO),能与Na反应的官能团为醇羟基
8 8 2
(−OH)或酚羟基(−OH),结合含有苯环,其中核磁共振氢谱峰面积比为1:2:2:2:1的同分异构体有两种,
结构简式分别为 和 。
(7)参照合成路线,对比 H与H′结构简式可知,相应的 F′和G′的结构简式分别为 、
,G′与足量 H 反应产物分子的结构简式为 ,根据手性碳原子的定义,
2
中无手性碳原子。
14
学科网(北京)股份有限公司15
学科网(北京)股份有限公司