文档内容
2024 届新高三开学摸底考试卷(全国通用,新教材)01
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Sr 88 Cu 64 Ti 48
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.我国“嫦娥五号”成功携带月球样品返回地球。下列有关说法错误的是
A.运载火箭使用煤油液氧推进剂,煤油是石油分馏产品,分馏属于物理变化
B.探测器装有太阳能电池板,能将太阳能转化为电能
C.返回器带回的月壤中含有 He,它与地球上 He的性质完全相同
D.嫦娥五号中超声电机的心脏——压电陶瓷是一种无机非金属材料
2.科学家利用氦核 撞击氮原子,发生反应: ,下列说法正确的
是
A. 的质子数为2 B. 的中子数为9
C. 和 互为同位素 D. 与 化学性质不同
3.下列说法正确的是
A.NaCl、HCl的水溶液都能导电,NaCl、HCl属于离子化合物
B.CaC 、CaCl 都含有离子键和非极性共价键
2 2
C.石油分馏、煤的干馏都属于物理变化
D.NaSiO 和SiC都属于无机非金属材料
2 3
4.下列图示或化学用语错误的是
A.羟基的电子式:
B.HO的VSEPR模型:
2
1
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司C.Mn2+的价电子的轨道表示式:
D.中子数为5的铍原子:
5.对乙酰氨基酚是感冒冲剂的有效成分,其结构简式如图所示。下列有关说法正确的是
A.难溶于热水,能发生消去反应 B.在人体内能发生水解反应
C.分子中所有原子可能共平面 D.不能与FeCl 溶液发生显色反应
3
6.下列有关物质性质与用途对应关系错误的是
物质性质 物质用途
A NaO 吸收CO 产生O NaO 用作呼吸面具供氧剂
2 2 2 2 2 2
B Al O 熔融状态可电离 电解熔融Al O 制取单质Al
2 3 2 3
C 铁比铜金属性强 FeCl 腐蚀Cu刻制印刷电路板
3
D HF与SiO 反应 HF在玻璃器皿上刻蚀标记
2
A.A B.B C.C D.D
7.下列解释实验事实的离子方程式书写正确的是
A.钠投入氯化铜溶液中:
B.氯气通入水中:
C.二氧化硫与酸性高锰酸钾溶液反应:
D.硫酸溶液中加入氢氧化钡溶液:
8.设 为阿伏加德罗常数的值。下列说法正确的是
A.50℃, 的 溶液中含有 的数目为
B. 的 溶液中含 分子的数目为
C. 和 于密闭容器中充分反应后,分子总数为
D.浓度均为 的 溶液和 溶液中, 数目均为
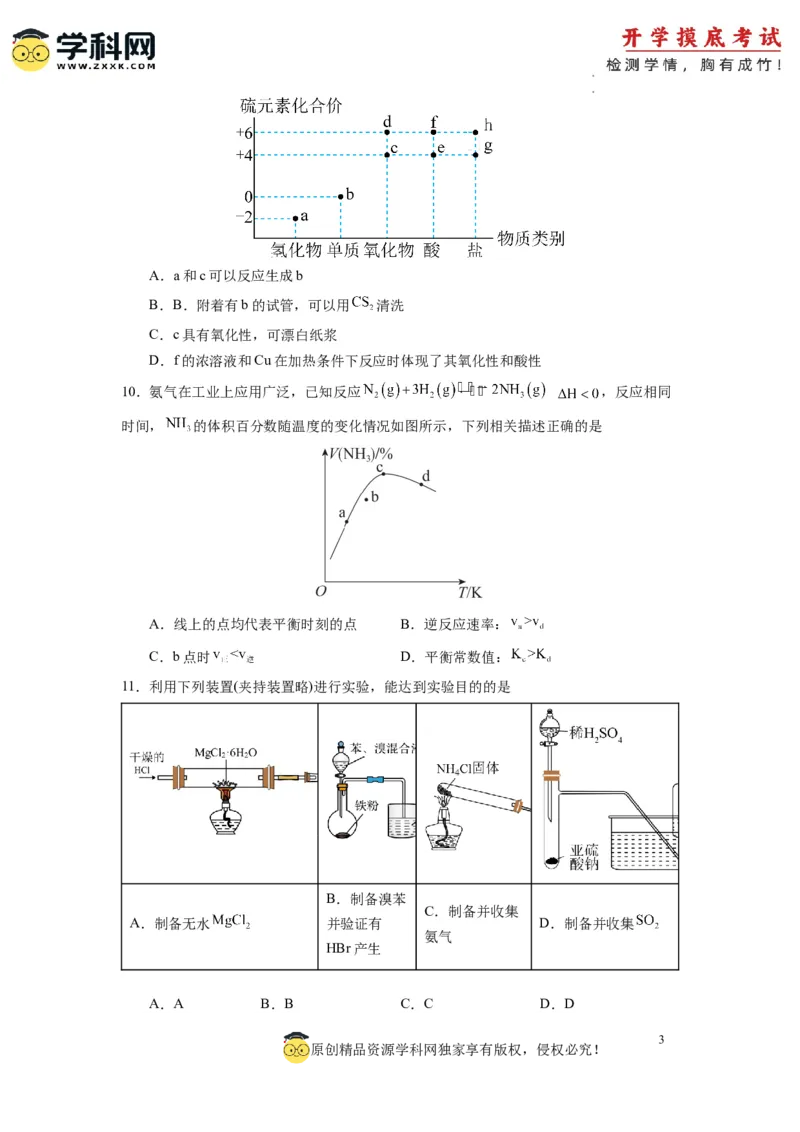
9.物质的类别和核心元素的化合价是研究物质性质的两个重要维度。如图为硫及其部分化
合物的价态-类别图。下列说法不正确的是
2
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司A.a和c可以反应生成b
B.B.附着有b的试管,可以用 清洗
C.c具有氧化性,可漂白纸浆
D.f的浓溶液和Cu在加热条件下反应时体现了其氧化性和酸性
10.氨气在工业上应用广泛,已知反应 ,反应相同
时间, 的体积百分数随温度的变化情况如图所示,下列相关描述正确的是
A.线上的点均代表平衡时刻的点 B.逆反应速率:
C.b点时 D.平衡常数值:
11.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
B.制备溴苯
C.制备并收集
A.制备无水 并验证有 D.制备并收集
氨气
HBr产生
A.A B.B C.C D.D
3
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司12.化合物 是一种高效消毒漂白剂,其结构式如图所示。 、 、 、 是原子序数
依次增大的短周期主族元素, 的 轨道电子总数与 轨道电子数相同, 、 不在同一
周期。下列叙述错误的是
A.电负性: B. 与 能形成多种化合物
C.最简单氢化物的稳定性: D.该分子中所有原子最外层均满足8电子结构
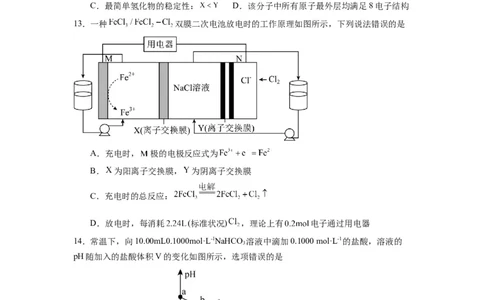
13.一种 双膜二次电池放电时的工作原理如图所示,下列说法错误的是
A.充电时, 极的电极反应式为
B. 为阳离子交换膜, 为阴离子交换膜
C.充电时的总反应:
D.放电时,每消耗 (标准状况) ,理论上有 电子通过用电器
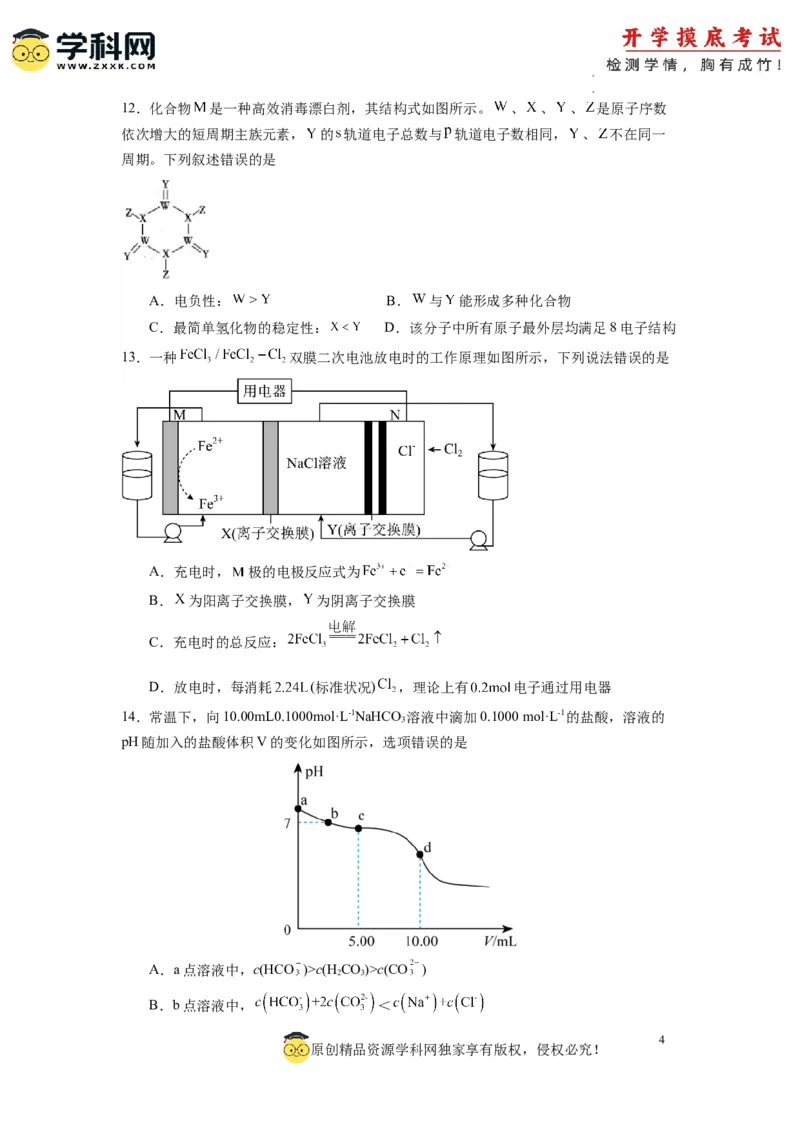
14.常温下,向10.00mL0.1000mol·L-1NaHCO 溶液中滴加0.1000 mol·L-1的盐酸,溶液的
3
pH随加入的盐酸体积V的变化如图所示,选项错误的是
A.a点溶液中,c(HCO )>c(H CO)>c(CO )
2 3
B.b点溶液中, <
4
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司C.c点溶液中,共含有7种微粒。
D.d点溶液中, 0.1000
第II卷(非选择题 共58分)
二、非选择题:本题共4个小题,共58分。
15.(14分)碳酸锶(SrCO )难溶于水,主要用于电磁材料和金属冶炼。一种由工业碳酸锶
3
(含少量Ba2+、Ca2+、Mg2+、Pb2+等)制备高纯碳酸锶的工艺流程如下:
已知:①Sr(OH) 为强碱,Cr(OH) 为两性氢氧化物;
2 3
②常温下,各物质的溶度积常数如表所示。
化合物 Cr(OH) Ca(OH) Mg(OH) SrCO
3 2 2 3
K 近似值
sp
回答下列问题:
(1)“酸溶”时能提高反应速率的措施有________________________(答1条即可),基态Cr
原子的价电子排布式是_____________。
(2)“酸化”步骤发生如下反应: ,则“还原”时发生反应
的离子方程式为____________________。
(3)滤渣1的主要成分为________(填化学式)。
(4)用氨水和NaOH分步调节pH,而不直接用NaOH调节溶液的pH≈13的原因是
________。
(5)“碳化”时,反应 的化学平衡常数K的
计算关系式为____________。(不用写出具体数值,用以下平衡常数表达:SrCO 的溶度积
3
常数K (SrCO )、HCO 的电离常数为K 、K )
sp 3 2 3 a1 a2
(6)上述流程合成的碳酸锶与TiO 在高温下反应,可以制得高温超导基片材料SrTiO ,
2 3
SrTiO 的立方晶胞结构如图所示,其中Ti处在体心位置,晶胞边长为a nm,已知SrTiO 的
3 3
相对分子质量为M,阿佛加德罗常数的值为N ,则SrTiO 晶体的密度为_____________g/c
A 3
m3(列出M、N 、a相关的算式即可)。
A
5
原创精品资源学科网独家享有版权,侵权必究!
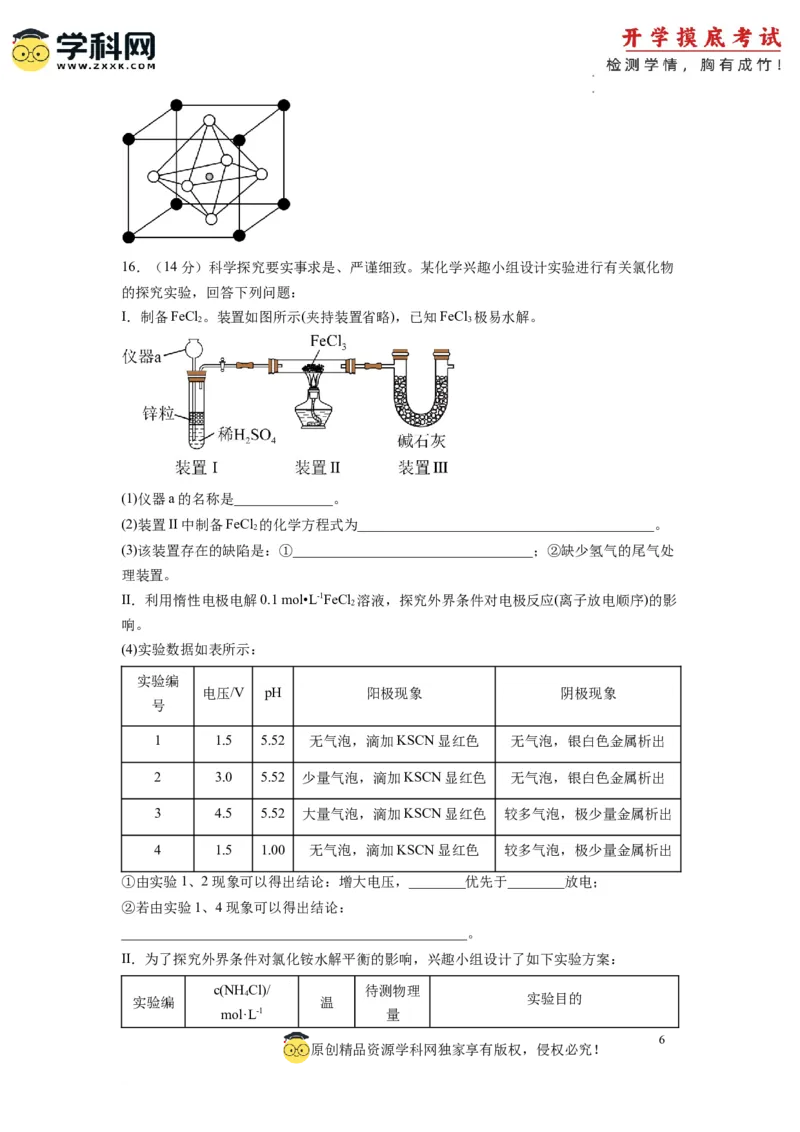
学学科科网网((北北京京))股股份份有有限限公公司司16.(14分)科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物
的探究实验,回答下列问题:
I.制备FeCl 。装置如图所示(夹持装置省略),已知FeCl 极易水解。
2 3
(1)仪器a的名称是______________。
(2)装置II中制备FeCl 的化学方程式为__________________________________________。
2
(3)该装置存在的缺陷是:①__________________________________;②缺少氢气的尾气处
理装置。
II.利用惰性电极电解0.1 mol•L-1FeCl 溶液,探究外界条件对电极反应(离子放电顺序)的影
2
响。
(4)实验数据如表所示:
实验编
电压/V pH 阳极现象 阴极现象
号
1 1.5 5.52 无气泡,滴加KSCN显红色 无气泡,银白色金属析出
2 3.0 5.52 少量气泡,滴加KSCN显红色 无气泡,银白色金属析出
3 4.5 5.52 大量气泡,滴加KSCN显红色 较多气泡,极少量金属析出
4 1.5 1.00 无气泡,滴加KSCN显红色 较多气泡,极少量金属析出
①由实验1、2现象可以得出结论:增大电压,________优先于________放电;
②若由实验1、4现象可以得出结论:
_________________________________________________。
II.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
c(NH Cl)/ 待测物理
实验编 4 温 实验目的
mol·L-1 量
6
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司号 度/℃
5 0.5 30 a ——
6 1.5 i b 探究浓度对氯化铵水解平衡的影响
7 0.5 35 c ii
探究温度、浓度同时对氯化铵水解平
8 2.0 40 d
衡的影响
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol.L-1硝酸银溶液、蒸馏
水和各种浓度的NH Cl溶液。
4
①实验中,“待测物理量”是________________;
②实验目的ii是_________________;
③上述表格中,b____ d(填“>”、“<”或“=”)。
17.(15分)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以CO 和NH 为原料合成尿素的反应为:2NH (g)+CO (g) CO(NH)(s)+HO(g),该反
2 3 3 2 2 2 2
应为放热反应。
(1)上述反应中,有利于提高CO 平衡转化率的措施是_______(填序号)。
2
A.高温低压 B.低温高压 C.高温高压 D.低温低压
(2)研究发现,合成尿素反应分两步完成,其能量变化如图所示:
第一步:2NH (g)+CO (g) HNCOONH (s) ΔH=-159.5kJ·mol-1
3 2 2 4 1
第二步:HNCOONH (s) CO(NH)(s)+HO(g) ΔH=+72.5kJ·mol-1
2 4 2 2 2 2
①合成尿素总反应的热化学方程式为_______。
②反应速率较快的是_______反应(填“第一步”或“第二步”),理由是_______。
II.以CO 和CH 催化重整制备合成气:CO(g)+CH (g) 2CO(g)+2H(g)
2 4 2 4 2
(3)在密闭容器中通入物质的量均为0.2mol的CH 和CO 在一定条件下发生反应:CH(g)
4 2 4
7
原创精品资源学科网独家享有版权,侵权必究!
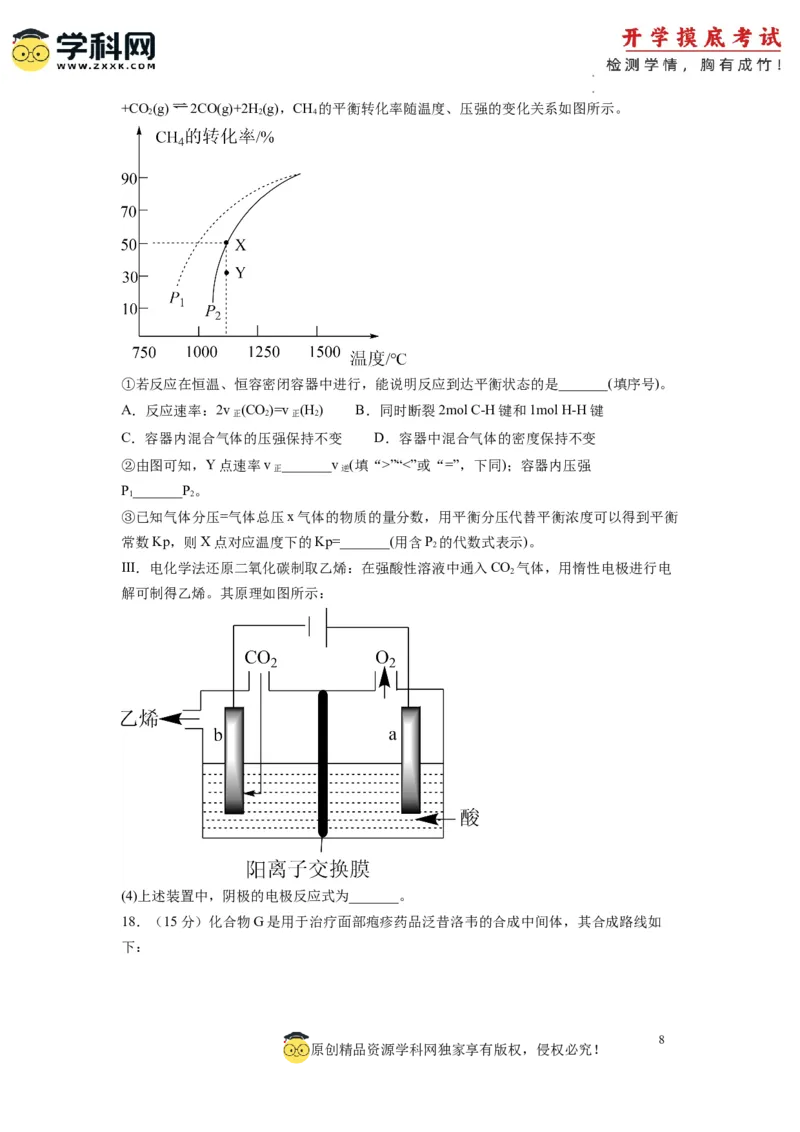
学学科科网网((北北京京))股股份份有有限限公公司司+CO (g) 2CO(g)+2H(g),CH 的平衡转化率随温度、压强的变化关系如图所示。
2 2 4
①若反应在恒温、恒容密闭容器中进行,能说明反应到达平衡状态的是_______(填序号)。
A.反应速率:2v (CO)=v (H ) B.同时断裂2mol C-H键和1mol H-H键
正 2 正 2
C.容器内混合气体的压强保持不变 D.容器中混合气体的密度保持不变
②由图可知,Y点速率v _______v (填“>”“<”或“=”,下同);容器内压强
正 逆
P_______P。
1 2
③已知气体分压=气体总压x气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡
常数Kp,则X点对应温度下的Kp=_______(用含P 的代数式表示)。
2
III.电化学法还原二氧化碳制取乙烯:在强酸性溶液中通入CO 气体,用惰性电极进行电
2
解可制得乙烯。其原理如图所示:
(4)上述装置中,阴极的电极反应式为_______。
18.(15分)化合物G是用于治疗面部疱疹药品泛昔洛韦的合成中间体,其合成路线如
下:
8
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司回答下列问题:
(1)A的结构简式为_____________;C中官能团的名称为____________。
(2)C→D的反应类型为_____________。
(3)B→C的反应方程式为______________。
(4)C有多种同分异构体,同时满足下列条件的同分异构体有____________种。
①与 溶液发生显色反应
②苯环上含有2个取代基
③ 该物质与足量的 反应产生
写出其中一种核磁共振氢谱中峰面积之比为6∶2∶2∶1∶1的结构简式___________。
(5)参照上述合成路线,设计以乙醇、苯甲醇和 为主要原料(其它试剂任选)
制备 的路线___________。
9
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司10
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司