文档内容
2024 届新高三开学摸底考试卷(全国通用,新教材)02
化 学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如
需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cu 64 Ga 70 Ni 59
第Ⅰ卷(选择题 共42分)
一、选择题:本题共14个小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.化学与生活、社会密切相关。下列说法不正确的是
A.我国规定商家不得无偿提供塑料袋,目的是减少“白色污染”
B.乙醇是一种易燃烧污染小的可再生能源,但只能在实验室内作燃料
C.化石燃料不可再生,使用太阳能代替化石燃料,有利于节约资源、保护环境
D.积极开发废电池的综合利用技术,防止其中的重金属盐对土壤和水源造成污染
【答案】B
【详解】A.聚乙烯塑料难以降解,易导致白色污染,A项正确;
B. 乙醇是一种易燃烧污染小的可再生能源,可用于汽车燃料,B项错误;
C.化石燃料不可再生,使用太阳能代替化石燃料,可减少对化石燃料的使用,有利于节约
资源、保护环境,C项正确;
电池中的重金属会污染土壤和水源,积极开发废电池的综合利用技术,防止其中的重金属
盐对土壤和水源造成污染,D项正确;
答案选B。
2.乙硼烷 常应用于有机合成领域,可通过反应
制得。下列说法正确的是
A.基态B原子的轨道表示式为
B.基态F原子核外电子排布式为
C. 分子空间构型为三角锥形
D. 中含有配位键
1
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司【答案】D
【详解】A.基态B原子的轨道表示式为 ,A错误;
B. F是9号元素,基态F原子核外电子排布式为 ,B错误;
C. 形成3个σ键,中心原子B无孤电子对,所以BF 分子空间构型为平面三角形,C
3
错误;
D. 中Na+与BF 离子键结合,BF 含有共价键和配位键,D正确;
故答案选D。
3. 是一种常用的消毒剂,可通过反应 制取,
下列有关说法正确的是
A.还原性:
B.每消耗 ,转移 电子
C.氧化剂与还原剂的物质的量之比为2∶1
D.若该反应通过原电池来实现,则 是负极产物
【答案】C
【详解】A. 反应中,SO 是还原剂、ClO 是还
2 2
原产物,还原性 ,故A错误;
B.SO 中S元素化合价由+4升高为+6,每消耗 ,转移 电子,故B错误;
2
C.NaClO 中Cl元素化合价降低,NaClO 是氧化剂,SO 中S元素化合价升高,SO 是还原
3 3 2 2
剂,氧化剂与还原剂的物质的量之比为2∶1,故C正确;
D.若该反应通过原电池来实现,负极发生氧化反应,正极发生还原反应,则 是正极产
物,故D错误;
选C。
4.用N 表示阿伏加德罗常数的值,下列叙述中正确的是
A
A. 的 中,含有的中子数为1.1N
A
B. 、 时, 中含有的原子数为1.5N
A
C. 与足量 反应,转移的电子数为3N
A
D.标准状况下, 和 的混合气体中分子总数为0.2N
A
【答案】B
【详解】A.1个 原子中含有6个中子,则 的 中,含有的中子数为0.6N ,A
A
不正确;
2
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司B. 的物质的量为 =0.5mol,则含有的原子数为0.5mol×3N =1.5N ,B正确;
A A
C. 与足量 反应,Cl由0价降低到-1价,则转移的电子数为2N ,C不正确;
A
D.标准状况下, 和 的混合气体物质的量为0.1mol,则含分子总数为0.1N ,D
A
不正确;
故选B。
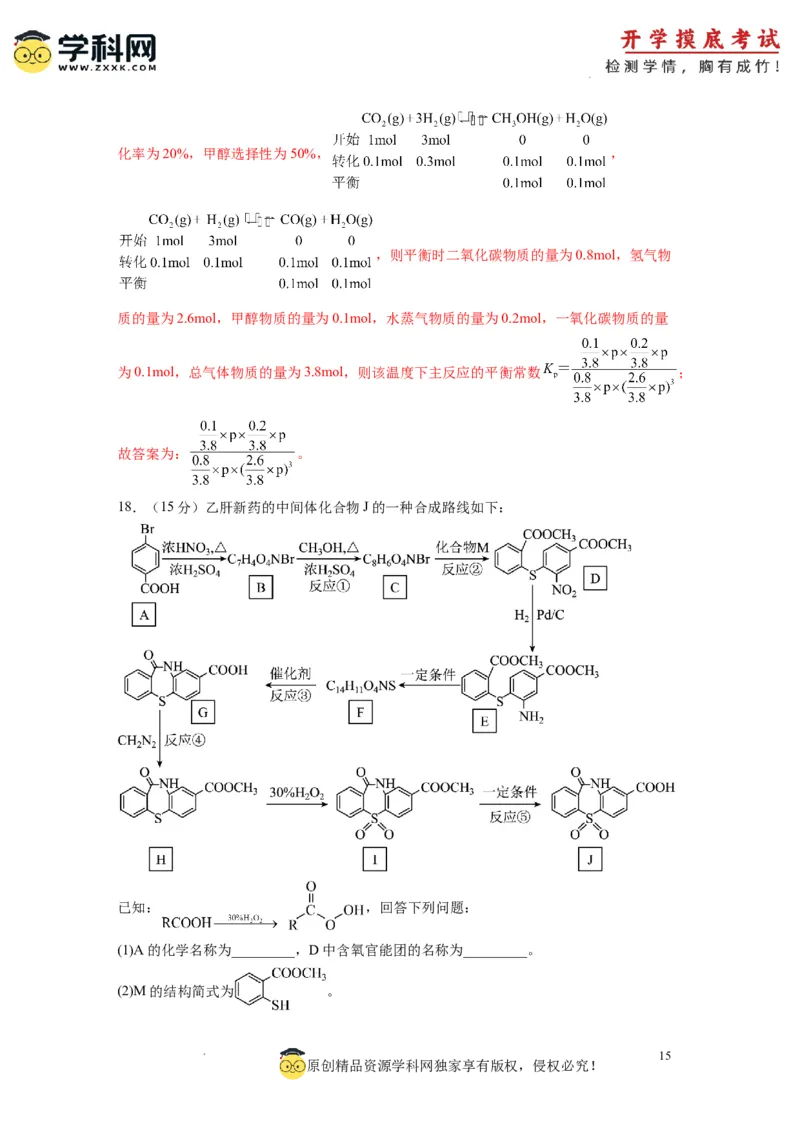
5.《Chem.sci.》报道麻生明院士成功合成某种非天然活性化合物(结构如下图)。下列有
关该化合物的说法错误的是
A.分子式为 C H NO
18 17 2
B.能使溴水和酸性高锰酸钾溶液褪色
C.所有氢原子不可能共平面
D.苯环上的一氯代物有 7 种
【答案】D
【详解】A.按碳呈四价的原则,确定各碳原子所连的氢原子数,从而确定分子式为
C H NO ,A正确;
18 17 2
B.题给有机物分子内含有碳碳双键,能使溴水和酸性高锰酸钾溶液褪色,B正确;
C.题给有机物分子中,最右边的端基为-CH,3个氢原子与苯环氢原子不可能共平面,C
3
正确;
D.从对称性考虑,苯环上的一氯代物有 5 种,D错误;
故选D。
6.下列实验探究方案能达到探究目的的是
选
探究方案 探究目的
项
将硫酸钡粉末和碳酸钠饱和溶液混合,充分振荡、静
探究 和 的溶
A 置,取上层清液1~2mL,滴加盐酸和 溶液,观
度积常数相对大小
察是否有沉淀产生
将二氧化硫气体通入碘和淀粉的混合溶液中,观察溶
B 探究还原性:
液颜色的变化
向过氧化氢和氯化钡混合液中滴加亚硫酸钠溶液,观 探究过氧化氢能否将亚硫
C
察是否产生沉淀 酸盐氧化
3
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司探究溴乙烷在此条件下发
加热溴乙烷和氢氧化钠-乙醇混合溶液,将产生的气
D 生取代反应还是发生消去
体通入高锰酸钾溶液中,观察溶液颜色的变化
反应
A.A B.B C.C D.D
【答案】B
【详解】A.硫酸钡粉末和碳酸钠饱和溶液混合,会有部分硫酸钡转化为碳酸钡,上层清液
中含有硫酸根和碳酸根,滴加盐酸时碳酸根反应生成二氧化碳气体,再加氯化钡溶液会生
成硫酸钡沉淀,无法比较硫酸钡和碳酸钡溶度积常数的相对大小,A错误;
B.二氧化硫通入碘和淀粉混合溶液中,若蓝色逐渐退去,则发生反应,
I+SO+2H O=2HI+HSO ,其中二氧化硫是还原剂,故还原性: ,B正确;
2 2 2 2 4
C.亚硫酸钠与氯化钡溶液可以发生反应生成亚硫酸钡,无法证明过氧化氢能否将亚硫酸氧
化,C错误;
D.溴乙烷发生取代反应,生成的溴化氢气体,以及发生消去反应生成的乙烯气体都可以使
酸性高锰酸钾溶液褪色,D错误;
故选B。
7.下列指定反应的离子方程式正确的是
A.用NaOH溶液吸收少量SO :
2
B.向稀FeSO 溶液中滴加稀硝酸:
4
C.向AlCl 溶液中加入过量氨水:
3
D.用盐酸、淀粉KI溶液检验含碘盐中的 :
【答案】B
【详解】A.用NaOH溶液吸收少量SO ,反应产生NaSO 、HO,反应的离子方程式为:
2 2 3 2
SO +2OH-= +H O,A错误;
2 2
B.向稀FeSO 溶液中滴加稀硝酸,会发生氧化还原反应产生Fe3+、NO、HO,反应符合事
4 2
实,遵循物质的拆分原则,B正确;
C.向AlCl 溶液中加入过量氨水,反应产生Al(OH) 沉淀和NH Cl,反应的离子方程式为:
3 3 4
Al3++3NH·H O=Al(OH) ↓+3 ,C错误;
3 2 3
D.电子不守恒,电荷不守恒,反应的离子方程式应该为: ,D
错误;
故合理选项是B。
8.下列“类比”结果正确的是
A.苯不能使酸性KMnO 溶液褪色,甲苯也不能使酸性KMnO 溶液褪色
4 4
B.NH 的分子构型为三角锥形,PCl 的分子构型也为三角锥形
3 3
4
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司C.Ca(HCO ) 的溶解度比CaCO 的大,NaHCO 的溶解度也比NaCO 的大
3 2 3 3 2 3
D.NaO 与CO 反应生成NaCO 与O,NaO 与SO 反应生成NaSO 与O
2 2 2 2 3 2 2 2 2 2 3 2
【答案】B
【详解】A.苯不与酸性高锰酸钾溶液反应,甲苯可与酸性高锰酸钾溶液反应从而使其褪色,
A错误;
B.NH 中N原子的价层电子对数为3+ =4,PCl 中P原子的价层电子对数也是3+
3 3
=4,两者均有一对孤电子对,分子构型为三角锥形,B正确;
C.碳酸氢钠的溶解度小于NaCO,C错误;
2 3
D.NaO 具有强氧化性,SO 具有较强的还原性,两者反应生成NaSO ,D错误;
2 2 2 2 4
故答案选B。
9.一种用作锂离子电池电解液的锂盐的阴离子结构如图所示,X、Y、Z、W为原子序数依
次增大的短周期主族元素,W的核外电子中有3个未成对电子。下列说法正确的是
A.W元素最高价氧化物对应的水化物是强酸B.该阴离子中不存在非极性键
C.X的氢化物沸点可能高于Z的氢化物 D.该离子中所有原子最外层均为8电子结构
【答案】C
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,W的核外电子中有3个未
成对电子,则其p轨道上有3个电子,价电子排布式为3s23p3,W为P元素,由结构简式知
Z形成1个共价键,Y形成2个共价键,X形成4个共价键,则Z为F元素,Y为O元素,
X为C。
【详解】A.W为P元素,最高价氧化物对应的水化物是磷酸,磷酸不是强酸,故A错误;
B.该阴离子中含有C-C非极性键,故B错误;
C.X为C,C元素的氢化物有很多种,分子量越大沸点越高,可能高于Z的氢化物HF,故
C正确;
D.该离子中P未形成8电子结构,故D错误;
故选C。
10.陈述Ⅰ和Ⅱ均正确并具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用明矾净水 胶体具有吸附性
5
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司B Na着火不能用水扑灭 Na可与水反应产生
C 二氧化硅可用于制备光导纤维 二氧化硅是良好的半导体材料
D 用84消毒液进行消毒 NaClO溶液呈碱性
A.A B.B C.C D.D
【答案】A
【详解】A.明矾中的Al3+水解生成 胶体, 胶体具有吸附性,能用于净水,
A符合题意;
B.Na着火不能用水扑灭,但Na与水反应产生的是H,B不符合题意;
2
C.二氧化硅可用于制备光导纤维,但二氧化硅不是良好的半导体材料,C不符合题意;
D.用84消毒液进行消毒,是因为NaClO溶液具有强氧化性,D不符合题意;
故选A。
11.向密闭容器中充入1molA,发生反应aA(g)=bB(g)+cC(g),达到平衡时,体系中B的体
积分数φ(B)随温度、压强的变化如图所示。下列说法正确的是
A.该反应的 H<0, S<0
B.M、N两点对应的化学平衡常数:M>N
△ △
C.P、M两点对应的A的转化率:P<M
D.恒温恒容时,再充入少量A,达到新平衡,φ(B)增大
【答案】C
【详解】A.由题图可知,压强不变时,升高温度, 减小,平衡逆向移动,故正反应
为放热反应, ,温度不变时,增大压强, 减小,平衡逆向移动,故 ,则
,A项错误;
B.M、N点的温度相同,化学平衡常数相同,B项错误;
C.P、M点的压强相同,降低温度, 增大,平衡正向移动,A的转化率增大,转化率:
P<M,C项正确;
D.恒温恒容条件下,向容器中再充入少量A,相当于对体系加压,结合题图可知,达到新
平衡时, 减小,D项错误。
答案选C。
6
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司12.金刚砂与金刚石具有相似的晶体结构,硬度为9.5,熔点为2700℃,其晶胞结构如图所
示。下列说法错误的是
A.金刚砂的化学式为SiC
B.SiC晶体中碳原子和硅原子均采用sp3杂化
C.距离碳原子最近的碳原子数为12
D.金刚石的熔点低于2700℃
【答案】D
【详解】A.由 可知,C原子位于顶点和面心,晶胞结构
中C原子数为8× +6× =4,4个Si原子位于晶胞内,则Si:C=4:4=1:1,金刚砂的化学式为
SiC,故A正确;
B.SiC晶体中碳原子周围有4个硅原子,而硅原子有4个碳原子,均采用sp3杂化,故B正
确;
C.以4个Si原子形成立体结构看,距离最短的Si位于顶点和面心,每个顶点为12个面共
有,则距离硅原子最近的硅原子数为12,故C正确;
D.共价键的键长越短,键能越大,则熔沸点越高,C-C键键长比C-Si键键长短,金刚石
的熔点高于2700℃,故D错误;
答案为D。
13.下列溶液或浊液中,关于离子浓度的说法正确的是
A.一定浓度的氨水加水稀释的过程中, 的比值减小
B.浓度均为0.1mol·L-1的NaCO、NaHCO 混合溶液中:c(CO )