文档内容
2023—2024—1 高三年级 10 月学情检测
化学试卷
满分:100分 考试时间:90分钟
一、单选题(本大题共18小题,每小题3分,共54分,每题只有一个正确答案)
1.很多成语与化学知识密切相关,下列有关解读正确的是( )
选项 成语 化学角度解读
A 甘之如饴 “饴”是麦芽糖,具有独特的甜味。在人体内水解最终产物为葡萄糖和果糖
火药爆炸能产生“石破天惊”的效果,火药的基本成份为硝石(硝酸钾)、硫磺及木
B 石破天惊
炭,三者按一定的比例混合加热后,发生激烈的化学反应,产生大量的光和热
C 信口雌黄 雌黄( )颜色金黄鲜艳,有剧毒,其中S元素的化合价和黄铁矿( )中S
元素的相同
D 火树银花 火树就是指焰火,俗称烟花。多彩的烟花是金属单质的焰色试验,属于物理变化
A.A B.B C.C D.D
2.污水处理厂处理含 废水的过程分两步进行:①向含 的废水中加入过量 将 转化为
;②调节①所得溶液为酸性,使 继续被 转化为两种无污染的气体。下列关于上述过程
的叙述错误的是( )
A. 的电子式为
B.过程①中,生成 的反应中氧化剂与还原剂的物质的量之比为
C.过程②中,生成的两种无污染的气体为 和
D.氧化性:
3.对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
选项 粒子组 判断和分析
不能大量共存,因发生反应
A
、 、 、
不能大量共存,因发生反应:
B
、 、 、
C 能大量共存,粒子间不反应
、 、 、
D 能大量共存,粒子间不反应
、 、 、
A.A B.B C.C D.D
4.对于下列实验,不能正确描述其反应的离子方程式是( )A.向苯酚钠溶液中通入少量二氧化碳:
B.向饱和碳酸钠溶液中通入足量 :
C.向 溶液中通入过量 :
D.向澄清石灰水中滴加少量 溶液:
5.下列关于溶液中所含离子检验的说法正确的是( )
A.取少量某溶液于试管中,向其中先滴加稀硝酸,再滴加 溶液,有白色沉淀生成,说明该溶液
中含有
B.取少量某溶液于试管中,向其中加入少量新制氯水,再滴加 溶液,若溶液变红,说明该溶液中含
有
C.取少量某溶液于试管中,加入 溶液并加热,用湿润的红色石荵试纸检验产生的气体,若红色石荵
试纸变蓝,说明该溶液中含有
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有
6.工业中制取高铁酸钾 ,是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入 至饱
和就可以析出高铁酸钾。湿法制备 ,的主要反应为:
;
干法制备 ,的主要反应为:
。
下列有关说法不正确的是( )
A.湿法和干法制备中,生成质量相同的 转移电子数目相同B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小
C.干法制备的主要反应中 既是氧化剂又是还原剂
D. 处理水时,既能杀菌消毒,生成的 胶体还能吸附水中的悬浮杂质
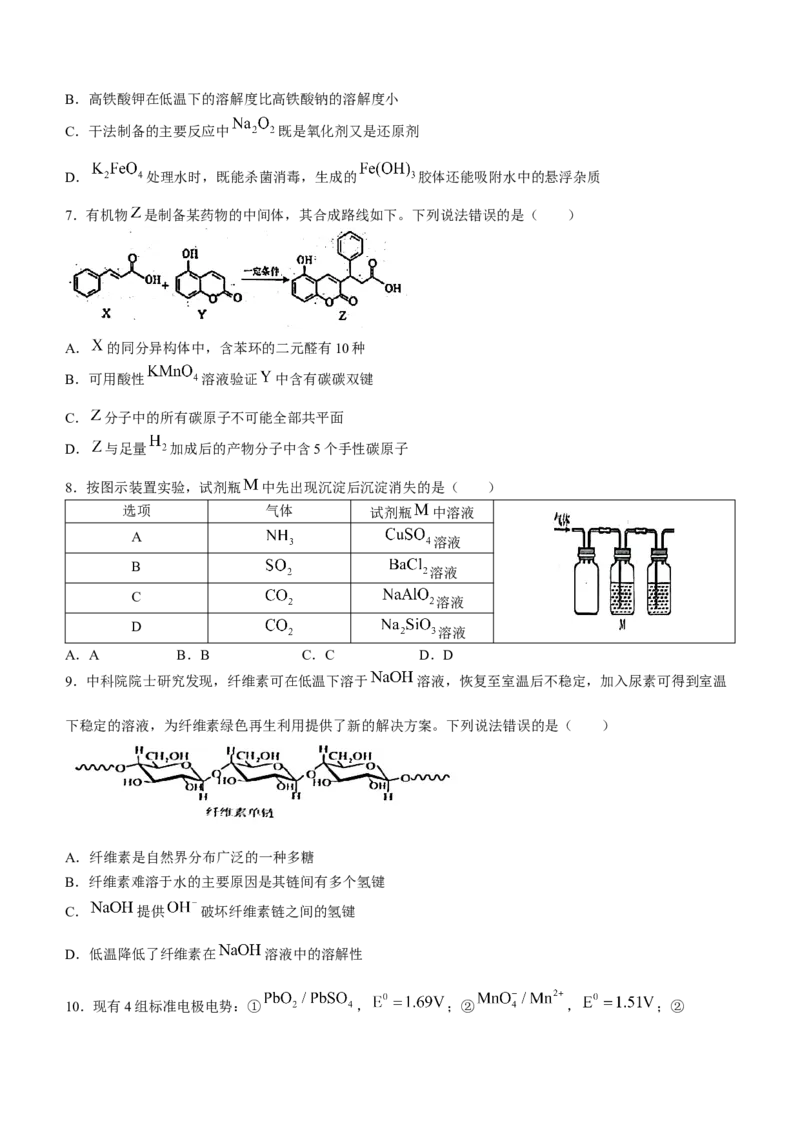
7.有机物 是制备某药物的中间体,其合成路线如下。下列说法错误的是( )
A. 的同分异构体中,含苯环的二元醛有10种
B.可用酸性 溶液验证 中含有碳碳双键
C. 分子中的所有碳原子不可能全部共平面
D. 与足量 加成后的产物分子中含5个手性碳原子
8.按图示装置实验,试剂瓶 中先出现沉淀后沉淀消失的是( )
选项 气体 试剂瓶 中溶液
A
溶液
B
溶液
C
溶液
D
溶液
A.A B.B C.C D.D
9.中科院院士研究发现,纤维素可在低温下溶于 溶液,恢复至室温后不稳定,加入尿素可得到室温
下稳定的溶液,为纤维素绿色再生利用提供了新的解决方案。下列说法错误的是( )
A.纤维素是自然界分布广泛的一种多糖
B.纤维素难溶于水的主要原因是其链间有多个氢键
C. 提供 破坏纤维素链之间的氢键
D.低温降低了纤维素在 溶液中的溶解性
10.现有4组标准电极电势:① , ;② , ;②, ;④ , 。已知电势越高对应物质的氧化性越强,则下列离子
方程式或相应的描述中正确的是( )
A.
B.向含 的溶液中加 能观察到黄绿色气体
C.酸化高锰酸钾时既可以用硫酸也可以用盐酸
D.氧化性由强到弱的顺序为
11. 可作高能燃料的氧化剂,它可由以下反应制得: (未配平)。
下列说法错误的是( )
A.氧化性:
B.上述反应中,氧化剂与还原剂的物质的量之比为
C.若生成标准状况下 ,转移电子
D. 作氧化剂时,其还原产物可能是 和
12.1923年由布朗斯特和劳里提出酸碱质子理论认为,在反应过程中能给出质子( )的分子或离子都是
酸,凡是能接受质子的分子或离子都是碱。按照“酸碱质子理论”,下列叙述错误的是( )
A.水既属于酸又属于碱
B.可以根据 的性质推断 的碱性较强
C.根据 ,则碱性:
D. 是酸碱反应
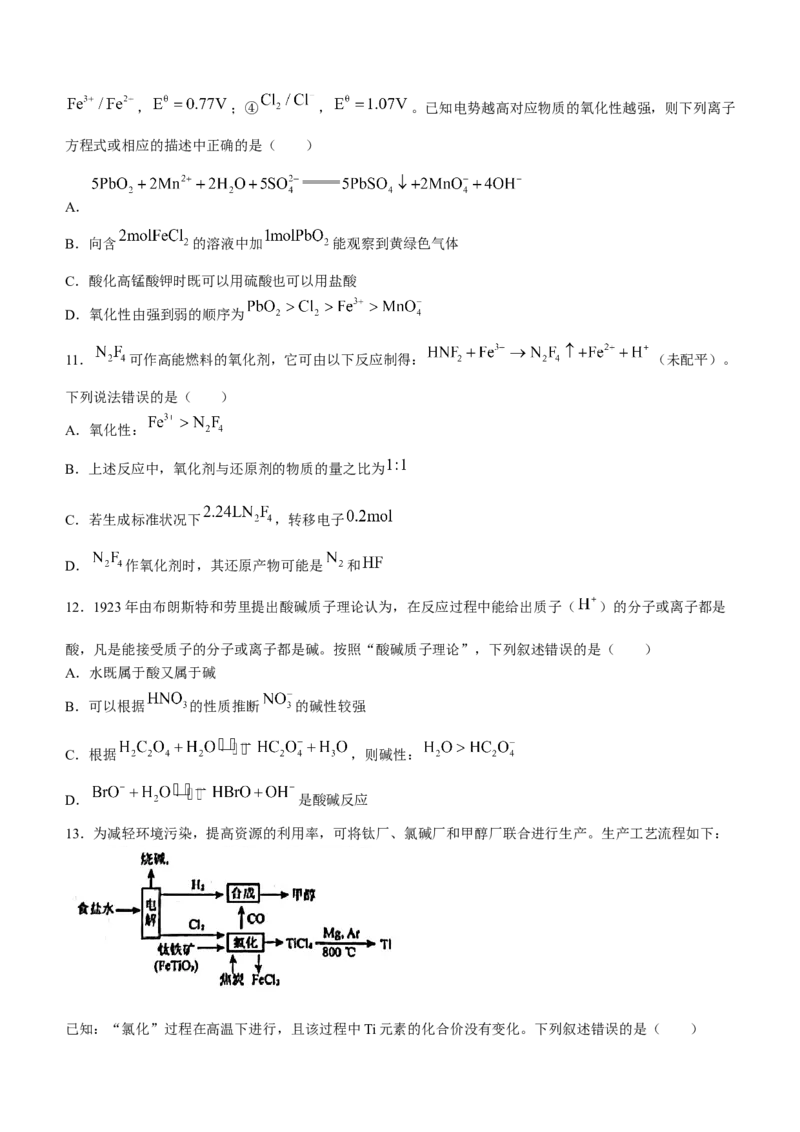
13.为减轻环境污染,提高资源的利用率,可将钛厂、氯碱厂和甲醇厂联合进行生产。生产工艺流程如下:
已知:“氯化”过程在高温下进行,且该过程中Ti元素的化合价没有变化。下列叙述错误的是( )A.氯碱工业中生成的氯气可用于生产漂白粉
B.“合成”过程中原子利用率为
C.“氯化”时发生反应的化学方程式为 ,还原剂只有
C
D.上述流程中生成钛时不可用 代替
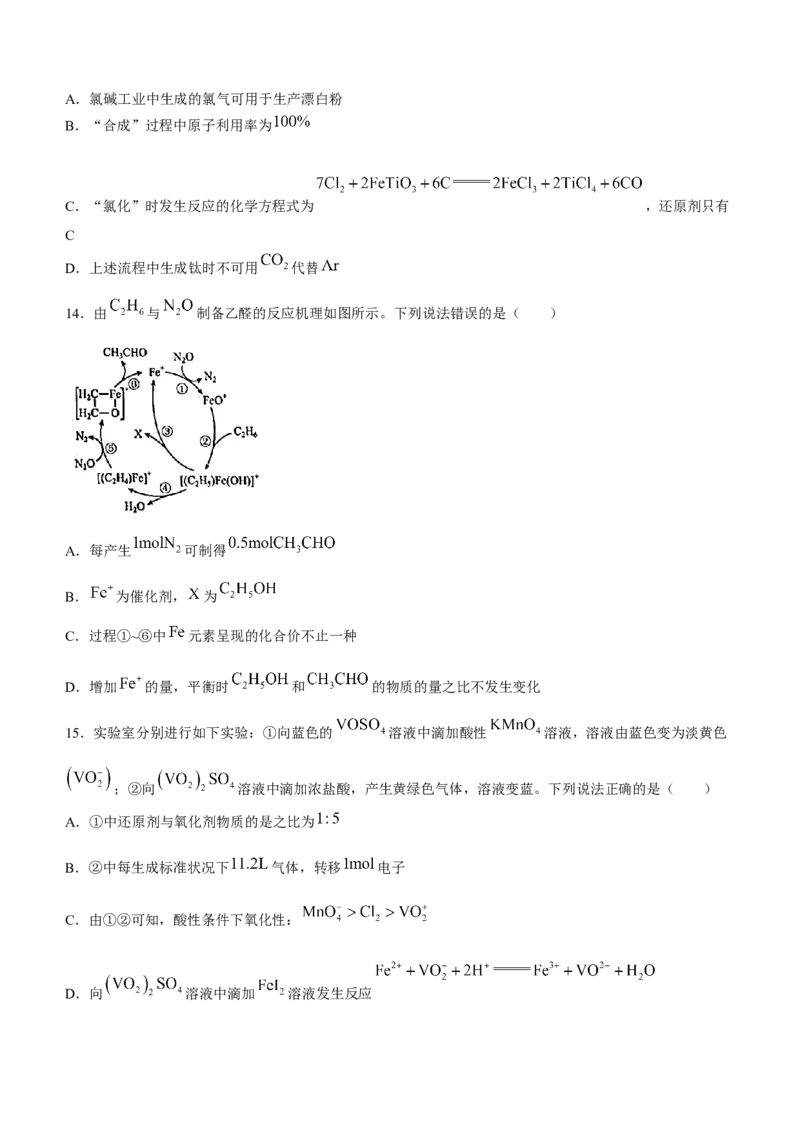
14.由 与 制备乙醛的反应机理如图所示。下列说法错误的是( )
A.每产生 可制得
B. 为催化剂, 为
C.过程①~⑥中 元素呈现的化合价不止一种
D.增加 的量,平衡时 和 的物质的量之比不发生变化
15.实验室分别进行如下实验:①向蓝色的 溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色
;②向 溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝。下列说法正确的是( )
A.①中还原剂与氧化剂物质的是之比为
B.②中每生成标准状况下 气体,转移 电子
C.由①②可知,酸性条件下氧化性:
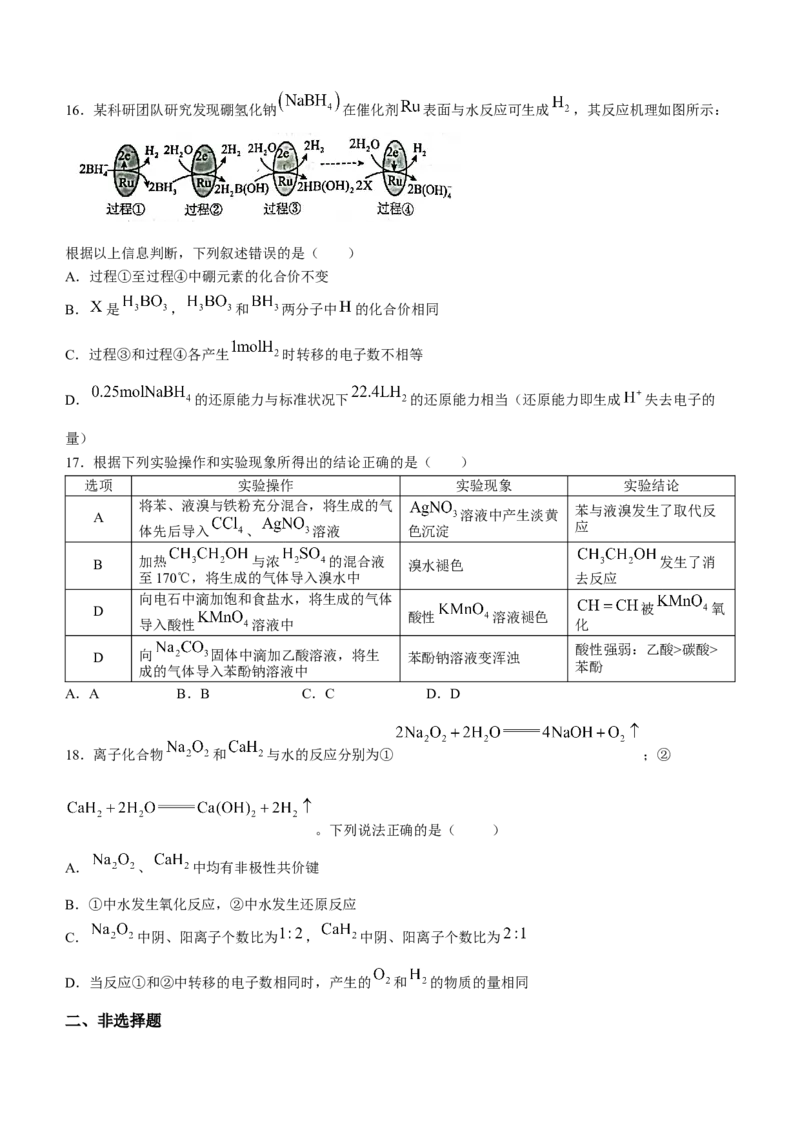
D.向 溶液中滴加 溶液发生反应16.某科研团队研究发现硼氢化钠 在催化剂 表面与水反应可生成 ,其反应机理如图所示:
根据以上信息判断,下列叙述错误的是( )
A.过程①至过程④中硼元素的化合价不变
B. 是 , 和 两分子中 的化合价相同
C.过程③和过程④各产生 时转移的电子数不相等
D. 的还原能力与标准状况下 的还原能力相当(还原能力即生成 失去电子的
量)
17.根据下列实验操作和实验现象所得出的结论正确的是( )
选项 实验操作 实验现象 实验结论
将苯、液溴与铁粉充分混合,将生成的气
苯与液溴发生了取代反
A 溶液中产生淡黄
应
体先后导入 、 溶液 色沉淀
B 加热 与浓 的混合液 溴水褪色 发生了消
至170℃,将生成的气体导入溴水中 去反应
向电石中滴加饱和食盐水,将生成的气体
D 被 氧
酸性 溶液褪色
导入酸性 溶液中 化
酸性强弱:乙酸>碳酸>
D 向 固体中滴加乙酸溶液,将生 苯酚钠溶液变浑浊
苯酚
成的气体导入苯酚钠溶液中
A.A B.B C.C D.D
18.离子化合物 和 与水的反应分别为① ;②
。下列说法正确的是( )
A. 、 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
二、非选择题19.(12分)根据提供的情境书写指定反应的方程式。
(1)通过如图转化可回收废旧锂电池电极材料 (难溶于水)中钴元素和锂元素。
写出反应1的离子方程式:_________。
(2)活性自由基 可有效除去废水中的苯酚等有机污染物,原理如图所示。写出 除去苯酚
反应的化学方程式:____________________________。
(3)现代工业上用氧化锌烟灰(主要成分为 ,含少量 、 和 )制取高纯锌的部分工艺流
程如图所示。
①已知:“溶浸”后浸出液中含 等。写出该过程中生成 的相关离子方程式:
_______________。
②“氧化除杂”的目的是将“ ”转化为 胶体,再经吸附聚沉除去。写出“氧化除杂”反应的
离子方程式:______________。
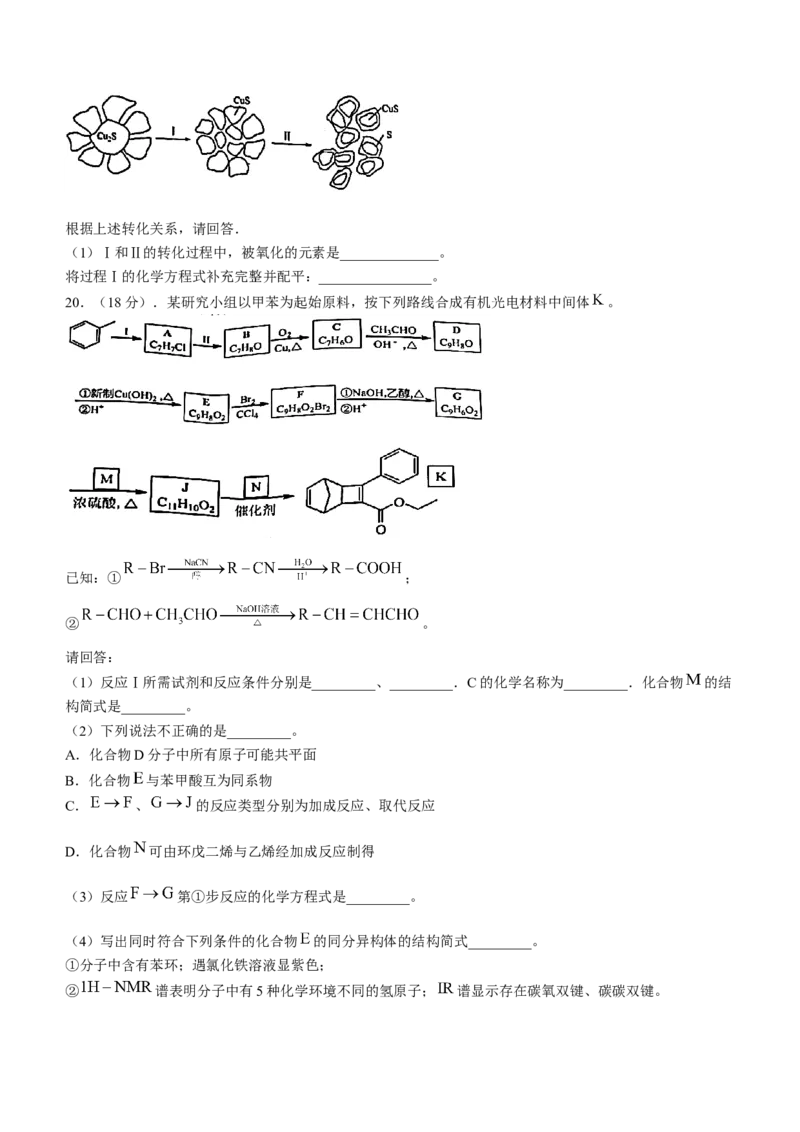
(4)辉铜矿(主要成分是 )是提炼铜的重要矿物原料之一、以 作为氧化剂在硫酸环境中对辉铜
矿浸出生成 的模型如下:根据上述转化关系,请回答.
(1)Ⅰ和Ⅱ的转化过程中,被氧化的元素是______________。
将过程Ⅰ的化学方程式补充完整并配平:________________。
20.(18分).某研究小组以甲苯为起始原料,按下列路线合成有机光电材料中间体 。
已知:① ;
② 。
请回答:
(1)反应Ⅰ所需试剂和反应条件分别是_________、_________.C的化学名称为_________.化合物 的结
构简式是_________。
(2)下列说法不正确的是_________。
A.化合物D分子中所有原子可能共平面
B.化合物 与苯甲酸互为同系物
C. 、 的反应类型分别为加成反应、取代反应
D.化合物 可由环戊二烯与乙烯经加成反应制得
(3)反应 第①步反应的化学方程式是_________。
(4)写出同时符合下列条件的化合物 的同分异构体的结构简式_________。
①分子中含有苯环;遇氯化铁溶液显紫色;
② 谱表明分子中有5种化学环境不同的氢原子; 谱显示存在碳氧双键、碳碳双键。(5)设计以 、 为原料合成的合成 路线_________(用流程图表示,其
它无机试剂任选)。
21.(16分)
我国河南、广西和贵州等省份高硫铝土矿储量较高,其主要成分为 和 ,还含有少量 、
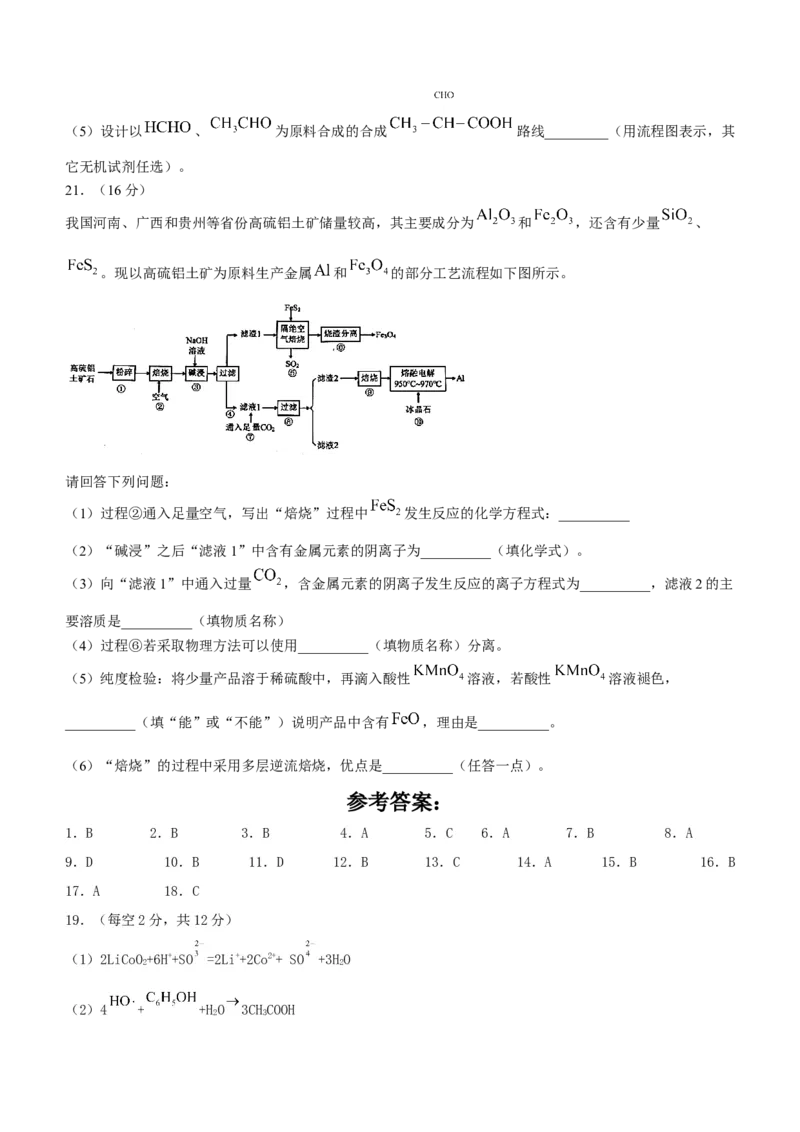
。现以高硫铝土矿为原料生产金属 和 的部分工艺流程如下图所示。
请回答下列问题:
(1)过程②通入足量空气,写出“焙烧”过程中 发生反应的化学方程式:__________
(2)“碱浸”之后“滤液1”中含有金属元素的阴离子为__________(填化学式)。
(3)向“滤液1”中通入过量 ,含金属元素的阴离子发生反应的离子方程式为__________,滤液2的主
要溶质是__________(填物质名称)
(4)过程⑥若采取物理方法可以使用__________(填物质名称)分离。
(5)纯度检验:将少量产品溶于稀硫酸中,再滴入酸性 溶液,若酸性 溶液褪色,
__________(填“能”或“不能”)说明产品中含有 ,理由是__________。
(6)“焙烧”的过程中采用多层逆流焙烧,优点是__________(任答一点)。
参考答案:
1.B 2.B 3.B 4.A 5.C 6.A 7.B 8.A
9.D 10.B 11.D 12.B 13.C 14.A 15.B 16.B
17.A 18.C
19.(每空2分,共12分)
(1)2LiCoO+6H++SO =2Li++2Co2++ SO +3HO
2 2
(2)4 + +HO 3CHCOOH
2 3(3) ZnO+2NH·HO+2NH = +3HO 2 +2HO+6NH·HO=AsO(胶体)+10Cl-+6NH +5HO
3 2 2 2 2 3 2 2 5 2
(4) 、S
、
20. (18分)(第五问4分,其它每空2分)
(1) 氯气 光照 苯甲醛 CHCHOH
3 2
(2)BD
(3)
(4) 、
(5)
或
21.(每空2分,共16分)(1)
(2) 或者
(3) 碳酸氢钠(或小苏打)
(4) 磁铁
(5)不能 和稀硫酸反应会生成 和 ,生成的 能让酸性高锰酸钾褪色